Журнал физической химии, 2023, T. 97, № 1, стр. 46-54
Экспериментальное исследование и термодинамическое моделирование тройной системы Ag–In–Pd
А. С. Павленко a, Е. А. Пташкина a, Г. П. Жмурко a, Е. Г. Кабанова a, *, М. А. Карева a, А. В. Хорошилов b, В. Н. Кузнецов a
a Московский государственный университет им. М.В. Ломоносова, Химический факультет
Москва, Россия
b Институт общей и неорганической химии им. Н.С. Курнакова Российской академии наук
Москва, Россия
* E-mail: kabanovaeg@gmail.com
Поступила в редакцию 11.05.2022
После доработки 25.05.2022
Принята к публикации 27.05.2022
- EDN: BCRZNU
- DOI: 10.31857/S0044453723010235
Аннотация
Фазовые равновесия в тройной системе Ag–In–Pd изучены с использованием сканирующей электронной микроскопии, микрорентгеноспектрального (МРСА) и рентгенофазового (РФА) методов анализа. Установлена растворимость третьих компонентов в двойных фазах систем Ag–In и In–Pd, а также границы существования (от 4 до 17.5 ат. % Ag при 25 ат. % In) и кристаллическая структура (Al3Ti) тройного соединения τ. По полученным в настоящей работе и литературным экспериментальным результатам выполнен новый термодинамический расчет системы Ag–In–Pd. Достигнуто хорошее согласие с экспериментальными данными как по фазовым равновесиям, так и по термодинамическим свойствам фаз системы. Корректность полученного описания дополнительно подтверждена хорошей сходимостью результатов расчета с результатами ДСК/ДТА исследования трех образов, которые в оптимизацию не включались.
Сплавы на основе палладия находят широкое применение в различных областях промышленности: химической, электротехнической, автомобильной, в водородной энергетике и медицине. Компонентами палладиевых сплавов чаще всего являются металлы 11 группы, а также непереходные низкоплавкие элементы, например, индий и олово [1]. Два последних металла заметно понижают температуры обработки сплавов, но образуют большое число интерметаллических соединений, свойства которых необходимо учитывать при разработке составов и выборе способов технологической обработки новых материалов.
Основным инструментом при разработке многокомпонентных сплавов являются фазовые диаграммы. В настоящее время для построения диаграмм состояния многокомпонентных систем успешно используется метод термодинамического моделирования CALPHAD-метод. Этот метод позволяет не только обобщать экспериментальные данные по фазовым равновесиям и свойствам фаз, но и предсказывать равновесия в сложных многокомпонентных системах при наличии термодинамических описаний граничных двойных и тройных систем.
Целью настоящего исследования являлся пересмотр термодинамического описания системы Ag–In–Pd с учетом всей имеющейся в литературе информации по свойствам ее фаз.
Фазовые равновесия в системе Ag–In–Pd при температурах 500 и 700°С изучались в работах [2, 3]. Следует отметить, что результаты этих исследований требуют некоторых уточнений, не была достоверно установлена граница существования ГЦК-твердого раствора в палладиевом углу системы, а также область гомогенности и кристаллическая структура обнаруженного тройного соединения. Что касается выполненного авторами [3] CALPHAD-расчета системы Ag–In–Pd, то он хорошо согласуется с их собственными экспериментальными данными при 500 и 700°С, но, по мнению авторов, требует дополнения, связанного с описанием обнаруженной тройной фазы. В расчете [3] также не проводилось моделирование расплава, хотя в литературе имеются термодинамические данные для этой фазы: энтальпии смешения [4] и парциальные энергии Гиббса компонентов, определенные методом ЭДС [5].
В настоящей работе для пересмотра термодинамического описания системы Ag–In–Pd установлены фазовые равновесия в богатой палладием области системы Ag–In–Pd при 500°C: определена растворимость индия в твердом растворе на основе палладия, а также область гомогенности и кристаллическая структура тройного соединения. Для получения экспериментальной информации в более широком интервале температур дополнительно изучены фазовые равновесия при 800°C. Кроме того, методом ДТА получены температуры фазовых переходов нескольких сплавов, которые использованы для валидации расчета.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для исследования фазовых равновесий в системе Ag–In–Pd было синтезировано 34 образца, 19 из которых отжигали при 500°С, 15 – при 800°С. Сплавы для исследования выплавляли из металлов высокой степени чистоты: палладий штрипсы (99.95 мас. %), серебро пластины (99.95 мас. %), индий полупроводниковой чистоты (99.999 мас. %). Сплавы готовили методом дуговой плавки в атмосфере аргона, предварительно очищенного плавкой геттера (титан). Угар полученных сплавов не превышал 1 мас. %.
Для достижения равновесного состояния сплавы подвергали отжигу в вакуумированных кварцевых ампулах в трубчатых печах сопротивления. Время отжига сплавов варьировали от 720 до 2880 ч в зависимости от состава сплава и температуры отжига.
Микроструктуры образцов исследовали c использованием сканирующего электронного микроскопа Carl Zeiss LEO EVO 50XPV. Съемку осуществляли в вакууме с остаточным давлением 10‒7 Па при ускоряющем напряжении 20 кВ. Микроскоп был оборудован системой EDX энергодисперсионного анализа INCA Energy 450 фирмы Oxford Instruments (относительная точность измерений составляет 3–5%). С целью увеличения контрастности изображения использовали детектор Q-BSD.
Рентгенофазовый анализ проводили на автодифрактометре “STOE STADI P” на монохроматизированном CuKα1-излучении (германиевый монохроматор, λ = 1.54056 Å, интервал углов 2θ = = 20–90°, шаг 0.01°, время экспозиции – 10 с на точку). Для расшифровки полученных рентгенограмм использовали программное обеспечение STOE WinXPOW, версия 2.24 [6].
Для определения температур солидуса и ликвидуса сплавов использовали метод дифференциально-термического анализа (ДТА). Образцы исследовали на термоанализаторе Jupiter STA 449 F1, NETZSCH-GERAETEBAU GmbH. Нагрев образцов осуществляли в токе гелия высокой очистки (99.9999%), скорость нагрева (охлаждения) составляла 5 К/мин.
Для расчета и термодинамического моделирования фазовых равновесий в тройной системе Ag–In–Pd использовали ряд модулей программы Thermo-Calc® (версия 2022a): SYSTEM, DATA, GIBBS–ENERGY–SYSTEM, POLY, SCHEIL и PARROT [7].
Модуль SYSTEM осуществляет общее управление программой. Работа с базами данных, выбор компонентов систем, а также чтение значений параметров проходит в модуле DATA. Для внесения изменений в описания моделей фаз используется модуль GIBBS–ENERGY–SYSTEM. Параметры моделей фаз находили с помощью модуля PARROT. Расчет термодинамических свойств и фазовых равновесий выполняется в модуле POLY. С помощью постпроцессора POST модуля POLY осуществлялось графическое представление результатов.
Метод CALPHAD [8] основан на аналитическом представлении энергий Гиббса всех возможных фаз в зависимости от состава и температуры. При этом расплав и твердый раствор на основе ГЦК-компонентов описываются моделью неупорядоченного раствора замещения:
(1)
$\begin{gathered} {{G}^{\psi }}(x,T) = \mathop \sum \limits_i \,{{x}_{i}}{}_{~}^{0}G_{i}^{\psi }(T) + \\ + \;RT{\kern 1pt} \mathop \sum \limits_i \,{{x}_{i}}\ln ({{x}_{i}}) + {}_{~}^{{Xs}}{{G}^{\psi }}(\bar {x},T), \\ \end{gathered} $(2)
${}_{~}^{{Xs}}G({{x}_{i}},~{{x}_{j}}) = {\text{\;}}{{x}_{i}}{{x}_{j}}\mathop \sum \limits_{{v} = 0}^n \,{}_{{\text{\;}}}^{{v}}{{L}_{{i,j}}}{{({{x}_{i}} - {{x}_{j}})}^{{v}}},$Для описания энергии Гиббса упорядоченных фаз используют подрешеточные модели, при этом количество подрешеток и типы атомов, находящихся в них, определяются в соответствии с кристаллической структурой и составом фазы. Параметрами подрешеточной модели фазы являются энергии Гиббса квазикомпонентов – соединений, содержащих только один компонент в каждой подрешетке, а также параметры взаимодействий между компонентами в одной и той же подрешетке. Энергии Гиббса квазикомпонентов, также называемые параметрами стабильности этих квазикомпонентов, описываются выражением
(3)
${{G}_{{{{{\text{A}}}_{{\text{m}}}}{{{\text{B}}}_{n}}}}}~(T) = m~G_{{\text{A}}}^{{{\text{ref}}}} + n~{\text{G}}_{{\text{B}}}^{{{\text{ref}}}} + ~\,\,{{{{\Delta }}}_{{\text{f}}}}G({{{\text{A}}}_{m}}{{{\text{B}}}_{n}}),$Параметры взаимодействия в подрешеточной модели описываются выражением (2), в которое вместо концентраций компонентов xi подставляются их концентрации в подрешетках yi.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Экспериментальные исследования фазовых равновесий
Результаты рентгенофазового и микрорентгеноспектрального анализа образцов, отожжeнных при 500 и 800°С, представлены в табл. 1 и 2. Коноды двухфазных и трехфазных равновесий нанесены на рис. 1.
Таблица 1.
Результаты МРСА и РФА образцов системы Ag–In–Pd, отожжeнных при 500°С
| № | Средний состав образца, ат. % | Фаза | Состав фазы, ат. % | Параметры кристаллической решетки, Å | Структ. тип | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Ag | In | Pd | Ag | In | Pd | a | b | c | |||
| 1 | 3 | 21 | 76 | α | 3.5 | 19.0 | 77.5 | 3.900(2) | – | – | Cu |
| InPd3 | 2.8 | 22.7 | 74.5 | 2.8699(8) | – | 3.828(1) | Al3Zr | ||||
| 2 | 9 | 22 | 69 | α | 27.6 | 14 | 58.4 | 3.9141(4) | – | – | Cu |
| InPd3 | 4.0 | 22.3 | 73.7 | 2.8724(5) | – | 3.8189(8) | Al3Zr | ||||
| 3 | 17 | 20 | 63 | α | 32.7 | 14.2 | 53.1 | 4.0310(8) | – | – | Cu |
| τ | 10.9 | 22.9 | 66.2 | 4.1589(6) | – | 7.3494(8) | Al3Ti | ||||
| 4 | 23 | 21 | 56 | α | 61.7 | 8.8 | 29.5 | 4.0578(4) | – | – | Cu |
| τ | 15.9 | 24.1 | 60.0 | 4.1825(6) | – | 7.3114(8) | Al3Ti | ||||
| 5 | 32 | 25 | 43 | α | 92.3 | 2.5 | 5.2 | 4.0777(6) | – | – | Cu |
| InPd | 17.3 | 31.2 | 51.5 | 3.2140(5) | – | – | CsCl | ||||
| 6 | 47 | 28 | 25 | α | 87.5 | 12.5 | 0.0 | 4.1189(3) | – | – | Cu |
| InPd | 4.4 | 45.7 | 49.9 | 3.2403(8) | – | – | CsCl | ||||
| 7 | 72 | 19 | 9 | α | 87.0 | 13.0 | 0.0 | 4.1194(9) | – | – | Cu |
| InPd | 4.6 | 46.1 | 49.3 | 3.2420(9) | – | – | CsCl | ||||
| 8 | 16 | 25 | 59 | τ | 16.1 | 25.3 | 58.6 | 4.1900(1) | – | 7.3342(2) | Al3Ti |
| 9 | 20 | 27 | 53 | αа | – | – | – | 4.0767(7) | – | – | Cu |
| τ | 17.8 | 25.1 | 57.1 | 4.1985(8) | – | 7.326(2) | Al3Ti | ||||
| InPd | 13.8 | 31.0 | 55.2 | 3.2125(1) | – | – | CsCl | ||||
| 10 | 13 | 37 | 50 | α | 89.0 | 4.9 | 6.1 | 4.081(1) | – | – | Cu |
| InPd | 10.2 | 38.2 | 51.6 | 3.2236(5) | – | – | CsCl | ||||
| 11 | 2 | 44 | 54 | InPd | 2.3 | 43.5 | 54.2 | 3.2390(3) | – | – | CsCl |
| 12 | 6 | 57 | 37 | Lб | 64.2 | 35.8 | 0.0 | 9.853(2) | – | – | Al4Cu9 |
| InPdа | – | – | – | 3.2411(8) | – | – | CsCl | ||||
| In3Pd2 | 0.6 | 59.4 | 40.0 | 4.5444(6) | – | 5.5180(8) | Al3Ni2 | ||||
| 13 | 17 | 25 | 58 | αа | – | – | – | 4.071(1) | – | – | Cu |
| τ | 17.2 | 25.4 | 57.4 | 4.1985(4) | – | 7.3338(6) | Al3Ti | ||||
| 14 | 3 | 24 | 73 | InPd3 | 2.7 | 23.7 | 73.6 | 2.8854(5) | – | 3.7869(8) | Al3Zr |
| 15 | 79 | 21 | 0 | α | 79.0 | 21.0 | 0.0 | 4.1328(7) | – | – | Cu |
| 16 | 77 | 22 | 1 | α | 78.8 | 20.6 | 0.6 | 4.1335(3) | – | – | Cu |
| InPd | 6.9 | 45.5 | 47.6 | 3.2415(7) | – | – | CsCl | ||||
| 17 | 69 | 29 | 2 | ζ | 69.0 | 29.3 | 1.7 | 2.9537(5) | – | 4.7877(8) | Mg |
| 18 | 75 | 25 | 0 | ζ | 76.1 | 23.9 | 0.0 | 2.9566(6) | – | 4.7914(5) | Mg |
| 19 | 66 | 28 | 6 | ζ | 72.6 | 26.2 | 1.2 | 2.9588(8) | – | 4.7866(9) | Mg |
| InPd | 45.0 | 49.4 | 5.6 | 3.2424(7) | – | – | CsCl | ||||
Таблица 2.
Результаты МРСА и РФА образцов системы Ag–In–Pd, отожжeнных при 800°С
| № | Средний состав образца, ат. % | Фаза | Состав фазы, ат. % | Параметры кристаллической решетки, Å | Структ. тип | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Ag | In | Pd | Ag | In | Pd | a | b | c | |||
| 1 | 3 | 20 | 77 | α | 5.5 | 16.0 | 78.5 | 3.9102(7) | – | – | Cu |
| InPd3 | 0.0 | 23.4 | 76.6 | 2.8830(5) | – | 3.7882(9) | Al3Zr | ||||
| 2 | 8 | 21 | 71 | α | 15.2 | 16.6 | 68.2 | a | – | – | Cu |
| InPd3 | 2.8 | 23.2 | 74.0 | a | – | – | Al3Zr | ||||
| 3 | 16 | 20 | 64 | α | 58.4 | 4.9 | 36.7 | 4.0430(2) | – | – | Cu |
| τ | 7.3 | 24.3 | 68.4 | 4.1722(6) | – | 7.3270(9) | Al3Ti | ||||
| 4 | 33 | 23 | 44 | α | 85.5 | 2.5 | 12.0 | 4.0658(6) | – | – | Cu |
| InPd | 17.0 | 29.3 | 53.7 | 3.2002(4) | – | – | CsCl | ||||
| 5 | 34 | 21 | 45 | α | 84.6 | 2.9 | 12.5 | 4.0537(4) | – | – | Cu |
| InPd | 16.6 | 28.3 | 54.5 | 3.198(2) | – | – | CsCl | ||||
| 6 | 58 | 18 | 24 | α | 91.0 | 4.9 | 4.1 | 4.0797(7) | – | – | Cu |
| InPd | 13.6 | 36.7 | 49.7 | 3.2207(2) | – | – | CsCl | ||||
| 7 | 18 | 25 | 57 | α | 83.9 | 2.6 | 13.5 | 4.0622(8) | – | – | Cu |
| τ | 17.5 | 24.7 | 57.8 | 4.1960(6) | – | 7.336(1) | Al3Ti | ||||
| 8 | 24 | 29 | 47 | α | 90.4 | 2.2 | 7.4 | 4.0737(6) | – | – | Cu |
| InPd | 15.6 | 32.0 | 52.4 | 3.2088(6) | – | – | CsCl | ||||
| 9 | 10 | 34 | 56 | InPd | 10.5 | 33.9 | 55.6 | 3.2230(7) | – | – | CsCl |
| 10 | 19 | 35 | 46 | α | 89.8 | 6.9 | 3.3 | 4.0849(4) | – | – | Cu |
| InPd | 12.9 | 38.0 | 49.1 | 3.2290(8) | – | – | CsCl | ||||
| 11 | 2 | 44 | 54 | InPd | 2.3 | 43.5 | 54.2 | 3.2328(6) | – | – | CsCl |
| 12 | 11 | 40 | 49 | InPd | 11.4 | 39.5 | 49.1 | 3.2289(9) | – | – | CsCl |
| 13 | 6 | 43 | 51 | InPd | 6.0 | 43.2 | 50.8 | 3.2351(9) | – | – | CsCl |
| 14 | 12 | 27 | 61 | τ | 11.9 | 26.8 | 51.3 | 4.1862(6) | – | 7.3350(9) | Al3Ti |
| InPdb | 12.6 | 30.0 | 57.4 | – | – | – | CsCl | ||||
| 15 | 5 | 28 | 67 | τ | 10.5 | 26.9 | 62.6 | 4.1557(6) | – | 7.3576(9) | Al3Ti |
| InPd2 | 0 | 32.9 | 67.1 | 5.6060(9) | 4.223(1) | 8.207(5) | Co2Si | ||||
| InPd | 6.5 | 35.5 | 58.0 | – | – | – | CsCl | ||||
Рис. 1.
Рассчитанные изотермические сечения системы Ag–In–Pd при 500°С (а) и 800°С (б) в сравнении с экспериментальными данными, полученными в настоящем исследовании и в [2].
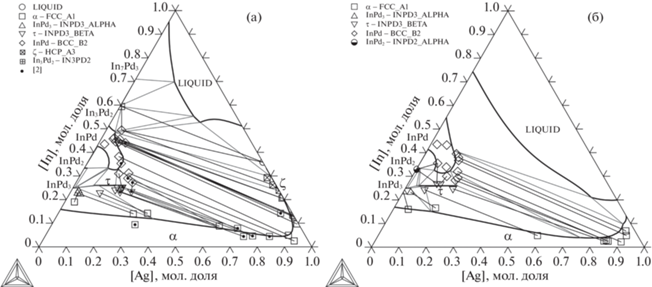
Установлено, что в интерметаллидах InPd2 и In3Pd5 серебро практически не растворяется. Область гомогенности эквиатомной фазы InPd направлена вдоль изоконцентраты 50 ат. % и максимальное содержание серебра в ней при обеих температурах составляет ∼17 ат. %. Следует отметить, что в работе [3] при 500°С растворимость серебра в InPd несколько больше (∼20 ат).
Растворимость индия в ГЦК-твердом растворе системы Ag–In–Pd проходит через минимум. В чистом палладии она составляет ~19 ат. % In, при добавлении ~90 ат. % Ag снижается до ~2 ат. % In, потом вновь резко возрастает. Подобный характер растворимости индия в ГЦК-твердом растворе отмечался и в работах [2, 3]. Однако минимум растворимости индия (5 ат. %) наблюдался при 80 ат. % серебра. Следует также отметить, что при 700°С растворимость индия в α‑твердом растворе значительно ниже, чем установлено в настоящей работе при 500 и 800°С.
Кроме того, фаза ζ на изотермическом сечении при 500°С находится в равновесии с фазой InPd, в то время как авторы [2, 3] утверждают, что при 500°С реализуется равновесие ζ + In3Pd2.
На изоконцентрате ∼25 ат. % In до 18 ат. % Ag существуют две фазы – твердый раствор на основе низкотемпературной модификации InPd3 и тройная фаза τ. Стоит отметить, что обе эти фазы имеют родственные кристаллические структуры и из-за близости факторов рассеяния рентгеновского излучения атомами палладия, серебра и индия рентгенограммы этих соединений идентичны и соответствуют структурному типу индия. Кольман и Риттер [9] показали, что в сплавах Pd с непереходными металлами тетрагональные сверхструктуры к ГЦК-решетке (CuAu, Al3Ti и Al3Zr) можно различить рентгенографически по отношению c/a гранецентрированнной тетрагональной ячейки или субъячейки структуры.
Найденные в настоящей работе значения c/a приведены в табл. 3. Видно, что при содержании серебра до 4 ат. % с/а равно 0.94, что соответствует фазе на основе низкотемпературной модификации InPd3 со структурой Al3Zr. При содержании серебра от 7 до 18 ат. % отношение параметров тетрагональной субъячейки с/а имеет значение 0.88. Такое значение соответствует структурному типу Al3Ti, предложенному [9, 10] для высокотемпературной модификации InPd3. Таким образом, можно утверждать, что на изоконцентрате 25 ат. % In при содержании серебра от ∼7 до 18 ат. % существует тройная фаза τ со структурой Al3Ti.
Таблица 3.
Значение отношения параметров ячейки с/а для фаз InPd3 и τ системы Ag–In–Pd (образцы отжигались при 500°С)
| № | Фаза | Состав фазы, ат. % | c/a |
|---|---|---|---|
| 1 | InPd3 | Ag2.8 In22.7 Pd74.5 | 0.94 |
| 2 | InPd3 | Ag4 In22.3 Pd73.7 | 0.94 |
| 3 | τ | Ag9.9 In23.9 Pd66.2 | 0.88 |
| 4 | τ | Ag16 In24 Pd60 | 0.87 |
| 8 | τ | Ag16.1 In25.3 Pd58.6 | 0.88 |
| 9 | τ | Ag17.8 In25.1 Pd57.1 | 0.87 |
| 13 | τ | Ag17.2 In25.4 Pd57.4 | 0.87 |
| 14 | InPd3 | Ag2.7 In23.7 Pd73.6 | 0.93 |
Образование нового тройного соединения на изоконцентрате индия 25 ат. % наблюдалось авторами также и в системе Cu–In–Pd. Поскольку фактор рассеяния рентгеновского излучения у атома меди заметно отличается, на рентгенограмме были обнаружены сверхструктурные линии, которые позволили определить кристаллическую структуру тройной фазы как структуру VRh2Sn [11]. Эта структура является результатом дополнительного упорядочения структуры Al3Ti.
В табл. 4 приведены результаты исследования трех сплавов системы Ag–In–Pd методом ДТА/ДСК. Составы этих сплавов лежат на линии In13Ag87–In47Pd53 и примерно соответствуют одной из конод равновесия фазы InPd с ГЦК-твердым раствором на основе серебра.
Термодинамическое моделирование фазовых равновесий
Данные о чистых компонентах и двойных системах. Энергии Гиббса для Ag, In и Pd в жидком, ГЦК- и ОЦК-состояниях были взяты из базы данных Pure Element SGTE PURE5, которая распространяется с программным обеспечением Thermo-Calc [7].
Термодинамические описания ограничивающих двойных систем приняты по следующим источникам: Ag–In [12], Ag–Pd [13], In–Pd [14]. Эти описания с достаточной точностью воспроизводят как фазовые равновесия в указанных системах, так и результаты измерения термодинамических свойств существующих в них фаз.
Модели интерметаллических соединений. Поскольку экспериментально было установлено, что серебро практически не растворяется в соединениях InPd2 и In3Pd5, а растворимость палладия в фазе ζ системы Ag–In не превышает 2 ат. %, при термодинамическом моделировании тройной системы Ag–In–Pd растворимость третьего компонента в этих фазах не учитывалась и оценка параметров стабильности квазикомпонентов моделей этих фаз в соответствующих двойных системах, Ag–In и In–Pd, не проводилась.
Фаза InPd3, со структурой Al3Zr, растворимость серебра в которой составляет не менее 4 ат. %, описывалась двухподрешеточной моделью (Ag,Pd)0.75(In)0.25. Для воспроизведения экспериментально установленной области гомогенности фазы InPd, направленной к стороне Ag–Pd по изоконцентрате палладия, использовалась двухподрешеточная модель (Ag,In,Pd)0.5(Pd,Va)0.5.
Для описания тройной фазы τ со структурой Al3Ti использовалась модель (Ag,Pd)0.74(In,Pd)0.26, предложенная [14] для высокотемпературной модификации фазы InPd3, несмотря на то, что модель дает смещение области существования этой фазы от экспериментально установленной на 1 ат. %.
Исходные данные. Параметры моделей фаз подбирались под экспериментально установленные фазовые равновесия в системе Ag–In–Pd при 500 и 800°С. Поскольку растворимость индия в α-фазе, полученная в работе [3] при 700°С, плохо согласуется с результатами настоящего исследования, при нахождении параметров мы в основном опирались на данные настоящей работы.
При моделировании расплава использовались литературные данные по энтальпиям смешения [4] и парциальные энергии Гиббса компонентов, определенные методом ЭДС [5], а также полученные в настоящей работе температуры ликвидус.
Расчет системы Ag–In–Pd. Первоначально параметры моделей фаз подбирались под фазовые границы при каждой температуре, 500 и 800°С, отдельно, затем определялись параметры a и b в выражении $L_{{{\text{ABC}}}}^{i} = a_{{{\text{ABC}}}}^{i} + b_{{{\text{ABC}}}}^{i}T$. В заключение, в модуле PARROT пакета Thermo-Calc проводилась общая оптимизация системы.
Несмотря на использование нового термодинамического описания системы Ag–Pd [13], при высоких температурах (1000–1100°С) в богатой серебром части диаграммы наблюдалась тенденция к появлению области фиктивного расслоения ГЦК-фазы. Для ее устранения пришлось, во-первых, присвоить параметрам тройных взаимодействий в α-фазе достаточно высокие по модулю значения, а во-вторых, при окончательной оптимизации системы несколько понизить веса равновесий α + InPd.
Использовать значения параметров тройных взаимодействий для жидкости, полученные [4] при описании энтальпий образования расплава, оказалось невозможно, поскольку на рассчитанных изотермических сечениях наблюдалась избыточная стабилизация жидкой фазы. Поэтому параметры взаимодействия расплава в настоящем исследовании были найдены заново по фазовым равновесиям, энтальпиям смешения [4] и активностям компонентов [5].
Параметры моделей фаз, полученные в настоящей работе, приведены в табл. 5. Рассчитанные изотермические сечения системы Ag–In–Pd при температуре 500 и 800°С представлены на рис. 1.
Таблица 5.
Параметры моделей фаз системы Ag–In–Pd
| Фаза | Параметр | Значение, Дж/моль |
|---|---|---|
| Расплав (LIQUID) | Модель (Ag,In,Pd) | |
| 0$L_{{{\text{Ag}},{\text{In}},{\text{Pd}}}}^{{}}$ | –210 999 + 167.1T | |
| 1$L_{{{\text{Ag}},{\text{In}},{\text{Pd}}}}^{{}}$ | +8187 – 162T | |
| 2$L_{{{\text{Ag}},{\text{In}},{\text{Pd}}}}^{{}}$ | –338 955 + 109.8T | |
| α (FCC_A1) | Модель (Ag,In,Pd)(Va) | |
| 0$L_{{{\text{Ag}},{\text{In}},{\text{Pd}}:{\text{Va}}}}^{{}}$ | –643 369 + 554.28T | |
| 1$L_{{{\text{Ag}},{\text{In}},{\text{Pd}}:{\text{Va}}}}^{{}}$ | +700 000 | |
| 2$L_{{{\text{Ag}},{\text{In}},{\text{Pd}}:{\text{Va}}}}^{{}}$ | –640 199 + 202.68T | |
| InPd (BCC_B2) | Модель (Ag,In,Pd)0.5(Pd,Va)0.5 | |
| $G_{{{\text{Ag}}:{\text{Va}}}}^{{}}$ | +1000 + 0.5 GBCCAG | |
| $G_{{{\text{Ag}}:{\text{Pd}}}}^{{}}$ | +23 000 + 0.5 GBCCAG + 0.5 GBCCPD | |
| 0$L_{{{\text{Ag}},{\text{In}}:{\text{Pd}}}}^{{}}$ | –89 783 + 10.85T | |
| 0$L_{{{\text{Ag}},{\text{Pd}}:{\text{Pd}}}}^{{}}$ | –44 596T | |
| αInPd3 | Модель (In)0.25(Ag,Pd)0.75 | |
| 0$L_{{{\text{In}}:{\text{Ag}},{\text{Pd}}}}^{{}}$ | –20 000 | |
| τ (βInPd3) | Модель (In,Pd)0.26(Ag,Pd)0.74 | |
| $G_{{{\text{In}}:{\text{Pd}}}}^{{}}$ | –53 227 + 13.154T + 0.26 GHSERIN + 0.74 GHSERPD | |
| $G_{{{\text{In}}:{\text{Ag}}}}^{{}}$ | +2000 + 0.26 GHSERIN + 0.74 GHSERAG | |
| $G_{{{\text{Pd}}:{\text{Pd}}}}^{{}}$ | +100 + GHSERPD | |
| $G_{{{\text{Pd}}:{\text{Ag}}}}^{{}}$ | +100 + 0.26 GHSERPD + 0.74 GHSERAG | |
| 0$L_{{{\text{In}}:{\text{Ag}},{\text{Pd}}}}^{{}}$ | –38 584 + 8T | |
| 0$L_{{{\text{In}},{\text{Pd}}:{\text{Pd}}}}^{{}}$ | –1072 | |
В целом полученное описание системы Ag–In–Pd находится в хорошем согласии с соответствующими экспериментальными данными. Можно отметить, что расчет дает несколько заниженную растворимость серебра в фазе InPd. Однако любые попытки увеличить ее приводили к появлению расслоения α-фазы.
На рис. 2 представлено сравнение энтальпий смешения, рассчитанных по полученным в настоящей работе параметрам, с результатами аппроксимации экспериментальных данных по [4]. Можно отметить очень хорошее согласие между экспериментом и расчетом (расхождения не превышают 2 кДж/моль).
Рис. 2.
Энтальпия образования расплава, рассчитанная по разрезам (а) Pd0.5Ag0.5–In, (б) Ag0.5In0.5–Pd. Пунктир – параметры [4], сплошная линия – параметры, полученные в настоящей работе.

На рис. 3 представлено сравнение рассчитанного политермического разреза тройной системы Ag–In–Pd с полученными в настоящей работе данными ДТА (табл. 4). В целом результаты расчета и эксперимента хорошо согласуются, хотя рассчитанные температуры плавления фазы InPd несколько выше, чем установленные экспериментально. С учетом того, что результаты ДТА не использовались в процессе оптимизации при нахождении параметров моделей фаз, можно утверждать, что полученное в настоящей работе термодинамическое описание системы Ag–In–Pd является корректным и хорошо воспроизводит имеющиеся экспериментальные данные.
Рис. 3.
Рассчитанный политермический разрез системы Ag–In–Pd между составами In13Ag87–In47Pd53 (крестиками показаны данные ДТА).

Таким образом, методами СЭМ, МРСА и РФА построены изотермические сечения тройной системы Ag–In–Pd при 500°С и 800°С. В целом они согласуются с данными более раннего исследования фазовых равновесий [2, 3]. Подтверждено существование в системе Ag–In–Pd тройного соединения τ. Установлена область его существования и кристаллическая структура – Al3Ti. Методом ДТА определены температуры фазовых переходов в образцах трех составов. Температуры ликвидус использовались при нахождении параметров модели расплава, температуры фазового перехода (α + InPd + L) → (InPd + L) для проверки адекватности проведенных расчетов.
Выполнен CALPHAD-расчeт тройной системы Ag–In–Pd. Получено хорошее согласие расчетных и экспериментальных данных по фазовым границам, установленных в настоящей работе, и литературным термодинамическим данным для расплава. Корректность полученного описания системы Ag–In–Pd подтверждается хорошим согласием рассчитанных температур фазовых переходов с экспериментальными данными ДТА, не использованных при оптимизации.
Исследование выполнено за счет гранта Российского научного фонда № 22-23-00565, https://rscf.ru/project/22-23-00565/.
Список литературы
Shin H.-J., Kwon Y.H., Seol H.-J. // J. Mech. Behav. Biomed. Mater. 2020. V. 107. P. 103728. https://doi.org/10.1016/j.jmbbm.2020.103728
Zemanová A., Semenova O., Kroupa A. et al. // Monatsch. Chem. 2005. V. 136. № 11. P. 1931.https://doi.org/10.1007/s00706-005-0384-x
Zemanová A., Semenova O., Kroupa A. et al. // Intermetallics. 2007. V.15. № 1. P. 77. https://doi.org/10.1016/j.intermet.2006.03.002
Luef C., Flandorfer H., Ipser H. // Metall. Mater. Trans. A. 2005. V. 36. № 5. P. 1273. https://doi.org/10.1007/s11661-005-0219-8
Garzeł G., Zabdyr L.A. // Rare Met. 2006. V. 25. № 5. P. 587. https://doi.org/10.1016/S1001-0521(06)60104-6
STOE WinXPow, version 2.24. Darmstadt электронный ресурс. – Software package (10.2 Mb). Germany: STOE & Cie GmbH; 2009.
Thermo-Calc®-Academic (Version 2022а) электронный ресурс. – Software package (235 Mb). – Stockholm: Thermo-Calc® Software AB.; 2022.
Saunders N., Miodovnik A.P. CALPHAD (Calculation of Phase Diagrams): A comprehensive guide. London: Pergamon, 1998. 479 p.
Kohlmann H., Ritter C. // Z. Anorg. Allg. Chem. 2009. V. 635. P. 1573. https://doi.org/10.1002/zaac.200900053
Bhan S., Schubert K. // J. Less-Common Met. 1969. V. 17 P. 73. https://doi.org/10.1016/0022-5088(69)90038-1
Ptashkina E.A., Kabanova E.G., Kalmykov K.B. et al. // J. of Alloys Comps. 2020. V. 845. P. 156166. https://doi.org/10.1016/j.jallcom.2020.156166
Muzzillo C.P., Anderson T. // J. Mater. Sci. 2018. V. 53. № 9. P. 6893. https://doi.org/10.1007/s10853-018-1999-8
Pavlenko A.S., Kabanova E.G., Kuznetsov V.N. // Russ. J. Phys. Chem. A. 2020. V. 94. № 13. P. 2691. https://doi.org/10.1134/s0036024420130178
Jiang C., Liu Z.K. // Metall. Mater. Trans. A. 2002. V. 33. № 12. P. 3597. https://doi.org/10.1007/s11661-002-0235-x
Дополнительные материалы отсутствуют.
Инструменты
Журнал физической химии


