Координационная химия, 2019, T. 45, № 1, стр. 32-37
Комплексы Sm, Eu и Gd с 4-(2,1,3-бензотиадиазол-4-иламино)-пент-3-ен-2-онатомТ. С. Сухих, Д. С. Огиенко, Д. А. Баширов, Н. В. Куратьева, А. И. Смоленцев, С. Н. Конченко
Т. С. Сухих 1, 2, *, Д. С. Огиенко 1, Д. А. Баширов 1, 2, Н. В. Куратьева 1, 2, А. И. Смоленцев 1, С. Н. Конченко 1, 2
1 Институт неорганической химии им. А.В. Николаева СО РАН
, Новосибирск, Россия
2 Новосибирский государственный университет
, Новосибирск, Россия
* E-mail: sukhikh@niic.nsc.ru
Поступила в редакцию 04.04.2018
После доработки 15.06.2018
Принята к публикации 24.05.2018
Аннотация
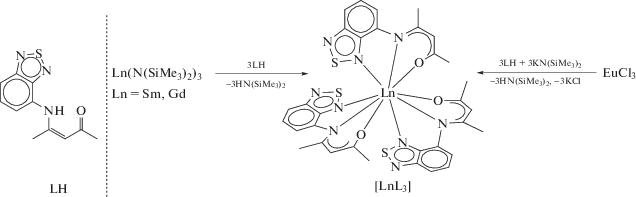
Новые комплексы лантанидов с 4-(2,1,3-бензотиадиазол-4-иламино)-пент-3-ен-2-онатом (L–) [Ln(L)3] получены двумя способами: взаимодействием Ln(N(SiMe3)2)3 с протонированной формой лиганда LH (Ln = Sm, Gd) и реакцией LnCl3 (Ln = Eu) с LH в присутствии основания KN(SiMe3)2. По данным РСА, полученные комплексы [Ln(L)3] · 0.5Solv (Solv = ТГФ, C7H8) изотипны (CIF files CCDC № 1826520, 1826521, 1826522 для Sm, Eu, Gd соответственно). Особенностью структур является разупорядочение атома металла и одного из лигандов по двум позициям, при котором фрагменты лигандов в молекуле комплексов располагаются “голова” к “хвосту”, занимая одинаковый объем пространства, что с некоторой вероятностью приводит к сбою в кристаллической упаковке. Записаны спектры фотолюминесценции [Sm(L)3] · 0.5ТГФ, выявлена корреляция способа координации лиганда и положения длинноволновой полосы электронных переходов в комплексах с лигандом L–.
2,1,3-Бензотиадиазол (Btd) и его производные – объекты, представляющие интерес как предшественники и/или составные части материалов для органических светодиодов (OLED) и другой оптоэлектроники: телекоммуникационных систем, сенсоров, преобразователей солнечной энергии и др. [1, 2]. Среди этих объектов в настоящее время наибольшее внимание уделяется органическим полимерам на основе Btd, обладающие рядом важных свойств, необходимых для создания люминесцентных функциональных материалов: 1) проявляют электроноакцепторные свойства и могут выступать в качестве буфера электронов [3–6]; 2) являются эффективными флуорофорами [7–10]; 3) формируют в твердом состоянии супрамолекулярные структуры вследствие образования сероазотных контактов и π–π-взаимодействий в сопряженных системах [11]. Наряду с сопряженными полимерными системами интерес представляют координационные молекулярные комплексы и координационные полимеры d- и f-элементов с функционализованными производными Btd. Они позволяют устранить некоторые недостатки органических полимеров, например повысить стабильность работы светоизлучающих диодов за счет более высокой термической, химической и фотохимической устойчивости, а также снять ограничение на квантовую эффективность.
Ранее на примере некоторых комплексов с лигандами-производными Btd было показано, что они обладают нетривиальными люминесцентными свойствами [12–17]. Однако соединения как d-, так и f-металлов с производными Btd в качестве лигандов все еще изучены мало, поэтому их синтез, выявление способов координации и исследование свойств, в первую очередь люминесцентных, является актуальной задачей.
Недавно мы синтезировали комплексы Zn, Ag и Cd с 4-амино-2,1,3-бензотиадиазолом [18–21] и лантанидов с 4-окси-2,1,3-бензотиадиазолатом (O-Btd)− [22, 23], обладающие интересными фотофизическими свойствами. Например, установлено, что (O-Btd)− проявляет свойства лиганда-антенны в комплексах Er и Yb: они обладают интенсивной люминесценцией в ИК-диапазоне [22, 23]. Кроме того, мы получили новый представитель класса функционализованных бензотиадиазолов – 4-(2,1,3-бензотиадиазол-4-иламино)-пент-3-ен-2-он (LH, схема 1), обладающий интенсивной эмиссией и высоким квантовым выходом [18]. Легко депротонируемая кетоиминная группа делает LH перспективным хелатирующим лигандом по отношению к d- и f-металлам. Так, ранее мы сообщали о синтезе и изучении строения и свойств комплекса [Zn(L)2] [18].
Настоящая работа направлена на развитие координационной химии этого лиганда – разработку методов синтеза и РСА комплексов самария, европия и гадолиния с L–.
Схема 1.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Коммерчески доступные безводные LnCl3 (Ln = = Sm, Eu, Gd) использовали без дополнительной очистки. Амиды лантанидов Ln(N(SiMe3)2)3 (Ln = = Sm, Gd) [24] и кетоимин LH [18] синтезировали по известным методикам. Растворители осушали кипячением и перегонкой над натрием в атмосфере аргона, после чего дегазировали многократным вакуумированием и хранили над калий-натриевым сплавом, откуда их загружали в реакционный сосуд путем конденсации в вакууме. Синтез и выделение комплексов проводили в вакуумированных сосудах без использования инертного газа. Образцы для физико-химических анализов готовили в аргоновом перчаточном боксе для предотвращения их гидролиза. Элементный анализ образцов на C, H, N, S проводили на приборе Euro EA 3000. Несколько завышенное содержание углерода и водорода в комплексе [Gd(L)3] · 0.5C7H8 связано, по-видимому, с неполным удалением растворителя из твердого образца. Спектры люминесценции твердых образцов записывали на флуоресцентном спектрофотометре Horiba Jobin Yvon Fluorolog 3 при 298 K, щель 5 × 5 нм, длина волны возбуждения 380 нм для LH и 450 нм для [Sm(L)3] · 0.5ТГФ. Коррекцию интенсивности источника излучения и спектрального отклика проводили с помощью стандартных корректировочных кривых. Спектры твердых веществ записывали для порошкообразных образцов, помещенных между двумя нефлуоресцентными кварцевыми стеклами.
РСА соединений [Ln(L)3] · 0.5Solv был выполнен на дифрактометре Bruker APEX DUO (излучение МоКα, λ = 0.71073 Å, графитовый монохроматор) при 150 K. Интенсивности отражений измерены методом φ- и ω-сканирования узких (0.5°) фреймов. Поглощение учтено по программе SADABS [25]. Структуры расшифрованы прямым методом и уточнены полноматричным МНК в анизотропном для неводородных атомов приближении по комплексу программ SHELXTL [26, 27] и графическому интерфейсу OLEX2 [28].
Атомы H локализованы геометрически и уточнены по модели “наездника”. Атомы Ln и один лиганд разупорядочены по двум позициям с общей уточняемой заселенностью от 92/8 до 84/16%. Атомы C, N, O фрагментов с меньшей заселенностью уточнены в изотропном приближении с ограничениями на некоторые длины связей DFIX, угловые расстояния DANG и отклонения атомов от плоскости кольца C6 FLAT. Для атомов сольватных молекул ТГФ и толуола, лежащих рядом с центром инверсии, было учтено разупорядочение по двум позициям с фиксированной заселенностью 50/50%. Фенильное кольцо толуола уточнено как жесткий фрагмент; на длину связи C–CH3 наложено ограничение DFIX. На длины связей и угловые расстояния молекул ТГФ также наложены соответствующие ограничения. Кристаллографические данные приведены в табл. 1.
Таблица 1.
Кристаллографические данные и результаты уточнения структур комплексов [Ln(L)3] · 0.5Solv
| Параметр | Значение | ||
|---|---|---|---|
| Брутто-формула | C35H34N9O3.5S3Sm | C35H34N9O3.5S3Eu | C36.5H34N9O3S3Gd |
| M | 883.24 | 884.85 | 900.16 |
| Сингония | Моноклинная | Моноклинная | Моноклинная |
| Пр. гр. | P21/c | P21/c | P21/c |
| a, Å | 15.2112(5) | 15.2112(5) | 15.2112(5) |
| b, Å | 14.7836(5) | 14.7836(5) | 14.7836(5) |
| c, Å | 19.0856(5) | 19.0856(5) | 19.0856(5) |
| β, град | 121.666(2) | 121.666(2) | 121.666(2) |
| V, Å3 | 3652.9(2) | 3652.9(2) | 3652.9(2) |
| Z | 4 | 4 | 4 |
| ρ (выч.), г/см3 | 1.606 | 1.609 | 1.637 |
| μ, мм–1 | 1.830 | 1.939 | 2.038 |
| F(000) | 1780.0 | 1784.0 | 1808.0 |
| Размер кристалла, мм | 0.35 × 0.23 × 0.10 | 0.30 × 0.12 × 0.08 | 0.20 × 0.10 × 0.08 |
| Диапазон сбора данных по 2θ, град | 3.726–57.398 | 3.146–51.364 | 3.146–51.364 |
| Диапазоны h, k, l | –20 ≤ h ≤ 20, –19 ≤ k ≤ 19, –22 ≤ l ≤ 25 | –18 ≤ h ≤ 18, –18 ≤ k ≤ 17, –23 ≤ l ≤ 20 | –18 ≤ h ≤ 18, –17 ≤ k ≤ 18, –23 ≤ l ≤ 23 |
| Число измеренных рефлексов | 36 586 | 25 645 | 36 976 |
| Число независимых рефлексов (Rint) | 9424 (0.0246) | 6938 (0.0226) | 6936 (0.0404) |
| Rσ | 0.0203 | 0.0194 | 0.0313 |
| Число уточняемых параметров | 536 | 536 | 572 |
| Число ограничений | 24 | 27 | 18 |
| GOOF по F 2 | 1.383 | 1.215 | 1.036 |
| R-фактор (I > 2σ(I)) | R1 = 0.0469, wR2 = 0.1042 | R1 = 0.0294, wR2 = 0.0617 | R1 = 0.0270, wR2 = 0.0550 |
| R-фактор (все данные) | R1 = 0.0484, wR2 = 0.1046 | R1 = 0.0315, wR2 = 0.0624 | R1 = 0.0360, wR2 = 0.0572 |
| Δρmax/Δρmin, e Å–3 | 1.59/–1.13 | 0.94/–0.63 | 0.70/–0.40 |
Данные РСА для структур [Ln(L)3] · 0.5Solv (Ln = Sm, Eu, Gd) депонированы в Кембриджском банке структурных данных (CCDC № 1826520–1826522; deposit@ccdc.cam.ac.uk или http:// www.ccdc.cam.ac.uk/data_request/cif) и могут быть получены у авторов.
Синтез [Sm(L)3] · 0.5ТГФ. На смесь твердых LH (0.045 г, 0.193 ммоль) и Sm(N(SiMe3)2)3 (0.040 г, 0.0633 ммоль), охлажденную жидким азотом, конденсировали ∼10 мл ТГФ. Полученный красный раствор перемешивали в течение суток при комнатной температуре, затем концентрировали до объема ∼2 мл. Образовавшиеся красные кристаллы продукта отфильтровывали и высушивали в вакууме. Выход 0.010 г (20%).
| Найдено, %: | C 47.7; | H 4.0; | N 14.0; | S 10.0. |
| Для C33H30N9O3S3Sm · 0.5C4H8O | ||||
| Вычислено, %: | C 47.6; | H 3.9; | N 14.3; | S 10.9. |
Синтез [Gd(L)3] · 0.5C7H8. На смесь твердых Gd(N(SiMe3)2)3 (0.050 г, 0.078 ммоль) и LH (0.056 г, 0.24 ммоль), охлажденную жидким азотом, конденсировали ∼10 мл толуола. Реакционную смесь перемешивали при 50°С в течение 3 сут. Темно-красный раствор фильтровали и упаривали досуха. Полученный маслянистый остаток промывали гексаном для получения порошкообразного продукта и высушивали в вакууме. Выход 0.043 г (60%). Кристаллы, пригодные для РСА, получали при упаривании раствора комплекса в смеси толуол–ТГФ (1 : 1).
| Найдено, %: | C 49.8; | H 4.6; | N 13.6; | S 10.6. |
| Для C33H30N9O3S3Gd · 0.5C7H8 | ||||
| Вычислено, %: | C 48.7; | H 3.8; | N 14.0; | S 10.7. |
Реакция EuCl3 с LH и KN(SiMe3)2. На смесь твердых LH (0.068 г, 0.29 ммоль), KN(SiMe3)2 (0.057 г, 0.028 ммоль) и EuCl3 (0.026 г, 0.10 ммоль), охлажденную жидким азотом, конденсировали ∼10 мл ТГФ. Полученный красный раствор c белесым осадком перемешивали при 50°C в течение 3 сут. Раствор фильтровали и концентрировали до 1 мл, при этом в небольшом количестве образовались пригодные для РСА красные кристаллы соединения [Eu(L)3] · 0.5ТГФ.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для синтеза комплексов Sm(III) и Gd(III) с 4-(2,1,3-бензотиадиазол-4-иламино)-пент-3-ен-2-онатом (L–) было использовано взаимодействие силилированных амидов Ln(N(SiMe3)2)3 с LH (схема 1). Это достаточно распространенный подход, основанный на взаимодействии кислотно-основного типа. В результате реакции происходит перенос протона от “сильной” кислоты LH к координированному аниону (N(SiMe3)2)−, элиминирование “слабой” кислоты HN(SiMe3)2 и координация L− к катиону лантанида. Взаимодействием Ln(N(SiMe3)2)3 с LH были получены соединения [Ln(L)3], выделенные в виде кристаллических фаз [Sm(L)3] · 0.5ТГФ и [Gd(L)3] · · 0.5C7H8 с выходами 20 и 60% соответственно.
По неизвестным причинам выход Eu(N(SiMe3)2)3 при его синтезе по стандартной методике из EuCl3 и LiN(SiMe3)2 воспроизводится нестабильно. Иногда он не превышает 10% [24]. Чтобы избежать данной стадии, для синтеза комплекса Eu(III) был использован другой вариант – взаимодействие EuCl3 c LH в присутствии сильного основания KN(SiMe3)2 (схема 1). Однако выход в данной реакции оказался крайне низким: при концентрировании маточного раствора удалось выделить лишь несколько кристаллов целевого продукта [Eu(L)3] · 0.5ТГФ.
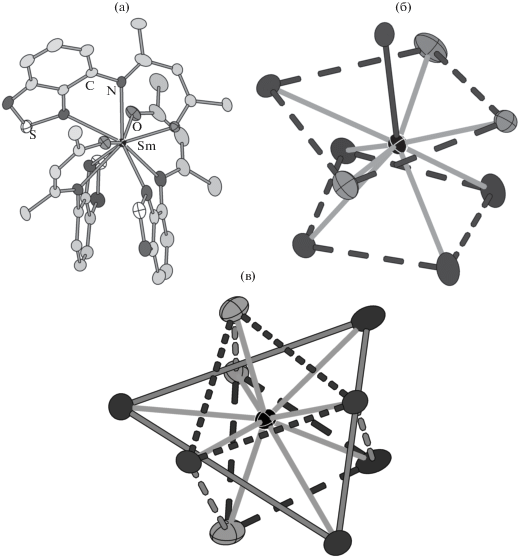
Строение всех комплексов установлено методом РСА на монокристаллах. Все полученные соединения изотипны. Различие структур состоит в наличии разных молекул сольватного растворителя: ТГФ в случае Sm и Eu и толуола для Gd. По сравнению с опубликованными ранее данными о комплексе [Zn(L)2] [18] лиганд в [Ln(L)3] · 0.5Solv связан с металлом другим способом: кроме атомов N и O кетоиминатного фрагмента в координации участвует еще атом N гетероцикла (рис. 1а). Таким образом, в данных соединениях L– является тридентатным лигандом. КЧ центрального атома равно 9, и ближайшее окружение Ln можно описать трехшапочной тригональной призмой с тремя дополнительными вершинами над боковыми гранями (рис. 1б) или квадратной одношапочной антипризмой с одной дополнительной вершиной над основанием (рис. 1в).
Рис. 1.
Строение соединений [Ln(L)3 ] · 0.5Solv на примере Ln = Sm. Эллипсоиды приведены с вероятностью 50%. Разупорядочение, атомы H и сольватные молекулы не показаны (a). Ближайшее координационное окружение Ln (б, в).
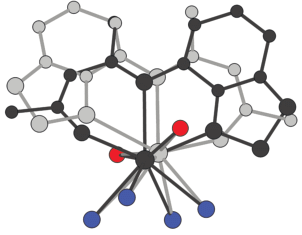
Длины связей Ln–N и Ln–O варьируют в широких пределах 2.58–2.77 и 2.28–2.36 Å соответственно, что характерно для комплексов лантанидов (анализ длин связей проводили только для фрагментов с целой и наибольшей для разупорядоченных атомов занятостью позиций, см. далее). Корреляции длины связи Ln–N и типа атома азота (тиадиазольного фрагмента или иминогруппы) не наблюдается, т.е. расположение лигандов относительно центральных атомов обусловлено в значительной степени стерическими факторами. Поскольку Sm, Eu и Gd имеют близкие ионные радиусы, значимых различий в длинах связей Ln–N и Ln–O нет. В отличие от комплекса [ZnL2] с плоским строением металлоцикла, атомы Ln в [Ln(L)3] · 0.5Solv существенно отклоняются от плоскости кетоиминатного фрагмента (в среднем на 0.8 Å). По-видимому, искажение связано с различной дентатностью лиганда (бидентатная в комплексе Zn и тридентатная в комплексах Ln). Особенностью структур исследованных соединений является то, что атом Ln и один из трех лигандов разупорядочены по двум позициям (рис. 2). В разных кристаллах их уточненная заселенность составляет от 92/8 до 84/16%. Расстояние между разупорядоченными атомами Ln не превышает 0.62 Å. Соответствующие координированные гетероатомы в лиганде также попарно имеют близкие позиции, однако атом O одного разупорядоченного фрагмента находится рядом с атомом N гетероцикла другого, т.е. данные фрагменты располагаются по типу “голова” к “хвосту” (рис. 2). Несмотря на такое расположение, разупорядоченные фрагменты занимают практически идентичный объем пространства, что и приводит к сбою в упаковке молекул комплексов. Данный феномен разупорядочения обнаружен для всех образцов монокристаллов комплексов.
Рис. 2.
Схема разупорядочения центрального атома и лиганда соединений [Ln(L)3 ] · 0.5Solv на примере Ln = Sm.
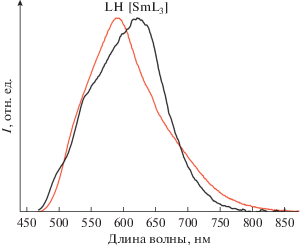
Таким образом, в комплексах тиадиазольные фрагменты находятся достаточно близко к центральным атомам, что немаловажно для осуществления эффективного переноса энергии возбуждения с лиганда на ионы лантанидов [29]. С другой стороны, цвет комплексов [Ln(L)3] · 0.5Solv ярко-красный, т.е. полоса эмиссии ионов Sm3+ и Eu3+ слишком близка по энергии к полосе поглощения комплексов и, как следствие, процесс переноса энергии с лиганда на эти лантаниды с последующим излучением маловероятен [29]. Действительно, в спектре эмиссии [Sm(L)3] · 0.5ТГФ не наблюдается характерной лантанид-центрированной люминесценции, а лишь широкая полоса, относящаяся к внутрилигандным переходам (рис. 3). Максимум этой полосы при 625 нм сдвинут в длинноволновую область по сравнению со свободным LH (595 нм). Важно отметить, что комплекс [Zn(L)2] с бидентатной координацией лиганда только атомами кетоиминатного фрагмента имеет желтый цвет: положение длинноволновой полосы поглощения этого соединения практически идентично таковой для исходного LH [18]. На основании имеющихся данных можно заключить, что батохромный сдвиг длинноволновой полосы комплексов [Ln(L)3] · 0.5Solv определен наличием связи металла с атомом N гетероцикла, отсутствующей в [Zn(L)2]. Подобный феномен наблюдается и в ряде комплексов Zn, Cd и Ag с архетипным 4-амино-2,1,3-бензотиадиазолом [18–21]: в том случае, когда этот лиганд координирован монодентатно атомом N аминогруппы, полоса поглощения и эмиссии смещена в коротковолновую область. Если лиганд координирован монодентатно атомом N гетероцикла или мостиковым образом, то данная полоса смещается в длинноволновую область. С этим предположением согласуются как экспериментальные данные, так и результаты квантово-химических расчетов [20].
Таким образом, в настоящей работе получены новые комплексы с 4-(2,1,3-бензотиадиазол-4-иламино)-пент-3-ен-2-онатом [Ln(L)3] · 0.5Solv (Ln = Sm, Eu, Gd; Solv = ТГФ, C7H8), строение которых установлено методом РСА. В структурах обнаружен феномен разупорядочения, возникающего из-за близких объемов кетоиминового и бензотиадиазольного фрагментов. Обнаружена корреляция способа координации лиганда и положения длинноволновой полосы в электронных спектрах комплексов с L–.
Авторы благодарят А.П. Зубареву и О.С. Кощееву за проведение элементного анализа и А.А. Рядуна за запись спектров люминесценции.
Работа выполнена в рамках реализации государственного задания и при финансовой поддержке Российского фонда фундаментальных исследований (№ 16-03-00637).
Список литературы
Neto B.A.D., Lapis A.A.M., da Silva Júnior E.N. et al. // Eur. J. Org. Chem. 2013. P. 228.
Gu C., Liu D., Wang J. et al. // J. Mater. Chem. A. 2018. V. 6. P. 2371.
Crossley D.L., Urbano L., Neumann R. et al. // ACS Ap-pl. Mater. Interfaces. 2017. V. 9. P. 28243.
Chulanova E.A., Pritchina E.A., Malaspina L.A. et al. // Chem. Eur. J. 2017. V. 23. P. 852.
Lonchakov A., Rakitin O., Gritsan N, et al. // Molecules. 2013. V. 18. P. 9850.
Xu Z., Kong L., Wang Y, et al. // Org. Electron. 2018. V. 54. P. 94.
Neto B.A.D., Carvalho P.H.P.R., Correa J.R. // Acc. Chem. Res. 2015. V. 48. P. 1560.
da Cruz E.H.G., Carvalho P.H.P.R., Correa J.R. et al. // New J. Chem. 2014. V. 38. P. 2569.
Mota A.A.R., Corrêa J.R., Carvalho P.H.P.R. et al. // J. Org. Chem. 2016. V. 81. P. 2958.
Aguiar L.d.O., Regis E., Tuzimoto P. et al. // Liq. Cryst. 2018. V. 45. P. 49.
Langis-Barsetti S., Maris T., Wuest J.D. // J. Org. Chem. 2017. V. 82. P. 5034.
Cheng Q., Han X., Tong Y. et al. // Inorg. Chem. 2017. V. 56. P. 1696.
Plebst S., Bubrin M., Schweinfurth D. et al. // Z. Naturforsch. B. 2017. V. 72. P. 839.
Goswami S., Winkel R.W., Schanze K.S. // Inorg. Chem. 2015. V. 54. P. 10007.
Mancilha F.S., Barloy L., Rodembusch F.S. et al. // Dalton Trans. 2011. V. 40. P. 10535.
Gallardo H., Conte G., Bortoluzzi A.J. et al. // Inorg. Chim. Acta. 2011. V. 365. P. 152.
Gallardo H., Conte G., Tuzimoto P. et al. // Inorg. Chem. Commun. 2008. V. 11. P. 1292.
Sukhikh T.S., Bashirov D.A., Ogienko D.S. et al. // RSC Adv. 2016. V. 6. P. 43901.
Sukhikh T.S., Ogienko D.S., Bashirov D.A. et al. // J. Coord. Chem. 2016. V. 69. P. 3284.
Sukhikh T.S., Komarov V.Y., Konchenko S.N. et al. // Polyhedron. 2018. V. 139. P. 33.
Sukhikh T.S., Bashirov D.A., Shuvaev S. et al. // Polyhedron. 2018. V. 141. P. 77.
Sukhikh T.S., Bashirov D.A., Kolybalov D.S. et al. // Polyhedron. 2017. V. 124. P. 139.
Sukhikh T.S., Bashirov D.A., Kuratieva N.V. et al. // Dalton Trans. 2015. V. 44. P. 5727.
Herrmann W.A. Synthetic Methods of Organometallic and Inorganic Chemistry: Lanthanides and Actinides. Thieme Publishing Group, 1997. V. 6.
APEX2 (version 2.0). SAINT (version 8.18c), and SADABS (version 2.11). Madison (WI, USA): Bruker Advanced X-ray Solutions, 2000–2012.
Sheldrick G.M. // Acta Crystallogr. A. 2008. V. 64. P. 112.
Sheldrick G.M. // Acta Crystallogr. C. 2015. V. 71. P. 3.
Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. A-ppl. Crystallogr. 2009. V. 42. P. 339.
Armelao L., Quici S., Barigelletti F. et al. // Coord. Chem. Rev. 2010. V. 254. P. 487.
Дополнительные материалы отсутствуют.
Инструменты
Координационная химия