Нефтехимия, 2020, T. 60, № 5, стр. 701-707
Катализаторы эпоксидирования циклогексена на основе пористых ароматических каркасов
Л. А. Куликов 1, *, В. А. Ярчак 1, А. В. Золотухина 1, 2, А. Л. Максимов 1, 2, Э. А. Караханов 1
1 Московский государственный университет имени М.В. Ломоносова, Химический факультет
119991 Москва, Россия
2 Институт нефтехимического синтеза им. А.В. Топчиева РАН
119991 Москва, Россия
* E-mail: mailforleonid@mail.ru
Поступила в редакцию 28.04.2020
После доработки 12.05.2020
Принята к публикации 12.05.2020
Аннотация
Молибденовый и вольфрамовый катализаторы PAF-30-Mo и PAF-30-W, синтезированные на основе пористого ароматического каркаса PAF-30, были испытаны в эпоксидировании циклогексена трет-бутилгидропероксидом. Изучено влияние температуры и соотношение субстрата к окислителю на особенности протекания процесса. Показано, что катализаторы проявляют высокую активность и позволяют получать с высоким выходом эпоксидциклогексена, однако теряют свою активность со временем из-за вымывания металла из пор полимера.
Эпоксиды – важнейший класс органических соединений в современной полимерной и нефтехимической промышленности. Их широко применяют в тонком органическом синтезе, в производстве красителей, поверхностно-активных веществ, лекарств, пластификаторов, полимеров и т.п. [1–3]. Общий метод получения эпоксидов – селективное окисление олефинов. Однако, способ окисления зависит от структуры олефина. Так, промышленный способ производства оксида этилена основан на прямом окислении этилена кислородом воздуха на серебряных катализаторах [4]. Окисление пропилена в тех же условиях неселективное, иприводит к образованию акролеина в качестве второго продукта. Из-за этого получение оксида пропилена осуществляют либо по хлоргидринному методу [4], либо по более современным методам окисления пропилена органическими гидропероксидами в присутствии различных катализаторов [1]. Несмотря на успешность внедрения в промышленность новых способов получения эпоксидов, все еще актуальна разработка новых катализаторов эпоксидирования олефинов.
Как правило, основой таких катализаторов служат комплексы и соли различных переходных металлов – молибдена [5, 6], титана [7], ванадия [8], вольфрама [9] и т.п. Данные металлы в высшей степени окисления обладают низкими потенциалами окисления, благодаря чему они достаточно легко образуют пероксидные соединения и проявляют высокую активность в реакции эпоксидирования [10]. Среди них наибольшую активность проявляет молибден и его различные комплексные соединения, например Mo(CO)6, MoO2(acac)2, MoO2-фталоцианин, MoO2(октан-1,2-диол)2, MoO2(циклогексан-1,2-диол)2, MoO2(оксинат)2 [11]. Благодаря этому, а также доступности и относительно низкой цене, катализаторы на основе молибдена получили широкое распространение как в лаборатории, так и в промышленности [12]. Например, для получения оксида пропилена по Халкон-процессу в качестве катализатора применяют нафтенат молибдена [13, 14].
Наибольший интерес представляют гетерогенные катализаторы эпоксидирования олефинов. По сравнению с гомогенными катализаторами они стабильнее и их проще отделять от продуктов реакции. Были синтезированы и изучены катализаторы эпоксидирования олефинов на основе соединений молибдена, гетерогенизированных на различных носителях: цеолитах [15–17], мезопористых силикагелях [18–21], металл-органических каркасах (MOFs) [22–25], полимерах [26–29], оксиде графена [30, 31]. Стоит отметить, что свойства таких катализаторов во многом определяются свойствами носителя: особенностями его взаимодействия с реагентами и комплексом молибдена, пористостью, химическим строением и природой.
Ранее нами были синтезированы молибденовые и вольфрамовые катализаторы окисления сернистых соединений на основе пористых ароматических каркасов (PAF) [32] – углеродных материалов, состоящих из соединенных в прочную, жесткую пористую структуру остатков ароматических молекул. Катализаторы проявили высокую активность в окислении различного класса серосодержащих соединений в мягких условиях. Отмечалось, что носитель сохранил свою структуру в присутствии окислителей, пероксида водорода и трет-бутилгидропероксида, что делает PAF перспективными материалами для создания катализаторов различных окислительных процессов.
Данная работа посвящена изучению активности данных катализаторов в эпоксидировании представителя олефинов – циклогексена.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реактивы. В работе применяли следующие реактивы: 1,2-дихлорэтан (х. ч., Экос-1), трет-бутилгидропероксид (70%-ный раствор в воде, Aldrich), циклогексен (99%, Aldrich), толуол (ос. ч., Химмед).
Синтез катализаторов PAF-30-Mo, PAF-30-W. Подробная методика синтеза катализаторов изложена в работе [32]. Она включает растворение Mo(CO)6 (486 мг) или W(CO)6 (338 мг) в мезитилене (40 мл) при 100°С в обернутой фольгой колбе (для предотвращения попадания света), добавление PAF-30 (1 г) и перемешивание полученной суспензии при 155°С в течение 5 ч. Далее полученный катализатор выделяли из реакционной смеси фильтрованием, промывали небольшим количеством толуола, затем гексаном, после чего сушили при 50°С в вакууме. Оба катализатора содержали наночастицы металла; наблюдалось также уменьшение удельной площади поверхности и объема пор при введении в носитель металлов. Характеристики катализаторов и исходного носителя представлены в табл. 1.
Таблица 1.
Характеристики исходного материала PAF-30 и катализаторов на его основе
| Материал | Площадь поверхности, м2/г | Объем пор, см3/г | Средний размер частиц Me, нм | Содержание металла, мас. % |
|---|---|---|---|---|
| PAF-30 | 383 | 0.21 | – | – |
| PAF-30-Mo | 79 | 0.05 | 5.2 | 9.44 |
| PAF-30-W | 124 | 0.08 | 6.7/5.6* | 6.28 |
Проведение каталитических экспериментов. В стеклянный реактор, оснащенный рубашкой для подачи теплоносителя и двумя горлышками, помещали якорь магнитной мешалки, предварительно взвешенные 20 мг катализатора, 5 мл дихлорэтана, 0.5 мл циклогексена, 0.5 мл толуола (в качестве внутреннего стандарта). Реактор присоединяли к термостату и снабжали обратным холодильником с септой и иглой наверху. Далее к смеси быстро через второе горлышко добавляли необходимое количество трет-бутилгидропероксида (1 мл в типичных экспериментах), после чего в него вставляли септу и включали перемешивание. Эпоксидирование проводили при температуре 60–80°С, отбор проб осуществляли через септу с помощью шприца. Объем отбираемой пробы не превышал 20 мкл.
Приборы и методы. Газовая хроматография. Состав продуктов реакции определяли на газовом хроматографе HewlettPackard 6890, оснащеннoм пламенно-ионизационным детектором и колонкой HP-1 (50 м × 0.32 мм × 1.05 мкм, фаза – 100% диметилсилоксан). Газ-носитель – гелий. Режим анализа – постоянный поток, 1 мл/мин. Запись и обработку хроматограмм производили с помощью программы HPChemStationRev.A.06.01 (403). Содержание продуктов определяли по отношению площадей соответствующих пиков и площади внутреннего стандарта.
Просвечивающая электронная микроскопия (ПЭМ) высокого разрешения. Микрофотографии катализаторов были получены на приборе JEOL JEM-2100F/Cs/GIF (разрешение изображения: 0.19 нм). Потенциал электронного пучка составлял 200 кВ. Обработку микрофотографий производили с помощью программы ImageJ.
Рентгеновская фотоэлектронная спектроскопия (РФЭС). Состав поверхности катализаторов определяли при помощи метода РФЭС на приборе PHI5500VersaProbeII. Для возбуждения фотоэмиссии использовали монохроматизированное AlKα-излучение (hν = 1486.6 эВ). Напряжение на аноде составляло 14 кВ, мощность – 50 Вт. Давление остаточных газов в тестовой камере в процессе измерений составляло (5–7) × 10–8 Па.
Метод атомно-эмиссионной спектрометрии с индуктивно-связанной плазмой (АЭС-ИСП). Содержание молибдена было определено при помощи метода АЭС-ИСП на приборе IRISInterpidIIXPL (ThermoElectronCorp., США).
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Окисление циклогексена проводили на молибденовом и вольфрамовом катализаторах PAF-30-Mo и PAF-30-W, синтез и подробное описание свойств которых приведено в работе [32]. Отметим, что катализатор PAF-30-Mo содержал 9.44 мас. %. молибдена, металл был равномерно распределен по объему носителя в виде наночастиц и кластеров металлов. Средний размер частиц металла составлял 5.2 нм, что немногим больше среднего размера пор в исходном носителе PAF-30. В случае катализатора PAF-30-W содержание металла было 6.28 мас. %, при этом часть частиц располагалась на поверхности носителя. Средний размер частиц металла внутри пор материала составлял около 5.6 нм, а усредненный размер всех частиц металла – 6.7 нм.
Катализаторы были испытаны в эпоксидировании циклогексена. Кроме того, были поставлены дополнительные эксперименты без катализатора и с использованием в качестве катализаторов исходного носителя PAF-30 и молибдата аммония (табл. 2). Заметные количества эпоксида циклогексена образовывались только в присутствии катализаторов PAF-30-W и PAF-30-Mo. Молибденовый катализатор был активнее вольфрамового, что согласуется с литературными данным [11, 33].
Таблица 2.
Эпоксидирование циклогексена в присутствии различных катализаторов и соединений
| Катализатор | Выход эпоксида |
|---|---|
| Без катализатора | <1% |
| PAF-30 | <1% |
| (NH4)2MoO4 | 2% |
| PAF-30-W | 14% |
| PAF-30-Mo | 88% |
Условия реакции: 80°C; 3 ч; 0.5 мл циклогексена, 5 мл дихлорэтана, 1 мл трет-бутил гидропероксид : циклогексена; 20 мг катализатора (2 мг в случае (NH4)2MoO4).
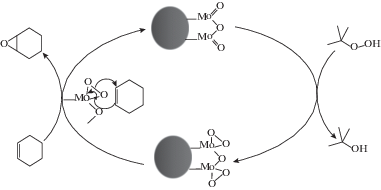
Механизм протекания окисления на поверхности наночастиц молибдена обсуждался ранее нами [32], а также в работе [34]. В случае эпоксидирования циклогексена, он упрощенно может быть выражен в следующей схеме (рис. 1): вначале происходит окисление поверхности молибдена с образованием пероксидных групп; далее циклогексен координируется и внедряется по связи Mo–O пероксидной группы с образованием эпоксида, после чего цикл повторяется.
Стоит отметить, что катализаторы проявили высокую селективность: основным продуктом реакции был эпоксидциклогексен. Побочные продукты, образующиеся при окислении углерода в α-положении при двойной связи (циклогексенол, циклогексенон, циклогексен-трет-бутил-пероксид) [35], или при раскрытии оксиранового кольца (циклогександиолы) либо не были обнаружены, либо содержались в следовых количествах. Так как наибольшую активность проявил молибденовый катализатор PAF-30-Mo, то дальнейшие эксперименты по изучению кинетических особенностей протекания реакции эпоксидирования циклогексена проводили с его использованием.
На рис. 2 представлены кинетические кривые процесса эпоксидирования циклогексена на катализаторе PAF-30-Mo при различных температурах. При 60°C кинетическая кривая описывается линейным уравнением, что говорит о независимости скорости процесса от концентраций субстрата и окислителя. Можно предположить, что в данном случае лимитирующей стадией является образование пероксо-комплексов молибдена. С другой стороны, это может быть связано с диффузионными ограничениями субстратов к поверхности частиц молибдена [34, 36]. Интересно отметить, что в первые 10 мин реакции выход составил всего 1%, в дальнейшем скорость реакции увеличилась. Данный индукционный период наблюдался и для других температур, и может быть связан с окислением поверхности молибдена и образованием пероксо-комплексов. За 3 ч реакции выход циклогексена составил 29%.
При увеличении температуры до 70°C скорость реакции незначительно возрастает. Вид кинетической кривой также близок к линейному. Однако можно заметить, что в первые 30 мин скорость реакции была выше, чем в конце реакции. После 30 мин скорость окисления циклогексена становится постоянной. Это может объясняться увеличением скорости образования активного пероксидного комплекса на поверхности частиц молибдена, и, как следствие, возрастающей ролью диффузии циклогексена к активным центрам катализатора.
Наибольшей скорости окисления циклогексена удалось достичь при температуре реакции 80°C. Как и в предыдущих экспериментах, в начале процесса наблюдается индукционный период. Также скорость реакции уменьшается с увеличением конверсии субстрата. Данный вид кинетической зависимости характерен для процесса эпоксидирования циклогексена на гетерогенных катализаторах [34, 37, 38].
Было изучено влияние соотношения субстрат : окислитель на выход эпоксидациклогексена (рис. 3). С увеличением количества окислителя в системе происходит увеличение конверсии циклогексена с 47 до 88%. Однако, дальнейшее увеличение соотношения субстрат : окислитель от 1 : 1 до 1 : 2 и 1 : 4 приводит к падению активности катализатора. Это может объясняться адсорбцией кислородсодержащих соединений, в первую очередь воды, находящейся в растворе трет-бутилгидропероксида, на поверхности частиц молибдена, а также следующей за адсорбцией деактивацией катализатора.
Рис. 3.
Зависимость конверсии циклогексена от соотношения субстрат : окислитель. Условия реакции: 80°С; 3 ч; 0.5 мл циклогексена, 5 мл 1,2-дихлорэтана; 20 мг PAF-30-Mo.

После реакции катализатор был выделен, промыт спиртом, водой и еще раз спиртом, после чего исследован методами РФЭС и ПЭМ высокого разрешения, и испытан повторно.
Согласно данным РФЭС, поверхностная концентрация молибдена существенно снизилась, что говорит о его вымывании из катализатора (табл. 3, 4). Аналогичные данные получены и при исследовании содержания молибдена методом АЭС-ИСП: содержание металла снизилось с 9.44 до 5.18 мас. %. При этом оставшийся молибден по большей части представлен валентным состоянием триоксидом молибдена MoO3, и в меньшей степени – смешанным оксидом молибдена MoOx (x = 2–3).
Таблица 3.
Содержание элементов на поверхности катализатора PAF-30-Mo до и после реакции
| Элемент | Содержание в PAF-30-Mo, ат. % | |
|---|---|---|
| до реакции | после реакции | |
| С | 85.8% | 88.9% |
| O | 12.0% | 10.2% |
| Mo | 1.8% | 0.6% |
| P | 0.4% | 0.3% |
Таблица 4.
Содержание различных форм молибдена на поверхности катализатора PAF-30-Mo до и после реакции
| Катализатор | Валентное состояние и содержание, % | Энергия связывания электронов, эВ |
|---|---|---|
| PAF-30-Mo до реакции | Mo0, 1% | 3d5/2, 227.78 3d3/2, 230.80 |
| MoOx (x = 2–3), 60% | 3d5/2, 231.53 3d3/2, 234.77 |
|
| MoO3, 39% | 3d5/2, 232.86 3d3/2, 236.02 |
|
| PAF-30-Mo после реакции | MoOx (x = 2–3), 15% | 3d5/2, 232.07 3d3/2, 235.55 |
| MoO3, 84% | 3d5/2, 232.89 3d3/2, 236.11 |
Микрофотографии катализатора после реакции представлены на рис. 4. Катализатор все еще содержит значительное количество наночастиц молибдена. Агломерации частиц не наблюдается.
Катализатор был повторно испытан в эпоксидировании циклогексена (рис. 5). Как видно из кинетической кривой, активность катализатора существенно снижается на втором цикле использования, что связано с вымыванием молибдена из носителя. Чтобы понять, какая форма молибдена в действительности катализирует процесс эпоксидирования, нами был поставлен дополнительный эксперимент. Реакция была проведена со свежим катализатором и остановлена после одного часа ее проведения. Реакционная среда была отделена от катализатора и помещена в реактор повторно. При этом наблюдалась остановка каталитического процесса. Это означает, что наибольшую активность в эпоксидировании циклогексена проявляет именно молибден, иммобилизованный в порах ароматического каркаса.
ЗАКЛЮЧЕНИЕ
Исследована активность в эпоксидировании циклогексена катализаторов на основе пористых ароматических каркасов. Показано, что катализаторы на основе данных носителей могут быть использованы в окислительных процессах при высоких концентрациях окислителя. Молибденовые катализаторы активнее вольфрамовых, что согласуется с литературными данными. С ростом температуры возрастает скорость реакции, что может быть связано с увеличением скорости диффузии субстратов к активным центрам катализатора. Показано, что металл вымывается из пор катализатора, из-за чего катализатор теряет активность. Данная проблема может быть решена с помощью перехода от катализаторов на основе наночастиц к катализаторам на основе иммобилизованных комплексов металлов.
Список литературы
Oyama S.T., Mechanisms in Homogeneous and Heterogeneous Epoxidation Catalysis. 1st ed. Elsevier Science, 2008. 528 p
Yudin A.K., Aziridines and Epoxides in Organic Synthesis. Wiley: VCH, 2006. 492 p.
Baigrie B.D. // Food Chem. 1986. V. 21. № 3. P. 238.
Лебедев Н. Химия и технология основного органического и нефтехимического синтеза. М.: Химия, 1988. 592 с.
Pisk J., Rubčić M., Kuzman D., Cindrić M., Agustin D., Vrdoljak V. // New J. Chem. 2019. V. 43. № 14. P. 5531.
Wang G., Chen G., Luck R.L., Wang Z., Mu Z., Evans D.G., Duan X. // Inorganica Chim. Acta. 2004. V. 357. № 11. P. 3223.
Fraile J.M., García J.I., Mayoral J.A., Vispe E. // Appl. Catal. A Gen. 2003. V. 245. № 2. P. 363.
Vandichel M., Leus K., Van Der Voort P., Waroquier M., Van Speybroeck V. // J. Catal. 2012. V. 294. P. 1.
Xiao Y., Liu J., Mai J., Pan C., Cai X., Fang Y. // J. Colloid Interface Sci. 2018. V. 516. P. 172.
Shen Y., Jiang P., Wai P.T., Gu Q., Zhang W. // Catalysts. 2019. V. 9. № 1. Article 31. P. 1.
Sheldon R.A. // J. Mol. Catal. 1980. V. 7. № 1. P. 107.
Morales-delaRosa S., Campos-Martin J.M., Terreros P., Fierro J.L.G. // Top. Catal. 2015. V. 58. № 4–6. P. 325.
Tsuji J., Yamamoto J., Ishino M., Kagaku N.O. // Sumitomo Kagaku. 2006. V. 1. P. 1.
Calderazzo F., Carmona D., Catellani M., Brintzinger H. Metal-Catalysis in Industrial Organic Processes. RSC Publishing, 2006. 290 p.
Bagherzadeh M., Hosseini H. // J. Coord. Chem. 2017. V. 70. № 13. P. 2212.
Sakthivel A., Zhao J., Kühn F.E. // Springer. 2005. V. 102. № 3–4. P. 115.
Dai P.S.E., Lunsford J.H. // J. Catal. 1980. V. 64. № 1. P. 184.
Coelho A.C., Balula S.S., Bruno S.M., Alonso J.C., Bion N., Ferreira P., Pillinger M., Valente A.A., Rocha J., Gonçalves I.S. // Adv. Synth. Catal. 2010. V. 352. № 10. P. 1759.
Bagherzadeh M., Hosseini H., Akbayrak S., Özkar S. // Chemistry Select. 2019. V. 4. № 19. P. 5911.
Ishikawa S., Maegawa Y., Waki M., Inagaki S. // ACS Catal. 2018. V. 8. № 5. P. 4160.
Jia M., Seifert A., Thiel W.R. // Chem. Mater. 2003. V. 15. № 11. P. 2174.
Afzali N., Tangestaninejad S., Moghadam M., Mirkhani V., Mechler A., Mohammadpoor-Baltork I., Kardanpour R., Zadehahmadi F. // Appl. Organomet. Chem. 2018. V. 32. № 1. V. 32. № 1. Article aoc. 3959. P. 1
Abednatanzi S., Abbasi A., Masteri-Farahani M. // J. Mol. Catal. A Chem. 2015. V. 399. P. 10.
Abednatanzi S., Abbasi A., Masteri-Farahani M. // New J. Chem. 2015. V. 39. № 7. P. 5322.
Song X., Hu D., Yang X., Zhang H., Zhang W., Li J., Jia M., Yu J. // ACS Sustain. Chem. Eng. 2019. V. 7. № 3. P. 3624.
Tangestaninejad S., Moghadam M., Mirkhani V., Mohammadpoor-Baltork I., Torki M. // Comptes Rendus Chim. 2011. V. 14. № 6. P. 604.
Grivani G., Halili A. // J. Iran. Chem. Soc. 2014. V. 11. № 1. P. 163.
Grivani G., Tangestaninejad S., Halili A. // Inorg. Chem. Commun. 2007. V. 10. № 8. P. 914.
Miller M.M., Sherrington D.C. // J. Catal. 1995. V. 152. № 2. P. 368.
Masteri-Farahani M., Mirshekar S. // Colloids Surfaces. A Physicochem. Eng. Asp. 2018. V. 538. P. 387.
Masteri-Farahani M., Ghahremani M. // J. Phys. Chem. Solids. 2019. V. 130. P. 6.
Kulikov L.A., Akopyan A.V., Polikarpova P.D., Zolotukhina A.V., Maximov A.L., Anisimov A.V., Karakha-nov E.A. // Ind. Eng. Chem. Res. 2019. V. 58. № 45. P. 20 562.
Sheldon R.A., Van Doorn J.A. // J. Catal. 1973. V. 31. № 3. P. 427.
Shen Y., Jiang P., Wai P. T., Zhang P., Dong Y. // J. Saudi Chem. Soc. 2019. V. 23. № 8. P. 1157.
Khare S., Shrivastava S. // J. Mol. Catal. A Chem. 2004. V. 217. № 1–2. P. 51.
Shen Y., Jiang P., Wang Y., Bian G., Wai P.T., Dong Y. // J. Solid State Chem. 2018. V. 264. P. 156.4
Shen Y., Jiang P., Zhang J., Bian G., Zhang P., Dong Y., Zhang W. // Mol. Catal. 2017. V. 433. P. 212.
Zhang J., Jiang P., Shen Y., Zhang W., Li X. // Micro-porous Mesoporous Mater. 2015. V. 206. № C. P. 161.
Дополнительные материалы отсутствуют.