Неорганические материалы, 2021, T. 57, № 6, стр. 663-669
Получение и исследование оптических свойств стекол системы TeO2–MoO3–Pr2O3
М. Ф. Чурбанов 1, 2, А. А. Сибиркин 1, 2, *, В. М. Горяев 1, Л. В. Булдакова 1
1 Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, пр. Гагарина, 23, Россия
2 Институт химии высокочистых веществ им. Г.Г. Девятых Российской академии наук
603950 Нижний Новгород, ул. Тропинина, 49, Россия
* E-mail: as641641@yandex.ru
Поступила в редакцию 09.11.2020
После доработки 11.12.2020
Принята к публикации 16.12.2020
Аннотация
Исследовано стеклообразование в системе TeO2–MoO3–Pr2O3, установлены границы области стеклообразования. Показана возможность получения стекол, содержащих до 30 мол. % PrO1.5. Рассчитаны оптические характеристики спектров пропускания полученных образцов.
ВВЕДЕНИЕ
Интерес к празеодимсодержащим теллуритно-молибдатным стеклам обусловлен возможностью их применения в магнитооптике. Для изготовления компактных магнитооптических устройств необходимы вещества с большой величиной постоянной Верде. Это может быть достигнуто введением в стекло достаточного количества оксида празеодима. Материалы для изготовления магнитооптических элементов должны быть прозрачными для преобразуемого излучения во избежание их разогрева и, как следствие, разрушения элемента [1, 2]. Этим требованиям удовлетворяют празеодимсодержащие теллуритно-молибдатные стекла, которые прозрачны в видимой и ближней инфракрасной областях спектра. Теллуритно-молибдатные расплавы способны растворять достаточное количество оксидов редкоземельных элементов, что необходимо для получения стекол с высоким содержанием оксида празеодима. Этот компонент обладает наиболее высокой величиной удельного вращения плоскости поляризации электромагнитного излучения [3] среди редкоземельных элементов.
Цель работы – исследование стеклообразования в системе TeO2–MoO3–Pr2O3, установление границ области стеклообразования, изучение оптических свойств празеодимсодержащих теллуритно-молибдатных стекол.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Для синтеза стекол использовали бинарные оксиды теллура, молибдена и празеодима. Диоксид теллура TeO2 квалификации “ч.” (ТУ 6-09-1401-76) использовали без предварительной обработки. Триоксид молибдена MoO3 получали термическим разложением гептамолибдата аммония (NH4)6Mo7O24 ⋅ 4H2O квалификации “ч. д. а.” (ГОСТ 3765-78) в результате длительного нагревания на воздухе при температуре 400°С, что позволяло достичь полноты разложения исходного вещества и получить триоксид молибдена с возможно более низким содержанием молибдена в промежуточных состояниях окисления. Оксид празеодима Pr6O11 получали прокаливанием при 500°С на воздухе нитрата празеодима Pr(NO3)3 ⋅ 6H2O, полученного действием избытка раствора азотной кислоты (квалификация “х. ч.” по ГОСТ 4461-77) на товарный оксид празеодима марки ПрО-1 (ТУ 48-4-183-72). Это обеспечивало нахождение празеодима в заданной химической форме.
Рассчитанные количества бинарных оксидов, отвечающие составу стекла, были взвешены на аналитических весах Shimadzu AUX320 с точностью 0.0001 г и тщательно перемешаны в фарфоровой ступке. Полученную шихту нагревали в глазурованном фарфоровом тигле в муфельной печи ПМ-12 для расплавления при температуре 800–1000°С в зависимости от содержания оксида празеодима в шихте в течение 15–20 мин для гомогенизации. Извлеченный из печи расплав перемешивали на воздухе в течение 5–10 с и выливали в стальную разборную форму, выдержанную при температуре 300–400°С. Скорость охлаждения расплава, соответствующая условиям формования стекол, оценивается величиной порядка 10 К/с [4]. Полученные образцы стекол в виде пластин толщиной 2.5–5 мм охлаждали в режиме выключенной печи от 300–400 до 30–70°C в течение 10–18 ч.
Стеклообразный характер образцов подтверждали методом рентгеновской дифрактометрии на дифрактометре Shimadzu XRD-6000 (излучение CuKα, сканирование в диапазоне 2θ от 10° до 60° со скоростью 4 град/мин). Плотность образцов стекол определена методом гидростатического взвешивания. Спектры пропускания получены на двухлучевом спектрофотометре Shimadzu UV-3600 в диапазоне длин волн 400–2500 нм с шагом сканирования 2 нм.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Область стеклообразования. На рис. 1 отмечены границы области стеклообразования системы TeO2–MoO3–PrO1.5. Эта область охватывает интервал содержаний (мол. %): 25–90 TeO2, 10–75 MoO3, до 30 PrO1.5. В отсутствие оксида празеодима интервал стеклообразования подсистемы TeO2–MoO3 находится в пределах 10–75 мол. % MoO3, что хорошо согласуется со значениями 30–70% [5], 12.5–58.5% [6], 12–62% [7] и приближается к составу 20–50% [8]. Наиболее высокое содержание оксида празеодима в теллуритно-молибдатном стекле, равное 30 мол. % PrO1.5, достигнуто на образце с равным мольным содержанием оксидов теллура и молибдена.
Стеклообразное состояние исследованных образцов подтверждено методом рентгенофазового анализа. Порошковые дифрактограммы не содержат узких интенсивных пиков, характерных для кристаллических веществ.
Плотность и молярный объем стекол. Плотность образцов стекла определяли по методу Архимеда. Молярный объем стекол Vm как функция мольной доли каждого компонента рассчитан по формуле
где xi – мольная доля компонента i, Mi – молярная масса компонента i, ρ – плотность стекла.Молярный объем атомов кислорода VO (объем стекла, содержащий 1 моль атомов кислорода) был рассчитан по формуле
где xi – мольная доля компонента i, ni – число атомов кислорода в формульной единице компонента i.Плотность кислородной упаковки η рассчитана по формуле
Молярный объем стекла, молярный объем атомов кислорода и плотность кислородной упаковки приведены в табл. 1. При одинаковом отношении содержаний оксидов теллура и молибдена в стеклах повышение концентрации оксида празеодима увеличивает плотность и уменьшает молярный объем стекла. Плотность образцов варьируется в пределах от 4.56 до 5.47 г/см3, причем в рядах с равным отношением содержаний оксидов теллура и молибдена она возрастает с увеличением содержания оксида празеодима. Увеличение содержания триоксида молибдена в стекле приводит к снижению плотности стекла, и это согласуется с результатами измерений плотности двойных теллуритно-молибдатных стекол [7, 9–14]. Молярный объем принимает значения от 29.0 до 32.6 см3/моль, и его зависимость от состава образцов противоположна таковой для плотности стекол.
Таблица 1.
Физические параметры празеодимсодержащих теллуритно-молибдатных стекол
| Состав стекла, мол. % | ρ, г/см3 | Vm, см3/моль | VO, см3/моль | η, моль/дм3 | ||
|---|---|---|---|---|---|---|
| TeO2 | MoO3 | PrO1.5 | ||||
| TeO2 : MoO3 = 9 : 1 | ||||||
| 81 | 9 | 10 | 5.47 | 29.0 | 14.2 | 70.4 |
| TeO2 : MoO3 = 4 : 1 | ||||||
| 76 | 19 | 5 | 5.32 | 29.5 | 13.6 | 73.4 |
| 72 | 18 | 10 | 5.40 | 29.1 | 13.7 | 73.2 |
| 64 | 16 | 20 | 5.46 | 29.0 | 14.1 | 71.1 |
| TeO2 : MoO3 = 2 : 1 | ||||||
| 62 | 31 | 7 | 5.17 | 30.0 | 13.2 | 75.8 |
| 58 | 29 | 13 | 5.22 | 29.8 | 13.4 | 74.6 |
| 54 | 27 | 19 | 5.27 | 29.7 | 13.6 | 73.3 |
| 50 | 25 | 25 | 5.31 | 29.6 | 13.9 | 71.9 |
| TeO2 : MoO3 = 1 : 1 | ||||||
| 47 | 47 | 6 | 4.84 | 31.5 | 12.9 | 77.5 |
| 44 | 44 | 12 | 4.98 | 30.8 | 12.9 | 77.3 |
| 41 | 41 | 18 | 5.06 | 30.5 | 13.1 | 76.2 |
| 38 | 38 | 24 | 5.20 | 29.8 | 13.2 | 75.8 |
| TeO2 : MoO3 = 1 : 2 | ||||||
| 31 | 62 | 7 | 4.69 | 32.1 | 12.4 | 80.6 |
| 29 | 58 | 13 | 4.77 | 31.7 | 12.6 | 79.3 |
| 27 | 54 | 19 | 4.86 | 31.3 | 12.8 | 78.2 |
| 25 | 50 | 25 | 4.96 | 30.9 | 13.0 | 76.9 |
| TeO2 : MoO3 = 1 : 4 | ||||||
| 18 | 72 | 10 | 4.56 | 32.6 | 12.2 | 81.9 |
| 17 | 68 | 15 | 4.60 | 32.6 | 12.5 | 80.0 |
Молярный объем атомов кислорода в стекле находится в пределах от 12.2 до 14.2 см3/моль и увеличивается с ростом содержания оксида празеодима при равном молярном соотношении количеств оксидов теллура и молибдена. Увеличение содержания триоксида молибдена в стекле уменьшает молярный объем атомов кислорода. Плотность кислородной упаковки в стекле изменяется от 70.4 до 81.9 моль/дм3. Она уменьшается по мере увеличения содержания оксида празеодима в стекле при равном мольном соотношении количеств оксидов теллура и молибдена. Увеличение содержания триоксида молибдена в стекле увеличивает плотность кислородной упаковки.
Оптические свойства стекол. На рис. 2 представлен типичный спектр поглощения празеодимсодержащего теллуритно-молибдатного стекла. В этих спектрах наблюдаются характерные для празеодима полосы поглощения, вызванные электронными переходами с основного уровня 3H4 атома празеодима на уровни 1D2, 1G4, 3F4, 3F3, 3F2, 3H6. Соответствующие им полосы поглощения отмечены на рис. 2. Интенсивность полос поглощения увеличивается с ростом содержания оксида празеодима в образце.
Из спектров поглощения рассчитаны оптические характеристики изучаемых стекол, которые систематизированы в табл. 2.
Таблица 2.
Оптические характеристики празеодимсодержащих теллуритно-молибдатных стекол
| Состав стекла, мол. % | ΔE, эВ | Eg, эВ | Rm, см3/моль | ${{\alpha }_{{{{{\text{O}}}^{{2 - }}}}}}$, Å3 | Λ | M | ||
|---|---|---|---|---|---|---|---|---|
| TeO2 | MoO3 | PrO1.5 | ||||||
| TeO2 : MoO3 = 4 : 1 | ||||||||
| 76 | 19 | 5 | 0.121 | 2.39 | 19.3 | 2.94 | 1.10 | 0.346 |
| 72 | 18 | 10 | 0.098 | 2.38 | 19.1 | 2.94 | 1.10 | 0.345 |
| 68 | 17 | 15 | 0.078 | 2.41 | 19.3 | 3.03 | 1.12 | 0.347 |
| 64 | 16 | 20 | 0.051 | 2.45 | 18.8 | 3.00 | 1.11 | 0.350 |
| TeO2 : MoO3 = 2 : 1 | ||||||||
| 62 | 31 | 7 | 0.115 | 2.34 | 19.7 | 2.95 | 1.10 | 0.342 |
| 58 | 29 | 13 | 0.101 | 2.37 | 19.6 | 2.98 | 1.11 | 0.344 |
| 54 | 27 | 19 | 0.083 | 2.42 | 19.4 | 3.01 | 1.11 | 0.348 |
| 50 | 25 | 25 | 0.052 | 2.44 | 19.2 | 3.05 | 1.12 | 0.349 |
| TeO2 : MoO3 = 1 : 1 | ||||||||
| 44 | 44 | 12 | 0.099 | 2.19 | 20.6 | 3.04 | 1.12 | 0.331 |
| 41 | 41 | 18 | 0.094 | 2.36 | 20.0 | 3.01 | 1.12 | 0.344 |
| 38 | 38 | 24 | 0.061 | 2.42 | 19.4 | 2.98 | 1.11 | 0.348 |
| TeO2 : MoO3 = 1 : 2 | ||||||||
| 25 | 50 | 25 | 0.100 | 2.35 | 20.3 | 3.06 | 1.12 | 0.342 |
| 23 | 46 | 31 | 0.049 | 2.46 | 20.0 | 3.08 | 1.13 | 0.351 |
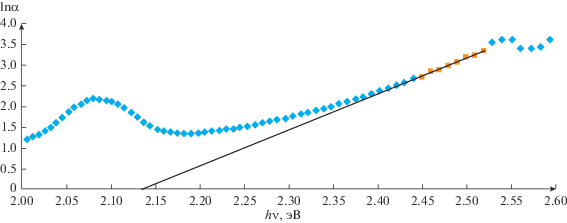
Край поглощения многих разупорядоченных материалов в области малого поглощения (коэффициент поглощения α(ν) < 104 см–1) описывается уравнением Урбаха [15]
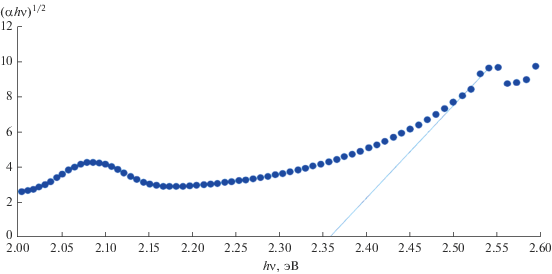
где hν – энергия фотона; ΔE – ширина хвостовой части полосы поглощения, связанная с отсутствием дальнего порядка в стекле; A – некоторая константа. Пример расчета энергии Урбаха ΔE приведен на рис. 3. Во всех рядах изученных стекол энергия Урбаха снижается по мере возрастания содержания оксида празеодима в стекле (табл. 2).Величиной, характеризующей электронные переходы в стеклах, является ширина запрещенной зоны Eg, которая рассчитывается из оптических спектров. Для аморфных веществ эта величина связана с энергией фотона hν уравнением [16, 17]
где B – некоторая константа. Эта математическая зависимость соответствует непрямому разрешенному переходу, имеющему место в стеклах. Расчет Eg выполняется из линейной зависимости величины (α(ν)hν)1/2 от энергии кванта света hν (рис. 4).Ширина запрещенной зоны используется для расчета молярной рефракции стекол Rm по эмпирической зависимости [18]
где Vm – молярный объем стекла. Найденные по этой формуле значения молярной рефракции приведены в табл. 2.Поляризуемость иона кислорода ${{\alpha }_{{{{{\text{O}}}^{{2 - }}}}}}$ в стекле рассчитывается из соображений аддитивности на основе той же эмпирической зависимости по формуле [18, 19]
Результаты расчета поляризуемости иона кислорода в празеодимсодержащих теллуритно-молибдатных стеклах представлены в табл. 2. Поляризуемость иона кислорода в исследованных стеклах находится на уровне 3 Å3 и превышает таковую для бинарных теллуритно-молибдатных стекол (около 2.3 Å3 [14]). Аналогичное явление имеет место и при введении в теллуритное стекло других редкоземельных элементов [21]. Примерное постоянство значений поляризуемости иона кислорода для празеодимсодержащих теллуритно-молибдатных стекол исследованных составов связано с тем, что во всех случаях имеет место пропорциональное замещение атомов теллура и молибдена на атомы празеодима, который характеризуется промежуточным значением поляризуемости.
Оптическая основность Λ (табл. 2) характеризует электронодонорные свойства атомов кислорода в стекле [22]. Ее расчет выполнен на основании корреляционной зависимости [18, 22]
В празеодимсодержащих стеклах оптическая основность находится на уровне 1.1, тогда как в бинарных теллуритно-молибдатных стеклах она принимает значения от 0.9 до 1.0 [14]. Это объясняется введением в стекло основного оксида и характерно для других теллуритных стекол, содержащих редкоземельные элементы [21].
Критерий металлизации M [14], рассчитываемый по формуле
указывает на неметаллическую природу (M > 0) празеодимсодержащих теллуритно-молибдатных стекол. Для бинарных теллуритно-молибдатных стекол он находится на уровне 0.45 [14] и снижается до значений порядка 0.35 в наших образцах в присутствии оксида редкоземельного элемента. Подобными значениями характеризуются и другие теллуритные стекла, содержащие оксиды редкоземельных элементов [21].
ЗАКЛЮЧЕНИЕ
Получены празеодимсодержащие теллуритно-молибдатные стекла из бинарных оксидов элементов, содержащие (мол. %) 25–90 TeO2, 10–75 MoO3, до 30 PrO1.5. Найдены границы области стеклообразования в системе TeO2–MoO3–Pr2O3.
Измерены плотности и рассчитаны молярные объемы празеодимсодержащих теллуритно-молибдатных стекол. При постоянном молярном отношении оксидов теллура и молибдена с ростом содержания оксида празеодима в стеклах их плотность увеличивается и молярный объем уменьшается.
Зарегистрированы спектры поглощения стекол системы TeO2–MoO3–Pr2O3. В спектрах представлены полосы поглощения атомов празеодима. Из оптических спектров рассчитаны характеристики празеодимсодержащих теллуритно-молибдатных стекол, которые аналогичны таковым для теллуритных стекол с другими редкоземельными элементами.
Список литературы
Borelli N.F. Faraday Rotation in Glasses // J. Chem. Phys. 1964. V. 41. № 11. P. 3289–3293.
Айхлер Ю., Айхлер Г.-И. Лазеры. Исполнение, управление, применение. М.: Техносфера, 2008. 440 с.
Аппен А.А. Химия стекла. Л.: Химия, 1974. 352 с.
Фельц А. Аморфные и стеклообразные неорганические твердые тела. М.: Мир, 1986. 558 с.
Pal M., Tsujigami Y., Yoshikado A., Sakata H. Electrical and Optical Properties of MoO3–TeO2 Amorphous Films Prepared by PVD Method // Phys. Status Solidi A. 2000. V. 182. P. 727–736.
Kozhukharov V., Marinov M., Grigorova G. Glass-Formation Range in Binary Tellurite Systems Containing Transition Metal Oxides // J. Non-Cryst. Solids. 1978. V. 28. P. 429–430.
Kozhukharov V., Marinov M., Nikolov S., Bliznakov G., Klissurski D. Investigation on the TeO2–MoO3–V2O5 System. II. Properties of the Obtained Glasses // Z. Anorg. Allg. Chem. 1981. V. 476. P. 179–187.
Kaur A., Khanna A., González F., Pesquera C., Chen B. Structural, Optical, Dielectric and Thermal Properties of Molybdenum Tellurite and Borotellurite Glasses // J. Non-Cryst. Solids. 2016. V. 444. P. 1–10.
Singh R., Chakravarthi J.S. DC Conductivity of Molybdenum Tellurite Glasses // Phys. Rev. B. 1995. V. 51. № 22. P. 16396–16399.
Sekiya T., Mochida N., Ogawa Sh. Structural Study of TeO2–MoO3 Glasses // J. Non-Cryst. Solids. 1995. V. 185. P. 135–144.
Neov S., Gerasimova I., Sidzhimov B., Kozhukharov V., Mikula P. Investigation of Short-Range Atomic Order in Glasses from the MoO3–TeO2 System // J. Mater. Sci. 1988. V. 23. P. 347–352.
El-Mallawany R., Sidkey M., Khafagy A., Afifi H. Elastic Constants of Semiconducting Tellurite Glasses // Mater. Chem. Phys. 1994. V. 37. P. 295–298.
Ghosh A. Electrical Transport Properties of Molybdenum Tellurite Glassy Semiconductors // Philos. Mag. B. 1990. V. 61. № 1. P. 87–96.
Dimitrov V., Komatsu T. Electronic Polarizability, Optical Basicity and Non-Linear Optical Properties of Oxide Glasses // J. Non-Cryst. Solids. 1999. V. 249. P. 160–179.
Urbach F. The Long-Wavelength Edge of Photographic Sensitivity and of the Electronic Absorption of Solids // Phys. Rev. 1953. V. 92. P. 1324.
Tauc J., Grigorovici R., Vancu A. Optical Properties and Electronic Structure of Amorphous Germanium // Phys. Status Solidi. 1966. V. 15. P. 627–637.
Davis E.A., Mott N.F. Conduction in Non-Crystalline Systems. V. Conductivity, Optical Absorption and Photoconductivity in Amorphous Semiconductors // Philos. Mag. 1970. V. 22. P. 903–922.
Dimitrov V., Sakka S. Electronic Oxide Polarizability and Optical Basicity of Simple Oxides // J. Appl. Phys. 1996. V. 79. P. 1736–1740.
Dimitrov V., Komatsu T. Classification of Oxide Glasses: A Polarizability Approach // J. Solid State Chem. 2005. V. 178. P. 831–846.
Бацанов С.С. Структурная рефрактометрия. М.: Высш. школа, 1976. 304 с.
Elkhoshkhany N., Marzouk S.Y., Moataz N., Kandil Sh.H. Structural and Optical Properties of TeO2–Li2O–ZnO–Nb2O5–Er2O3 Glass System // J. Non-Cryst. Solids. 2018. V. 500 P. 289–301.
Duffy J.A. Optical Basicity of Titanium(IV) Oxide and Zirconium(IV) Oxide // J. Am. Ceram. Soc. 1989. V. 72. № 10. P. 2012–2013.
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы