БИОФИЗИКА, 2021, том 66, № 4, с. 811-822
БИОФИЗИКА СЛОЖНЫХ СИСТЕМ
УДК 004.942
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ АРМИРУЮЩЕЙ
КОНСТРУКЦИИ ПРОТЕЗА КРОВЕНОСНОГО СОСУДА НА ОСНОВЕ
ВНУТРЕННЕЙ ГРУДНОЙ АРТЕРИИ КРУПНОГО РОГАТОГО СКОТА
© 2021 г. К.Ю. Клышников*, М.А. Резвова*, Е.А. Овчаренко*, Т.В. Глушкова*,
А.В. Батранин**, Д.В. Нуштаев***, Ю.Н. Захаров****, *****, В.Г. Борисов****,
Ю.А. Кудрявцева*, Л.С. Барбараш*
*Научно-исследовательский институт комплексных проблем сердечно-сосудистых заболеваний,
650002, Кемерово, Сосновый бульвар, 6
**Томский политехнический университет, 634050, Томск, просп. Ленина, 30
***3АО «Северсталь Менеджмент», 127299, Москва, ул. Клары Цеткин, 2
****Кемеровский государственный университет, 650000, Кемерово, ул. Красная, 6
*****Кемеровский филиал Института вычислительных технологий СО РАН,
650025, Кемерово, ул. Рукавишникова, 21
E-mail: KlyshnikovK@gmail.com
Поступила в редакцию 25.07.2019 г.
После доработки 14.07.2020 г.
Принята к публикации 02.06.2021 г.
Исследование посвящено оценке сохранения остаточного просвета армированного биопротеза со-
судистого русла ксеногенного происхождения «КемАнгиоПротез» (ЗАО «НеоКор», Кемерово) при
перегибе. Использованный в работе комплекс натурных и численных методов позволил определить
механические свойства исследуемых объектов. В работе были использованы параметры шага спи-
рали - 4 мм и толщины нити - 0.3-0.5 мм. Показано, что свойства материала сосудистой стенки
анизотропны при сравнении продольного и поперечного направлений приложения нагрузки. Так,
модули упругости составили 1.37 (0.90, 1.12, 1.44, 1.72) МПа против 0.80 (0.97, 1.23, 1.61, 2.15) МПа,
соответственно, статистически значимо различаясь (p < 0.05). С помощью метода конечных элемен-
тов, использованного в работе на этапе подбора параметров армирующего слоя, показано, что оста-
точный просвет сосудистого протеза нелинейно зависит от особенностей армирования - количе-
ства нанесенных спиралей. Показано, что использование внешнего полимерного армирующего
слоя позволяет снизить эффект перекрытия сосудистого протеза в случаях его изгиба, что характер-
но для инфраингвинальных реконструкций, в особенности при сравнении с исходным неармиро-
ванным изделием. Дополнительно, введение усиления повышает радиальную жесткость протеза,
что, потенциально, способно привести к снижению риска образования аневризм сосудистой стен-
ки в отдаленном периоде.
Ключевые слова: численное моделирование, протез сосудистого русла, армирование, остаточный
просвет сосуда.
DOI: 10.31857/S0006302921040219
Проведение операций реваскуляризации в на-
Преимущества биопротезов перед синтетиче-
стоящее время является актуальным направлени-
скими заключаются в изначальной схожести их
ем решения проблемы атеросклероза артерий
механических и функциональных характеристик
нижних конечностей при критических ишемиях
с тканями пациента: эластичности, податливости
[1]. «Золотым стандартом» таких операций явля-
(комплаентности), прочности, биомеханики и
ется использование аутологичного нативного
высокой биосовместимости [3, 4]. Тем не менее
сосуда, однако вследствие ограниченности соб-
имеющийся опыт показывает, что в 10% случаев
ственного материала ввиду патологических из-
клинического использования биологических со-
менений широкое распространение в хирургиче-
судов возникает патологическое растяжение со-
ской практике получили синтетические протезы
судистой стенки - образование аневризм, что в
и протезы биологического происхождения (из со-
результате приводит к необходимости повторной
судов крупного рогатого скота) [2, 3].
операции [5].
811
812
КЛЫШНИКОВ и др.
Описанную проблему способны решить вари-
ставляет собой платформу, обеспечивающую вза-
анты армирования - упрочнения сосудистой
имосвязанное перемещение экструдирующего
стенки каркасом биоинертных материалов (поли-
блока относительно вращающегося вала, на кото-
мерами, металлическими сетками) [6, 7]. Для ре-
рый монтирован участок протеза для армирова-
ализации заявленной идеи был выбран способ,
ния (рис.
1а-в). Таким образом последова-
основанный на принципах метода послойного
тельное скоординированное движение двух эле-
плавления (FDM - Fused Deposition Modeling)
ментов позволяет наносить полимерный
[8]. FDM-технология предполагает изготовление
армирующий материал в виде спиралей на по-
моделей путем продавливания расплава материа-
верхность сосуда (рис. 1в,г).
ла через формующее отверстие в экструдере, рас-
Дизайн исследования. Исследование остаточ-
положенном над коллектором заданной формы,
ного просвета при перегибе сосудистого биологи-
при этом скорость подачи расплава (экструзии) и
ческого протеза осуществляли в три этапа:
перемещение головки экструдера контролирует-
ся числовым программным управлением [9]. Ис-
1. Определение физико-механических свойств.
пользуя данную технологию, возможно получать
Этап предполагал исследование эксперименталь-
усиливающие конструкции различной формы
ных и контрольных образцов в условиях одноосно-
для коррекции комплаентности, жесткости и дав-
го продольного и радиального нагружения
ления разрыва сосудистых протезов. При проек-
(рис. 2а,б) с определением основных упруго-де-
тировании армирующего слоя важно провести
формативных показателей биологического и поли-
обоснованный выбор ключевых параметров: ша-
мерного материалов.
га спирали и ее диаметра в сечении. Метод ком-
2. Калибровка численных методов. Для обес-
пьютерного моделирования сегодня является
печения соответствия между результатами чис-
наиболее предпочтительным среди прочих до-
ленного моделирования и натурным эксперимен-
ступных ввиду возможности проведения итера-
том проводили предварительную настройку пара-
тивного анализа конструкционных свойств в за-
метров моделирования в четырех тестах.
висимости от заданных параметров [10]. Постро-
3. Итеративный подбор параметров армирую-
ение модели сосудистого протеза с заданными,
щего слоя. Этап был реализован в виде серии чис-
определяющими свойства параметрами, и после-
ленных экспериментов, оценивающих изгибную
дующий инженерный анализ напряженно-де-
жесткость в зависимости от варьирования пара-
формированного состояния конструкции в усло-
метров спиралей для армирования - количества,
виях физиологических нагрузок, выполненный
толщины нити, шага.
на основе метода конечных элементов, позволяет
провести итеративную оптимизацию структуры
Определение физико-механических свойств.
конструкции и определить ее наиболее эффек-
Физико-механическим испытаниям подвергали
тивные параметры.
серию из пяти армированных сосудистых проте-
зов и пяти контрольных образцов без упрочне-
Настоящая работа посвящена анализу воз-
можности создания армирующего каркаса сосу-
ния. Армирование заключалось в нанесении
дистого протеза методом послойного плавления с
двойной полимерной спирали толщиной 0.5 мм с
учетом результатов компьютерного моделирова-
шагом спирали 2 мм. Определение свойств образ-
цов осуществляли на универсальной испытатель-
ния.
ной машине Z50 (Zwick/Roell, Германия) в усло-
виях одноосного растяжения в продольном и по-
МАТЕРИАЛЫ И МЕТОДЫ
перечном направлениях (рис.
2). Характер
распределения в выборках оценивали при помо-
Объект исследования. В работе исследовали
щи критерия Шапиро-Уилка. Показано, что для
протезы сосудистого русла человека, выполнен-
большинства показателей распределение отлич-
ные из биологического ксеногенного материала
но от нормального (р < 0.01), в связи с чем вся
- внутренней грудной артерии крупного рогатого
описательная статистика результатов исследова-
скота, коммерческие образцы (N = 5) которых
ния физико-механических свойств представлена
были предоставлены компанией ЗАО «НеоКор».
как медианная величина, 25-я и 75-я процентили,
Каждый сосудистый протез разделяли на два
максимум и минимум. Для попарного сравнения
участка равной длины по 60 мм, один из которых
количественных показателей физико-механиче-
выступал в качестве контрольного, а другой был
ских испытаний, с учетом того, что выборки яв-
модифицирован дополнительным армирующим
ляются независимыми, использовали U-крите-
слоем. Создание армирующего слоя, представля-
рий Манна-Уитни, при этом достоверными счи-
ющего собой полимерную спираль из биоинерт-
тали различия при уровне значимости р < 0.05.
ного поливинилиденфторида, осуществляли на
опытной установке, реализующей принцип кон-
Полученные результаты в виде зависимостей
тролируемой экструзии термопластичного мате-
«сила-перемещение» использовали на этапе ка-
риала на поверхность сосуда. Оборудование пред-
либровки в качестве референсных для подбора
БИОФИЗИКА том 66
№ 4
2021
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ АРМИРУЮЩЕЙ КОНСТРУКЦИИ
813
Рис. 1. Опытный образец изготовления спирали на прототипе установки: (а) - вид установки в сборе, (б) - первый
этап нанесения упрочняющей спирали в один слой в одном направлении, (в) - наложение повторного слоя в
противоположном направлении для повышения армирующих свойств, (г) - габаритный вид полученного образца с
армированием.
параметров линейной модели материала числен-
а) окружное растяжение участка протеза без
ного моделирования
армирования - выбор модели материала для био-
логической компоненты;
Калибровка численных методов. В рамках чис-
ленной калибровки полностью воспроизводили
б) продольное одноосное растяжение сосуди-
стого протеза без армирования - выбор модели
параметры физико-механического натурного ис-
пытания и граничные условия, т.е. зажимы уни-
материала для биологической компоненты;
версальной испытательной машины (рис.
2).
в) окружное растяжение участка протеза с экс-
Трехмерными моделями для проведения данного
периментальным режимом армирования (толщи-
исследования выступили реконструкции, полу-
на спирали 0.5 мм, шаг спирали 2 мм) - выбор
ченные в результате компьютерного микротомо-
модели материала для полимерной компоненты;
графического сканирования [10] на установке с
г) продольное одноосное растяжение протеза с
субмиллиметровым разрешением Орел-МТ (НИ
аналогичным режимом армирования - выбор мо-
ТПУ, Россия). Реконструкцию моделей сосуди-
дели материала для полимерной компоненты.
стых протезов с армированием и без такового осу-
ществляли в среде MATLAB (MathWorks, США) с
При этом настройку материалов проводили
получением stl-файлов для дальнейшего экспорта
последовательно: изолированное сравнение и
в среду инженерного анализа Abaqus/CAE (Das-
выбор свойств биологической компоненты, а за-
sault Systemes, Франция). В ходе калибровки по-
тем - аналогичный подбор и выбор свойств про-
парно сравнивали результаты расчетов и экспе-
теза в сборе (совокупность сосуда и полимерного
риментальные данные в осях «сила-перемеще-
усиления). Тип аппроксимации модели материа-
ние», выбирая модели материалов для модели-
ла при расчете выбирали среди наиболее часто
рования, демонстрирующие наиболее близкие к
используемых вариантов, используемых в каче-
натурным значения в четырех случаях:
стве описания биологических сосудов [11]:
БИОФИЗИКА том 66
№ 4
2021
814
КЛЫШНИКОВ и др.
а) линейная модель, аппроксимируемая моду-
в) нелинейная модель Ogden:
лем упругости, согласно уравнению Гука;
б) нелинейная модель Neo Hooke:
2μ
α
α
α
W
=
λ
+
λ
+
λ
−
3
,
Ogden
2
(
1
2
2
)
WNH = C10 (I1 - 3),
α
где I1 - первый инвариант деформации, такой
где λ - отношения растяжения, α и μ - параметры
материала [11].
что I1 = tr(C), где C - тензор деформации Коши-
Грина, а C10 - механическая постоянная [12].
г) полиномиальная модель второго порядка:
2
3
W
poly
=C
10
(I
1
−3)
+C
01
(I
2
−3)
+C
20
(I
1
−3)
+C
11
(I
1
−3)(I
2
−3)
+C
30
(I
1
−3)
,
где I1, I2 и I3 - инварианты деформации, а C10,
а) размер сетки конечных элементов, выра-
C01, C20, C11, C30, - гиперэластичные константы
женный итоговым количеством элементов
860 тыс. - 9 тыс. элементов.
[12, 13].
б) тип конечного элемента, различающийся
Для полимерной компоненты выбирали ана-
точностью - трехмерные тетраэдры вида C3D4 и
логичные модели материала.
C3D4H с четырьмя точками интегрирования, а
также C3D10 и C3D10H с десятью точками инте-
Дополнительно для определения оптималь-
грирования.
ных размеров и типов сетки конечных элементов
при расчете проводили анализ чувствительности.
Критерием удовлетворительности настроек
сетки конечных элементов стало последователь-
Для этого формировали серию расчетов на одной
из моделей неармированного сосудистого проте-
ное сравнение результатов приложения к моде-
за, при которых варьировали:
лям внутреннего давления 120 мм рт. ст. с по-
следующим анализом различий максимального
напряжения; максимальной деформации; ради-
ального перемещения. В качестве референсных
значений выбирали результаты расчетов с наибо-
лее мелкой сеткой (860 тыс. элементов) и наибо-
лее точным типом конечных элементов
(C3D10H). После этого упрощали сетку и сни-
жали точность элементов до тех пор, пока откло-
нение количественных результатов от референс-
ных - не превышали 5%. Данный анализ призван
снизить время расчета с приемлемым сохранени-
ем количественных результатов, поэтому крите-
рием выбора настроек сетки конечных элементов
стало время расчета, в зависимости от применен-
ных настроек.
Верификация численных методов. Выбранные в
результате калибровки численных методов и оп-
тимальные настройки моделирования применя-
ли для отдельного расчета на примере образца со-
суда, армированного одинарной спиралью с ша-
гом 2 мм, отличного от использованного при
калибровке. Верификацию моделирования про-
водили путем сравнения расчетных результатов и
результатов натурного одноосного теста в кривых
«сила-перемещение».
Подбор параметров армирующего слоя. Одной
из функциональных характеристик, на повыше-
ние которой рассчитано введение армирующей
оболочки исследуемого сосудистого протеза, яв-
Рис. 2. Этапы исследования сосудистых протезов:
ляется поддержание просвета сосуда в случае пе-
(а) - физико-механическое одноосное исследование
региба на критические углы. Для подбора свойств
экспериментальных сосудов в продольном направле-
упрочняющего слоя был выбран тест на изгиб до
нии; (б) - то же в радиальном направлении; (в) - чис-
ленная версия исследования в продольном направле-
90° с оценкой диаметра остаточного просвета в
нии; (г) - то же в радиальном направлении.
зависимости от характеристик армирования -
БИОФИЗИКА том 66
№ 4
2021
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ АРМИРУЮЩЕЙ КОНСТРУКЦИИ
815
Рис. 3. Этапы подбора параметров армирующего слоя: (а) - трехмерная модель одного из вариантов (толщина 0.5 мм,
шаг спирали 2 мм); (б) - сетка конечных элементов, построенная на основе трехмерной модели; (в) - финальное
состояние модели сосудистого протеза после нагружения (изгиба до 90°); (г) - принцип определения диаметра
остаточного просвета экспериментального сосуда после изгиба до 90° (продольный срез).
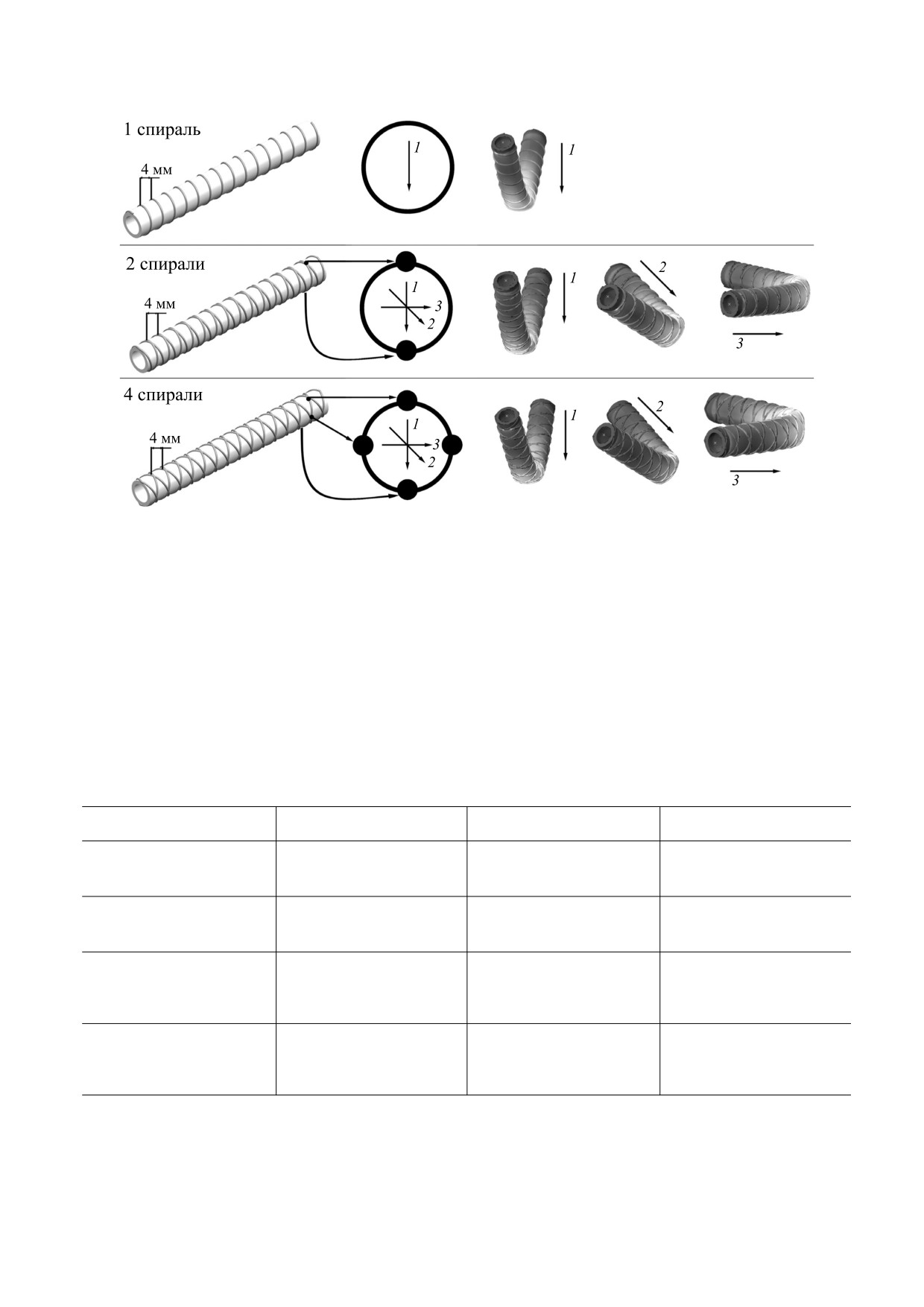
количества спиралей, толщины нити, шага спи-
визуализации областей высоких значений данных
рали [14]. Для этого в системе NX 9.0 (Siemens,
показателей с позиции оценки риска разрушения
Германия) проектировали соответствующие
участков сосудистого протеза.
трехмерные модели таким образом, чтобы полу-
Учитывая радиальную асимметрию наложе-
чить комбинацию вариантов, включающую:
ния армирующего слоя - прежде всего, образова-
1) одну, две или четыре спирали;
ния сплавлений спиралей для вариантов двух и
четырех спиралей, - предполагается, что при из-
2) толщину нити 0.1-0.3-0.5 мм;
гибе по разным осям (оси 1, 2 или 3 на рис. 4)
3) шаг спирали 4-5-6 мм.
свойства армирования будут различаться. В связи
Полученные таким образом модели импорти-
с чем, каждую модель сосудистого протеза с
ровали в ПО Abaqus/CAE, где на основе твердо-
армированием тестировали для нескольких на-
тельных объектов получали трехмерную сетку ко-
правлений, для учета такой геометрической ани-
нечных элементов, состоящую из 316000-427000
зотропии.
тетраэдров второго порядка с 10 точками инте-
грирования (тип C3D10). Приложение изгибаю-
щей нагрузки осуществляли с использованием
РЕЗУЛЬТАТЫ
референсных точек, управляющих концевыми
Определение физико-механических свойств. Ре-
участками модели протеза.
зультаты одноосного тестирования при попарном
К каждой такой точке прикладывали граничное
сравнении экспериментальных образцов с арми-
условие на перемещение (26.5 мм) и на вращение
рованием и без такового продемонстрировали
(1.57 радиана) таким образом, чтобы осуществить
значительное изменение механических свойств
одновременно сближение и изгиб проксимального
для случая поперечного и радиального растяже-
и дистального участков на необходимый угол - 90°
ний. Важно отметить, что при сравнении двух ва-
(рис. 3в). При этом для наиболее физиологическо-
риантов нагружения исходного (без усиления)
го воспроизведения условий функционирования
протеза модули упругости были различны для
сосуда на всем протяжении исследования на его
обоих вариантов нагрузок: 1.67 для продольного
внутреннюю поверхность оказывало влияние дав-
направления против 0.80 МПа для радиального
ление в 120 мм рт. ст. В работе оценивали в каче-
направления. Это обусловлено анизотропией ма-
стве основного параметра минимальный остаточ-
териала за счет слоистой структуры сосудистой
ный просвет армированного сосудистого протеза
стенки. Введение в состав конструкции спирале-
при изгибе на референсный угол 90°. Дополни-
видных элементов несколько нивелирует анизо-
тельно оценивали напряженно-деформированное
тропию изделия в целом: сосудистый протез с
состояние: количественные значения напряжения
упрочнением повысил свою жесткость в 1.44 раза
по Мизесу и логарифмической деформации, а так-
при продольной нагрузке и в 2.9 раза при попе-
же качественное их распределение на эпюрах для
речной (табл. 1).
БИОФИЗИКА том 66
№ 4
2021
816
КЛЫШНИКОВ и др.
Рис. 4. Особенности тестирования сосудистых протезов с учетом геометрической анизотропии нанесения армирую-
щих спиралей, слева-направо: исходная трехмерная модель, визуализирующая сохранение шага (на примере 4 мм);
схематичная визуализация образования точек сплавления для случаев одной, двух и четырех спиралей армирования с
пояснением направления нагрузки изгиба; пример нагруженных состояний в зависимости от направления изгиба.
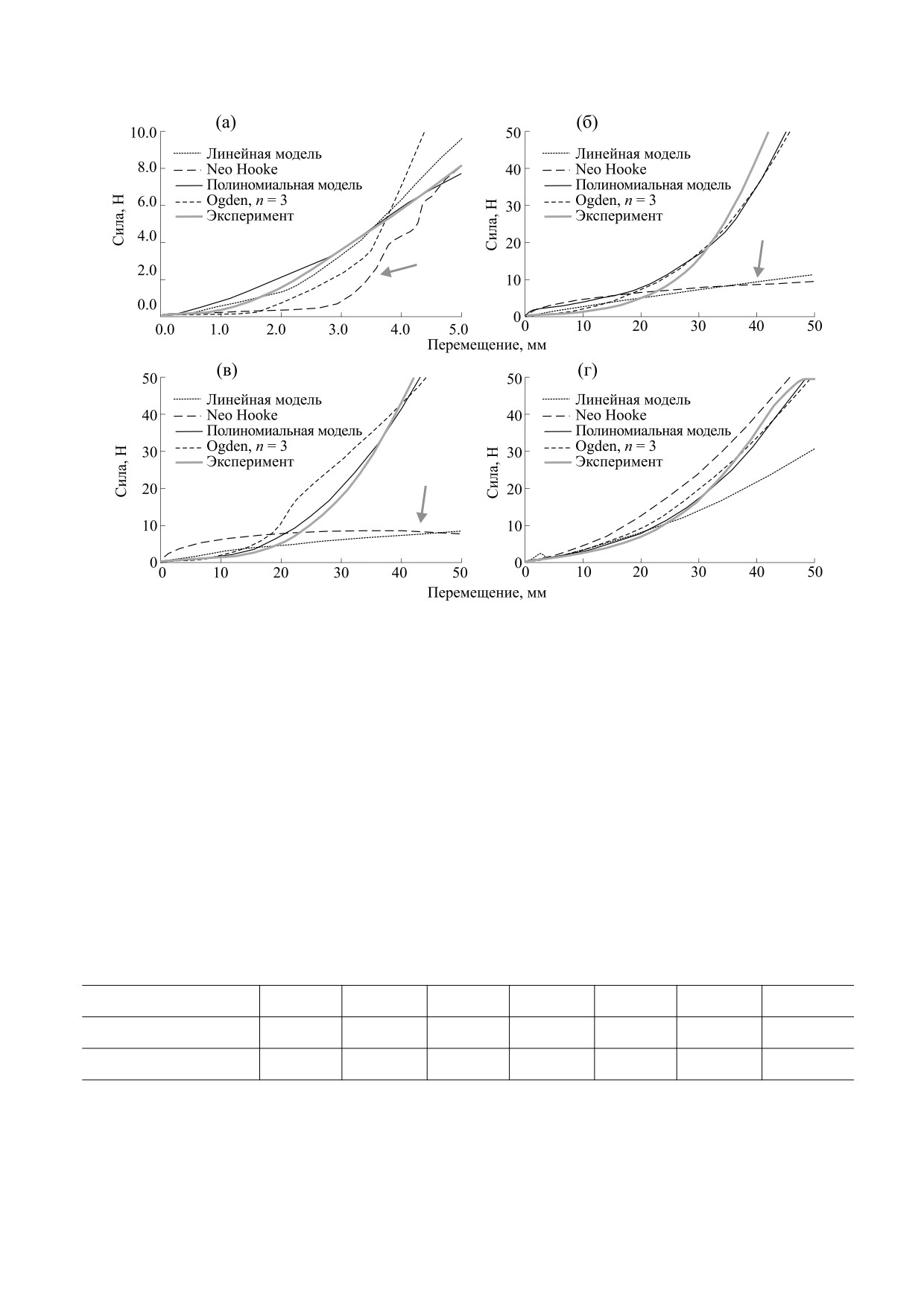
При этом статистический анализ показал до-
лов для описания биологической компоненты не
стоверное (p < 0.05) различие свойств только для
позволяет воспроизвести экспериментальные
неармированного варианта сосудистых протезов.
данные - это линейная модель, модели Neo
Hooke и Ogden (рис. 5а,б). При этом отмечено
Калибровка численных методов. В ходе этапа
калибровки при сравнении результатов натурных
значительное несоответствие результатов для
физико-механических испытаний и расчетных
двух моделей - линейной и Neo Hooke, принци-
данных было показано, что ряд моделей материа-
пиально не воспроизводящих характер кривой
Таблица 1. Упруго-деформативные характеристики исследуемых образцов
Объект
Модуль упругости, МПа
Предел прочности, МПа
Предел прочности, %
Без армирования
1.37*,†
1.61†
87†
(продольная нагрузка)
(0.90, 1.12, 1.44, 1.72)
(1.35, 1.56, 1.85, 2.05)
(65, 77, 91, 101)
Без армирования
0.80*,‡
1.5‡
85†
(поперечная нагрузка)
(0.57, 0.75, 0.96, 1.44)
(1.3, 1.4, 1.7, 2.1)
(72, 80, 99, 120)
Армирование
1.92†
4.36†
97‡
поливинилиденфторидом
(1.15, 1.24, 2.14, 2.60)
(3.44, 4.12, 4.53, 5.73)
(84, 91, 103, 115)
(продольная нагрузка)
Армирование
1.45‡
2.46‡
141‡
поливинилиденфторидом
(1.23, 1.34, 1.76, 2.60)
(1.78, 2.24, 2.79, 3.41)
(97, 121, 159, 164)
(поперечная нагрузка)
Примечание. Данные представлены в виде медианы (минимум, 25-я процентиль, 75-я процентиль, максимум); *, †, ‡ -
достоверно значимые различия с уровнем значимости p < 0.05.
БИОФИЗИКА том 66
№ 4
2021
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ АРМИРУЮЩЕЙ КОНСТРУКЦИИ
817
Рис. 5. Калибровка модели материала, используемой для расчета на основе экспериментальных данных: (а) - выбор
модели материала для биологической компоненты в случае растяжения в радиальном направлении; (б) - то же, при
продольном растяжении; (в) - определение модели материала всего протеза в сборе, с учетом полимерной
компоненты; (г) - то же, в продольном направлении.
для продольного растяжения (рис. 5б). Таким об-
риментом также для модели полиномиальной мо-
разом, на первом этапе - подборе свойств биоло-
дели (табл. 2).
гической компоненты - наилучшие показатели
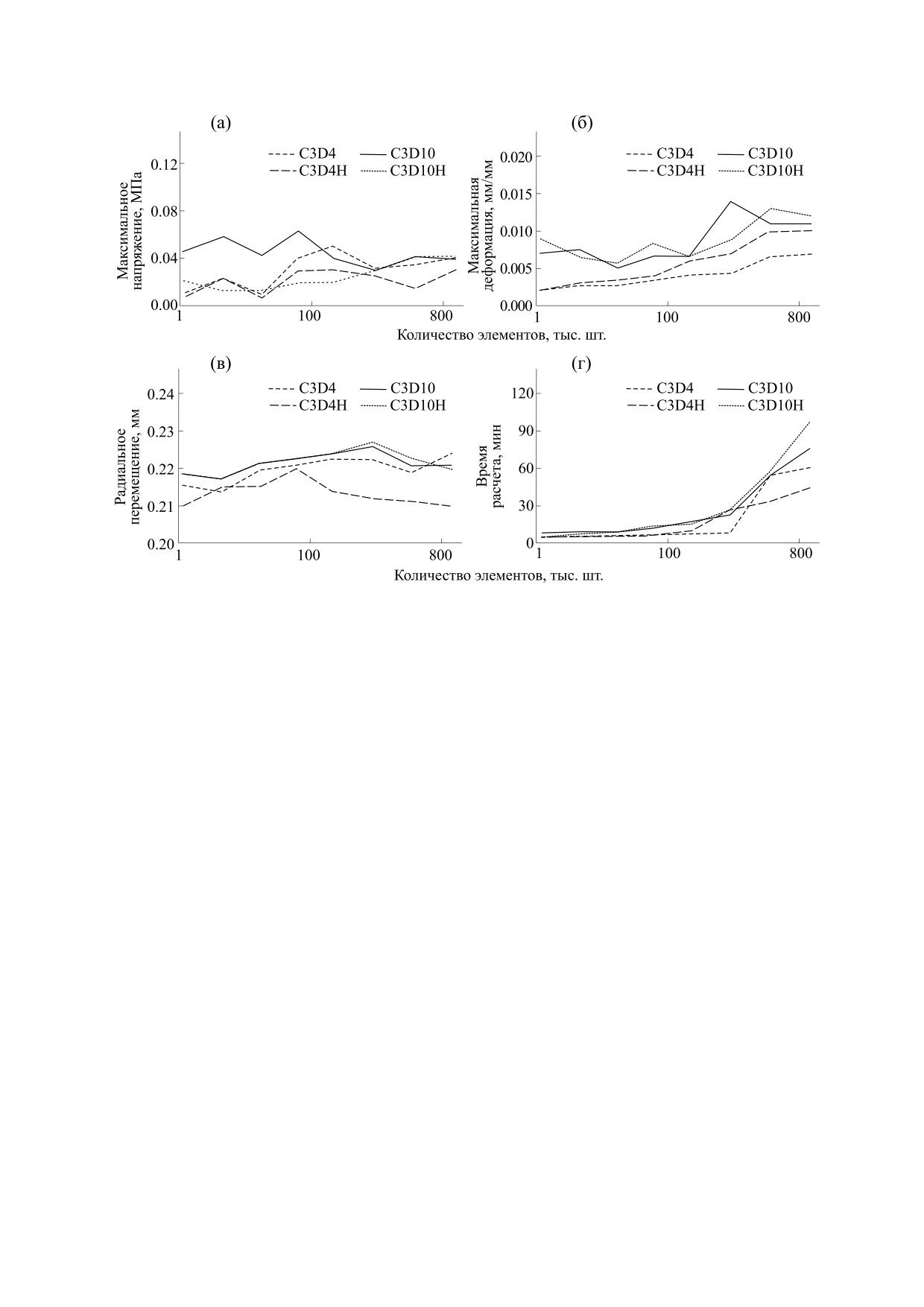
Анализ чувствительности (рис. 6) продемон-
сходимости продемонстрировала полиномиаль-
стрировал, что упрощение расчетной модели не-
ная модель. Последующее включение в расчет-
гативно сказывается на точности результатов.
ную модель полимерного армирующего элемента
Сравнение с референсной - самой плотной сет-
также продемонстрировало неприемлемость двух
кой конечных элементов (860 тыс. элементов) -
вариантов - линейной модели и Neo Hooke, в
показало, что возможно снижение размерности
особенности при численном расчете деформации
не более чем в два раза (до 430 тыс. элементов), не
в окружном направлении (рис. 5в). Моделирова-
вызывая значимых отклонений количественных
ние продольного растяжения протеза в сборе в
результатов. Дальнейшее упрощение существен-
значительной мере совпадало с натурным экспе- но искажает результат моделирования. Аналогич-
Таблица 2. Характеристики исследуемых при численном моделировании материалов
Объект
C10, МПа
C01, МПа
C20, МПа
C11, МПа
C02, МПа
D1, мм/мм
D2, мм/мм
Сосудистый протез
-0.015
0.015
7.1
-10.11
4.4
0.01
0.01
Полимерная спираль
-0.035
0.035
13.2
-19.61
7.8
0.01
0.01
Примечание. Представлены феноменологические коэффициенты моделей материала, применимые в
Abaqus/CAE - изотропной полиномиальной модели второго порядка, согласно представлению в разделе
«Материалы и методы» [12, 13].
БИОФИЗИКА том 66
№ 4
2021
818
КЛЫШНИКОВ и др.
Рис. 6. Результаты анализа чувствительности моделирования в зависимости от настроек: (а) - зависимость
максимального напряжения от количества и типа конечных элементов при расчете; (б) - зависимость максимального
значения деформации от количества и типа конечных элементов при расчете; (в) - зависимость радиального
перемещения от количества и типа конечных элементов; (г) - время расчета моделирования в зависимости от
количества и типа конечных элементов.
ные результаты были получены при варьирова-
однако его характер не линеен: показано, что
нии типа конечных элементов: только тип
наибольший скачок показателя происходит при
C3D10 - трехмерные тетраэдры с 10 точками ин-
переходе от одной к двум спиралям, при добавле-
тегрирования - позволил обеспечить приемле-
нии еще пары спиралей остаточный просвет уве-
мый уровень точности по сравнению с референ-
личивается, но не столь значительно. Так, диа-
сом (гибридными элементами C3D10H). Сово-
метр просвета вырос на 11-32% для перехода «1-2»
купность внесенных изменений настроек
спирали в исследуемых моделях. В случаях пере-
моделирования позволила снизить расчетное
хода «2-4» спирали рост диаметра остаточного
время с 96 до 53 мин для данной упрощенной по-
просвета составил 21.5-44.3%.
становки - приложения внутреннего давления,
Шаг спирали. Была получена линейная обратно
однако с сохранением точности.
пропорциональная зависимость остаточного
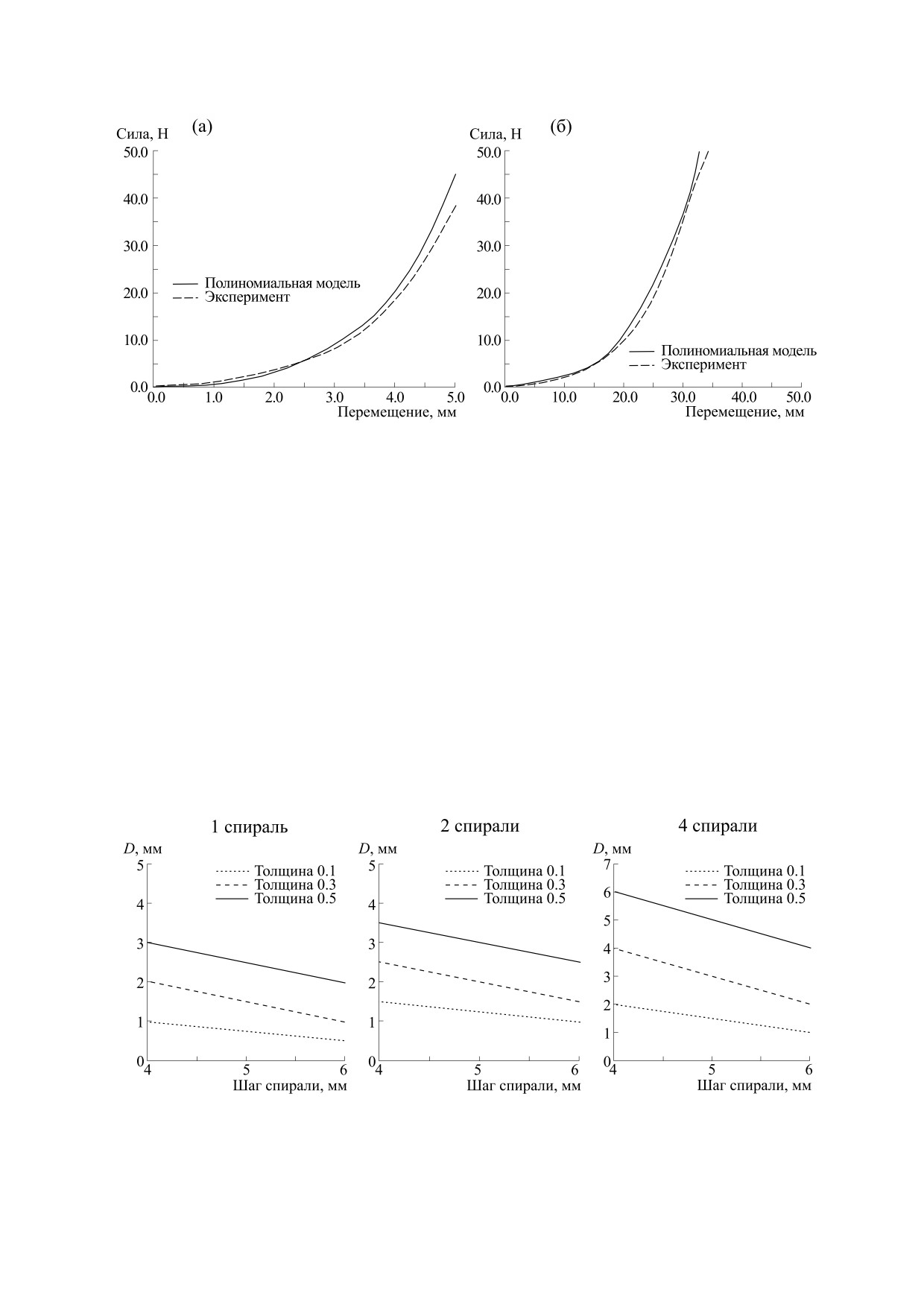
Верификация численных методов. В целом ре-
просвета от шага спирали, сохраняющаяся для
зультаты численного верификационного расчета
всех вариантов армирования - рост шага спирали
сходятся с экспериментальными данными, одна-
приводил к падению диаметра просвета (рис. 8).
ко в зоне больших деформаций - в правой части
Толщина нити. Влияние толщины нити арми-
кривой «сила-перемещение» - наступает рас-
рующего слоя спирали на диаметр остаточного
хождение показателей (рис. 7). Расчетная модель
просвета также было в достаточной мере прогно-
в случае окружного и продольного перемещений
зируемо - наблюдали прямо пропорциональную
завышает значение силы на 26 и 2.6% соответ-
зависимость силы сжатия (рис. 8).
ственно.
Направление изгиба. Исследования силы сжатия
Подбор параметров армирующего слоя. Количе-
для различных направлений (1, 2, 3) подтвердило
ство спиралей. Ожидаемо при численном анализе
предположение об анизотропии свойств армирую-
с ростом количества спиралей до четырех проис-
щей спирали. При этом наибольшую разницу меж-
ходит рост диаметра остаточного просвета сосуда,
ду всеми тремя направлениями изгиба продемон-
БИОФИЗИКА том 66
№ 4
2021
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ АРМИРУЮЩЕЙ КОНСТРУКЦИИ
819
Рис. 7. Результаты верификации подобранной модели материала и настроек расчета в сравнении с эксперименталь-
ными данными для двух случаев нагрузки: (а) - в радиальном и (б) - в продольном направлениях.
стрировали варианты армирования с двумя спира-
ев с одной спиралью, при которых образовывался
лями: вариативность показателя силы составила до
«излом» центральной части протеза, в особенно-
68% (между направлением 1 и 3). Для варианта с
сти при большом шаге спирали. Так, для случая
четырьмя спиралями направления 1 и 3 значимо не
одной спирали с толщиной нити 0.5 мм и шагом
различались (до 11%), а направление 2, напротив,
спирали 6 мм значение напряжения биоматериа-
продемонстрировало снижение силы относитель-
ла составило 0.96 МПа, деформации - 0.66.
но направления 1 на 16%.
Для аналогичного случая, но с использованием
четырех спиралей, в биоматериале наблюдали
Напряженно-деформированное состояние. Ана-
максимальные значения 0.575 МПа и 0.24 соот-
лиз количественных показателей напряженно-
ветственно.
деформированного состояния - напряжения по
Мизесу и логарифмической деформации - не вы-
Контроль. Анализ результатов расчета остаточ-
явил наличия в моделях областей, для которых
ного просвета неармированной модели сосуди-
были превышены значения предела прочности
стого протеза продемонстрировал наименьшее
как по напряжению, так и по деформации. Мак-
среди всех вариантов значение диаметра остаточ-
симум данных показателей наблюдали для случа-
ного просвета - 0.46 мм.
Рис. 8. Зависимости диаметра остаточного просвета (D, мм) от основных параметров армирующей спирали,
сгруппированные по количеству нитей - от одной до четырех, при сравнении изгиба по направлению 1.
БИОФИЗИКА том 66
№ 4
2021
820
КЛЫШНИКОВ и др.
Рис. 9. Эпюры напряжения в исследуемых образцах и визуализация остаточного просвета сосудистого протеза на
примере нити 0,5 мм: (а), (г), (ж) - односпиральное армирование с шагом 4, 5 и 6 мм соответственно; (б), (д), (з) - то
же, с двумя спиралями армирования; (в), (е), (и) - то же, с четырьмя спиралями.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
выбуханию сосудистой стенки и образованию
аневризм за счет структурной дегенерации [16,
Определение физико-механических свойств.
17]. Введение армирующего слоя позволяет повы-
Исследование биологических протезов подтвер-
сить радиальную жесткость, при этом геометрия
дило анизотропию материала изделия для на-
армирования в виде спирали(ей) позволяет кон-
чального состояния без усиления. Исходная
тролируемо влиять раздельно на радиальную со-
жесткость «живой» сосудистой стенки артерий в
ставляющую и продольную за счет плотности на-
значительной мере обусловлена свойствами ме-
мотки, толщины нитей и количества спиралей.
дии и адвентиции - мышечный слой, располо-
Калибровка и верификация численных методов.
женный циркулярно, обеспечивает ограничение
В целом показано, что калибровка и подбор моде-
подвижности (т.е. ограничение диаметра) в ради-
ли материала могут быть достаточно эффективны
альном направлении; соединительно-тканный
даже для сложных конструкций, содержащих раз-
слой - в продольном [15]. При консервации био-
нородные объекты - биологического и синтети-
логического сосудистого протеза диглицидило-
ческого происхождения. Полученные в данной
вым эфиром этилен гликоля или глутаровым аль-
работе модели могут быть использованы для про-
дегидом, мышечные клетки медии погибают и не
ведения дальнейших тестов и численных расче-
могут поддерживать достаточную радиальную
тов. Описанные в литературе аналогичные иссле-
жесткость, так как этот процесс является актив-
дования изгиба стент-графтов дополнительно
ным и требует поддержания тонуса гладкой му-
подтверждают состоятельность метода [18, 19].
скулатуры. При этом коллагеновые и эластино-
Однако биологическая компонента конструкции
вые волокна адвентиции являются пассивными
сосудистого протеза в значительной мере услож-
структурами и после консервации в значительной
няет численный анализ за счет нелинейности
мере сохраняют свои упруго-эластические свой-
своей физико-механической характеристики,
ства. Таким образом, происходит значимое сни-
выраженной необходимостью использовать по-
жение жесткости радиального направления и со-
линомиальные модели материала (табл. 2). Тем не
хранение жесткости продольного (модуль упруго-
менее в работе показано, что при использовании
сти 0.8 МПа против 1.37 МПа соответственно).
корректных моделей материала и высокодетали-
Предположительно, данный механизм и приво-
зированных реконструкций протеза на основе
дит к наблюдаемым в клинике осложнениям -
микротомографических методов исследования
БИОФИЗИКА том 66
№ 4
2021
ЭКСПЕРИМЕНТАЛЬНОЕ ИССЛЕДОВАНИЕ АРМИРУЮЩЕЙ КОНСТРУКЦИИ
821
возможно добиться высокой сходимости натур-
характерно минимальное сохранение остаточно-
ных и компьютерных экспериментов.
го диаметра. Кроме того, изменение радиальной
жесткости сосудистого протеза за счет нанесения
Подбор параметров армирующего слоя. Иссле-
армирующего слоя способно привести к профи-
дования параметров армирования сосудистого
лактированию аневризм сосудистой стенки в от-
протеза позволили выявить основные закономер-
даленном периоде.
ности для выбора свойств упрочняющего слоя -
зависимости от толщины нити, шага и общей его
плотности. Немаловажным оказалось раскрытие
ФИНАНСИРОВАНИЕ РАБОТЫ
нелинейности при наборе количества спиралей -
Работа выполнена в рамках фундаментальной
прирост диаметра остаточного просвета для пере-
темы НИИ КПССЗ № 0546-2019-0002 «Патогене-
хода «1-2» спирали оказался ниже, чем для пере-
тическое обоснование разработки имплантатов
хода «2-4» спирали (рис. 9в,е,и). Предположи-
для сердечно-сосудистой хирургии на основе
тельно, данный эффект обусловлен созданием
биосовместимых материалов, с реализацией па-
устойчивой геометрии армирующего слоя за счет
циент-ориентированного подхода с использова-
сплавлений, которые ограничивают движения
нием математического моделирования, тканевой
спиралей как относительно друг друга, так и для
инженерии и геномных предикторов».
биологической части сосуда в продольном на-
правлении, чего нельзя ожидать в случае одно-
спирального варианта. Введение в армирующий
КОНФЛИКТ ИНТЕРЕСОВ
слой дополнительных двух спиралей значимо не
Авторы заявляют об отсутствии конфликта
влияет на описанную подвижность, однако сни-
интересов.
жает влияние направления изгиба на диаметр
остаточного просвета, что, по-видимому, являет-
ся дополнительным преимуществом варианта из
СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ
четырех спиралей.
Настоящая работа не содержит описания ка-
Два других параметра - толщина спирали и ее
ких-либо исследований с использованием людей
шаг - оказали значимое влияние на итоговую
и животных в качестве объектов.
конфигурацию и механических отклик армиро-
ванного сосудистого протеза. В связи с этим об-
щая рекомендация для подбора параметров арми-
СПИСОК ЛИТЕРАТУРЫ
рования - значимые толщины (0.3-0.5 мм) и
1. L. Haghighat, S. E. Altin, R. R. Attaran, et al., J. Clin.
плотность (4 мм) намотки - способны поддержи-
Med. 7 (4), E82 (2018).
вать достаточный уровень проходного отверстия
2. A. Farber and R. T. Eberhardt, JAMA Surgery 151 (11),
даже при перегибе на критический угол.
1070 (2016).
Сравнение диаметра остаточного просвета при
3. Б. С. Суковатых, Л. Н. Беликов, О. А. Родионов и
перегибе с контролем, в качестве которого высту-
др., Вестн. Нац. медико-хирургич. Центра им.
пила модель сосуда без армирования, продемон-
Н.И. Пирогова 12 (1), 32 (2017).
стрировало преимущества нанесения полимера,
4. Б. С. Суковатых, Л. Н. Беликов, М. Б. Суковатых и
даже в случае односпирального варианта с мини-
Д. В. Сидоров, Анналы хирургии 21 (5), 312 (2016).
мальной плотностью. Так, остаточный просвет
для контроля составил 0.46 мм (7.6% от исходно-
5. Л. С. Барбараш, Н. Н. Бурков, Ю. А. Кудрявцева и
го), а для наихудшего случая армирования -
др., Ангиология и сосудистая хирургия 18 (2), 21
0.52 мм (8.7%); для наиболее плотного нанесения
(2012).
спиралей - 4 спирали с толщиной нити 0.5 мм и
6. C. Singh and X. Wang, J. Mech. Behav. Biomed. Mater.
шагом 4 мм - просвет составил 5.1 мм (85%). Та-
48, 125 (2015).
ким образом, возможно рекомендовать создание
7. M. S. El-Kurdi, Y. Hong, J. J. Stankus, et al., Biomate-
армирующего слоя, в том числе «минимальной»
rials 29 (22), 3213 (2008).
конфигурации, в задачах поддержания просвета
8. S. M. Giannitelli, D. Accoto, M. Trombetta, and
сосудистого протеза при перегибе.
A. Rainer, Acta Biomater. 10 (2), 580 (2014).
9. H. V. Raeisdasteh, S. Davaran, A. Ramazani, and
ЗАКЛЮЧЕНИЕ
R. Salehi, J. Biomater. Sci. Polym. Ed. 28 (16), 1797
(2017).
Использование армирующего слоя позволяет
снизить эффект перекрытия сосуда при критиче-
10. M. L. Neal and R. Kerckhoffs, Brief. Bioinformatics 11
ских перегибах, что важно для инфраингвиналь-
(1), 111 (2010).
ных реконструкций. Описанный эффект особен-
11. S. Misra, K. T. Ramesh, and A. M. Okamura, Comput.
но наглядно проявляется при сравнении с неар-
Methods Biomech. Biomed. Engin. 13 (6), 811 (2010).
мированным сосудистым протезом, для которого
DOI: 10.1080/10255840903505121
БИОФИЗИКА том 66
№ 4
2021
822
КЛЫШНИКОВ и др.
12. C. Noble, K. D. Carlson, E. Neumann, et al., J. Mech.
16. К. Жункейра и Ж. Л. Карнейро, Гистология: атлас:
Behav. Biomed. Mater. 101, 103453 (2020). DOI:
учебное пособие (ГЭОТАР-Медиа, М., 2009).
10.1016/j.jmbbm.2019.103453
17. Л. С. Барбараш, С. В. Иванов, И. Ю. Журавлева и др.,
13. C. Lally, F. Dolan, and P. J. Prendergast, J Biomech. 38
Ангиология и сосудистая хирургия 12 (3), 91 (2006).
(8), 1574 (2005). DOI: 10.1016/j.jbiomech.2004.07.022
14. С. Г. Стучебров, А. В. Батранин, И. А. Милойчико-
18. Н. Н. Бурков и И. Ю. Журавлева, Медицина и об-
ва и др., Вестн. Нац. исслед. ядерного университе-
разование в Сибири, № 4, 65 (2013).
та МИФИ 6 (1), 31 (2017).
15. N. Demanget, S. Avril, P. Badel, et al., J. Mech. Behav.
19. N. Demanget, P. Latil, L. Orgéas, et al., Ann. Biomed.
Biomed. Mater. 5 (1), 272 (2012).
Eng. 40 (12), 2674 (2012).
Experimental Study of the Reinforcing Element of a Vascular Prosthesis Fabricated
Using Internal Thoracic Artery of Big Cattle
K.U. Klyshnikov*, M.A. Rezvova*, E.A. Ovcharenko*, T.V. Glushkova*, A.V. Batranin**,
D.V. Nyshtaev***, Yu.N. Zakharov****, *****, V.G. Borisov****,
Yu.A. Kudryavtseva*, and L.S. Barbarash*
*Research Institute for Complex Issues of Cardiovascular Diseases, Sosnovy bulvar 6, Kemerovo, 650002 Russia
**Tomsk Polytechnic University, prosp. Lenina 30, Tomsk, 634050 Russia
***CJSC «Severstal Management», ul. Clary Zetkin 2, Moscow, 127299 Russia
****Kemerovo State University, ul. Krasnaya 6, Kemerovo, 650000 Russia
*****Kemerovo Branch of the Institute of Computational Technologies, Siberian Branch of the Russian Academy of Sciences,
ul. Rukavishnikova 21, Kemerovo, 650025 Russia
The goal of this study was to assess a patency rate for a reinforced vascular bioprosthesis with xenogenic cells
KemAngioProsthesis (JSC “NeoСor”, Kemerovo) in case of its mechanical deformation. The complex of
natural and numerical methods used in the work made it possible to determine the mechanical properties of
the objects under study. In the work, we used the parameters of the pitch of the helix, 4 mm, and the thickness
of the thread, 0.3-0.5 mm. It is shown that the material properties of the vascular wall are anisotropic as com-
pared to the longitudinal and transverse directions under loading. Thus, the elastic moduli were 1.37 (0.90,
1.12, 1.44, 1.72) MPa versus 0.80 (0.97, 1.23, 1.61, 2.15) MPa, respectively; and the statistical analysis showed
significant differences of these moduli among layers (p < 0.05). With the finite element method used to select
parameters for the reinforcing lining it was found that the patency rate for a vascular prosthesis depends non-
linearly on the number of spirals used. It is shown that the external polymeric reinforcing lining in case of its
mechanical deformation can offer satisfying patency rates and outcomes, what is typical of infra-inguinal re-
constructions, especially when compared to the original non-reinforced product. Additionally, the introduc-
tion of reinforcement increases the radial stiffness of the prosthesis, which, potentially, can lead to a decrease
in the risk of vascular wall aneurysms in the long term.
Keywords: numerical modeling, vascular bioprosthesis, reinforcing element, patency rate
БИОФИЗИКА том 66
№ 4
2021