БИОФИЗИКА, 2021, том 66, № 5, с. 865-870
МОЛЕКУЛЯРНАЯ БИОФИЗИКА
УДК 577.32+57.083.1
БИОЭЛЕКТРОХИМИЧЕСКОЕ МОДЕЛИРОВАНИЕ ДИФФУЗИИ
ТОЛУИДИНОВОГО СИНЕГО В ГИДРОГЕЛЕ В ПРИСУТСТВИИ
ПЕРОКСИДАЗЫ И ТРИПСИНА
© 2021 г. И.А. Черенков*, **, М.Д. Кривилев*, ***, М.М. Игнатьева*,
Е.В. Вахрушева*, **, В.Г. Сергеев*, **
*Удмуртский государственный университет, 426034, Ижевск, ул. Университетская, 1
**Ижевская государственная медицинская академия, 426034, Ижевск, ул. Коммунаров, 281
***Удмуртский федеральный исследовательский центр УрО РАН, 426067, Ижевск, ул. Татьяны Барамзиной, 34
E-mail: ivch75@yandex.ru
Поступила в редакцию 15.03.2021 г.
После доработки 29.03.2021 г.
Принята к публикации 20.07.2021 г.
Методом циклической вольтамперометрии изучено электрохимическое поведение фенотиазиново-
го красителя толуидинового синего в желатиновом гидрогеле в присутствии трипсина, пероксидазы
и их комбинации. Показано, что содержащаяся в гидрогеле пероксидаза оказывает существенное
влияние на электрохимические превращения толуидинового синего в течение первых 30 с измере-
ний. Добавление трипсина усиливает эффект пероксидазного катализа. Экспериментально обосно-
вана возможность одновременной оценки протеолиза и окислительно-восстановительного равно-
весия в модельной гидрогелевой системе при анализе вольтамперных кривых циклической вольт-
амперометрии. Полученные результаты обосновывают схему и принципы биоэлектрохимического
моделирования диффузии электроактивных молекул в межклеточном матриксе.
Ключевые слова: циклическая вольтамперометрия, биоэлектрохимия, гидрогели, трипсин, пероксидаза,
толуидиновый синий, in electrode-модели.
DOI: 10.31857/S0006302921050045
ствами матрикса [11]. Такие модели оптимальны
Электрохимические методы стали неотъемле-
и для изучения свойств матриксов тканеинже-
мым элементом современной физико-химиче-
нерных конструкций, и для конструирования
ской биологии [1-5], а в последнее десятилетие
электрохимических биосенсоров [10, 12-14].
электрохимия из аналитического метода превра-
тилась в информативный инструмент моделиро-
Одной из проблем при создании in electrode-
моделей является то, что окислительно-восстано-
вания биологических процессов in electrode [6]. В
вительные реакции, сравнительно легко воспро-
контексте электрохимического моделирования
изводимые в электрохимическом эксперименте,
процессов, происходящих на уровне тканей,
в биологических средах, как правило, осложня-
большой интерес представляет исследование гид-
ются ферментативным катализом. При этом фер-
рогелевых сред, являющихся естественными для
менты матрикса оказывают влияние не только на
большинства клеток многоклеточного организма
скорость собственно редокс-превращений реа-
[7-11]. На наш взгляд, электрохимические экспе-
гентов, но и на диффузионные свойства биологи-
рименты с использованием гидрогелевых сред
ческого гидрогеля, определяющие их локальные
наиболее адекватно отражают процессы, проис-
концентрации.
ходящие во внеклеточном матриксе, и могут слу-
Для сопряжения биохимических реакций с
жить прототипами in electrode-моделей биологи-
электродными целесообразно использовать ме-
чески значимых процессов (воспаление, морфо-
диаторы - молекулы, способные к быстрым и об-
генез, регенерация, синтез и выделение
ратимым окислительно-восстановительным пре-
гормональных продуктов, и др.), которые во мно-
вращениям как в биологических, так и в электро-
гом определяются физико-химическими свой-
химических процессах [15]. В настоящей работе в
качестве электрохимического медиатора исполь-
Сокращения: ТС - краситель толуидиновый синий, ФСБ -
фосфатно-солевой буферный раствор, ЦВА - цикличе-
зовали фенотиазиновый краситель толуидино-
ская вольтамперометрия.
вый синий (ТС). В предыдущих исследованиях
865
866
ЧЕРЕНКОВ и др.
мы выяснили, что ТС в нейтральных буферных
Измерения проводили методом циклической
растворах обладает воспроизводимым электрохи-
вольтамперометрии (ЦВА) на потенциостате-
мическим поведением [16], которое хорошо соот-
микроамперметре «Эколаб-2А» (ООО «Эковек-
ветствует диагностическим критериям обратимо-
тор», Ижевск, Россия) (точность измерений по-
сти [17]. При этом лимитирующей стадией элек-
тенциала ±1 мкВ, токов - ±1 нА). Использовали
трохимических превращений ТС является его
диапазон потенциалов 0…+460 мВ со скоростью
диффузия к электродной поверхности. Это под-
развертки потенциала 130 мВ/с. Измеряемым па-
тверждается экспериментами в гидрогелевых сре-
раметром были значения силы тока на рабочем
дах, когда протеолиз существенно ускоряет рост
электроде. Для оценки диффузии измерения про-
пиковых значений силы тока, повышая значения
водили в течение 21 мин с интервалом 7 с в
эффективного коэффициента диффузии ТС в ге-
первую минуту, а затем каждые 3 мин. Согласно
левой среде [16, 18]. Пероксидаза способна ис-
рекомендациям ИЮПАК на графиках ЦВА отри-
пользовать ТС в качестве восстановителя [19],
цательные токи соответствуют процессам элек-
оказывая влияние на соотношение окисленных и
тровосстановления, a положительные - процес-
восстановленных форм красителя в системе, что
сам электроокисления [16]. Значения потенциа-
позволяет применять ее для моделирования сдви-
лов приведены относительно хлорсеребряного
гов окислительно-восстановительного равнове-
электрода.
сия в тканях при использовании ТС как электро-
активной метки.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Таким образом, на поведение электроактив-
При отсутствии ферментов вольтамперные кри-
ной метки в межклеточном матриксе влияет ком-
вые ЦВА толуидинового синего, диффундирующего в
плекс разнообразных факторов, нуждающийся в
желатиновом гидрогеле в среде фосфатно-солевого
детальном изучении, в том числе и методами
буферного раствора, характеризуются наличием хо-
электрохимического моделирования. Поэтому
рошо выраженных анодного пика (Epa = -219.8 мВ),
целью настоящей работы стало исследование
электрохимического поведения толуидинового
соответствующего электроокислению ТС, и катодно-
синего как электроактивного медиатора в услови-
го пика (Epc = -280.2 мВ), сопровождающего его
ях модельной гидрогелевой среды при действии
электровосстановление. Значение ΔЕ = 60.4 мВ, а по-
трипсина и пероксидазы.
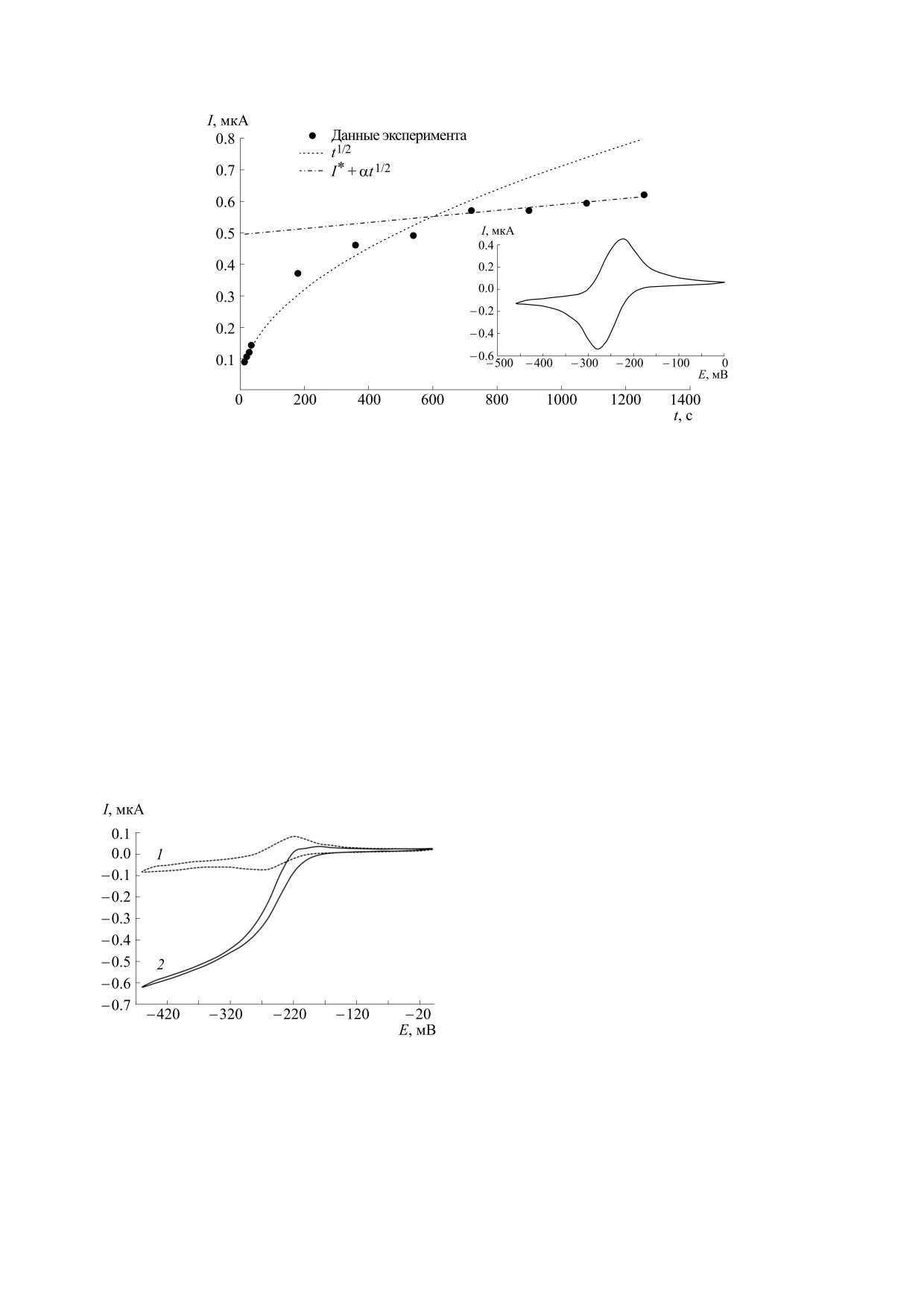
тенциал полуволны Е1/2 = 250 мВ (рис. 1, врезка). Пи-
ковые значения силы тока нарастают в ходе экспери-
мента, достигая 0.62 мкА в анодной области (рис. 1) и
МАТЕРИАЛЫ И МЕТОДЫ
-0.80 мкА - в катодной области, отражая поступле-
ние красителя к электродной поверхности.
В экспериментах использовали планарные
Анализ характера изменения анодного тока
электродные системы (ООО НПП «Автоком»,
показывает (рис. 1), что процесс электроокисле-
Москва, Россия), изготовленные методом трафа-
ния ТС в среде с ограниченной диффузией (гид-
ретной печати и включающие рабочий и вспомо-
рогеле) имеет две стадии, отличающиеся меха-
гательный электроды на основе графита, элек-
низмом формирования тока окисления. В интер-
трод сравнения - хлорсеребряный.
вале времени 0-720 с анодный ток возрастает за
Фоновым электролитом во всех измерениях
счет поступления красителя к поверхности со-
служил фосфатно-солевой буферный раствор
гласно закону Ipa ~ t до значения I*, которое в
(ФСБ) (рН 7.2), на котором готовили и все рабо-
проведенном эксперименте достигается при
чие растворы. Перед измерениями электроды
t = 720 с. Такая зависимость соответствует диф-
подвергали циклированию в буферном растворе в
фузионно-лимитируемому характеру электрохи-
диапазоне потенциалов +1000…-1000 мВ для ста-
мической реакции. Свыше t = 720 с наблюдается
билизации характеристик. Для формирования
переход к линейному характеру Ipa ~ I* + αt, что
гидрогеля на рабочий электрод наносили 1 мкл
может быть объяснено насыщением поверхности
раствора желатина (1.5 масс.%) или 1 мкл раство-
электрода толуидиновым синим и затруднением
ра желатина, содержащего пероксидазу из корней
отвода прореагировавших молекул от электрода.
хрена (RZ
>3.0) с удельной активностью
250 ед/мг. После формирования на рабочем элек-
Внесение в ячейку трипсина не приводило к
троде гидрогеля в ячейку вносили раствор ТС
существенному изменению пиковых значений
(0.1 мМ) с эквимолярным раствором пероксида
силы тока по сравнению с условиями гидрогеля,
водорода. В отдельной серии экспериментов для
не содержащего фермента. При используемых со-
моделирования протеолиза к перечисленным реа-
отношениях желатина и трипсина явных измене-
гентам добавляли трипсин из поджелудочной желе-
ний диффузионных свойств геля, регистрируе-
зы свиньи с удельной активностью 250 ед/мг до ко-
мых по скорости роста пиковых значений катод-
нечной концентрации в ячейке 0.001 масс. %.
ных и анодных токов, не обнаружено.
БИОФИЗИКА том 66
№ 5
2021
БИОЭЛЕКТРОХИМИЧЕСКОЕ МОДЕЛИРОВАНИЕ ДИФФУЗИИ
867
Рис. 1. Графики зависимости пиковых значений анодного тока от времени эксперимента в интервале 0-1260 с. На
врезке: типичная вольтамперная кривая ЦВА толуидинового синего (0.1 мМ) на графитовом планарном электроде
в среде желатинового геля, не содержащего ферментов, соответствующая моменту времени 720 с. Фоновый
электролит - ФСБ (рН 7.2) с добавлением пероксида водорода (0.1 мМ). Скорость развертки потенциала 130 мВ/с.
При диффузии ТС в желатиновом гидрогеле,
ют эффективный пероксидазный катализ. Вос-
содержащем пероксидазу, характер вольтамперо-
становленная форма ТС выступает в качестве
грамм наиболее существенно менялся на началь-
второго субстрата - донора электронов для пе-
ной стадии эксперимента. На 7-й-14-й секундах
роксидазы [19]. В результате высокой скорости
в анодной области ожидаемый (Epa = -219.8 мВ)
ферментативного окисления ТС в приэлектрод-
ном слое повышается концентрация окисленной
пик электроокисления ТС (рис. 2, кривые 1)
формы красителя, что сопровождается ростом то-
практически отсутствует (рис. 2, кривые 2), а в ка-
ков электровосстановления (катодных) и отсут-
тодной области наблюдается выраженный рост
ствием локального повышения значений силы
силы тока, достигающий максимума в точке раз-
тока электроокисления ТС в анодной области
ворота развертки потенциала.
(рис. 3).
Качественные изменения кривых ЦВА на на-
К третьей минуте эксперимента становятся за-
чальных этапах эксперимента, очевидно, отража- метными характерные пики (Epa = -219.8 мВ;
Epc = -280.2 мВ), соответствующие электрохими-
ческим превращениям красителя, и кривые ЦВА
приобретают сходство с зависимостями, полу-
ченными при отсутствии пероксидазы (рис. 4).
Вероятной причиной таких изменений кривых
ЦВА во времени может служить избранная схема
иммобилизации фермента на электроде. При на-
несении фермента в составе геля в приэлектрод-
ной области оказывается сравнительно неболь-
шое количество пероксидазы, которое и форми-
рует картину ЦВА на начальных этапах.
Еще одной гипотезой, объясняющей характер
изменения вольтамперных кривых, может слу-
жить представление об адсорбции красителя на
поверхность электрода, ограничивающей участие
в электрохимических превращениях диффунди-
Рис. 2. Вольтамперные кривые ЦВА толуидинового
рующих из геля молекул ТС, окисленных перок-
синего (0.1 мМ) в среде желатинового геля (кривые 1) и
сидазой. Поскольку большая часть молекул фер-
в присутствии пероксидазы (кривые 2) на
14-й
мента находится в геле на относительно большом
секунде эксперимента. Фоновый электролит - ФСБ
(рН 7.2) с добавлением 0.1 мМ пероксида водорода.
расстоянии от электродной поверхности, эффект
Скорость развертки потенциала 130 мВ/с.
ферментативного катализа существенен только
БИОФИЗИКА том 66
№ 5
2021
868
ЧЕРЕНКОВ и др.
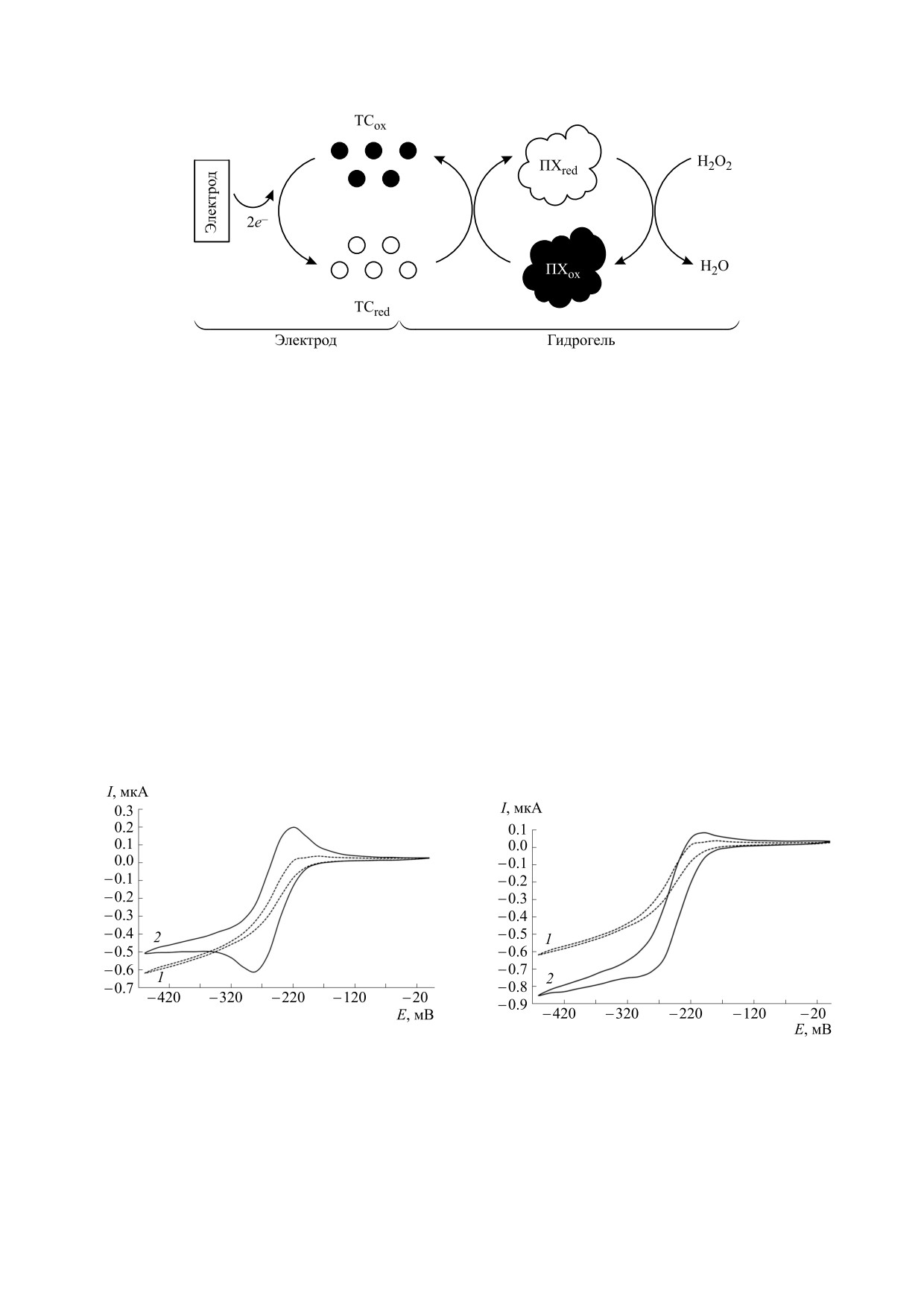
Рис. 3. Общая схема сопряжения электрохимического и биокаталитического процессов в эксперименте (по работе
[19] с изменениями). ПХ - пероксидаза из корней хрена.
на начальных этапах эксперимента. Затем основ-
диффузии субстратов пероксидазы (ТС и перок-
ной вклад в формирование вольтамперограмм
сида водорода) и самого фермента к приповерх-
вносят молекулы красителя, адсорбированные на
ностному слою электрода, где его каталитическая
электроде, состояние которых определяется
активность начинает более существенно влиять
электрохимическими циклами окисления-вос-
на электрохимические превращения ТС.
становления, а диффузия их от электрода затруд-
Протеолиз желатина облегчает диффузию ТС
нена гидрогелем.
в направлении раствора, что повышает вероят-
Если в растворе присутствует трипсин, то кри-
ность электровосстановления окисленных пе-
вые ЦВА на начальных стадиях эксперимента
роксидазой молекул. Подтверждением ускорения
(7-я-14-я секунды) приобретают характерную
диффузионных процессов служит формирование
S-образную форму, соответствующую перокси-
в условиях протеолиза более выраженного пика в
дазному окислению ТС (рис. 5, кривые 2). Значе-
анодной области (Е ≈ -200 мВ), соответствующе-
ния катодных токов и скорость их нарастания су-
го электроокислению ТС.
щественно превосходят показатели, полученные
Информативным показателем, характеризую-
в отсутствие протеолиза (рис. 5, кривые 1).
щим процессы, происходящие на электроде, ока-
Роль трипсина в формировании таких вольт-
залось соотношение пиковых значений силы тока
амперограмм, вероятно, сводится к ускорению (рис. 6). Для идеально обратимого электрохими-
ческого процесса этот показатель стремится к
Рис. 4. Вольтамперные кривые ЦВА толуидинового
синего
(0.1 мМ) в среде желатинового геля в
Рис. 5. Вольтамперные кривые ЦВА толуидинового
присутствии пероксидазы: на
14-й секунде
синего (0.1 мМ) в среде желатинового геля в присут-
эксперимента (кривые 1) и через 3 мин (кривые 2)
ствии пероксидазы хрена (кривые 1), при добавле-
после начала измерений. Фоновый электролит -
нии трипсина (кривые 2) на 14-й секунде экспери-
ФСБ (рН 7.2) с добавлением 0.1 мМ пероксида
мента. Фоновый электролит - ФСБ (рН 7.2). Ско-
водорода. Скорость развертки потенциала 130 мВ/с.
рость развертки потенциала 130 мВ/с.
БИОФИЗИКА том 66
№ 5
2021
БИОЭЛЕКТРОХИМИЧЕСКОЕ МОДЕЛИРОВАНИЕ ДИФФУЗИИ
869
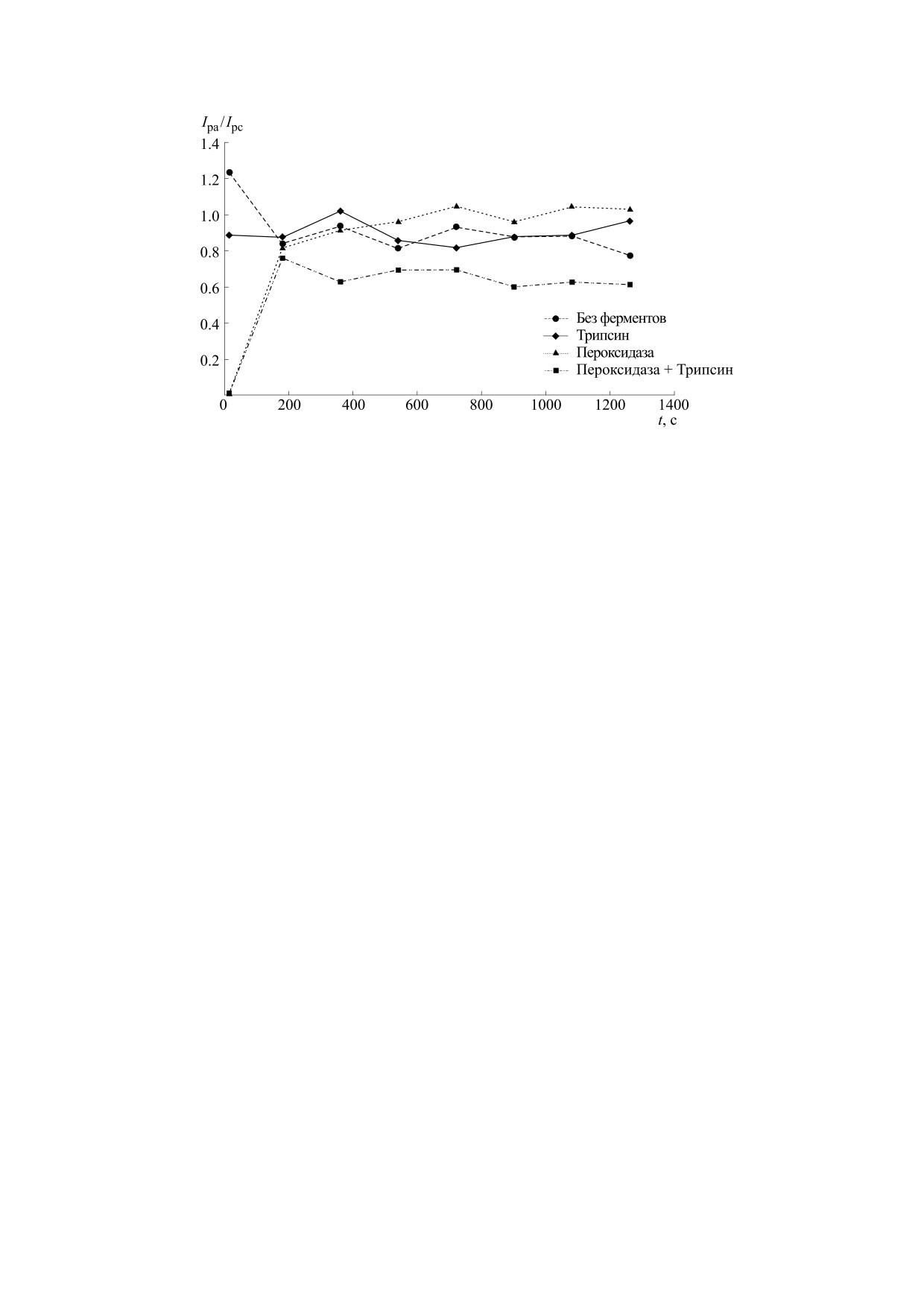
Рис. 6. Изменения соотношения пиковых значений анодных и катодных токов при разных условиях эксперимента.
Фоновый электролит - ФСБ (рН 7.2) с добавлением пероксида водорода (0.1 мМ). Скорость развертки потенциала
130 мВ/с.
единице [17]. В условиях наших экспериментов
затель близок к критериям так называемого EC'-
соотношение токов определялось прежде всего
процесса (каталитической электродной реакции)
присутствием пероксидазы или трипсина, либо
[17], но в условиях диффузионных ограничений
их комбинации, а также диффузионными огра-
белкового гидрогеля его удается достичь только с
ничениями, накладываемыми гидрогелевой
помощью протеолиза.
средой.
Таким образом, комбинированное действие
В среде гидрогеля с естественным насыщени-
трипсина и пероксидазы в желатиновом гидрогеле
ем кислородом соотношение пиковых значений
усиливает ферментативное окисление ТС и облег-
силы тока Ipа/Ipс в начале измерений составило
чает его регистрацию методом циклической вольт-
1.2, что может быть объяснено некоторым преоб-
амперометрии. При создании моделей биологиче-
ладанием на начальном этапе окисленной формы
ских тканей in electrode или при использовании
ТС. К концу эксперимента этот показатель вы-
электрохимических методов in vivo необходимо
равнивался, и среднее значение в серии измере-
учитывать, что протеолиз, как правило, не приво-
ний составляло 0.9.
дящий к образованию электроактивных продук-
тов, может оказывать существенное влияние на ре-
Трипсиновый протеолиз, не оказывая суще-
зультаты электрохимического эксперимента.
ственного влияния на пиковые значения силы то-
ка, отражался на их соотношении. Оно оказалось
близким к единице и более стабильным в ходе
ВЫВОДЫ
эксперимента, чем в отсутствие трипсина, что
может быть объяснено меньшими диффузионны-
1. Диффузия толуидинового синего в желати-
ми ограничениями.
новом гидрогеле (1.5 масс. %) в отсутствие фер-
ментов может быть оценена как серия вольтам-
Особенно выраженное влияние на соотноше-
перных кривых ЦВА с логарифмическим ростом
ние Ipа/Ipс оказывает пероксидаза. Вследствие
пиковых значений силы тока (от 0.0072 мкА
ферментативного окисления в начальный мо-
до 0.8 мкА в анодной области (Epa = -219.8 мВ);
мент времени соотношение токов резко смеща-
от -.0089 мкА до -0.62 мкА - в катодной (Epc =
лось в сторону электровосстановления ТС. К тре-
тьей минуте показатель выравнивался и сохра-
= -280.2 мВ)).
нялся близким к единице до конца эксперимента.
2. Внесение в желатиновый гидрогель перок-
В присутствии трипсина эффект пероксидаз-
сидазы приводит к формированию на начальных
ного катализа отражался на значениях силы тока
этапах эксперимента катодных токов, достигаю-
до конца эксперимента. Соотношение Ipа/Ipс
щих -0.6 мкА, и снижению анодных токов до
0.004 мкА.
оказалось низким в начале эксперимента, затем
сместилось к единице, а с девятой минуты для
3. Трипсин, вносимый одновременно с суб-
всех циклов было стабильным (≈ 0.6). Этот пока-
стратами пероксидазы, приводит к повышению
БИОФИЗИКА том 66
№ 5
2021
870
ЧЕРЕНКОВ и др.
на 14-й секунде катодных токов до -0.85 мкА и
4. Л. М. Балашова, И. И. Колесниченко, В. А. На-
стабильному снижению соотношения Ipа/Ipс до
миот и др., Биофизика 63 (6), 1088 (2019).
5. M. Stoytcheva, R. Zlateva, S. Cosnier, et al., Electro-
0.6 с девятой минуты эксперимента.
chim. Acta 76, 43 (2012).
4. Исследование вольтамперного поведения
6. В. В. Шумянцева, Т. В. Булко, Е. В. Супрун и др.,
толуидинового синего в модельном белковом
Биомед. химия 61 (2), 188 (2015).
гидрогеле позволяет оценить его диффузионные
7. J. T. Trevors and G. H. Pollack, Prog. Biophys. Mol.
свойства и пероксидазную активность с учетом
Biol. 89 (1), 1 (2005).
влияния протеолиза.
8. K. B. Fonseca, S. J. Bidarra, M. J. Oliveira, et al., Acta
Biomater. 7 (4), 1674 (2011).
ФИНАНСИРОВАНИЕ РАБОТЫ
9. B. Sarker, R. Singh, R. Silva, et al., PLoS One 9 (9), 1
(2014).
Исследование выполнено при финансовой
10. M. T. Spang and K. L. Christman, Acta Biomater. 68,
поддержке Российского научного фонда (проект
1 (2019).
№ 19-79-20012).
11. S. Park, S. Lim, P. Siriviriyakul, et al., Phys. Rev. E 101
(5), 052414 (2020).
КОНФЛИКТ ИНТЕРЕСОВ
12. G. G. Giobbe, C. Crowley, C. Luni, et al., Nat. Com-
mun. 10 (1), 1 (2019).
Авторы заявляют об отсутствии конфликта
13. J. H. Traverse, T. D. Henry, N. Dib, at al., JACC Basic
интересов.
to Transl. Sci. 4 (6), 659 (2019).
14. D. Buenger, F. Topuz, and J. Groll, Prog. Polym. Sci.
37 (12), 1678 (2012).
СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ
15. E. Katz, A. N. Shipway, and I. Willner, in Encyclopedia
Настоящая работа не содержит описания ис-
of Electrochemistry, Ed. by G. S. Wilson (Wiley-VCH
следований с использованием людей и животных
GmbH, Weinheim, 2002), pp. 559-626.
в качестве объектов.
16. И. А. Черенков, К. С. Раевских, В. Г. Сергеев и др.,
Актуальные вопросы биологической физики и
химии 3 (2), 422 (2018).
СПИСОК ЛИТЕРАТУРЫ
17. Электроаналитические методы, под ред. Ф.М. Шоль-
1. A. Heiskanen and J. Emnéus, in Modern aspects of elec-
ца (Бином «Лаборатория знаний», М., 2010).
trochemistry, Ed. by N. Eliaz 52, 1 (2011).
18. И. А. Черенков, Л. С. Березина, М. Д. Кривилев
2. Y. Cao, J. Yu, B. Bo, et al., Biosens. Bioelectron. 45, 1
и др., Актуальные вопросы биологической физики
(2013).
и химии 5 (3), 481 (2020).
3. E. González-Fernández, N. Avlonitis, A. F. Murray,
19. K. Thenmozhi and S. S. Narayanan, Mater. Sci. Eng.
et al., Biosens. Bioelectron. 84, 82 (2016).
C. 70, 223 (2017).
Bioelectrochemical Modeling of Toluidine Blue Diffusion in a Hydrogel
in the Presence of Peroxidase and Trypsin
I.A. Cherenkov*, **, M.D. Krivilev*, ****, M.M. Ignat’eva*,
E.V. Vahrusheva*, **, and V.G. Sergeev*, **
*Udmurt State University, Universitetskaya ul. 1, Izhevsk, 426034 Russia
**Izhevsk State Medical Academy, ul. Kommunarov 281, Izhevsk, 426034 Russia
***Udmurt Federal Research Center, Ural Branch of the Russian Academy of Sciences,
ul. Tatiany Baramzinoj 34, Izhevsk, 426067 Russia
The electrochemical properties of toluidine blue, a phenothiazine dye, in a gelatin hydrogel in the presence
of trypsin, peroxidase, and their combination have been studied by means of cyclic voltammetry. It was shown
that peroxidase present in the hydrogel has a significant effect on the electrochemical transformations of tolu-
idine blue during the first 30 seconds of measurements. The addition of trypsin enhances the effect of perox-
idase catalysis. The feasibility of simultaneous assessment of proteolysis and redox equilibrium in a model hy-
drogel system in the analysis of voltammetric curves of cyclic voltammetry has been experimentally validated.
The obtained results demonstrate that the scheme and principles of bioelectrochemical modeling of the dif-
fusion of electroactive molecules in the intercellular matrix work reasonably well.
Keywords: cyclic voltammetry, bioelectrochemistry, hydrogels, trypsin, peroxidase, toluidine blue, in electrode-
models
БИОФИЗИКА том 66
№ 5
2021