БИОФИЗИКА, 2022, том 67, № 2, с. 264-266
БИОФИЗИКА КЛЕТКИ
УДК 577.321
РЯД КАТИОННОЙ СЕЛЕКТИВНОСТИ КАНАЛОВ,
ФОРМИРУЕМЫХ ПЕРОКСИРЕДОКСИНОМ-6
В БИМОЛЕКУЛЯРНЫХ ФОСФОЛИПИДНЫХ МЕМБРАНАХ
© 2022 г. П.А. Григорьев
Институт биофизики клетки РАН - обособленное подразделение ФИЦ «Пущинский научный центр биологических
исследований РАН», 142290, Пущино Московской области, Институтская ул., 3
E-mail: greegorjev@mail.ru
Поступила в редакцию 30.11.2021 г.
После доработки 10.12.2021 г.
Принята к публикации 12.12.2021 г.
Пероксиредоксин-6 - фермент, защищающий клетку от действия пероксидов, а также, в зависимо-
сти от локализации в клетке, участвующий в метаболизме фосфолипидов клеточных мембран. Так-
же было показано, что пероксиредоксин-6 формирует катионные каналы в липидных бислойных
мембранах. В данной работе изучена сравнительная проницаемость этих каналов для одно- и двух-
валентных катионов. Полученный ряд проницаемостей имеет вид: РСа2+ : РК+ : РNa+ = 8.5 : 5.0 : 1.0.
Ключевые слова: пероксиредоксин-6, ионные каналы, катионная селективность.
DOI: 10.31857/S000630292202089
Был применен раствор фосфатидилхолина (Sig-
Пероксиредоксины защищают клетки от пе-
ma, США) в гептане (10 мг/мл).
роксидов и участвуют во внутри и внеклеточной
сигнализации. Особый интерес представляет пе-
Токи мембран измеряли в режиме фиксации
роксиредоксин-6 (Prx6), который восстанавлива-
напряжения электрометром, собранным на осно-
ет гидроперекиси и обладает фосфолипазной ак-
ве микросхемы К544УД1А.
тивностью [1].
Для оцифровки, записи и анализа сигнала с
При изучении взаимодействия Prx6 с бислой-
выхода электрометра использовали цифроанало-
говый преобразователь NI USB-6009 (National In-
ной фосфолипидной мембраной было показано,
struments, США) и программу Strathclyde Electro-
что этот фермент формирует в мембране катион-
селективные ионные каналы, и было предполо-
physiology Software WinEDR v. 3.2.3.
жено, что механизм клеточной активности Prx6
включает функцию формирования ионных кана-
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
лов в липидном матриксе клеточных мембран
(рис. 1) [2]. Определенный интерес представляет
Характерное возрастание тока мембраны при
встраивании в нее Prx6-каналов в растворах КСl и
дальнейшее изучение свойств этих каналов. В
СаСl2 показано на рис 1. Наблюдаемое неравен-
предлагаемой работе представлены результаты
исследования ряда катионной селективности
ство амплитуд последовательных токовых ступе-
Prx6-каналов.
нек объяснимо тем, что встраиваемые кластеры
каналов содержат разное количество одиночных
ионных каналов.
МАТЕРИАЛЫ И МЕТОДЫ
Приведенные ниже уравнения Нернста для
Был использован рекомбинантный перокси-
мембранного потенциала одновалентных ионов
редоксин-6 человека, методика выделения кото-
(1) и двухвалентных ионов (2) показывают, что
рого детально описана в работе [2].
Prx6-каналы проницаемы только для катионов.
Действительно, потенциал нулевого тока, равный
Бимолекулярные липидные мембраны фор-
-25 мВ при трехкратной трансмембранной раз-
мировали на круглом, диаметром 0.3 мм, отвер-
нице концентраций КСl, соответствует идеаль-
стии в тефлоновом цилиндрическом стаканчике.
ной селективности каналов для катионов К+
Сокращениe: Prx6 - пероксиредоксин-6.
(рис. 2а), тогда как при двукратном градиенте
264
РЯД КАТИОННОЙ СЕЛЕКТИВНОСТИ КАНАЛОВ
265
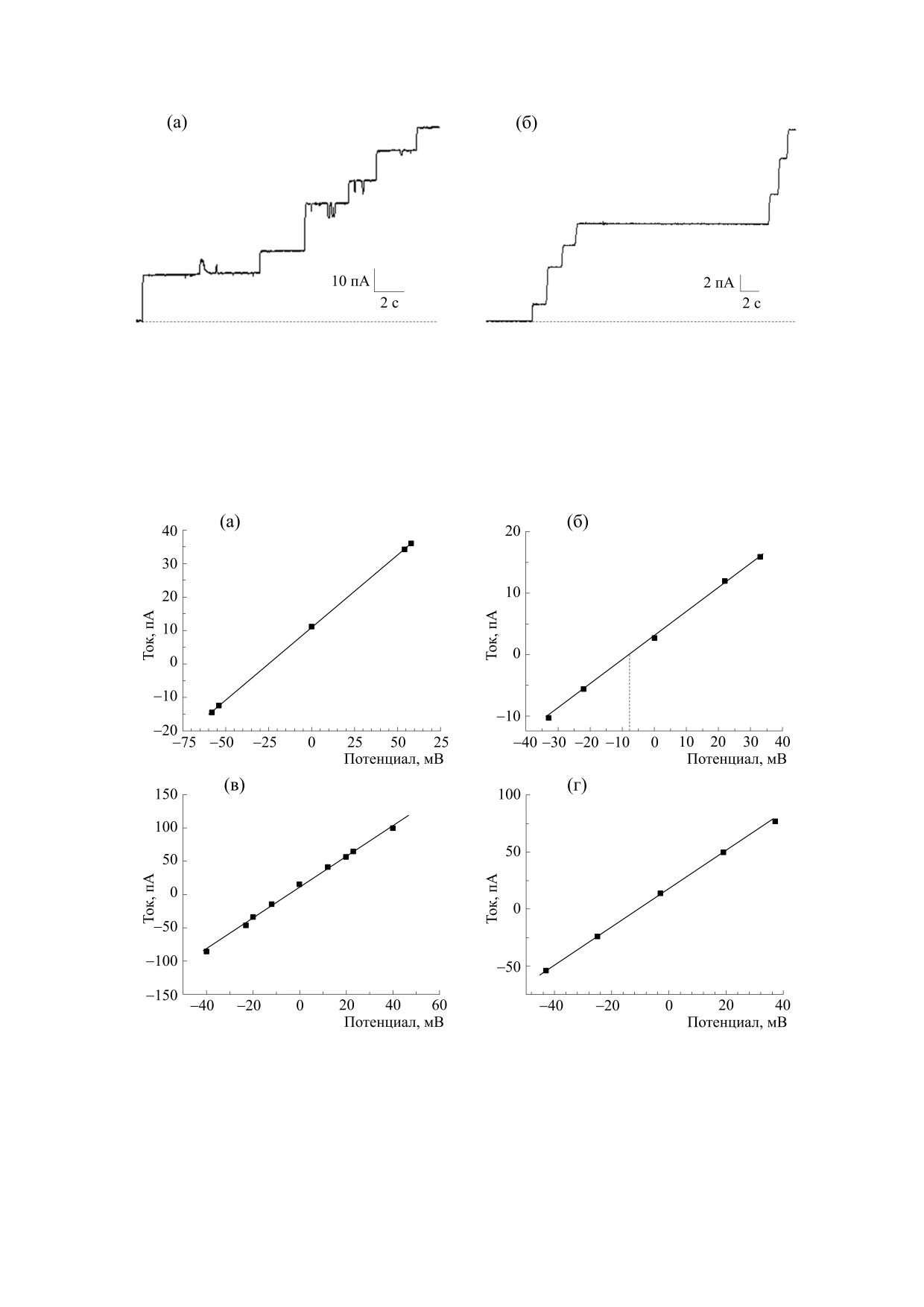
Рис. 1. Нарастание тока мембраны с Prx6-каналами. Условия: (а) - 200 мМ КСl (по обе стороны мембраны), V = 30 мВ,
калибровки: 10 пA и 2 с; (б) - 10 мМ СaCl2 (по обе стороны мембраны), V = 30 мВ, калибровки: 2 пA и 2 с.
СаСl2 потенциал нулевого тока равен -8 мВ
V (мВ) = 60 log(K0+/Ki+),
(1)
(рис. 2б), т. е. каналы проницаемы только для
ионов кальция.
V (мВ) = 30 log(Ca02+/Cai2+).
(2)
Рис. 2. Вольт-амперные характеристики Prx6-каналов: (а) - при трехкратном трансмембранном градиенте концентраций
KCl (300 : 100 мМ), потенциал нулевого тока равен -25 мВ; (б) - при двукратном градиенте концентрации СаСl2
(20 : 10 мМ), потенциал нулевого тока равен -8 мВ; (в) - при 100 мM КСl + 300 мM NaCl с одной стороны мембраны и
100 мM KCl - с другой стороны мембраны, потенциал нулевого тока равен -12 мВ; (г) - при 50 мМ КС1 + 20 мМ
СаС12 с одной стороны мембраны и 50 мМ КС1 + 37 мМ СаС12 - с другой стороны мембраны, потенциал нулевого тока
равен -15 мВ.
БИОФИЗИКА том 67
№ 2
2022
266
ГРИГОРЬЕВ
Для определения соотношения проницаемо-
при условии, что РСа2+ : РК+ = 1.7 и РК+ : РNa+ =
стей канала: РСа2+ : РNa+ и РС2+ : РК+ использова-
= 5.0, и нормировке на РNa+ = 1.0.
ли данные, представленные на рис. 2в и 2г, при-
Видно, что Prx6-канал является в основном
меняя уравнение Гольдмана (3) и формулу (4) из
кальциевым каналом. Это особенно интересно в
работы [3].
связи с появлением ряда работ, в которых пока-
зан синергизм действия кальция и пероксиредок-
V (мВ) = 60 log[(РK+[К0] +
синов в клеточных реакциях. Так, например, по-
+ РNa+[Na0])/(РK+[Кi] + РNa+[Nai])],
(3)
казано, что кальций влияет на олигомеризацию
пероксиредоксинов [5] и что пероксиредоксины
V0 = (PK+VK+ + PCa2+VCa2+) / (PK+ + PCa2+),
(4)
взаимодействуют с активатором кальциевых ка-
налов - белком STIM1 плазматической мембра-
где PK+ - калиевая проводимость канала, PCa2+ -
ны [6].
кальциевая проводимость канала, V0 - потенциал
нулевого тока, VK+
- калиевый потенциал,
КОНФЛИКТ ИНТЕРЕСОВ
VCa2+ - кальциевый потенциал.
Автор заявляет об отсутствии конфликта инте-
На рис. 2в показано, что потенциал нулевого
ресов.
тока при условиях, когда с одной стороны мем-
браны электролит содержит 100 мM КСl + 300 мM
СОБЛЮДЕНИЕ ЭТИЧЕСКИХ СТАНДАРТОВ
NaCl, а с другой стороны мембраны - 100 мM
KCl, равен -12 мВ. Решение уравнения для этих
Настоящая работа не содержит описания ис-
параметров дает отношение РК+ : РNa+ = 5.0.
следований с использованием людей и животных
в качестве объектов.
Значение РСа2+ : РК+ = 1.7 было определено из
формулы (4) для условий, когда с одной стороны
мембраны электролит содержал 50 мМ КС1 и
СПИСОК ЛИТЕРАТУРЫ
20 мМ СаС12, а с другой стороны мембраны -
1. М. Г. Шарапов, В. И. Новоселов и В. К. Равин,
50 мМ КС1 и 37 мМ СаС12 (одинаковые концен-
Молекуляр. биология 43 (3), 505 (2009).
трации для КС1 и разные по СаС12). Параметры
2. П. А. Григорьев, М. Г. Шарапов и В. И. Новосе-
формулы для этих условий равны: V0 = 15 мВ
лов, Биофизика 60 (4), 696 (2015).
(рис. 2г), VСа2+ = 8 мВ и VК+ = 0 (получены как ре-
3. C. A. Lewis, J. Physiol. 286, 417 (1979).
шения уравнений Нернста (1) и (2)).
4. M. A. B. Morais, P. O. Giuseppe, T. A. C. B. Souza,
В итоге суммарное соотношение проницаемо-
et al., J. Biol. Chem. 292 (17), 7023 (2017).
стей Prx6-канала для катионов кальция, калия и
5. K. Ch. Tam, E. Ali, J. Hua, et al., Cell Calcium, 74, 14
натрия имеет вид РСа2+ : РК+ : РNa+ = 8.5 : 5.0 : 1.0
(2018).
Cation Selectivity Sequence of Channels Formed by Peroxiredoxin 6 in Membranes
Composed of Phospholipid Bimolecular Leaflets
P.A. Grigoriev
Institute of Cell Biophysics, Russian Academy of Sciences, Institutskaya ul. 3, Pushchino, Moscow Region, 142290 Russia
Peroxiredoxin 6 is an enzyme that protects against cellular damage by peroxides and participates in phospho-
lipid metabolism in the cell’s membranes depending on its location. It has also been shown that peroxiredoxin
6 forms cation channels in the lipid bilayer membranes. In this study, we evaluated the relative selectivity of
these channels for monovalent and divalent cations. The resulted selectivity sequence is РСа2+ : РК+ : РNa+ =
8.5 : 5.0 : 1.0.
Keywords: peroxiredoxin 6, ion channels, cation selectivity
БИОФИЗИКА том 67
№ 2
2022