БИОХИМИЯ, 2019, том 84, вып. 5, с. 603 - 615
УДК 577.152.211
РЕПАРАЦИЯ БЕЛКОВ С УЧАСТИЕМ PIMT:
МЕХАНИЗМ И ЗНАЧЕНИЕ
Мини обзор
© 2019 P.K.K. Mishra*, M. Mahawar
Division of Biochemistry, Indian Veterinary Research Institute,
Izatnagar, Bareilly, Uttar Pradesh, India, 243122;
E mail: prasantmodel@gmail.com
Поступила в редакцию 25.07.2018
После доработки 18.12.2018
Принята к публикации 29.12.2018
Известны различные ковалентные модификации аминокислотных остатков белков. Однако было иденти
фицировано лишь несколько ферментов, восстанавливающих аминокислотные остатки до исходного состо
яния. Фермент PIMT (L изоаспартат (D аспартат) O метилтрансфераза), также известный как PCMT
(L изоаспартил/D аспартилметилтрансфераза карбоксильных групп белка), метилирует ковалентно моди
фицированные остатки изоаспартата (iso Asp). Остатки iso Asp накапливаются в белках в результате деами
дирования остатка аспарагина (Asn) или при гидролизе остатка аспарагиновой кислоты (Asp). Эта реакция
протекает в цитоплазме, и в ходе этой реакции образуется промежуточный продукт - сукцинимид. Затем
эта циклическая молекула снова превращается как в iso Asp, так и Asp. Превращение сукцинимида в аспар
тат происходит спонтанно, в то время как восстановление iso Asp осуществляется с помощью фермента
PIMT с использованием S аденозилметионина (SAM) в качестве донора метильной группы. PIMT превра
щает сукцинимид обратно в iso Asp и, таким образом, создает условия для дальнейшего превращения в ас
партат. Кроме нормальных физиологических условий, повышенное образование остатков iso Asp в белках
могут вызывать различные стрессовые факторы. Образующиеся остатки iso Asp могут формировать петли
или изгибы (повороты) в полипептидном остове, вызывая изменения конформации и функционирования
белков. Показано, что в различных эукариотических клетках, а также и в некоторых прокариотических
клетках присутствуют многочисленные белки, которые взаимодействуют с PIMT (у этих белков есть остат
ки iso Asp). Кроме того, обширные исследования, проведенные на мышах, показали важность этого белка
при нейродегенеративных условиях. Детальное изучение функций PIMT может создать платформу для
борьбы с такими заболеваниями, как болезнь Альцгеймера и рак.
КЛЮЧЕВЫЕ СЛОВА: L изоаспартат (D аспартат) O метилтрансфераза, изоаспартат, S аденозилметио
нин, сукцинимид.
DOI: 10.1134/S0320972519050014
Метилирование белка - это сложный и раз
тине амебы [6] и среди свободных аминокислот
нообразный процесс [1]. Значение метилирова
в моче человека [7] присутствует ε N диметил
ния белка, а также его роль в регуляции генов и
лизин. Миозин и актин скелетной мышцы кро
передаче сигналов в настоящее время хорошо
лика содержат 3 N метилгистидин [8, 9]. Было
известны [2]. Во многих белках были выявлены
также показано, что в овальбумине селезенки
метильные производные различных аминокис
теленка [10] присутствуют остатки карбоксиме
лот естественного происхождения. Так, было
тиласпарагиновой кислоты. Кроме того, следует
показано, что белок жгутиков Salmonella typhi
отметить, что метилирование аминокислотных
murium [3] и гистоновые белки тимуса содержат
остатков в белках происходит после образова
ε N метиллизин [4]. Также было показано, что в
ния пептидной связи, и этот процесс играет
миозине камбаловидной мышцы кошки [5], ак
важную роль в физиологии клетки [11]. Фер
менты, ответственные за метилирование бел
ков, образуют обширный класс и обозначаются
Принятые сокращения: iso Asp - изоаспартат (isoas
как метилтрансферазы белков (PMT - protein
partate); PIMT - L изоаспартат (D аспартат) O метилтранс
фераза (L isoaspartate (D aspartate) O methyltransferase);
methyl transferase) [12]. По видимому, во всех
SAM - S аденозилметионин (S adenosyl methionine).
живых организмах почти 2% генов кодируют
* Адресат для корреспонденции.
метилтрансферазы. Этот класс белков включает
603
604
MISHRA, MAHAWAR
в себя значительное количество ферментов, ис
установлено, что у E. coli связывание аспартил
пользующих белок в качестве субстрата [13].
тРНК с остатком L Asp иногда происходит с
Метилтрансферазы белков (PMTs) подразделя
участием β COOH , а не α COOH группы [24].
ются на три класса на основе их предпочтений
Этот механизм имитирует тривиальный путь
относительно аминокислотных остатков, под
включения аминокислот в полипептидную
вергающихся метилированию (Arg, Gln/Asp и
цепь. У многих короткоживущих белков, таких
Lys соответственно). В качестве донора метиль
как мембранные белки эритроцитов человека
ной группы эти ферменты используют S адено
(RBCs - red blood cells) и стареющие белки, ос
зилметионин (SAM) [13]. В последнее время бы
татки D Asp образуются вследствие деамидиро
ли получены доказательства, которые сущест
вания белка. Кроме того, происходит спонтан
венно расширили понимание функционирова
ное образование D сукцинимида из L сукцини
ния этих ферментов, как, например, вопросы,
мида. D сукцинимид может снова превратиться
касающиеся их роли в эпигенетической регуля
в L сукцинимид или же может образовать струк
ции посредством модификации гистоновых
туру D Asp/D iso Asp. В свою очередь, D Asp
концевых участков, и в проявлении таких видов
может подвергнуться метилированию с по
активности, как сенсорная адаптация бактерий
мощью фермента PIMT с образованием исход
к воздействию химических стимулов, ответы
ного остатка L Asp (рис. 1) [25]. Это предотвра
клеток на стресс, клеточное старение, репара
щает накопление в организме аномального D сте
ция белков и реактивация некоторых из них
реоизомера.
[14-18]. Так, белки PCMT осуществляют репа
Iso Asp вызывает конформационные измене
рацию остатков iso Asp в белках с образованием
ния в белке. Для нормального функционирова
остатков аспарагиновой кислоты. Поэтому они
ния белка необходимым условием является це
также известны как изоаспартатметилтрансфе
лостность его структуры и конформационная
разы белков (PIMT - protein isoaspartate methyl
стабильность. Но во многих случаях различные
transferase). К настоящему времени распростра
необычные аминокислотные остатки, такие как
ненность белков PIMT и их роль в репарации
окисленный метионин или изоаспарагиновая
белков достаточно хорошо изучены. В данном
кислота, могут внести хаос в структурную ие
обзоре обсуждаются последние достижения в
рархию белка, тем самым ставя под угрозу его
области изучения структуры и функций этих
функционирование [26, 27]. Подробное описа
ферментов.
ние различных повреждений белков и их послед
ствий приведено в работе Chondrogianni et al. [27].
В присутствии измененного остатка аспартата
ОБРАЗОВАНИЕ ИЗОАСПАРТАТА
можно наблюдать изменения конформации или
И ЕГО ПОСЛЕДСТВИЯ
Образование остатков iso Asp происходит в
результате деамидирования или дегидратации
аспарагиновой кислоты. Хотя и не всегда, но та
кая рацемизация является спонтанным физио
логическим процессом, и обращение этого про
цесса с возвращением белка в его нативное сос
тояние ускоряется ферментом PIMT [19].
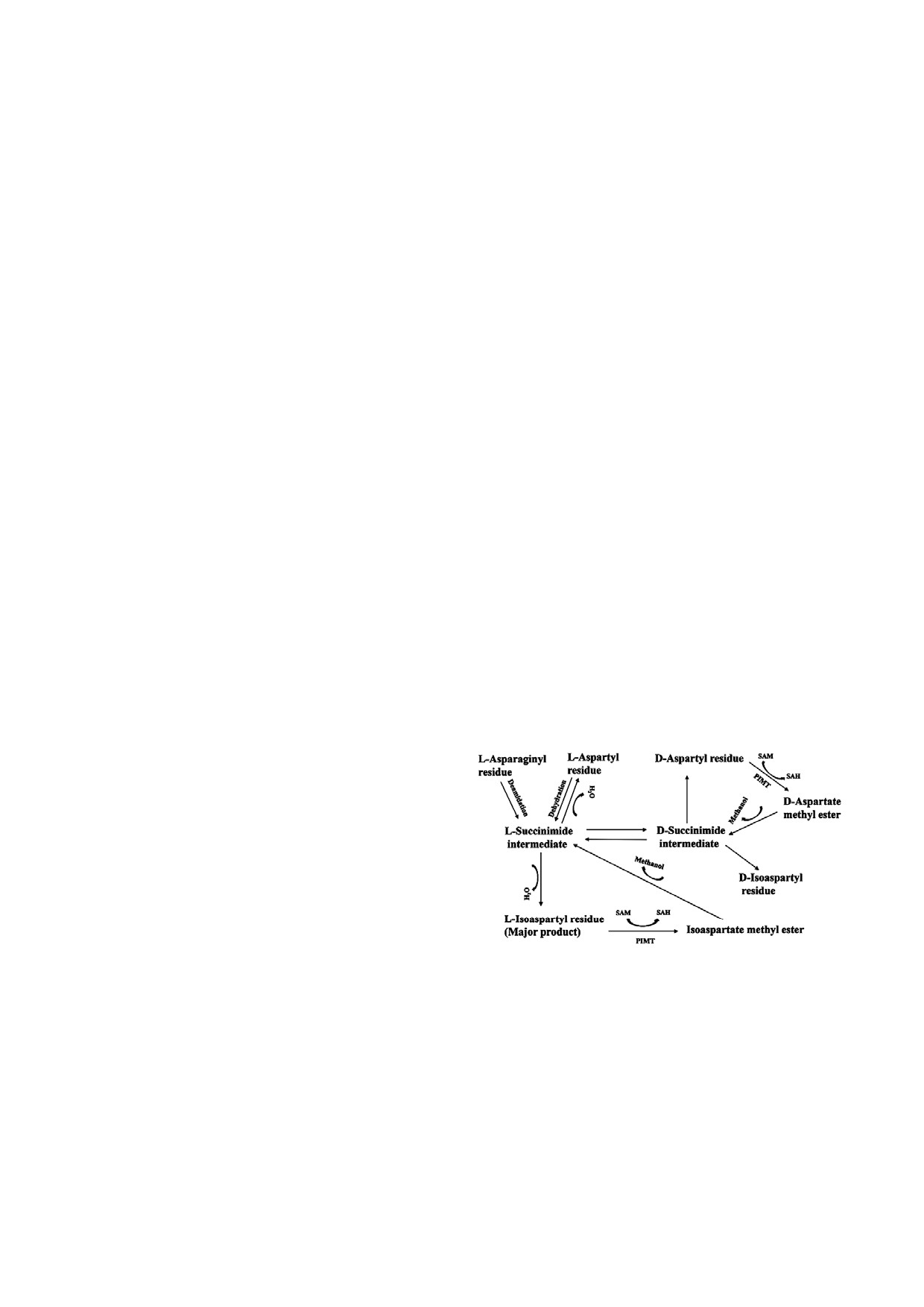
Образование iso Asp (и D Asp). Этот процесс
представляет собой межмолекулярную реакцию
перераспределения, протекающую при различ
ных физиологических условиях, минуя стадию
промежуточного продукта (сукцинимид), с об
Рис. 1. Репарация L iso Asp ускоряется белком PIMT: ме
разованием изомеризованных остатков L iso Asp
тилирование остатков L iso Asp и D Asp увеличивает ско
рость их превращения в L сукцинимид и D сукцинимид
(рис. 1) [20]. Как правило, консенсусная после
соответственно. Будучи промежуточным продуктом, сук
довательность Asn/Asp Gly/Ser благоприятству
цинимид спонтанно превращается обратно в L Asp, таким
ет деамидированию и образованию остатков iso
образом продолжая цикл. Количественное определение
Asp [21]. Следует отметить, что в пептидах остат
высвобождающегося метанола во время реакции является
ки аспарагина в 10 раз более подвержены деами
важным способом измерения активности PIMT. Хотя
только 25% сукцинимида обратно превращаются в исход
дированию, чем остатки аспарагиновой кисло
ную форму аспартата, тем не менее циклическая реакция
ты. В то же время в случае белков остатки аспа
приводит к полному восстановлению исходного остатка.
рагиновой кислоты являются более лабильны
Адаптировано и представлено с доработками исходного
ми, чем остатки аспарагина [22, 23]. Было также
рисунка из статьи Furuchi et al. [100]
БИОХИМИЯ том 84 вып. 5 2019
PIMT ОПОСРЕДОВАННАЯ РЕПАРАЦИЯ БЕЛКОВ
605
образование изгибов в пептидном остове белка
ратуры в бактериальном белке HPr [39]. Очевид
(рис. 2). Приставка «изо» используется для обоз
но, что воздействие органического растворите
начения пептидной связи, образованной с учас
ля, такого как метанол, и адаптация к стацио
тием групп, отличных от α амино и карбо
нарной фазе способствовали образованию iso Asp
ксильной групп аминокислоты. Остаток аспар
у прокариот [40]. Lyon et al. недавно показали,
тата содержит две СООН группы, в то время
что белок, склонный к образованию iso Asp,
как в аспарагине имеются две NH2 группы (т.е.
располагается в кристаллине человека, для ко
β группы). Эта β группа ответственна за пеп
торого характерно присутствие непрерывного
тидную связь в измененной структуре. Струк
участка, образованного остатками аспарагина.
турно остаток iso Asp содержит внешний атом
Кроме того, установлено, что предпочтительность
углерода в пептидном остове и аномальную кар
α варианта по сравнению с β кристаллином в
боксильную боковую цепь. Этот дополнитель
бóльшей степени обусловлена обилием в его
ный остаток вызывает значительное нарушение
структуре аспарагин содержащих участков [41].
характерных для белка вторичных и третичных
структур [28].
Идентификация остатков iso Asp в белках и
БИОХИМИЯ PIMT
пептидах. Аспартат и изоаспартат являются
структурными изомерами, что не позволяет раз
Нуклеофильная атака пептидным остовом
личить их по массе [29]. Такие ограничения мо
инициирует восстановление измененных остатков
гут быть преодолены с помощью химических и
Asn/Asp. Восстановление измененного остатка
ферментативных методов, включая определение
Asn/Asp начинается с нуклеофильной атаки
гидразина [30], методы масс спектрометрии
пептидного азота на карбонильный углерод ас
MALDI TOF MS [31], ESI MS [32] и метод ECD
парагина или карбоксилатный углерод остатка
(electron capture dissociation, диссоциация захва
аспарагиновой кислоты. В любом случае это
та электронов) MS [33]. Другой подход, с по
приводит к образованию неустойчивого цикли
мощью которого можно отличить остаток аспа
ческого промежуточного продукта - сукцини
рагина от изоаспарагиновой кислоты, заключа
мида. Этот промежуточный продукт имеет две
ется в использовании свойств Asp N - эндопро
карбонильные группы, которые подвержены
теазы, специфичной для остатка аспарагина;
гидролитическому расщеплению и определяют
iso Asp затем можно будет обнаружить с исполь
судьбу образования iso Asp. Гидролиз по одной
зованием метода диссоциации переноса элект
карбонильной группе приводит к образованию
ронов [34]. Остатки iso Asp также можно иден
нативного остатка Asp, в то время как другая
тифицировать путем включения изотопов O18 в
группа формирует искривленный остаток iso Asp
нужный пептидный остов на стадии гидролиза с
[21]. При этом образуется значительное коли
последующим его метилированием с использо
чество iso Asp и минимальное количество Asp.
ванием белка PIMT. Далее изменение массы
Эмпирическое соотношение между восстанов
белка на 2 Да может быть обнаружено с по
лением нативного остатка (т.е. Asp) и образова
мощью масс спектрометрии и использовано для
нием iso Asp составляет 1 : 3 [42] (рис. 1). Инку
количественного определения содержания ос
бация синтетических пептидов, содержащих
татков iso Asp [35].
L iso Asp, с PIMT и SAM приводила к восста
Факторы, влияющие на образование iso Asp.
Помимо спонтанного преобразования, также
наблюдалось вызванное стрессом ускорение об
разования iso Asp. Факторы, такие как темпера
тура, оксиданты и экстремальные значения рН,
которые могут привести к денатурации поли
пептида и нарушению конформации белка, де
лают измененный белок более уязвимым для
повреждений его ковалентной структуры, таким
как деамидирование и рацемизация [36-40].
Было показано, что в условиях in vivo и in vitro
накопление в белке остатков L iso Asp зависит
от рН среды [40]. При значениях рН от нейтраль
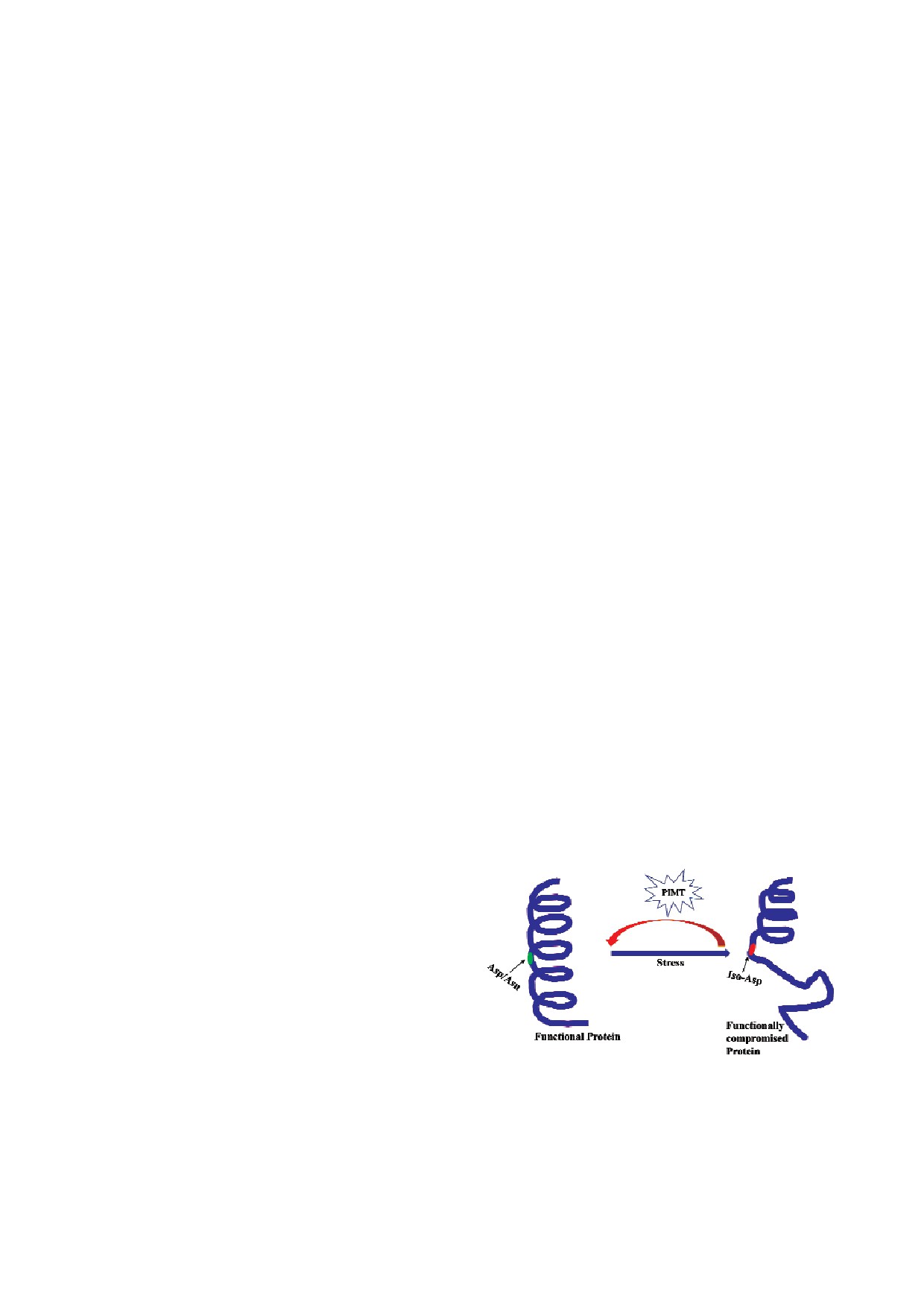
Рис. 2. Остатки iso Asp инактивируют белок. PIMT репа
ных до щелочных образование остатков iso Asp
рирует такие остатки и помогает белку восстановить свою
в белке значительно увеличивается [37]. Также
функцию.
было показано пропорциональное увеличение
С цветным вариантом рис. 2 можно ознакомиться в элект
содержания L iso Asp в зависимости от темпе
БИОХИМИЯ том 84 вып. 5 2019
606
MISHRA, MAHAWAR
новлению ~50% остатков до L Asp. Это можно
поставимой с активностью у термофильных
объяснить тем, что метилирование остатков
бактерий и являющейся более высокой, чем у
L iso Asp ускоряет образование сукцинимида
E. coli [47]. Проведенный анализ in silico позво
по сравнению с неметилированными остатками
лил получить данные касательно деталей связы
L iso Asp и L Asp [22]. Это циклическое восста
вающего окружения. Оказалось, что карбоксиль
новление и образование необычного остатка
ная группа в составе α и β изомеров D и L ас
продолжается до тех пор, пока полипептидный
парагиновой кислоты связывается с одним и
остов не вернется к своей нормальной конфор
тем же участком в PIMT. В этой же работе также
мации.
была продемонстрирована возможность распоз
Структурные и каталитические свойства
навания подходящего субстрата с помощью
PIMT. В белке PIMT можно выделить три суб
компьютерных методов [48]. Структура белка
домена [21], из которых центральный субдомен
PIMT дрозофилы отличает его от бактериаль
является консервативным и напоминает (за
ных аналогов. С Концевой домен в этом белке
исключением топологических связей) S адено
отходит на 90°. Это создает открытую форму ак
зилметионин зависимые метилтрансферазы.
тивного участка, что увеличивает доступ раство
Оптимальный контур этого белка обеспечивает
рителя внутрь активного центра [49]. У дрозо
подходящую среду для осуществления реакции
филы сайт направленный мутагенез определил
переноса метильной группы [43]. Активный
остаток Ser60 в качестве ключевого игрока при
сайт этого энзима выстлан β складчатой струк
катализе, т.к. его замена на остатки треонина
турой, богатой остатками серина и треонина.
или глутамина отменяла метилирующую актив
Эти гидрофильные аминокислоты облегчают
ность этого фермента. Также было подтвержде
образование водородной связи, которая опреде
но отсутствие остатков цистеина вблизи актив
ляет взаимодействие с остатками iso Asp, прояв
ного участка, что отличает этот фермент от дру
ляя таким образом склонность фермента в отно
гих цистеин содержащих протеаз, таких как
шении его субстрата. Процесс связывания и
каспазы, для которых показано взаимодействие
активный сайт PIMT были тщательно изучены у
с остатками аспарагиновой кислоты [21].
T. maritime. Было показано, что при этом образу
Структуры белков напрямую связаны с их
ется один сайт связывания остатка iso Asp. У че
функциями. Недавно была продемонстрирова
ловека, напротив, в структуре PIMT выявлены
на такая корреляция между последователь
четыре связывающих участка для остатков iso Asp
ностью аминокислот и функцией PIMT. Одно
[25, 44]. Было отмечено, что в структуре PIMT
нуклеотидные полиморфизмы PIMT человека,
человека три погруженных заряженных остатка
такие как L191S и A150V, приводили более чем к
отвечают за катализ и связывание с S аденозил
50% ному снижению активности нативного
метионином [45, 46].
фермента [50].
Этот фермент показывает два уникальных
Детальное исследование кинетики PIMT из
исключения из традиционных каталитических
мозга быка было проведено Johnson и Aswad [28].
процессов. Предполагается, что в отличие от
Они использовали синтетический пептид
обычных ферментов, PIMT проявляет свою ак
YAGGiso DASGN и определили для него значение
тивность без образования каких либо ковалент
Vmax как равное 32-34 нмоль/мин на 1 мг белка.
ных промежуточных структур. Хотя для прояв
В этой работе также было предположено, что
ления его активности необходим S аденозилме
метилирование белка с помощью PIMT прямо
тионин как донор метильных групп, в то же вре
пропорционально и показывает линейную зави
мя нет данных о необходимости наличия кофак
симость с таковым для субстрата, таким обра
торов, таких как ионы металлов. Атом кислоро
зом, позволяя классифицировать катализ по
да в изоаспартил α карбоксилатной группе яв
последовательному «bi bi» типу.
ляется очень сильным нуклеофилом, и он доста
SAM: донор метильной группы для реакции,
точен для катализа опосредованного трансфера
катализируемой PIMT. Полученные экспери
зой превращения [21].
ментальные данные позволили установить, что
На примере S аденозилгомоцистеина (SAH)
S аденозилметионин (SAM/AdoMet) является
было показано, что у Vibrio cholera за связывание
единственным донором группы углерода в виде
молекулы субстрата в активном центре отвечает
метильной группы во всех опосредованных
участок из 19 а.о. (39-58 а.о.). Энергия связыва
PIMT реакциях [42]. Кроме того, сродство к не
ния субстрата была первично рассчитана с ис
му остается неизменным для разных типов орга
пользованием пептидного остова PIMT. Для
низмов [51]. При этом одним из методических
синтетического пептида, содержащего iso Asp,
подходов является метод диффузии метанола,
константа ассоциации составляла 2,29 × 106 M-1.
хотя несомненным эталоном является метод пе
PIMT из V. cholerae обладает активностью, со
реноса радионуклида. В большинстве подобных
БИОХИМИЯ том 84 вып. 5 2019
PIMT ОПОСРЕДОВАННАЯ РЕПАРАЦИЯ БЕЛКОВ
607
экспериментов использовался S аденозилмети
мер, гидролиз [56]. Однако во время переноса
онин, меченный тритием. Перенос метки под
метильной группы структурные изменения не
тверждался на восстановленных остатках аспар
значительны, поэтому флуоресценцию наблю
тата. Интересно, что S аденозилгомоцистеин
дать затруднительно. В этом заключается при
(продукт S аденозилметионина, образующийся
чина ограниченного использования флуороген
при катализе PIMT) конкурентно ингибирует
ных субстратов для таких ферментов.
связывание S аденозилметионина с PIMT.
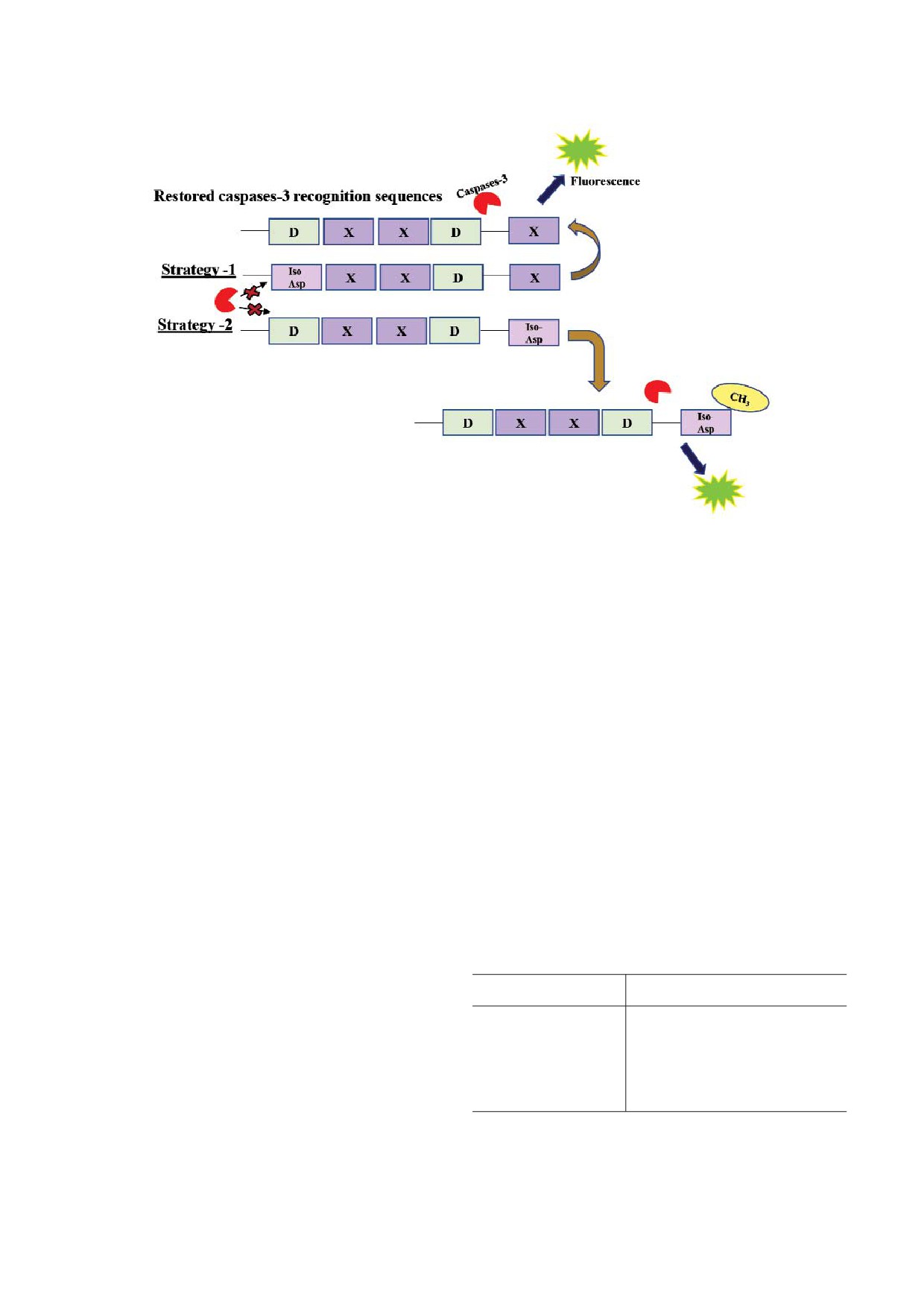
Тем не менее недавно был разработан метод
PIMT не обладает абсолютной стереоспеци
флуорогенного определения активности PIMT
фичностью. PIMT может взаимодействовать со
[57], в котором используются PIMT и каспазы 3
стереоизомерами (такими как формы L iso Asp
(протеазы, содержащие остаток аспарагиновой
и D Asp соответствующих аминокислот) и ме
кислоты). Как правило, каспазы 3 распознают
тилировать их. Но до сих пор нет сообщений о
пептидные мотивы D1XXD2 и расщепляют рас
взаимодействии с D iso Asp и L Asp. У прокари
положенную по соседству пептидную связь.
от PIMT нацелена исключительно на L iso Asp [21].
Kimura et al. получили два различных флуоро
В то же время у млекопитающих D Asp также
генных пептида, исходя из следующих положе
может быть субстратом для фермента в дополне
ний.
ние к рацемизированному аналогу. В таком слу
1) Остаток D1 в D1XXD2 был заменен на оста
чае репарация приводит к преобразованию ос
ток изоаспартата. Ожидалось, что после репара
татков D Asp в L Asp [25]. Эффективность этих
ции с помощью PIMT остаток Asp будет восста
путей зависит от сродства PIMT к D Asp [20].
новлен, и затем пептид будет расщеплен каспа
Различное сродство фермента к стереоизомерам
зой 3. В результате произойдет испускание флуо
субстрата подтверждается экспериментами, в
ресценции, которое можно измерить количест
которых белки мембраны эритроцитов больных
венно. Однако этот подход не дал ожидаемых
уремией с недостаточным уровнем метилирова
результатов.
ния имели более низкие уровни содержания ос
2) Другая стратегия была основана на пред
татков D iso Asp, что могло быть вызвано сни
положении о том, что отрицательно заряжен
женной активностью PIMT у этих пациентов [52].
ный остаток в положении P1 предотвращает рас
Четыре изоформы аспартата, а именно D Asp,
щепление каспазой 3. После метилирования за
D iso Asp, L Asp, L iso Asp, отличаются друг от
ряд нейтрализуется, происходит расщепление
друга только по ориентации их атома азота в
пептида, и наблюдается флуоресценция (рис. 3).
изопептиде. Таким образом, вполне возможно,
С помощью этого похода Kimura et al. разрабо
что PIMT предпочитает, чтобы атом N оста
тали высокоэффективный метод определения
вался позади плоскости, как в случае L iso Asp
различных ингибиторов PIMT.
и D Asp [20].
Методы измерения активности PIMT. Для из
мерения активности PIMT было предложено
РАСПРЕДЕЛЕНИЕ PIMT СРЕДИ
несколько методов, основанных на переносе
РАЗЛИЧНЫХ ВИДОВ, СОХРАНЕНИЕ ЕЕ
метки, диффузии метанола и высокоэффектив
ПЕРВИЧНОЙ И ТРЕТИЧНОЙ
ной жидкостной хроматографии (HPLC, ВЭЖХ)
СТРУКТУРЫ В ХОДЕ ЭВОЛЮЦИИ
[47, 53]. Химические методы определения менее
чувствительны, в то время как методы, основан
PIMT играет важную роль в восстановлении
ные на ВЭЖХ, требуют наличия высококлас
нативной структуры белка, катализируя превра
сных приборов, обученного персонала, сложных
щение остатка iso Asp в Asp. Согласно аннота
систем мониторинга и анализа данных [54]. Ме
ции, этот фермент обозначается как EC 2.1.1.77
тод с использованием радиоактивной метки
и в широком смысле относится к семейству
также имеет некоторые недостатки. К ним отно
трансфераз [20, 58, 59]. В связи с участием этого
сятся такие аспекты, как надлежащие экспери
белка в восстановлении структуры денатуриро
ментальные установки, утилизация отходов, на
ванных белков он также входит в семейство бел
личие обслуживающего персонала, опасность
ков шаперонов [60]. Установлено, что этот фер
для здоровья и токсичность для окружающей
мент широко распространен среди различных
среды [55]. В настоящее время большая часть
организмов, как про , так и эукариот [61, 62].
радиоактивных химических анализов заменена
В настоящее время (до декабря 2018 г.) в базе
методами анализа, в которых используются
данных UniProt насчитывалось > 15 тыс. после
флуорогенные соединения. Флуоресцентная
довательностей PIMT различных видов (таблица).
эмиссия связана с большими структурными из
Более того, принято рассматривать его как вы
менениями в молекуле химического субстрата,
сококонсервативный белок благодаря высокой
вызываемыми такими реакциями, как, напри
степени гомологии последовательности у раз
БИОХИМИЯ том 84 вып. 5 2019
608
MISHRA, MAHAWAR
Рис. 3. Флуориметрический способ измерения активности PIMT.
С цветным вариантом рис. 3 можно ознакомиться в электронной версии статьи на сайте: www.elibrary.ru
личных видов. При сравнении аминокислотных
хотя у некоторых эукариот этот фермент также
последовательностей нами было обнаружено,
связан с клеточной мембраной.
что PIMT человека на 96% идентичен PIMT мы
Согласно недавнему исследованию Juang et al.
ши. Степень идентичности составила 83,8% при
[70], всего было выявлено 15 вариантов PIMT
его сравнении с PIMT Danio rerio. Далее следуют
человека. В этой работе изучалось влияние за
PIMT дрозофилы и кишечной палочки со сте
мены одной аминокислоты среди различных ва
пенью идентичности, равной 53,8 и 30,3% соот
риантов фермента, и был сделан вывод, что му
ветственно. Кроме того, структурное сходство
тация в позиции 36 (от R до C) инактивировала
между PIMT из E. coli и PIMT человека было
фермент. Такие варианты аминокислотных за
проанализировано in silico, результаты представ
мен, как А7P и I58V, приводили к различным из
лены на рис. 4. Также есть сообщения о PIMT,
менениям ферментативной активности в срав
обнаруживаемых в клетках эубактерий и архей [52].
нении с ферментом дикого типа. Замена Gly на
Clarke и Li в 1998 г. подтвердили на различных
Arg в положении 175 вызывала агрегацию белка,
бактериальных экстрактах широкое распростра
а замена остатка Arg в положении 17 на остаток
нение этого фермента среди γ ветви грамотри
His или Ser делала этот белок термолабильным.
цательных бактерий [63].
У человека PIMT с изолейцином в положении 119
PIMT в основном кодируется одним геном,
доминирует среди азиатов/африканцев. Эта изо
но были зарегистрированы несколько исключе
форма отличается более высокой (на 20%) удель
ний, как в случае Archaeoglobus fulgidus [64] и
Arabidopsis thaliana [65], для которых сообщается
Количество различных последовательностей PIMT (ЕС 2.1.1.77),
о кодировании PIMT более чем одним геном.
представленных в базе данных UniРrot по состоянию на де
Хотя у эукариот в гене присутствуют интроны,
кабрь 2018 г.
кодирующие области отличаются относитель
Таксон
Число последовательностей
ной консервативностью. Профиль экспрессии
этого фермента у разных организмов различен.
Как у бактерий, так и у животных экспрессия
Бактерии
13 434
PIMT является конститутивной, но у растений
Археи
713
экспрессия регулируется сложным образом и
контролируется гормонами, факторами разви
Эукариоты
1125
тия и окружающей среды [66, 67]. L Изоаспар
тилметилтрансфераза существует в качестве мо
Примечание. Неклассифицированные последовательности
номера в цитозольной фракции клетки [20, 68, 69],
в подсчет не включались.
БИОХИМИЯ том 84 вып. 5 2019
PIMT ОПОСРЕДОВАННАЯ РЕПАРАЦИЯ БЕЛКОВ
609
ной активностью, чем другой вариант PIMT с
мент отсутствовал, что поставило под угрозу вы
остатком Val в том же положении. Интересно,
живаемость этой бактерии при 42 °C в организме
что вариант фермента с остатком Val показал на
домашних птиц [72]. Кроме того, в этой работе
30% большее сродство к эндогенному субстрату
также было продемонстрировано более чем
в головном мозге. Но изолейциновый вариант
трехкратное увеличение уровня экспрессии
PIMT обладает большей гибкостью и большей
PIMT у S. typhimurium. Недавно было показано,
склонностью к образованию солевого мостика
что дефицитный по PIMT S. typhimurium подвер
вблизи места связывания субстрата [59, 71].
гался воздействию окислительного стресса [73].
У E. coli PIMT играет важную роль в выживае
мости клеток в условиях долгосрочного стресса и
ФИЗИОЛОГИЯ
недостатка питательных веществ [40].
Персисторы (рersistors, персистирующие,
Роль PIMT. Все больше данных, полученных
упорствующие) представляют собой группу бак
при изучении различных видов, свидетельствуют
терий, устойчивых к антибиотикам и способ
об участии PIMT в восстановлении стационар
ных выживать в течение длительного времени.
ной фазы, при старении, окислительном стрессе
Было показано, что удаление PIMT делает бак
и выживании бактерий в условиях теплового
терии устойчивыми к офлоксацину. Двойная
стресса. В эксперименте PIMT способствовала
мутация по PIMT и глицерол 3 фосфатдегидро
повышению степени выживаемости клеток E. coli
геназе (glpD) дополнительно увеличивала вы
при старении и стрессе, вызванном действием
живаемость персистирующих клеток и их сопро
метанола и параквата [14]. Был продемонстриро
тивляемость действию антибиотика. Удаление
ван вклад этого фермента в выживаемость штам
PIMT способствовало накоплению неправиль
ма Salmonella typhimurium (S. typhimurium) с ослаб
но свернутых белков в этих клетках, но не влия
ленной вирулентностью, у которого этот фер
ло на их выживаемость в стационарной фазе
роста [74]. Модификация концевой части гисто
нов вносит вклад в эпигенетическую модифика
цию, а также в экспрессию различных генов у
эукариот. Было показано, что в клетках мозга
млекопитающих, по меньшей мере, в 12% вари
антов гистона Н2В обнаруживаются необычные
остатки D Asp. Также было показано, что в гис
тоне Н2В активного хроматина количество ос
татков D iso Asp выше, чем в молчащем хрома
тине. Таким образом, было предположено, что
PIMT играет важную роль в сохранении этих ос
татков в активно экспрессирующемся хромати
не [75].
Нарушение выживаемости клеток Arabidopsis
thaliana после удаления PIMT (как и у E. coli)
было также отмечено во время пролонгирован
ной стационарной фазы или при инкубации
этих клеток при 55 °C. Максимальная актив
ность PIMT при этой температуре была зафик
сирована в случае клеток A. thaliana [76]. Повы
шение активности ферментов наблюдалось при
42 °C в клеточной линии эпителия шейки матки
человека [77]. Тканеспецифичная экспрессия
Рис. 4. Данные, касающиеся структуры PIMT человека и
различных изоформ ферментов является эф
E. coli, были получены из базы данных PDB (ID 1KR5 для
фективным способом осуществления катализа
PIMT человека и 3LBF для PIMT E. coli). Элементы струк
целого ряда биохимических реакций в различ
туры были наложены друг на друга и проанализированы на
ных средах. Patla et al. [78] показали экспрессию
совпадение с помощью программы PDBeFold [101]. Уста
новлено, что элементы вторичной структуры (SSEs -
изоформ PIMT в зависимости от ткани и стадии
secondary structural elements) сходны на 83% при значении
развития в клетках риса (Оryza sativa). Макси
среднеквадратичного отклонения (RMSD), равном 1,374.
мальное накопление наблюдалось в созревших
PIMT человека показан зеленым цветом, а PIMT из E. coli -
зернах риса, что может быть связано с поддер
желтым и синим.
жанием структурной целостности клеточных
С цветным вариантом рис. 4 можно ознакомиться в элект
антиоксидантных ферментов в процессе старе
БИОХИМИЯ том 84 вып. 5 2019
610
MISHRA, MAHAWAR
ния. Таким образом, можно избежать накопле
внеклеточных активностей. PIMT также репа
ния активных форм кислорода (АФК), что при
рировала Ca2+ связывающий белок кальмоду
ведет к увеличению сохранности зерна.
лин и восстанавливала его функцию [87]. Кроме
У крыс была выявлена зависимость актив
того, было установлено PIMT опосредованное
ности фермента от возраста. Содержание iso Asp
ингибирование синтеза белка путем стабилиза
в кристаллике глаза 18 месячной крысы резко
ции активности антитрансляционного фактора
отличалось от его содержания в кристаллике
4E BP2 [88]. Это может указывать на косвенную
глаза крысы 2 месячного возраста. Следует от
роль PIMT в регуляции пролиферации клеток
метить, что после 18 месяцев концентрация
путем подавления действия многих генов, регу
iso Asp далее не повышалась, что свидетельствует
лируемых 4E BP2.
об активном участии PIMT в удалении этих ос
PIMT негативно регулирует уровень белка
татков из белков кристаллика [79]. У мышей де
p53, репарируя белок mdm2, который необхо
леция гена pimt приводила к накоплению в ней
дим для мечения белка p53 перед его последую
ронах измененных белков, что проявлялось в за
щей убиквитин опосредованной деградацией.
медлении роста и эпилептических припадках.
Необходимо отметить, что делеция гена pimt
Возможно, эти результаты свидетельствуют о за
приводила к усилению контроля со стороны
щитной роли PIMT при нейродегенеративных
р53 [89]. Показано, что у растений, подобных ара
заболеваниях [80, 81]. У человека было выявле
бидопсису, PIMT способствует восстановлению
но 15 изоформ PIMT. Нарушение функции и не
активности АТР зависимой DEAD бокс РНК
достаток этого белка могут проявляться различ
хеликазы (ATP dependent DEAD box RNA heli
ными способами, от нарушения когнитивной
case) [90]. В то же время имеется очень мало дан
функции до тяжелых неврологических заболе
ных о PIMT зависимых белках в клетках чело
ваний, возникающих в соответствии с мутант
века. Можно упомянуть два примера: Na+/K+
ным генотипом, кодирующим различные изо
АТРаза [91] и SOD1 [92].
формы фермента [70].
Значение PIMT в клетке: дифференцировка,
Также было показано, что в отсутствие белка
миграция и апоптоз. Дифференцировка нервных
PIMT происходит нарушение клеточного ответа
волокон вызывает целостное изменение в ней
на действие различных оксидантов (хинон, па
ронах, выражающееся в удлинении отростков,
ракват, гомоцистеин и гомоцистеин тиолактон)
экспрессии маркеров и сжатии тела клетки. Ос
не только у млекопитающих, но и у животных
новной фактор роста фибробластов (bFGF -
более низкого порядка, таких как, например,
basic fibroblast growth factor) - это нейротрофи
C. elegans [82].
ческий фактор, ответственный за дифференци
Белки, взаимодействующие с PIMT: роль
ровку нейронов, опосредованную нижележащи
PIMT опосредованной репарации в функциониро
ми каскадами передачи сигнала, такими как
вании белков. Было показано, что у E. coli PIMT
mTOR , MAPK и ERK опосредованные сиг
осуществляет репарацию белка HPr (гистидин
нальные пути. Dung et al. [93] обнаружили, что
фосфотрансфераза) после его деамидирования.
bFGF опосредованная дифференцировка кле
Белок HPr является компонентом системы фос
ток РС 12 останавливается при действии инги
фоенолпируват/гликозилфосфотрансфераза и
биторов метилирования, подобных SAH. Куль
активным участником процесса усвоения саха
тивируемые клетки, в которые была введена
ров у бактерий [39, 83]. Было показано, что
PIMT специфичная siРНК конструкция, вели
структурные и транспортные белки везикул кле
себя сходным образом, что указывает на значи
ток мозга мышей взаимодействуют с этой ме
мость метилирования, осуществляемого этим
тилтрансферазой. К ним относятся, в частности,
ферментом. PIMT участвует не только в процес
α и β тубулин, β и γ актин, α интернексин,
се дифференцировки клеток, но и в их мигра
дианамин 1, аконитаза 2, α енолаза и креатин
ции. Результаты, полученные при работе с клет
киназа В [84]. Кроме того, с PIMT также взаи
ками эндотелия сосудов человека (HUVEC), по
модействуют ассоциированный с микротрубоч
казывают роль этого фермента в миграции клет
кой мыши белок 2, калретикулин, легкие цепи
ки и формировании микрососудов. Подавление
клатрина a/b, гидролаза С концевого участка
экспрессии гена pimt с помощью siРНК и его де
убиквитина L1, фосфатидилэтаноламин связы
леция также подтверждают роль PIMT в мигра
вающий белок и статмин [26]. В последнее вре
ции клеток и тубулогенезе [94].
мя в этот перечень также включены синуклеины
Нейротрансмиттеры, такие как дофамин, в
α и β [85]. Было показано, что в мозге мыши
ходе метаболизма подвергают клетки действию
происходит PIMT опосредованная репарация
окислительного стресса. В этих условиях PIMT
гистонового белка H4 [86]. Гомеостаз кальция
ингибирует повреждения путем метилирования
важен в поддержании различных клеточных и
и репарации остатков iso Asp в различных анти
БИОХИМИЯ том 84 вып. 5 2019
PIMT ОПОСРЕДОВАННАЯ РЕПАРАЦИЯ БЕЛКОВ
611
оксидантах. Это помогает клеткам избежать
деградации упорядоченным образом внутри ау
апоптоза. Исследования клеток нейробластомы
тофагосомы [98]. Используя аутофагосомный
(SH SY5Y) показало антиапоптотическую роль
маркер, Gomez et al. заметили, что клетки
этого фермента. В этих клетках PIMT ингибиро
Caenorhabditis elegans, у которых произошла де
вала активацию каспазы 3 и каспазы 9, тем са
леция гена pimt, не подвергаются аутофагии во
мым блокируя внешние и внутренние пути
время статической стадии спящей личинки (да
апоптоза соответственно [95].
уэр) этой нематоды. Было также отмечено, что
Недавно было предположено наличие кор
вышеупомянутый мутант не смог выжить при не
реляции между уровнем экспрессии PIMT и
достатке энергии, когда был помещен в среду M9
прогнозом возникновения рака [60]. В исследо
без питательных веществ. Мутагенез гена pimt у
вании 208 образцов, собранных от пациентов с
C. еlegans с использованием траспозона Tc1 дела
аденокарциномой легких, была выявлена зна
ет эту генетически измененную нематоду неспо
чительная ассоциация между послеоперацион
собной выживать на стадии дауэра. Репродуктив
ной выживаемостью пациентов и повышенной
ная способность мутанта была на 16% меньше по
экспрессией PIMT в тканях легких. При адено
сравнению с диким типом C. elegans [99].
карциноме легких некоторые органеллы, такие
Деамидирование аспарагина и гидролиз аспа
как эндоплазматический ретикулум, испытыва
рагиновой кислоты в белках происходит спонтан
ют стресс, который можно количественно изме
но, однако различные стрессы усиливают этот
рить, контролируя уровень экспрессии регули
процесс. Белок PIMT играет важную роль в вы
руемого глюкозой белка (GRP - glucose regula
живании клеток в условиях стресса, репарируя де
ted protein), который увеличивается пропорцио
амидированные остатки и возвращая их в натив
нально уровню экспрессии PIMT. Этот фактор
ное состояние. Значение PIMT в выживаемости
также может служить дополнительным показа
клеток было показано путем получения нокаути
телем для прогноза. Повышенная экспрессия
рованных штаммов и анализа восприимчивости
PIMT связана с уменьшением выживаемости
этих штаммов к различным стрессам. В эукарио
больных после хирургического вмешательства
тических клетках были выявлены различные бел
при лечении рака. Также было выявлено повы
ки (iso Asp), взаимодействующие с PIMT, и лишь
шение уровня экспрессии PCMT1 (вариант
несколько таких белков обнаружено у бактерий.
PIMT у человека) в опухолевой ткани мочевого
Механистический анализ PIMT опосредованной
пузыря [96]. Таким образом, оценка уровня
репарации изоаспартат содержащих белков мо
экспрессии PIMT in situ может позволить опре
жет помочь в разработке новых активаторов и ин
делить необходимость послеоперационного ле
гибиторов, способных ускорить или ингибиро
чения рака химиотерапевтическими средствами.
вать этот процесс репарации. Применение таких
Белок внеклеточного матрикса фибронек
активаторов может проложить путь к профилак
тин (FN - fibronectin) способствует адгезии кле
тике хронических нейродегенеративных заболе
ток, взаимодействуя с интегриновыми рецепто
ваний, таких как болезнь Альцгеймера, а исполь
рами на поверхности клеток. Образованные раз
зование ингибиторов - предложить новые спосо
личными модулями молекулы фибронектина
бы лечения бактериальных заболеваний.
содержат линейный мотив RGD, который необ
ходим для прикрепления к интегринам, таким
Благодарности. Авторы благодарят директо
как α3β5. Кроме того, фибронектин человека
ра Индийского научно исследовательского ве
содержит последовательности NGR в своем мо
теринарного института и NFBSFARA за предос
дуле FN I5, которые также необходимы для ад
тавление необходимых финансовых средств и
гезии клеток. Деамидирование остатка Asn263
услуг для работ по изучению PIMT, выполнен
приводит к образованию iso Asp и переходу к
ных в лаборатории Mahawar.
iso DGR, который является активированной
Вклад авторов. Mishra P.K.K. - сбор данных,
формой линейного мотива NGR и ключевым
построение филогенетических деревьев, моде
фактором при связывании с α3β5. PIMT деакти
лирование белков, составление таблиц и подго
вирует этот «липкий» участок, восстанавливая
товка черновой версии статьи; Mahawar M. -
остаток аспарагина, и, таким образом, может
исправления и доработка черновой версии
служить в качестве «молекулярных часов» при
статьи.
образовании опухоли и росте клеток [97].
Конфликт интересов. Авторы заявляют об от
Нарушение системы репарации белков мо
сутствии конфликта интересов.
жет также негативно влиять на пути деградации
Соблюдение этических норм. Настоящая
белков. Аутофагия включает рециркуляцию и
статья не содержит описания выполненных ав
повторное использование состарившихся ком
торами исследований с участием людей или ис
понентов клеток путем их целенаправленной
пользованием животных в качестве объектов.
БИОХИМИЯ том 84 вып. 5 2019
612
MISHRA, MAHAWAR
СПИСОК ЛИТЕРАТУРЫ
1.
Paik, W.K., and Kim, S. (1971) Protein methylation,
22.
McFadden, P.N., and Clarke, S. (1987) Conversion of
Science, 174, 117-119.
isoaspartyl peptides to normal peptides: implications for
2.
Paik, W.K., and Kim, S. (2007) Historical review: the field
the cellular repair of damaged proteins, Proc. Natl. Acad.
of protein methylation, Trends Biochem. Sci., 32, 146-152.
Sci. USA, 84, 2595-2599.
3.
Ambler, R.P., and Rees, M.W. (1959) ε N Methyl lysine
23.
Geiger, T., and Clarke, S. (1987) Deamidation, isomeriza
in bacterial flagellar protein, Nature, 184, 56-57.
tion, and racemization at asparaginyl and aspartyl residues
4.
Murray, K. (1964) The occurrence of е N methyl lysine in
in peptides, J. Biol. Chem., 26, 2785-2794.
histones, Biochemistry, 3, 10-15.
24.
Momand, J.A., and Clarke, S. (1990) The fidelity of pro
5.
Kuehl, W.M., and Adelstein, R.S. (1970) The absence of
tein synthesis: can mischarging by aspartyl tRNA(Asp)
3 methylhistidine in red, cardiac and fetal myosins,
synthetase lead to the formation of isoaspartyl residues in
Biochem. Biophys. Res. Commun., 39, 956-964.
proteins? Biochim. Biophys. Acta, 1040, 153-158.
6.
Weihing, R.R., and Korn, E.D. (1970) ε N Dimethyl
25.
Lowenson, J.D., and Clarke, S. (1992) Recognition of
lysine in amoeba actin, Nature, 227, 1263-1264.
D aspartyl residues in polypeptides by the erythrocyte L iso
7.
Kakimoto, Y., and Akazawa, S. (1970) Isolation and iden
aspartyl/D aspartyl protein methyltransferase. Implications
tification of NG, NG and NG, N'G dimethylarginine,
for the repair hypothesis, J. Biol. Chem., 267, 5985-5995.
Nе mono , di , and trimethyllysine, and glucosylgalacto
26.
Levine, R.L., Moskovitz, J., and Stadtman, E.R. (2000)
syl and galactosyl δ hydroxylysine from human urine,
Oxidation of methionine in proteins: roles in antioxidant
J. Biol. Chem., 245, 5751-5758.
defense and cellular regulation, IUBMB Life, 50, 301-307.
8.
Johnson, P., Harris, C.I., and Perry, S.V. (1967) 3 Me
27.
Chondrogianni, N., Petropoulos, I., Grimm, S., Georgila, K.,
thylhistidine in actin and other muscle proteins, Biochem.
Catalgol, B., Friguet, B., Grune, T., and Gonos, E.S.
J., 105, 361-370.
(2014) Protein damage, repair and proteolysis, Mol. Aspects
9.
Asatoor, A.M., and Armstrong, M.D. (1967) 3 Methyl
Med., 35, 1-71.
histidine, a component of actin, Biochem. Biophys. Res.
28.
Johnson, B.A., and Aswad, D.W. (1993) Kinetic properties
Comm., 26, 168-174.
of bovine brain protein L isoaspartyl methyltransferase de
10.
Liss, M., Maxam, A.M., and Cuprak, L.J.
(1969)
termined using a synthetic isoaspartyl peptide substrate,
Methylation of protein by calf spleen methylase a new
Neurochem. Res., 18, 87-94.
protein methylation reaction, J. Biol. Chem.,
244,
29.
Yang, H., and Zubarev, R.A. (2010) Mass spectrometric
1617-1622.
analysis of asparagine deamidation and aspartate isomeri
11.
Kleinsmith, L.J., Allfrey, V.G., and Mirsky, A.E. (1966)
zation in polypeptides, Electrophoresis, 31, 1764-1772.
Phosphoprotein metabolism in isolated lymphocyte nuclei,
30.
Alfaro, J.F., Gillies, L.A., Sun, H.G., Dai, S., Zang, T.,
Proc. Natl. Acad. Sci. USA, 55, 1182-1189.
Klaene, J.J., Kim, B.J., Lowenson, J.D., Clarke, S.G.,
12.
Clarke, S. (1993) Protein methylation, Curr. Opin. Cell
Karger, B.L., and Zhou, Z.S. (2008) Chemo enzymatic
Biol., 5, 977-983.
detection of protein isoaspartate using protein isoaspartate
13.
Clarke, S.G. (2013) Protein methylation at the surface and
methyltransferase and hydrazine trapping, Anal. Chem., 80,
buried deep: thinking outside the histone box, Trends
3882-3889.
Biochem. Sci., 38, 243-252.
31.
Kameoka, D., Ueda, T., and Imoto, T. (2003) A method
14.
Visick, J.E., Cai, H., and Clarke, S. (1998) The L isoas
for the detection of asparagine deamidation and aspartate
partyl protein repair methyltransferase enhances survival of
isomerization of proteins by MALDI/TOF mass spec
aging Escherichia coli subjected to secondary environmen
trometry using endoproteinase Asp N, J. Biochem., 134,
tal stresses, J. Bacteriol., 180, 2623-2629.
129-135.
15.
Li, C., and Clarke, S. (1992) A protein methyltransferase
32.
Lehmann, W.D., Schlosser, A., Erben, G., Pipkorn, R.,
specific for altered aspartyl residues is important in
Bossemeyer, D., and Kinzel, V. (2000) Analysis of isoas
Escherichia coli stationary phase survival and heat shock
partate in peptides by electrospray tandem mass spectrome
resistance, Proc. Natl. Acad. Sci. USA, 89, 9885-9889.
try, Protein Sci., 9, 2260-2268.
16.
Visick, J.E., and Clarke, S. (1995) Repair, refold, recycle:
33.
Cournoyer, J.J., Lin, C., and O’Connor, P.B.
(2006)
how bacteria can deal with spontaneous and environmen
Detecting deamidation products in proteins by electron
tal damage to proteins, Mol. Microbiol., 16, 835-845.
capture dissociation, Anal. Chem., 78, 1264-1271.
17.
Nguyen, V.T., Morange, M., and Bensaude, O. (1989)
34.
Ni, W., Dai, S., Karger, B.L., and Zhou, Z.S. (2010)
Protein denaturation during heat shock and related stress.
Analysis of isoaspartic acid by selective proteolysis with
Escherichia coli β galactosidase and Photinus pyralis
Asp N and electron transfer dissociation mass spectrome
luciferase inactivation in mouse cells, J. Biol. Chem., 264,
try, Anal. Chem., 82, 7485-7491.
10487-10492.
35.
Liu, M., Cheetham, J., Cauchon, N., Ostovic, J., Ni, W.,
18.
Stadtman, E.R. (1992) Protein oxidation and aging,
Ren, D., and Zhou, Z.S. (2011) Protein isoaspartate me
Science, 257, 1220-1224.
thyltransferase mediated 18O labeling of isoaspartic acid for
19.
Reissner, K.J., and Aswad, D.W. (2003) Deamidation and
mass spectrometry analysis, Anal. Chem., 84, 1056-1062.
isoaspartate formation in proteins: unwanted alterations or
36.
MacLaren, D.C., and Clarke, S. (1995) Expression and
surreptitious signals? Cell. Mol. Life Sci., 60, 1281-1295.
purification of a human recombinant methyltransferase that
20.
Clarke, S. (1999) A protein carboxyl methyltransferase that
repairs damaged proteins, Protein Expr. Purif., 6, 99-108.
recognizes age damaged peptides and proteins and partici
37.
Brennan, T.V., and Clarke, S. (1993) Spontaneous degra
pates in their repair, in S Adenosylmethionine dependent
dation of polypeptides at aspartyl and asparaginyl residues:
methyltransferases: structures and functions (Xiaodong, C.,
effects of the solvent dielectric, Protein Sci., 2, 331-338.
and Blumenthal, R.M., eds), World Scientific, Singapore,
38.
Brennan, T.V., and Clarke, S. (1995) Effect of adjacent his
pp. 123-148.
tidine and cysteine residues on the spontaneous degrada
21.
Skinner, M.M., Puvathingal, J.M., Walter, R.L., and
tion of asparaginyl and aspartyl containing peptides, Int.
Friedman, A.M. (2000) Crystal structure of protein isoas
J. Pept. Protein Res., 45, 547-553.
partyl methyltransferase: a catalyst for protein repair,
39.
Sharma, S., Hammen, P.K., Anderson, J.W., Leung, A.,
Structure, 8, 1189-1201.
Georges, F., Hengstenberg, W., Klevit, R.E., and Way
БИОХИМИЯ том 84 вып. 5 2019
PIMT ОПОСРЕДОВАННАЯ РЕПАРАЦИЯ БЕЛКОВ
613
good, E.B. (1993) Deamidation of HPr, a phosphocarrier
seed vigor and longevity by reducing abnormal isoaspartyl
protein of the phosphoenolpyruvate: sugar phosphotrans
accumulation predominantly in seed nuclear proteins,
ferase system, involves asparagine
38 (HPr 1) and
Plant Physiol., 161, 1141-1157.
asparagine 12 (HPr 2) in isoaspartyl acid formation, J. Biol.
54.
Zheng, Q.X., Fu, H.Y., Li, H.D., Wang, B., Peng, C.H.,
Chem., 268, 17695-17704.
Wang, S., Cai, J.L., Liu, S.F., Zhang, X.B., and Yu, Y.J.
40.
Hicks, W.M., Kotlajich, M.V., and Visick, J.E. (2005)
(2017) Automatic time shift alignment method for chro
Recovery from long term stationary phase and stress sur
matographic data analysis, Sci. Rep., 7, 256.
vival in Escherichia coli require the L isoaspartyl protein
55.
Nascimento, E.D.S., and Tenuta Filho, A.
(2010)
carboxyl methyltransferase at alkaline pH, Microbiology,
Chemical waste risk reduction and environmental impact
151, 2151-2158.
generated by laboratory activities in research and teaching
41.
Lyon, Y.A., Sabbah, G.M., and Julian, R.R.
(2018)
institutions, Brazil. J. Pharmac. Sci., 46, 187-198.
Differences in α crystallin isomerization reveal the activity
56.
Itoh, T. (2012) Fluorescence and phosphorescence from
of protein isoaspartyl methyltransferase (PIMT) in the
higher excited states of organic molecules, Chem. Rev.,
nucleus and cortex of human lenses, Exp. Eye Res., 171,
112, 4541-4568.
131-141.
57.
Kimura, Y., Komatsu, T., Yanagi, K., Hanaoka, K., Ueno, T.,
42.
Vigneswara, V., Lowenson, J.D., Powell, C.D., Thakur, M.,
Terai, T., Kojima, H., Okabe, T., Nagano, T., and Urano, Y.
Bailey, K., Clarke, S., and Carter, W.G. (2006) Proteomic
(2017) Development of chemical tools to monitor and con
identification of novel substrates of a protein isoaspartyl
trol isoaspartyl peptide methyltransferase activity, Angew.
methyltransferase repair enzyme, J. Biol. Chem., 281,
Chem. Int. Ed. Engl., 56, 153-157.
32619-32629.
58.
Fu, J.C., Ding, L., and Clarke, S. (1991) Purification, gene
43.
Kagan, R.M., and Clarke, S. (1994) Widespread occur
cloning, and sequence analysis of an L isoaspartyl protein
rence of three sequence motifs in diverse S adenosylme
carboxyl methyltransferase from Escherichia coli, J. Biol.
thionine dependent methyltransferases suggests a common
Chem., 266, 14562-14572.
structure for these enzymes, Arch. Biochem. Biophys., 310,
59.
Kagan, R.M., McFadden, H.J., McFadden, P.N., O’Con
417-427.
nor, C., and Clarke, S. (1997) Molecular phylogenetics of
44.
Lowenson, J.D., and Clarke, S. (1991) Spontaneous degra
a protein repair methyltransferase, Compar. Biochem.
dation and enzymatic repair of aspartyl and asparaginyl
Physiol. B Biochem. Mol. Biol., 117, 379-385.
residues in aging red cell proteins analyzed by computer
60.
Saito, H., Yamashita, M., Ogasawara, M., Yamada, N.,
simulation, Gerontology, 37, 128-151.
Niisato, M., Deguchi, M.H., Tanita, T., Ishida, K., Sugai, T.,
45.
Ryttersgaard, C., Griffith, S.C., Sawaya, M.R., MacLaren, D.C.,
and Yamauchi, K. (2016) Chaperone protein L isoaspar
Clarke, S., and Yeates, T.O. (2002) Crystal structure of
tate (D aspartyl) O methyltransferase as a novel predictor
human L isoaspartyl methyltransferase, J. Biol. Chem., 277,
of poor prognosis in lung adenocarcinoma, Hum. Pathol.,
10642-10646.
50, 1-10.
46.
Dutta, T., Banerjee, S., Soren, D., Lahiri, S., Sengupta, S.,
61.
Johnson, B.A., Ngo, S.Q., and Aswad, D.W. (1991)
Rasquinha, J.A., and Ghosh, A.K. (2012) Regulation of
Widespread phylogenetic distribution of a protein methyl
enzymatic activity by deamidation and their subsequent
transferase that modifies L isoaspartyl residues, Biochem.
repair by protein L isoaspartyl methyl transferase, Appl.
Int., 24, 841-847.
Biochem Biotechnol., 168, 2358-2375.
62.
Johnson, B.A., Shirokawa, J.M., Hancock, W.S.,
47.
Chatterjee, T., Mukherjee, D., Banerjee, M., Chatterjee, B.K.,
Spellman, M.W., Basa, L.J., and Aswad, D.W. (1989)
and Chakrabarti, P. (2015) Crystal structure and activity of
Formation of isoaspartate at two distinct sites during in
protein L isoaspartyl O methyltransferase from Vibrio
vitro aging of human growth hormone, J. Biol. Chem., 264,
cholerae, and the effect of AdoHcy binding, Arch. Biochem.
14262-14271.
Biophys., 583, 140-149.
63.
Ichikawa, J.K., and Clarke, S. (1998) A highly active pro
48.
Oda, A., Noji, I., Fukuyoshi, S., and Takahashi, O. (2015)
tein repair enzyme from an extreme thermophile: the
Prediction of binding modes between protein L isoaspartyl
L isoaspartyl methyltransferase from Thermotoga maritima,
(D aspartyl) O methyltransferase and peptide substrates
Arch. Biochem. Biophys., 358, 222-231.
including isomerized aspartic acid residues using in silico
64.
Li, C., and Clarke, S. (1992) Distribution of an L isoas
analytic methods for the substrate screening, J. Pharm.
partyl protein methyltransferase in eubacteria, J. Bacteriol.,
Biomed. Anal., 116, 116-122.
174, 355-361.
49.
Bennett, E.J., Bjerregaard, J., Knapp, J.E., Chavous, D.A.,
65.
Xu, Q., Belcastro, M.P., Villa, S.T., Dinkins, R.D., Clarke, S.G.,
Friedman, A.M., Royer, W.E., and O’Connor, C.M.
and Downie, A.B. (2004) A second protein L isoaspartyl
(2003) Catalytic implications from the Drosophila protein
methyltransferase gene in Arabidopsis produces two trans
L isoaspartyl methyltransferase structure and site directed
cripts whose products are sequestered in the nucleus, Plant
mutagenesis, Biochemistry, 42, 12844-12853.
Physiol., 136, 2652-2664.
50.
Kim, J., Chen, B., Bru, J.L., Huynh, E., Momen, M., and
66.
Mudgett, M.B., and Clarke, S. (1994) Hormonal and envi
Aswad, D.W. (2018) New findings on SNP variants of
ronmental responsiveness of a developmentally regulated
human protein L isoaspartyl methyltransferase that affect
protein repair L isoaspartyl methyltransferase in wheat,
catalytic activity, thermal stability, and aggregation, PLoS
J. Biol. Chem., 269, 25605-25612.
One, 13, e0198266.
67.
Mudgett, M.B., Lowenson, J.D., and Clarke, S. (1997)
51.
Mudgett, M.B., and Clarke, S. (1993) Characterization of
Protein repair L isoaspartyl methyltransferase in plants
plant L isoaspartyl methyltransferases that may be invol ved
(phylogenetic distribution and the accumulation of sub
in seed survival: purification, cloning, and sequence analysis
strate proteins in aged barley seeds), Plant Physiol., 115,
of the wheat germ enzyme, Biochemistry, 32, 11100-11111.
1481-1489.
52.
Fujii, N., Satoh, K., Harada, K.Y., and Ishibashi, Y. (1994)
68.
Clarke, S. (1987) Propensity for spontaneous succinimide
Simultaneous stereoinversion and isomerization at specific
formation from aspartyl and asparaginyl residues in cellular
aspartic acid residues in αA crystallin from human lens,
proteins, Int. J. Pept. Protein Res., 30, 808-821.
J. Biochem., 116, 663-669.
69.
DeVry, C.G., and Clarke, S. (1999) Polymorphic forms of
53.
Verma, P., Kaur, H., Petla, B.P., Rao, V., Saxena, S.C., and
the protein L isoaspartate (D aspartate) O methyltrans
Majee, M. (2013) Protein L isoaspartyl methyltransferase
ferase involved in the repair of age damaged proteins, J. Hum.
2 gene is differentially expressed in chickpea and enhances
Genet., 44, 275-288.
БИОХИМИЯ том 84 вып. 5 2019
614
MISHRA, MAHAWAR
70.
Juang, C., Chen, B., Bru, J.L., Nguyen, K., Huynh, E.,
85. Morrison, G.J., Ganesan, R., Qin, Z., and Aswad, D.W.
Momen, M., Kim, J., and Aswad, D.W.
(2017)
(2012) Considerations in the identification of endogenous
Polymorphic variants of human protein L isoaspartyl
substrates for protein L isoaspartyl methyltransferase: the
methyltransferase affect catalytic activity, aggregation,
case of synuclein, PLoS One, 7, e43288.
and thermal stability; implications for the etiology of neu
86. Biterge, B., Richter, F., Mittler, G., and Schneider, R.
rological disorders and cognitive aging, J. Biol. Chem., 292,
(2014) Methylation of histone H4 at aspartate 24 by protein
3656-3665.
L isoaspartate O methyltransferase (PCMT1) links histone
71.
Rutherford, K., and Daggett, V. (2009) The V119I poly
modifications with protein homeostasis, Sci. Rep., 4, 66-74.
morphism in protein L isoaspartate O methyltransferase
87. Johnson, B.A., Langmack, E.L., and Aswad, D.W. (1987)
alters the substrate binding interface, Protein Eng. Des.
Partial repair of deamidation damaged calmodulin by
Sel., 22, 713-721.
protein carboxyl methyltransferase, J. Biol.Chem., 262,
72.
Pesingi, P.K., Kumawat M., Behera P., Dixit, S.K.,
12283-12287.
Agarwal, R.K., Goswami, T.K., and Mahawar, M. (2017)
88. Bidinosti, M., Martineau, Y., Frank, F., and Sonenberg, N.
Protein L isoaspartyl methyltransferase (PIMT) is
(2010) Repair of isoaspartate formation modulates the
required for survival of Salmonella typhimurium at 42 °C
interaction of deamidated 4E BP2 with mTORC1 in
and contributes to the virulence in poultry, Front. Micro
brain, J. Biol. Chem., 285, 19402-19408.
biol., 8, 361.
89. Lee, J.C., Kang, S.U., Jeon, Y., Park, J.W., You, J.S.,
73.
Kumawat, M., Pesingi, P.K., Agarwal, R.K, Goswami, T.K.,
Ha, S.W., and Han, J.W. (2012) Protein L isoaspartyl
and Mahawar, M. (2016) Contribution of protein isoaspar
methyltransferase regulates p53 activity, Nat. Commun., 3,
tate methyl transferase (PIMT) in the survival of Sal
927.
monella typhimurium under oxidative stress and viru
90. Nayak, N.R., Putnam, A.A., Addepalli, B., Lowenson, J.D.,
lence, Int. J. Med. Microbiol., 306, 222-230.
Chen, T., Jankowsky, E., and Downie, A.B. (2013) An
74.
VandenBerg, K.E., Ahn, S., and Visick, J.E.
(2016)
Arabidopsis ATP dependent, DEAD box RNA helicase
(p)ppGpp Dependent persisters increase the fitness of
loses activity upon isoAsp formation but is restored by
Escherichia coli bacteria deficient in isoaspartyl protein
protein isoaspartyl methyltransferases, Plant Cell, 25,
repair, Appl. Environ. Microbiol., 825, 5444-5454.
2573-2586.
75.
Qin, Z., Zhu, J.X., and Aswad, D.W. (2016) The D iso
91. Adav, S.S., Qian, J., Ang, Y.L., Kalaria, R.N., Lai, M.K.,
Asp 25 variant of histone H2B is highly enriched in active
Chen, C.P., and Sze, S.K. (2014) iTRAQ quantitative
chromatin: potential role in the regulation of gene expres
clinical proteomics revealed role of Na+K+ ATPase and its
sion? Amino Acids, 48, 599-603.
correlation with deamidation in vascular dementia, J. Pro
76.
Villa, S.T., Xu, Q., Downie, A.B., and Clarke, S.G. (2006)
teome Res., 11, 4635-4646.
Arabidopsis protein repair L isoaspartyl methyltransferases:
92. Bierczynska Krzysik, A., Lopaciuk, M., Pawlak Morka, R.,
predominant activities at lethal temperatures, Physiol.
and Stadnik, D. (2014) Investigation of asparagine deami
Plant., 128, 581-592.
dation in a SOD1 based biosynthetic human insulin pre
77.
Ladino, C.A., and O’Connor, C.M. (1992) Methylation of
cursor by MALDI TOF mass spectrometry, Acta Biochim.
atypical protein aspartyl residues during the stress response
Pol., 61, 349-357.
of HeLa cells, J. Cell. Physiol., 153, 297-304.
93. Dung, T.T.M., Yi, Y.S., Heo, J., Yang, W.S., Kim, J.H.,
78.
Petla, B.P., Kamble, N.U., Kumar, M., Verma, P., Ghosh, S.,
Kim, H.G., Park, J.G., Yo, B.C., Cho, J.Y., and Hong, S.
Singh, A., Rao, V., Saxena, S.C., Salvi, P., Kaur, H., and
(2016) Critical role of protein L isoaspartyl methyltrans
Majee, M. (2016) Rice protein L isoaspartyl methyltrans
ferase in basic fibroblast growth factor mediated neuronal
ferase isoforms differentially accumulate during seed matu
cell differentiation, BMB Rep., 49, 437-442.
ration to restrict deleterious isoAsp and reactive oxygen
94. Ouanouki, A., and Desrosiers, R.R. (2016) The enzyme
species accumulation and are implicated in seed vigor and
L isoaspartyl (D aspartyl) methyltransferase is required for
longevity, New Phytol., 211, 627-645.
VEGF dependent endothelial cell migration and tubulo
79.
Warmack, R.A., Mansilla, E., Goya, R.G., and Clarke, S.G.
genesis, Mol. Cell. Biochem., 413, 37-46.
(2016) Racemized and isomerized proteins in aging rat
95. Ouazia, D., Levros, L.C., Jr, Rassart, E., and Desrosiers, R.R.
teeth and eye lens, Rejuvenation Res., 19, 309-317.
(2015) The protein L isoaspartyl (D aspartyl) methyltrans
80.
Kim, E., Lowenson, J.D., MacLaren, D.C., Clarke, S.,
ferase protects against dopamine induced apoptosis in
and Young, S.G. (1997) Deficiency of a protein repair
neuroblastoma SH SY5Y cells, Neuroscience, 295, 139-150.
enzyme results in the accumulation of altered proteins,
96. Dong, L., Li, Y., Xue, D., and Liu, Y. (2018) PCMT1 is an
retardation of growth, and fatal seizures in mice, Proc.
unfavorable predictor and functions as an oncogene in
Natl. Acad. Sci. USA, 94, 6132-6137.
bladder cancer, IUBMB Life, 70, 291-299.
81.
Dimitrijevic, A., Qin, Z., and Aswad, D.W.
(2014)
97. Curnis, F., Longhi, R., Crippa, L., Cattaneo, A., Don
Isoaspartyl formation in creatine kinase B is associated
dossola, E., Bachi, A., and Corti, A. (2006) Spontaneous
with loss of enzymatic activity; implications for the linkage
formation of L isoaspartate and gain of function in
of isoaspartate accumulation and neurological dysfunction
fibronectin, J. Biol. Chem., 281, 36466-36476.
in the PIMT knockout mouse, PLoS One, 9, e100622.
98. Klionsky, D.J. (2008) Autophagy revisited: a conversation
82.
Khare, S., Gomez, T., Linster, C.L., and Clarke, S.G.
with Christian de Duve, Autophagy, 4, 740-743.
(2009) Defective responses to oxidative stress in protein
99. Gomez, T.A., Banfield, K.L., Trogler, D.M., and Clarke, S.G.
L isoaspartyl repair deficient Caenorhabditis elegans, Mech.
(2007) The L isoaspartyl O methyltransferase in Caenor
Ageing Dev., 130, 670-680.
habditis elegans larval longevity and autophagy, Dev. Biol.,
83.
Brennan, T.V., Anderson, J.W., Jia, Z., Waygood, E.B., and
303, 493-500.
Clarke, S. (1994) Repair of spontaneously deamidated HPr
100. Furuchi, T., Sakurako, K., Katane, M., Sekine, M., and
phosphocarrier protein catalyzed by the L isoaspartate
Homma, H. (2010) The role of protein L isoaspartyl/
(D aspartate) O methyltransferase, J. Biol. Chem., 269,
D aspartyl O methyltransferase (PIMT) in intracellular
24586-24595.
signal transduction, Chem. Biodivers., 71, 1337-1348.
84.
Zhu, J.X., Doyle, H.A., Mamula, M.J., and Aswad, D.W.
101. Krissinel, E., and Henrick, K. (2004) Secondary structure
(2006) Protein repair in the brain, proteomic analysis of
matching (SSM), a new tool for fast protein structure
endogenous substrates for protein L isoaspartyl methyltrans
alignment in three dimensions, Acta Crystallogr. D Biol.
ferase in mouse brain, J. Biol. Chem., 281, 33802-33813.
Crystallogr., 60, 2256-2268.
БИОХИМИЯ том 84 вып. 5 2019
PIMT ОПОСРЕДОВАННАЯ РЕПАРАЦИЯ БЕЛКОВ
615
PIMT MEDIATED PROTEIN REPAIR:
MECHANISM AND IMPLICATIONS
P. K. K. Mishra* and M. Mahawar
Division of Biochemistry, Indian Veterinary Research Institute,
Izatnagar, Bareilly, Uttar Pradesh, India, 243122;
E mail: prasantmodel@gmail.com
Received July 25, 2018
Revised December 18, 2018
Accepted December 29, 2018
Many covalent modifications of amino acids are known, but only few amino acid repair enzymes have been identi
fied. Protein L isoaspartate (D aspartate) O methyltransferase (PIMT), also known as L isoaspartyl/D aspartyl pro
tein carboxyl methyltransferase (PCMT), methylates covalently modified isoaspartate (iso Asp) residues. The iso Asp
residues accumulate in proteins due to deamidation of Asn or hydrolysis of Asp. This cytoplasmic reaction is mediated
via a succinimide intermediate and generates either iso Asp or Asp from the succinimide. Conversion of succinimide
to Asp is spontaneous, while iso Asp is restored by PIMT using S adenosylmethionine as a methyl donor. PIMT
shunts back iso Asp to succinimide form and thus creates a chance to get converted into Asp residue. Apart from nor
mal cell physiology, various stress conditions enhance formation of iso Asp in proteins. Iso Asp can form a kink or
bend in a protein backbone thus making the protein conformationally and functionally distorted. Many PIMT inter
acting proteins (proteins that have iso Asp residues) have been reported in eukaryotes and few in prokaryotes. Further,
extensive research in mice has shown the importance of this protein in neurodegenerative conditions. Detailed eluci
dation of PIMT function can pave the platform for addressing diseases like Alzheimer’s and cancer.
Keywords: protein L isoaspartate (D aspartate) O methyltransferase, isoaspartate, S adenosylmethionine, succini
mide
БИОХИМИЯ том 84 вып. 5 2019