БИОХИМИЯ, 2019, том 84, вып. 5, с. 616 - 633
УДК 577.112, 577.181
ПЕДИОЦИН ПОДОБНЫЕ АНТИМИКРОБНЫЕ
ПЕПТИДЫ БАКТЕРИЙ
Обзор
© 2019
С.В. Баландин, Э.В. Шереметьева, Т.В. Овчинникова*
Институт биоорганической химии им. академиков М.М. Шемякина
и Ю.А. Овчинникова РАН, 117997 Москва, Россия;
электронная почта: ovch@ibch.ru
Поступила в редакцию 06.08.2018
После доработки 11.10.2018
Принята к публикации 11.10.2018
Бактериоцины - антимикробные пептиды бактерий, являющиеся, в отличие от классических пептидных
антибиотиков, продуктами рибосомального синтеза и, как правило, обладающие узким спектром антибак
териальной активности в отношении родственных продуцентам видов. Педиоцин подобные бактериоцины
(PLB) относят к подклассу IIa бактериоцинов грамположительных бактерий. PLB проявляют высокую ак
тивность в отношении патогенных бактерий родов Listeria и Enterococcus. Молекулярной мишенью для PLB
служит мембранный маннозо фосфотрансферазный комплекс (Man PTS). PLB могут синтезироваться
симбиотической микробиотой человека и участвовать в поддержании гомеостаза в пищеварительном трак
те и на поверхности эпителия, контактирующего с внешней средой. На основе PLB может быть создана но
вая группа антибиотиков узкого спектра действия.
КЛЮЧЕВЫЕ СЛОВА: антимикробные пептиды, бактериоцины, педиоцин подобные пептиды, антибиоти
корезистентность, маннозо фосфотрансфераза.
DOI: 10.1134/S0320972519050026
Бактериоцины - рибосомально синтезируе
ний в области медицинского применения бакте
мые антимикробные пептиды бактериального
риоцинов, является глобальное распростране
происхождения [1]. Активность этих соедине
ние патогенных штаммов, резистентных к лекар
ний наиболее выражена в отношении видов
ственным средствам, используемым в клини
бактерий, родственных продуцентам, хотя изве
ческой практике в настоящее время. В отличие
стно небольшое число бактериоцинов с широ
от пептидных антибиотиков, биосинтез которых
ким спектром действия [2, 3]. Интерес к бакте
осуществляется нерибосомальным путем (поли
риоцинам связан с потенциальной возмож
миксинов, грамицидинов), ни один из бактерио
ностью их применения в медицине, животно
цинов пока не нашел применения в качестве ле
водстве и пищевой промышленности в качестве
карственного средства. Высокая селективность
новых антибиотиков и консервантов [1, 4-6].
действия отличает большинство бактериоцинов
Примером использования бактериоцинов для
от классических антибиотиков и антимикроб
консервации пищевых продуктов служит полу
ных пептидов животного происхождения [9].
вековая история применения лантибиотика ни
Исследование механизмов такой селективности
зина, до настоящего времени не утратившего
открывает путь к разработке лекарственных
своей эффективности [7, 8]. Важнейшим факто
средств, избирательно действующих на патоген
ром, определяющим актуальность исследова
ные микроорганизмы и не подавляющих жизне
деятельность нормальной микробиоты, колони
Принятые сокращения: PLB - педиоцин подобные
зирующей организм человека [10, 11]. Еще од
бактериоцины; а.о. - аминокислотные остатки; МИК - ми
ним преимуществом подобной селективности
нимальная ингибирующая концентрация; Man PTS - ман
является снижение риска развития кросс резис
нозо фосфотрансферазный комплекс; PTS - фосфоенол
тентности к антимикробным агентам других
пируват:углевод фосфотрансферазная система; EI - фер
классов. Использование лекарственных средств
мент I PTS; HPr - гистидин содержащий переносчик фос
фата PTS; EII - фермент II PTS; EIIA, EIIB, EIIC, EIID -
узкого спектра действия, наряду с организацией
субъединицы фермента II PTS.
системы строгого контроля применения анти
* Адресат для корреспонденции.
биотиков, позволит хотя бы частично решить
616
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
617
проблему распространения полирезистентных
вырабатываются молочнокислыми бактериями ро
штаммов.
дов Lactobacillus, Pediococcus, Leuconostoc, Strep(
В настоящее время классификация бактерио
tococcus, Carnobacterium, Enterococcus, Weissella [20].
цинов по источнику получения (природному
Кроме того, бактериоцины IIa подкласса были
продуценту) вытеснена структурной классифи
найдены у таких бактерий, как Bifidobacterium bi(
кацией [1]. Пептиды, независимо от происхожде
fidum [21], Bifidobacterium infantis [22], Bacillus co(
ния, подразделяют на два класса: I) бактериоци
agulans [23], Listeria innocua [24]. Продуценты
ны, содержащие посттрансляционные модифи
PLB встречаются в пищевых продуктах, в желу
кации (лантибиотики, лассо пептиды, сактибио
дочно кишечном тракте человека и животных,
тики, тиопептиды и др.) и II) немодифицирован
на поверхности растений. Большое число генов,
ные бактериоцины и бактериоцины с минималь
кодирующих PLB, идентифицировано в нуклео
ными посттрансляционными модификациями,
тидных последовательностях при секвенирова
к числу которых можно отнести циклизацию за
нии геномов микроорганизмов, составляющих
счет пептидной связи, образование дисульфид
микробиом человека [25].
ных связей, формилирование N концевого мети
PLB привлекают внимание благодаря своей
онина. Некоторые авторы относят к бактериоци
высокой активности, проявляемой в наномо
нам более крупные термолабильные молекулы,
лярном диапазоне концентраций, а также низ
выделяя их в дополнительные классы: III) белки
кой токсичности для человека [26]. Пептиды
с молекулярной массой >30 кДа и IV) белки, ко
этого класса известны в первую очередь своей
валентно связанные с небелковым (липидным,
способностью подавлять рост бактерий рода
углеводным) компонентом [12, 13]. Бактериоцины
Listeria, в т.ч. патогенных штаммов, вызываю
класса II включают следующие подклассы: IIa -
щих тяжелые пищевые и оппортунистические
педиоцин подобные линейные пептиды, IIb -
инфекции [27]. Несмотря на то что резистент
двухкомпонентные системы, IIc - циклические
ность листерий к классическим антибиотикам
бактериоцины, IId - бактериоцины с линейной
не получила еще широкого распространения,
структурой, не включенные в другие подклассы,
тенденция к этому прослеживается [28, 29], что
IIe - микроцин E492 подобные пептиды [1].
повышает интерес к поиску резервных антилис
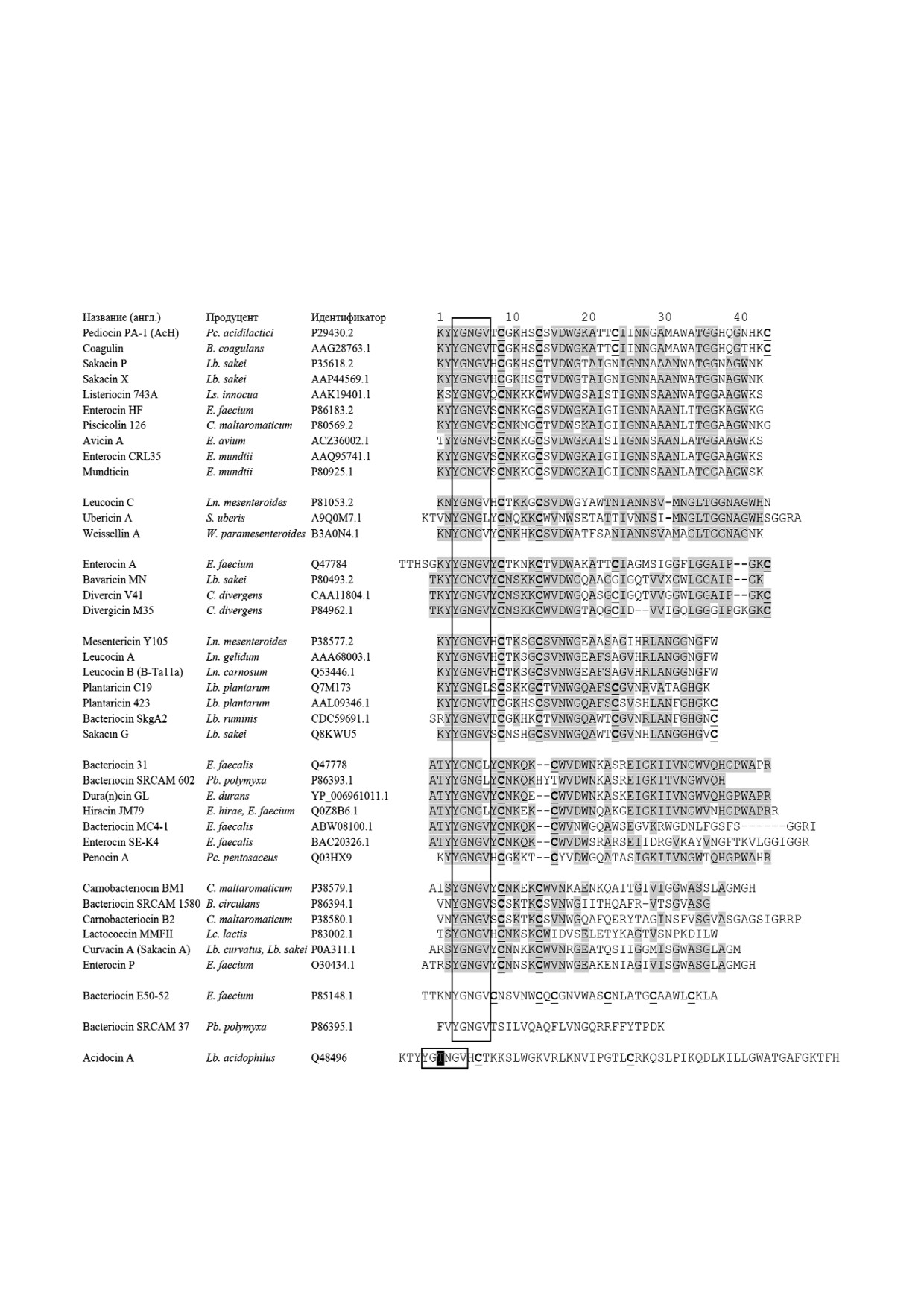
Отличительным признаком педиоцин по
териозных средств. Потенциальными мишеня
добных бактериоцинов (PLB, pediocin like bacte(
ми для PLB могут быть и другие пищевые грам
riocins) является наличие последовательности
положительные патогены [30]. Среди грамполо
YGNG(V/L), называемой «педиоциновым бок
жительных бактерий, чувствительных к PLB,
сом» («pediocin box») и, как правило, входящей в
наибольшую опасность представляют ванкоми
состав более крупного мотива, стабилизирован
цин резистентные энтерококки (VRE) - возбу
ного дисульфидной связью и расположенного в
дители тяжелых нозокомиальных инфекций [31,
N концевой части молекулы: YGNG(V/L)XCX
32]. У нескольких представителей подкласса вы
(K/N)XXC, где X - любые полярные (заряжен
явлена активность в отношении бактерий рода
ные или незаряженные) аминокислотные остат
Campylobacter - грамотрицательных возбудите
ки (а.о.) [14, 15] (рис. 1).
лей заболеваний домашней птицы, способных
Первый охарактеризованный бактериоцин
вызывать острые кишечные инфекции с синд
подкласса IIa, давший название всей группе пеп
ромом общей интоксикации у человека (кампи
тидов, педиоцин AcH - был выделен из штамма
лобактериозы) [5], однако в настоящее время
Pediococcus acidilactici H в 1988 г. [16]. Однако
достоверность первоначальных сведений об ак
первым представителем подкласса, первичная
тивности этих соединений поставлена под сом
структура которого была определена, стал лей
нение [33, 34]. Кроме того, у некоторых PLB об
коцин A [17]. Аминокислотная последователь
наружена противовирусная активность [35, 36].
ность педиоцина AcH была опубликована лишь
Согласно классификации Управления по са
в 1992 г. [18] вслед за публикацией первичной
нитарному надзору за качеством пищевых про
структуры педиоцина PA 1, выделенного из штам
дуктов и медикаментов США (FDA), молочно
ма Pediococcus acidilactici PAC 1.0 [19] (рис. 1, a).
кислые бактерии имеют статус «общепризнанно
Сравнение структур показало, что педиоцины
безопасных» (generally recognized as safe, GRAS),
AcH и PA 1 идентичны друг другу. Педиоцин
что делает вырабатываемые ими пептиды прив
PA 1/AcH - единственный известный предста
лекательными объектами биотехнологического
витель подкласса, синтезируемый разными ви
производства. К достоинствам PLB, наряду с
дами бактерий (причем двух разных родов -
высокой биологической активностью и термоста
Pediococcus и Lactobacillus) [20].
бильностью, можно отнести и то, что их био
В настоящее время идентифицировано >50 бак
синтез не требует участия ферментов, осущест
териоцинов IIa подкласса. Большинство из них
вляющих посттрансляционные модификации.
2 БИОХИМИЯ том 84 вып. 5 2019
618
БАЛАНДИН и др.
Это делает возможным получение рекомби
КЛАССИФИКАЦИЯ PLB
нантных аналогов данных пептидов в наиболее
экономичных прокариотических системах, на
В основе современной классификации PLB
пример, в E. coli [37]. Альтернативой очищен
лежит гомология их первичной структуры [20,
ным препаратам в некоторых случаях могут
41, 42]. С увеличением числа известных предс
стать микроорганизмы пробиотики в качестве
тавителей подкласса постепенно меняется вид
формы доставки этих веществ в организм чело
филогенетического древа, построенного на ос
века и сельскохозяйственных животных [27, 31,
нове установленных структур. Наиболее широ
38-40].
кой известностью пользуется классификация
Рис. 1. Первичная структура представителей бактериоцинов IIa подкласса. Рамкой выделен педиоциновый бокс, отмечен
дополнительный остаток треонина в педиоциновом боксе ацидоцина A, подчеркнуты остатки цистеина. Использованы
сокращенные названия родов бактерий: B. - Bacillus, C. - Carnobacterium, E. - Enterococcus, Lb. - Lactobacillus, Lc. - Lacto(
coccus, Ln. - Leuconostoc, Ls. - Listeria, Pb. - Paenibacillus, Pc. - Pediococcus, S. - Streptococcus, W. - Weissella
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
619
Nissen Meyer et al., разделивших 28 известных
лейкоцина A и сакацина P характеризуется уме
на момент публикации бактериоцинов подклас
ренно выраженной амфифильностью [44, 46].
са IIa на четыре подгруппы [41]. В более поздней
Соответствующая область курвацина A имеет
работе Cui Y. et al. состав этих подгрупп был до
несколько менее «правильную» β складчатую
полнен новыми пептидами, а пять пептидов с
укладку, чем у лейкоцина А и сакацина P [47].
принципиально новой структурой были выделе
Исключение составляет карнобактериоцин B2,
ны в дополнительные четыре подгруппы [20].
N концевая часть которого не упорядочена [45].
При этом подгруппам II, III и IV в данной рабо
Вариабельная гидрофобная C концевая часть
те соответствуют подгруппы 4, 2 и 3 по класси
молекулы состоит из упорядоченного участка,
фикации Nissen Meyer et al., а общее число опи
включающего одну или две (у курвацина A) ам
санных структур возросло до 50.
фифильные α спирали, и неупорядоченного
Некоторые бактериальные антимикробные
участка. Между двумя этими участками наблю
пептиды, обладающие очевидным эволюцион
дается резкий изгиб цепи, делающий всю C кон
ным родством с PLB, не были включены в дан
цевую часть молекулы похожей на шпильку. У пе
ный подкласс ввиду отсутствия в их структуре
диоцина PA 1/AcH и некоторых других бакте
педиоцинового бокса. К ним относятся, в част
риоцинов подкласса IIa (коагулина, сакацина G,
ности, энтероцин B и карнобактериоцин A, вы
плантарицина 423, диверцина V41, дивергицина
рабатываемые теми же штаммами, из которых
M35, энтероцина A) имеется вторая дисульфидная
были выделены энтероцин A и карнобактерио
связь, соединяющая середину α спиральной об
цин B2. Эволюционное родство между данными
ласти с неупорядоченным C концевым участ
парами пептидов подтверждается гомологией
ком [41]. Большое количество гидрофобных остат
лидерной последовательности и C концевой
ков и амфифильная структура C концевой части
части полипептидной цепи [43].
PLB, хорошо заметная на проекции Шиффера-
Эдмундсона, указывают на то, что именно эта
часть пептида погружается в липидный бислой
СТРУКТУРА PLB
мембраны [13]. В структуре курвацина A присут
ствуют два спиральных участка - небольшой гид
Первичная структура известных PLB вклю
рофильный, находящийся в середине молекулы,
чает от 25 (мутацин F 59.1) до 58 (ацидоцин А) а.о.
и более протяженный амфифильный C концевой.
Бактериоцины этого класса не содержат пост
Между N концевой и C концевой частями
трансляционных модификаций, за исключени
молекулы расположен шарнирный участок,
ем дисульфидных связей. К настоящему време
обеспечивающий их взаимную подвижность и
ни определена пространственная структура пя
относительную функциональную независи
ти природных PLB: лейкоцина A [44], карнобак
мость. В структуре курвацина A имеется допол
териоцина B2 [45], сакацина P [46], курваци
нительный шарнир между двумя α спиральны
на A [47] и энтероцина HF [48] (рис. 2, б-е).
ми фрагментами [47]. Таким образом, рассмот
Кроме того, была исследована третичная струк
ренные здесь пространственные структуры де
тура искусственных аналогов сакацина P [46],
монстрируют высокую степень сходства, и толь
лейкоцина A [49] и педиоцина PA 1 [50] (рис. 2, а).
ко у карнобактериоцина B2 и курвацина A име
Исследования проводили методом ЯМР спект
ются заметные отличия от остальных установ
роскопии в средах, имитирующих мембранное
ленных структур в N концевой и C концевой
окружение: в растворе трифторэтанола (TFE) и
области соответственно.
мицеллах додецилфосфохолина (DPC).
Как и многие другие антимикробные пепти
ды, PLB в водном растворе не имеют упорядо
ВЗАИМОСВЯЗЬ СТРУКТУРЫ
ченной пространственной структуры, однако в
И ФУНКЦИЙ PLB
гидрофобном окружении или на границе разде
ла двух фаз приобретают стабильную, отчетливо
За три десятилетия, прошедших со времени
выраженную конформацию. Несмотря на раз
открытия педиоцина PA 1/AcH, проведена
личия в деталях, можно выделить ряд призна
большая работа, посвященная выявлению клю
ков, общих для всех исследованных структур.
чевых а.о., детерминирующих антимикробную
Катионный гидрофильный N концевой участок
активность и специфичность действия PLB. В боль
образует тройной антипараллельный β складча
шинстве подобных экспериментов объектами
тый лист, стабилизированный одной дисуль
становились педиоцин PA 1/AcH, лейкоцин A,
фидной и несколькими водородными связями.
сакацин P, карнобактериоцин B2.
Консервативный педиоциновый бокс соответ
Предметом исследования являлись не толь
ствует первому β изгибу. β Складчатый участок
ко антимикробные свойства PLB, но и взаимо
БИОХИМИЯ том 84 вып. 5 2019
2*
620
БАЛАНДИН и др.
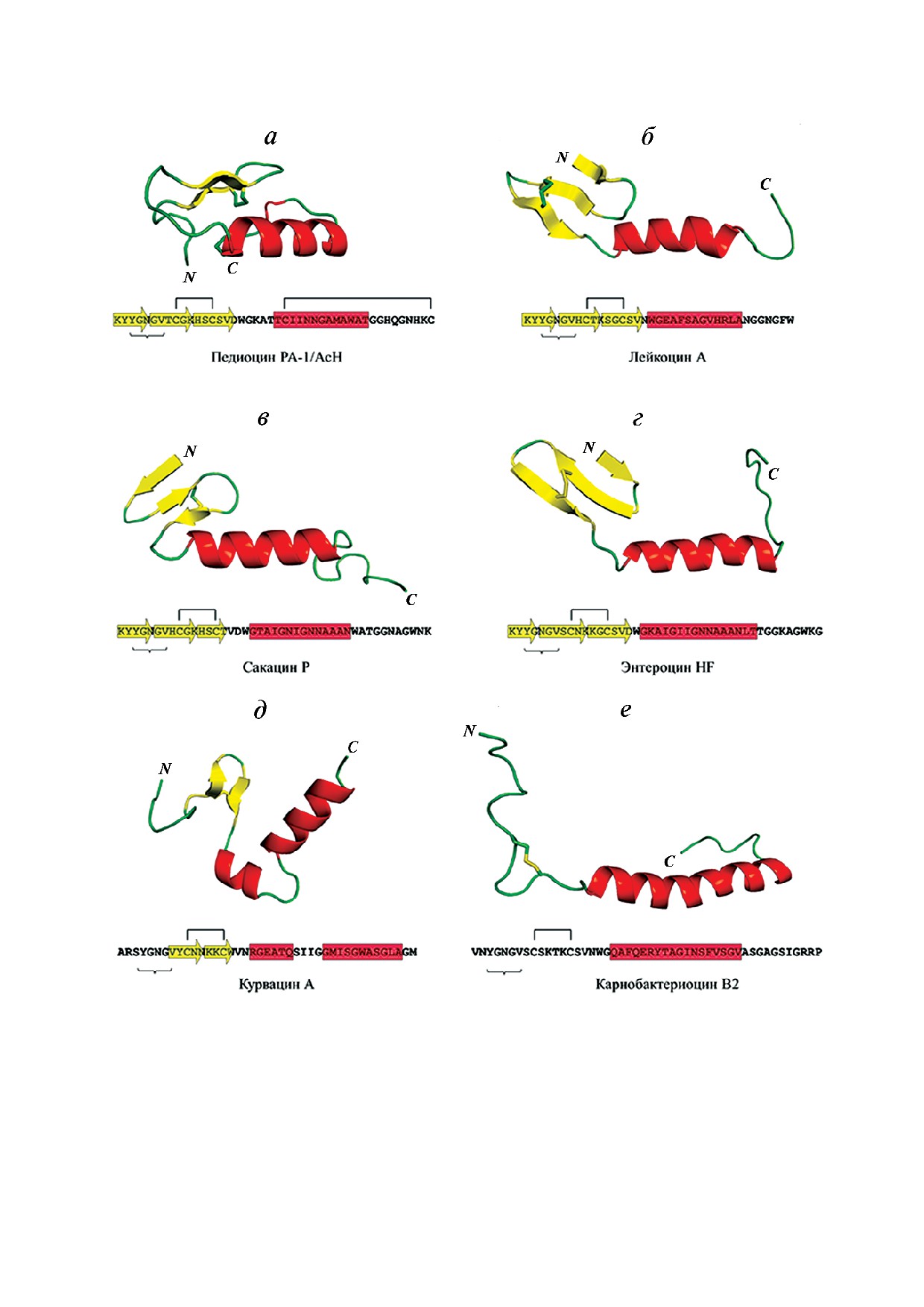
Рис. 2. Пространственная структура представителей подкласса IIa бактериоцинов грамположительных бактерий. Приве
дены: а - первичная структура педиоцина PA 1/AcH из бактерий Pediococcus и Lactobacillus (UniProt P29430.2) и простран
ственная структура его искусственного аналога с заменой M31L (PDB 5UKZ); б - структуры лейкоцина A из Leuconostoc
gelidum (P34034.1, 1CW6), в - сакацина P из Lactobacillus sakei (P35618.2, 1OG7), г - энтероцина HF из Enterococcus faecium
(P86183.2, 2N4K), д - курвацина A из Lactobacillus curvatus (P0A311.1, 2A2B), е - карнобактериоцина B2 из Carnobacterium
maltaromaticum (P38580.1, 1CW5). Стрелками обозначены участки структуры, обладающие β складчатой конформацией,
прямоугольниками - спиральные фрагменты; показана аранжировка дисульфидных связей; фигурными скобками отме
чено расположение педиоцинового бокса.
С цветным вариантом рис. 2 можно ознакомиться в электронной версии статьи на сайте: www.elibrary.ru
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
621
действие этих пептидов со следующими струк
сульфидной связью. Исключением служат бак
турами и системами: липидным бислоем [51, 52],
териоцины OR 7 (несет один Cys), L 1077 и 37
белками иммунитета [53], собственным C кон
(не содержат Cys), существенно отличающиеся
цевым фрагментом и фрагментами других PLB
от большинства других PLB своей аминокислот
[54-56], системой посттрансляционного про
ной последовательностью [20]. Восстановление
цессинга и секреции [57]. Полученные данные
дисульфидных связей в той или иной мере сни
позволяют сформулировать закономерности,
жает антибактериальную активность PLB. Из
общие для всех или большинства известных
вестно, что представители группы педиоцина
PLB.
PA 1 утрачивают ее почти полностью, в то время
1) N Концевой педиоциновый бокс YGNG(V/L)
как пептиды, родственные мезэнтерицину Y105,
чрезвычайно важен для проявления антимик
в значительной степени сохраняют свои анти
робной активности. Аминокислотные замены в
биотические свойства [65]. В последнем случае
этой области пептида в большинстве случаев
наличие активности может объясняться спон
полностью лишают его антимикробных свойств
танным рефолдингом добавляемых к тест куль
[58, 59], хотя некоторые типы замен все же до
туре пептидов. Химическая модификация остат
пустимы [51, 60]. Известно лишь два природных
ков Cys или замена их на остатки Ser у лейкоци
пептида, в структуре которых наблюдается от
на А [66] и мезэнтерицина Y105 [67] делает эти
клонение от указанной выше формулы педиоци
пептиды неактивными. Было показано, что для
нового бокса - ацидоцин A [61] и бактериоцин
сохранения N концевой пространственной струк
OR 7 [62]. Интересно отметить, что в обоих
туры лейкоцина А достаточно силы нековалент
случаях речь идет не об аминокислотной замене,
ных гидрофобных или π стэкинг взаимодей
а о более значительном нарушении консерва
ствий между алифатическими или ароматичес
тивной структуры - встраивании остатка трео
кими остатками аллилглицина, норвалина, фе
нина между первым остатком глицина и аспара
нилаланина, замещающими в полипептидной
гином (YGTNGV). Данные пептиды заметно от
цепи остатки Cys. Полученные аналоги лишь
личаются по своей первичной структуре от
немногим менее активны, чем природный пеп
большинства PLB, что стало основанием для
тид, и при этом устойчивы к действию восстано
вынесения их в отдельную группу [20].
вителей [66, 68]. Однако попытка повторить
2) N Концевая часть бактериоцина несет по
данные результаты в экспериментах с педиоци
ложительный заряд, обеспечивающий электро
ном PA 1 не увенчались успехом - лишенный
статическое притяжение на первоначальном
ковалентно замкнутого N концевого цикла пеп
этапе взаимодействия с мембраной бактерий и
тид полностью утрачивал активность [68]. Та
липидным бислоем липосом [63]. Тем не менее
ким образом, на актибактериальные свойства
между величиной заряда и антибактериальной
PLB влияет не только наличие цикла в N конце
активностью не выявлено прямой зависимости
вой части молекулы, но и детали его химическо
[59, 64]. Так, например, замена H12K в структу
го строения. Так, карбоциклический аналог лей
ре сакацина P не оказывает заметного влияния
коцина А, содержащий вместо дисульфидной свя
на его антимикробные свойства, замена T20K
зи более прочную ковалентную связь между ато
повышает активность, а добавление дополни
мами углерода, отличается от исходного пептида
тельного N концевого остатка лизина или заме
в ~10 раз более высоким значением минималь
на D17N приводят к значительному снижению
ной ингибирующей концентрации (МИК) [66].
активности [64]. Кроме того, консервативная
4) C Kонцевая часть бактериоцинов под
мутация D17E, увеличивающая расстояние
класса IIa характеризуется высокой эволюцион
между карбоксильной группой боковой цепи и
ной изменчивостью, однако ее присутствие в
пептидным остовом за счет наличия дополни
составе молекулы является обязательным усло
тельной метиленовой группы в боковой цепи,
вием сохранения биологической активности.
оказывает более выраженное негативное влия
Как показали эксперименты с укороченными
ние на уровень активности, чем замена D17N,
аналогами мезэнтерицина Y105, синтетический
подтверждая предположение, что заряженные
C концевой фрагмент длиной 23 а.о., включаю
остатки не просто вносят вклад в суммарный за
щий в себя всю амфифильную α спиральную
ряд молекулы, но могут участвовать в компле
область данного пептида, не обладает собствен
ментарных взаимодействиях с рецептором. По
ной антимикробной активностью [67]. Более то
казано также, что при изменении заряда моле
го, удаление даже одного C концевого остатка
кулы активность в отношении различных штам
(Trp) приводит к росту значений МИК на четы
мов может изменяться в разной степени.
ре порядка. Это резко контрастирует со свой
3) Структура N концевой части молекулы
ствами α спиральных антимикробных пептидов
почти всех известных PLB стабилизирована ди
животных, аминокислотные последовательнос
БИОХИМИЯ том 84 вып. 5 2019
622
БАЛАНДИН и др.
ти которых могут быть укорочены до фрагмен
дом молекулярной динамики показало, что вто
тов длиной 15-20 а.о. без существенной потери
рая дисульфидная связь стабилизирует α спи
активности в отношении бактерий [69-73].
ральную конформацию и амфифильность данно
Важной функциональной особенностью C кон
го участка цепи при повышенной температуре [78].
цевой части PLB является то, что именно она
В аминокислотной последовательности природ
определяет спектр действия пептида [13], что
ных PLB вместо С концевой пары цистеинов мо
было продемонстрировано в экспериментах по
гут находиться остатки триптофана, которые
созданию гибридных молекул путем комбини
участвуют в π стэкинг взаимодействиях друг с
рования N концевых и C концевых частей раз
другом и тем самым стабилизируют «шпильку» в
ных бактериоцинов подкласса IIa [74].
этой области молекулы [79].
Исследование укороченных аналогов педио
цина PA 1 показало, что ни один из 30 химичес
ки синтезированных фрагментов, включающих
МЕХАНИЗМ ДЕЙСТВИЯ PLB
все возможные 15 членные последовательнос
ти, содержащиеся в структуре данного пептида
Первые работы по исследованию действия
(от 1-15 до 30-44), не обладает антимикробной
бактериоцинов класса IIa на бактериальные
активностью в отношении индикаторного штам
клетки явно указывали на то, что эти вещества
ма Lactobacillus sake NCDO 2714 в концентрации
относятся к числу мембранотропных агентов,
до 100 мкМ включительно [54]. Некоторые из
вызывающих образование пор, диссипацию
протестированных фрагментов, а именно те из
трансмембранного потенциала и истощение за
них, которые соответствуют средней и C конце
пасов ATP, потерю неорганических ионов, ами
вой части пептида, в концентрации 5 мкМ инги
нокислот и других низкомолекулярных соеди
бируют действие полноразмерного педиоцина
нений [80-82]. Как и в случае с другими анти
PA 1 и, в меньшей степени, других PLB - энте
микробными пептидами
[83], диссипация
роцина A, курвацина А, сакацина P, лейкоцина А.
трансмембранной разности потенциалов может
Значение МИК возрастает в 2-20 раз, причем,
происходить в присутствии сублетальных кон
наиболее выраженным эффектом обладает
центраций бактериоцина [84]. Большинство
фрагмент 20-34. Конкурентное ингибирование
предпринимавшихся в разное время попыток
действия бактериоцина его С концевым фраг
объяснить антимикробное действие PLB укла
ментом указывает на то, что соответствующая
дываются в рамки одной из трех моделей: 1) фор
область полноразмерного пептида принимает
мирование трансмембранных пор в результате
участие во взаимодействии с рецептором. С эти
низкоспецифичного связывания с липидным
ми результатами согласуются данные о том, что
бислоем; 2) формирование или активация бел
N концевой 15 членный фрагмент энтероцина
ковых трансмембранных каналов за счет высо
CRL35 (концентрация в работе не указана) уси
коспецифичного лиганд рецепторного взаимо
ливает действие полноразмерного пептида, взя
действия; 3) формирование трансмембранных
того в концентрации 500 нМ, на Listeria innocua 7,
пор после связывания с белковым рецептором
тогда как фрагменты из средней и C концевой
(гибридная модель) [4, 13].
областей аналогичной длины ингибируют его [75].
Первоначально считалось, что связывание
Авторы подчеркивают, что эффект от добавле
несущих положительный заряд бактериоцинов
ния укороченных фрагментов проявляется в
IIa класса с мембраной осуществляется исклю
уменьшении значения КОЕ после инкубации с
чительно за счет электростатического притяже
пептидом и изменении трансмембранной раз
ния и не требует наличия специфического ре
ности потенциалов, при этом значения МИК
цептора [63, 80, 85, 86]. Было показано, что по
остаются на исходном уровне. Как и в случае с
вышение содержания анионных фосфолипидов
педиоцином PA 1, ни один из протестирован
в составе мембраны увеличивает аффинность к
ных фрагментов не обладает собственной актив
ней бактериоцина [86]. Согласно данной модели,
ностью в концентрации до 100 мкМ.
PLB способны самостоятельно формировать по
5) Вторая дисульфидная связь, встречающая
ры в мембране. Между консервативным гидро
ся в C концевой части некоторых PLB, не являет
фильным N концевым и вариабельным C кон
ся необходимым элементом структуры, но нали
цевым участками находится «шарнир», обеспе
чие такой связи расширяет спектр их активности
чивающий возможность изменения угла между
[76], а также поднимает верхнюю границу темпе
этими двумя частями молекулы [53]. После свя
ратурного диапазона, в котором активность со
зывания N концевого участка с поверхностью
храняется [77]. Исследование PLB с одной и двумя
мембраны C концевая часть пептида погружает
дисульфидными связями с помощью КД спект
ся в гидрофобную область липидного бислоя.
роскопии и моделирование их структуры мето
Избирательность антимикробного действия оп
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
623
ределяется не наличием специфических моле
раны со стороны периплазмы. Известно, что
кулярных структур (паттернов) на поверхности
клетки E. coli обладают устойчивостью к боль
мембраны клетки мишени, а составом ее ли
шинству бактериоцинов грамположительных
пидного бислоя, влияющим на эффективность
бактерий вследствие малой проницаемости
последующего внедрения C концевого участка
внешней мембраны [93, 94] и того факта, что
молекулы PLB [46, 47]. Популяризации выше
комплексы Man PTS данной бактерии принад
описанной модели способствовала публикация
лежат к группам II и III, структурно отличаю
результатов первых экспериментов c педиоци
щимся от Man PTS группы I, имеющихся у лис
ном PA 1 и везикулами, построенными из липи
терий [95]. Тем не менее индукция синтеза опи
дов L. monocytogenes, свидетельствовавших о
санной выше конструкции приводила к гибели
том, что белковый компонент мембраны не иг
клетки продуцента. По всей вероятности, им
рает сколько нибудь существенной роли в обра
мобилизация пептида на поверхности мембра
зовании поры [80].
ны путем гибридизации с периплазматическим
Позже появились данные об отсутствии ак
доменом резко повышает его локальную кон
тивности у all D энантиомера лейкоцина А, ко
центрацию и вероятность встраивания C конце
торые указывали на стереоспецифичную приро
вой части в липидный бислой [92]. Данная мо
ду его взаимодействия с клеткой мишенью [55].
дель дает ответ на вопрос, почему бактерии, ли
Появились свидетельства того, что высокая
шенные Man PTS группы I, а также липосомы
чувствительность бактерий к PLB, добавляемым
могут становиться мишенями для PLB при до
в наномолярном диапазоне концентраций, свя
бавлении последних в высоких (микромоляр
зана с оперонами и генами, кодирующими
ных) концентрациях. Вместе с тем, о структуре
мембранный рецептор белковой природы. Было
пор, образуемых PLB в мембране, как в присут
установлено, что таким рецептором служит ман
ствии рецептора, так и в его отсутствие, в насто
нозо фосфотрансферазный комплекс (Man PTS),
ящее время ничего не известно.
осуществляющий фосфорилирование и транс
Наряду с повышением проницаемости мемб
мембранный транспорт ряда углеводов и род
раны заслуживает внимания способность PLB
ственных соединений [87-89]. Гены, отвечаю
затруднять транспорт жизненно важных моно
щие за синтез Man PTS, находятся под контро
сахаридов внутрь клетки. Рост клеток, обладаю
лем σ54(RpoN) зависимых промоторов. Чувстви
щих иммунитетом к PLB, хотя и не прекращает
тельность к бактериоцинам подкласса IIa обес
ся, но замедляется в присутствии этих веществ,
печивают ассоциированные с мембраной субъе
если единственный углевод в составе питатель
диницы Man PTS EIIC и EIID, как было пока
ной среды - глюкоза или манноза [90]. Очевид
зано в экспериментах по гетерологической
но, что данный эффект является следствием ин
экспрессии их генов [90]. Было высказано пред
гибирования нормальной транспортной функ
положение, что N концевая часть PLB связыва
ции Man PTS белком иммунитета или самим
ется с внеклеточной петлей субъединицы EIIC,
бактериоцином.
после чего C концевой участок взаимодействует
Высокая специфичность взаимодействия
с трансмембранным сегментом рецептора, фор
PLB с субъединицей EIIC Man PTS обусловли
мируя в комплексе с ним трансмембранный ка
вает риск быстрого развития резистентности к
нал [56, 78, 91].
данному подклассу бактериоцинов. Один из ме
Третья из перечисленных выше моделей сов
ханизмов выработки резистентности, подтверж
мещает отдельные элементы первых двух. В со
денный экспериментально, состоит в селекции
ответствии с ней, связывание PLB с рецептором
штаммов, отличающихся пониженным уровнем
служит промежуточным этапом перед встраива
экспрессии Man PTS [96, 97]. Однако известны
нием пептидных молекул в липидный бислой, в
случаи развития резистентности при нормаль
котором они олигомеризуются и образуют пору.
ном или повышенном уровне синтеза данного
В пользу предположения о том, что Man PTS
белкового комплекса [97-100]. Описанные иск
служит лишь мишенью для докинга, но не
лючения демонстрируют, насколько значитель
участвует в формировании поры, свидетельству
ным может быть влияние таких параметров
ют эксперименты с гибридными конструкция
мембраны, как ее липидный состав, вязкость,
ми, секретируемыми в периплазму E. coli и со
поверхностный заряд на пептид липидное взаи
держащими периплазматический домен интег
модействие и, в конечном счете, на чувствитель
рального мембранного белка EtpM, способный
ность клетки к бактериоцину. Изменениями
закрепляться в цитоплазматической мембране [92].
этих параметров, по видимому, объясняется ре
Синтезируемые гибридные белки содержали
зистентность к PLB в низких концентрациях,
последовательность PLB, которая экспонирова
тогда как мутации или пониженный уровень
на на поверхности цитоплазматической мемб
экспрессии Man PTS обеспечивают резистент
БИОХИМИЯ том 84 вып. 5 2019
624
БАЛАНДИН и др.
ность к пептидам и в более высоких концентра
EIIA и EIIB, к молекулам субстрата, которые
циях [98, 100].
проникают в цитоплазму путем облегченной
диффузии с помощью EIIC/EIID. Трансмемб
ранный транспорт может осуществляться в обо
Man PTS КАК РЕЦЕПТОР ДЛЯ PLB
их направлениях, однако фосфорилирование
субстрата, по видимому, снижает его аффин
Фосфоенолпируват:углевод фосфотрансфе
ность к переносчику, что делает процесс необра
разная система (PTS) - ассоциированный с ци
тимым [105]. Ранее предполагалось, что молеку
топлазматической мембраной бактерий и архей
ла субстрата движется по каналу, сформирован
белковый комплекс, осуществляющий транс
ному EIIC/EIID [102], но недавние исследова
порт внутрь клетки и сопряженное с ним фос
ния кристаллической структуры субъединиц
форилирование ряда моно и дисахаридов, их про
EIIC переносчиков диацетилхитобиозы [109] и
изводных и многоатомных спиртов [101-105].
мальтозы [110, 111] из Bacillus cereus и перенос
Комплексы и отдельные компоненты PTS обна
чика аскорбиновой кислоты из E. coli [112] ука
ружены у большого числа представителей раз
зывают на то, что PTS, относящиеся к суперсе
ных типов бактерий, однако распределение
мейству Glc Fru Lac, функционируют по прин
структурных вариантов между видами характе
ципу «лифта» или «подъемника» («elevator car»):
ризуется высокой степенью неоднородности:
подвижный С концевой домен EIIC образует
наиболее богатыми арсеналами PTS отличаются
комплекс с молекулой переносимого вещества на
молочнокислые бактерии и энтеробактерии, в то
одной стороне мембраны и, сохраняя собствен
время как некоторые другие группы бактерий
ную конформацию, за счет изменения своего
(например, цианобактерии) этой системы пол
положения относительно статичного N конце
ностью лишены [106]. Структура комплекса
вого домена перемещается на другую сторону
включает три части: фермент I (EI), гистидин
мембраны, где происходит отщепление субстра
содержащий переносчик фосфата (HPr) и фер
та [110, 111]. N концевой домен отвечает за ди
мент II (EII). Последний состоит из трех (EIIA,
меризацию EIIC [110].
ранее известного как EIII, EIIB и EIIC) или че
Вторая, не менее важная функция PTS, за
тырех (EIIA, EIIB, EIIC, EIID) компонентов,
ключается в регуляции метаболизма [105]. Из
которые могут быть доменами одного белка или
вестно, что PTS участвует в регуляции обмена уг
отдельными белковыми субъединицами [102].
леводов, азотсодержащих соединений, фосфа
Белки EI, HPr и субъединицы EIIA и EIIB лока
тов и координации транспорта ионов калия, а
лизованы в цитоплазме, а субъединицы EIIC и
также влияет на процесс хемотаксиса по нап
EIID пронизывают мембрану [102]. Именно EII
равлению к питательным субстратам, формиро
отвечает за субстратную специфичность комп
вание биопленок и вирулентность ряда патоген
лекса и определяет принадлежность PTS к тому
ных штаммов. PTS играет роль центра, обраба
или иному семейству.
тывающего информацию об энергетическом
Выделяют четыре суперсемейства PTS, не об
статусе клетки и наличии питательных субстра
ладающих гомологией между собой: 1) Glc Fru Lac
тов в окружающей среде, а также координирую
(переносчики глюкозы, фруктозы, лактозы);
щего процессы катаболизма разных соедине
2) Asc Gat (переносчики аскорбата и галактито
ний. Фосфатные группы присоединяются с об
ла); 3) Man (переносчики маннозы); 4) Dha (пе
разованием высокоэнергетической связи к ос
реносчики дигидроксиацетона) [107, 108]. Внут
таткам гистидина и реже цистеина компонентов
ри каждого из них наблюдается значительная
комплекса. Это приводит к тому, что реакции
эволюционная изменчивость структуры и суб
переноса фосфата характеризуются обрати
стратной специфичности. В геноме бактерий
мостью (необратимо лишь фосфорилирование
одного вида может содержаться множество раз
субстрата), вследствие чего фосфорилирование
ных генов EII. У E. coli гены, кодирующие об
или дефосфорилирование любого из компонен
щие для разных вариантов PTS компоненты,
тов влияет на состояние системы в целом [103].
собраны в оперон pts, а гены, отвечающие за
Этим бактериальные PTS отличаются от боль
субстратную специфичность комплекса, в боль
шинства эукариотических регуляторных каска
шинстве своем локализованы в одном опероне с
дов, где фосфорилирование по остаткам тирози
генами, обеспечивающими катаболизм данного
на, серина, треонина сопровождается потерей
субстрата [102].
энергии и лишь изменяет каталитическую ак
Основной механизм функционирования PTS
тивность ферментов, не делая их донорами фос
состоит в последовательном переносе фосфата
фатной группы [113].
от фосфоенолпирувата по цепи, образованной
При наличии в окружающей среде субстрата,
цитоплазматическими компонентами EI, HPr,
распознаваемого и транспортируемого PTS,
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
625
компоненты EI, HPr, EII по цепочке передают
но, что рецепторами для PLB служат лишь бел
ему свои фосфатные группы, в результате чего
ки, составляющие группу I. Внутри группы аф
доля фосфорилированной формы этих компо
финность к бактериоцинам и соответствующие
нентов в клетке падает. Это служит сигналом для
значения МИК значительно варьируют: 1) наи
перестройки ферментативного аппарата с целью
более высокой чувствительностью обладают
преимущественной утилизации данного источ
представители родов Enterococcus, Listeria, Carno(
ника энергии и подавления иных путей катабо
bacterium (низкие значения МИК); 2) средняя
лизма. Передача сигнала от компонентов PTS
чувствительность характерна для видов, относя
осуществляется путем прямого фосфорилирова
щихся к Lactobacillus, Pediococcus, Clostridium;
ния или зависимого от фосфорилирования бе
3) низкой чувствительностью отличаются штам
лок белкового взаимодействия с факторами
мы Streptococcus и Leuconostoc (очень высокие
транскрипции и другими белками (например, с
значения МИК) [95, 116, 117]. Интересно отме
белком CcpA у бактерий рода Bacillus [114]).
тить, что у бактерий, способных продуцировать
В противоположной ситуации, когда PTS
бактериоцины подкласса IIa, обнаруживаются
субстраты в среде отсутствуют, происходит на
белки Man PTS именно I группы - факт, биоло
сыщение системы фосфорилированными ком
гическое значение которого еще предстоит вы
понентами, что служит сигналом к использова
яснить [95].
нию альтернативных источников энергии, нап
При сравнении аминокислотных последова
ример, путем активации аденилатциклазы у эн
тельностей белков EIIC и EIID, представляю
теробактерий [103].
щих разные ветви филогенетического дерева,
Комплексы суперсемейства Man PTS, воп
были выявлены три области, отличающие груп
реки закрепившемуся в литературе наименова
пу I от двух других групп: 1) «α область» в N кон
нию, обеспечивают транспорт и фосфорилиро
цевой части EIIC; 2) «β область» в C концевой
вание не только маннозы, но также глюкозы и
части EIIC; 3) «γ область» в структуре EIID [95].
некоторых других углеводов [115]. Углевод спе
В составе функционально активного комплекса
цифичный фермент EII в составе Man PTS
эти области, предположительно, экспонирова
построен из трех или четырех субъединиц:
ны на внешней стороне мембраны бактерии.
EIIAB + EIIC + EIID или EIIA + EIIB + EIIC +
Интересен тот факт, что пермеазы EIIC/EIID
+ EIID [102]. Это единственный тип PTS, в ко
служат мишенью не только для PLB, но и для
тором содержится субъединица EIID [107].
бактериоцинов других классов, например, лак
Трехмерная структура пермеаз Man PTS и меха
тококцина A (класс IIc) и микроцина E492
низм их функционирования не исследованы. Ге
(класс IIe), а также «входными воротами» для
ны белков данного семейства обнаруживаются
некоторых бактериофагов [91, 102, 118].
преимущественно у представителей двух эволю
ционно отдаленных друг от друга типов бакте
рий: грамположительных Firmicutes и грамотри
ИММУНИТЕТ
цательных Proteobacteria [95]. Такая картина
БАКТЕРИЙ ПРОДУЦЕНТОВ
распределения генов могла сформироваться
вследствие их горизонтального переноса [115].
Защита вырабатывающих бактериоцины штам
Общим свойством большинства носителей ге
мов от летального действия продуктов собствен
нов Man(PTS является их способность в качест
ного синтеза осуществляется путем коэкспрес
ве симбионтов заселять поверхность эпителия
сии генов иммунитета, локализованных в тех же
животных и человека. В некоторых случаях гены
оперонах, кодирующих небольшие цитозольные
Man(PTS соседствуют с генами секретируемых
белки размером 90-120 а.о. [90, 119, 120]. Осно
бактериями ферментов, обеспечивающих рас
ву пространственной структуры данных белков
щепление полисахаридов. Сравнительный ана
составляют четыре антипараллельных α спи
лиз первичных структур более чем 80 пар белков
ральных участка. Многообразие белков, обеспе
EIIC и EIID системы Man PTS показал, что фи
чивающих самозащиту продуцента, соответ
логенетические деревья двух семейств белков
ствует структурному разнообразию самих PLB.
полностью повторяют друг друга. При этом бел
Активность белков иммунитета характеризуется
ки разных семейств из одного вида бактерии за
специфичностью как по отношению к PLB, так
нимают одинаковое положение в соответствую
и по отношению к мембранному рецептору. Ис
щем дереве, что служит свидетельством парал
следование ингибирующей активности гибрид
лельной эволюции EIIC и EIID [95]. В каждом
ных иммунных белков, полученных путем при
из двух деревьев можно выделить три обособ
соединения различных C концевых участков к
ленные ветви, что позволяет разделить все се
одному и тому же N концевому фрагменту, в от
мейство Man PTS на три группы. Было показа
ношении природных [121] и гибридных [53]
БИОХИМИЯ том 84 вып. 5 2019
626
БАЛАНДИН и др.
PLB, а также изучение пространственной струк
та гибридного белка EtpM Ent35 [92]. В данной
туры иммунных белков [122, 123] показало, что
работе коэкспрессия гена иммунитета (munC)
именно C концевая последовательность отвеча
к энтероцину CRL35 обеспечивала выживание
ет за специфическое распознавание молекулы
бактериальных клеток. Как отмечалось выше, в
бактериоцина. На основании этого был сделан
описанной экспериментальной модели отсут
вывод о том, что C концевая часть иммунного
ствует специфический рецептор, из чего следует,
белка самостоятельно или в комплексе с рецеп
что белок MunC блокирует пору, напрямую вза
тором взаимодействует с C концевой (вариа
имодействуя с молекулами бактериоцина. В от
бельной, определяющей антимикробный спектр)
личие от бактериоцина, иммобилизованного на
частью PLB. Формирование тройного комплекса
внешней стороне мембраны, белок иммунитета
«рецептор-PLB-белок иммунитета» было впо
накапливается в цитоплазме и не способен к са
следствии подтверждено экспериментально [90].
мостоятельной транслокации. Следовательно,
Комплекс образуется лишь в том случае, если
для проявления его ингибирующей активности
пептид атакует бактериальную мембрану с
пора уже должна быть сформирована. Нетрудно
внешней стороны.
заметить, что эти результаты противоречат фак
В одной из недавних работ были опублико
там, полученным на других модельных объектах
ваны данные о проведении гетерологической
и свидетельствующим о важности участия субъ
экспрессии рецепторов Man PTS EII из четырех
единиц рецептора в связывании белка иммуни
разных видов бактерий, чувствительных к педио
тета. Таким образом, вопрос о роли рецептора в
цину PA 1, в штамме Lactobacillus plantarum W903,
механизме инактивации бактериоцина в настоя
мутантном по Man PTS EII и устойчивом к
щее время остается открытым.
действию данного пептида [124]. Каждый из по
лученных штаммов приобретал чувствитель
ность к PA 1, однако только один из них (штамм,
РАЗРАБОТКА ТЕРАПЕВТИЧЕСКИ
экспрессирующий EII из Lactobacillus plantarum
ЦЕННЫХ АНАЛОГОВ PLB
WQ081) становился устойчивым к PA 1 при од
новременной экспрессии гена иммунитета pedB.
Изучение PLB дает в руки исследователей
На следующем этапе в этой же системе была
новую перспективную модель для создания ан
проведена экспрессия шести гибридных вари
тибиотиков узкого спектра действия. В литера
антов рецептора, полученных путем комбина
туре описаны попытки изменения структуры
ции субъединиц EIIC или EIID из Man PTS
PLB с целью повышения антимикробной актив
Lactobacillus plantarum WQ081 (рецептора, взаи
ности, расширения спектра действия, повыше
модействующего с иммунным белком PedB) с
ния устойчивости в биологических средах. В от
дополняющими их субъединицами EIID или
личие от многих других антимикробных пепти
EIIC из трех других видов бактерий, рецепторы
дов, PLB не проявляют активности в отношении
которых не способны взаимодействовать с PedB.
клеток млекопитающих - этим объясняется от
Гибридные рецепторы успешно выполняли
сутствие публикаций, посвященных разработке
функцию мишени для педиоцина PA 1, однако
аналогов бактериоцинов данного подкласса с
ни в одном из шести случаев коэкспрессия PedB
пониженной токсичностью, а также противо
не обеспечивала защиты от антибактериального
опухолевых средств на их основе [1]. Хотя тести
действия пептида. Таким образом, был сделан
рование педиоцина PA 1 на культурах клеток
вывод о том, что во взаимодействии комплекса
обезьяны и человека показало, что этот пептид в
Man PTS и педиоцина с белком иммунитета
концентрации 10-20 мкг/мл, многократно пре
участвуют обе субъединицы рецептора.
вышающей антибактериальные МИК, обладает
Несмотря на то что попытки воспроизвести
определенными токсическими свойствами [127],
образование комплекса белка иммунитета с мо
другие PLB (в частности, карнобактериоцины
лекулой PLB без участия Man PTS в эксперимен
BM1 и B2 [128]), не проявляют даже такого уров
тах in vitro не привели к желаемому результату,
ня цитотоксичности. Высокая специфичность
косвенные данные указывают на то, что такое вза
действия природных пептидов, являющаяся ре
имодействие в принципе возможно [85, 125, 126].
зультатом длительной биологической эволю
Вероятным условием для прямого связывания
ции, практически исключает возможность до
является упорядоченная конформация молеку
биться существенного повышения активности в
лы бактериоцина, которую пептид приобретает
отношении тех штаммов, для которых значения
лишь после встраивания в липидный бислой [44].
МИК находятся в низком наномолярном и пи
В пользу этой гипотезы свидетельствуют резуль
комолярном диапазоне. Большинство попыток
таты уже упоминавшегося эксперимента по
точечного мутагенеза приводят к снижению ак
экспрессии летального для бактерии продуцен
тивности [59, 60, 129]. Тем не менее с помощью
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
627
насыщающего NNK мутагенеза отдельных участ
помощью которых эти пептиды могут проявлять
ков аминокислотной последовательности были
свой антимикробный эффект, а также предпри
получены мутанты энтероцина A, обладающие
нят ряд попыток объяснить иммунитет к ним со
повышенной активностью в отношении ванко
стороны бактерий продуцентов. В настоящее вре
мицин резистентных энтерококков [32]. Неко
мя можно считать неоспоримой роль Man PTS
торые успехи были достигнуты за счет повыше
как рецептора, обусловливающего чувствитель
ния положительного заряда пептида [130]. Но,
ность к PLB. Тем не менее липидный состав
по видимому, более эффективным подходом к
мембраны также вносит значительный вклад в
получению привлекательных в прикладном ас
эффективность порообразования на поздних
пекте PLB является одновременная замена сра
стадиях этого процесса. Известно, что в высо
зу нескольких аминокислотных остатков. При
ких (микромолярных) концентрациях PLB спо
мером подобных исследований служат работы
собны вести себя как классические мембрано
по гибридизации структуры педиоцина PA 1 с
литические антимикробные пептиды широкого
другими PLB методом ДНК шаффлинга [131].
спектра действия, что заставляет с осторож
Гибридизация PLB с антимикробными пептида
ностью подходить к анализу литературных дан
ми других классов позволяет создавать новые
ных, касающихся видоспецифичности бактери
молекулы с измененной видоспецифичностью
оцинов этого класса. Нейтрализация токсич
действия. Так, гибридный полипептид, состоя
ности PLB белками иммунитета происходит, по
щий из полноразмерных цепей PLB энтероцина
видимому, лишь в гидрофобном окружении пос
(N концевая часть гибрида) и бактериоцина
ле внедрения молекул пептида в липидный бис
MccV, относящегося к подклассу IId, сочетает
лой; при этом роль рецептора в механизме нейт
способность исходных молекул ингибировать
рализации остается под вопросом.
рост как грамположительных, так и грамотрица
PLB ингибируют рост ряда важных микро
тельных бактерий [132].
организмов, вызывающих заболевания человека
Важным направлением исследований явля
и животных. Наиболее перспективным прик
ется получение аналогов PLB, более стабильных
ладным направлением в исследованиях PLB яв
в желудочно кишечном тракте и во внутренней
ляется разработка антимикробных агентов для
среде организма [14]. Общепринятые подходы, та
борьбы с листериозами и инфекциями, вызыва
кие как модификация сайтов расщепления трип
емыми резистентными штаммами энтерокок
сином, введение неканонических а.о. и D изо
ков. Преимущество этих соединений, по срав
меров аминокислот, ограниченно применимы при
нению с обычными антибиотиками, состоит в
работе с бактериоцинами подкласса IIa вслед
том, что они в минимальной степени затрагива
ствие их высокой чувствительности к любым из
ют жизнедеятельность нормальной микробиоты
менениям структуры. Стереоспецифический ха
[27, 136, 137]. Молекулы PLB, построенные из
рактер взаимодействия с мембранным рецепто
протеиногенных L аминокислот, легко расщеп
ром обусловливает отсутствие активности D энан
ляются в организме, не давая токсичных и акку
тиомеров [55]. Устойчивость PLB может быть по
мулирующихся метаболитов [136]. При этом пе
вышена путем введения дополнительной кова
риод их полужизни в желудочно кишечном
лентной связи или остатков, стабилизирующих
тракте достаточен для достижения антимикроб
шпильку в C концевой области молекулы посред
ного эффекта.
ством нековалентных взаимодействий [77-79].
Число публикаций, посвященных исследо
Падение антимикробной активности может
ваниям эффективности антибиотического дейст
быть связано не только с протеолитическим рас
вия PLB на моделях in vivo, в настоящее время
щеплением PLB, но и с окислением входящих в
невелико. В частности, на модели листериоза у
их состав остатков метионина под действием
мышей показано, что пероральное введение пе
кислорода воздуха. Так, окислению подвержен
диоцина PA 1 подавляет развитие патогена в
M31 в структуре педиоцина PA 1 [133]. Мутации
желудочно кишечном тракте и замедляет его
M31A, M31L, M31I делают пептид устойчивым к
транслокацию в печень и селезенку [27]. Сход
окислению ценой лишь незначительной потери
ные данные на аналогичной модели были полу
активности. Кроме того, 4-8 кратное возраста
чены для энтероцина CRL35 [138]. Заслуживают
ние МИК наблюдается и при окислении карно
внимания данные по активности включенного в
бактериоцина BM1 [134]. В этом случае стабиль
липосомы бактериоцина E50-52, ингибирующе
ный аналог был получен путем замены остатка
го внутримакрофагальный рост Mycobacterium
метионина на валин [135].
tuberculosis и продлевающего срок жизни мышей
на модели острого туберкулеза [139]. Получен
За годы исследований PLB было предложено
ные результаты вселяют надежду на то, что ис
несколько гипотез, описывающих механизмы, с
следования в данной области увенчаются созда
БИОХИМИЯ том 84 вып. 5 2019
628
БАЛАНДИН и др.
нием препаратов, способных занять свою уни
никова сформировала концепцию исследова
кальную нишу среди используемых в клинике
ния, обеспечила его координацию и финанси
антимикробных средств.
рование, проанализировала собранные литера
турные данные и подготовила рукопись к пуб
Финансирование. Работа выполнена при фи
ликации. Все авторы утвердили окончательную
нансовой поддержке Российского научного
версию обзора.
фонда (грант 19 14 00326).
Конфликт интересов. Авторы заявляют об от
Вклад авторов. С.В. Баландин участвовал в
сутствии конфликта интересов.
сборе и анализе литературных данных, осущест
Соблюдение этических норм. Настоящая
вил планирование и написание первой версии
статья не содержит описания каких либо иссле
рукописи; Э.В. Шереметьева участвовала в сбо
дований с участием людей или использованием
ре и анализе литературных данных; Т.В. Овчин
животных в качестве объектов исследований.
СПИСОК ЛИТЕРАТУРЫ
1.
Cotter, P.D., Ross, R.P., and Hill, C. (2013) Bacteriocins -
13.
Drider, D., Fimland, G., Hechard, Y., McMullen, L.M.,
a viable alternative to antibiotics? Nat. Rev. Microbiol., 11,
and Prevost, H. (2006) The continuing story of class IIa
95-105, doi: 10.1038/nrmicro2937.
bacteriocins, Microbiol. Mol. Biol. Rev., 70, 564-582,
2.
Kemperman, R., Kuipers, A., Karsens, H., Nauta, A.,
doi: 10.1128/MMBR.00016 05.
Kuipers, O., and Kok, J. (2003) Identification and charac
14.
Papagianni, M., and Anastasiadou, S. (2009) Pediocins:
terization of two novel clostridial bacteriocins, circularin A
the bacteriocins of pediococci. sources, production, proper
and closticin
574, Appl. Environ. Microbiol.,
69,
ties and applications, Microb. Cell Fact., 8, 3, doi: 10.
1589-1597, doi: 10.1128/AEM.69.3.1589 1597.2003.
1186/1475 2859 8 3.
3.
Svetoch, E.A., Eruslanov, B.V., Perelygin, V.V., Mitse
15.
Rios Colombo, N.S., Chalon, M.C., Navarro, S.A., and
vich, E.V., Mitsevich, I.P., Borzenkov, V.N., Levchuk, V.P.,
Bellomio, A. (2018) Pediocin like bacteriocins: new per
Svetoch, O.E., Kovalev, Y.N., Stepanshin, Y.G., Sira
spectives on mechanism of action and immunity, Curr.
gusa, G.R., Seal, B.S., and Stern, N.J. (2008) Diverse
Genet., 64, 345-351, doi: 10.1007/s00294 017 0757 9.
antimicrobial killing by Enterococcus faecium E 50-52 bac
16.
Bhunia, A.K., Johnson, M.C., and Ray, B.
(1988)
teriocin, J. Agric. Food Chem., 56, 1942-1948, doi: 10.
Purification, characterization and antimicrobial spectrum
1021/jf073284g.
of a bacteriocin produced by Pediococcus acidilactici, J. Appl.
4.
Cotter, P.D., Hill, C., and Ross, R.P. (2005) Bacteriocins:
Bacteriol., 65, 261-268, doi: 10.1111/j.1365 2672.1988.
developing innate immunity for food, Nat. Rev. Microbiol.,
tb01893.x.
3, 777-788, doi: 10.1038/nrmicro1273.
17.
Hastings, J.W., Sailer, M., Johnson, K., Roy, K.L.,
5.
Svetoch, E.A., and Stern, N.J. (2010) Bacteriocins to con
Vederas, J.C., and Stiles, M.E. (1991) Characterization of
trol Campylobacter spp. in poultry - a review, Poult. Sci.,
leucocin A UAL 187 and cloning of the bacteriocin gene
89, 1763-1768, doi: 10.3382/ps.2010 00659.
from Leuconostoc gelidum, J. Bacteriol., 173, 7491-7500,
6.
Desriac, F., Defer, D., Bourgougnon, N., Brillet, B., Le
doi: 10.1128/jb.173.23.7491 7500.1991.
Chevalier, P., and Fleury, Y. (2010) Bacteriocin as weapons
18.
Motlagh, A.M., Bhunia, A.K., Szostek, F., Hansen, T.R.,
in the marine animal associated bacteria warfare: invento
Johnson, M.C., and Ray, B. (1992) Nucleotide and amino
ry and potential applications as an aquaculture probiotic,
acid sequence of pap gene (pediocin AcH production) in
Mar. Drugs, 8, 1153-1177, doi: 10.3390/md8041153.
Pediococcus acidilactici H, Lett. Appl. Microbiol., 15,
7.
Gharsallaoui, A., Oulahal, N., Joly, C., and Degraeve, P.
45-48, doi.org/10.1111/j.1472 765x.1992.tb00721.x.
(2016) Nisin as a food preservative: part 1: physicochemi
19.
Henderson, J.T., Chopko, A.L., and van Wassenaar, P.D.
cal properties, antimicrobial activity, and main uses, Crit.
(1992) Purification and primary structure of pediocin PA 1
Rev. Food Sci. Nutr., 56, 1262-1274, doi: 10.1080/
produced by Pediococcus acidilactici PAC 1.0, Arch.
10408398.2013.763765.
Biochem. Biophys., 295, 5-12, doi: 10.1016/0003 9861(92)
8.
Shin, J.M., Gwak, J.W., Kamarajan, P., Fenno, J.C.,
90480 k.
Rickard, A.H., and Kapila, Y.L. (2016) Biomedical appli
20.
Cui, Y., Zhang, C., Wang, Y., Shi, J., Zhang, L., Ding, Z.,
cations of nisin, J. Appl. Microbiol., 120, 1449-1465,
Qu, X., and Cui, H. (2012) Class IIa bacteriocins: diversity
doi: 10.1111/jam.13033.
and new developments, Int. J. Mol. Sci., 13, 16668-16707,
9.
Panteleev, P.V., Balandin, S.V., Ivanov, V.T., and
doi: 10.3390/ijms131216668.
Ovchinnikova, T.V. (2017) A therapeutic potential of ani
21.
Yildirim, Z., and Johnson, M.G. (1998) Characterization
mal β hairpin antimicrobial peptides, Curr. Med. Chem.,
and antimicrobial spectrum of bifidocin B, a bacteriocin
24, 1724-1746, doi: 10.2174/0929867324666170424124416.
produced by Bifidobacterium bifidum NCFB 1454, J. Food
10.
Maxson, T., and Mitchell, D.A. (2016) Targeted treatment
Prot., 61, 47-51, doi: 10.4315/0362 028x 61.1.47.
for bacterial infections: prospects for pathogen specific
22.
Cheikhyoussef, A., Cheikhyoussef, N., Chen, H., Zhao, J.,
antibiotics coupled with rapid diagnostics, Tetrahedron, 72,
Tang, J., Zhang, H., and Chen, W. (2010) Bifidin I -
3609-3624, doi: 10.1016/j.tet.2015.09.069.
A new bacteriocin produced by Bifidobacterium infantis
11.
Melander, R.J., Zurawski, D.V., and Melander, C. (2018)
BCRC 14602: purification and partial amino acid
Narrow spectrum antibacterial agents, Medchemcomm, 9,
sequence, Food Control, 21, 746-753, doi: 10.1016/j.food
12-21, doi: 10.1039/c7md00528h.
cont.2009.11.003.
12.
Klaenhammer, T.R. (1993) Genetics of bacteriocins pro
23.
Le Marrec, C., Hyronimus, B., Bressollier, P., Verneuil, B.,
duced by lactic acid bacteria, FEMS Microbiol. Rev., 12,
and Urdaci, M.C. (2000) Biochemical and genetic charac
39-85, doi: 10.1111/j.1574 6976.1993.tb00012.x.
terization of coagulin, a new antilisterial bacteriocin in the
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
629
pediocin family of bacteriocins, produced by Bacillus coa
37.
Lohans, C.T., and Vederas, J.C. (2012) Development of
gulans I(4), Appl. Environ. Microbiol., 66, 5213-5220,
class IIa bacteriocins as therapeutic agents, Int. J. Mic(
doi: 10.1128/aem.66.12.5213 5220.2000.
robiol., 386410, doi: 10.1155/2012/386410.
24.
Kalmokoff, M.L., Banerjee, S.K., Cyr, T., Hefford, M.A.,
38.
Corr, S.C., Li, Y., Riedel, C.U., O’Toole, P.W., Hill, C.,
and Gleeson, T. (2001) Identification of a new plasmid
and Gahan, C.G.M. (2007) Bacteriocin production as a
encoded sec dependent bacteriocin produced by Listeria
mechanism for the antiinfective activity of Lactobacillus
innocua 743, Appl. Environ. Microbiol., 67, 4041-4047,
salivarius UCC118, Proc. Natl. Acad. Sci. USA, 104,
doi: 10.1128/aem.67.9.4041 4047.2001.
7617-7621, doi: 10.1073/pnas.0700440104.
25.
Zheng, J., Ganzle, M.G., Lin, X.B., Ruan, L., and Sun, M.
39.
Dobson, A., Cotter, P.D., Ross, R.P., and Hill, C. (2012)
(2015) Diversity and dynamics of bacteriocins from human
Bacteriocin production: a probiotic trait? Appl. Environ.
microbiome, Environ. Microbiol., 17, 2133-2143, doi: 10.
Microbiol., 78, 1-6, doi: 10.1128/aem.05576 11.
1111/1462 2920.12662.
40.
O’Shea, E.F., Cotter, P.D., Stanton, C., Ross, R.P., and
26.
Cleveland, J., Montville, T.J., Nes, I.F., and Chikin
Hill, C. (2012) Production of bioactive substances by
das, M.L. (2001) Bacteriocins: safe, natural antimicrobials
intestinal bacteria as a basis for explaining probiotic mecha
for food preservation, Int. J. Food Microbiol., 71, 1-20,
nisms: bacteriocins and conjugated linoleic acid, Int. J.
doi: 10.1016/s0168 1605(01)00560 8.
Food Microbiol., 152, 189-205, doi: 10.1016/j.ijfoodmi
27.
Dabour, N., Zihler, A., Kheadr, E., Lacroix, C., and Fliss, I.
cro.2011.05.025.
(2009) In vivo study on the effectiveness of pediocin PA 1
41.
Nissen Meyer, J., Rogne, P., Oppegard, C., Haugen, H.S.,
and Pediococcus acidilactici UL5 at inhibiting Listeria
and Kristiansen, P.E. (2009) Structure function relation
monocytogenes, Int. J. Food Microbiol., 133, 225-233,
ships of the non lanthionine containing peptide (class II)
doi: 10.1016/j.ijfoodmicro.2009.05.005.
bacteriocins produced by gram positive bacteria, Curr.
28.
Charpentier, E., and Courvalin, P. (1999) Antibiotic resis
Pharm. Biotechnol., 10, 19-37, doi: 10.2174/1389201097
tance in Listeria spp., Antimicrob. Agents Chemother., 43,
87048661.
2103-2108, doi: 10.1128/aac.43.9.2103.
42.
Zouhir, A., Hammami, R., Fliss, I., and Hamida, J.B.
29.
Bertsch, D., Muelli, M., Weller, M., Uruty, A., Lacroix, C.,
(2010) A new structure based classification of gram posi
and Meile, L. (2014) Antimicrobial susceptibility and
tive bacteriocins, Protein J., 29, 432-439, doi: 10.1007/
antibiotic resistance gene transfer analysis of foodborne,
s10930 010 9270 4.
clinical, and environmental Listeria spp. isolates including
43.
Casaus, P., Nilsen, T., Cintas, L.M., Nes, I.F., Hernan
Listeria monocytogenes, Microbiologyopen, 3, 118-127,
dez, P.E., and Holo, H. (1997) Enterocin B, a new bacte
doi: 10.1002/mbo3.155.
riocin from Enterococcus faecium T136 which can act syn
30.
Cintas, L.M., Casaus, P., Fernandez, M.F., and Hernan
ergistically with enterocin A, Microbiology,
143,
dez, P.E. (1998) Comparative antimicrobial activity of
2287-2294, doi: 10.1099/00221287 143 7 2287.
enterocin L50, pediocin PA 1, nisin A and lactocin S
44.
Fregeau Gallagher, N.L., Sailer, M., Niemczura, W.P.,
against spoilage and foodborne pathogenic bacteria, Food
Nakashima, T.T., Stiles, M.E., and Vederas, J.C. (1997)
Microbiol., 15, 289-298, doi: 10.1006/fmic.1997.0160.
Three dimensional structure of leucocin A in trifluo
31.
Millette, M., Cornut, G., Dupont, C., Shareck, F.,
roethanol and dodecylphosphocholine micelles: spatial
Archambault, D., and Lacroix, M. (2008) Capacity of
location of residues critical for biological activity in type
human nisin and pediocin producing lactic acid bacteria
IIa bacteriocins from lactic acid bacteria, Biochemistry, 36,
to reduce intestinal colonization by vancomycin resistant
15062-15072, doi: 10.1021/bi971263h.
enterococci, Appl. Environ. Microbiol., 74, 1997-2003,
45.
Wang, Y., Henz, M.E., Gallagher, N.L., Chai, S., Gibbs, A.C.,
doi: 10.1128/aem.02150 07.
Yan, L.Z., Stiles, M.E., Wishart, D.S., and Vederas, J.C.
32.
McClintock, M.K., Kaznessis, Y.N., and Hackel, B.J.
(1999) Solution structure of carnobacteriocin B2 and
(2016) Enterocin A mutants identified by saturation muta
implications for structure activity relationships among
genesis enhance potency towards vancomycin resistant
type IIa bacteriocins from lactic acid bacteria, Biochemistry,
enterococci, Biotechnol. Bioeng., 113, 414-423, doi: 10.
38, 15438-15447, doi: 10.1021/bi991351x.
1002/bit.25710.
46.
Uteng, M., Hauge, H.H., Markwick, P.R.L., Fimland, G.,
33.
Jimenez, J.J., Borrero, J., Gutiez, L., Arbulu, S., Herranz, C.,
Mantzilas, D., Nissen Meyer, J., and Muhle Goll, C.
Cintas, L.M., and Hernandez, P.E. (2014) Use of synthetic
(2003) Three dimensional structure in lipid micelles of the
genes for cloning, production and functional expression of
pediocin like antimicrobial peptide sakacin P and a
the bacteriocins enterocin A and bacteriocin E 50-52 by
sakacin P variant that is structurally stabilized by an inserted
Pichia pastoris and Kluyveromyces lactis, Mol. Biotechnol.,
C terminal disulfide bridge, Biochemistry, 42, 11417-11426,
56, 571-583, doi: 10.1007/s12033 014 9731 7.
doi: 10.1021/bi034572i.
34.
Arbulu, S., Jimenez, J.J., Gutiez, L., Cintas, L.M.,
47.
Haugen, H.S., Fimland, G., Nissen Meyer, J., and
Herranz, C., and Hernandez, P.E. (2015) Cloning and
Kristiansen, P.E. (2005) Three dimensional structure in
expression of synthetic genes encoding the broad antimic
lipid micelles of the pediocin like antimicrobial peptide
robial spectrum bacteriocins SRCAM 602, OR 7, E 760,
curvacin A, Biochemistry, 44, 16149-16157, doi: 10.1021/
and L 1077, by recombinant Pichia pastoris, Biomed. Res.
bi051215u.
Int., 767183, doi: 10.1155/2015/767183.
48.
Arbulu, S., Lohans, C.T., van Belkum, M.J., Cintas, L.M.,
35.
Wachsman, M.B., Castilla, V., de Ruiz Holgado, A.P., de
Herranz, C., Vederas, J.C., and Hernandez, P.E. (2015)
Torres, R.A., Sesma, F., and Coto, C.E. (2003) Enterocin
Solution structure of enterocin HF, an antilisterial bacteri
CRL35 inhibits late stages of HSV 1 and HSV 2 replica
ocin produced by Enterococcus faecium M3K31, J. Agric.
tion in vitro, Antiviral Res., 58, 17-24, doi: 10.1016/s0166
Food Chem., 63, 10689-10695, doi: 10.2210/pdb2n4k/
3542(02)00099 2.
pdb.
36.
Todorov, S.D., Wachsman, M., Tome, E., Dousset, X.,
49.
Sit, C.S., Lohans, C.T., van Belkum, M.J., Campbell, C.D.,
Destro, M.T., Dicks, L.M.T., Franco, B.D.G., de M., Vaz
Miskolzie, M., and Vederas, J.C. (2012) Substitution of a
Velho, M., and Drider, D. (2010) Characterisation of an
conserved disulfide in the type iia bacteriocin, leucocin A,
antiviral pediocin like bacteriocin produced by Entero(
with L leucine and L serine residues: effects on activity
coccus faecium, Food Microbiol., 27, 869-879, doi: 10.
and three dimensional structure, Chembiochem,
13,
1016/j.fm.2010.05.001.
35-38, doi: 10.1002/cbic.201100634.
БИОХИМИЯ том 84 вып. 5 2019
630
БАЛАНДИН и др.
50.
Bedard, F., Hammami, R., Zirah, S., Rebuffat, S., Fliss, I.,
motif, govern the binding of pediocin PA 1 and its frag
and Biron, E. (2018) Synthesis, antimicrobial activity and
ments to phospholipid vesicles, Appl. Environ. Microbiol.,
conformational analysis of the class IIa bacteriocin
63, 4770-4777.
pediocin PA 1 and analogs thereof, Sci. Rep., 8, 9029,
64.
Kazazic, M., Nissen Meyer, J., and Fimland, G. (2002)
doi.org/10.1038/s41598 018 27225 3.
Mutational analysis of the role of charged residues in tar
51.
Fimland, G., Pirneskoski, J., Kaewsrichan, J., Jutila, A.,
get cell binding, potency and specificity of the pediocin
Kristiansen, P.E., Kinnunen, P.K.J., and Nissen Meyer, J.
like bacteriocin sakacin P, Microbiology, 148, 2019-2027,
(2006) Mutational analysis and membrane interactions of
doi: 10.1099/00221287 148 7 2019.
the beta sheet like N terminal domain of the pediocin like
65.
Simon, L., Fremaux, C., Cenatiempo, Y., and Berjeaud, J.M.
antimicrobial peptide sakacin P, Biochim. Biophys. Acta,
(2002) Sakacin G, a new type of antilisterial bacteriocin,
1764, 1132-1140, doi.org/10.1016/j.bbapap.2006.04.007.
Appl. Environ. Microbiol., 68, 6416-6420, doi: 10.1128/
52.
Haugen, H.S., Kristiansen, P.E., Fimland, G., and Nissen
aem.68.12.6416 6420.2002.
Meyer, J. (2008) Mutational analysis of the class IIa bacte
66.
Derksen, D.J., Stymiest, J.L., and Vederas, J.C. (2006)
riocin curvacin A and its orientation in target cell memb
Antimicrobial leucocin analogues with a disulfide bridge
ranes, Appl. Environ. Microbiol., 74, 6766-6773, doi.org/
replaced by a carbocycle or by noncovalent interactions of
10.1128/aem.01068 08.
allyl glycine residues, J. Am. Chem. Soc., 128, 14252-14253,
53.
Johnsen, L., Fimland, G., and Nissen Meyer, J. (2005)
doi: 10.1021/ja066203q.
The C terminal domain of pediocin like antimicrobial
67.
Fleury, Y., Dayem, M.A., Montagne, J.J., Chaboisseau, E.,
peptides (class IIa bacteriocins) is involved in specific
Le Caer, J.P., Nicolas, P., and Delfour, A. (1996) Covalent
recognition of the C terminal part of cognate immunity
structure, synthesis, and structure function studies of
proteins and in determining the antimicrobial spectrum,
mesentericin Y 105(37), a defensive peptide from gram
J. Biol. Chem., 280, 9243-9250, doi: 10.1074/jbc.m412712200.
positive bacteria Leuconostoc mesenteroides, J. Biol. Chem.,
54.
Fimland, G., Jack, R., Jung, G., Nes, I.F., and Nissen
271, 14421-14429, doi: 10.1074/jbc.271.24.14421.
Meyer, J. (1998) The bactericidal activity of pediocin PA 1
68.
Derksen, D.J., Boudreau, M.A., and Vederas, J.C. (2008)
is specifically inhibited by a 15 mer fragment that spans the
Hydrophobic interactions as substitutes for a conserved
bacteriocin from the center toward the C terminus, Appl.
disulfide linkage in the type IIa bacteriocins, leucocin A
Environ. Microbiol., 64, 5057-5060.
and pediocin PA 1, Chembiochem, 9, 1898-1901, doi: 10.
55.
Yan, L.Z., Gibbs, A.C., Stiles, M.E., Wishart, D.S., and
1002/cbic.200800272.
Vederas, J.C. (2000) Analogues of bacteriocins: antimicro
69.
Mor, A., and Nicolas, P. (1994) The NH2 terminal alpha
bial specificity and interactions of leucocin A with its enan
helical domain 1-18 of dermaseptin is responsible for
tiomer, carnobacteriocin B2, and truncated derivatives,
antimicrobial activity, J. Biol. Chem., 269, 1934-1939.
J. Med. Chem., 43, 4579-4581, doi: 10.1021/jm000416n.
70.
Skerlavaj, B., Gennaro, R., Bagella, L., Merluzzi, L.,
56.
Haugen, H.S., Fimland, G., and Nissen Meyer, J. (2011)
Risso, A., and Zanetti, M. (1996) Biological characteriza
Mutational analysis of residues in the helical region of the
tion of two novel cathelicidin derived peptides and identi
class IIa bacteriocin pediocin PA 1, Appl. Environ.
fication of structural requirements for their antimicrobial
Microbiol., 77, 1966-1972, doi: 10.1128/aem.02488 10.
and cell lytic activities, J. Biol. Chem., 271, 28375-28381,
57.
Oppegard, C., Fimland, G., Anonsen, J.H., and Nissen
doi: 10.1074/jbc.271.45.28375.
Meyer, J. (2015) The pediocin PA 1 accessory protein
71.
Shin, S.Y., Park, E.J., Yang, S.T., Jung, H.J., Eom, S.H.,
ensures correct disulfide bond formation in the antimicro
Song, W.K., Kim, Y., Hahm, K.S., and Kim, J.I. (2001)
bial peptide pediocin PA 1, Biochemistry, 54, 2967-2974,
Structure activity analysis of SMAP 29, a sheep leuko
doi: 10.1021/acs.biochem.5b00164.
cytes derived antimicrobial peptide, Biochem. Biophys. Res.
58.
Quadri, L.E., Yan, L.Z., Stiles, M.E., and Vederas, J.C.
Commun., 285, 1046-1051, doi: 10.1006/bbrc.2001.5280.
(1997) Effect of amino acid substitutions on the activity of
72.
Xiao, Y., Dai, H., Bommineni, Y.R., Soulages, J.L.,
carnobacteriocin B2. Overproduction of the antimicrobial
Gong, Y. X., Prakash, O., and Zhang, G. (2006) Struc
peptide, its engineered variants, and its precursor in
ture activity relationships of fowlicidin 1, a cathelicidin
Escherichia coli, J. Biol. Chem., 272, 3384-3388, doi: 10.
antimicrobial peptide in chicken, FEBS J., 273, 2581-2593,
1074/jbc.272.6.3384.
doi: 10.1111/j.1742 4658.2006.05261.x.
59.
Miller, K.W., Schamber, R., Osmanagaoglu, O., and
73.
Zhang, Y., Zhao, H., Yu, G. Y., Liu, X. D., Shen, J. H.,
Ray, B. (1998) Isolation and characterization of pediocin
Lee, W. H., and Zhang, Y. (2010) Structure function rela
AcH chimeric protein mutants with altered bactericidal
tionship of king cobra cathelicidin, Peptides,
31,
activity, Appl. Environ. Microbiol., 64, 1997-2005.
1488-1493, doi: 10.1016/j.peptides.2010.05.005.
60.
Tominaga, T., and Hatakeyama, Y. (2006) Determination
74.
Fimland, G., Blingsmo, O.R., Sletten, K., Jung, G.,
of essential and variable residues in pediocin PA 1 by NNK
Nes, I.F., and Nissen Meyer, J. (1996) New biologically
scanning, Appl. Environ. Microbiol., 72, 1141-1147, doi: 10.
active hybrid bacteriocins constructed by combining
1128/aem.72.2.1141 1147.2006.
regions from various pediocin like bacteriocins: C termi
61.
Kanatani, K., Oshimura, M., and Sano, K.
(1995)
nal region is important for determining specificity, Appl.
Isolation and characterization of acidocin A and cloning of
Environ. Microbiol., 62, 3313-3318.
the bacteriocin gene from Lactobacillus acidophilus, Appl.
75.
Saavedra, L., Minahk, C., de Ruiz Holgado, A.P., and
Environ. Microbiol., 61, 1061-1067.
Sesma, F. (2004) Enhancement of the enterocin CRL35
62.
Stern, N.J., Svetoch, E.A., Eruslanov, B.V., Perelygin, V.V.,
activity by a synthetic peptide derived from the NH2 ter
Mitsevich, E.V., Mitsevich, I.P., Pokhilenko, V.D.,
minal sequence, Antimicrob. Agents Chemother.,
48,
Levchuk, V.P., Svetoch, O.E., and Seal, B.S.
(2006)
2778-2781, doi: 10.1128/aac.48.7.2778 2781.2004.
Isolation of a Lactobacillus salivarius strain and purifica
76.
Richard, C., Canon, R., Naghmouchi, K., Bertrand, D.,
tion of its bacteriocin, which is inhibitory to Campylobacter
Prevost, H., and Drider, D. (2006) Evidence on correlation
jejuni in the chicken gastrointestinal system, Antimicrob.
between number of disulfide bridge and toxicity of class IIa
Agents Chemother., 50, 3111-3116, doi: 10.1128/aac.
bacteriocins, Food Microbiol., 23, 175-183, doi: 10.1016/
00259 06.
j.fm.2005.02.001.
63.
Chen, Y., Ludescher, R.D., and Montville, T.J. (1997)
77.
Fimland, G., Johnsen, L., Axelsson, L., Brurberg, M.B.,
Electrostatic interactions, but not the YGNGV consensus
Nes, I.F., Eijsink, V.G., and Nissen Meyer, J. (2000) A C ter
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
631
minal disulfide bridge in pediocin like bacteriocins renders
91. Kjos, M., Salehian, Z., Nes, I.F., and Diep, D.B. (2010)
bacteriocin activity less temperature dependent and is a
An extracellular loop of the mannose phosphotransferase
major determinant of the antimicrobial spectrum, J. Bac(
system component IIC is responsible for specific targeting
teriol., 182, 2643-2648, doi: 10.1128/jb.182.9.2643
by class IIa bacteriocins, J. Bacteriol., 192, 5906-5913,
2648.2000.
doi: 10.1128/jb.00777 10.
78.
Kaur, K., Andrew, L.C., Wishart, D.S., and Vederas, J.C.
92. Barraza, D.E., Rios Colombo, N.S., Galvan, A.E., Acuna, L.,
(2004) Dynamic relationships among type IIa bacteriocins:
Minahk, C.J., Bellomio, A., and Chalon, M.C. (2017)
temperature effects on antimicrobial activity and on struc
New insights into enterocin CRL35: mechanism of action
ture of the C terminal amphipathic alpha helix as a recep
and immunity revealed by heterologous expression in
tor binding region, Biochemistry, 43, 9009-9020, doi: 10.
Escherichia coli, Mol. Microbiol., 105, 922-933, doi: 10.
1021/bi036018e.
1111/mmi.13746.
79.
Fimland, G., Eijsink, V.G.H., and Nissen Meyer, J. (2002)
93. Stevens, K.A., Sheldon, B.W., Klapes, N.A., and
Mutational analysis of the role of tryptophan residues in an
Klaenhammer, T.R. (1991) Nisin treatment for inactiva
antimicrobial peptide, Biochemistry, 41, 9508-9515, doi: 10.
tion of Salmonella species and other gram negative bacte
1021/bi025856q.
ria, Appl. Environ. Microbiol., 57, 3613-3615.
80.
Chikindas, M.L., Garcia Garcera, M.J., Driessen, A.J.,
94. Chalon, M.C., Acuna, L., Morero, R.D., Minahk, C.J.,
Ledeboer, A.M., Nissen Meyer, J., Nes, I.F., Abee, T.,
and Bellomio, A. (2012) Membrane active bacteriocins to
Konings, W.N., and Venema, G. (1993) Pediocin PA 1, a
control Salmonella in foods: are they the definite hurdle?
bacteriocin from Pediococcus acidilactici PAC1.0, forms
Food Res. Int., 45, 735-744, doi: 10.1016/j.foodres.
hydrophilic pores in the cytoplasmic membrane of target
2011.08.024.
cells, Appl. Environ. Microbiol., 59, 3577-3584.
95. Kjos, M., Nes, I.F., and Diep, D.B. (2009) Class II one
81.
Bruno, M.E., and Montville, T.J. (1993) Common mecha
peptide bacteriocins target a phylogenetically defined sub
nistic action of bacteriocins from lactic acid bacteria, Appl.
group of mannose phosphotransferase systems on sensitive
Environ. Microbiol., 59, 3003-3010.
cells, Microbiology, 155, 2949-2961, doi: 10.1099/mic.0.
82.
Minahk, C.J., Farias, M.E., Sesma, F., and Morero, R.D.
030015 0.
(2000) Effect of enterocin CRL35 on Listeria monocyto(
96. Opsata, M., Nes, I.F., and Holo, H. (2010) Class IIa bac
genes cell membrane, FEMS Microbiol. Lett., 192, 79-83,
teriocin resistance in Enterococcus faecalis V583: the man
doi: 10.1111/j.1574 6968.2000.tb09362.x.
nose PTS operon mediates global transcriptional responses,
83.
Wu, M., Maier, E., Benz, R., and Hancock, R.E. (1999)
BMC Microbiol., 10, 224, doi: 10.1186/1471 2180 10 224.
Mechanism of interaction of different classes of cationic
97. Kjos, M., Borrero, J., Opsata, M., Birri, D.J., Holo, H.,
antimicrobial peptides with planar bilayers and with the
Cintas, L.M., Snipen, L., Hernandez, P.E., Nes, I.F., and
cytoplasmic membrane of Escherichia coli, Biochemistry,
Diep, D.B. (2011) Target recognition, resistance, immuni
38, 7235-7242, doi: 10.1021/bi9826299.
ty and genome mining of class II bacteriocins from gram
84.
Minahk, C.J., Dupuy, F., and Morero, R.D. (2004)
positive bacteria, Microbiology, 157, 3256-3267, doi: 10.
Enhancement of antibiotic activity by sub lethal concen
1099/mic.0.052571 0.
trations of enterocin CRL35, J. Antimicrob. Chemother.,
98. Vadyvaloo, V., Hastings, J.W., van der Merwe, M.J., and
53, 240-246, doi: 10.1093/jac/dkh079.
Rautenbach, M. (2002) Membranes of class IIa bacteriocin
85.
Venema, K., Kok, J., Marugg, J.D., Toonen, M.Y.,
resistant Listeria monocytogenes cells contain increased
Ledeboer, A.M., Venema, G., and Chikindas, M.L. (1995)
levels of desaturated and short acyl chain phosphatidyl
Functional analysis of the pediocin operon of pediococcus
glycerols, Appl. Environ. Microbiol., 68, 5223-5230,
acidilactici PAC1.0: PedB is the immunity protein and
doi: 10.1128/aem.68.11.5223 5230.2002.
PedD is the precursor processing enzyme, Mol. Microbiol.,
99. Tessema, G.T., Moretro, T., Kohler, A., Axelsson, L., and
17, 515-522, doi: 10.1111/j.1365 2958.1995.mmi_17030515.x.
Naterstad, K. (2009) Complex phenotypic and genotypic
86.
Chen, Y., Ludescher, R.D., and Montville, T.J. (1998)
responses of Listeria monocytogenes strains exposed to the
Influence of lipid composition on pediocin PA 1 binding
class IIa bacteriocin sakacin P, Appl. Environ. Microbiol.,
to phospholipid vesicles, Appl. Environ. Microbiol., 64,
75, 6973-6980, doi: 10.1128/aem.00608 09.
3530-3532.
100. Masias, E., Dupuy, F.G., da Silva Sanches, P.R., Farizano, J.V.,
87.
Ramnath, M., Beukes, M., Tamura, K., and Hastings, J.W.
Cilli, E., Bellomio, A., Saavedra, L., and Minahk, C.
(2000) Absence of a putative mannose specific phospho
(2017) Impairment of the class IIa bacteriocin receptor
transferase system enzyme IIAB component in a leucocin
function and membrane structural changes are associated
A resistant strain of Listeria monocytogenes, as shown by
to enterocin CRL35 high resistance in Listeria monocyto(
two dimensional sodium dodecyl sulfate polyacrylamide gel
genes, Biochim. Biophys. Acta, 1861, 1770-1776, doi: 10.
electrophoresis, Appl. Environ. Microbiol., 66, 3098-3101,
1016/j.bbagen.2017.03.014.
doi: 10.1128/aem.66.7.3098 3101.2000.
101. Kundig, W., Ghosh, S., and Roseman, S.
(1964)
88.
Dalet, K., Briand, C., Cenatiempo, Y., and Hechard, Y.
Phosphate bound to histidine in a protein as an intermedi
(2000) The RpoN gene of Enterococcus faecalis directs sen
ate in a novel phospho transferase system, Proc. Natl.
sitivity to subclass IIa bacteriocins, Curr. Microbiol., 41,
Acad. Sci. USA, 52, 1067-1074, doi: 10.1073/pnas.52.
441-443, doi: 10.1007/s002840010164.
4.1067.
89.
Dalet, K., Cenatiempo, Y., Cossart, P., Hechard, Y., and
102. Postma, P.W., Lengeler, J.W., and Jacobson, G.R. (1993)
European Listeria Genome Consortium (2001) A sig
Phosphoenolpyruvate: carbohydrate phosphotransferase
ma(54) dependent PTS permease of the mannose family is
systems of bacteria, Microbiol. Rev., 57, 543-594.
responsible for sensitivity of Listeria monocytogenes to
103. Deutscher, J., Francke, C., and Postma, P.W. (2006) How
mesentericin Y105, Microbiology, 147, 3263-3269, doi: 10.
phosphotransferase system related protein phosphoryla
1099/00221287 147 12 3263.
tion regulates carbohydrate metabolism in bacteria,
90.
Diep, D.B., Skaugen, M., Salehian, Z., Holo, H., and
Microbiol. Mol. Biol. Rev., 70, 939-1031, doi: 10.1128/
Nes, I.F. (2007) Common mechanisms of target cell recog
mmbr.00024 06.
nition and immunity for class II bacteriocins, Proc. Natl.
104. Deutscher, J., Ake, F.M.D., Derkaoui, M., Zebre, A.C.,
Acad. Sci. USA, 104, 2384-2389, doi: 10.1073/pnas.
Cao, T.N., Bouraoui, H., Kentache, T., Mokhtari, A.,
0608775104.
Milohanic, E., and Joyet, P. (2014) The bacterial phospho
БИОХИМИЯ том 84 вып. 5 2019
632
БАЛАНДИН и др.
enolpyruvate: carbohydrate phosphotransferase system:
120. Fimland, G., Johnsen, L., Dalhus, B., and Nissen Meyer, J.
regulation by protein phosphorylation and phosphoryla
(2005) Pediocin like antimicrobial peptides (class IIa bac
tion dependent protein protein interactions, Microbiol. Mol.
teriocins) and their immunity proteins: biosynthesis, struc
Biol. Rev., 78, 231-256, doi: 10.1128/mmbr.00001 14.
ture, and mode of action, J. Pept. Sci., 11, 688-696, doi: 10.
105. Galinier, A., and Deutscher, J. (2017) Sophisticated regu
1002/psc.699.
lation of transcriptional factors by the bacterial phospho
121. Johnsen, L., Fimland, G., Mantzilas, D., and Nissen
enolpyruvate: sugar phosphotransferase system, J. Mol.
Meyer, J. (2004) Structure function analysis of immunity
Biol., 429, 773-789, doi: 10.1016/j.jmb.2017.02.006.
proteins of pediocin like bacteriocins: C terminal parts of
106. Saier, M.H., and Paulsen, I.T. (1999) Paralogous genes
immunity proteins are involved in specific recognition of
encoding transport proteins in microbial genomes, Res. Mic(
cognate bacteriocins, Appl. Environ. Microbiol.,
70,
robiol., 150, 689-699, doi: 10.1016/s0923 2508(99)00123 0.
2647-2652, doi: 10.1128/aem.70.5.2647 2652.2004.
107. Saier, M.H., Hvorup, R.N., and Barabote, R.D. (2005)
122. Sprules, T., Kawulka, K.E., and Vederas, J.C. (2004) NMR
Evolution of the bacterial phosphotransferase system: from
solution structure of ImB2, a protein conferring immunity
carriers and enzymes to group translocators, Biochem. Soc.
to antimicrobial activity of the type IIa bacteriocin, car
Trans., 33, 220-224, doi: 10.1042/bst0330220.
nobacteriocin B2, Biochemistry, 43, 11740-11749, doi: 10.
108. Nguyen, T.X., Yen, M. R., Barabote, R.D., and Saier, M.H.
1021/bi048854+.
(2006) Topological predictions for integral membrane per
123. Johnsen, L., Dalhus, B., Leiros, I., and Nissen Meyer, J.
meases of the phosphoenolpyruvate: sugar phosphotrans
(2005) 1.6 angstroms crystal structure of EntA im. A bac
ferase system, J. Mol. Microbiol. Biotechnol., 11, 345-360,
terial immunity protein conferring immunity to the
doi: 10.1159/000095636.
antimicrobial activity of the pediocin like bacteriocin ente
109. Cao, Y., Jin, X., Levin, E.J., Huang, H., Zong, Y., Quick, M.,
rocin A, J. Biol. Chem., 280, 19045-19050, doi: 10.2210/
Weng, J., Pan, Y., Love, J., Punta, M., Rost, B.,
pdb2bl8/pdb.
Hendrickson, W.A., Javitch, J.A., Rajashankar, K.R., and
124. Zhou, W., Wang, G., Wang, C., Ren, F., and Hao, Y.
Zhou, M. (2011) Crystal structure of a phosphorylation
(2016) Both IIC and IID components of mannose phos
coupled saccharide transporter, Nature, 473, 50-54, doi: 10.
photransferase system are involved in the specific recogni
1038/nature09939.
tion between immunity protein PedB and bacterio
110. McCoy, J.G., Ren, Z., Stanevich, V., Lee, J., Mitra, S.,
cin-receptor complex, PLoS One, 11, e0164973, doi: 10.
Levin, E.J., Poget, S., Quick, M., Im, W., and Zhou, M.
1371/journal.pone.0164973.
(2016) The structure of a sugar transporter of the glucose
125. Nissen Meyer, J., Havarstein, L.S., Holo, H., Sletten, K.,
EIIC superfamily provides insight into the elevator mecha
and Nes, I.F. (1993) Association of the lactococcin A
nism of membrane transport, Structure, 24, 956-964,
immunity factor with the cell membrane: purification and
doi: 10.1016/j.str.2016.04.003.
characterization of the immunity factor, J. Gen. Microbiol.,
111.
Ren, Z., Lee, J., Moosa, M.M., Nian, Y., Hu, L., Xu, Z.,
139, 1503-1509, doi: /10.1099/00221287 139 7 1503.
McCoy, J.G., Ferreon, A.C.M., Im, W., and Zhou, M.
126. Quadri, L.E., Sailer, M., Terebiznik, M.R., Roy, K.L.,
(2018) Structure of an EIIC sugar transporter trapped in an
Vederas, J.C., and Stiles, M.E. (1995) Characterization of
inward facing conformation, Proc. Natl. Acad. Sci. USA,
the protein conferring immunity to the antimicrobial pep
115, 5962-5967, doi: 10.1073/pnas.1800647115.
tide carnobacteriocin B2 and expression of carnobacteri
112. Luo, P., Yu, X., Wang, W., Fan, S., Li, X., and Wang, J.
ocins B2 and BM1, J. Bacteriol., 177, 1144-1151, doi: 10.
(2015) Crystal structure of a phosphorylation coupled
1128/jb.177.5.1144 1151.1995.
vitamin C transporter, Nat. Struct. Mol. Biol., 22, 238-241,
127. Murinda, S.E., Rashid, K.A., and Roberts, R.F. (2003) In
doi: 10.1038/nsmb.2975.
vitro assessment of the cytotoxicity of nisin, pediocin, and
113. Stock, J.B., Ninfa, A.J., and Stock, A.M. (1989) Protein
selected colicins on simian virus 40 transfected human
phosphorylation and regulation of adaptive responses in
colon and vero monkey kidney cells with trypan blue staining
bacteria, Microbiol. Rev., 53, 450-490.
viability assays, J. Food Prot., 66, 847-853, doi: 10.4315/
114. Fujita, Y. (2009) Carbon catabolite control of the metabolic
0362 028x 66.5.847.
network in Bacillus subtilis, Biosci. Biotechnol. Biochem.,
128. Jasniewski, J., Cailliez Grimal, C., Chevalot, I., Milliere, J. B.,
73, 245-259, doi: 10.1271/bbb.80479.
and Revol Junelles, A. M. (2009) Interactions between
115. Zuniga, M., Comas, I., Linaje, R., Monedero, V., Yebra, M.J.,
two carnobacteriocins Cbn BM1 and Cbn B2 from
Esteban, C.D., Deutscher, J., Perez Martinez, G., and
Carnobacterium maltaromaticum CP5 on target bacteria and
Gonzalez Candelas, F. (2005) Horizontal gene transfer in
Caco 2 cells, Food Chem. Toxicol., 47, 893-897, doi: 10.
the molecular evolution of mannose PTS transporters,
1016/j.fct.2009.01.025.
Mol. Biol. Evol., 22, 1673-1685, doi: 10.1093/molbev/
129. Ju, X., Chen, X., Du, L., Wu, X., Liu, F., and Yuan, J. (2015)
msi163.
Alanine scanning mutational analysis of durancin GL reveals
116. Eijsink, V.G., Skeie, M., Middelhoven, P.H., Brurberg, M.B.,
residues important for its antimicrobial activity, J. Agric.
and Nes, I.F. (1998) Comparative studies of class IIa bac
Food Chem., 63, 6402-6409, doi: 10.1021/acs.jafc.5b02114.
teriocins of lactic acid bacteria, Appl. Environ. Microbiol.,
130. Song, D.F., Li, X., Zhang, Y.H., Zhu, M.Y., and Gu, Q.
64, 3275-3281.
(2014) Mutational analysis of positively charged residues in
117. Diep, D.B., Godager, L., Brede, D., and Nes, I.F. (2006)
the N terminal region of the class IIa bacteriocin pediocin
Data mining and characterization of a novel pediocin like
PA 1, Lett. Appl. Microbiol., 58, 356-361, doi: 10.1111/
bacteriocin system from the genome of Pediococcus pen(
lam.12197.
tosaceus ATCC 25745, Microbiology, 152, 1649-1659, doi: 10.
131. Tominaga, T., and Hatakeyama, Y. (2007) Development of
1099/mic.0.28794 0.
innovative pediocin PA 1 by DNA shuffling among class
118. Erni, B. (2006) The mannose transporter complex: an open
IIa bacteriocins, Appl. Environ. Microbiol., 73, 5292-5299,
door for the macromolecular invasion of bacteria, J. Bac(
doi: 10.1128/aem.00558 07.
teriol., 188, 7036-7038, doi: 10.1128/jb.01074 06.
132. Acuna, L., Picariello, G., Sesma, F., Morero, R.D., and
119. Fimland, G., Eijsink, V.G.H., and Nissen Meyer, J. (2002)
Bellomio, A. (2012) A new hybrid bacteriocin, Ent35
Comparative studies of immunity proteins of pediocin like
MccV, displays antimicrobial activity against pathogenic
bacteriocins, Microbiology, 148, 3661-3670, doi: 10.1099/
gram positive and gram negative bacteria, FEBS Open Bio,
00221287 148 11 3661.
2, 12-19, doi: 10.1016/j.fob.2012.01.002.
БИОХИМИЯ том 84 вып. 5 2019
ПЕДИОЦИН ПОДОБНЫЕ БАКТЕРИОЦИНЫ
633
133. Johnsen, L., Fimland, G., Eijsink, V., and Nissen Meyer, J.
change the HMA rat microbiota, Int. J. Food Microbiol.,
(2000) Engineering increased stability in the antimicrobial
130, 251-257, doi: 10.1016/j.ijfoodmicro.2009.02.003.
peptide pediocin PA 1, Appl. Environ. Microbiol., 66,
137. Umu, O.C.O., Bauerl, C., Oostindjer, M., Pope, P.B.,
4798-4802, doi: 10.1128/aem.66.11.4798 4802.2000.
Hernandez, P.E., Perez Martinez, G., and Diep, D.B.
134. Quadri, L.E., Sailer, M., Roy, K.L., Vederas, J.C., and
(2016) The potential of class II bacteriocins to modify gut
Stiles, M.E. (1994) Chemical and genetic characterization
microbiota to improve host health, PLoS One, 11,
of bacteriocins produced by Carnobacterium piscicola
e0164036, doi: 10.1371/journal.pone.0164036.
LV17B, J. Biol. Chem., 269, 12204-12211.
138. Salvucci, E., Saavedra, L., Hebert, E.M., Haro, C., and
135. Jasniewski, J., Cailliez Grimal, C., Gelhaye, E., and
Sesma, F. (2012) Enterocin CRL35 inhibits Listeria mono(
Revol Junelles, A. M. (2008) Optimization of the produc
cytogenes in a murine model, Foodborne Pathog. Dis., 9,
tion and purification processes of carnobacteriocins Cbn
68-74, doi: org/10.1089/fpd.2011.0972.
BM1 and Cbn B2 from Carnobacterium maltaromaticum
139. Sosunov, V., Mischenko, V., Eruslanov, B., Svetoch, E.,
CP5 by heterologous expression in Escherichia coli, J. Mic(
Shakina, Y., Stern, N., Majorov, K., Sorokoumova, G.,
robiol. Methods, 73, 41-48, doi: 10.1016/j.mimet.2008.01.008.
Selishcheva, A., and Apt, A. (2007) Antimycobacterial
136. Bernbom, N., Jelle, B., Brogren, C. H., Vogensen, F.K.,
activity of bacteriocins and their complexes with lipo
Norrung, B., and Licht, T.R. (2009) Pediocin PA 1 and a
somes, J. Antimicrob. Chemother., 59, 919-925, doi: org/
pediocin producing Lactobacillus plantarum strain do not
10.1093/jac/dkm053.
PEDIOCIN LIKE ANTIMICROBIAL PEPTIDES
OF BACTERIA
S. V. Balandin, E. V. Sheremeteva, and T. V. Ovchinnikova*
Shemyakin-Ovchinnikov Institute of Bioorganic Chemistry,
Russian Academy of Sciences, 117997 Moscow, Russia;
E(mail: ovch@ibch.ru
Received August 6, 2018
Revised October 11, 2018
Accepted October 11, 2018
Bacteriocins are bacterial antimicrobial peptides that, unlike classical peptide antibiotics, are products of ribosomal
synthesis and usually have a narrow spectrum of antibacterial activity against species closely related to the producers.
Pediocin like bacteriocins (PLBs) belong to the class IIa of the bacteriocins of Gram positive bacteria. PLBs are
highly active against pathogenic bacteria of the genera Listeria and Enterococcus. The molecular target for PLBs is a
membrane mannose phosphotransferase complex. PLBs could be synthesized by a symbiotic human microbiota and
participate in maintaining homeostasis in various compartments of the digestive tract and on the surface of epithelial
tissues contacting with the external environment. The structure of PLBs could be used as a template for engineering
of a new group of narrow spectrum antibiotics.
Keywords: antimicrobial peptides, bacteriocins, pediocin like peptides, antibiotic resistance, mannose phosphotrans
ferase
3 БИОХИМИЯ том 84 вып. 5 2019