БИОХИМИЯ, 2019, том 84, вып. 5, с. 730 - 738
УДК 577.323.3
СТАБИЛЬНЫЕ G КВАДРУПЛЕКСЫ ПРОМОТОРОВ
ОНКОГЕНОВ ВЫЗЫВАЮТ ЗАВИСИМЫЕ ОТ ИОНОВ КАЛИЯ
ОСТАНОВКИ ТЕРМОСТАБИЛЬНОЙ ДНК ПОЛИМЕРАЗЫ
© 2019 Г.В. Чащина1,2, А.Д. Бениаминов1, Д.Н. Калюжный1*
1 Институт молекулярной биологии им. В.А. Энгельгардта РАН,
119991 Москва, Россия; электронная почта: uzhny@mail.ru
2 Московский физико*технический институт (государственный университет),
141701 Долгопрудный Московской обл., Россия
Поступила в редакцию 25.10.2018
После доработки 21.12.2018
Принята к публикации 21.12.2018
Амплификация GC богатых участков геномной ДНК может быть затруднена из за высокой стабильности
двойной спирали ДНК или образования альтернативных структур G богатой нитью ДНК. Такие последова
тельности ДНК, потенциально способные образовывать G квадруплексные (G4) структуры, широко рас
пространены в промоторах генома человека. В работе исследована эффективность ПЦР амплификации пя
ти промоторных последовательностей онкогенов человека (MYC, KIT, TERT, NRAS, KRAS). Показано, что
эффективность ДНК полимеразы в присутствии ионов калия значительно снижена. Методом удлинения
праймера локализованы места остановок ДНК полимеразы на 3' концах потенциальных G4 структур. Про
веден анализ структурных и термодинамических свойств коротких G богатых олигонуклеотидов, соответ
ствующих местам остановки ДНК полимеразы. Показано, что олигонуклеотиды образуют параллельные
G4 структуры, а также выявлена зависимость между стабильностью G4 структур и эффективностью оста
новки ДНК полимеразы. Полученные результаты демонстрируют метод детекции G4 структур в протяженных
геномных последовательностях, а также проясняют механизм ингибирования ДНК полимеразы на G бога
тых участках ДНК.
КЛЮЧЕВЫЕ СЛОВА: ДНК, G квадруплекс, промоторные последовательности, ПЦР, ДНК полимераза.
DOI: 10.1134/S0320972519050105
Помимо канонической B формы, молекула
Анализ G богатых областей генома имеет
ДНК может образовывать множество альтерна
важное практическое значение для скрининга и
тивных структур, примером которых являются
диагностики некоторых генетических заболева
G квадруплексные (G4) структуры. Биоинфор
ний [10]. Однако амплификация и секвенирова
матический анализ показал, что в геноме чело
ние G богатых участков ДНК представляет со
века присутствует большое количество высоко
бой серьезную проблему из за образования вто
консервативных гуаниновых последовательнос
ричных структур, которые могут ингибировать
тей, обладающих потенциалом для формирова
ДНК полимеразу и приводить к образованию
ния G4 структур [1-3]. Предполагается, что
укороченного ПЦР продукта или к его отсут
G4 структуры играют важную роль в биологи
ствию. Для некоторых участков генома показа
ческих процессах: репликации, регуляции транс
но подавление синтеза ДНК только в присут
крипции и др. [4]. Недавние исследования по
ствии ионов калия и при использовании именно
визуализации G4 структур в клетках показали
G богатой цепи в качестве матрицы [11].
их существование и распространенность в раз
Выявление мест остановок ДНК полимеразы
личных участках хромосом [5]. Повышенный
может быть удобным подходом к обнаружению
уровень квадруплексных структур, обнаружен
альтернативных структур ДНК, в т.ч. G4 струк
ный окрашиванием G4 специфичными антите
тур, в геномной ДНК [12]. В 1999 г. для отбора
лами, характерен для ряда опухолевых клеток [6].
соединений, взаимодействующих с G4 ДНК,
G4 структуры рассматриваются в качестве по
Han et al. предложили метод, основанный на эф
тенциальных молекулярных мишеней для про
фекте остановки ДНК полимеразы на G бога
тивоопухолевой терапии [7-9].
той матрице из за стабилизации G4 структуры.
Так, соединение BSU 1051 приводит к останов
* Адресат для корреспонденции.
ке синтеза ДНК в присутствии ионов калия пу
730
G4 ДНК ВЫЗЫВАЕТ ОСТАНОВКИ ДНК ПОЛИМЕРАЗЫ
731
тем стабилизации внутримолекулярных G4 струк
анализировали в УФ свете, используя трансил
тур [13].
люминатор GelDoc™ XR+ («Bio Rad», США).
Целью данной работы являлся анализ пози
Удлинение флуоресцентно меченного праймера.
ций остановок термофильной ДНК полимера
Реакцию удлинения праймера проводили в 25 мкл
зы в присутствии ионов калия для пяти промо
смеси, содержавшей 20 мМ Tris HCl, pH 9,5;
торных последовательностей онкогенов челове
2,5 мМ MgCl2; 5% DMSO; 8% PEG 200; 20 мМ
ка (MYC, KIT, TERT, NRAS, KRAS) и изучение
CsCl; 0,1 мМ dNTP; 0,5 ед активности Taq ДНК
связи эффективности остановки ДНК полиме
полимеразы Encyclo; 2 нМ ДНК матрицу; 100 нМ
разы со стабильностью G4 структур.
флуоресцентно меченный праймер. Концентра
цию KCl варьировали от 0 до 50 мМ.
Реакционная смесь для секвенирования по
МЕТОДЫ ИССЛЕДОВАНИЯ
Сэнгеру (25 мкл) содержала: 20 мМ Tris HCl,
pH 9,5; 2,5 мМ MgCl2; 5% DMSO; 8% PEG 200;
Олигонуклеотиды. Модельные олигонуклео
20 мМ CsCl; 2 нМ ПЦР продукт; 0,1 мкМ флуо
тиды и праймеры для ПЦР были синтезированы
ресцентно меченный праймер; 0,1 мМ dNTP;
в ЗАО «Евроген» (Россия), флуоресцентно ме
0,5 ед активности SNP полимеразы (ЗАО «Евро
ченные праймеры - в ООО «ДНК синтез» (Рос
ген», Россия). Для получения четырех секвени
сия). Последовательности праймеров представ
рующих дорожек геля ddG, ddA, ddT и ddC до
лены в табл. 1.
бавляли в указанную смесь до концентрации
ПЦР амплификация фрагментов ДНК. Амп
0,1; 1; 0,1 и 0,01 мкМ соответственно. Обозначе
лификацию фрагментов ДНК in vitro осущест
ние дорожек на секвенирующем геле соответ
вляли при помощи ПЦР с использованием Taq
ствует ddNTP, добавленному в реакционную
ДНК полимеразы Encyclo (ЗАО «Евроген», Рос
смесь. Полученные реакционные смеси инку
сия). ПЦР проводили в 25 мкл реакционной
бировали при 95 °C в течение 3 мин, а затем про
смеси, содержавшей 60 мМ Tris HCl, pH 9,5; 20 мМ
водили 20 циклов амплификации: денатурация
CsCl; 2,5 мМ МgCl2; 5% DMSO; 0,25 мМ dNTP;
при 95 °C - 30 с; отжиг - 30 с; удлинение прай
0,5 мкM праймер; 1 ед активности Taq ДНК по
мера при 72 °C - 30 с. Температуры отжига прай
лимеразы Encyclo. В качестве матрицы исполь
меров подбирали при помощи программы
зовали 100 нг геномной ДНК из культуры клеток
человека Raji (ЗАО «Евроген», Россия). Реакци
ровали опытным путем.
онную смесь инкубировали при 95 °C в течение
Образцы осаждали добавлением 200 мкл 0,3 М
3 мин, а затем проводили 30 циклов ПЦР по
ацетата натрия (pH 5,3) и 600 мкл 96% ного эта
программе: 95 °C - 30 с, 60 °C - 30 с, 72 °C - 30 с;
нола с последующим центрифугированием в те
терминальная элонгация - 3 мин при 72 °С.
чение 10 мин при 14 000 об/мин. После промы
Продукты реакции разделяли в 2% ном агароз
вания 70% ным этанолом к образцам добавляли
ном геле. После электрофореза гель окрашива
раствор, содержавший 30 мМ натрий фосфатный
ли в растворе бромистого этидия (1,5 мкг/мл) и
буфер, pH 7,8; 80% ный формамид; 0,025% ный
Таблица 1. Праймеры, использованные для анализа промоторных участков онкогенов человека
Последовательности праймеров
Последовательности флуоресцентно меченных
Название гена
для амплификации промоторных участков
праймеров для локализации мест остановки
генов (5' 3')
ДНК полимеразы (5' 3')
MYC
F: d(GAGGAGCAGCAGAGAAAGGG)
FAM d(AGTGCTCGGCTGCCCGGCTG)
R: d(TCCCTCCGTTCTTTTTCCCG)
KIT
F: d(GTGGAGAGAGAAAGGGGCTC)
FAM d(CGCCGGCCACGCCCCT)
R: d(AAGCAGTAGGAGCAGAACGC)
TERT
F: d(CAGCGCTGCCTGAAACTC)
FAM d(CTTCCAGCTCCGCCTCCTCC)
R: d(GGCCGATTCGACCTCTCT)
NRAS
F: d(AAATGTTGGAGACCCCGGAA)
FAM d(CGAACCACGAGTCATGCG)
R: d(TCTCTGGGTAAAGAGGCCGT)
KRAS
F: d(AGAGCTATCGATGCGTTCCG)
FAM d(TCTCCCCGCCGGCGC)
R: d(TTCGCAGCTTCTCTGTGGAG)
БИОХИМИЯ том 84 вып. 5 2019
9*
732
ЧАЩИНА и др.
бромфеноловый синий и 0,025% ный ксилен
Все выбранные промоторные области содер
цианол, денатурировали в течение 5 мин при 95 °С
жат последовательности, способные образовы
и наносили на 10% ный ПААГ (акриламид : бис
вать G4 структуры ДНК. Известно, что стабиль
акриламид 19 : 1), содержавший 7 М мочевину
ность G4 структур зависит от присутствия од
и 1× ТВЕ буфер. Гель визуализировали на флуо
новалентных ионов: ионы калия сильно стаби
ресцентном сканере Typhoon 9500 («GE Health
лизируют G4 структуры, в то время как ионы
care», США).
цезия и лития дестабилизируют их. Большин
Подвижность олигонуклеотидов в ПААГ. От
ство буферов для термофильных ДНК полимераз
жиг модельных олигонуклеотидов (4 мкM) для
содержат соли калия в концентрациях 20-50 мМ.
формирования квадруплексных структур прово
Также известно, что активность ДНК полиме
дили в буфере (20 мМ Tris HCl, pH 8,0; 2,5 мМ
раз часто снижается при увеличении концентра
MgCl2; 20 мМ CsCl; 7,5 мМ KCl) путем нагрева
ции ионов калия [15, 16]. Ранее было показано,
ния при 95 °С в течение 5 мин и быстрого охлаж
что ионы цезия в значительно меньшей степени
дения во льду. Образцы наносили на 8% ный
влияют на активность ДНК полимеразы, чем
ПААГ (акриламид : бисакриламид 19 : 1), содер
ионы лития [17]. Подбирая оптимальные усло
жавший 20 мМ KCl и 0,5× ТВЕ буфер. Электро
вия для амплификации, было решено заменить
форез проводили в электродном 0,5× ТВЕ буфе
ионы калия на другие одновалентные противо
ре с 20 мМ KCl при 12 В. После электрофореза
ионы. Оказалось, что замена KCl на CsCl позво
гель окрашивали красителем SYBR Gold («Invit
лила получить более высокий выход ПЦР про
rogen», США) и сканировали на флуоресцент
дуктов. При помощи ПЦР в присутствии 20 мМ
ном сканере Typhoon 9500 («GE Healthcare»,
CsCl были наработаны участки промоторов пя
США).
ти онкогенов.
Круговой дихроизм (КД). Спектры КД запи
Известно, что G4 структуры могут оказы
сывали на спектрополяриметре Jasco J715
вать влияние на эффективность ПЦР. Проведе
(«Jasco», Япония), оснащенном термостатируе
но сравнение эффективности амплификации
мой ячейкой Пельтье, с использованием квар
фрагментов, содержащих и не содержащих
цевой кюветы. Длина оптического пути - 1 см,
квадруплексные последовательности, при по
скорость сканирования - 100 нм/мин, время
вышении концентрации KCl в реакционной
отклика - 1 с. Данные КД получали усреднени
смеси (рис. 1).
ем трех сканирований. Спектры регистрировали
Была обнаружена тенденция к уменьшению
при 25 °C в диапазоне длин волн 220-320 нм.
количества полноразмерного ПЦР продукта
Температурную зависимость КД исследовали в
при увеличении концентрации ионов калия в
диапазоне температур 20-90 °C. Данные получе
реакционной смеси. Данный эффект может
ны для 4 мкМ олигонуклеотидов в буфере (2,5 мМ
быть обусловлен несколькими причинами: сни
MgCl2; 20 мМ Tris HCl, pH 8,0; 20 мМ CsCl) и
жением активности ДНК полимеразы в неопти
при добавлении 20 мМ KCl.
мальном буфере, увеличением стабильности
двойной спирали при увеличении ионной силы,
а также остановками ДНК полимеразы на квад
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
руплексных участках. Для участка промоторной
области гена TERT наблюдалось значительное
Квадруплексные последовательности ДНК
снижение выхода ПЦР продукта уже при кон
уменьшают эффективность ПЦР в зависимости от
центрациях 20-30 мМ KCl, в то время как уро
концентрации ионов калия. Известно, что потен
вень амплификации участка, не содержащего
циальные квадруплексные последовательности
квадруплексных последовательностей, незначи
широко распространены в промоторах генома
тельно снижался, по всей видимости, из за сни
человека и могут быть вовлечены в регуляцию
жения активности ДНК полимеразы в растворе
экспрессии генов [7, 14]. ПЦР амплификация
с высокой ионной силой [15, 16]. Таким обра
таких G богатых промоторных участков генома
зом, было обнаружено зависимое от ионов ка
в стандартных для ДНК полимераз буферах час
лия значительное снижение эффективности
то проходила с крайне низким выходом ПЦР
амплификации участков ДНК, содержащих
продуктов, что подтолкнуло нас к проведению
квадруплексные последовательности.
данного исследования. Пять участков генома,
Локализация мест остановки ДНК полимеразы
соответствующих промоторным областям онко
в зависимости от концентрации ионов калия. Что
генов человека (MYC, KIT, TERT, NRAS, KRAS),
бы показать, что квадруплексные структуры, ста
были выбраны для исследования причин низ
билизированные ионами калия, могут препят
кой эффективности амплификации и поиска
ствовать работе ДНК полимеразы, был проведен
способов преодоления данной проблемы.
анализ продуктов удлинения флуоресцентно
БИОХИМИЯ том 84 вып. 5 2019
G4 ДНК ВЫЗЫВАЕТ ОСТАНОВКИ ДНК ПОЛИМЕРАЗЫ
733
п.н.
TERT
noG4
5000
2000
850
400
100
1
2
3
4
1
2
3
4
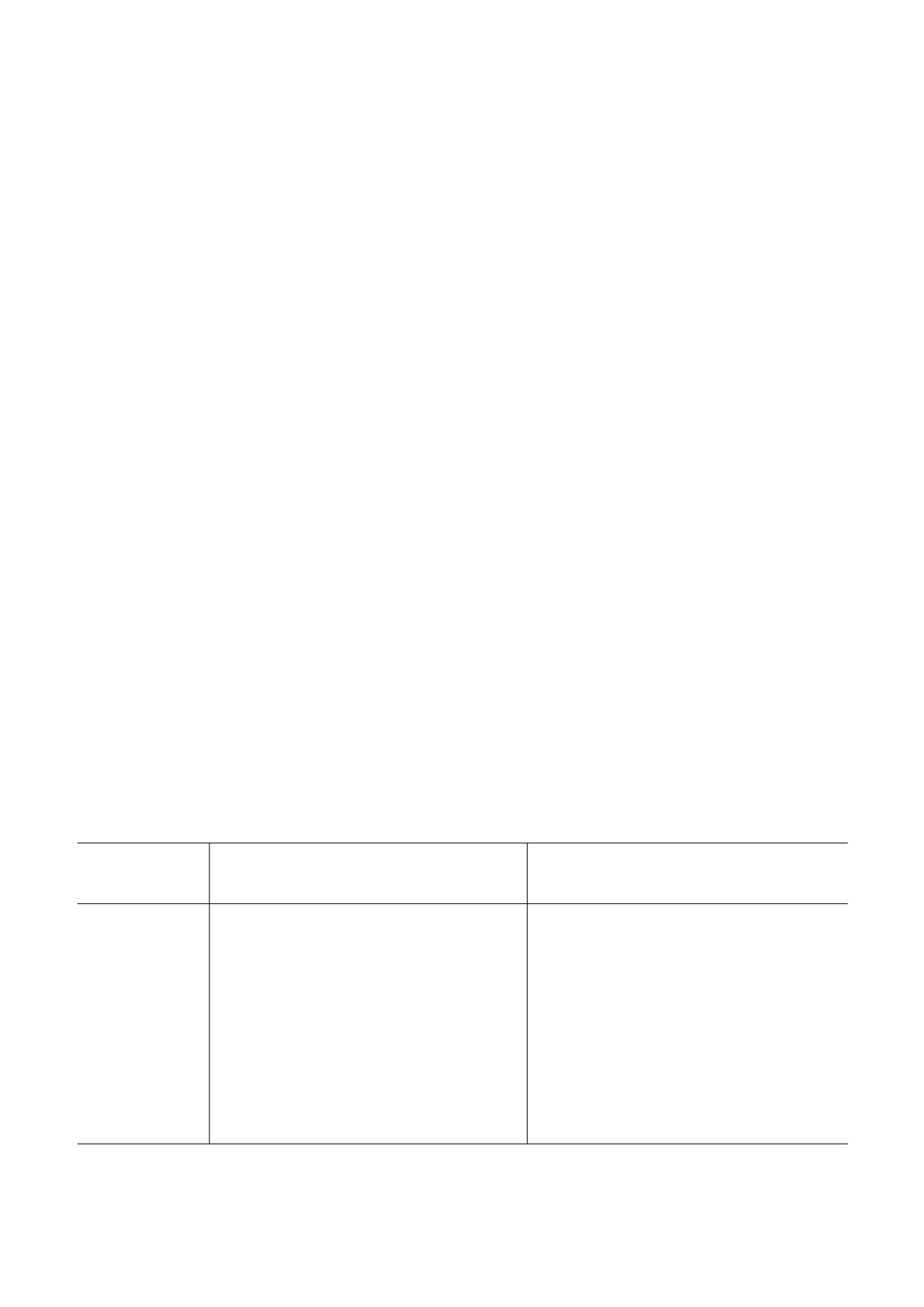
Рис. 1. Эффективность ПЦР амплификации потенциальной квадруплексной последовательности промотора гена тело
меразы человека TERT (378 п.н.) и контрольной последовательности noG4 (486 п.н.), не содержащей квадруплексных по
следовательностей, с использованием Taq ДНК полимеразы Encyclo («Евроген», Россия) при увеличении концентрации
ионов калия в реакционном буфере: дорожки 1-4 - 10, 20, 30 и 40 мМ KCl соответственно
меченного праймера. Праймер выбирали таким
при различных концентрациях KCl (0-50 мM)
образом, чтобы матричная нить содержала G бо
на матрице ДНК, полученной с помощью ПЦР
гатые потенциальные квадруплексные участки
и соответствующей участкам промоторных об
(табл. 1). Длину продуктов удлинения анализи
ластей онкогенов.
ровали в денатурирующем ПААГ, сравнивая с
Прямая зависимость эффективности оста
нуклеотидной последовательностью, прочитан
новки ДНК полимеразы от концентрации ио
ной с того же праймера (рис. 2). Удлинение флуо
нов калия обнаружена для последовательностей
ресцентно меченного праймера было проведено
промоторных участков всех пяти генов. Для
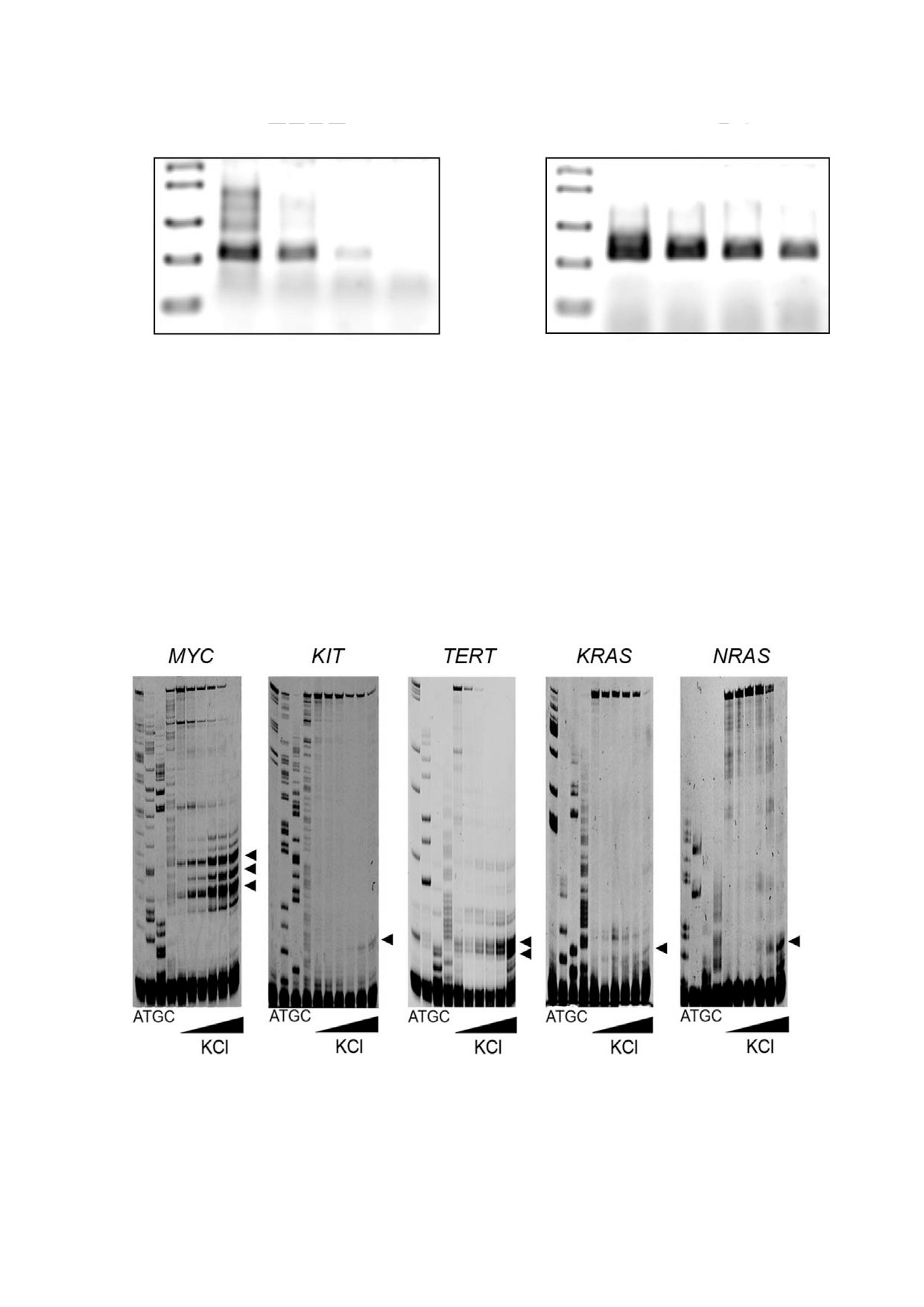
Рис. 2. Продукты удлинения флуоресцентно меченного праймера на квадруплексных последовательностях в промотор
ных областях пяти онкогенов человека (MYC, KIT, TERT, NRAS, KRAS) при увеличении концентрации ионов калия: 0, 2,
5, 10, 20 и 50 мМ. Для определения точных мест остановок ДНК полимеразы проводили секвенирование ДНК методом
Сэнгера (первые четыре дорожки). Профиль получен в денатурирующем 10% ном ПААГ. Места остановки ДНК полиме
разы отмечены черными треугольниками
БИОХИМИЯ том 84 вып. 5 2019
734
ЧАЩИНА и др.
последовательностей генов MYC, NRAS и TERT
личных квадруплексных структур, при этом воз
наблюдаются несколько остановок, для которых
можность формирования одной из них исклю
зависимость от концентрации ионов калия оче
чает формирование других. Каждый G богатый
видна и ярко выражена: укороченные вслед
участок может иметь равные возможности для
ствие остановки ДНК полимеразы ПЦР про
формирования G квадруплексной структуры.
дукты появились даже при минимальной кон
Для проверки данной гипотезы было синте
центрации ионов калия (2 мМ). Для последова
зировано несколько модельных олигонуклеоти
тельностей генов KRAS и KIT также выявлены
дов, 3' конец которых совпадает с местом оста
позиции остановок ДНК полимеразы, однако
новки ДНК полимеразы, а их последователь
эффект зависимости от ионов калия выражен
ности содержат только четыре гуаниновых бло
слабее, т.е. позиции остановок обнаруживаются
ка. Последовательности олигонуклеотидов, ис
при более высоких концентрациях ионов калия.
пользуемых для изучения межмолекулярных аг
Это может быть связано с тем, что потенциаль
регатов квадруплексных структур, а также топо
ные квадруплексные участки в промоторах этих
логии и стабильности квадруплексов методом
генов формируют менее стабильные G квадруп
КД, приведены на рис. 3. Квадруплексные
лексные структуры.
структуры, образованные последовательностя
Места остановок ДНК полимеразы были со
ми, которые оканчиваются на повторяющиеся
отнесены с позициями квадруплексных после
остатки гуанозина, склонны к агрегации. Для
довательностей ДНК. Как видно из рис. 3, места
уменьшения межмолекулярной агрегации к
остановок совпадают с 3' концом последова
последовательностям олигонуклеотидов на 5' и
тельности, способной образовывать G4 струк
3' концы были добавлены динуклеотиды ТT.
туру.
Известно, что внутримолекулярные G квад
Для некоторых последовательностей харак
руплексные структуры в неденатурирующем
терно обнаружение нескольких позиций оста
ПААГ мигрируют быстрее, чем однонитевая
новок ДНК полимеразы внутри G богатых участ
ДНК той же длины. При помощи электрофоре
ков. Было замечено, что более длинные G бога
за в ПААГ олигонуклеотиды были проверены на
тые повторы могут формировать несколько раз
предмет образования межмолекулярных агрега
Рис. 3. Локализация остановок ДНК полимеразы на промоторных последовательностях пяти онкогенов человека (MYC,
KIT, TERT, NRAS, KRAS). Места остановок ДНК полимеразы (отмечены черными треугольниками) соотнесены с нуклео
тидными последовательностями исследуемых участков ДНК. Потенциальная квадруплексная последовательность подчерк
нута и выделена полужирным шрифтом. Последовательности модельных олигонуклеотидов, используемых для подтверж
дения структуры, приведены под нуклеотидными последовательностями промоторов. Для уменьшения межмолекуляр
ной агрегации к последовательностям модельных олигонуклеотидов на 5' и 3' концы были добавлены динуклеотиды ТT
БИОХИМИЯ том 84 вып. 5 2019
G4 ДНК ВЫЗЫВАЕТ ОСТАНОВКИ ДНК ПОЛИМЕРАЗЫ
735
тов (рис. 4). В качестве контролей были взяты
тельную полосу с максимумом при 265 нм и от
олигонуклеотид TQ24 d(TTAGGGTTAGGGT
рицательную с максимумом при 240 нм, что ха
TAGGGTTAGGG), формирующий квадруп
рактеризует образование параллельных G квад
лекс, и его мутантная форма TelM d(TTAGGGT
руплексов. При наличии в буфере ионов цезия
TAGAGTTAGGGTTAGGG) c заменой в одном
спектры КД характеризуются меньшей ампли
нуклеотиде (подчеркнута), которая препятству
тудой, что может говорить о неполном форми
ет образованию квадруплекса.
ровании G4 структуры или о меньшей ее ста
Сравнение подвижности олигонуклеотидов
бильности. Для некоторых олигонуклеотидов
в геле с подвижностью контрольной пары
(Q myc2, Q myc3, Q nras, Q tert1) наблюдался
TQ24-TelM позволяет предположить, что все
небольшой положительный пик при 295 нм, что
модельные олигонуклеотиды образуют внутри
может свидетельствовать о присутствии конфор
молекулярные G4 структуры. Можно заметить
маций, альтернативных параллельным G4 струк
небольшую долю полос с меньшей подвиж
турам. В данном случае возможно присутствие
ностью, которые могут соответствовать межмо
небольшого количества антипараллельных или
лекулярным комплексам. Доля таких межмоле
смешанных G квадруплексов.
кулярных агрегатов составляет не более ~5-10%
Для определения термостабильности обра
для каждой олигонуклеотидной модели. Таким
зованных структур была получена температур
образом, было установлено, что выбранные
ная зависимость амплитуды КД при 265 нм. На
олигонуклеотиды образуют главным образом
рис. 5, б, г приведены данные для олигонуклео
внутримолекулярные структуры.
тидов Q myc1 и Q tert1 (аналогичные измене
Вероятность остановки ДНК полимеразы за
ния были выявлены для всех олигонуклеоти
висит от стабильности квадруплексной структуры.
дов). Падение амплитуды при 265 нм характери
Для определения конформации и термодинами
зует переход из G4 конформации к денатуриро
ческой стабильности структур, образованных
ванной форме олигонуклеотида. По положению
модельными олигонуклеотидами, был применен
полуперехода между этими формами можно
метод кругового дихроизма, являющийся высо
оценить температуру плавления G4 структур
кочувствительным к структурным изменениям в
(табл. 2). Как и ожидалось, термостабильность
нуклеиновых кислотах. На рис. 5, а, в приведе
G4 структур в присутствии ионов калия значи
ны спектры КД для олигонуклеотидов Q myc1 и
тельно выше, чем в присутствии ионов цезия.
Q tert1 в присутствии ионов цезия или ионов
Представленные в табл. 2 данные свидетель
калия. Для остальных олигонуклеотидов изме
ствуют о том, что температура плавления для
нения в спектрах КД имели схожий характер
модельных олигонуклеотидов близка к темпера
(данные не приведены). Спектры КД, получен
туре, при которой работает ДНК полимераза в
ные в растворе с ионами калия, имеют положи
линейной ПЦР (72 °С). В связи с этим для каж
дой олигонуклеотидной модели была оценена
доля нативных (неденатурированных) структур
при 72 °С. Оказалось, что эффективность остано
вок ДНК полимеразы связана с долей G4 струк
тур при температуре проведения линейной ПЦР.
Таблица 2. Результаты анализа температурной зависимости
кругового дихроизма изученных модельных олигонуклео
тидов в присутствии 20 мМ ионов калия
Модельные
Температура
Доля неденатуриро
олигонуклео
плавления,
ванных G4 структур
тиды
°С
при 72 °С, %
Q myc1
80
77
Q myc2
68
28
Q myc3
75
52
Q kit
68
38
Q tert1
74
60
Q tert2
66
24
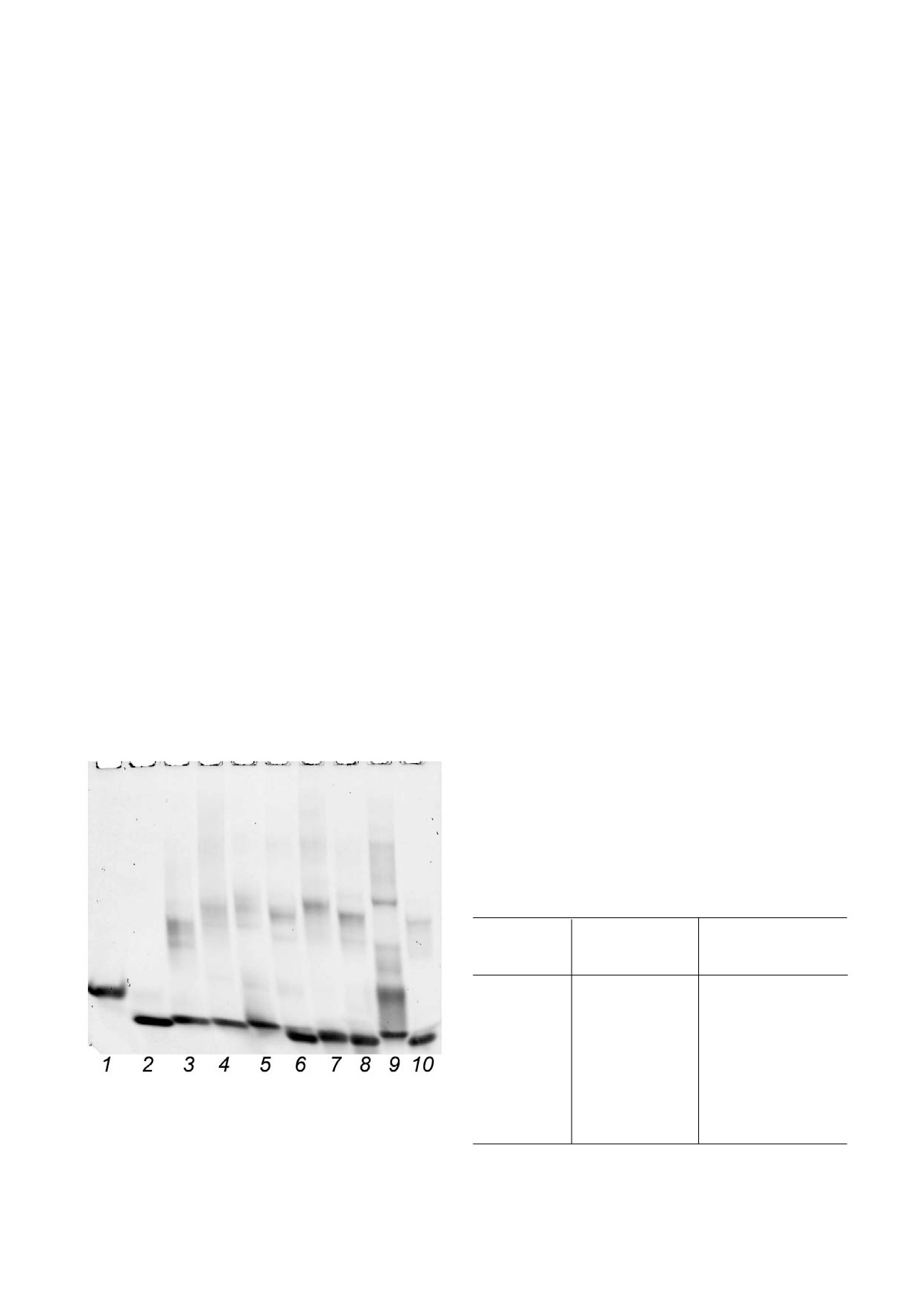
Рис. 4. Подвижность G4 структур, образованных модель
Q nras
59
14
ными олигонуклеотидами в нативных условиях: 1 - TelM,
2 - TQ24, 3 - Q myc1, 4 - Q myc2, 5 - Q myc3, 6 - Q kit,
Q kras
54
5
7 - Q tert1, 8 - Q tert2, 9 - Q kras, 10 - Q nras
БИОХИМИЯ том 84 вып. 5 2019
736
ЧАЩИНА и др.
Результаты термодинамического плавления
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
подтверждают высказанное нами ранее предпо
ложение о том, что последовательности G квад
В данном исследовании было определено
руплексных участков в промоторах генов MYC,
положение G квадруплексных структур в про
NRAS и TERT образуют более устойчивые или
моторных участках пяти онкогенов человека.
стабильные структуры, чем в промоторах генов
Большинство известных G4 структур было изу
KRAS и KIT. Нами впервые показано, что эф
чено на коротких модельных одно или двухце
фективность остановки ДНК полимеразы на
почечных последовательностях ДНК. Особен
G богатых участках промоторов онкогенов за
ность данной работы состоит в том, что нами
висит от стабильности G4 структур.
были использованы природные длинные двух
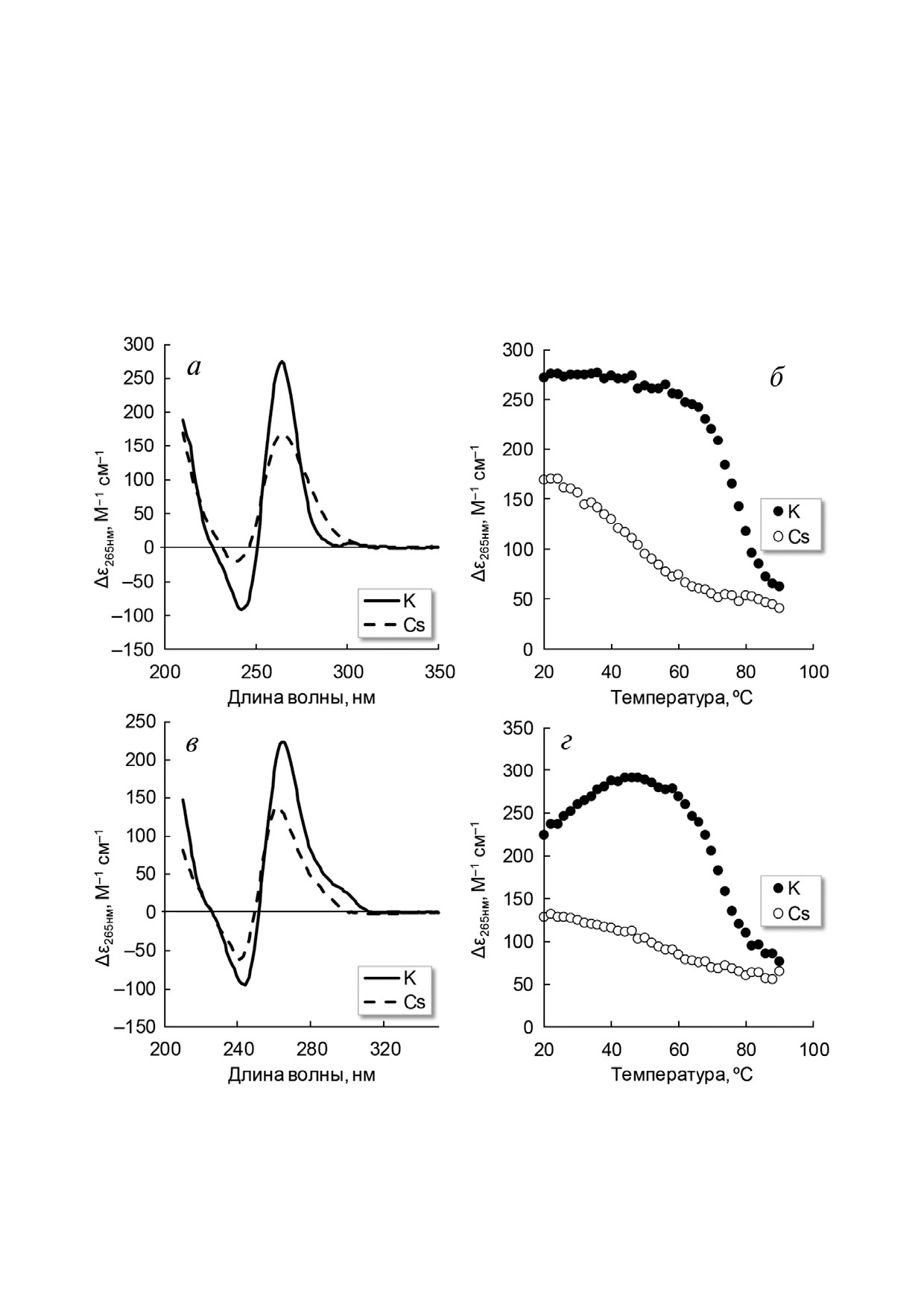
Рис. 5. Спектры КД и температурная зависимость амплитуды КД модельных олигонуклеотидов Q myc1 (а, б) и Q tert1 (в, г)
при длине волны 265 нм в присутствии 20 мМ ионов калия (сплошная кривая и заштрихованные кружки) и 20 мМ ионов
цезия (пунктирная кривая и незаштрихованные кружки). Концентрация олигонуклеотидов - 4 мкМ
БИОХИМИЯ том 84 вып. 5 2019
G4 ДНК ВЫЗЫВАЕТ ОСТАНОВКИ ДНК ПОЛИМЕРАЗЫ
737
цепочечные участки ДНК из промоторов онко
на KRAS была ранее исследована при помощи
генов человека (MYC, NRAS, TERT, KRAS, KIT),
кругового дихроизма и фотохимического зонди
содержащие квадруплексные последовательнос
рования G4 ДНК [22], и было показано участие
ти. Продемонстрировано, что остановки ДНК
данной альтернативной структуры ДНК в регу
полимеразы при продвижении по G богатой
ляции экспрессии гена KRAS.
нити происходят на 3' концах квадруплексных
ДНК квадруплекс в промоторе гена NRAS
последовательностей. Это позволяет предполо
ранее детектирован не был, однако была показа
жить, что остановки ДНК полимеразы связаны
на возможность формирования РНК квадруп
с появлением препятствия в результате образо
лекса, который находится в 5' некодируемой об
вания термодинамически устойчивой G4 струк
ласти гена NRAS [23]. Обнаруженная нами пози
туры. Обнаруженная нами связь между эффек
ция остановки ДНК полимеразы соответствует
тивностью возникновения остановок ДНК по
положению хорошо изученного РНК квадруп
лимеразы и термостабильностью квадруплекса
лекса гена NRAS. Таким образом, используемый
подтверждает это предположение. Таким обра
метод остановки ДНК полимеразы позволяет
зом, методом остановки ДНК полимеразы в
детектировать не только ДНК квадруплексы, но
присутствии ионов калия нами локализованы
и указывать на наличие РНК квадруплексов в
G4 структуры, способные образовываться в
транскрипте данного участка.
промоторах онкогенов человека.
При помощи метода удлинения флуорес
Полученные результаты хорошо согласуются
центно меченного праймера было показано, что
с некоторыми данными, описанными в литера
квадруплексные структуры, стабилизированные
туре. Так, подтверждается модель G4 структуры
ионами калия, могут препятствовать работе
в промоторе TERT, которая была предложена
ДНК полимеразы. Впервые продемонстрирова
Palumbo et al. [18]. Позже данная модель была
но, что эффективность остановки ДНК поли
улучшена Chaires et al. [19]. Один из самых ста
меразы на квадруплексных участках коррелиру
бильных модельных олигонуклеотидов Q myc1
ет со стабильностью соответствующей квадруп
совпадает с 3' концом хорошо изученной после
лексной структуры. Более стабильные квадруп
довательности pu27 (5' TGGGAGGGTGGGGA
лексы ингибируют амплификацию ДНК более
GGGTGGGG 3') промотора гена MYC [20]. Ме
эффективно. Данный метод можно использо
тод остановки ДНК полимеразы позволил об
вать для детекции не только ДНК квадруплек
наружить большее число G4 структур в промо
сов, но и РНК квадруплексных структур.
торе MYC ближе к старту транскрипции гена.
Согласно нашим результатам, выявленные
G4 структуры являются менее стабильными.
Финансирование. Работа выполнена при под
В промоторе гена KIT известны два потенциаль
держке Российского научного фонда (проект
ных квадруплексных участка c kit1 и c kit2.
№ 16 14 10396).
Структура, образованная последовательностью
Конфликт интересов. Авторы заявляют об от
c kit2, полностью согласуется с полученными
сутствии конфликта интересов.
нами результатами. Для данной последователь
Соблюдение этических норм. Настоящая
ности параллельная квадруплексная структура
статья не содержит описания каких либо иссле
была установлена ранее методом ЯМР [21]. Об
дований с участием людей и использованием
наруженная нами G4 структура в промоторе ге
животных в качестве объектов исследований.
СПИСОК ЛИТЕРАТУРЫ
1.
Lam, E.Y.N., Beraldi, D., Tannahill, D., and
4.
Bochman, M.L., Paeschke, K., and Zakian, V.A. (2012)
Balasubramanian, S. (2013) G Quadruplex structures are
DNA secondary structures: stability and function of
stable and detectable in human genomic DNA, Nat.
G quadruplex structures, Nat. Rev. Genet., 13, 770-780,
Commun., 4, 1796, doi: 10.1038/ncomms2792.
doi: 10.1038/nrg3296.
2.
Todd, A.K., Johnston, M., and Neidle, S. (2005) Highly
5.
Biffi, G., Tannahill, D., McCafferty, J., and Balasubrama
prevalent putative quadruplex sequence motifs in human
nian, S. (2013) Quantitative visualization of DNA G quad
DNA, Nucleic Acids Res., 33, 2901-2907, doi: 10.1093/
ruplex structures in human cells, Nat. Chem., 5, 182-186,
nar/gki553.
doi: 10.1038/nchem.1548.
3.
Verma, A., Halder, K., Halder, R., Yadav, V.K., Rawal, P.,
6.
Biffi, G., Tannahill, D., Miller, J., Howat, W.J., and Bala
Thakur, R.K., Mohd, F., Sharma, A., and Chowdhury, S.
subramanian, S. (2014) Elevated levels of G quadruplex
(2008) Genome wide computational and expression
formation in human stomach and liver cancer tissues, PLoS
analyses reveal G quadruplex DNA motifs as conserved
One, 9, e102711, doi: 10.1371/journal.pone.0102711.
cis regulatory elements in human and related species,
7.
Balasubramanian, S., Hurley, L.H., and Neidle, S. (2011)
J. Med. Chem., 51, 5641-5649, doi: 10.1021/jm800448a.
Targeting G quadruplexes in gene promoters: a novel anti
БИОХИМИЯ том 84 вып. 5 2019
738
ЧАЩИНА и др.
cancer strategy? Nat. Rev. Drug Discov., 10, 261-275, doi: 10.
16. Abu Al Soud, W., and Radstrom, P. (1998) Capacity of
1038/nrd3428.
nine thermostable DNA polymerases to mediate DNA
8. Tauchi, T., Shin ya, K., Sashida, G., Sumi, M., Okabe, S.,
amplification in the presence of PCR inhibiting samples,
Ohyashiki, J.H., and Ohyashiki, K. (2006) Telomerase
Appl. Environ. Microbiol., 64, 3748-3753.
inhibition with a novel G quadruplex interactive agent,
17. Ramos Aleman, F., Gonzalez Jasso, E., and Pless, R.C.
telomestatin: in vitro and in vivo studies in acute leukemia,
(2018) Use of alternative alkali chlorides in RT and PCR of
Oncogene, 25, 5719-5725, doi: 10.1038/sj.onc.1209577.
polynucleotides containing G quadruplex structures, Anal.
9. Ilyinsky, N.S., Varizhuk, A.M., Beniaminov, A.D., Puza
Biochem., 543, 43-50, doi: 10.1016/j.ab.2017.11.021.
nov, M.A., Shchyolkina, A.K., and Kaluzhny, D.N. (2014)
18. Palumbo, S.L., Ebbinghaus, S.W., and Hurley, L.H.
G quadruplex ligands: mechanisms of anticancer action
(2009) Formation of a unique end to end stacked pair of
and target binding, Mol. Biol., 48, 778-794, doi: 10.1134/
G quadruplexes in the hTERT core promoter with impli
s0026893314060077.
cations for inhibition of telomerase by G quadruplex
10. Haeusler, A.R., Donnelly, C.J., Periz, G., Simko, E.A.J.,
interactive ligands, J. Am. Chem. Soc., 131, 10878-10891,
Shaw, P.G., Kim, M. S., Maragakis, N.J., Troncoso, J.C.,
doi: 10.1021/ja902281d.
Pandey, A., Sattler, R., Rothstein, J.D., and Wang, J.
19. Chaires, J.B., Trent, J.O., Gray, R.D., Dean, W.L.,
(2014) C9orf72 nucleotide repeat structures initiate molecu
Buscaglia, R., Thomas, S.D., and Miller, D.M. (2014) An
lar cascades of disease, Nature, 507, 195-200, doi: 10.
improved model for the hTERT promoter quadruplex,
1038/nature13124.
PLoS One, 9, e115580, doi: 10.1371/journal.pone.0115580.
11. Woodford, K.J., Howell, R.M., and Usdin, K. (1994)
20. Phan, A.T., Modi, Y.S., and Patel, D.J. (2004) Propeller
A novel K+ dependent DNA synthesis arrest site in a com
type parallel stranded G quadruplexes in the human c*myc
monly occurring sequence motif in eukaryotes, J. Biol.
promoter, J. Am. Chem. Soc., 126, 8710-8716, doi: 10.
Chem., 269, 27029-27035.
1021/ja048805k.
12. Kumari, R., Nambiar, M., Shanbagh, S., and Raghavan, S.C.
21. Hsu, S.T., Varnai, P., Bugaut, A., Reszka, A.P., Neidle, S.,
(2015) Detection of G quadruplex DNA using primer
and Balasubramanian, S. (2009) A G rich sequence within
extension as a tool, PLoS One, 10, e0119722, doi: 10.1371/
the c*kit oncogene promoter forms a parallel G quadruplex
journal.pone.0119722.
having asymmetric G tetrad dynamics, J. Am. Chem. Soc.,
13. Han, H., Hurley, L.H., and Salazar, M. (1999) A DNA
131, 13399-13409, doi: 10.1021/ja904007p.
polymerase stop assay for G quadruplex interactive com
22. Cogoi, S., and Xodo, L.E. (2006) G quadruplex formation
pounds, Nucleic Acids Res., 27, 537-542.
within the promoter of the KRAS proto oncogene and its
14. Qin, Y., and Hurley, L.H. (2008) Structures, folding pat
effect on transcription, Nucleic Acids Res., 34, 2536-2549,
terns, and functions of intramolecular DNA G quadru
doi: 10.1093/nar/gkl286.
plexes found in eukaryotic promoter regions, Biochimie,
23. Kumari, S., Bugaut, A., and Balasubramanian, S. (2008)
90, 1149-1171, doi: 10.1016/j.biochi.2008.02.020.
Position and stability are determining factors for transla
15. Klenow, H., and Henningsen, I. (1969) Effect of monova
tion repression by an RNA G quadruplex forming
lent cations on the activity of the DNA polymerase of
sequence within the 5' UTR of the NRAS proto oncogene,
Escherichia coli B, Eur. J. Biochem., 9, 133-141.
Biochemistry, 47, 12664-12669, doi: 10.1021/bi8010797.
STABLE G QUADRUPLEX STRUCTURES IN ONCOGENE
PROMOTERS INDUCE POTASSIUM DEPENDENT STOPS
OF THERMOSTABLE DNA POLYMERASE
G. V. Chashchina1,2, A. D. Beniaminov1, and D. N. Kaluzhny1*
1 Engelhardt Institute of Molecular Biology, Russian Academy of Sciences,
119991 Moscow, Russia; E*mail: uzhny@mail.ru
2 Moscow Institute of Physics and Technology (State University),
141701 Dolgoprudny, Moscow Region, Russia
Received October 25, 2018
Revised December 21, 2018
Accepted December 21, 2018
Amplification of GC rich regions of genomic DNA can be hindered either by the high stability of DNA double helix
or as a result of an alternative structure formation by guanine rich DNA strand. Such potential G quadruplex (G4)
sequences are fairly common in promoters of the human genome. The efficiency of PCR amplification of promoter
sequences for five human oncogenes (MYC, NRAS, TERT, KRAS, KIT) was studied. We demonstrate that the effi
ciency of DNA polymerase is reduced in the presence of potassium ions. Primer extension technique localized DNA
polymerase stops at the 3' ends of potential quadruplex sequences. Analysis of structural and thermodynamic proper
ties of short G rich oligonucleotides corresponding to the stops of DNA polymerase was carried out. The oligo
nucleotides formed stable parallel G quadruplexes in the presence of potassium ions. Correlation between the stabi
lity of G4 structures and the efficiency of DNA polymerase stops was revealed. The results provide the method of
detecting G4 structures in extended genomic sequences and clarify the mechanism of inhibition of DNA poly
merase in G rich regions of DNA.
Keywords: DNA, G quadruplex, promoter sequences, PCR, DNA polymerase
БИОХИМИЯ том 84 вып. 5 2019