БИОХИМИЯ, 2019, том 84, вып. 5, с. 739 - 744
УДК 541.14
СВОЙСТВА РЕАКЦИОННЫХ ЦЕНТРОВ
Rhodobacter sphaeroides С АМИНОКИСЛОТНЫМИ
ЗАМЕЩЕНИЯМИ Ile НА Tyr В ПОЗИЦИЯХ L177 И М206
© 2019 Т.Ю. Фуфина1*, Г.К. Селиханов2, И.И. Проскуряков1,
В.А. Шувалов1, Л.Г. Васильева1
1 Институт фундаментальных проблем биологии РАН,
ФИЦ ПНЦБИ РАН, 142290 Пущино Московской обл., Россия;
электронная почта: tat-fufina@yandex.ru
2 Институт белка РАН, 142290 Пущино Московской обл., Россия
Поступила в редакцию 17.12.2018
После доработки 28.01.2019
Принята к публикации 07.02.2019
Исследование пигмент белковых взаимодействий в реакционных центрах фотосинтеза важно для понима
ния детальных механизмов фотохимического процесса. В статье описаны спектральные и фотохимические
характеристики, пигментный состав и стабильность реакционных центров (РЦ) Rhodobacter sphaeroides с
аминокислотными замещениями I(L177)Y и I(M206)Y. Полученные результаты сравнены с описанными ра
нее свойствами РЦ I(L177)H, I(L177)D и I(M206)H. Показано, что мутации I(L177)Y и I(М206)Y вызывают
сходные смещения полосы QYP в спектрах поглощения мутантных РЦ и, очевидно, не влияют на распреде
ление спиновой плотности внутри фотоокисленного димера Р+. Обнаружены различия в положениях мак
симумов и величинах амплитуд полосы QYB в РЦ I(L177)Y и I(М206)Y. Полученные результаты указывают
на возможное образование новых пигмент белковых взаимодействий вблизи мономерных бактериохлоро
филлов А и В цепей, которые представляют интерес для дальнейшего исследования.
КЛЮЧЕВЫЕ СЛОВА: Rhodobacter sphaeroides, фотосинтетический реакционный центр, пигмент белковые
взаимодействия, пурпурные бактерии, направленный мутагенез.
DOI: 10.1134/S0320972519050117
Фотосинтез - это многостадийный процесс
так называемую специальную пару (Р), которая
преобразования энергии света в энергию хими
является первичным донором электрона [1].
ческих связей. На первых этапах этого процесса
Согласно современным представлениям, высо
в фотосинтетических реакционных центрах
кая эффективность фотохимической реакции в
(РЦ) световая энергия трансформируется в
РЦ определяется свойствами кофакторов, их
энергию разделенных зарядов с квантовой эф
взаимодействием друг с другом и с белковым ок
фективностью, близкой к 100%. РЦ пурпурной
ружением. В связи с этим выявление аминокис
бактерии Rhodobacter sphaeroides представляет
лотных участков, критически значимых для
собой трансмембранный пигмент белковый
функционирования комплекса, а также изуче
комплекс, состоящий из трех белковых субъеди
ние особенностей пигмент белковых взаимо
ниц (H, M и L) и десяти кофакторов переноса
действий представляют значительный интерес.
электрона. Кофакторы представлены четырьмя
Бактериохлориновые кофакторы РЦ имеют хо
молекулами бактериохлорофилла (БХл), двумя
рошо различаемые полосы в ближней инфра
молекулами бактериофеофитина (БФео), двумя
красной, видимой и ближней ультрафиолетовой
убихинонами, атомом негемового железа и мо
областях спектра поглощения РЦ. Изменение
лекулой каротиноида. Два БХл образуют димер,
спектральных характеристик кофакторов в му
тантных РЦ позволяет давать предварительную
Принятые сокращения: РЦ - реакционный центр; оценку влияния аминокислотных замен на
БХл - бактериохлорофилл; БФео - бактериофеофитин; структуру и свойства РЦ.
Р - специальная пара бактериохлорофиллов; Р+ - окис
Ранее нами были описаны свойства РЦ с
ленный первичный донор электрона; РА и РВ - бактериохло
рофиллы специальной пары; ВА и ВВ - мономерные бакте
симметричными аминокислотными заменами
риохлорофиллы.
Ile → His в положениях L177 и М206 вблизи мо
* Адресат для корреспонденции.
лекул БХл специальной пары и мономерных
739
740
ФУФИНА и др.
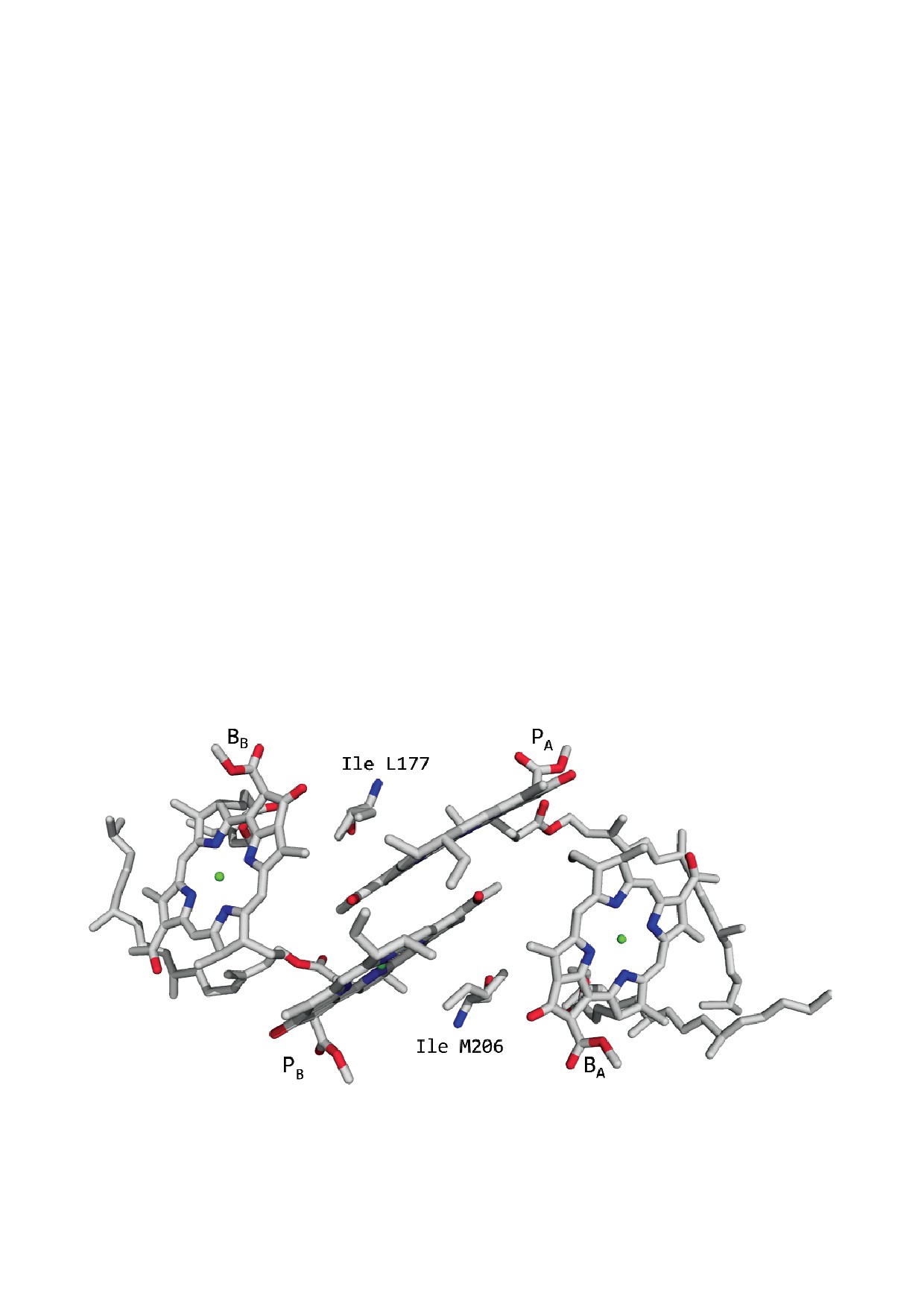
БХл (рис. 1). Было показано, что в спектрах по
РЦ пурпурных бактерий способствует стабили
глощения РЦ I(L177)H и I(М206)H наблюдают
зации состояния с разделенными зарядами
ся сходные изменения: коротковолновый сдвиг
Р+B– [6-8]. В данной работе описаны спект
максимума полосы поглощения специальной
ральные и фотохимические свойства РЦ с заме
пары и сдвиг максимума полосы поглощения
щениями I(L177)Y и I(М206)Y.
мономерных БХл в длинноволновую область с
одновременным уменьшением амплитуды этих
полос [2, 3]. Также обнаружены и существенные
МЕТОДЫ ИССЛЕДОВАНИЯ
различия свойств данных РЦ. Показано, что му
тация I(L177)H приводит к образованию проч
Рекомбинантные штаммы R. sphaeroides вы
ной (возможно ковалентной) связи между остат
ращивали на среде Хатнера в присутствии тетра
ком гистидина L177 и молекулой БХл РА. Кроме
циклина (1 мкг/мл) и канамицина (5 мкг/мл),
того, в структуре этого РЦ с β стороны БХл ВВ
как описано ранее [3]. Реакционные центры вы
появляется молекула воды, которая выступает
деляли методом ионообменной хроматографии,
вторым аксиальным лигандом атома магния
как описано ранее [9]. Количество РЦ после
БХл ВВ [4]. В РЦ I(М206)H не обнаружено зна
очистки из мембран оценивали по длинновол
чительных изменений пигмент белковых взаимо
новой полосе поглощения мономерных БХл
действий, но было показано, что мутация при
вблизи 800 нм в кювете с длиной оптического
водит к существенному снижению удельного
пути 1 см (ODV800) в расчете на 1 л трехдневной
выхода этого РЦ при его очистке из мембран [5].
культуры. Полученные реакционные центры со
Для дальнейшего исследования пигмент
любилизировали в буфере, содержавшем 20 мМ
белковых взаимодействий в РЦ R. sphaeroides,
Tris HCl, pH 8,0 и 0,1% лаурилдиметиламинок
а также для выяснения причин разных послед
сида. Спектры поглощения РЦ регистрировали
ствий замещения Ile → His в положениях L177 и
при комнатной температуре на спектрофото
М206, были введены новые аминокислотные за
метре UV 1800 («Shimadzu», Япония) и норми
мещения Ile → Tyr в этих позициях. Как и His,
ровали по QY полосе поглощения БФео вблизи
Tyr относится к полярным аминокислотным ос
760 нм. Дифференциальные спектры (свет ми
таткам, а его гидроксифенольная группа может
нус темнота) измеряли на том же спектрофото
участвовать во взаимодействиях с пигмент бел
метре с использованием скрещенных свето
ковым матриксом РЦ. В частности, ранее было
фильтров СЗС22 и КС19. Пигментный анализ
показано, что изменение ориентации ОН груп
проводили по ранее описанному методу [4, 10].
пы Tyr M210 в процессе разделения зарядов в
Измерения спектров ЭПР проводили на спект
Рис. 1. Расположение молекул БХл первичного донора электронов РА и РВ, мономерных БХл ВА и ВВ, а также аминокис
лотных остатков Ile L177 и Ile М206 в структуре РЦ дикого типа. Номер структуры в PDB банке - 3V3Y.
С цветным вариантом рис. 1 можно ознакомиться в электронной версии статьи на сайте: www.elibrary.ru
БИОХИМИЯ том 84 вып. 5 2019
СВОЙСТВА МУТАНТНЫХ РЕАКЦИОННЫХ ЦЕНТРОВ I(L177)Y и I(М206)Y
741
рометре EMX 6 («Bruker», Германия) при ком
смещен на 2 нм в коротковолновую область,
натной температуре. Образец возбуждали све
максимум полосы БФео в QX области спектра
том с длиной волны λ > 650 нм и интенсив
смещен на 3 нм в длинноволновую область до
ностью 10 мВт/см2. Мощность СВЧ составляла
536 нм. В спектре поглощения РЦ I(M206)Y по
2 мВт, модуляция - 0,4 мТл, постоянная време
лоса QYР имеет максимум при 860 нм, QY поло
ни - 1,3 с.
са мономерных БХл - при 810 нм, а QY полоса
молекул БФео - при 760 нм. Максимум QX по
лосы поглощения молекул БХл в РЦ I(M206)Y
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
расположен при 599 нм, а полосы QX БФео -
при 530 нм (рис. 2, спектр 3).
Показано, что удельный выход при очистке
При освещении РЦ I(L177)Y и I(M206)Y в диф
для РЦ I(L177)Y и I(M206)Y сравним с таковым
ференциальных спектрах (свет минус темнота)
для РЦ дикого типа и составил 4-5 ODV800 на
наблюдается уменьшение поглощения первич
литр культуры. Отмечено, что после процедуры
ного донора электрона, коротковолновый сдвиг
замораживания с последующим оттаиванием
полосы поглощения мономерных БХл и длинно
спектральные свойства РЦ I(L177)Y и I(M206)Y
волновый сдвиг полосы поглощения БФео, так
не меняются. Полученные данные сходны с ана
же как и в РЦ дикого типа. Эти данные указыва
логичными показателями для РЦ дикого типа и
ют на то, что в РЦ I(L177)Y и I(M206)Y происхо
свидетельствуют о стабильности мутантных РЦ.
дит фотоиндуцированный процесс переноса
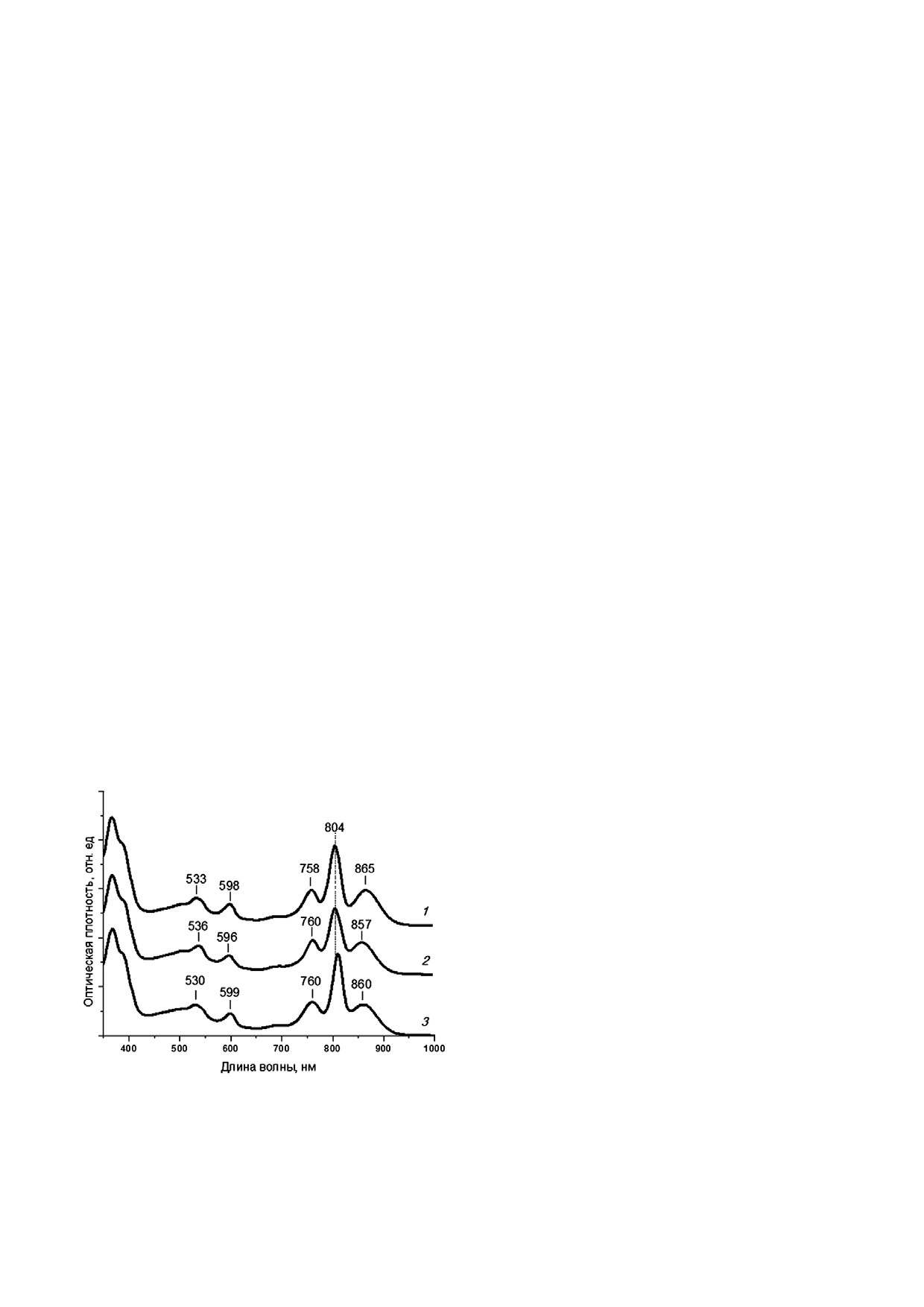
В спектре поглощения РЦ дикого типа длин
электрона с образованием состояния P+Q– (дан
новолновый максимум полосы поглощения
ные не приведены).
первичного донора электрона расположен при
Пигментный анализ показал, что состав пиг
865 нм, максимум полосы поглощения моно
ментов в РЦ I(L177)Y и I(M206)Y не изменился.
мерных БХл находится при 804 нм, а БФео -
Соотношение БХл/БФео в РЦ дикого типа сос
при 758 нм. В QX области спектра полоса погло
тавило 2,00 ± 0,05, а в РЦ I(L177)Y и I(M206)Y -
щения всех молекул БХл в РЦ расположена при
1,90 ± 0,05 и 2,10 ± 0,05 соответственно. Полу
598 нм, а максимум поглощения молекул БФео -
ченные результаты свидетельствуют о том, что в
при 533 нм (рис. 2, спектр 1). В спектре погло
мутантных РЦ, как и в РЦ дикого типа, на две мо
щения РЦ I(L177)Y длинноволновый максимум
лекулы БФео приходится четыре молекулы БХл.
QY полосы поглощения Р претерпевает коротко
С помощью методов двойного электронно
волновый сдвиг до 857 нм (рис. 2, спектр 2). По
ядерного резонанса и ЭПР ранее было показа
ложение максимума QY полосы поглощения мо
но, что в димере БХл Р R. sphaeroides R26 спино
номерных БХл не меняется, но амплитуда этой
вая плотность распределена неравномерно: око
полосы уменьшается. Максимум QY полосы
ло 2/3 плотности приходится на БХл РА и около
поглощения БФео смещается к 760 нм. Макси
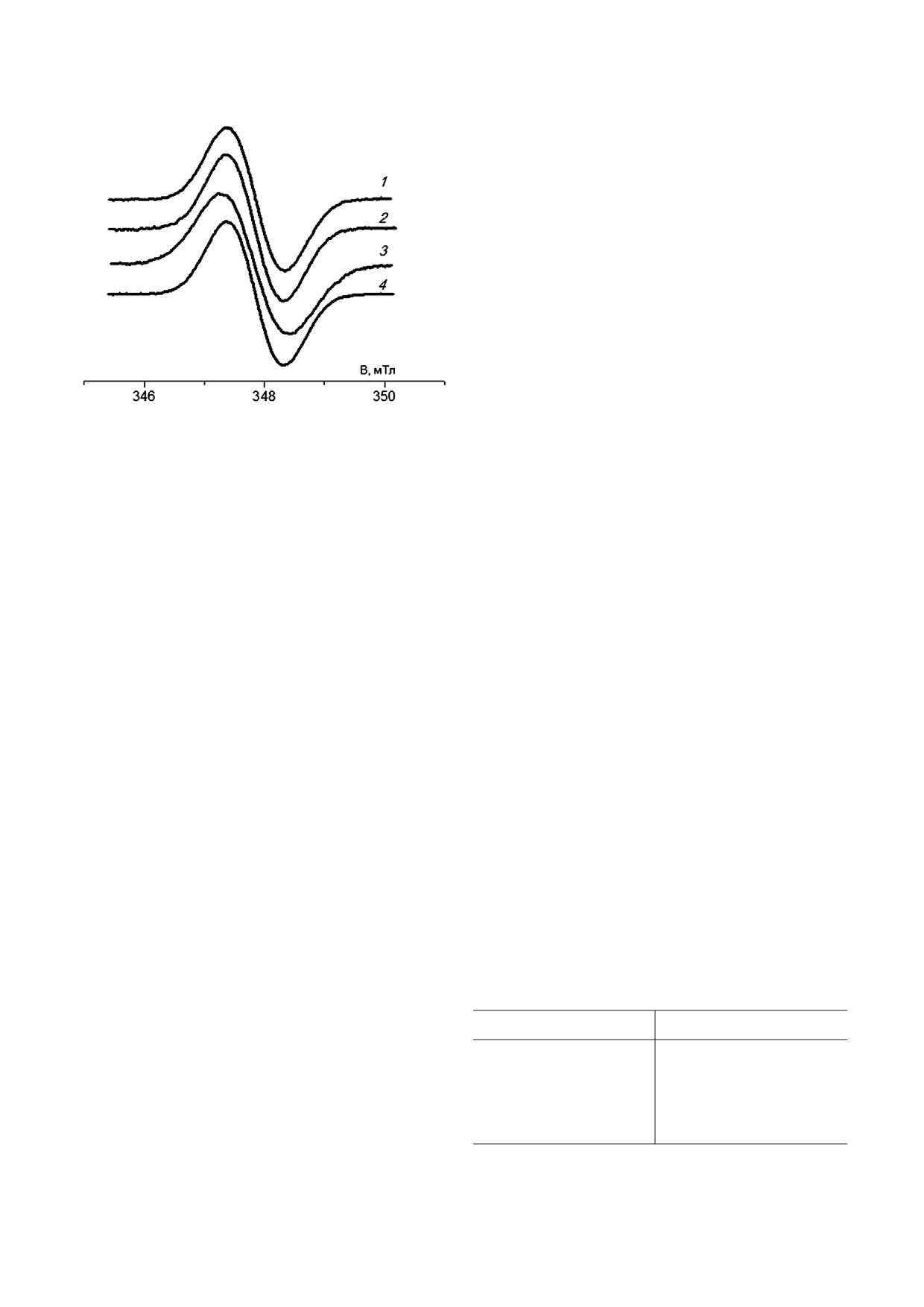
1/3 - на БХл РВ [11]. На рис. 3 приведены фото
мум QX полосы поглощения молекул БХл в РЦ
индуцированные сигналы ЭПР для РЦ дикого
типа и мутантных РЦ. Величина g фактора во
всех случаях составляет 2,0026 и соответствует
известному значению Р+. Для РЦ I(L177)Y и
I(М206)Y ширина сигнала Р+ остается такой же,
как для РЦ дикого типа (таблица). В то же время
в РЦ I(L177)H наблюдается уширение линии
сигнала ЭПР парамагнитного окисленного сос
тояния катион радикала Р до 1,14 мТл, что ука
зывает на изменение распределения спиновой
плотности внутри димера БХл. Эти результаты
согласуются с ранее полученными данными об
изменении электронной структуры Р из за об
разования прочной, предположительно ковалент
ной, связи БХл РА с белком [4].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Рис. 2. Спектры поглощения РЦ дикого типа (1), I(L177)Y
Полученные результаты показывают, что
(2) и I(M206)Y (3), измеренные при комнатной температу
аминокислотные замещения Ile → Tyr в симмет
ре. Спектры нормировали по QY полосе поглощения моле
кулы БФео
ричных позициях М206 и L177 вызывают сход
БИОХИМИЯ том 84 вып. 5 2019
742
ФУФИНА и др.
в ~2 раза, РЦ I(M206)Н - более чем на порядок [5].
Дополнительным свидетельством стабильности
РЦ I(L177)Y и I(М206)Y является отсутствие
фракции без длинноволновой полосы поглоще
ния Р при очистке этих комплексов из мембран,
что также отличает их от РЦ I(L177)H и
I(M206)Н [5]. Таким образом, внесение поляр
ных остатков Tyr в окружение бактериохлоро
филлов РА и ВВ (мутация I(L177)Y) и РВ и ВА (му
тация I(М206)Y) не дестабилизирует структуру
РЦ. Совокупность полученных результатов поз
воляет предположить, что характеристики этих
взаимодействий отличаются от таковых, выз
ванных внесением полярных остатков His в те
же позиции.
Имеющиеся литературные данные свиде
тельствуют о том, что обязательным условием
Рис. 3. Спектры ЭПР фотоиндуцированного окисленного
для внедрения аминокислотных остатков с по
состояния первичного донора (Р+) в РЦ дикого типа (1) и с
лярными группами в гидрофобную среду мемб
аминокислотными замещениями вблизи молекул БХл
I(L177)Y (2), I(L177)H (3), I(M206)Y (4), измеренные при
ранных белков является вовлечение этих групп в
комнатной температуре
стабильные взаимодействия с пигмент белко
вым окружением [15]. Нарушение этого условия
может приводить к таким последствиям, как
ные изменения в спектрах мутантных РЦ в об
утеря мономерного БХл ВА из структуры РЦ
ласти поглощения димера БХл Р. Мутация
H(L153)Y [15] или дестабилизация и снижение
I(L177)Y приводит к коротковолновому сдвигу
количества РЦ в мембране при внесении мута
полосы QYP на 8 нм, а мутация I(M206)Y - к ана
ции I(M206)H [5]. Результаты ЭПР и анализ
логичному сдвигу на 5 нм. Замещение I(L177)Y
спектров поглощения мутантных РЦ указывают
практически не влияет на максимум полосы
на то, что гидроксильные группы тирозинов в
QYB, однако отмечается заметное снижение
положениях М206 и L177, по всей вероятности,
амплитуды этой полосы в спектре поглощения
вступают в устойчивые взаимодействия с белко
РЦ. В свою очередь, мутация I(M206)Y вызыва
вым окружением мономерных БХл ВА и ВВ.
ет смещение полосы QYB в длинноволновую об
Ранее было показано, что с помощью ряда
ласть спектра на 6 нм без видимого уменьшения
замещений можно модифицировать пигмент бел
ее амплитуды.
ковые взаимодействия с β стороны макроцикла
Результаты ЭПР спектроскопии свидетель
БХл ВВ [4, 16] вблизи положения L177. Так,
ствуют о том, что в РЦ I(L177)Y и I(М206)Y
Фролов с соавт. показали, что мутация F(L181)R
распределение спиновой плотности внутри ди
приводит к образованию шестой координацион
мера БХл Р не изменилось. Эти данные согласу
ной связи, сформированной между молекулой во
ются с результатами компьютерного моделиро
ды, расположенной с β стороны БХл ВВ, и ато
вания замещений I(L177)Y и I(М206)Y с исполь
мом магния этого пигмента. Добавление допол
зованием программы визуализации белковых мо
нительной мутации H(M182)L + F(L181)H при
лекул PyMol [12], показывающими, что наибо
водило к формированию РЦ, в которых акси
лее вероятное расположение гидроксифеноль
альный лиганд БХл ВВ располагался с β сторо
ной группы тирозина направлено в сторону мо
номерных БХл (не показано). Можно предполо
жить, что коротковолновый сдвиг полосы QYP,
Ширина сигнала ЭПР Р+ в изолированных РЦ дикого типа
ранее также наблюдавшийся в спектрах погло
и генетически модифицированных РЦ I(L177)Y, I(L177)H
щения мутантных РЦ с замещениями в позици
и I(M206)Y
ях L177 и М206 [2, 3, 13], а также ряда РЦ с дру
РЦ
Ширина сигнала, мТл
гими замещениями [14], является ответом на из
менения белкового окружения димера БХл.
Дикий тип
0,98 ± 0,01
Удельный выход РЦ одиночных мутантов
I(L177)Y
0,97 ± 0,01
I(L177)Y и I(М206)Y при их очистке из мембран
был соизмерим с аналогичной величиной для
I(L177)Н
1,14 ± 0,01
РЦ дикого типа. Для сравнения, ранее было по
I(M206)Y
0,95 ± 0,01
казано снижение удельного выхода РЦ I(L177)H
БИОХИМИЯ том 84 вып. 5 2019
СВОЙСТВА МУТАНТНЫХ РЕАКЦИОННЫХ ЦЕНТРОВ I(L177)Y и I(М206)Y
743
ны макроцикла пигмента [16]. Аналогичные ре
таллической структуры РЦ I(L177)Y и I(М206)Y,
зультаты были получены позднее на мутантных
и такая работа в настоящее время ведется.
РЦ I(L177)H. Было показано, что в структуре
Таким образом, замещения Ile → Tyr в пози
РЦ I(L177)H БХл ВВ имеет два аксиальных ли
циях М206 и L177 оказывают сходное влияние
ганда, одним из которых, как и в РЦ F(L181)R,
на спектральные свойства Р, но приводят к раз
выступает молекула воды [4]. При удалении на
ным изменениям в области поглощения моно
тивного аксиального лиганда БХл ВВ в РЦ
мерных БХл. РЦ I(L177)Y и I(М206)Y фотохи
H(M182)L + I(L177)H данная молекула воды,
мически активны, относительно стабильны при
очевидно, координирует атом магния ВВ с β сто
выделении из мембран и, благодаря интересным
роны макроцикла [4, 17].
спектральным характеристикам, представляют
Внесение His в позицию М206, расположен
собой перспективные объекты для исследова
ную симметрично сайту L177, приводило к ка
ния роли белка в обеспечении функциональной
чественно иным результатам, прежде всего, к
активности А цепи и неактивности В цепи.
значительной дестабилизации структуры РЦ [5].
Было выдвинуто предположение, что полярный
остаток His в этом положении мог нарушить
Финансирование. Работа выполнена в рамках
взаимодействие РЦ с молекулой гликолипида,
госзадания № АААА А17 117030110140 5 (изме
необходимое для поддержания стабильности
рение спектральных свойств изолированных ре
комплекса [5]. В этой связи значительный инте
акционных центров), а также при частичной
рес представляет вопрос о том, за счет каких взаи
финансовой поддержке Российского фонда фун
модействий полярный Tyr М206, имеющий боль
даментальных исследований (проекты № 17 00
ший молекулярный объем (118 см3 · моль-1), чем
0207 (К) - направленный мутагенез реакцион
объем Ile (99,9 см3 · моль-1) и His (93,1 см3 · моль-1)
ных центров; № 17 44 500828 - выращивание
[18], не влияет на стабильность РЦ, и, предпо
рекомбинантных штаммов и выделение реакци
ложительно, на связывание гликолипида с по
онных центров).
верхностью комплекса. Можно ожидать, что Tyr
Конфликт интересов. Авторы заявляют об от
М206 и L177 занимает все пространство вблизи
сутствии конфликта интересов.
атома магния с β стороны плоскости мономер
Соблюдение этических норм. Настоящая
ных БХл, не оставляя возможности для допол
статья не содержит описания каких либо иссле
нительного встраивания молекул воды. Ответы
дований с использованием людей и животных в
на эти вопросы может дать расшифровка крис
качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1.
Allen, J.P., Feher, G., Yeates, T.O., Komiya, H., and
dimer in the photosynthetic reaction center of Rhodobacter
Rees, D.C. (1987) Structure of the reaction center from
sphaeroides, Biochemistry (Moscow), 80, 647-653.
Rhodobacter sphaeroides R-26: the cofactors, Proc. Natl.
6. Parson, W.W., Chu, Z.T., and Warshel, A.
(1990)
Acad. Sci. USA, 84, 5730-5734, doi: 10.1073/pnas.84.
Electrostatic control of charge separation in bacterial
16.5730.
photosynthesis, Biochim. Biophys. Acta, 1017, 251-272,
2.
Болгарина Т.И., Хатыпов Р.А., Васильева Л.Г., Шкуро
doi: 10.1016/0005 2728(90)90192 7.
патов А.Я., Шувалов В.А. (2004) Замещение изолей
7
Alden, R.G., Parson, W.W., Chu, Z.T., and Warshel, A.
цина М206 на гистидин в реакционных центрах
(1996) Orientation of the OH dipole of tyrosine (M)210
Rhodobacter sphaeroides приводит к изменению струк
and its effect on electrostatic energies in photosynthetic
туры молекулы бактериохлорофилла специальной па
bacterial reaction centers, J. Phys. Chem., 100, 16761-16770,
ры, Доклады Академии наук, 394, 265-268.
doi: 10.1021/jp961271s.
3.
Khatypov, R.A., Vasilieva, L.G., Fufina, T.Y., Bolga
8. Yakovlev, A.G., Vasilieva, L.G., Shkuropatov, A.Ya.,
rina, T.I., and Shuvalov, V.A. (2005) Substitution of
Bolgarina, T.I., Shkuropatova, V.A., and Shuvalov, V.A.
isoleucine L177 by histidine affects the pigment composi
(2003) Mechanism of charge separation and stabilization
tion and properties of the reaction center of the purple bac
of separated charges in reaction centers of Chloroflexus
terium Rhodobacter sphaeroides, Biochemistry (Moscow),
aurantiacus and of YM210W(L) mutants of Rhodobacter
70, 1256-1261.
sphaeroides excited by 20 fs pulses at 90 K, J. Phys. Chem. A,
4.
Vasilieva, L.G., Fufina, T.Y., Gabdulkhakov, A.G.,
107, 8330-8338, doi: 10.1021/jp0300647.
Leonova, M.M., Khatypov, R.A., and Shuvalov, V.A.
9. Fufina, T.Y., Vasilieva, L.G., Khatypov, R.A., Shkuropa
(2012) The site directed mutation I(L177)H in Rba.
tov, A.Y., and Shuvalov, V.A. (2007) Substitution of
sphaeroides reaction center affects coordination of PA and
isoleucine L177 by histidine in Rhodobacter sphaeroides
BB bacteriochlorophylls, Biochim. Biophys. Acta, 1817,
reaction center results in the covalent binding of PA bacte
1407-1417, doi: 10.1016/j.bbabio.2012.02.008.
riochlorophyll to the L subunit, FEBS Lett.,
581,
5.
Vasilieva, L.G., Fufina, T.Y., Shuvalov, V.A., and
5769-5773, doi: 10.1016/j.febslet.2007.11.032.
Gabdulkhakov, A.G. (2015) Different effects of identical
10. Van der Rest, M., and Gingras, G. (1974) The pigment
symmetry related mutations near the bacteriochlorophyll
complement of the photosynthetic reaction center isola
БИОХИМИЯ том 84 вып. 5 2019
744
ФУФИНА и др.
ted from Rhodospirillum rubrum, J. Biol. Chem., 249,
sphaeroides: spectroscopy and structure, Biochim Biophys
6446-6453.
Acta, 1554, 75-93, doi: 10.1016/S0005 2728(02)00215 3.
11. Lendzian, F., Huber, M., Isaacson, R.A., Endeward, B.,
15. Леонова М.М., Фуфина Т.Ю., Шувалов В.А., Василье
Plato, M., Bonigk, B., Mobius, K., Lubitz, W., and Feher, G.
ва Л.Г. (2014) Исследование пигмент белковых взаимо
(1993) The electronic structure of the primary donor
действий в фотосинтетическом реакционном центре пур
cation radical in Rhodobacter sphaeroides R 26: ENDOR
пурных бактерий. Глава в кн. Современные проблемы
and TRIPLE resonance studies in single crystals of reac
фотосинтеза, том. 1 (под ред. Аллахвердиева С.И., Ру
tion centers, Biochim. Biophys. Acta, 1183, 139-160, doi:
бина А.Б., Шувалова В.А.), Москва-Ижевск, Ижевский
10.1016/0005 2728(93)90013 6.
Институт компьютерных исследований, с. 157-196.
12. DeLano, W.L. (2002) The PyMOL Molecular Graphics
16. Frolov, D., Marsh, M., Crouch, L.I., Fyfe, P.K., Robert, B.,
van Grondelle, R., Hadfield, A., and Jones, M.R. (2010)
sourceforge.net/.
Structural and spectroscopic consequences of hexacoordi
13. Williams, J.C., Alden, R.G., Murchison, H.A., Peloquin, J.M.,
nation of a bacteriochlorophyll cofactor in the Rhodobacter
Woodbury, N.W., and Allen, J.P. (1992) Effects of muta
sphaeroides reaction center, Biochemistry, 49, 1882-1892,
tions near the bacteriochlorophylls in reaction centers from
doi: 10.1021/bi901922t.
Rhodobacter sphaeroides, Biochemistry, 31, 11029-11037,
17. Fufina, T.Yu., Vasilieva, L.G., Khatypov, R.A., and Shu
doi: 10.1021/bi00160a012.
valov, V.A. (2011) Properties of Rhodobacter sphaeroides
14. Spiedel, D., Roszak, A.W., McKendrick, K., McAuley, K.E.,
photosynthetic reaction center with double amino acid
Fyfe, P.K., Nabedryk, E., Breton, J., Robert, B., Cogdell, R.J.,
substitution I(L177)H+H(M182)L, Biochemistry (Moscow),
Isaacs, N.W., and Jones, M.R. (2002) Tuning of the optical
76, 450-454.
and electrochemical properties of the primary donor bacte
18. Нолтинг Б. Новейшие методы исследования биосис
riochlorophylls in the reaction centre from Rhodobacter
тем, Москва, Техносфера, 2005, 256 с.
THE PROPERTIES OF Rhodobacter sphaeroides REACTION
CENTERS WITH AMINO ACID SUBSTITUTIONS
OF Ile FOR Tyr AT L177 AND М206 POSITIONS
T. Yu. Fufina1*, G. K. Selikhanov2, I. I. Proskuryakov1,
V. A. Shuvalov1, and L. G. Vasilieva1
1 Institute of Basic Biological Problems, Russian Academy of Sciences,
142290 Pushchino, Moscow Region, Russia; E-mail: tat-fufina@yandex.ru
2 Institute of Protein Research, Russian Academy of Sciences,
142290 Pushchino, Moscow Region, Russia
Received December 17, 2018
Revised January 28, 2019
Accepted February 7, 2019
Study of pigment-protein interactions in photosynthetic reaction centers is important for understanding detailed
mechanisms of the photochemical process. The article describes the spectral and photochemical characteristics, pig
ment composition and stability of the Rhodobacter sphaeroides reaction centers (RCs) with amino acid substitutions
I(L177)Y and I(M206)Y. The data obtained are compared with the properties of the I(L177)H, I(L177)D, and
I(M206)H RCs, which were described earlier. It is shown that the I(L177)Y and I(M206)Y mutations cause similar
shifts of the QYP band in absorption spectra of the mutant RCs and, obviously, do not affect the distribution of
electron spin density within the photooxidized P+ dimer. Differences in the peak positions and the amplitudes of the
QYB band in the I(L177)Y and I(M206)Y RCs were found. The results indicate the possibility of formation of new pig
ment-protein interactions in the vicinity of monomeric bacteriochlorophylls in A and B chains, which is of interest
for future research.
Keywords: Rhodobacter sphaeroides, photosynthetic reaction center, pigment-protein interactions, purple bacteria,
directed mutagenesis
БИОХИМИЯ том 84 вып. 5 2019