БИОХИМИЯ, 2020, том 85, вып. 3, с. 399 - 411
УДК 577.322
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО
БЕЛКА bS1 И ЕГО СТАБИЛЬНОГО ФРАГМЕНТА
ИЗ Thermus thermophilus
© 2020
С.Ю. Гришин1, У.Ф. Джус1, О.М. Селиванова1,
В.А. Балобанов1, А.К. Сурин1,2,3, О.В. Галзитская1,4*
1 Институт белка РАН, 142290 Пущино, Моcковcкая обл., Россия; электронная почта: ogalzit@vega.protres.ru
2 Государственный научный центр прикладной микробиологии и биотехнологии,
142279 Оболенск, Моcковcкая обл., Россия; электронная почта: alan@vega.protres.ru
3 Филиал Института биоорганической химии им. акад. М.М. Шемякина и Ю.А. Овчинникова РАН,
142290 Пущино, Моcковcкая обл., Россия
4 Институт теоретической и экспериментальной биофизики РАН, 142290 Пущино Моcковcкая обл., Россия
Поступила в редакцию 21.10.2019
После доработки 24.12.2019
Принята к публикации 11.01.2020
Многодоменный бактериальный белок bS1 является самым большим и функционально важным белком 30S
субъединицы рибосомы, взаимодействующим как с мРНК, так и с белками. Известно, что белок bS1 обла'
дает высокой склонностью к формированию ассоциатов, однако детально этот процесс не изучали. Для ри'
босомного белка bS1, а также его стабильного фрагмента из Thermus thermophilus нами были получены супер'
продуцентные штаммы, выделены и очищены препараты рекомбинантного рибосомного белка bS1 из
T. thermophilus, а также его стабильного фрагмента bS1(49). Методами флуоресцентной спектроскопии, ди'
намического рассеяния света и высокоэффективной жидкостной хроматографии, совмещенной с масс'
спектрометрическим анализом продуктов ограниченного протеолиза, показано, что неструктурированные
участки на N' и С'концах белка bS1 могут играть ключевую роль в его агрегации. При этом полученный
фрагмент белка bS1(49) менее склонен к формированию агрегатов по сравнению с целым белком из T. ther>
mophilus. Выявленные особенности могут быть использованы для получения белковых кристаллов и выяс'
нения структуры стабильного фрагмента белка bS1.
КЛЮЧЕВЫЕ СЛОВА: агрегация белков, рибосомный белок, bS1, домен, Thermus thermophilus, ионная сила
раствора, масс'спектрометрия.
DOI: 10.31857/S0320972520030100
В настоящее время известно, что склонность
[9, 10], является самым большим (~60 кДа) бел'
к агрегации и формированию амилоидоподоб'
ком 30S рибосомной субчастицы. В составе ри'
ных фибрилл является общим свойством пепти'
босомы данный РНК'связывающий белок вы'
дов и белков [1-4]. Отдельный интерес пред'
полняет структурные и регуляторные функции
ставляет изучение агрегации рибосомных бел'
[11-14]. Многие РНК'связывающие белки со'
ков в связи с их повсеместной представлен'
держат в своей структуре либо домены холодо'
ностью в клетке и вовлеченностью в надмолеку'
вого шока (ДХШ), либо структурно аналогич'
лярные ансамбли с другими белками и нуклеи'
ные им S1'домены, которые от одной до не'
новыми кислотами [5-8].
скольких копий повторяются в рибосомальном
Белок bS1, также обозначаемый как S1, по
белке bS1 [15-20]. Однако трехмерная структура
номенклатуре, предложенной до
2014 года bS1 до сих пор не определена в связи с невоз'
можностью получить ее в кристаллической фор'
Принятые сокращения: I320/I380 - отношение интен'
сивностей флуоресценции на длинах волн 320 и 380 нано'
ме, что, в свою очередь, обусловлено относи'
метров; bS1(49) - фрагмент белка bS1 из Thermus ther>
тельной подвижностью S1'доменов в растворе.
mophilus c молекулярной массой ~49 кДа; m/z - отношение Каждый S1'домен состоит из ~70 аминокислот'
массы иона к его заряду; ВЭЖХ'МС - высокоэффектив' ных остатков (а.о.), разделенных гибкими участ'
ная жидкостная хроматография с масс'спектрометрией;
ками (15-20 а.о.) [21]. Большинство экспери'
ДРС - динамическое рассеяние света; ДХШ - домен холо'
дового шока; КД - круговой дихроизм; ЭМ - электронная
ментальных исследований проведено на выде'
микроскопия.
ленном из Escherichia coli белке bS1, в состав ко'
* Адресат для корреспонденции.
торого входит шесть доменов [22-25]. Белок bS1
399
400
ГРИШИН и др.
из термофильного микроорганизма Thermus
МС). Cклонность этих белков к формированию
thermophilus имеет пять S1'доменов (D1-D5) и
ассоциатов была изучена в буферных растворах
меньше изучен. Однако белки из термофилов
с низкой ионной силой (25 мМ HEPES'NaOH,
стабильны, с ними удобнее работать при обыч'
pH 7,5), умеренной (25 мМ HEPES'NaOH,
ных температурах, и они лучше поддаются крис'
pH 7,5; 150 мМ NaCl) и высокой (25 мМ
таллизации [26, 27].
HEPES'NaOH, pH 7,5; 2 М LiCl).
Рибосомный белок bS1 из T. thermophilus
был идентифицирован относительно недавно
[28]. В серии экспериментов для белка bS1 была
МЕТОДЫ ИССЛЕДОВАНИЯ
выявлена склонность образовывать ассоциаты
при низкой (25 мМ HEPES'NaOH, pH 7,5) и
Выделение белков. Ген белка bS1 T. ther>
умеренной (25 мМ HEPES'NaOH, pH 7,5 в при'
mophilus и фрагмент гена, соответствующий бел'
сутствии 100-150 мМ NaCl) ионной силе рас'
ку bS1(49) T. thermophilus, были клонированы в
твора [29-31]. Как отмечалось выше, S1'доме'
экспрессионный вектор pET28b («Novagen»,
ны белка bS1 хотя и отличаются по последова'
Германия) и суперэкспрессированы в культуре
тельности от ДХШ, тем не менее сходны с по'
клеток E.coli BL21 (DE3) («Novagen», Германия)
следними по структуре и принадлежат к семей'
[35]. Рекомбинантный белок bS1 был выделен
ству ОБ'мотивов [32]. В предыдущих работах
из штамма'суперпродуцента E. coli BL21(DE3) и
было показано, что только в условиях с высокой
очищен по ранее описанной методике с некото'
ионной силой раствора (2 М LiCl) белок YB'1,
рыми изменениями [28]. Для увеличения доли
имеющий в составе ДХШ, способен формиро'
связанного на колонке белка при хроматогра'
вать фибриллы [33], причем именно ДХШ вно'
фической очистке вместо DEAE'Sepharose была
сит основной вклад в фибриллогенез [34]. Вли'
использована колонка Q'Sepharose
(«GE
яние высокой ионной силы раствора на про'
Healthcare», Швеция).
цесс формирования агрегатов S1'доменами не
bS1(49), фрагмент белка bS1 из T. thermo>
было изучено.
philus, был выделен из штамма'суперпродуцента
Формирование белком bS1 из T. thermophilus
E. coli аналогично целому белку [28]. В связи с
ассоциатов обусловлено взаимодействием друг с
тем, что белок термостабилен, для очистки ис'
другом его аминокислотных последовательнос'
пользовали стадию прогрева супернатанта при
тей, склонных к агрегации. Однако до сих пор
75 °С 15 мин, в результате которой удаляется
не был выявлен вклад в этот процесс конкрет'
большая часть термолабильных белков E. coli.
ных а.о. из S1'доменов N' и С'концевых фраг'
Далее белковую фракцию осаждали путем выса'
ментов данного белка. В то же время с целью
ливания сульфатом аммония. Поскольку
выяснения особенностей агрегации белка bS1 из
bS1(49) обладает сильными РНК'связывающи'
T. thermophilus можно использовать для сравне'
ми свойствами, препарат последовательно до'
ния его усеченный фрагмент c молекулярной
очищали вначале с помощью аффинной хрома'
массой 49 кДа - bS1(49). Данный фрагмент уко'
тографии на Heparin'Sepharose («GE Health'
рочен с N' и С'концов на 25 а.о. и 71 а.о. соответ'
care», Швеция), затем на гидрофобном хрома'
ственно, но сохраняет пять S1'доменов и также
тографическом носителе Butyl'Sepharose («GE
как целый белок способен связываться с рибо'
Healthcare», Швеция). Конечной стадией очист'
сомной 30S субъединицей [30]. В связи с этим
ки стала гель'фильтрация на носителе
имеет значение выяснить, есть ли отличия в
Superdex 75 («GE Healthcare», Швеция). Гель'
процессе агрегации и в морфологии формируе'
фильтрацию белков осуществляли в буферном
мых агрегатов для целого белка и его фрагмента
растворе, содержащем 50 мМ Tris'HCl (pH 7,5),
bS1(49), связанные с различием в их аминокис'
10 мМ MgCl2, 200 мМ NaCl и 5 мМ β'меркапто'
лотной последовательности? В то же время сле'
этанола. Для хранения препаратов при -20 °C
дует уточнить, будут ли высокие концентрации
белковые фракции высаливали добавлением
LiCl вызывать фибриллогенез белка bS1 и его
(NH4)2SO4 до конечной концентрации 3 М.
стабильного фрагмента, имеющих в своей
Подготовка препаратов белков bS1 и bS1(49)
структуре 5 повторяющихся доменов структур'
для исследований. Для изучения агрегации бел'
ных аналогов ДХШ? Чтобы ответить на эти воп'
ков использовали буферные растворы с низкой
росы, мы охарактеризовали агрегационные
ионной силой - буфер 1 (25 мМ HEPES'NaOH,
свойства bS1 и bS1(49) с помощью методов флуо'
pH 7,5), умеренной ионной силой - буфер 2
ресцентной спектроскопии, динамического
(25 мМ HEPES'NaOH, pH 7,5; 150 мМ NaCl) и
рассеяния света (ДРС), электронной микроско'
высокой ионной силой - буфер 3 (25 мМ
пии (ЭМ) и высокоэффективной жидкостной
HEPES'NaOH, pH 7,5; 2 М LiCl). Перед экспе'
хроматографии с масс'спектрометрией (ВЭЖХ'
риментами сульфатный осадок белков раство'
БИОХИМИЯ том 85 вып. 3 2020
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО БЕЛКА bS1
401
ряли в 25 мМ HEPES'NaOH, pH 7,5 и перево'
составляло 2 мин для каждого шага. Средние
дили диализом в соответствующие буферные
значения температуры агрегации определяли
растворы при 4 °С в течение 16 ч. После диали'
для образцов bS1 и bS1(49) (при концентрации
за аликвоты раствора (по 4 мг белка) хранили
белков 20 мкМ) в трех буферах (1, 2 и 3) на осно'
при -20 °С. Перед экспериментами белковые
ве трех независимых измерений.
препараты центрифугировали в течение 20 мин
Электронная микроскопия. Препараты све'
(4 °С) при 50 тыс. об./мин на ультрацентрифуге
жевыделенного белка bS1 T. thermophilus и его
Beckman 100 («Beckman Coulter», Канада).
фрагмента bS1(49) в условиях 25 мM HEPES'
Концентрацию белков определяли по методу
NaOH, pH 7,5 и препараты после прогревания
Бредфорда [36], а также спектрофотометричес'
при 70 °С в течение 24 ч в условиях 25 мM
ким методом с учетом коэффициента экстинк'
HEPES'NaOH, pH 7,5; 25 мM HEPES'NaOH,
ции ε278 = 0,65 (мл × мг-1 × см-1) [37]. Получен'
pH 7,5;150 мM NaCl; 25 мM HEPES'NaOH,
ные образцы bS1 и bS1(49) в концентрации
pH 7,5; 2 M LiCl анализировали с помощью
20 мкМ использовались в дальнейших экспе'
электронного микроскопа JEM'1200EX («JEOL»,
риментах.
Япония). Перед анализом концентрацию пре'
Спектры кругового дихроизма (КД). Спектры
паратов доводили соответствующим буфером
белковых растворов bS1 и bS1(49) регистриро'
до 0,2 мг/мл. Образцы готовили для анализа
вали на спектрополяриметре Chirascan («Photo'
методом негативного контрастирования. На
physics», Англия) в кварцевой ячейке с длиной
каплю препарата (~10 мкл) помещали медную
пути 0,01 см (концентрация белков 20 мкМ).
сеточку
(400 Mesh,
«Electron Microscopy
Изменения во вторичной структуре bS1 и
Sciences», США), покрытую формваровой
bS1(49) контролировали в дальней области УФ'
пленкой (0,2%'ный раствор формвара в хлоро'
спектра (190-250 нм) для каждого буфера (1, 2 и 3)
форме). После адсорбции (5 мин) сеточки с
при температуре 25 °С. Каждый спектр записы'
препаратом переносили на 1%'ный (w/v) вод'
вали трижды с разрешением 0,5 нм, усредняли,
ный раствор уранилацетата (1 мин). Излишки
затем вычитали базовый спектр буферного
препарата и уранилацетата убирали с помощью
раствора и применяли сглаживание методом
фильтровальной бумаги. Анализ препаратов
Savitzky и Golay [38], используя программное
проводили при ускоряющем напряжении
обеспечение Chirascan
(«Photophysics», Ан'
80 кВ. Съемку осуществляли на пленку Kodak
глия). Полученные данные КД были проана'
(SO'163) для электронной микроскопии при
лизированы с помощью онлайн'сервера
увеличении 40 тыс.
Bestsel [39].
ВЭЖХGМС анализ продуктов протеолиза агG
Кривые температурной денатурации. Спектры
регатов bS1 и bS1(49). Для анализа ВЭЖХ'МС
флуоресценции получали с помощью четырех'
разделения продуктов ограниченного протеоли'
кюветного спектрофлуориметра Varian Cary
за агрегатов bS1 и bS1(49) препараты белков де'
Eclipse («Varian», США) в кварцевых кюветах с
лили на контрольные (25 мМ HEPES'NaOH,
длиной оптического пути 0,3 × 0,3 см и объемом
pH 7.5) и опытные образцы. Первые хранились
100 мкл, скорость прогрева 1 °С/мин. Длина
при -20 °С, а ко вторым добавляли LiCl (конеч'
волны возбуждения составляла 280 нм, спектры
ная концентрация 2 М LiCl) и инкубировали
испускания регистрировали в диапазоне
при 70 °C в течение суток с целью получения аг'
300-450 нм. Для белков bS1 и bS1(49) из T. ther>
регатов. После этого контрольные и опытные
mophilus кривые температурной денатурации по'
образцы отдельно инкубировали со смесью про'
лучали на основе расчета отношения интенсив'
теаз (трипсина, химотрипсина («Sigma'Aldrich»,
ностей флуоресценции триптофанов при длинах
Германия) и протеиназы К
(«AppliChem»,
волн 320 и 380 нм (I320/I380) [40].
США)) в течение 8 ч при 37 °C со скоростью пе'
Динамическое рассеяние света (ДРС). Изме'
ремешивания 450 об./мин в термостатируемом
рения ДРС осуществляли с помощью прибора
миксере Thermomixer comfort («Eppendorf», Гер'
Zetasizer Nano ZS («Malvern Instruments Ltd.»,
мания). Конечная концентрация белка в препа'
Великобритания), оснащенного гелий'неоно'
ратах составила 20 мкМ, концентрация каждой
вым лазером мощностью 4 мВт и с температур'
протеазы 0,27 мкМ. После инкубации реакцию
ным контролем кюветы (± 0,1 °С для объема
протеолиза останавливали добавлением концент'
100 мкл). Измерения светорассеяния проводили
рированной муравьиной кислоты (0,2% (v/v)).
в кварцевых кюветах при длине волны 532 нм,
Контрольные и опытные образцы центрифуги'
под углом 173°. Температурную зависимость
ровали 20 мин при 10 000 об./мин на центрифу'
увеличения интенсивности светорассеяния оп'
ге Eppendorf 5418R («Eppendorf», Германия).
ределяли в диапазоне 25-90 °С с шагом 5 °С.
Осадок дважды промывали 100 мM NH4HCO3
Время уравновешивания и термостатирования
(pH 7,5), затем все препараты высушивали и
БИОХИМИЯ том 85 вып. 3 2020
402
ГРИШИН и др.
растворяли в 20 мкл 0,5%'ной трифторуксусной
ней области УФ'спектра (190-250 нм) для бел'
кислоты для последующей жидкостной хрома'
ков в буферных растворах 1 (25 мМ HEPES'
тографии и масс'спектрометрии, как описано в
NaOH), 2 (25 мМ HEPES'NaOH, 150 мМ NaCl)
работе Surin et al. [41].
и 3 (25 мМ HEPES'NaOH, 2М LiCl). Cпектры
После смыва с колонки пептиды ионизуют,
КД для препаратов целого белка bS1 и bS1(49)
затем они попадают в масс'спектрометр. В ходе
были получены с учетом базовых спектров бу'
масс'спектрометрического анализа определяют
ферных растворов (рис. 1).
заряд каждого иона, отношение его массы к за'
Как видно из рис. 1, ионная сила раствора
ряду (m/z) и, в случае тандемной масс'спектро'
оказывала наибольший эффект на вторичную
метрии, определяют отношение массы к заряду
структуру bS1 белка, в то время как для bS1(49)
для его фрагментов. Данные характеристики
спектры практически не изменялись. По дан'
являются уникальными для каждой последова'
ным программы Bestsel, c увеличением ионной
тельности пептидов. Полученные значения
силы раствора увеличивалось содержание α'
m/z, в свою очередь, анализировали програм'
спиралей в структуре белка (табл. 1). Так, для
мой PEAKS Studio 7.5 для идентификации пеп'
препаратов bS1 этот показатель увеличивался в
тидов.
три раза, одновременно с уменьшением содер'
Предварительный отбор идентифицирован'
жания β'поворотов и других вторичных струк'
ных пептидов с молекулярной массой >600 Да
тур. Очевидно, что существенные изменения
проводили согласно критерию оценки програм'
происходили в участках, отсутствующих во
мы PEAKS Studio 7.5 («Bioinformatics Solution
фрагменте bS1(49). Таким образом, увеличение
Inc.», Канада), т.е. значимыми считались пепти'
ионной силы раствора привело к более сущест'
ды, имеющие значение пороговой функции
венному изменению вторичной структуры для
T = -10 lgP > 15, где P - это вероятность того,
целого bS1 белка по сравнению с bS1(49).
что ложная идентификация в текущем поиске
Анализ денатурационных кривых для белков
достигнет такой же или лучшей оценки соответ'
bS1 и bS1(49). Изменения в структуре белков
ствия. Значение Т, равное >15, соответствует
bS1 и bS1(49) наблюдали по изменению интен'
p'критерию < 0,03 [42].
сивности флуоресценции триптофанов в ульт'
рафиолетовой области [40]. Снижение соотно'
шения I320/I380 указывало на то, что происходят
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
изменения в экспонированности и локальном
окружении триптофанов, связанные с форми'
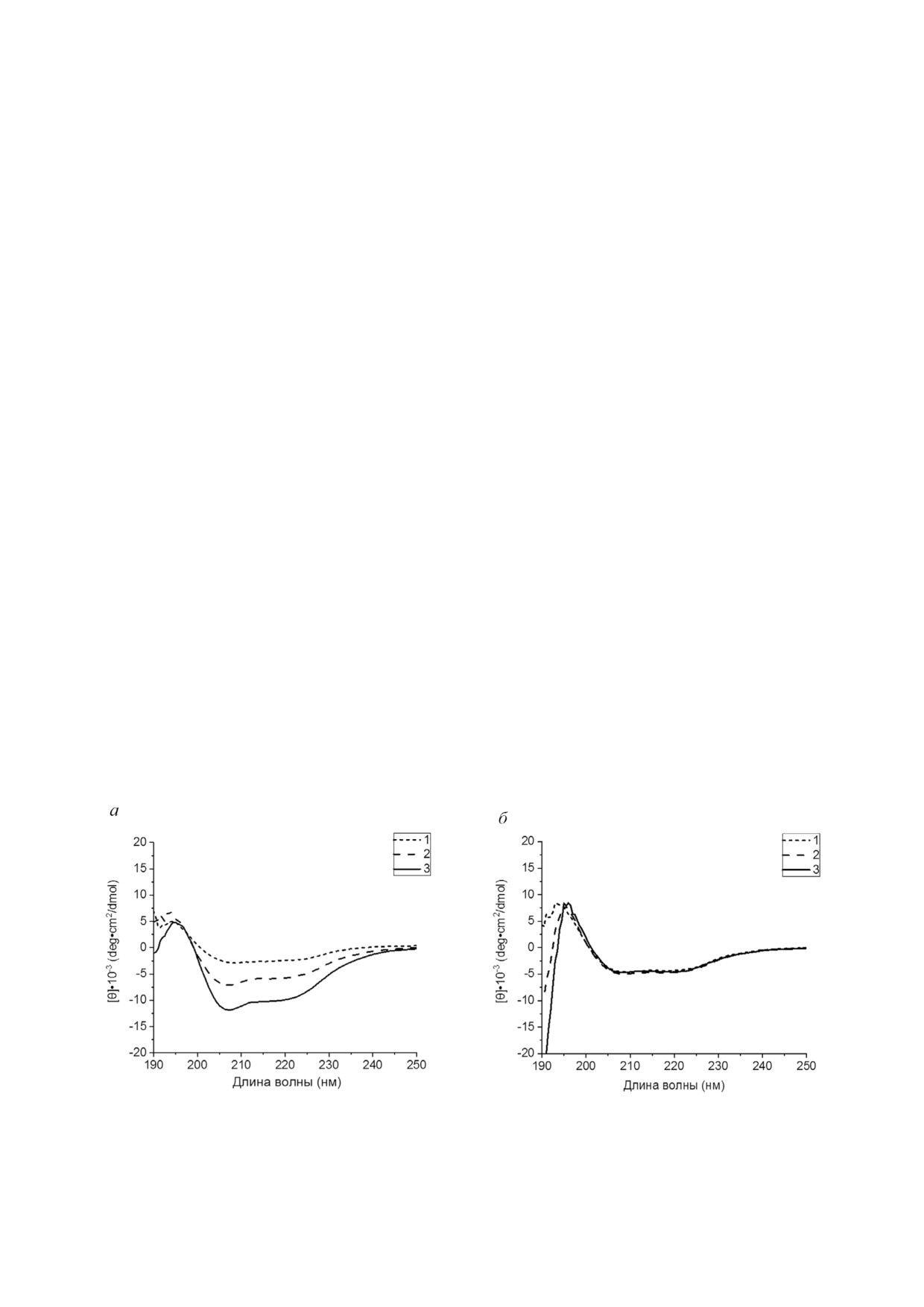
Спектры кругового дихроизма. Мы рассмот'
рованием интермедиатов при переходе от на'
рели эффекты различной ионной силы буфер'
тивного состояния белка к денатурированному
ных растворов на вторичную структуру белков
(рис. 2).
bS1 и bS1(49). Конформационные изменения
Поэтому сравнение кривых денатурации для
выявляли с помощью КД спектроскопии в даль'
bS1 и bS1(49) позволяет сделать вывод, что су'
bS1
bS1(49)
Рис. 1. Спектры КД в дальней УФ'области для препаратов bS1 и bS1(49) при различной ионной силе раствора. Обозначе'
ны данные, полученные для образцов белка в соответствующих буферных растворах с различной ионной силой: 1 - 25 мМ
HEPES'NaOH; 2 - 25 мМ HEPES'NaOH, 150 мМ NaCl; 3 - 25 мМ HEPES'NaOH, 2 M LiCl
БИОХИМИЯ том 85 вып. 3 2020
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО БЕЛКА bS1
403
Таблица 1. Параметры вторичной структуры, полученные программой Bestsel из анализа данных КД (диапазон
200-250 нм), для препаратов белков bS1 и bS1(49)
Элементы
bS1, 25 мМ
bS1, 25 мМ
bS1, 25 мМ
bS1(49), 25 мМ
bS1(49), 25 мМ
bS1(49), 25 мМ
вторичной
HEPES'NaOH
HEPES'NaOH,
HEPES'NaOH,
HEPES'NaOH
HEPES'NaOH,
HEPES NaOH,
структуры
150 мМ NaCl
2 М LiCl
150 мМ NaCl
2 М LiCl
α'Спирали
16%
42%
52%
31%
36%
41%
β'Структура
18%
11%
21%
18%
8%
0%
β'Поворот
20%
8%
0%
11%
11%
11%
Другие
46%
39%
27%
40%
45%
48%
щественные конформационные изменения бел'
ших экспериментах не было выявлено сущест'
ков, вызванные повышением температуры, про'
венных эффектов ионной силы раствора, с уче'
исходили с ростом температуры выше 80 °C.
том погрешности измерений, для образцов од'
Значимых различий между bS1 и bS1(49) не бы'
ного и того же белка. С ростом температуры
ло выявлено в температурных зависимостях из'
выше 80 °C интенсивность светорассеяния па'
менения I320/I380. В то же время следует отме'
дала, часть агрегатов оседала на дно кюветы, а
тить, что кривая изменения I320/I380 в буфере 3
новые уже не формировались. В то же время
расположена ниже соответствующих кривых
температурная зависимость агрегации для пре'
для буферных условий с низкой и средней ион'
паратов bS1 и bS1(49) несколько различалась.
ной силой (буферы 1 и 2), что указывает на сдвиг
Последний был более устойчив к формирова'
спектров флуоресценции триптофанов в длин'
нию агрегатов с повышением температуры.
новолновую область и большую доступность
Так, если значительный рост интенсивности
этих а.о. для растворителя.
светорассеяния для препаратов bS1 отмечали
Температурная зависимость накопления агреG
при 60 °C, то для bS1(49) аналогичное увеличе'
гатов. Мы исследовали температурную зависи'
ние агрегации происходило при температуре
мость интенсивности светорассеяния агрегатов
75 °C.
белков bS1 и bS1(49) соответственно для трех
ЭлектронноGмикроскопические изображения
различных буферных условий (рис. 3).
агрегатов. ЭМ является прямым методом визуа'
С увеличением температуры инкубации
лизации морфологии агрегатов (табл. 2).
росло количество регистрируемых фотонов,
По данным ЭМ видно, что изменение ион'
рассеянных от частиц, что указывало на увели'
ных условий от низкой (буфер 1), средней (бу'
чение количества и размеров агрегатов. В на'
фер 2) до высокой ионной силы (буфер 3) при
bS1
bS1(49)
1
1
2
2
3
3
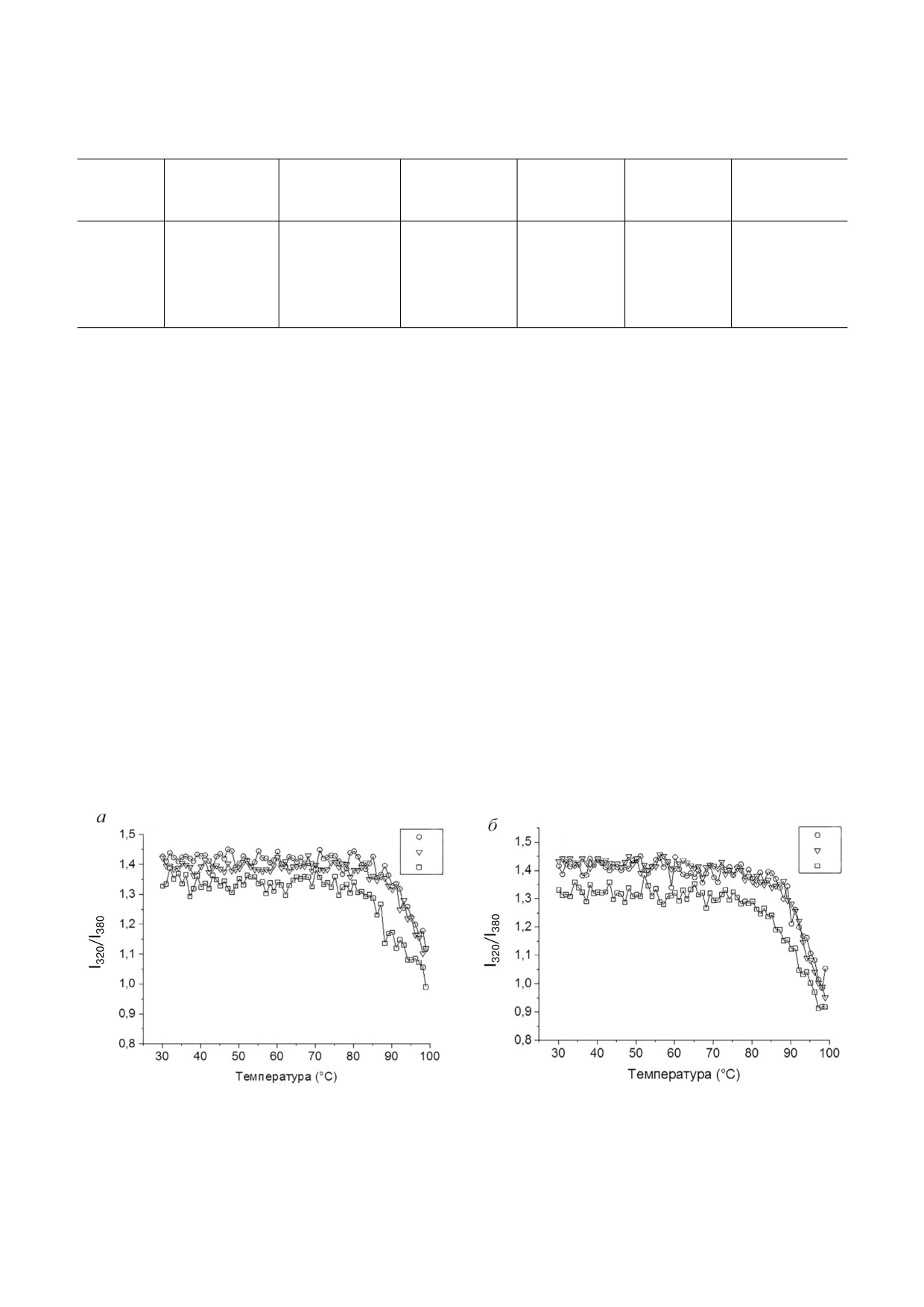
Рис. 2. Температурная зависимость изменения I320/I380, соответствующая конформационным изменениям в структуре бел'
ков bS1 (а) и bS1(49) (б), в буферных растворах с различной ионной силой: 1 - 25 мМ HEPES'NaOH; 2 - 25 мМ HEPES'
NaOH, 150 мМ NaCl; 3 - 25 мМ HEPES'NaOH, 2 M LiCl
БИОХИМИЯ том 85 вып. 3 2020
404
ГРИШИН и др.
bS1
bS1(49)
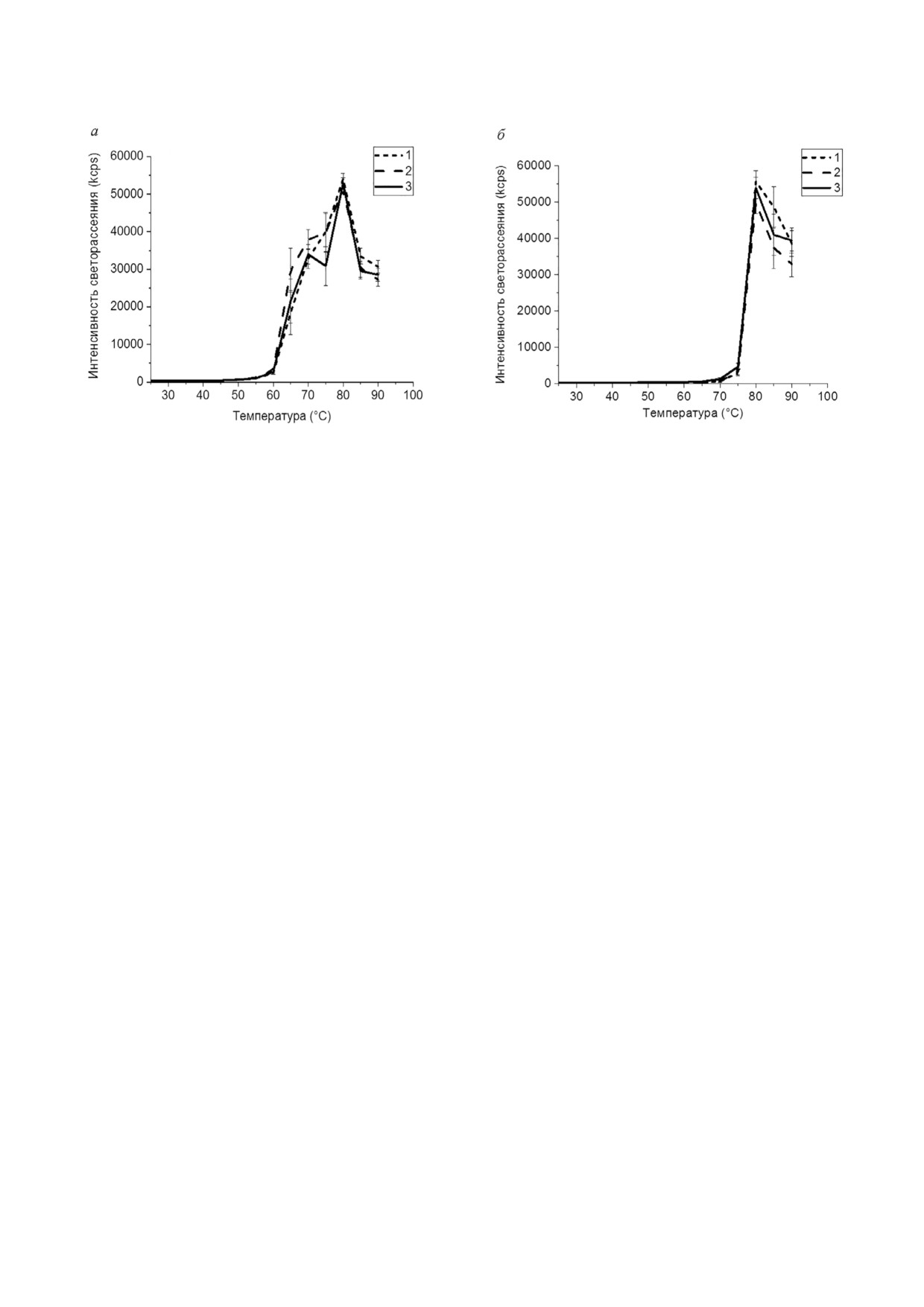
Рис. 3. Графики температурной зависимости интенсивности светорассеяния агрегатов для препаратов bS1 (а) и bS1(49) (б)
в буферных растворах с различной ионной силой: 1 - 25 мМ HEPES'NaOH; 2 - 25 мМ HEPES'NaOH, 150 мМ NaCl;
3 - 25 мМ HEPES'NaOH, 2 M LiCl
прогревании при 70 °С в течение 24 ч как для
нению с результатами для протеолиза кон'
белка bS1 T. thermophilus, так и для bS1(49) не
трольных образцов белков (рис. 4, a и в) было
приводило к видимым изменениям морфологии
идентифицировано больше фрагментов с моле'
препаратов. Во всех случаях на изображениях
кулярной массой 3000-7500 Да. Такие более
были видны большие агрегаты разного размера.
протяженные фрагменты в белковых агрегатах
Однако следует отметить, что компоненты агре'
соответствуют участкам молекул, защищенным
гатов белка bS1 имели большие размеры по
от действия протеаз, а значит содержащим
сравнению с его 49 кДа фрагментом. В исследуе'
аминокислотные последовательности, склон'
мых условиях оба препарата не формировали
ные к агрегации.
фибриллы.
В дальнейшем мы ранжировали значимые
Результаты ВЭЖХGМСGанализа участков,
пептиды, выявленные в гидролизатах контро'
склонных к агрегации в белке bS1 и его стабильG
лей и опытных образов белков bS1 и bS1(49), по
ном фрагменте bS1(49). С помощью ВЭЖХ про'
длине и нанесли самые длинные из них на по'
водится предварительное разделение пепти'
следовательность белка bS1, чтобы определить
дов, полученных после гидролиза различных
места, наиболее защищенные от воздействия
образцов белков. Всего было идентифицирова'
протеаз в контрольных препаратах и агрегатах
но 883 пептида в продуктах гидролиза агрега'
(рис. 5).
тов bS1 и 513 пептидов для контрольного об'
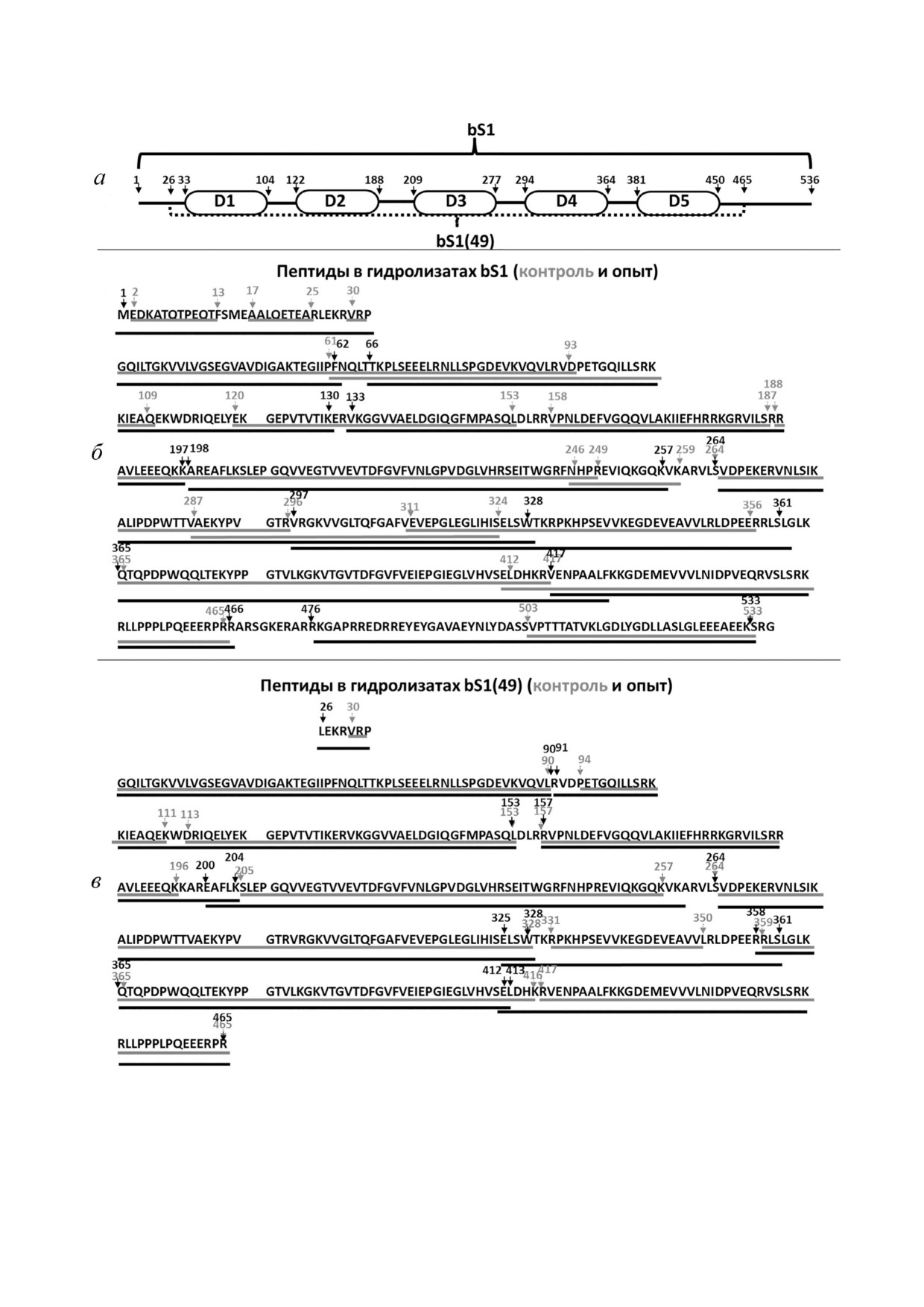
На рис. 5, б можно видеть, что фрагменты,
разца bS1. В то же время в продуктах гидроли'
выявленные в агрегатах опытных образцов, в
за агрегатов bS1(49) было выявлено 572 пепти'
целом длиннее, чем в контрольных образцах. В
да и 482 пептида для контрольного образца
то же время есть общие последовательности в
bS1(49).
контрольных и опытных образцах (агрегатах), а
На рис. 4 представлены результаты распре'
именно последовательности а.о.: 30-60, 66-92,
деления пептидов по их массам и относитель'
133-153, 158-188, 198-246, 264-287, 328-356,
ным интенсивностям, соответствующие бел'
365-412, 417-465, 503-533, которые не преры'
кам bS1 и bS1(49) в различных условиях. Преж'
ваются местами протеолитического расщепле'
де всего, следует подчеркнуть, что укорочен'
ния, что может указывать на их относительную
ный белок bS1(49) был менее склонен форми'
защищенность от протеолиза как в агрегатах,
ровать агрегаты в опыте по 24'часовой инкуба'
так и в контроле. С другой стороны, в контроль'
ции при 70 °C с 2M LiCl по сравнению с целым
ном образце bS1 не удалось идентифицировать в
белком bS1, о чем свидетельствует относитель'
продуктах протеолиза протяженную целую по'
но низкая интенсивность пиков, соответствую'
следовательность а.о. 466-502 на С'конце белка,
щая пептидам в гидролизатах агрегатов bS1(49)
так как она подвергается полному расщепле'
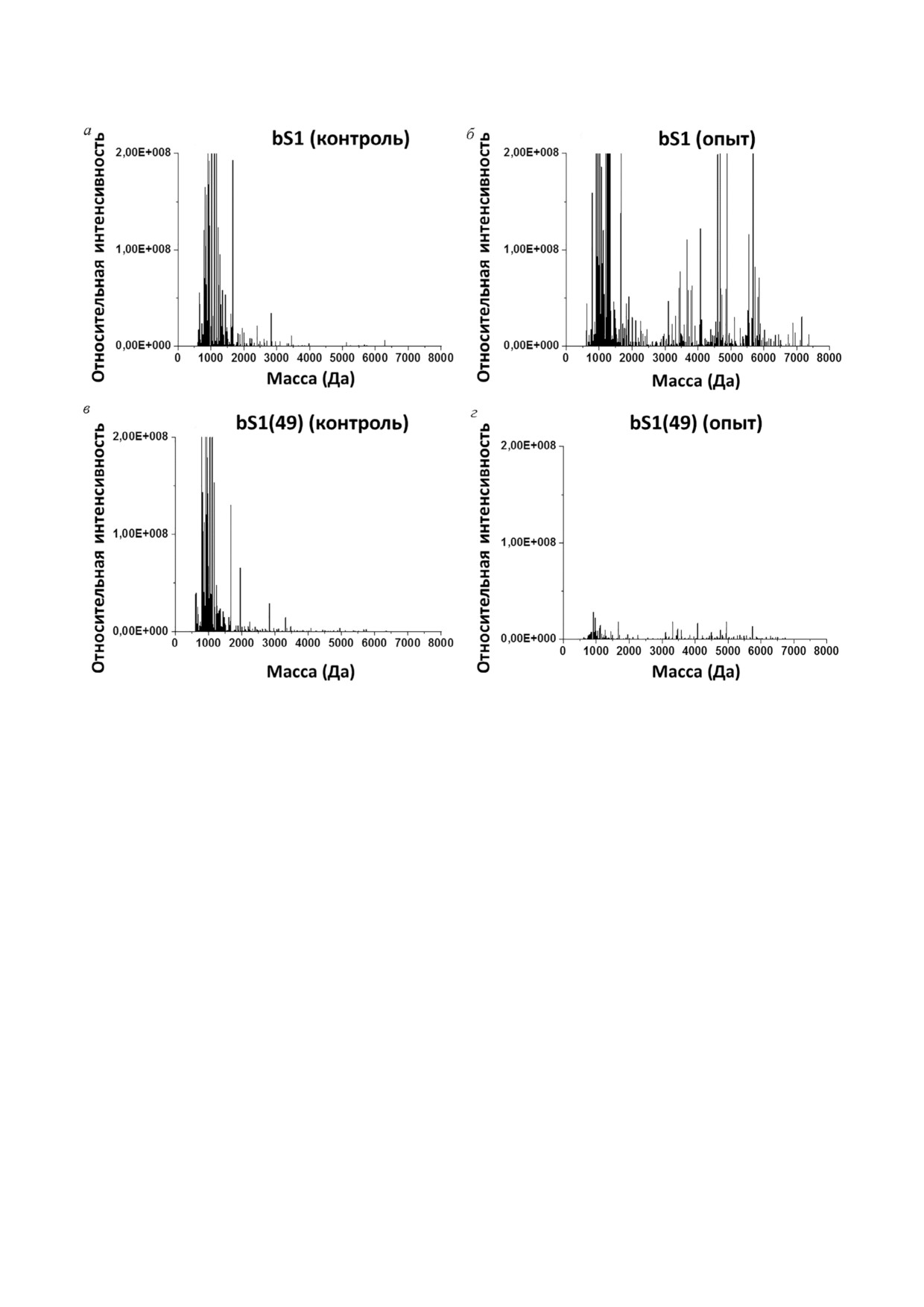
(рис. 4, г). Кроме того, на рис. 4, б и г показано,
нию, но большая ее часть (476-502 а.о.) сохра'
что в продуктах протеолиза агрегатов по срав'
няется во фрагменте 476-533 а.о., выявленной в
БИОХИМИЯ том 85 вып. 3 2020
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО БЕЛКА bS1
405
Таблица 2. Электронно'микроскопический анализ препаратов белка bS1 T. thermophilus и его 49 кДа фрагмента в различ'
ных ионных условиях
Препарат
bS1
bS1(49)
25 мМ HEPES'
NaOH, pH 7,5
(без прогревания)
Результаты ЭМ'анализа образцов после прогревания (70 °С, 24 ч)
25 мM HEPES'
NaOH, pH 7,5
25 мМ HEPES'
NaOH, pH 7,5;
150 мМ NaCl
25 мМ HEPES'
NaOH, pH 7,5;
2 M LiCl
БИОХИМИЯ том 85 вып. 3 2020
406
ГРИШИН и др.
Рис. 4. Сравнение результатов распределения пептидов по массам и относительным интенсивностям для белков bS1 (а) и
bS1(49) (в), а также белковых агрегатов, полученных после инкубации в буферном растворе с 2 М LiCl bS1 (б) и bS1(49) (г)
гидролизатах агрегатов. Такие последователь'
ров на вторичную структуру белков bS1 и
ности а.о. (1-29, 94-119, 298-327, 476-502), ко'
bS1(49). В ходе этого исследования было показа'
торые расщепляются в контрольных образцах,
но, что в отличие от bS1 изменение ионной си'
но остаются целыми в продуктах гидролиза аг'
лы буферного раствора не приводит к видимым
регатов, могут играть ключевую роль в агрега'
изменениям во вторичной структуре bS1(49).
ции белка bS1 в опыте при высокой концентра'
Этим объясняется и низкая склонность к агрега'
ции соли.
ции bS1(49) при изменениях ионной силы рас'
На рис. 5, в показано, что как в контроле, так
твора.
и в агрегатах белка bS1(49) в продуктах протео'
Сравнение выявленных сайтов протеолиза
лиза сохраняются длинные фрагменты, которые
(рис. 5, б, в) с распределением доменов в белках
имеют сходные сайты расщепления (небольшие
(рис. 5, а) указывает на то, что большинство сай'
вариации в длине гидролизатов обусловлены
тов протеолиза приходится на гибкие участки на
особенностями работы протеаз) [43]. Отсутствие
концах или вне доменов. Чтобы выявить воз'
существенных различий с контрольным образ'
можную роль S1'доменов в процессах агрега'
цом указывает на то, что в отличие от целого
ции, мы сравнили распределение всех иденти'
белка bS1 увеличение ионной силы раствора
фицированных пептидов, которые выявлены во
вплоть до 2M LiCl существенно не влияет на
внутренних последовательностях доменов (Д1:
способность к агрегации усеченного фрагмента
33-104, Д2: 122-188, Д3: 209-277, Д4: 294-364,
белка bS1(49). Эти результаты согласуются с
Д5: 381-450), для самих доменов и для анало'
данными КД, полученными при изучении влия'
гичного по длине неупорядоченного участка
ния различной ионной силы буферных раство'
белка bS1 (С: 449-518) (рис. 6, а).
БИОХИМИЯ том 85 вып. 3 2020
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО БЕЛКА bS1
407
Рис. 5. Схематическое представление доменной организации белков bS1 и bS1(49) из T. thermophilus (а) и результаты пеп'
тидного картирования после ВЭЖХ'МС анализа контрольных белков и агрегатов bS1 (б) и bS1(49) (в). Серым и черным
цветом подчеркнуты пептиды, выявленные в контрольных и опытных образцах соответственно. Последовательность а.о.
БИОХИМИЯ том 85 вып. 3 2020
408
ГРИШИН и др.
а
б
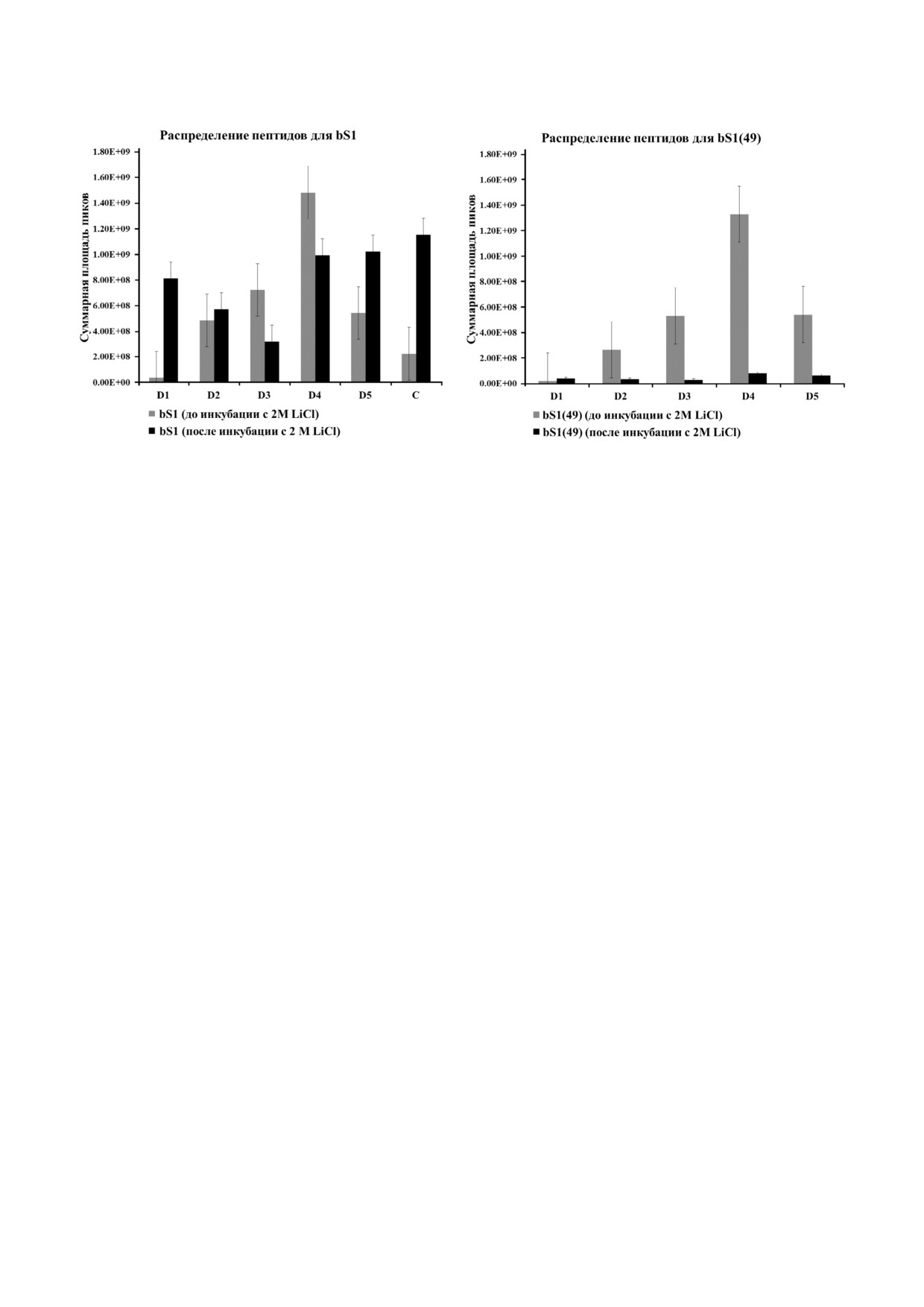
Рис. 6. Гистограммы распределения пептидов по белковым фрагментам, соответствующим доменам (D1: 33-104 а.о., D2:
122-188 а.о., D3: 209-277 а.о., D4: 294-364 а.о., D5: 381-450 а.о.), и внутри неструктурированного участка
(C: 449-518 а.о.) для белков bS1 (1-536 а.о) (а) и bS1(49) (26-465 а.о.) (б) до и после инкубации в буферном растворе с
2 М LiCl. Показаны планки погрешностей со стандартными ошибками
Из рис. 6, а следует, что в продуктах гидро'
показывает низкую стабильность, при длитель'
лиза агрегатов, полученных в опыте с 24'часо'
ном хранении происходит частичная деграда'
вой инкубацией при 70 °C в условиях с 2M LiCl,
ция белка, в связи с этим был выделен стабиль'
существенно возросла относительная доля
ный фрагмент белка bS1(49) [30]. В настоящей
пептидов, входящих в 1'й домен и участок
работе было проведено сравнение агрегацион'
449-518 а.о. Такое поведение свидетельствует о
ных свойств белков bS1 и bS1(49) из T. ther>
высокой степени защищенности данных пеп'
mophilus в растворах с различной ионной си'
тидов от воздействия протеаз. Увеличение за'
лой - низкой (25 мМ HEPES'NaOH, pH 7,5),
щищенности данных участков белка bS1 от
умеренной (в присутствии 150 мМ NaCl) и вы'
воздействия протеаз в случае длительной инку'
сокой (в присутствии 2 М LiCl). Следует отме'
бации при высокой концентрации соли можно
тить, что особый интерес представляло изуче'
объяснить тем, что эти участки белка (1'й до'
ние свойств белков в условиях раствора с высо'
мен и участок 449-518 а.о.) вовлечены в меж'
кой ионной силой, так как такие исследования
молекулярные взаимодействия в процессе аг'
для целого белка bS1 не проводили. Кроме то'
регации. Кроме того, наблюдается сходство
го, было необходимо проверить (возможные)
распределения пептидов между образцами bS1
стимулирующие фибрилогенез эффекты при'
и bS1(49) как внутри контрольной группы (рис.
сутствия 2 M LiCl, как это было сделано для
6, а), так и между образцами эксперименталь'
белка YB'1 [33]. Как подчеркивалось выше,
ной группы (рис. 6, б).
белки bS1 и bS1(49) мультидоменные, каждый
состоит из пяти S1'доменов, которые являются
структурными аналогами домена холодового
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
шока YB'1. Поэтому мы предположили, что
сходство во вторичной структуре ДХШ и S1'до'
Ранее было показано, что белок bS1 (60 кДа)
мена может иметь отражение в аналогичных
из T. thermophilus обладает высокой склон'
механизмах формирования фибрилл белками
ностью формировать ассоциаты в растворах с
YB'1 и bS1, в частности вызываться присут'
низкой и умеренной ионной силой [31]. Спо'
ствием в растворе 2 M LiCl.
собность белка bS1 к ассоциации обусловлена
В настоящем исследовании было показано,
особенностями структуры белка и выполняе'
что целый белок bS1 (1-536 а.о.) из T. ther>
мыми функциями, в частности формированием
mophilus более склонен к агрегации по сравне'
гомодимеров и связыванием с рибосомными
нию с его фрагментом bS1(49) (26-465 а.о.). Ме'
белками в 30S рибосомной субчастице. В опы'
тодом ДРС показано, что температура начала
тах in vitro целый bS1 белок из T. thermophilus
процесса агрегации для белков bS1 и bS1(49) -
БИОХИМИЯ том 85 вып. 3 2020
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО БЕЛКА bS1
409
60 °C и 75 °C соответственно. При этом денату'
фрагмента). Выяснение условий и механизмов
рация белков, оцененная по флуоресценции
агрегации рибосомного белка bS1 из T. ther>
триптофанов W111, W242, W284, W328 и W371
mophilus, в свою очередь, значимо для решения
(находящихся в центральной части белка), на'
этой задачи. Кроме того, результаты ВЭЖХ'МС
чинается при температуре выше 80 °С, т.е. про'
анализа продуктов протеолиза могут быть ис'
цесс агрегации начинается раньше, чем процесс
пользованы для выявления последовательнос'
денатурации доменов основной части белков.
тей белка bS1 из T. thermophilus, важных для бел'
Сравнительный анализ данных ВЭЖХ'МС
ковой мультимеризации, а также для выяснения
продуктов ограниченного протеолиза агрегатов
роли отдельных доменов N' и С'конца молеку'
целого белка bS1 показал, что участки 1-25 и
лы во взаимодействии с другими белками рибо'
466-502, отсутствующие в белке bS1(49), играют
сомы и мРНК [30].
важную роль в агрегации целого белка bS1.
По данным ЭМ агрегаты обоих белков сход'
ны по морфологии. Увеличение ионной силы
Финансирование. Работа выполнена при фи'
раствора вплоть до 2М LiCl не приводит к замет'
нансовой поддержке гранта РНФ (проект № 18'
ному формированию фибрилл, которые могут
14'00321) и при участии Центра коллективного
формировать, например, инсулин [44] или белок
пользования «Структурно'функциональные ис'
YB'1 [33] для обоих белков (bS1 и bS1(49)), как
следования белков и РНК» ИБ РАН (584307).
это предполагалось в начале исследования.
ЭМ исследования были проведены на базе обо'
T. thermophilus, как и E. coli, является модель'
рудования ЦКП (№ 670266).
ным объектом для изучения структуры бактери'
Конфликт интересов. Авторы заявляют об от'
альной рибосомы в целом и отдельных образую'
сутствии конфликта интересов.
щих ее белков [45, 46]. В связи с тем, что трех'
Соблюдение этических норм. Настоящая
мерная структура bS1 T. thermophilus до сих пор
статья не содержит каких'либо исследований с
не определена, актуальной задачей является
участием людей или использованием животных
кристаллизация белка (или его стабильного
в качестве объектов исследований.
СПИСОК ЛИТЕРАТУРЫ
1.
Chiti, F., and Dobson, C.M. (2006) Protein misfolding,
(1971) Correlation of
30S ribosomal proteins of
functional amyloid, and human disease, Annu. Rev.
Escherichia coli isolated in different laboratories, Mol. Gen.
Biochem., 75, 333-366.
Genet., 111, 327-330.
2.
Dovidchenko, N.V., and Galzitskaya, O.V.
(2015)
10. Ban, N., Beckmann, R., Cate, J.H., Dinman, J.D.,
Computational approaches to identification of aggregation
Dragon, F., Ellis, S.R., Lafontaine, D.L., Lindahl, L.,
sites and the mechanism of amyloid growth, Adv. Exp. Med.
Liljas, A., Lipton, J.M., McAlear, M.A., Moore, P.B.,
Biol., 855, 213-239.
Noller, H.F., Ortega, J., Panse, V.G., Ramakrishnan, V.,
3.
Galzitskaya, O. (2019) New mechanism of amyloid fibril
Spahn, C.M., Steitz, T.A., Tchorzewski, M., Tollervey, D.,
formation, Curr. Protein Pept. Sci., 20, 630-640.
Warren, A.J., Williamson, J.R., Wilson, D., Yonath, A.,
4.
Solovyov, K.V., Gasteva, A.A., Egorov, V.V., Aleinikova, T.D.,
and Yusupov, M. (2014) A new system for naming riboso'
Sirotkin, A.K., Shvartsman, A.L., and Shavlovsky, M.M.
mal proteins, Curr. Opin. Struct. Biol., 24, 165-169.
(2006) Role of the C'terminal fragment of human
11. Giri, L., and Subramanian, A.R. (1977) Hydrodynamic
transthyretin in abnormal fibrillogenesis, Biochemistry
properties of protein S1 from Escherichia coli ribosome,
(Moscow), 71, 543-549.
FEBS Lett., 81, 199-203.
5.
Pilla, S.P., Thomas, A., and Bahadur, R.P.
(2019)
12. Laughrea, M., and Moore, P.B. (1977) Physical properties
Dissecting macromolecular recognition sites in ribo'
of ribosomal protein S1 and its interaction with the 30 S
some: implication to its self'assembly, RNA Biol., 16,
ribosomal subunit of Escherichia coli, J. Mol. Biol., 112,
1300-1312.
399-421.
6.
Pechmann, S., Willmund, F., and Frydman, J. (2013) The
13. Tedin, K., Resch, A., and Bläsi, U. (1997) Requirements
ribosome as a hub for protein quality control, Mol. Cell, 49,
for ribosomal protein S1 for translation initiation of
411-421.
mRNAs with and without a 5′ leader sequence, Mol.
7.
Chaillou, T. (1985) Ribosome specialization and its poten'
Microbiol., 25, 189-199.
tial role in the control of protein translation and skeletal
14. Wower, I.K. (2000) Binding and cross'linking of tmRNA to
muscle size, J. Appl. Physiol., 127, 599-607.
ribosomal protein S1, on and off the Escherichia coli ribo'
8.
Schieber, G.L., and O’Brien, T.W. (1982) Extraction of
some, EMBO J., 19, 6612-6621.
proteins from the large subunit of bovine mitochondrial
15. Deryusheva, E.I., Machulin, A.V., Selivanova, O.M., and
ribosomes under nondenaturing conditions, J. Biol. Chem.,
Galzitskaya, O.V. (2017) Taxonomic distribution, repeats,
257, 8781-8787.
and functions of the S1 domain'containing proteins as
9.
Wittmann, H.G., Stöfflet, G., Hindennach, I., Kurland, C.G.,
members of the OB'fold family, Proteins, 85, 602-613.
Birge, E.A., Randall'Hazelbauer, L., Nomura, M.,
16. Bycroft, M., Hubbard, T.J.P., Proctor, M., Freund, S.M.V.,
Kaltschmidt, E., Mizushima, S., Traut, R.R., and Bickle, T.A.
and Murzin, A.G. (1997) The solution structure of the S1
8 БИОХИМИЯ том 85 вып. 3 2020
410
ГРИШИН и др.
RNA binding domain: a member of an ancient nucleic
32.
Theobald, D.L., Mitton'Fry, R.M., and Wuttke, D.S.
acid'binding fold, Cell, 88, 235-242.
(2003) Nucleic acid recognition by OB'fold proteins,
17.
Mihailovich, M., Militti, C., Gabaldón, T., and Gebauer, F.
Annu. Rev. Biophys. Biomol. Struct., 32, 115-133.
(2010) Eukaryotic cold shock domain proteins: highly ver'
33.
Selivanova, O.M., Guryanov, S.G., Enin, G.A., Skabkin, M.A.,
satile regulators of gene expression, BioEssays, 32,
Ovchinnikov, L.P., and Serdyuk, I.N. (2010) YB'1 is capa'
109-118.
ble of forming extended nanofibrils, Biochemistry
18.
Machulin, A.V., Deryusheva. E.I., Selivanova, O.M., and
(Moscow), 75, 115-120.
Galzitskaya, O.V. (2019) The number of domains in the
34.
Guryanov, S.G., Selivanova, O.M., Nikulin, A.D., Enin, G.A.,
ribosomal protein S1 as a hallmark of the phylogenetic
Melnik, B.S., Kretov, D.A., Serdyuk, I.N., and
grouping of bacteria, PLoS One, 14, e0221370.
Ovchinnikov, L.P. (2012) Formation of amyloid'like fibrils
19.
Дерюшева Е.И., Мачулин А.В., Селиванова О.М.,
by Y'box binding protein 1 (YB'1) is mediated by its cold
Сердюк И.Н. (2010) Семейство рибосомных белков S1
shock domain and modulated by disordered terminal
содержит уникальный консервативный домен, Моле>
domains, PLoS One, 7, e36969.
кулярная биология, 44, 728-734.
35.
William Studier, F., Rosenberg, A.H., Dunn, J.J., and
20.
Machulin, A., Deryusheva, E., Lobanov, M., and
Dubendorff, J.W. (1990) Use of T7 RNA polymerase to
Galzitskaya, O. (2019) Repeats in S1 proteins: flexibility
direct expression of cloned genes, Methods Enzymol., 185,
and tendency for intrinsic disorder, Int. J. Mol. Sci., 20,
60-89.
2377.
36.
Bradford, M.M. (1976) A rapid and sensitive method for
21.
Subramanian, A.R. (1983) Structure and functions of ribo'
the quantitation of microgram quantities of protein utiliz'
somal protein S1, Prog. Nucleic Acid Res. Mol. Biol., 28,
ing the principle of protein'dye binding, Anal. Biochem.,
101-142.
72, 248-254.
22.
Sengupta, J., Agrawal, R.K., and Frank, J.
(2001)
37.
Gill, S.C., and von Hippel, P.H. (1989) Calculation of pro'
Visualization of protein S1 within the 30S ribosomal sub'
tein extinction coefficients from amino acid sequence data,
unit and its interaction with messenger RNA, Proc. Natl.
Anal. Biochem., 182, 319-326.
Acad. Sci. USA, 98, 11991-11996.
38.
Savitzky, A., and Golay, M.J.E. (1964) Smoothing and dif'
23.
Boni, I.V., Artamonova, V.S., and Dreyfus, M. (2000) The
ferentiation of data by simplified least squares procedures,
last RNA'binding repeat of the Escherichia coli ribosomal
Anal. Biochem., 36, 1627-1639.
protein S1 is specifically involved in autogenous control, J.
39.
Micsonai, A., Wien, F., Bulyáki, É., Kun, J., Moussong, É.,
Bacteriol., 182, 5872-5879.
Lee, Y. H., Goto, Y., Réfrégiers, M., and Kardos, J.
24.
Salah, P., Bisaglia, M., Aliprandi, P., Uzan, M., Sizun, C.,
(2018) BeStSel: a web server for accurate protein sec'
and Bontems, F. (2009) Probing the relationship between
ondary structure prediction and fold recognition from the
gram'negative and gram'positive S1 proteins by sequence
circular dichroism spectra, Nucleic Acids Res., 46,
analysis, Nucleic Acids Res., 37, 5578-5588.
315-322.
25.
Loveland, A.B., and Korostelev, A.A. (2018) Structural
40.
Balobanov, V.A., Katina, N.S., Finkelstein, A.V., and
dynamics of protein S1 on the 70S ribosome visualized by
Bychkova, V.E. (2017) Intermediate states of apomyoglo'
ensemble cryo'EM, Methods, 137, 55-66.
bin: are they parts of the same area of conformations dia'
26.
Cava, F., Hidalgo, A., and Berenguer, J. (2009) Thermus
gram? Biochemistry (Moscow), 82, 625-631.
thermophilus as biological model, Extremophiles, 13,
41.
Surin, A.K., Grishin, S.Y., and Galzitskaya, O.V. (2019)
213-231.
Identification of amyloidogenic regions in the spine of
27.
Sedelnikova, S.E., Agalarov, S.C., Garber, M.B., and
insulin fibrils, Biochemistry (Moscow), 84, 47-55.
Yusupov, M.M. (1987) Proteins of the Thermus ther>
42.
Zhang, J., Xin, L., Shan, B., Chen, W., Xie, M., Yuen, D.,
mophilus ribosome purification of several individual pro'
Zhang, W., Zhang, Z., Lajoie, G.A., and Ma, B. (2012)
teins and crystallization of protein TL7, FEBS Lett., 220,
PEAKS DB: de novo sequencing assisted database search
227-230.
for sensitive and accurate peptide identification, Mol. Cell.
28.
Shiryaev, V.M., Selivanova, O.M., Hartsch, T., Nazimov, I.V.,
Proteomics, 11, M111.010587.
and Spirin, A.S. (2002) Ribosomal protein S1 from
43.
Катина Н.С., Суворина М.Ю., Григорашвили Е.И.,
Thermus thermophilus: its detection, identification and
Марченков В.В., Рябова Н.А., Никулин А.Д.,
overproduction 1, FEBS Lett., 525, 88-92.
Сурин А.К. (2016) Определение участков апомиогло'
29.
Selivanova, O.M., Shiryaev, V.M., Tiktopulo, E.I.,
бина, образующих межмолекулярные взаимодей'
Potekhin, S.A., and Spirin, A.S. (2003) Compact globular
ствия в амилоидных агрегатах методом масс'спектро'
structure of Thermus thermophilus ribosomal protein S1 in
метрии высокого разрешения, Масс>спектрометрия,
solution, J. Biol. Chem., 278, 36311-36314.
13, 225-234.
30.
Selivanova, O.M., Fedorova, Y.Y., and Serduyk, I.N.
44.
Селиванова О.М., Гришин С.Ю., Глякина А.В., Сад'
(2007) Proteolysis of ribosomal protein S1 from
гян А.С., Ушакова Н.И., Галзитская О.В. (2018) Ана'
Escherichia coli and Thermus thermophilus leads to forma'
лиз аналогов инсулина и стратегия их дальнейшей
tion of two different fragment, Biochemistry (Moscow), 72,
разработки, Успехи биологической химии, 58, 313-346.
1225-1232.
45.
Yusupov, M.M., Garber, M.B., Vasiliev, V.D., and Spirin, A.S.
31.
Тимченко А.А., Ширяев В.М., Федорова Ю.Ю., Киха'
(1991) Thermus thermophilus ribosomes for crystallograph'
ра Х., Кимура К., Виллумайт Р., Гарамус В.М., Селива'
ic studies, Biochimie, 73, 887-897.
нова О.М. (2007) Конформация рибосомного белка S1
46.
Tung, C.S., and Sanbonmatsu, K.Y. (2004). Atomic model
из Thermus thermophilus в растворе при разных ионных
of the Thermus thermophilus 70S ribosome developed in sil>
условиях, Биофизика, 52, 216-222.
ico, Biophys. J., 87, 2714-2722.
БИОХИМИЯ том 85 вып. 3 2020
СРАВНИТЕЛЬНЫЙ АНАЛИЗ АГРЕГАЦИИ РИБОСОМНОГО БЕЛКА bS1
411
COMPARATIVE ANALYSIS OF THE AGGREGATION
OF THE bS1 RIBOSOMAL PROTEIN AND ITS STABLE
FRAGMENT FROM Thermus thermophilus
S. Yu. Grishin1, U. F. Dzhus1, O. M. Selivanova1,
V. A. Balobanov1, A. K. Surin1,2,3, and O. V. Galzitskaya1,4*
1 Institute of Protein Research, Russian Academy of Sciences,
142290 Pushchino, Moscow Region, Russia; E>mail: ogalzit@vega.protres.ru
2 State Research Center for Applied Microbiology and Biotechnology,
142279 Obolensk, Moscow Region, Russia; E>mail: alan@vega.protres.ru
3 The Branch of the Institute of Bioorganic Chemistry, Russian Academy of Sciences,
142290 Pushchino, Moscow Region, Russia
4 Institute of Theoretical and Experimental Biophysics, Russian Academy of Sciences,
142290 Pushchino, Moscow Region, Russia
Received October 21, 2019
Revised December 24, 2019
Accepted January 11, 2020
The multidomain bacterial protein bS1 is the largest and functionally important ribosome protein of subunit 30S that
interacts with both mRNA and proteins. It is known that bS1 protein has a high tendency to form associates, but this
process has not been studied in detail. We isolated and purified Thermus thermophilus recombinant bS1 ribosomal pro'
tein and its stable truncated bS1(49) fragment using superproducing Escherichia coli strains. Using fluorescence spec'
troscopy, dynamic light scattering, and high'performance liquid chromatography combined with mass'spectrometry
analysis of the limited proteolysis products, it has been shown that unstructured regions at the N' and C'ends of the
bS1 protein can play a key role in its aggregation. At that, the truncated bS1(49) fragment is less prone to form aggre'
gates compared to the whole T. thermophilus protein. The revealed features can be used to obtain protein crystals and
elucidate the structure of a stable fragment of the bS1 protein.
Keywords: protein aggregation, ribosomal protein, bS1, domain, Thermus thermophilus, ionic strength of a solution,
mass'spectrometry
БИОХИМИЯ том 85 вып. 3 2020
8*