БИОХИМИЯ, 2020, том 85, вып. 5, с. 620 - 636
УДК 577.2
МЕМБРАННЫЕ КОНТАКТЫ В СОСТАВЕ ПЛАЗМОДЕСМ:
СТРУКТУРНЫЕ КОМПОНЕНТЫ И ИХ ФУНКЦИИ
Обзор
© 2020
А.В. Панкратенко1, А.К. Атабекова1, С.Ю. Морозов1,2, А.Г. Соловьев1,2,3,4*
1 Московский государственный университет им. М.В. Ломоносова,
биологический факультет, кафедра вирусологии, 119991 Москва, Россия
2 Московский государственный университет им. М.В. Ломоносова, НИИ физико(химической биологии
им. А.Н. Белозерского, 119992 Москва, Россия; электронная почта: solovyev@belozersky.msu.ru
3 Институт Молекулярной Медицины, Первый Московский Государственный
Медицинский Университет им. И.М. Сеченова, 119991 Москва, Россия
4 Всероссийский Научно(Исследовательский Институт
Сельскохозяйственной Биотехнологии, 127550 Москва, Россия
Поступила в редакцию 12.02.2020
После доработки 10.03.2020
Принята к публикации 16.03.2020
Плазмодесмы представляют собой каналы, соединяющие клетки в тканях растений. В плазмодесмах проис
ходит соединение цитоплазмы, плазматической мембраны (ПМ) и эндоплазматического ретикулума (ЭПР)
соседних клеток. Через плазмодесмы происходит активный транспорт макромолекул, таких как белки и
РНК, что обеспечивает функциональную целостность тканей растений и передачу сигналов, необходимых
для индивидуального развития и ответов на внешние воздействия. Исследования последних лет показали,
что в состав плазмодесм входят мембранные контакты (МК), специализированные структуры, которые
формируются при участии ряда белковых компонентов, соединяющих мембраны ЭПР и ПМ. В общем слу
чае, как показано преимущественно для клеток животных, МК между ЭПР и ПМ участвуют в транспорте
липидных и белковых компонентов между этими мембранными компартментами, а также в поддержании
структурной целостности ЭПР и ответе на стрессы. Структура МК в составе плазмодесм растений изучена
существенно хуже, и в настоящее время активные исследования структурных элементов плазмодесм, обес
печивающих связь между ЭПР и ПМ в составе этих органелл, только начинают разворачиваться. В настоя
щем обзоре рассмотрены белковые компоненты, для которых показано или предполагается участие в фор
мировании МК в плазмодесмах, их структурные и функциональные особенности. Кроме того, обсуждается
роль цитоскелета, липидных микродоменов в составе мембран и компонентов клеточной стенки в поддер
жании структуры МК плазмодесм и ее ремоделировании в ответ на различные биотические и абиотические
воздействия.
КЛЮЧЕВЫЕ СЛОВА: плазмодесмы, мембранные контакты, эндоплазматический ретикулум, плазмати
ческая мембрана, мембранные микродомены, белки плазмодесм, белки мембранных контактов, вирусы
растений.
DOI: 10.31857/S0320972520050024
ВВЕДЕНИЕ
требует взаимодействия между органеллами.
Значительная роль в этом взаимодействии при
Координация различных метаболических
надлежит процессам, протекающим в зонах
процессов, протекающих в клетках растений, мембранных контактов (МК), - структурах,
Принятые сокращения: ЖК - жидкокристаллический; МК - мембранный контакт; ПМ - плазматическая мем
брана; ЭПР - эндоплазматический ретикулум; GIPC - гликозилинозитолфосфорил церамиды (glycosyl inositol phospho
ryl ceramides); GPI - гликозилфосфатидилинозитол (glycosylphosphatidylinositol); Lo - упорядоченные ЖК микродомены
мембран; LTP - липид транспортирующие белки (lipid transfer proteins); PA - фосфатидная кислота (phosphatidic acid);
PI(4,5)P2 - фосфатидилинозитол 4,5 бисфосфат (phosphatidylinositol 4,5 bisphosphate); PI(4)P - фосфатидилинозитол 4
фосфат (phosphatidylinositol 4 phosphate); PIP - фосфатидилинозитолфосфаты (phosphatidylinositol phospate); PS - фос
фатидилсерин (phosphatidylserine); PDCB - семейство белков плазмодесм, связывающих каллозу (plasmodesmata callose
binding family); RTNLB - ретикулон подобные белки (reticulon like proteins); SEL - предельная пропускная способность
(size exclusion limit).
* Адресат для корреспонденции.
620
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
621
обеспечивающих физическое взаимодействие и
ниманию механизмов межклеточной коммуни
транспорт различных молекул между состыко
кации в растениях, основанной на транспорте
ванными мембранами двух органелл.
через плазмодесмы. Ниже рассмотрены имею
Различные типы МК были обнаружены в
щиеся к настоящему времени данные о структу
клетках млекопитающих, дрожжей, растений и,
ре и функциях МК в составе плазмодесм.
по всей видимости, являются эволюционно
консервативными для эукариот [1, 2]. МК ха
рактеризуются малым (∼10-30 нм) расстоянием
БЕЛКОВЫЕ КОМПОНЕНТЫ
между мембранами, а также специфическим ли
МК ПЛАЗМОДЕСМ
пидным и белковым составом, в частности, на
личием связующих элементов белковой приро
Несмотря на то, что белки, локализующиеся
ды, благодаря которым мембраны удерживают
в плазмодесмах, были объектом пристального
ся вместе, не сливаясь [3]. Такое строение МК
интереса исследователей, и для их идентифика
позволяет органеллам функционально взаимо
ции применяли самые различные подходы [14],
действовать друг с другом посредством кальций
долгое время представления о белковом составе
зависимых сигналов, обмена молекулами липи
плазмодесм оставались довольно ограниченны
дов или транс взаимодействий белковых ком
ми. Значительный прорыв произошел в послед
плексов, которые, находясь на одной мембране,
ние годы благодаря разработке новых стратегий
могут регулировать процессы, протекающие на
анализа на основе масс спектрометрии, субкле
другой [4, 5]. В растительных клетках МК участ
точного фракционирования и других методов
вуют в целом ряде процессов, таких как регуля
[15-17].
ция развития [6], межклеточная коммуника
На сегодняшний день установлено, что в
ция [7], а также ответы на стресс, в которые во
функционировании плазмодесм принимает
влекаются пластиды, митохондрии, пероксисо
участие множество различных белков, как не
мы и другие органеллы клетки [2, 8, 9].
посредственно локализующихся в этих структу
Особым типом МК, характерным только для
рах, так и регулирующих их работу извне [15,
растений, являются МК в составе плазмодесм -
16]. В частности, было показано, что в плазмо
цитоплазматических каналов, которые соединя
десмах локализуются белки семейств PDLP (се
ют растительные клетки и представляют собой
мейство белков, локализующихся в плазмодес
основной путь межклеточной коммуникации и
мах, plasmodesmata located protein family) [18],
обмена веществами в тканях растений [10]. По
влияющие на пропускную способность плазмо
скольку плазмодесмы, имеющие диаметр
десм и, по всей видимости, участвующие в раз
∼30-50 нм, образованы плазматической мем
витии системной приобретенной устойчивости
браной (ПМ) и содержат в центре трубочку ЭПР
растений [19], и семейство белков плазмодесм,
(десмотрубочку), они представляют собой сис
связывающих каллозу (PDCB, plasmodesmata
тему (длиной обычно ∼500 нм [11]) из двух
callose binding family) [20], а также рецептор по
мембранных трубок, вставленных одна в дру
добные киназы [21, 22], гермин подобные белки
гую. ПМ и мембрана десмотрубочки расположе
(GLP, germin like proteins) [23] и ретикулон по
ны чрезвычайно близко друг к другу (на рассто
добные белки (RTNLB) [24].
янии ~10-15 нм [12], а в некоторых случаях это
Природа белковых структур, связующих
расстояние может достигать 3 нм [13]) и по всей
мембраны плазмалеммы и десмотрубочки в
длине канала плазмодесм скреплены неизвест
плазмодесмах, до сих пор не установлена. Одна
ными элементами, подобными спицам колеса и
ко, основываясь на структуре уже изученных
имеющими, по всей видимости, белковую при
МК [1, 2], можно предположить, что белки МК
роду [12]. Таким образом, система из двух мем
в составе плазмодесм имеют следующие харак
бранных структур в составе плазмодесмы может
терные черты: они (1) избирательно концентри
рассматриваться как специализированный МК
руются в зонах МК, (2) содержат ЭПР якорные
[1]. В настоящее время сформировалось пред
домены, (3) имеют липид связывающие моти
ставление о том, что именно компоненты МК в
вы, позволяющие им взаимодействовать с липи
составе плазмодесм организуют и поддержива
дами ПМ, (4) обладают достаточным размером,
ют их внутреннюю структуру, а также участвуют
чтобы обеспечивать контакт мембран через раз
в изменении функционального состояния плаз
деляющее их цитозольное пространство напря
модесм в ответ на различные воздействия. В со
мую (или, возможно, опосредованно через взаи
ответствии с этими взглядами, выявление моле
модействие с другими белками). Также можно
кулярных компонентов МК в составе плазмо
предположить, что в образовании МК в составе
десм и расшифровка механизмов их функцио
плазмодесм задействованы белки различных се
нирования может стать одним из ключей к по
мейств, как характерных непосредственно для
БИОХИМИЯ том 85 вып. 5 2020
622
ПАНКРАТЕНКО и др.
плазмодесм, так и функционирующих в других
ПМ, содержащими мотив FFAT (two phenylala
типах МК [1]. Среди семейств растительных
nines in an acid tract), тем самым обеспечивая об
белков известно по меньшей мере три, которые
разование МК между ПМ и ЭПР [29] (рисунок).
участвуют в создании МК между ЭПР и ПМ:
У различных эукариот с белками VAP могут взаи
белки VAP (the vesicle associated membrane pro
модействовать белки, которые содержат мотив
tein (VAMP) associated protein) [6], синаптотаг
StART (sterol binding steroidogenic acute regulato
мины (SYT) [25], а также MCTP [26] (рисунок).
ry (StAR) related lipid transfer motif) и участвуют
Семейство VAP. Белки семейства VAP кон
в переносе липидов между мембранами [3], а
сервативны для эукариот и включают С конце
также белки, содержащие домен PH (phospho
вой трансмембранный домен, центральный
inositide binding pleckstrin homology domain)
coiled coil домен и N концевой домен MSP
и/или оксистерол связывающий мотив, кото
(major sperm protein domain) [27]. Домен MSP
рые предположительно необходимы для состы
способен взаимодействовать с фосфатидилино
ковки мембран в зоне контакта [30]. Показано
зитол 4 фосфатом [PI(4)P] и фосфатидилсери
взаимодействие VAP27 с белками RTNLB3 и
ном (PS) плазмалеммы [28], а также с белками
RTNLB6 [31] (рисунок).
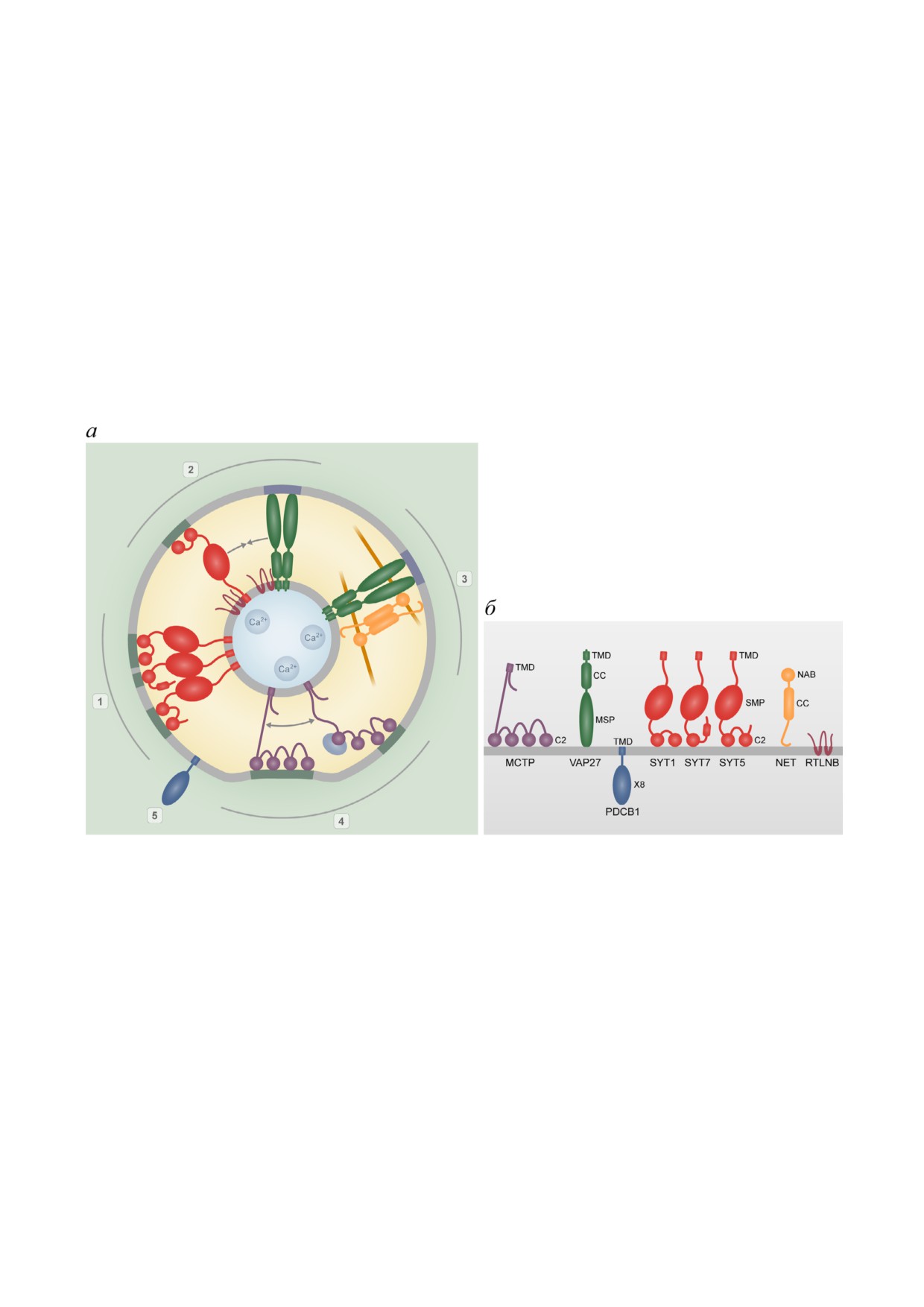
Предполагаемые компоненты мембранных контактов в составе плазмодесм. а - Схематическое изображение аксиальной
проекции канала плазмодесм. Показано пространственное расположение белков и белковых комплексов, образующих
контакты между мембраной десмотрубочки (в центре) и плазматической мембраной, прилежащей к клеточной стенке.
(1) Межмембранный контакт через комплекс белков SYT1, SYT5 и SYT7. (2) Белки SYT1 и VAP27 напрямую взаимодей
ствуют с ретикулонами семейства RTNLB и опосредованно - друг с другом. Последнее взаимодействие отмечено стрел
ками. (3) Межмембранный контакт через комплекс белков VAP27 и NET. VAP27 взаимодействует с белком семейства NET
через MSP домен, NET связывается с актином через домен NAB и с мембраной через С концевой участок. VAP27 взаимо
действует с липидами и/или белками плазмалеммы, а также с элементами клеточной стенки. (4) Межмембранный кон
такт через MCTP белки. MCTP белок взаимодействует с отрицательно заряженными липидами мембраны через С2 доме
ны. Взаимодействие с регуляторными белками или изменение концентрации ионов Ca2+ приводит к изменению конфор
мации MCTP и сокращению или увеличению расстояния между плазмалеммой и десмотрубочкой. Обратимое изменение
конформации MCTP показано стрелкой. (5) GPI заякоренный белок PDCB1, имеющий сродство к Lo микродоменам
мембраны, связывающийся с каллозой своим Х8 доменом и участвующий в процессах отложения каллозы. Мобилизация
белка PDCB1 в плазмодесмы может происходить в ответ на индуцированное перераспределение липидов в бислое и
образование новых микродоменов. Выделены участки плазмалеммы, обогащенные отрицательно заряженными липида
ми, которые взаимодействуют с С2 доменами, и зоны контакта VAP27, плазмалеммы и клеточной стенки.
Ca2+ - ионы кальция. б - Белки, формирующие мембранные контакты в составе плазмодесм, и их домены. TMD - транс
мембранный домен, C2 - C2 домен, CC - coiled coil домен, MSP - major sperm protein домен, X8 - X8 домен, SMP -
synaptotagmin like mitochondrial lipid binding protein домен, NAB - NET actin binding домен. (С цветным вариантом ри
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
623
В геноме Arabidopsis thaliana обнаружено 10
кул от мембраны к мембране [36, 37]; 4) два
генов, представляющих семейство VAP27 у рас
С концевых С2 (Ca2+ dependent lipid binding
тений. Нарушения в уровне экспрессии опреде
domain) домена. Трансмембранный домен и до
ленных белков этого семейства приводят к
мен SMP, по видимому, ограничивают локализа
плейотропным дефектам в развитии семян,
цию SYT1 в зонах контакта ЭПР и ПМ, в то вре
пыльцы и корневых волосков [6]. Белки VAP27
мя как С2 домены обеспечивают электростати
подразделяются на три клады. Клада II характе
ческое взаимодействие белка с отрицательно за
ризуется отсутствием трансмембранного доме
ряженными фосфолипидами плазмалеммы [25].
на; ее представители являются периферически
В клетках SYT1, по всей видимости, функци
ми белками плазмалеммы и не локализуются в
онирует в составе комплексов, т.к. молекулы
зонах МК между ЭПР и ПМ. Представители
SYT1 способны взаимодействовать друг с дру
клад I и III являются интегральными белками
гом, а также с белками SYT5 и SYT7, которые
ЭПР и участвуют в образовании МК; для белка
локализуются в зонах МК между ЭПР и плазма
VAP27 1 показано взаимодействие через MSP
леммой [34] (рисунок). Действуя вместе, эти
домен с белком NET3C, представителем расти
белки обеспечивают состыковку мембран и
тельного суперсемейства NET, которое обеспе
формирование неподвижных трубочек ЭПР, а
чивает связь актинового цитоскелета с различ
также сжатие ЭПР перед входом в плазмодесмы
ными мембранными компартментами клетки
для образования десмотрубочек в этих каналах.
[32]. Следует отметить, что оба белка, по види
Отсутствие функционального комплекса
мому, функционируют в виде ди/олигомеров
SYT1-SYT5-SYT7 приводит к нарушениям в
[27]. Для образования МК между ЭПР и плазма
морфологии ЭПР и влияет на межклеточный
леммой необходимы как трансмембранный до
транспорт и внутриклеточную локализацию
мен, так и домен MSP белка VAP27; кроме того,
транспортного белка вируса YoMV (Youcai
в этот процесс, по всей видимости, вовлечены
Mosaic Virus); возможно, это свидетельствует об
система цитоскелета и клеточной стенки [6, 27]
участии SYT белков в процессах активного
(рисунок).
транспорта липидов и мембранных белков в
На сегодняшний день не получено однознач
десмотрубочках плазмодесм [34].
ных доказательств существования пула VAP27
Ряд других данных также указывает на роль
и/или NET3C в плазмодесмах. Следует отме
SYT в функционировании плазмодесм: так,
тить, однако, что другой представитель семей
например, SYT1 перемещается к плазмодесмам
ства NET, белок NET1A, локализуется в плазмо
во время вирусной инфекции [7], а утрата его
десмах [32]. Также показано опосредованное
функции приводит к изменениям в регуляции
взаимодействие VAP27 с белком SYT1 A. thaliana
защитных ответов при инфекции [19]. Наконец,
из семейства синаптотагминов, который участ
в протеоме плазмодесм A. thaliana обнаружено
вует в ряде процессов в плазмодесмах [25, 33].
несколько SYT белков [1, 17].
Семейство SYT. Синаптотагмины растений
SYT1 физически контактирует с рядом бел
(белки SYT) охарактеризованы относительно
ков, таких как стигмастерол связующий белок
недавно; известно, что представители этого се
ROSY1 [38], ретикулоны RTNLB3 и RTNLB6,
мейства участвуют в образовании МК между
которые обнаруживаются в плазмодесмах и не
ЭПР и ПМ [7, 34] и гомологичны белкам E Syt и
обходимы для формирования трубочек ЭПР и
Tcb, которые являются связующими элемента
поддержания кривизны мембраны ЭПР [31]
ми в зонах МК клеток млекопитающих и дрож
(рисунок), а также белок VST (VAP RELATED
жей [35]. В геноме A. thaliana обнаружено семь
SUPPRESSOR OF TMM), который задейство
генов SYT (SYT1-SYT7) [34], и наиболее хорошо
ван в сигналинге с участием киназы ERECTA
изученным является белок SYT1.
LIKE2 (ERL2) из семейства LRR RLK (leucine
SYT1 содержит 1) N концевой трансмем
rich repeat receptor like kinase), локализующейся
бранный домен, заякоренный в ЭПР; 2) линкер
в ПМ [39]. Кроме того, SYT1 взаимодействует с
ный участок длиною ~40 аминокислот, что соот
комплексом SNARE (soluble N ethylmaleimide
ветствует дистанции в ~15 нм и может быть до
sensitive factor attachment protein receptor), участ
статочным для состыковки мембран сквозь ци
вующим в слиянии везикул [19]; возможно,
тозольное пространство в области МК; 3) цито
SYT1 регулирует этот процесс Ca2+ зависимым
плазматический домен SMP (synaptotagmin like
способом, аналогично белкам SYT млекопитаю
mitochondrial lipid binding protein domain), кото
щих [35].
рый необходим для димеризации E Syt в клетках
Изменение морфологии ЭПР при функцио
млекопитающих и осуществляет перенос липи
нальной инактивации SYT1 [7] сопровождается
дов между органеллами, образуя, по всей види
частичной деполимеризацией актинового ци
мости, гидрофобный канал для переноса моле
тоскелета и повышением чувствительности рас
БИОХИМИЯ том 85 вып. 5 2020
624
ПАНКРАТЕНКО и др.
тений к абиотическим стрессам, связанным с
(FTIP) и AtMCTP15/QUIRKY (QKY), были ра
изменением тургора клеток, например, осмоти
нее описаны как белки плазмодесм, участвую
ческому стрессу или замораживанию [40, 41], а
щие в межклеточном транспорте сигналов раз
также к механическому стрессу. При механичес
вития [46, 47].
ком стрессе возрастает экспрессия SYT1. Таким
Белки MCTP структурно сходны с синапто
образом, можно предположить, что SYT1, веро
тагминами и содержат несколько C концевых
ятно, является элементом системы механоре
трансмембранных доменов, заякоренных в ЭПР,
цепции в растительной клетке. Зоны МК между
и, возможно, участвующих в поддержании оп
ЭПР и плазмалеммой могут служить своеобраз
ределенной степени изгиба его мембраны, а так
ными деформируемыми платформами, коорди
же от трех до четырех доменов С2 в N концевой
нирующими ответ кортикального ЭПР и цито
части, способных связываться с отрицательно
скелета на механический стресс, что позволяло
заряженными фосфолипидами ПМ, в частнос
бы быстро минимизировать нагрузку на плазма
ти, с PI(4)P и с PS. Вероятно, наличие несколь
лемму, возникающую в результате механическо
ких С2 доменов позволяет белкам MCTP изме
го стресса. Альтернативная модель, основанная
нять расстояние между мембранами МК за счет
на данных, полученных для клеток млекопита
изменения конформации в ответ на различные
ющих, предполагает, что механический стимул
сигналы, например, изменение уровня Ca2+,
приводит к сокращению расстояния между ЭПР
состава ПМ или появление каких либо транс
и ПМ, тем самым, вероятно, усиливая структур
портируемых мобильных сигналов [26] (рису
ную стабилизацию и перенос сигналов между
нок). Это позволяло бы координировать межк
этими компартментами [25].
леточный транспорт и взаимодействия между
Еще одна гипотеза предполагает участие
органеллами (вероятно, при участии и других
SYT1 в передаче кальциевых сигналов по анало
белков).
гии с E Syt белками МК млекопитающих. Изве
Установлено, что AtMCTP1/FTIP является
стно, что у млекопитающих Ca2+ сигналы сти
партнером белка FT (Flowering Locus T) и необ
мулируют образование и стабилизацию МК или
ходим для его загрузки во флоэму
[46];
сокращение расстояния между ЭПР и ПМ [42,
AtMCTP15/QUIRKY взаимодействует с рецеп
43], что сопровождается высокоафинным свя
тор подобной киназой STRUBBELIG, локали
зыванием Ca2+ белками E Syt, их кластеризаци
зующейся в ПМ и, в том числе, в плазмодесмах
ей и усилением электростатического взаимодей
[47]; белки AtMCTP3/AtMCTP4 регулируют
ствия между E Syt и отрицательно заряженными
межклеточный транспорт белка SHOOTMERIS
фосфолипидами плазмалеммы [35]. Схожие
TEMLESS в апикальную меристему побега [48].
процессы могут протекать и в растительных
Показано, что белки AtMTCP3 и AtMTCP4 ло
клетках с участием белков МК, содержащих
кализованы в плазмодесмах, причем мутация
Ca2+ чувствительные модули, например, С2 до
Atmctp3.Atmctp4 приводит к снижению интен
мены SYT1. Через такие модули кальциевые сиг
сивности межклеточного транспорта в клетках
налы могут стимулировать взаимодействие бел
эпидермиса листа и значительным изменениям
ков SYT с определенными липидами и/или бел
в протеоме плазмодесм. Кроме того, экспрессия
ковыми партнерами с последующим изменени
AtMCTP4 в значительной степени восстанавли
ем архитектуры зон МК. Подобная модель объ
вает образование МК между ЭПР и плазмалем
ясняет ряд наблюдаемых явлений, например,
мой в мутантной линии дрожжей, лишенной
Ca2+ зависимое перемещение ионных каналов
шести собственных связующих белков МК [26].
от субдоменов ЭПР в субдомены плазмалеммы
Таким образом, вполне вероятно, что белки
при солевом стрессе [44], изменение локализа
MCTP координируют процессы, протекающие в
ции зон МК и Ca2+ зависимую активацию им
зонах МК плазмодесм, и межклеточную переда
мунных секреторных путей в ответ на грибковую
чу сигналов.
инфекцию [19] и Ca2+ зависимое изменение
Роль белков цитоскелета. Среди других бел
пропускной способности плазмодесм [45].
ков в качестве потенциальных кандидатов на
Белки семейства MTCP. Недавно опублико
роль связующих элементов в МК плазмодесм
ванное исследование показывает, что еще одним
также рассматривают некоторые миозины, ко
классом связующих элементов в зонах МК плаз
торые, возможно, способны связываться с ПМ
модесм, вероятно, являются белки семейства
через собственный С концевой домен, а через
MCTP (белки со множественными доменами С2
«головку», содержащую моторную область, -
и трасмембранным районом, multiple C2
с F актином, ассоциированным с десмотрубоч
domains and transmembrane region proteins) [26].
кой [49]. Например, миозин ATM1 класса VIII,
Два представителя белков MCTP A. thaliana,
который ассоциирован с плазмодесмами, содер
AtMCTP1/Flower Locus T Interacting Protein
жит в С концевом домене кластер основных
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
625
аминокислот, взаимодействующих с кислыми
ле определенного сигнала или модификации. В
фосфолипидами [50], и способен к димериза
обоих вариантах цитоскелет стабилизирует ло
ции (что согласуется с V образной формой не
кализацию NET3C и VAP27 в зонах МК [27].
которых связующих элементов, обнаруженной с
Ряд других данных свидетельствует о том,
помощью электронной микроскопии) [12]. По
что, вероятно, система кортикального цитоске
своим кинетическим свойствам он скорее явля
лета также предоставляет информацию для об
ется сенсором натяжения, чем моторным бел
разования и позиционирования новых зон МК
ком, поскольку ATM1 имеет высокое сродство к
между ЭПР и ПМ. При этом уже существующие
актину, но низкую скорость скольжения отно
зоны МК, содержащие SYT1 и VAP27, распола
сительно него и низкую АТФазную активность
гаются в областях, лишенных микротрубочек.
по сравнению с миозинами других классов [51].
Таким образом, можно предполагать, что корти
Другие исследования также указывают на то,
кальные микротрубочки не требуются для под
что в функционировании плазмодесм задей
держания уже установленных МК и даже, на
ствован цитоскелет. Так, установлено, что про
оборот, служат для них стерическим препят
пускная способность плазмодесм связана с ра
ствием [25].
ботой актин миозиновой системы, и разруше
Следует отметить, что популяция белка SYT1
ние актиновых филаментов может влиять на ви
в растительных клетках неоднородна: помимо
русный межклеточный транспорт [52]. Участие
пула кортикального SYT1, который преимуще
миозинов класса VIII в регулировании пропуск
ственно образует стационарные структуры в зо
ной способности плазмодесм подтверждается
нах МК между ЭПР и плазмалеммой, наблюда
экспериментами, в которых показано, что инги
ется также пул высокоподвижного внутрикле
бирование любого из трех миозинов этого клас
точного белка, чей транспорт прекращается при
са блокирует способность транспортного белка
деполимеризации F актина. Это указывает на
вируса табачной мозаики локализоваться в
роль актинового цитоскелета в адресном транс
плазмодесмах и супрессирует межклеточный
порте и обновлении популяции SYT1 в клетке
транспорт вируса [53]. Тем не менее вопрос о ро
[25]. Важно также подчеркнуть, что регуляция
ли элементов цитоскелета в создании и поддер
распределения SYT1 системой цитоскелета раз
жании МК плазмодесм остается открытым, и
личается в клетках эпидермиса побега и в зре
большая часть нынешних представлений об
лых клетках устьиц [25], что, вероятно, свиде
этих процессах основана на данных, получен
тельствует о взаимосвязи между этими процес
ных для МК между ЭПР и ПМ в других частях
сами и клеточной дифференцировкой.
клетки.
Недавнее исследование белка млекопитаю
Было показано, что молекулярные взаимо
щих E Syt1 указывает на вероятную связь между
действия между МК, содержащими SYT1,
цитоскелет зависимым установлением МК и
VAP27 и кортикальным актиновым цитоскеле
передачей кальциевого сигнала. Так, было обна
том необходимы для стабилизации системы
ружено, что Са2+ опосредованная активация
кортикального ЭПР
[33]. NET3C, партнер
PERK, сенсора стресса, локализованного в ЭПР,
VAP27, связывается с F актином через N конце
приводит к перераспределению связующих
вой домен NAB (NET actin binding domain) [27]
структур E Syt1, при участии в этом процессе
(рисунок). По видимому, F актин не определя
F актина [54]. В растительных клетках перест
ет исходную локализацию NET3C, но стабили
ройка и динамика цитоскелета часто интегриро
зирует его ассоциацию с липидами и/или други
вана с сигнальными путями Ca2+/кальмодулина
ми мембранными белками плазмалеммы, а так
[55]. Можно предположить, что координация
же участвует в обновлении пула NET3C. Мо
этих процессов происходит в зонах МК между
бильность и скорость обновления пула VAP27
ЭПР и ПМ. В пользу данной гипотезы свидетель
связана скорее с функционированием микро
ствует наблюдение, что различные представители
трубочек. Это указывает на участие элементов
семейства растительных белков IQD (IQ67
цитоскелета в организации МК между ЭПР и
DOMAIN), партнеров кальмодулина, локализу
плазмалеммой наравне со связующими элемен
ются в статичных субдоменах ПМ, по всей веро
тами МК. Были предложены две возможные мо
ятности, являющихся функционально различны
дели, описывающие этот процесс: (1) VAP27
ми сигнальными модулями, которые взаимодей
напрямую соединяет ЭПР и плазмалемму, взаи
ствуют с микротрубочками. Однако на данный
модействует с NET3C, который локализуется в
момент нет однозначного подтверждения, что
обоих типах мембран, а также с некими другими
эти субдомены являются зонами МК [56].
белками ПМ, или (2) NET3C при участии дру
Белки 4/1 и PBL. В функционировании МК
гих белков образует в зоне МК некие базовые
плазмодесм могут принимать участие белки, ко
структуры, к которым VAP27 перемещается пос
торые мобилизуются в эти структуры в ответ на
2 БИОХИМИЯ том 85 вып. 5 2020
626
ПАНКРАТЕНКО и др.
определенные воздействия, в частности стрессы
ниям, третичная структура белка Nt 4/1 форми
различной природы. К этой категории могут от
руется преимущественно α спиралями и прояв
носиться белки Nicotiana tabacum 4/1 (Nt 4/1) и
ляет определенное сходство с пространственной
PBL (plant Bap31 like protein), взаимодействую
укладкой полипептидной цепи белка She2p
щие друг с другом in vivo и in vitro [57]. Белок 4/1,
[58-60]. С другой стороны, показано, что белок
который специфичен для растений и не содер
Nt 4/1 способен к нуклео цитоплазматическо
жит известных функциональных доменов [58],
му транспорту [59]. С учетом этих данных мож
локализуется как в ядре, так и в цитоплазме. Ци
но предположить, что белок Nt 4/1 взаимодей
топлазматический пул белка образует тельца,
ствует в ядре с молекулами РНК, включающими
ассоциированные с мембранами ЭПР и, вероят
элементы вторичной структуры, которые явля
но, эндосом. Кроме того, 4/1 содержащие тель
ются сигналами транспорта, и обеспечивает их
ца взаимодействуют с актиновым цитоскелетом,
выход в цитоплазму. Дальнейший внутрикле
который участвует в их внутриклеточном транс
точный транспорт таких комплексов может про
порте, и могут быть ассоциированы с плазмо
исходить с участием белка PBL, взаимодейству
десмами [57, 59, 60]. Делеция N концевого
ющего как с белком Nt 4/1, так и с транспорти
фрагмента белка Nt 4/1 длиной 90 а.о. нарушает
руемыми молекулами РНК. Поскольку белок
ассоциацию белка с мембранами и его внутри
PBL является интегральным белком ЭПР, такой
клеточное распределение, приводя к диффузной
транспорт, вероятнее всего, происходит вдоль
локализации делеционного мутанта в цитоплаз
трубочек кортикального ЭПР.
ме [57]. Было обнаружено, что ко экспрессия с
NbVAP27 или NtPBL меняет внутриклеточное
распределение делеционного варианта Nt 4/1 и
РОЛЬ ЛИПИДОВ
приводит к его локализации вдоль трубочек
В ФУНКЦИОНИРОВАНИИ
кортикального ЭПР. Кроме того, в условиях ме
МК ПЛАЗМОДЕСМ
ханического стресса делеционный вариант Nt 4/1
мобилизуется в сферические структуры, ассоци
Функционирование мембран в клетке опре
ированные с микротрубочками [61].
деляется их белковым и липидным составом.
Белок NtPBL эволюционно родственен бел
Для мембран плазмалеммы, ЭПР и других орга
ку млекопитающих Bap31, участвующему в об
нелл характерно образование мембранных мик
разовании МК между митохондриями и ЭПР
родоменов, представляющих собой отдельные
[4]. Показано, что NtPBL является интеграль
функциональные зоны мембраны, которые
ным мембранным белком, эффективно связы
имеют специфичные липидные и белковые
вающим предшественники микро РНК
профили; в частности, был показан специфи
(миРНК), и экспрессия его РНК связывающего
ческий липидный состав для мембран плазмо
домена в растениях приводит к фенотипу, харак
десм [64]. В основе образования микродоменов
терному для нарушений функций миРНК [62].
лежат различные факторы: свойства молекул
Поскольку Nt 4/1 также имеет РНК связываю
липидов, биофизические характеристики
щую активность, взаимодействуя преимущест
мембраны (текучесть, толщина бислоя, изгиб,
венно с несовершенными дуплексами РНК [60],
электростатические свойства), а также согласо
эта пара белков может быть вовлечена в сигна
ванная работа определенных белковых ком
линг, связанный с транспортом РНК через плаз
плексов. Возникающие микродомены позволя
модесмы. С учетом изменения локализации му
ют создать сложную систему, распознаваемую
танта Nt 4/1 в условиях механического стресса и
различными белками с липид сенсорными до
данных о том, что уровень экспрессии гена 4/1
менами и обеспечивающую адресную доставку
может значительно изменяться при инфекции
и специфическую локализацию многих мемб
патогенных грибов [60], можно предположить,
ранных белков в клетке [11, 20]. По всей вероят
что такого рода сигналинг связан с ответом на
ности, строгий контроль липидного состава и
стрессовые воздействия. В связи с возможной
латеральной организации мембраны имеет
ролью белков Nt 4/1 и PBL в межклеточном
большое значение для архитектуры и структур
транспорте РНК интересно отметить, что белок
ной пластичности плазмодесм [1].
Nt 4/1 имеет структурное сходство с белком
Текучесть мембраны и формирование ли
дрожжей She2p [60], являющимся РНК связы
пидных микродоменов во многом обусловлива
вающим белком, обеспечивающим направлен
ются разделением жидкокристаллических (ЖК)
ный транспорт РНК ASH1, в которой She2p уз
фаз, которое возникает в результате взаимодей
нает шпилечные участки, являющиеся специ
ствия молекул стеролов с белками и липидами,
фическими сигналами внутриклеточного транс
содержащими насыщенные углеводородные це
порта [63]. Согласно компьютерным предсказа
почки. Благодаря этому формируются стерол
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
627
обогащенные упорядоченные ЖК микродоме
роокружения для взаимодействия между орга
ны (Lo) и неупорядоченные ЖК микродомены
неллами [11].
(Ld). Стабильность этого разделения фаз под
Один из потенциальных механизмов поддер
держивается благодаря наличию липидов с не
жания стабильности микродоменов в ПМ может
насыщенными ацильными цепями [65, 66]. Сте
заключаться в
«ограждении» этих доменов
пень жесткости/текучести мембраны связана с
структурными элементами, которые связаны с
относительным содержанием в ней стеролов,
кортикальным цитоскелетом [73] и влияют на
поскольку плоская жесткая структура их моле
мобильность периферических и интегральных
кул создает ограничения для ацильных цепей
белков. Кроме того, стеролы могут напрямую
соседних молекул липидов [67]. Уровень содер
взаимодействовать с каркасными белками, на
жания стеролов вкупе с упорядоченностью и
пример, из семейства тетраспанинов, которые, в
длиной ацильных цепей липидов влияет на тол
частности, обнаружены в плазмодесмах [64].
щину бислоя [66].
На образование и стабильность микродоме
Ряд данных указывает на связь между свой
нов мембраны влияют также ее искривление и
ствами липидных микродоменов и характерис
упаковка липидов в бислое. Эти параметры мо
тиками интегральных белков (в частности, их
гут определять взаимодействие с различными
трансмембранных доменов), что лежит в основе
периферическими белками, которые узнают
механизма сортировки мембранных белков, на
особенности локальной упаковки липидов.
зываемого принципом гидрофобного несоответ
Примером могут служить белки, чувствитель
ствия [68]. Так, например, исследование, опи
ные к изгибам мембраны, которые взаимодей
сывающее протеом плазмодесм Populus tri(
ствуют с ней своими амфипатическими спира
chocarpa, показало, что длина трансмембранных
лями [74]. Изгиб мембраны сам по себе может
доменов белков плазмодесм увеличена по срав
являться движущей силой для сортировки моле
нению с белками микросом [69]. Таким обра
кул в зависимости от их свойств, как это было
зом, можно предположить, что ПМ в составе
показано для липидов [75] и некоторых транс
плазмодесм обладает сравнительно большей
мембранных белков [76]. В свою очередь, опре
толщиной и имеет структуру, подобную стероль
деленные белки, такие как, например, полипеп
ным/сфинголипидным Lo микродоменам [10].
тиды, несущие домен ENTH (Epsin N terminal
Возможно, субкомпартментализация в мембра
homology domain; домен N концевой гомологии
нах плазмодесм происходит согласно другой мо
с эпсином) или локальные изменения в составе
дели: определенные интегральные белки или
липидов (см. ниже), могут вызывать искривле
липиды могут выступать в качестве «затравки»,
ние мембраны [77].
вокруг которой бислой переходит в твердое со
В плазмодесмах мембраны плазмалеммы и
стояние (гель фазу), образуя специфический
десмотрубочки имеют существенную кривизну.
упорядоченный микродомен [70].
Из за особенностей упаковки липидов во внеш
Одна из гипотез предполагает, что в расти
нем слое мембраны и кластеризации липидов,
тельных клетках образование микродоменов
имеющих маленькие полярные группы, вероят
ПМ происходит с участием специфичных для
но, происходит образование локальных липид
растений сфинголипидов GIPC (гликозилино
ных микродоменов и пространственная сегрега
зитолфосфорил церамидов). GIPC характери
ция белков, взаимодействующих с такими суб
зуются очень длинными (до 28 атомов углерода)
доменами, что обеспечивает функциональное
насыщенными ацильными цепями и, по всей
разделение разных зон МК [1, 11].
видимости, локализуются преимущественно в
Механизм, который вызывает и стабилизи
наружном слое мембраны [71]. Обнаружено,
рует изгиб ПМ в плазмодесмах, неизвестен. С
что полигликозилированные GIPC способству
другой стороны, недавно было показано, что
ют увеличению размеров и жесткости фитосте
формирование десмотрубочки в первичных
рол зависимых упорядоченных микродоменов
плазмодесмах происходит, по видимому, с учас
Lo [72]. Кроме того, длинные ацильные цепи
тием ретикулонов RTNLB3 и RTNLB6 [24]. Ло
GIPC могут взаимодействовать с ацильными
кальная геометрия мембраны в краевых участ
цепями липидов в полифосфоинозитид обога
ках плазмодесмы может стимулировать класте
щенных микродоменах внутреннего липидного
ризацию стеролов и сфинголипидов, что в опре
слоя ПМ, что приводит к «сцеплению» доменов
деленных условиях, вероятно, играет роль при
внутреннего и наружного слоев ПМ между со
сортировке гликофосфатидилинозитол (GPI)
бой [71]. Согласно ряду данных, определенные
заякоренных белков [64]. Следует отметить, что
зоны МК обогащены сфинголипидами и фи
метаболизм липидов может иметь значение для
тостеролами, однако, до сих пор неизвестно,
процессов передачи сигналов, протекающих с
какое значение имеет поддержание такого мик
участием плазмодесм, поскольку было показа
БИОХИМИЯ том 85 вып. 5 2020
2*
628
ПАНКРАТЕНКО и др.
но, что сфингоидные основания, продукт рас
D6PK (D6 PROTEIN KINASE) [85, 86]. Зоны
щепления сфинголипидов, выступают вторич
МК характеризуются повышенной концентра
ными мессенджерами при клеточной гибели,
цией анионных липидов, что указывает на их
индуцированной патогенами [78].
роль в поддержании и функционировании этих
Некоторые из известных белков, являющих
структур, возможно, связанную со взаимодей
ся связующими элементами МК, имеют доме
ствием таких липидов с компонентами МК [11].
ны, ассоциирующиеся с изгибами мембран. Так,
На сегодняшний день неизвестно, какие виды
например, белок Osh4p имеет мотив LPS (lipid
фосфатидилинозитол фосфатов (PIP) ассоци
packing sensor), который может обеспечивать
ированы с плазмодесмами. Однако существова
взаимодействие белка с искривленными мем
ние белков плазмодесм, имеющих С2 домены,
бранами [79]; домены С2 белков SYT млекопи
таких, как SYT1 и QUIRKY, позволяет предпо
тающих могут стимулировать Ca2+ зависимый
ложить, что PI(4)P и PI(4,5)P2 декорируют ПМ в
локальный изгиб мембраны [80]. Можно пред
этих каналах [7, 47].
положить, что AtSYT1, локализующийся в плаз
При рассматривании взаимодействий между
модесмах и содержащий два домена С2 [25],
анионными липидами и различными белками
преимущественно ассоциируется с положитель
следует учитывать влияние таких факторов, как
но изогнутыми концевыми участками плазмо
локальные модификации липидов, рН, а также
десм, а С2 мотивы, связывая конические липи
градиентные и локальные концентрации ионов,
ды, такие, как PIP, усиливают их кластеризацию
которые влияют на электростатический про
во внутреннем слое мембраны и вызывают пере
филь мембраны [11]. Так, зоны МК являются
стройку мембранных структур [1].
сайтами передачи Ca2+ сигналов, и Ca2+ модули
Кроме растительных белков MCTP и синап
рует функционирование E Syt1 [87]. Однако, с
тотагминов, описанных выше, стоит отметить
другой стороны, ионы Ca2+ могут экранировать
также липид транспортирующие белки (LTP,
полярные группы PIP, тем самым препятствуя
lipid transfer proteins), которые осуществляют
связыванию белков и липидов в этих областях
транспорт липидов и в ряде случаев сами могут
[88]. В недавних исследованиях показано, что
являться связующими элементами МК [81].
локальные колебания в концентрации бивалент
Многие белки LTP содержат определенные
ных катионов влияют на форму мембран, содер
комбинации доменов, что, возможно, обеспе
жащих анионные липиды, из за того, что ион
чивает их точную адресацию к зонам тех или
ные взаимодействия приводят к кластеризации
иных МК [5]. Часто встречающимися типами
PS и PI(4,5)P2, что, в свою очередь, вызывает
доменов LTP являются домены С2 и РН (pleck
возникновение кривизны липидного бислоя
strin homology) [82], которые взаимодействуют с
[89]. Эти и другие изменения в микроокружении
отрицательно заряженными липидами. Кроме
элементов МК, связывающих две мембраны,
того, некоторые домены LTP содержат мотив
влияют на их структурные модификации, что
ALPS (ArfGAP1 lipid packing sensor), способный
позволяет инициировать и передать сигнал на
связываться с сильно искривленными мембра
уровне МК в целом за счет сокращения рассто
нами [83].
яния между мембранами, обмена молекулами
Заряд полярных групп липидов является еще
липидов, сборки или разборки белковых ком
одним важным фактором, влияющим на разде
плексов [87].
ление мембран на различные функциональные
Важную роль в функционировании МК иг
зоны. Основной группой отрицательно заря
рает липидный обмен. При этом белки LTP свя
женных липидов, которые определяют элек
зываются с анионными липидами мембран и
тростатические характеристики внутреннего
производят перенос определенных молекул ли
слоя ПМ, являются фосфатидилинозитол 4
пидов от донорной мембраны к акцепторной,
фосфат PI(4)P и фосфатидилинозитол 4,5 бис
экранируя липиды от водного окружения с по
фосфат PI(4,5)P2 [84, 85]. Недавние исследова
мощью транспортных доменов [90]. В частнос
ния показывают, что, по видимому, электроста
ти, было показано, что белки OSBP и ORP/Osh
тическое поле мембраны регулируется сочета
(OSBP Related Proteins) в зонах МК взаимодей
нием нескольких типов анионных липидов
ствуют с белками VAP для обеспечения обмена
(фосфатидная кислота (PA), PI(4)P и PS) [86].
молекулами стеролов, PS и PIP между ЭПР и
Это комбинирование создает специфические
плазмалеммой [91]. Osh4 использует дисбаланс в
заряды в различных зонах мембраны и позволя
распределении PI(4)P, возникающий в результа
ет обеспечить локализацию в этих зонах катион
те работы фосфатазы Sac1p, для обмена PI(4)P
ных белков, таких как регулятор транспорта
из транс цистерн аппарата Гольджи на молеку
брассиностероидов BKI1 (BRI1 KINASE
лы стеролов ЭПР, тем самым обогащая мембра
INHIBITOR1) или AGC киназы PINOID и
ны транс АГ стеролами и поддерживая пул
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
629
PI(4)P в мембранах ЭПР [79]. Еще одним при
ность (SEL, size exclusion limit). Существующие
мером регуляции липидного состава является
на данный момент модели предполагают, что
перенос PS от мембраны ЭПР к плазмалемме в
SEL зависит от физических характеристик ци
обмен на PI(4)P и PI(4,5)P2, переносимые из
топлазматического рукава, основным регулято
плазмалеммы к ЭПР [92, 93], который обеспе
ром которых является β 1,3 глюкан каллоза:
чивается белками ORP5/8. Интересно, что под
многочисленные исследования показывают, что
держание пула PI(4)P в мембранах ЭПР связано
каллозо опосредованное изменение SEL плаз
с белком CERT, который обеспечивает перенос
модесм происходит в ответ на широкий спектр
сфинголипидов к мембранам транс цистерн АГ
сигналов развития и биотических/абиотических
[94]. Следует отметить, что некоторые белки E
стимулов [96, 97]. Откладывание и удаление кал
Syt млекопитающих, например, E Syt2, вероят
лозы во внеклеточном матриксе, окружающем
но, участвуют в транспорте липидов за счет об
плазмодесмы, вызывает сближение или расхож
разования липидных туннелей с помощью SMP
дение плазмалеммы и десмотрубочки, тем са
доменов [36].
мым влияя на объем цитоплазматического рука
Липидный обмен в зонах МК формирует
ва и определяя SEL. Однако данные, получен
специфичность мембран и позволяет создавать
ные в последние годы, свидетельствуют о том,
липидные градиенты, необходимые для работы
что регуляция проводимости плазмодесм значи
различных молекулярных механизмов [78, 91,
тельно сложнее и, по видимому, связана в пер
94]. Хотя наличие липидного обмена в плазмо
вую очередь не с собственно их архитектурой, а с
десмах не установлено окончательно, этот про
изменением их молекулярного состава [1].
цесс мог бы иметь большое значение для их
Уровень отложения каллозы определяется
функционирования, учитывая, что из за значи
работой трансмембранных каллозо синтазных
тельной длины этих каналов, особенно в зрелых
комплексов и β 1,3 глюканаз, заякоренных в
тканях, доставка везикул вглубь плазмодесм мо
мембране и обращенных основной частью в
жет быть сильно затруднена [11]. Кроме того,
апопласт. Было показано, что фенотипы расте
регулируемый перенос липидов позволял бы ре
ний, мутантных по синтезу стеролов и каллозо
гулировать форму мембран, поскольку ассимет
синтазным комплексам, сходны между собой
ричное распределение липидов конической
[98]. На основании этого исследователи выдви
формы между двумя слоями мембраны может
нули гипотезу, согласно которой в обмене кал
вызвать ее искривление независимо от эффекта
лозы в плазмодесмах играют роль структурные
интегрированных белков [95].
стеролы. Следует учесть, что сайт специфичное
отложение каллозы в краевых участках плазмо
десм означает, что ферменты, участвующие в
ВЗАИМОСВЯЗЬ
этом процессе, должны адресно доставляться в
МЕЖДУ ФУНКЦИОНИРОВАНИЕМ МК
определенные субдомены ПМ. Это тоже может
И КЛЕТОЧНОЙ СТЕНКОЙ
служить аргументом в пользу взаимосвязи меж
ду каллозным обменом и регуляцией липидного
В последние годы появляются данные, кото
состава мембраны [10, 98].
рые указывают на области МК между ЭПР и
Было обнаружено, что в клетках меристемы
плазмалеммой как на часть интегрированной
перед удалением каллозных пробок в районе
системы «ЭПР-плазмалемма-клеточная стен
плазмодесм наблюдается транспорт липидных
ка». Например, отсутствие клеточной стенки
телец, являющихся производными ЭПР, кото
влияет на мобильность VAP27 в зонах МК [6,
рые располагаются в местах входа в плазмодес
40]. Элементы внеклеточного матрикса взаимо
мы и содержат β 1,3 глюканазы. Можно пред
действуют с белками и липидами ПМ, ограни
положить, что эти ферменты встраиваются в
чивая их латеральную подвижность и стабили
ПМ в обход секреторного пути, вероятно, взаи
зируя микродомены плазмалеммы. Подобные
модействуя с липидными микродоменами ее
взаимодействия в зонах МК, вероятно, позволя
внутреннего слоя. Этот механизм мог бы обес
ют также стабилизировать структуру кортикаль
печивать доставку к плазмодесмам и других их
ного ЭПР и интегрировать сигналы, поступаю
компонентов [99].
щие от его компартментов и клеточной стенки
Отложение каллозы в области плазмодесм
[43]. Можно предположить, что эти процессы
регулируется целым рядом различных белков.
играют важную роль в функционировании плаз
Cинтез каллозы индуцируется в ответ на актива
модесм, поскольку в этих структурах ПМ и кле
цию рецепторов LYM2 и FLS2, локализованных
точная стенка тесно контактируют между собой.
в плазмодесмах, а также рецептор подобных
МК в плазмодесмах, вероятнее всего, могут
белков PDLP [22, 100, 101]. Кроме того, каллоз
напрямую определять их пропускную способ
ный обмен регулируется GPI заякоренными
БИОХИМИЯ том 85 вып. 5 2020
630
ПАНКРАТЕНКО и др.
белками PDCB, что также указывает на роль ли
щен пектиновыми полисахаридами, которые
пидного состава мембраны в регуляции SEL.
образуют гидрированный гель, облегчающий
Белки PDCB не имеют энзиматической актив
создание новых каналов в этой области клеточ
ности, но могут связываться с каллозой через
ной стенки [105]. Модификация пектинов влия
X8 домен [20]. Было показано, что PDCB1 риса
ет на жесткость клеточной стенки, а для плазмо
совместно с белком группы 6 семейства ремори
десм была показана активность пектин метил
нов регулируют проводимость плазмодесм, за
эстераз и пектиназ [106, 107], что, очевидно,
действуя отложение каллозы [102], и что ремо
связано с локальным изменением свойств кле
рин группы 1 в листьях Nicotiana benthamiana
точной стенки при осцилляции пор плазмодесм
влияет на вирусный транспорт, по видимому,
[1]. В протеоме плазмодесм был также обнару
являясь негативным регулятором SEL [103].
жен ряд других белков, участвующих в росте и
Интересно отметить, что сигналом локали
модификации клеточной стенки [17].
зации в плазмодесмах двух белков метаболизма
Важную роль в регуляции проводимости
каллозы, β 1,3 глюканазы BG_pap и PDCB1,
плазмодесм играет передача Ca2+ сигналов. Бы
является GPI, имеющий сродство к Lo микро
ло показано, что около плазмодесм локализуют
доменам мембраны [104]. В соответствии с эти
ся белки ЭПР из семейства кальретикулинов,
ми данными изменение биосинтеза стеролов
обладающие Ca2+ связывающей активностью
влияет на распределение GPI заякоренных бел
[108] и, кроме того, накопление активных форм
ков в плазмодесмах при делении клеток и, как
кислорода, вызывающее отложение каллозы в
следствие, на отложение каллозы и пропускную
клеточной стенке, индуцирует всплеск уровня
способность плазмодесм [64] (рисунок).
Ca2+ в цитозоле [109, 110]. Наконец, закупори
Следует отметить, что в ряде случаев процес
вание ситовидных элементов флоэмы при атаке
сы отложения каллозы могут регулироваться
патогена, по видимому, связано с локальным
белками, которые перемещаются к плазмодес
возрастанием концентрации Ca2+ около сито
мам в ответ на различные стрессы. Так, недавно
видных пластинок и в области плазмодесм, сое
предложенная модель изменения SEL при соле
диняющих ситовидные элементы с клетками
вом стрессе постулирует, что повышенные кон
спутницами [45]. Поскольку десмотрубочка мо
центрации соли индуцируют кальциевый сиг
жет выступать резервуаром Ca2+ в этих процес
нал, который, в свою очередь, активирует фос
сах, можно представить, что Ca2+ каналы плаз
фолипазу PLDα1 и вызывает ее перераспределе
малеммы и ЭПР могут действовать скоордини
ние из цитоплазмы к ПМ; это, в свою очередь,
ровано, локализуясь в зонах МК плазмодесм [1].
приводит к образованию PA и изменению
Согласно одной из моделей рецептор инду
свойств мембраны. В результате рецептор по
цированного сигнала Ca2+ в зонах МК между
добная киназа CRK2, в норме локализующаяся
ЭПР и плазмалеммой, повышение уровня Ca2+
в ПМ, мобилизуется к определенным доменам
вызывает расширение области МК и последую
плазмодесм и там взаимодействует с каллозо
щее привлечение белка Nir2, участвующего в
синтазой CALS1. Это приводит к отложению
переносе PI из мембраны ЭПР к плазмалемме
каллозы и повышает устойчивость растения к
[29]. Этот перенос обеспечивает индукцию ло
солевому стрессу [22]. Мобилизация к плазмо
кального сигнала за счет образования инозитол
десмам в ответ на осмотический стресс была по
трифосфата (IP3). Кроме того, как уже обсужда
казана и для рецептор подобных киназ QSK1
лось выше, ионы кальция, наряду с анионными
(Qiān Shou Kinase) и IMK2 (Inflorescence
липидами, могут влиять на функционирование
Meristem Kinase2). Обработка клеток маннито
связующих элементов в зонах МК: индуциро
лом, вызывающая осмотический стресс, при
ванное изменение конформации белков может
водила к фосфорилированию QSK1 и стреми
вызывать сокращение или увеличение цито
тельному перераспределению этих белков. В
зольного пространства между мембранами, тем
результате потеря функции QSK1 вызывала за
самым изменяя пропускную способность плаз
медленное развитие боковых корней у
модесм (рисунок). Кроме того, структура МК и,
Arabidopsis thaliana и повышенную чувствитель
соответственно, значение SEL может изменять
ность к осмотическому стрессу, а также сниже
ся при перераспределении связующих элемен
ние уровня отложения каллозы в плазмодесмах
тов. Совокупность этих процессов, вероятно,
[21].
обеспечивает динамичную перестройку плазмо
Контроль SEL может осуществляться и дру
десм в процессе их функционирования [1], а
гими путями, не связанными с каллозным обме
также контроль межклеточного транспорта. В
ном. Так, показано, что внеклеточный матрикс,
совокупности это указывает на плазмодесмы
в котором пролегают плазмодесмы, отличается
как на крайне важные узлы сигнальных путей в
пониженным содержанием целлюлозы и обога
растительных клетках.
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
631
УЧАСТИЕ ОБЛАСТЕЙ МК
десм; транспортные белки вирусов, в свою оче
В РАЗВИТИИ ВИРУСНОЙ ИНФЕКЦИИ
редь, взаимодействуют с клеточными фактора
ми, которые ингибируют эти процессы [1, 114,
Плазмодесмы являются единственным пу
115]. Эти наблюдения также указывают на взаи
тем межклеточного транспорта вирусной ин
мосвязь между развитием вирусной инфекции и
фекции в растении. Транспортные белки виру
изменением в работе плазмодесм на уровне ли
сов обеспечивают достаточную пропускную
пидных и белковых систем, в частности, на
способность этих каналов и транслокацию ви
уровне МК.
русного генома по их цитоплазматическому ру
каву. Вирусы также взаимодействуют с зонами
Накопление знаний о плазмодесмах, длив
МК и на другой стадии инфекции: РНК вирусы
шееся десятилетиями, привело к пониманию
реплицируются на значительно модифициро
того, что внутренняя структура плазмодесм име
ванных внутриклеточных мембранах хозяина,
ет характерные черты МК между ПМ и ЭПР.
образуя сложные «вирусные фабрики», содер
Развитие этих представлений позволило уйти от
жащие плотно состыкованные, сетеподобные
механистического понимания плазмодесм как
или изогнутые мембранные структуры [111].
межклеточных каналов, пропускная способ
Связующие белки МК могут быть вовлечены в
ность которых определяется несколькими прос
образование этих «фабрик». Так, например, ви
тыми факторами, и создало концептуальную ба
рус кустистой карликовости томата (Tomato
зу для дальнейших функциональных исследова
bushy stunt virus) при репликации в клетках
ний плазмодесм как сложных, многокомпонент
дрожжей и растений мобилизует белок дрожжей
ных систем, интегрирующих черты МК, специ
Scs2 и его растительный гомолог VAP27 3, а так
ализированных мембранных микродоменов и
же участвующие в липидном обмене белки
связанных с этими структурами функционально
ORP1 дрожжей и ORP3 растений, чтобы инду
обособленных районов клеточной стенки. По
цировать пролиферацию мембран в сайтах син
лученные к настоящему дню данные показыва
теза вирусной РНК [6, 112]. Интересно, что, по
ют, что МК в составе плазмодесм представляют
видимому, в ряде случаев взаимодействие виру
собой динамические структуры, вносящие важ
сов с компонентами МК для транспорта и для
ный вклад в регулирование пропускной способ
репликации может быть функционально связа
ности плазмодесм. Дальнейшее изучение ком
но: некоторые вирусы создают сайты реплика
понентов МК в составе плазмодесм, а также мо
ции на модифицированных мембранах непосред
лекулярных механизмов функционирования
ственно у входа в плазмодесмы [7, 113]. До сих
этих структур и способов их регуляции прибли
пор неясно, требуется ли это всего лишь для
жает нас к пониманию общих механизмов
большей скорости и эффективности межкле
межклеточной коммуникации в растениях.
точного транспорта вирусных рибонуклеопро
теидов или необходимо непосредственно для
модификации и открытия каналов плазмодесм.
Финансирование. Работа выполнена при фи
Однако тот факт, что SYT1 необходим для
нансовой поддержке Российского научного
транспорта ряда вирусов и при инфекции пере
фонда (грант № 17 14 01032).
мещается к плазмодесмам [7], говорит в пользу
Конфликт интересов. Авторы заявляют об от
второго предположения.
сутствии конфликта интересов.
Растительные клетки препятствуют вирусно
Соблюдение этических норм. Данная статья
му транспорту с помощью индукции отложений
не содержит исследований, в которых в качестве
каллозы в клеточных стенках вокруг плазмо
объектов использовали людей или животных.
СПИСОК ЛИТЕРАТУРЫ
1.
Tilsner, J., Nicolas, W., Rosado, A., and Bayer, E. M.
STARD3/STARD3NL and VAP make a novel molecular
(2016) Staying tight: plasmodesmal membrane contact
tether between late endosomes and the ER, J. Cell Sci.,
sites and the control of cell to cell connectivity in plants,
126, 5500 5512, doi: 10.1242/jcs.139295.
Annu. Rev. Plant Biol., 67, 23.1 23.28, doi: 10.1146/
4.
Iwasawa, R., Mahul Mellier, A. L., Datler, C.,
annurev arplant 043015 111840.
Pazarentzos, E., and Grimm, S. (2011) Fis1 and Bap31
2.
Prinz, W. A., Toulmay, A., and Balla, T. (2020) The func
bridge the mitochondria-ER interface to establish a plat
tional universe of membrane contact sites, Nat. Rev. Mol.
form for apoptosis induction, EMBO J., 30, 556 568,
Cell Biol., 21, 7 24, doi: 10.1038/s41580 019 0180 9.
doi: 10.1038/emboj.2010.346.
3.
Alpy, F., Rousseau, A., Schwab, Y., Legueux, F., Stoll, I.,
5.
Hanada, K. (2018) Lipid transfer proteins rectify inter
Wendling, C., Spiegelhalter, C., Kessler, P., Mathelin, C.,
organelle flux and accurately deliver lipids at membrane contact
Rio, M. C., Levine, T. P., and Tomasetto, C. (2013)
sites, J. Lipid Res., 59, 1341 1366, doi: 10.1194/jlr.R085324.
БИОХИМИЯ том 85 вып. 5 2020
632
ПАНКРАТЕНКО и др.
6.
Wang, P., Richardson, C., Hawkins, T. J., Sparkes, I.,
Plasma membrane associated receptor like kinases relo
Hawes, C., and Hussey, P. J. (2016) Plant VAP27 proteins:
calize to plasmodesmata in response to osmotic stress,
domain characterization, intracellular localization and role
Plant Physiol., 181, 142 160, doi: 10.1104/pp.19.00473.
in plant development, New Phytol., 210, 13111326,
22.
Hunter, K., Kimura, S., Rokka, A., Tran, H. C., Toyota, M.,
doi: 10.1111/nph.13857.
Kukkonen, J. P., and Wrzaczek, M. (2019) CRK2
7.
Levy, A., Zheng, J. Y., and Lazarowitz, S. G. (2015)
Enhances salt tolerance by regulating callose deposition in
Synaptotagmin SYTA forms ER plasma membrane junc
connection with PLDα1, Plant Physiol., 180, 2004 2021,
tions that are recruited to plasmodesmata for plant virus
doi: 10.1104/pp.19.00560.
movement, Curr. Biol., 25, 2018 2025, doi: 10.1016/j.cub.
23.
Ham, B. K., Li, G., Kang, B. H., Zeng, F., and Lucas, W. J.
2015.06.015.
(2012) Overexpression of Arabidopsis plasmodesmata
8.
Liu, L., and Li, J. (2019) Communications between the
germin like proteins disrupts root growth and develop
endoplasmic reticulum and other organelles during abiotic
ment, Plant Cell, 24, 3630 3648, doi: 10.1105/tpc.112.
stress response in plants, Front. Plant Sci., 10, 749,
101063.
doi: 10.3389/fpls.2019.00749.
24.
Knox, K., Wang, P., Kriechbaumer, V., Tilsner, J., Frigerio, L.,
9.
Michaud, M., and Jouhet, J. (2019) Lipid trafficking at
Sparkes, I., Hawes, C., and Oparka, K. (2015) Putting the
membrane contact sites during plant development and
squeeze on plasmodesmata: a role for reticulons in prima
stress response, Front. Plant Sci., 10, 2, doi: 10.3389/
ry plasmodesmata formation, Plant Physiol., 168, 1563
fpls.2019.00002.
1572, doi: 10.1104/pp.15.00668.
10.
Bayer, E. M., Mongrand, S., and Tilsner, J.
(2014)
25.
Pérez Sancho, J., Vanneste, S., Lee, E., McFarlane, H. E.,
Specialized membrane domains of plasmodesmata, plant
Esteban Del Valle, A., Valpuesta, V., Friml, J., Botella, M. A.,
intercellular nanopores, Front. Plant Sci.,
5,
507,
and Rosado, A. (2015) The Arabidopsis synaptotagmin1 is
doi: 10.3389/fpls.2014.00507.
enriched in endoplasmic reticulum plasma membrane
11.
Petit, J. D., Immel, F., Lins, L., and Bayer, E. M. (2019)
contact sites and confers cellular resistance to mechanical
Lipids or proteins: who is leading the dance at membrane
stresses, Plant Physiol., 168, 132 143, doi: 10.1104/pp.
contact sites, Front. Plant Sci., 10, 198, doi: 10.3389/fpls.
15.00260.
2019.00198.
26.
Brault, M. L., Petit, J. D., Immel, F., Nicolas, W. J.,
12.
Ding, B., Turgeon, R., and Parthasarathy, M. V. (1992)
Glavier, M., Brocard, L., Gaston, A., Fouché, M.,
Substructure of freeze substituted plasmodesmata,
Hawkins, T. J., Crowet, J. M., Grison, M. S., Germain, V.,
Protoplasma, 169, 28 41, doi: 10.1007/BF01343367.
Rocher, M., Kraner, M., Alva, V., Claverol, S., Paterlini, A.,
13.
Nicolas, W. J., Grison, M. S., Trépout, S., Gaston, A.,
Helariutta, Y., Deleu, M., Lins, L., Tilsner, J., and Bayer, E. M.
Fouché, M., Cordelières, F. P., Oparka, K., Tilsner, J.,
(2019) Multiple C2 domains and transmembrane region
Brocard, L., and Bayer, E. M. (2017) Architecture and per
proteins (MCTPs) tether membranes at plasmodesmata,
meability of post cytokinesis plasmodesmata lacking cyto
EMBO Rep., 20, e47182, doi: 10.15252/embr.201847182.
plasmic sleeves, Nat. Plants, 3, 17082, doi: 10.1038/
27.
Wang, P., Hawkins, T. J., Richardson, C., Cummins, I.,
nplants.2017.82.
Deeks, M. J., Sparkes, I., Hawes, C., and Hussey, P. J.
14.
Faulkner, C., and Maule, A. (2011) Opportunities and suc
(2014) The plant cytoskeleton, NET3C, and VAP27 medi
cesses in the search for plasmodesmal proteins,
ate the link between the plasma membrane and endoplas
Protoplasma, 248, 27 38, doi: 10.1007/s00709 010 0213 x.
mic reticulum, Curr. Biol., 24, 1397 1405, doi: 10.1016/
15.
Salmon, M. S., and Bayer, E. M. F. (2013) Dissecting plas
j.cub.2014.05.003.
modesmata molecular composition by mass spectrometry
28.
Kagiwada, S., and Hashimoto, M. (2007) The yeast VAP
based proteomics, Front. Plant Sci., 3, 307, doi: 10.3389/
homolog Scs2p has a phosphoinositide binding ability that
fpls.2012.00307.
is correlated with its activity, Biochem. Biophys. Res.
16.
Kraner, M. E., Müller, C., and Sonnewald, U. (2017) Com
Commun., 364, 870 876, doi: 10.1016/j.bbrc.2007.10.079.
parative proteomic profiling of the Choline transporter
29.
Chang, C. L., Hsieh, T. S., Yang, T. T., Rothberg, K. G.,
like1 (CHER1) mutant provides insights into plasmodes
Azizoglu, D. B., Volk, E., Liao, J. C., and Liou, J. (2013)
mata composition of fully developed Arabidopsis thaliana
Feedback regulation of receptor induced Ca2+ signaling
leaves, Plant J., 92, 696 709, doi: 10.1111/tpj.13702.
mediated by E Syt1 and Nir2 at endoplasmic reticulum
17.
Fernandez Calvino, L., Faulkner, C., Walshaw, J.,
plasma membrane junctions, Cell Rep., 5, 813825,
Saalbach, G., Bayer, E., Benitez Alfonso, Y., and Maule,
doi: 10.1016/j.celrep.2013.09.038.
A. (2011) Arabidopsis plasmodesmal proteome, PLoS One.,
30.
Murphy, S. E., and Levine, T. P. (2016) VAP, a versatile
6, e18880, doi: 10.1371/journal.pone.0018880.
access point for the endoplasmic reticulum: review and
18.
Thomas, C. L., Bayer, E. M., Ritzenthaler, C., Fernandez
analysis of FFAT like motifs in the VAPome, Biochim.
Calvino, L., and Maule, A. J. (2008) Specific targeting of a
Biophys. Acta, 1861, 952 961, doi: 10.1016/j.bbalip.2016.
plasmodesmal protein affecting cell to cell communica
02.009.
tion, PLoS Biol., 6, e7, doi: 10.1371/journal.pbio.0060007.
31.
Kriechbaumer, V., Botchway, S. W., Slade, S. E., Knox, K.,
19.
Kim, H., Kwon, H., Kim, S., Kim, M. K., Botella, M. A.,
Frigerio, L., Oparka, K., and Hawes, C.
(2015)
Yun, H. S., and Kwon, C. (2016) Synaptotagmin 1 nega
Reticulomics: protein protein interaction studies with two
tively controls the two distinct immune secretory pathways
plasmodesmata localized reticulon family proteins identify
to powdery mildew fungi in Arabidopsis, Plant Cell Physiol.,
binding partners enriched at plasmodesmata, endoplasmic
57, 1133 1141, doi: 10.1093/pcp/pcw061.
reticulum, and the plasma membrane, Plant Physiol., 169,
20.
Simpson, C., Thomas, C., Findlay, K., Bayer, E., and
1933 1945, doi: 10.1104/pp.15.01153.
Maule, A. J. (2009) An Arabidopsis GPI anchor plasmo
32.
Deeks, M. J., Calcutt, J. R., Ingle, E. K., Hawkins, T. J.,
desmal neck protein with callose binding activity and
Chapman, S., Richardson, A. C., Mentlak, D. A.,
potential to regulate cell to cell trafficking, Plant Cell., 21,
Dixon, M. R., Cartwright, F., Smertenko, A. P., Oparka, K.,
581 594, doi: 10.1105/tpc.108.060145.
and Hussey, P. J. (2012) A superfamily of actin binding
21.
Grison, M. S., Kirk, P., Brault, M. L., Wu, X. N., Schulze, W. X.,
proteins at the actin membrane nexus of higher plants,
Benitez Alfonso, Y., Immel, F., and Bayer, E. M. (2019)
Curr. Biol., 22, 1595 1600, doi: 10.1016/j.cub.2012.06.041.
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
633
33.
Siao, W., Wang, P., Voigt, B., Hussey, P. J., and Baluska, F.
for florigen transport, PLoS Biol.,
10, e1001313,
(2016) Arabidopsis SYT1 maintains stability of cortical
doi: 10.1371/journal.pbio.1001313.
endoplasmic reticulum networks and VAP27 1 enriched
47.
Vaddepalli, P., Herrmann, A., Fulton, L., Oelschner, M.,
endoplasmic reticulum plasma membrane contact sites,
Hillmer, S., Stratil, T. F., Fastner, A., Hammes, U. Z., Ott, T.,
J. Exp. Bot., 67, 6161 6171, doi: 10.1093/jxb/erw381.
Robinson, D. G., and Schneitz, K. (2014) The C2 domain
34.
Ishikawa, K., Tamura, K., Fukao, Y., and Shimada, T.
protein QUIRKY and the receptor like kinase STRUBBE
(2019) Structural and functional relationships between
LIG localize to plasmodesmata and mediate tissue mor
plasmodesmata and plant endoplasmic reticulum plasma
phogenesis in Arabidopsis thaliana, Development, 141,
membrane contact sites consisting of three synaptotag
4139 4148, doi: 10.1242/dev.113878.
mins, New Phytol., doi: 10.1111/nph.16391.
48.
Liu, L., Li, C., Song, S., Teo, Z. W. N., Shen, L., Wang, Y.,
35.
Fernández Busnadiego, R., Saheki, Y., and De Camilli, P.
Jackson, D., and Yu, H. (2018) FTIP dependent STM
(2015) Three dimensional architecture of extended synap
trafficking regulates shoot meristem development in
totagmin mediated endoplasmic reticulum plasma mem
Arabidopsis, Cell Rep., 23, 1879 1890, doi: 10.1016/j.celrep.
brane contact sites, Proc. Natl. Acad. Sci. USA, 112,
2018.04.033.
E2004 E2013, doi: 10.1073/pnas.1503191112.
49.
Robyn L. Overall, R. L., and Blackman, L. M. (1996)
36.
Schauder, C. M., Wu, X., Saheki, Y., Narayanaswamy, P.,
A model of the macromolecular structure of plasmodesma
Torta, F., Wenk, M. R., De Camilli, P., and Reinisch, K. M.
ta, Trends Plant Sci., 1, 307 311, doi: 10.1016/S1360
(2014) Structure of a lipid bound extended synaptotagmin
1385(96)88177 0.
indicates a role in lipid transfer, Nature, 510, 552 555,
50.
Knight, A. E., and Kendrick Jones, J. (1993) A myosin
doi: 10.1038/nature13269.
like protein from a higher plant. J. Mol. Biol., 231, 148
37.
Reinisch, K. M., and De Camilli, P. (2016) SMP domain
154, doi: 10.1006/jmbi.1993.1266.
proteins at membrane contact sites: structure and function,
51.
Haraguchi, T., Tominaga, M., Matsumoto, R., Sato, K.,
Biochim. Biophys. Acta, 1861, 924 927, doi: 10.1016/
Nakano, A., Yamamoto, K., and Ito, K. (2014) Molecular
j.bbalip.2015.12.003.
characterization and subcellular localization of Arabidopsis
38.
Dalal, J., Lewis, D. R., Tietz, O., Brown, E. M., Brown, C. S.,
class VIII myosin, ATM1, J. Biol. Chem., 289, 12343
Palme, K., Muday, G. K., and Sederoff, H. W. (2016)
12355, doi: 10.1074/jbc.M113.521716.
ROSY1, a novel regulator of gravitropic response is a stig
52.
Su, S., Liu, Z., Chen, C., Zhang, Y., Wang, X., Zhu, L.,
masterol binding protein, J. Plant Physiol., 196J197, 28
Miao, L., Wang, X. C., and Yuan, M. (2010) Cucumber
40, doi: 10.1016/j.jplph.2016.03.011.
mosaic virus movement protein severs actin filaments to
39.
Ho, C. M., Paciorek, T., Abrash, E., and Bergmann, D. C.
increase the plasmodesmal size exclusion limit in tobac
(2016) Modulators of stomatal lineage signal transduction
co, Plant Cell, 22, 13731387, doi: 10.1105/tpc.108.
alter membrane contact sites and reveal specialization
064212.
among ERECTA kinases, Dev. Cell.,
38,
345357,
53.
Amari, K., Di Donato, M., Dolja, V. V., and Heinlein, M.
doi: 10.1016/j.devcel.2016.07.016.
(2014) Myosins VIII and XI play distinct roles in reproduc
40.
Schapire, A. L., Voigt, B., Jasik, J., Rosado, A., Lopez
tion and transport of tobacco mosaic virus, PLoS Pathog.,
Cobollo, R., Menzel, D., Salinas, J., Mancuso, S.,
10, e1004448, doi: 10.1371/journal.ppat.1004448.
Valpuesta, V., Baluska, F., and Botella, M. A.
(2008)
54.
Van Vliet, A. R., Giordano, F., Gerlo, S., Segura, I., Van
Arabidopsis synaptotagmin 1 is required for the mainte
Eygen, S., Molenberghs, G., Rocha, S., Houcine, A.,
nance of plasma membrane integrity and cell viability,
Derua, R., Verfaillie, T., Vangindertael, J., De
Plant Cell, 20, 3374 3388, doi: 10.1105/tpc.108.063859.
Keersmaecker, H., Waelkens, E., Tavernier, J., Hofkens, J.,
41.
Yamazaki, T., Kawamura, Y., Minami, A., and Uemura, M.
Annaert, W., Carmeliet, P., Samali, A., Mizuno, H., and
(2008) Calcium dependent freezing tolerance in Arabi(
Agostinis, P. (2017) The ER stress sensor PERK coordi
dopsis involves membrane resealing via synaptotagmin
nates ER plasma membrane contact site formation
SYT1, Plant Cell, 20, 3389 3404, doi: 10.1105/tpc.108.
through interaction with filamin A and F actin remodel
062679.
ing, Mol. Cell,
65,
885899, doi:
10.1016/j.molcel.
42.
Dickson, E. J., Jensen, J. B., and Hille, B.
(2016)
2017.01.020.
Regulation of calcium and phosphoinositides at endoplas
55.
Hepler, P. K. (2016) The Cytoskeleton and its regulation by
mic reticulum membrane junctions, Biochem. Soc. Trans.,
calcium and protons, Plant Physiol.,
170,
3 22,
44, 467 473, doi: 10.1042/BST20150262.
doi: 10.1104/pp.15.01506.
43.
Bayer, E. M., Sparkes, I., Vanneste, S., and Rosado, A.
56.
Bürstenbinder, K., Möller, B., Plötner, R., Stamm, G.,
(2017) From shaping organelles to signalling platforms: the
Hause, G., Mitra, D., and Abel, S. (2017) The IQD fami
emerging functions of plant ER PM contact sites, Curr.
ly of calmodulin binding proteins links calcium signaling
Opin. Plant Biol., 40, 89 96, doi: 10.1016/j.pbi.2017.08.006.
to microtubules, membrane subdomains, and the nucleus,
44.
Held, K., Pascaud, F., Eckert, C., Gajdanowicz, P.,
Plant Physiol., 173, 1692 1708, doi: 10.1104/pp. 16.01743.
Hashimoto, K., Corratgé Faillie, C., Offenborn, J. N.,
57.
Pankratenko, A. V., Atabekova, A. K., Lazareva, E. A.,
Lacombe, B., Dreyer, I., Thibaud, J. B., and Kudla, J.
Baksheeva, V. E., Zhironkina, O. A., Zernii, E. Y.,
(2011) Calcium dependent modulation and plasma mem
Owens, R. A., Solovyev, A. G., and Morozov, S. Y. (2017)
brane targeting of the AKT2 potassium channel by the
Plant specific 4/1 polypeptide interacts with an endoplas
CBL4/CIPK6 calcium sensor/protein kinase complex,
mic reticulum protein related to human BAP31, Planta,
Cell Res., 21, 1116 1130, doi: 10.1038/cr. 2011.50.
245, 193 205, doi: 10.1007/s00425 016 2601 8.
45.
Musetti, R., Buxa, S. V., De Marco, F., Loschi, A.,
58.
Makarova, S. S., Minina, E. A., Makarov, V. V., Semenyuk, P. I.,
Polizzotto, R., Kogel, K. H., and van Bel, A. J. (2013)
Kopertekh, L., Schiemann, J., Serebryakova, M. V.,
Phytoplasma triggered Ca2+ influx is involved in sieve tube
Erokhina, T. N., Solovyev, A. G., and Morozov, S. Y.
blockage, Mol. Plant Microbe Interact., 26, 379386,
(2011) Orthologues of a plant specific At 4/1 gene in the
doi: 10.1094/MPMI 08 12 0207 R.
genus Nicotiana and the structural properties of bacterially
46.
Liu, L., Liu, C., Hou, X., Xi, W., Shen, L., Tao, Z., Wang, Y.,
expressed
4/1 protein, Biochimie,
93,
17701778,
and Yu, H. (2012) FTIP1 is an essential regulator required
doi: 10.1016/j.biochi.2011.06.018.
БИОХИМИЯ том 85 вып. 5 2020
634
ПАНКРАТЕНКО и др.
59.
Solovyev, A. G., Minina, E. A., Makarova, S. S., Erokhina, T. N.,
tosphingolipids and phytosterols, J. Biol. Chem., 290,
Makarov, V. V., Kaplan, I. B., Kopertekh, L., Schiemann, J.,
5810 5825, doi: 10.1074/jbc.M114.598805.
Richert Pöggeler, K. R., and Morozov, S. Y.
(2013)
73.
Konrad, S. S., and Ott, T. (2015) Molecular principles of
Subcellular localization and self interaction of plant spe
membrane microdomain targeting in plants, Trends Plant
cific Nt 4/1 protein, Biochimie,
95,
13601370,
Sci., 20, 351 361, doi: 10.1016/j.tplants.2015.03.016.
doi: 10.1016/j.biochi.2013.02.015.
74.
Cannon, K. S., Woods, B. L., Crutchley, J. M., and
60.
Morozov, S. Y., Makarova, S. S., Erokhina, T. N.,
Gladfelter, A. S. (2019) An amphipathic helix enables
Kopertekh, L., Schiemann, J., Owens, R. A., and
septins to sense micrometer scale membrane curvature,
Solovyev, A. G. (2014) Plant 4/1 protein: potential player
J. Cell Biol., 218, 1128 1137, doi: 10.1083/jcb.201807211.
in intracellular, cell to cell and long distance signaling,
75.
Baoukina, S., Ingólfsson, H. I., Marrink, S. J., and
Front. Plant Sci., 5, 26, doi: 10.3389/fpls.2014.00026.
Tieleman, D. P. (2018) Curvature induced sorting of lipids
61.
Atabekova, A. K., Lazareva, E. A., Strelkova, O. S.,
in plasma membrane tethers, Adv. Theory Simul., 1,
Solovyev, A. G., and Morozov, S. Y. (2018) Mechanical
1800034, doi: 10.1002/adts.201800034.
stress induced subcellular re localization of N terminally
76.
Aimon, S., Callan Jones, A., Berthaud, A., Pinot, M.,
truncated tobacco Nt 4/1 protein, Biochimie, 144, 98 107,
Toombes, G. E., and Bassereau, P. (2014) Membrane
doi: 10.1016/j.biochi.2017.10.020.
shape modulates transmembrane protein distribution, Dev.
62.
Atabekova, A. K., Pankratenko, A. V., Makarova, S. S.,
Cell, 28, 212 218, doi: 10.1016/j.devcel.2013.12.012.
Lazareva, E. A., Owens, R. A., Solovyev, A. G., and
77.
Makowski, S. L., Kuna, R. S., and Field, S. J. (2019)
Morozov, S. Y. (2017) Phylogenetic and functional analy
Induction of membrane curvature by proteins involved in
ses of a plant protein related to human B cell receptor
Golgi trafficking, Adv. Biol. Regul.,
75,
100661,
associated proteins, Biochimie, 132, 28 37, doi: 10.1016/
doi: 10.1016/j.jbior.2019.100661.
j.biochi.2016.10.009.
78.
González Sol s, A., Cano Ram rez, D. L., Morales
63.
Müller, M., Richter, K., Heuck, A., Kremmer, E.,
Cedillo, F., Tapia de Aquino, C., and Gavilanes Ruiz, M.
Buchner, J., Jansen, R. P., and Niessing, D.
(2009)
(2014) Arabidopsis mutants in sphingolipid synthesis as
Formation of She2p tetramers is required for mRNA bind
tools to understand the structure and function of mem
ing, mRNP assembly, and localization, RNA, 15, 2002
brane microdomains in plasmodesmata, Front. Plant Sci.,
2012, doi: 10.1261/rna.1753309.
5, 3, doi: 10.3389/fpls.2014.00003.
64.
Grison, M. S., Brocard, L., Fouillen, L., Nicolas, W.,
79.
De Saint Jean, M., Delfosse, V., Douguet, D., Chicanne, G.,
Wewer, V., Dörmann, P., Nacir, H., Benitez Alfonso, Y.,
Payrastre, B., Bourguet, W., Antonny, B., and Drin, G.
Claverol, S., Germain, V., Boutté, Y., Mongrand, S., and
(2011) Osh4p exchanges sterols for phosphatidylinositol
Bayer, E. M. (2015) Specific membrane lipid composition
4 phosphate between lipid bilayers, J. Cell Biol., 195, 965
is important for plasmodesmata function in Arabidopsis,
978, doi: 10.1083/jcb. 201104062.
Plant Cell.,
27,
1228 1250, doi:
10.1105/tpc.114.
80.
Martens, S., Kozlov, M. M., and McMahon, H. T. (2007)
135731.
How synaptotagmin promotes membrane fusion, Science,
65.
Marsh, D. (2010) Liquid ordered phases induced by cho
316, 1205 1208, doi: 10.1126/science.1142614.
lesterol: a compendium of binary phase diagrams, Biochim.
81.
Eisenberg Bord, M., Shai, N., Schuldiner, M., and
Biophys. Acta, 1798, 688 699, doi: 10.1016/j.bbamem.
Bohnert, M. (2016) A tether is a tether is a tether: tethering
2009.12.027.
at membrane contact sites, Dev. Cell, 39, 395409,
66.
Javanainen, M., Martinez Seara, H., and Vattulainen, I.
doi: 10.1016/j.devcel.2016.10.022.
(2017) Nanoscale membrane domain formation driven by
82.
Wong, L. H., Gatta, A. T., and Levine, T. P. (2019) Lipid
cholesterol, Sci. Rep., 7, 1143, doi: 10.1038/s41598 017
transfer proteins: the lipid commute via shuttles, bridges
01247 9.
and tubes, Nat. Rev. Mol. Cell Biol.,
20,
85101,
67.
Dufourc, E. J. (2008) Sterols and membrane dynamics,
doi: 10.1038/s41580 018 0071 5.
J. Chem. Biol., 1, 63 77, doi: 10.1007/s12154 008 0010 6.
83.
Drin, G., Casella, J. F., Gautier, R., Boehmer, T.,
68.
Milovanovic, D., Honigmann, A., Koike, S., Göttfert, F.,
Schwartz, T. U., and Antonny, B. (2007) A general amphi
Pähler, G., Junius, M., Müllar, S., Diederichsen, U.,
pathic α helical motif for sensing membrane curvature,
Janshoff, A., Grubmüller, H., Risselada, H. J., Eggeling, C.,
Nat. Struct. Mol. Biol., 14, 138146, doi: 10.1038/
Hell, S. W., van den Bogaart, G., and Jahn, R. (2015)
nsmb1194.
Hydrophobic mismatch sorts SNARE proteins into dis
84.
Simon, M. L., Platre, M. P., Assil, S., van Wijk, R.,
tinct membrane domains, Nat. Commun.,
6,
5984,
Chen, W. Y., Chory, J., Dreux, M., Munnik, T., and
doi: 10.1038/ncomms6984.
Jaillais, Y. (2014) A multi colour/multi affinity marker set
69.
Leijon, F., Melzer, M., Zhou, Q., Srivastava, V., and
to visualize phosphoinositide dynamics in Arabidopsis,
Bulone, V. (2018) Proteomic analysis of plasmodesmata
Plant J., 77, 322 37, doi: 10.1111/tpj.12358.
from populus cell suspension cultures in relation with cal
85.
Simon, M. L., Platre, M. P., Marquès Bueno, M. M.,
lose biosynthesis, Front. Plant Sci., 9, 1681, doi: 10.3389/
Armengot, L., Stanislas, T., Bayle, V., Caillaud, M. C., and
fpls.2018.01681.
Jaillais, Y. (2016) A PtdIns(4)P driven electrostatic field
70.
De Almeida, R. F., and Joly, E. (2014) Crystallization
controls cell membrane identity and signalling in plants,
around solid like nanosized docks can explain the speci
Nat. Plants, 2, 16089, doi: 10.1038/nplants.2016.89.
ficity, diversity, and stability of membrane microdomains,
86.
Platre, M. P., Noack, L. C., Doumane, M., Bayle, V.,
Front. Plant Sci., 5, 72, doi: 10.3389/fpls.2014.00072.
Simon, M. L. A., Maneta Peyret, L., Fouillen, L.,
71.
Gronnier, J., Germain, V., Gouguet, P., Cacas, J. L., and
Stanislas, T., Armengot, L., Pejchar, P., Caillaud, M. C.,
Mongrand, S. (2016) GIPC: Glycosyl Inositol Phospho
Potocký, M., Copic, A., Moreau, P., and Jaillais, Y. (2018)
Ceramides, the major sphingolipids on earth, Plant Signal.
A combinatorial lipid code shapes the electrostatic land
Behav., 11, e1152438, doi: 10.1080/15592324.2016.1152438.
scape of plant endomembranes, Dev. Cell., 45, 465 480,
72.
Grosjean, K., Mongrand, S., Beney, L., Simon Plas, F.,
e11, doi: 10.1016/j.devcel.2018.04.011.
and Gerbeau Pissot, P. (2015) Differential effect of plant
87.
Bian, X., Saheki, Y., and De Camilli, P. (2018) Ca2+ releas
lipids on membrane organization: specificities of phy
es E Syt1 autoinhibition to couple ER plasma membrane
БИОХИМИЯ том 85 вып. 5 2020
МЕМБРАННЫЕ КОНТАКТЫ ПЛАЗМОДЕСМ
635
tethering with lipid transport, EMBO J., 37, 219 234,
tance, Plant Physiol., 166, 14631478, doi: 10.1104/
doi: 10.15252/embj.201797359.
pp.114.246769.
88. Himschoot, E., Pleskot, R., Van Damme, D., and
103. Perraki, A., Binaghi, M., Mecchia, M. A., Gronnier, J.,
Vanneste, S. (2017) The ins and outs of Ca2+ in plant
German Retana, S., Mongrand, S., Bayer, E., Zelada, A. M.,
endomembrane trafficking, Curr. Opin. Plant Biol., 40, 131
and Germain, V. (2014) StRemorin1.3 hampers potato
137, doi: 10.1016/j.pbi.2017.09.003.
virus X TGBp1 ability to increase plasmodesmata perme
89. Graber, Z. T., Shi, Z., and Baumgart, T. (2017) Cations
ability, but does not interfere with its silencing suppressor
induce shape remodeling of negatively charged phospho
activity, FEBS Lett., 588, 1699 1705, doi: 10.1016/j.febslet.
lipid membranes, Phys. Chem. Chem. Phys., 19, 15285
2014.03.014.
15295, doi: 10.1039/c7cp00718c.
104. Zavaliev, R., Dong, X., and Epel, B. L. (2016) Glycosyl
90. Lahiri, S., Toulmay, A., and Prinz, W. A. (2015) Membrane
phosphatidylinositol (GPI) modification serves as a prima
contact sites, gateways for lipid homeostasis, Curr. Opin.
ry plasmodesmal sorting signal, Plant Physiol., 172, 1061
Cell Biol., 33, 82 87, doi: 10.1016/j.ceb.2014.12.004.
1073, doi: 10.1104/pp.16.01026.
91. Olkkonen, V. M. (2015) OSBP related protein family in
105. Faulkner, C., Akman, O. E., Bell, K., Jeffree, C., and
lipid transport over membrane contact sites, Lipid Insights,
Oparka, K. (2008) Peeking into pit fields: a multiple twin
8, 1 9, doi: 10.4137/LPI.S31726.
ning model of secondary plasmodesmata formation in
92. Chung, J., Torta, F., Masai, K., Lucast, L., Czapla, H.,
tobacco, Plant Cell,
20,
15041518, doi:
10.1105/
Tanner, L. B., Narayanaswamy, P., Wenk, M. R., Nakatsu, F.,
tpc.107.056903.
and De Camilli, P. (2015) PI4P/phosphatidylserine coun
106. Morvan, O., Quentin, M., Jauneau, A., Mareck, A., and
tertransport at ORP5 and ORP8 mediated ER-plasma
Morvan, C. (1998) Immunogold localization of pectin
membrane contacts, Science, 349, 428 432, doi: 10.1126/
methylesterases in the cortical tissues of flax hypocotyl,
science.aab1370.
Protoplasma, 202, 175 184, doi: 10.1007/BF01282545.
93. Ghai, R., Du, X., Wang, H., Dong, J., Ferguson, C.,
107. Yu, C. H., Guo, G. Q., Nie, X. W., and Zheng, G. C. (2004)
Brown, A. J., Parton, R. G., Wu, J. W., and Yang, H.
Cytochemical localization of pectinase activity in pollen
(2017) ORP5 and ORP8 bind phosphatidylinositol 4,
mother cells of tobacco during meiotic prophase I and Its
5 biphosphate (PtdIns(4,5)P2) and regulate its level at the
relation to the formation of secondary plasmodesmata and
plasma membrane, Nat. Commun., 8, 757, doi: 10.1038/
cytoplasmic channels, Acta Bot. Sin., 46, 1443 1453.
s41467 017 00861 5.
108. Baluska, F., Samaj, J., Napier, R., and Volkmann, D.
94. Yamaji, T., Kumagai, K., Tomishige, N., and Hanada, K.
(1999) Maize calreticulin localizes preferentially to plas
(2008) Two sphingolipid transfer proteins, CERT and
modesmata in root apex, Plant J.,
19,
481488,
FAPP2: their roles in sphingolipid metabolism, IUBMB
doi: 10.1046/j.1365 313x.1999.00530.x.
Life, 60, 511 518, doi: 10.1002/iub.83.
109. Foreman, J., Demidchik, V., Bothwell, J. H. F., Mylona, P.,
95. McMahon, H. T., and Boucrot, E. (2015) Membrane cur
Miedema, H., Torresk, M. A., Linstead, P., Costa, S.,
vature at a glance, J. Cell Sci.,
128,
10651070,
Brownlee, C., Jonesk, J. D. G., Davies, J. M., and Dolan, L.
doi: 10.1242/jcs.114454.
(2003) Reactive oxygen species produced by NADPH oxi
96. Sager, R., and Lee, J. Y. (2014) Plasmodesmata in integrat
dase regulate plant cell growth, Nature, 422, 442 446,
ed cell signalling: insights from development and environ
doi: 10.1038/nature01485.
mental signals and stresses, J. Exp. Bot., 65, 6337 6358,
110. Benitez Alfonso, Y., and Jackson, D. (2009) Redox homeo
doi: 10.1093/jxb/eru365.
stasis regulates plasmodesmal communication in
97. Dorokhov, Y. L., Ershova, N. M., Sheshukova, E. V., and
Arabidopsis meristems, Plant Signal. Behav., 4, 655 659,
Komarova, T. V. (2019) The role of plasmodesmata associ
doi: 10.4161/psb.4.7.8992.
ated receptor in plant development and environmental
111.
Xu, K., and Nagy, P. D. (2014) Expanding use of multi ori
response, Plants (Basel),
8, E595, doi:
10.3390/
gin subcellular membranes by positive strand RNA viruses
plants8120595.
during replication, Curr. Opin. Virol.,
9,
119126,
98. De Storme, N., and Geelen, D. (2014) Callose homeosta
doi: 10.1016/j.coviro.2014.09.015.
sis at plasmodesmata: molecular regulators and develop
112. Barajas, D., Xu, K., Fernandez de Castro Martin, I.,
mental relevance, Front Plant Sci.,
5,
138,
Sasvari, Z., Brandizzi, F., Risco, C., and Nagy, P. D. (2014)
doi: 10.3389/fpls.2014.00138.
Co opted oxysterol binding ORP and VAP proteins chan
99. Paul, L. K., Rinne, P. L., and van der Schoot, C. (2014)
nel sterols to RNA virus replication sites via membrane
Refurbishing the plasmodesmal chamber: a role for lipid
contact sites, PLoS Pathog., 10, e1004388, doi: 10.1371/
bodies, Front. Plant Sci., 5, 40, doi: 10.3389/fpls.2014.
journal.ppat.1004388.
00040.
113. Pitzalis, N., and Heinlein, M. (2017) The roles of mem
100. Lee, J. Y., Wang, X., Cui, W., Sager, R., Modla, S.,
branes and associated cytoskeleton in plant virus replica
Czymmek, K., Zybaliov, B., van Wijk, K., Zhang, C., Lu, H.,
tion and cell to cell movement, J. Exp. Bot., 69, 117 132,
and Lakshmanan, V. (2011) A plasmodesmata localized
doi: 10.1093/jxb/erx334.
protein mediates crosstalk between cell to cell communi
114. Epel, B. L. (2009) Plant viruses spread by diffusion on ER
cation and innate immunity in Arabidopsis, Plant Cell, 23,
associated movement protein rafts through plasmodesma
3353 3373, doi: 10.1105/tpc.111.087742.
ta gated by viral induced host beta 1,3 glucanases, Semin.
101. Wang, X., Sager, R., Cui, W., Zhang, C., Lu, H., and
Cell Dev. Biol., 20, 1074 1081, doi: 10.1016/j.semcdb.
Lee, J. Y. (2013) Salicylic acid regulates plasmodesmata
2009.05.010.
closure during innate immune responses in Arabidopsis,
115. Zavaliev, R., Levy, A., Gera, A., and Epel, B. L. (2013)
Plant Cell, 25, 2315 2329, doi: 10.1105/tpc.113.110676.
Subcellular dynamics and role of arabidopsis β 1,3 glu
102. Gui, J., Liu, C., Shen, J., and Li, L. (2014) Grain setting
canases in cell to cell movement of tobamoviruses, Mol.
defect1, encoding a remorin protein, affects the grain set
Plant Microbe Interact., 26, 1016 1030, doi: 10.1094/
ting in rice through regulating plasmodesmatal conduc
MPMI 03 13 0062 R.
БИОХИМИЯ том 85 вып. 5 2020
636
ПАНКРАТЕНКО и др.
MEMBRANE CONTACTS IN PLASMODESMATA:
STRUCTURAL COMPONENTS AND THEIR FUNCTIONS
Review
A. V. Pankratenko1, A. K. Atabekova1, S. Y. Morozov1,2, and A. G. Solovyev1,2,3,4*
1 Lomonosov Moscow State University, Faculty of Biology, Department of Virology, 119991 Moscow, Russia
2 Belozersky Institute of Physico(Chemical Biology, Lomonosov Moscow State University,
119992 Moscow, Russia; E(mail: solovyev@belozersky.msu.ru
3 Sechenov First Moscow State Medical University, Institute of Molecular Medicine, 119991 Moscow, Russia
4 Institute of Agricultural Biotechnology, 127550 Moscow, Russia
Received February 12, 2020
Revised March 10, 2020
Accepted March 16, 2020
Plasmodesmata (PDs) are channels connecting the cells in plant tissues. In plasmodesmata the cytoplasm, plasma
membrane (PM), and endoplasmic reticulum (EPR) of neighboring cells are joined. Through PDs macromolecules,
such as proteins and RNA, are transported that ensures the functional unity of plant tissues and transmission of sig
nals necessary for individual development and responses to external signals. Recent studies have shown that PDs
include membrane contacts (MCs), which are specialized structures formed with participation of a number of protein
components connecting EPR and PMs. In general, as shown mainly for animal cells, membrane contacts between
EPR and plasma membranes are involved in the transfer of lipid and protein components between these membrane
compartments, as well as in maintaining the structural integrity of EPR and in response to stress. The structure of MCs
in plasmodesmata of plants is studied much worse, and at present active studies on the structural elements of PDs
responsible for the connection between EPR and plasma membranes within these organelles are just started. In the
present review, the structural and functional properties of proteins are considered that are proven or supposed to estab
lish membrane contacts in plasmodesmata. In addition, we discuss the role of cytoskeleton, lipid microdomains with
in membranes, and cell wall components for the maintenance and remodeling of plasmodesmata MCs during various
external biotic and abiotic stresses.
Keywords: plasmodesmata, membrane contacts, endoplasmic reticulum, plasma membrane, membrane
microdomains, plasmodesmata proteins, membrane contact proteins, plant viruses
БИОХИМИЯ том 85 вып. 5 2020