БИОХИМИЯ, 2020, том 85, вып. 6, с. 755 - 762
УДК 576.315.42
РОЛЬ РАЗДЕЛЕНИЯ ЖИДКИХ ФАЗ В КОМПАРТМЕНТАЛИЗАЦИИ
КЛЕТОЧНОГО ЯДРА И ПРОСТРАНСТВЕННОЙ
ОРГАНИЗАЦИИ ГЕНОМА
Обзор
© 2020
С.В. Разин1,2*, А.А. Гаврилов1
1 Институт биологии гена Российской академии наук,
119334 Москва, Россия; электронная почта: sergey.v.razin@usa.net
2 Московский государственный университет имени М.В. Ломоносова,
биологический университет, 119991 Москва, Россия
Поступила в редакцию 24.03.2020
После доработки 07.04.2020
Принята к публикации 09.04.2020
Функциональная компартментализация клеточного ядра играет важную роль в регуляции работы генома,
обеспечивая возможность концентрации ферментов в реакционных центрах, таких как транскрипционные
фабрики, тельца Кахаля, спеклы и др. Механизмы, обеспечивающие функциональную компартментализа#
цию клеточного ядра, не до конца изучены. В настоящее время есть веские основания полагать, что веду#
щую роль здесь играет физический процесс разделения жидких фаз. В этом кратком обзоре проанализиро#
ваны экспериментальные работы, демонстрирующие, что разделение жидких фаз не только обеспечивает
функциональную компартментализацию клеточного ядра, но и вносит важный вклад в формирование 3D
архитектуры генома.
КЛЮЧЕВЫЕ СЛОВА: разделение жидких фаз, хроматин, клеточное ядро, транскрипция, ядерный ком#
партмент, пространственная организация генома.
DOI: 10.31857/S0320972520060019
ВВЕДЕНИЕ
ца Кахаля, PML#тельца, спеклы и др.), но не ог#
раничиваются ими. К числу функциональных
На роль стохастических процессов в компарт#
компартментов можно отнести, например, при#
ментализации клеточного ядра обратили внима#
ламеллярный и околоядрышковый слои ядра,
ние сравнительно недавно в связи с демонстра#
где сосредоточена значительная часть неактив#
цией того, что энтропийные силы, возникаю#
ного хроматина. Было показано, что ядерные
щие при очень высокой концентрации макро#
тельца легко разбираются при снижении уровня
молекул, имеющей место в клеточном ядре (т. н.
макромолекулярного краудинга и восстанавли#
условия макромолекулярного краудинга), игра#
ваются при его повышении. Силы, возникаю#
ют важную роль в формировании ядрышка, те#
щие в условиях макромолекулярного краудинга,
лец Кахаля, PML#телец и ряда других функцио#
способствуют агрегации любых крупных объек#
нальных внутриядерных компартметов [1-4]. В
тов [3]. Например, агрегации инициированных
данном обзоре функциональным компартмен#
транскрипционных комплексов с образованием
том обозначен локальный участок клеточного
т.н. транскрипционных фабрик [5]. Однако не#
ядра, в котором концентрация ферментов и
специфическая агрегация тех или иных макро#
вспомогательных факторов, участвующих в осу#
молекул и их комплексов не может объяснить
ществлении того или иного функционального
многих свойств ядерных телец, которые харак#
процесса, существенно превышает таковую в
теризуются, в частности, сферической формой,
остальных частях ядра. Функциональные ком#
способностью объединяться и быстрым обме#
партменты включают т.н. ядерные тельца (тель#
ном составляющими их компонентами с окру#
жающей средой. Все это типично для объектов,
возникших в результате разделения жидких фаз
Принятые сокращения: IDR (intrinsically disordered
regions) - неструктурированный домен; IC (interchromatin
[6, 7]. Примером таких объектов могут служить
compartment) - интерхроматиновый компартмент.
капельки жира в водной среде. Для того, чтобы
* Адресат для корреспонденции.
начался процесс разделения жидких фаз, необ#
755
756
РАЗИН, ГАВРИЛОВ
ходимо, чтобы составляющие выделяющуюся
ких фаз [22]. На первый взгляд, существует не#
фазу компоненты были способны взаимодей#
кое противоречие между тем, что ядерные ком#
ствовать друг с другом, причем взаимодействия
партменты являются относительно специфич#
должны быть множественными и неспецифи#
ными (т.е. содержат определенные наборы бел#
ческими [8]. Показано, что такие взаимодей#
ков), в то время как процесс выделения жидких
ствия легко возникают между неструктуриро#
фаз базируется на неспецифических взаимодей#
ванными (дезорганизованными) доменами
ствиях. В действительности, никакого противо#
(intrinsically disordered regions, IDRs), присут#
речия здесь нет. Для того, чтобы инициировать
ствующими в составе многих ядерных белков, в
процесс разделения жидких фаз, необходимо
том числе гистонов и белков гетерохроматина
обеспечить высокую локальную концентрацию
[9-16]. Будучи сконцентированными в ограни#
способных к взаимодействию белков. Это ста#
ченном пространстве, эти белки легко устанав#
новится возможным благодаря мультимериза#
ливают множественные взаимодействия, при#
ции, либо привлечения к некой платформе бел#
водящие к выделению их в отдельную жидкую
ков, обладающих способностью специфически
фазу [8] (рис. 1). Характер взаимодействий мо#
связываться с этой платформой (рис. 1).
жет быть различным, однако в биологических
Платформой может быть белок, например,
системах наиболее часто разделение жидких фаз
белок PML в PML тельцах [23, 24], или некоди#
стимулируется гидрофобными взаимодействия#
рующая РНК, например, NEAT в параспеклах
ми между IDR. Такие взаимодействия весьма
[25-27]. Индуцированная светом определенной
чувствительны к обработке 2,6#гександиолом
длины мультимеризация химерных белков ис#
[17], в силу чего эта обработка используется для
пользуется в оптогенетической системе, позво#
тестирования предположения о том, что изучае#
ляющей оценить потенциал различных IDR к
мый объект возник в силу разделения жидких
образованию фазовых конденсатов [28]. В этой
фаз [13, 18, 19]. Типичным примером внутрия#
системе тестируемый IDR экспрессируется в
дерного компартмента, возникшего посред#
составе химерного белка с активируемым све#
ством разделения жидких фаз, является ядрыш#
том, мультимеризующимся доменом белка Cry2
ко [20]. Находящиеся внутри ядрышка фибрил#
Arabidopsis thaliana. При достижении некой по#
лярные центры, в составе которых присутствует
роговой концентрации химерного белка в клет#
активная РНК полимераза I, выделяются из ос#
ках облучение их голубым светом приводит к
тальной части ядрышка также благодаря разде#
мультимеризации химерного белка и последую#
лению жидких фаз [21]. Таким образом, ядрыш#
щему разделению жидких фаз в том случае, ког#
ко является многкомпонентной системой,
да тестируемые IDR способны к неспецифичес#
сформированной посредством разделения жид#
кому взаимодействию.
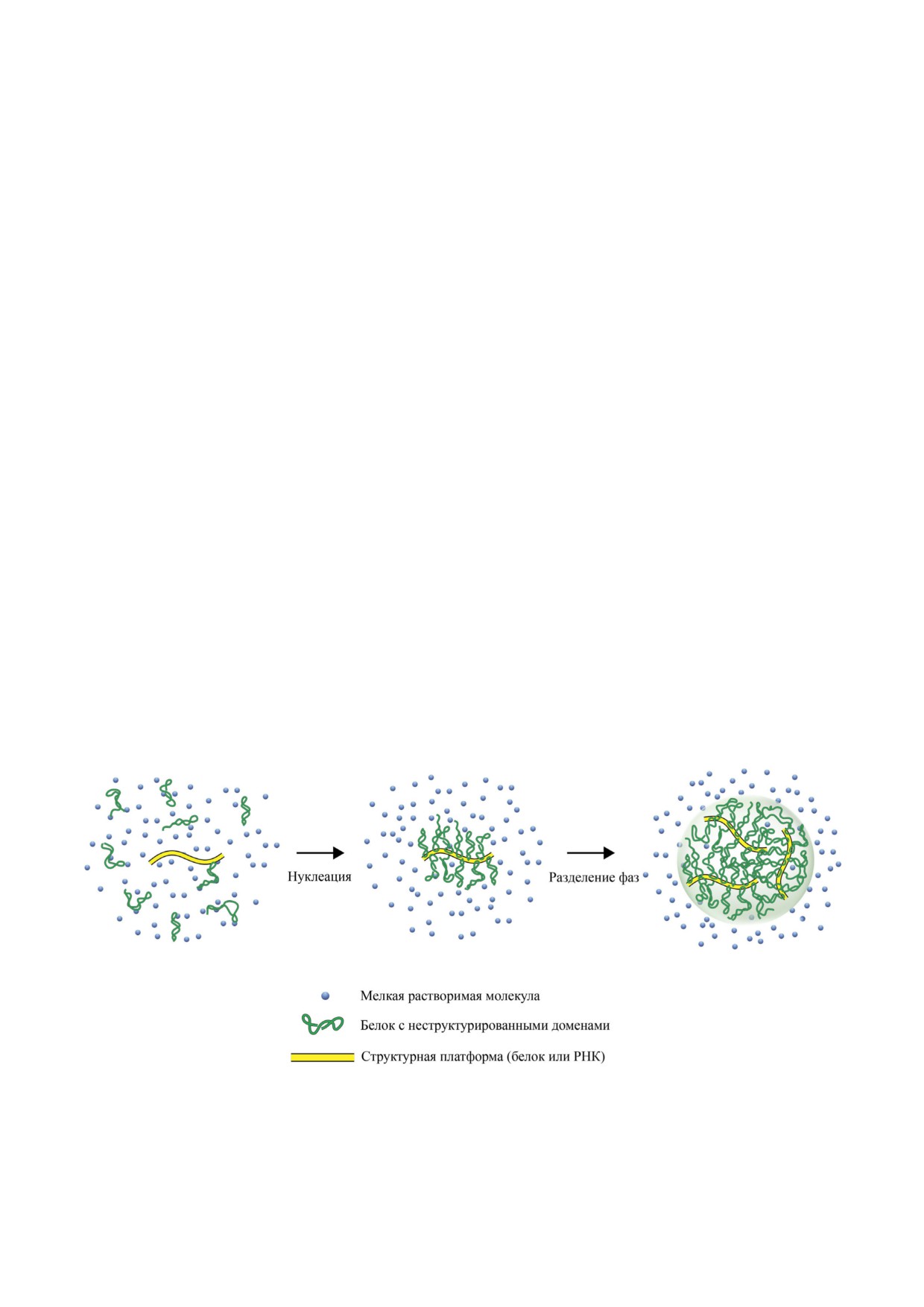
Рис. 1. Принцип разделения жидких фаз в клеточном ядре. Белки, несущие неструктурированные домены, взаимодей#
ствуют с общей структурной платформой, роль которой может выполнять белок или РНК. Дальнейшее взаимодействие
неструктурированных доменов между собой приводит к образованию «белковой капли». (С цветным вариантом рис. 1 и 2
БИОХИМИЯ том 85 вып. 6 2020
РАЗДЕЛЕНИЕ ЖИДКИХ ФАЗ И КОМПАРТМЕНТАЛИЗАЦИЯ ЯДРА
757
РОЛЬ РАЗДЕЛЕНИЯ
ный хроматин, а внутри - неактивный [45, 46].
ЖИДКИХ ФАЗ В ГЛОБАЛЬНОЙ
Хроматиновый домен пронизывают так называ#
КОМПАРТМЕНТАЛИЗАЦИИ ЯДРА
емые интерхроматиновые каналы, совокуп#
ность которых составляет интерхроматиновый
Говоря о компартментализации клеточного
компартмент (interchromatin compartment, IC),
ядра, стоит прежде всего упомянуть хроматино#
который служит для транспорта различных мак#
вый домен, состоящий из связанных друг с дру#
ромолекул, в том числе, новосинтезированных
гом хромосомных территорий. Излишне гово#
РНК, а также является местом расположения
рить о том, что в этом домене крайне высока
различных ядерных структур, таких как ядрыш#
концентрация гистонов. Хорошо известно, что
ко, спеклы, тельца Кахаля и др. [45-47]. Меха#
нуклеосомы могут устанавливать контакты че#
низмы, обеспечивающие существование IC, не
рез посредство N#концевых доменов гистонов
вполне понятны. Не исключено, что и здесь
[29-32]. Наиболее популярная модель объясня#
важную роль играет процесс разделения жидких
ет установление таких контактов электростати#
фаз, потому что заполняющие IC РНК и РНК#
ческим взаимодействием N#концевого домена
связывающие белки могут взаимодействовать
гистона H4 с отрицательно заряженным доме#
друг с другом, стимулируя процесс фазового
ном (acidic patch) на поверхности соседней нук#
разделения [48, 49].
леосомной глобулы [33-36]. Однако ряд резуль#
Важную роль в глобальной организации кле#
татов позволяет полагать, что не менее важным
точного ядра играют расположенные в IC функ#
для опосредованной межнуклеосомными взаи#
циональные компартменты, многие из которых
модействиями конденсации хроматина является
являются фазовыми конденсатами [40]. Если го#
процесс разделения жидких фаз [37]. Разные ти#
ворить о глобальной организации ядра, то преж#
пы хроматина, по#видимому, обладают неоди#
де всего следует обратить внимание на компарт#
наковой способностью к выделению в обособ#
менты, играющие важную роль в простран#
ленную фазу. Так, процесс образования фазовых
ственной организации хроматинового домена
конденсатов существенно стимулируется гисто#
посредством привлечения к ним определенных
ном H1, который в присутствии ДНК способен
типов хроматина. Давно известно, что значи#
образовывать фазовые конденсаты in vitro [38].
тельная часть неактивного хроматина располо#
Многие белки гетерохроматина, в том числе
жена рядом с ядрышком [50, 51]. Результаты
HP1 и белки комплексов Polycomb, также содер#
полногеномных исследований, выполненных с
жат IDR, способные взаимодействовать с обра#
использованием новых экспериментальных
зованием фазовых конденсатов [13, 14, 39-41].
подходов, позволяющих картировать гены, рас#
В ряде ситуаций жидкие фазовые конденсаты
положенные рядом с различными ядерными
могут в последующем переходить в гелеобразное
компартментами, показывают, что ядрышко
состояние [39, 42]. Этот процесс фактически
составляет своего рода инактивирующий хаб,
сводится к переходу от жидкого фазового кон#
рядом с которым сосредоточены неактивные ге#
денсата к полимерному фазовому конденсату,
ны [52, 53]. Другим таким хабом является ядер#
возникновение которого обеспечивается уста#
ная ламина [52]. Активные гены предпочтитель#
новлением внутренних сшивок в полимере.
но сосредоточены рядом со спеклами [52, 53],
Среди компонентов активного хроматина также
которые также являются ядерными компарт#
есть белки, способные при определенных кон#
ментами, возникающими вследствие разделе#
центрациях формировать фазовые конденсаты
ния жидких фаз. В спеклах сосредоточены фак#
[37]. IDR присутствуют в составе самой РНК
торы сплайсинга. Предполагается, что привле#
полимеразы II, медиатора и многих транскрип#
чение к этим компартментам активных генов
ционных факторов [15, 16, 43, 44].
обеспечивает возможность быстрого процес#
В силу всего сказанного выше можно пола#
синга новосинтезированных транскриптов. Су#
гать, что хроматиновый домен в целом выделя#
ществуют и другие объяснения повышения
ется внутри ядра посредством фазового перехо#
уровня транскрипции генов, расположенных
да. Более того, сам по себе хроматиновый домен
рядом со спеклами [54]. Хорошо изученными
состоит из двух раличающихся фазовых конден#
ядерными компартментами, возникающими
сатов, соответствующих эухроматину и гетеро#
посредством разделения жидких фаз, являются
хроматину. Анализ хромосомных территорий,
тельца Кахаля. В этих тельцах сосредоточены
выполненный с использованием микроскопии
ферменты, участвующие в модификации малых
высокого разрешения, свидетельствует о том,
ядерных РНК, процессинге концов не подверга#
что хромосомные территории состоят из глобу#
ющейся полиаденилированию РНК и ряде дру#
лярных структур, содержащих ~ 1000 т.п.н.
гих процессов [55]. Подобно спеклам, тельца
ДНК, на поверхности которых находится актив#
Кахаля также являются некими хабами, к кото#
БИОХИМИЯ том 85 вып. 6 2020
758
РАЗИН, ГАВРИЛОВ
рым могут привлекаться различные гены вне за#
ных доменов, присутствующих в составе РНК
висимости от близости их расположения на
полимеразы, медиатора и многих транскрипци#
ДНК [56, 57].
онных факторов [18, 70, 71]. Необходимая для
Еще одним типом внутриядерных компарт#
инициации процесса разделения жидких фаз
ментов, который стоит упомянуть в нашей дис#
концентрация взаимодействующих компонен#
куссии, являются транскрипционные фабрики.
тов обеспечивается наличием множественных
Достаточно давно было показано, что иници#
сайтов их связывания в границах энхансера.
ированные и элонгирующие молекулы РНК по#
Роль платформы, привлекающей дополнитель#
лимеразы II собраны в кластеры, которые и по#
ные белки, может играть энхансерная РНК [72,
лучили название «транскрипционные фабрики»
73]. Суперэнхансеры, как правило, состоят из
[58-61]. Механизмы формирования транскрип#
нескольких энхансерных модулей, разделенных
ционных фабрик и возможная роль этих струк#
спейсерами различной длины. Выпетливание
тур обсуждается в литературе в течение 25 лет [5,
разделяющих энхансерные модули сегментов
58, 62, 63]. В последние годы появились убеди#
хроматиновой фибриллы позволяет объеди#
тельные свидетельства того, что кластеризация
ниться собранным на этих доменах активатор#
транскрипционных комплексов обеспечивается
ным комплексам в единый комплекс [70]. Про#
процессом разделения жидких фаз, регулируе#
цесс этот может происходить без каких#либо
мого фосфорилированием С#концевого домена
затрат энергии, так как способность к слиянию
РНК полимеразы II [15]. Важно, что к тран#
является внутренним свойством жидких фазо#
скрипционным фабрикам могут привлекаться
вых конденсатов [74]. Для того, чтобы быть ак#
гены, расположенные на значительных геном#
тивированным тем или иным энхансером, про#
ных расстояниях, а иногда и на разных хромосо#
мотор должен оказаться внутри активаторного
мах [64, 65]. То же справедливо и для привлече#
комплекса, собранного на этом энхансере. По#
ния генов к ядрышку или спеклам. В результате
видимому, это происходит аналогично процессу
отдельные хромосомные территории оказыва#
объединения доменов суперэнхансера. На про#
ются объединенными в единый хроматиновый
моторе собирается свой жидкий конденсат,
домен. Этот домен является достаточно элас#
компоненты которого (транскрипционные
тичным в силу того, что уровень компактизации
факторы, РНК полимераза и т.д.) в значитель#
хроматина может изменяться в широких преде#
ной мере перекрываются компонентами соб#
лах в ответ на различные воздействия, напри#
ранного на энхансере активаторного комплекса
мер, в ответ на гипотонический шок. Было по#
[15, 75]. Такие комплексы могут легко слиться,
казано, что, будучи прикрепленным одновре#
в результате чего промотор будет удерживаться
менно к ядрышку и ядерной ламине, хроматин
в среде, обеспечивающей благоприятные усло#
механически растянут. Утрата заякориваний на
вия для его работы [71] (рис. 2). Детали всех
ядерной ламине приводит к сокращению объе#
этих процессов еще предстоит выяснить. В нас#
ма хроматинового домена [66].
тоящее время продемонстрировано, что на су#
перэнхансерах формируются фазовые конден#
саты, содержащие различные факторы тран#
РОЛЬ РАЗДЕЛЕНИЯ ЖИДКИХ ФАЗ
скрипции, РНК полимеразу II и медиатор, и
В РЕГУЛЯЦИИ ТРАНСКРИПЦИИ
что к этим конденсатам привлекаются актив#
ные гены, работа которых направляется данны#
Отличительной особенностью систем конт#
ми суперэнхансерами [18, 19]. Открытыми ос#
роля транскрипции в эукариотической клетке
таются вопросы о том, как определяется специ#
является наличие удаленных энхансеров. По
фика активации суперэнхансером определен#
современным представлениям, количество эн#
ных промоторов, как происходит освобождение
хансеров в геноме человека, по меньшей мере, в
элонгирующей РНК полимеразы из энхансер#
10 раз превосходит количество промоторов [67,
промоторного комплекса, влияет ли энхансер
68]. Механизм действия энхансеров остается
на процесс элонгации и т.д. Недавно было про#
предметом дискуссий [69]. В последние годы
демонстрировано, что фосфорилирование С#
опубликовано несколько работ, указывающих
концевого домена РНК полимеразы II регули#
на то, что на энхансере формируется активатор#
рует ее сродство к конденсатам, содержащим
ный комплекс, обогащенный различными
медиатор, и конденсатам, содержащим факто#
транскрипционными факторами и компонен#
ры сплайсинга [76]. Можно ожидать, что в бли#
тами транскрипционного аппарата [70]. В фор#
жайшее время число примеров регулируемого
мировании данного комплекса ключевую роль
перемещения макромолекул между различны#
играет процесс разделения жидких фаз, направ#
ми фазовыми компартментами существенно
ляемый взаимодействием неструктурирован#
возрастет.
БИОХИМИЯ том 85 вып. 6 2020
РАЗДЕЛЕНИЕ ЖИДКИХ ФАЗ И КОМПАРТМЕНТАЛИЗАЦИЯ ЯДРА
759
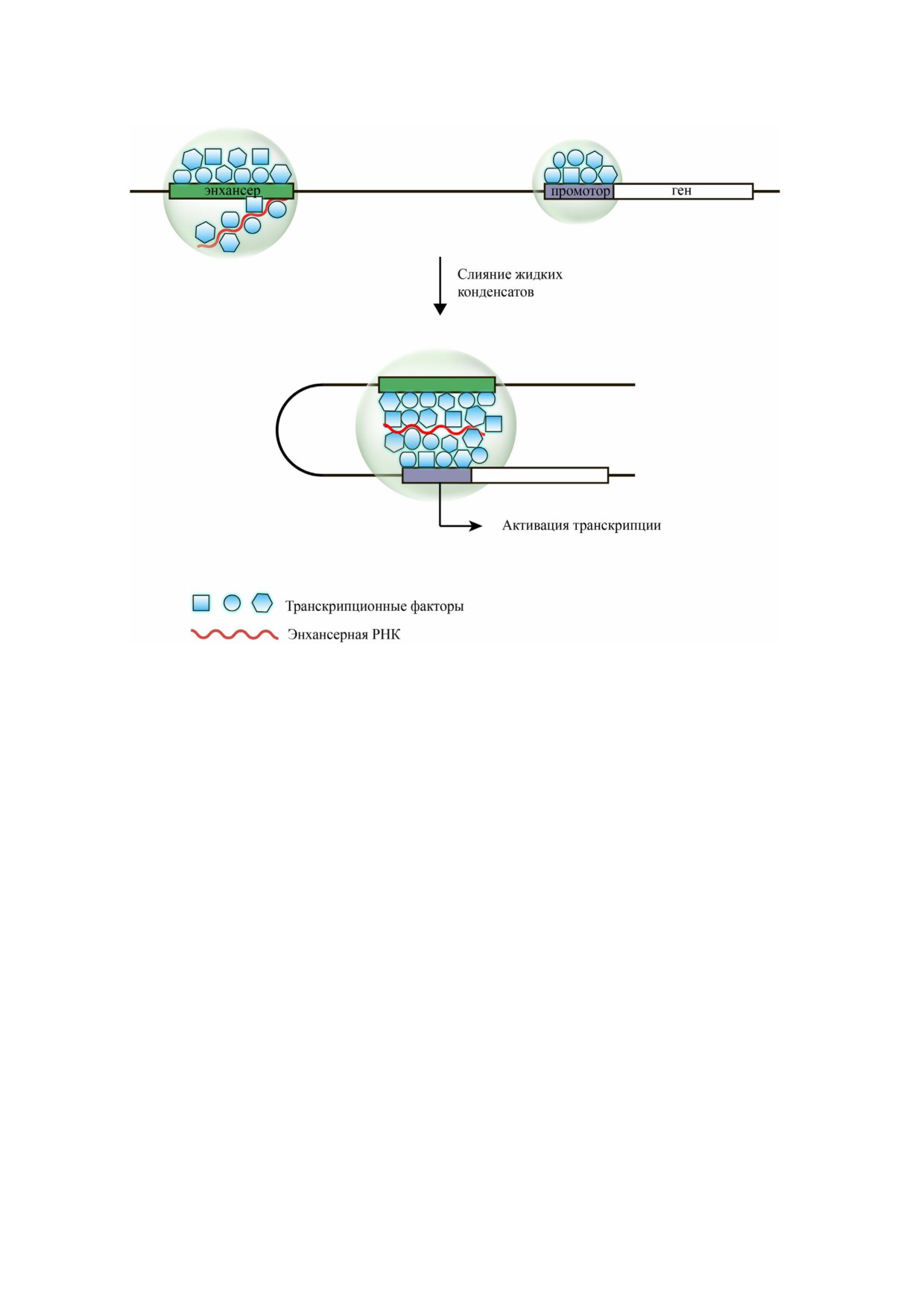
Рис. 2. Роль жидкостного разделения фаз в коммуникации энхансеров и промоторов. Транскрипционные факторы связы#
ваются с энхансером и промотором с образованием жидкостных конденсатов. Дальнейшее слияние конденсатов обеспе#
чивает сближение промотора и энхансера и активацию транскрипции
Изучение роли разделения жидких фаз в
выми конденсатами, удовлетворяют всем этим
клеточном ядре стало одним из наиболее дина#
критериям [42, 78]. Не отрицая важную роль
мично развивающихся направлений в молеку#
процесса разделения жидких фаз в формирова#
лярной биологии. Иногда складывается впечат#
нии внутриядерной архитектуры, включая и 3D
ление, что разделением жидких фаз пытаются
организацию генома, мы полагаем, что вся эта
объяснить все, что происходит в клеточном яд#
организация складывается в результате коопера#
ре. При этом нередко игнорируются те факты,
ции комплекса различных механизмов, вклад
которые не укладываются в развиваемую мо#
каждого из которых будет различен в конкрет#
дель. В этой связи хотелось бы обратить внима#
ных случаях. Так, формирование гетерохрома#
ние на необходимость более взвешенного ана#
тиновых доменов может начинаться с разделе#
лиза результатов. Если говорить о роли разделе#
ния жидких фаз и заканчиваться образованием
ния жидких фаз в формировании хроматиновых
гелей, которые по ряду параметров существенно
доменов, то стоит указать на то, что многие ре#
отличаются от жидких конденсатов [39, 42].
зультаты, указывающие на способность гисто#
нов и белков гетерохроматина образовывать фа#
Финансирование. Работа выполнена при фи#
зовые конденсаты, получены в экспериментах in
нансовой поддержке Российского научного
vitro [37]. Результаты экспериментов, предпри#
фонда (грант 18#14#00011).
нятых для того, чтобы продемонстрировать роль
Конфликт интересов. Авторы заявляют, что у
разделения жидких фаз в формировании гете#
них нет конфликта интересов.
рохроматина в живых клетках, остаются доволь#
Соблюдение этических норм. Настоящая
но противоречивыми [13, 77]. Критерии фазо#
статья не содержит описания исследований с
вых конденсатов остаются размытыми, и далеко
участием людей или использованием животных
не все объекты, которые принято считать фазо#
в качестве объектов.
БИОХИМИЯ том 85 вып. 6 2020
760
РАЗИН, ГАВРИЛОВ
СПИСОК ЛИТЕРАТУРЫ
1.
Hancock, R. (2004) Internal organisation of the nucleus:
through carboxy#terminal domain phase separation, Nat.
assembly of compartments by macromolecular crowding
Struct. Mol. Biol., 25, 833#840, doi: 10.1038/s41594#018#
and the nuclear matrix model, Biol. Cell, 96, 595#601.
0112#y.
2.
Hancock, R. (2004) A role for macromolecular crowding
16.
Nagulapalli, M., Maji, S., Dwivedi, N., Dahiya, P., and
effects in the assembly and function of compartments in
Thakur, J. K. (2016) Evolution of disorder in mediator
the nucleus, J. Struct. Biol., 146, 281#290, doi: 10.1016/
complex and its functional relevance, Nucleic Acids Res.,
j.jsb.2003.12.008.
44, 1591#1612, doi: 10.1093/nar/gkv1135.
3.
Hancock, R. (2018) Crowding, entropic forces, and con#
17.
Alberti, S., Gladfelter, A., and Mittag, T.
(2019)
finement: crucial factors for structures and functions in the
Considerations and challenges in studying liquid-liquid
cell nucleus, Biochemistry (Moscow), 83, 326#337, doi:
phase separation and biomolecular condensates, Cell, 176,
10.1134/S0006297918040041.
419#434, doi: 10.1016/j.cell.2018.12.035.
4.
Marenduzzo, D., Finan, K., and Cook, P. R. (2006) The
18.
Sabari, B. R., Dall’Agnese, A., Boija, A., Klein, I. A.,
depletion attraction: an underappreciated force driving
Coffey, E. L., Shrinivas, K., Abraham, B. J., Hannett, N. M.,
cellular organization, J. Cell. Biol., 175, 681#686, doi:
Zamudio, A. V., Manteiga, J. C., Li, C. H., Guo, Y. E.,
10.1083/jcb.200609066.
Day, D. S., Schuijers, J., Vasile, E., Malik, S., Hnisz, D.,
5.
Razin, S. V., Gavrilov, A. A., Pichugin, A., Lipinski, M.,
Lee, T. I., Cisse, I. I., Roeder, R. G., et al. (2018) Coactivator
Iarovaia, O. V., and Vassetzky, Y. S. (2011) Transcription
condensation at super#enhancers links phase separation and
factories in the context of the nuclear and genome organi#
gene control, Science, 361, doi: 10.1126/science.aar3958.
zation, Nucleic Acids Res., 39, 9085#9092, doi: 10.1093/
19.
Cho, W. K., Spille, J. H., Hecht, M., Lee, C., Li, C.,
nar/gkr683.
Grube, V., and Cisse, I. I. (2018) Mediator and RNA poly#
6.
Erdel, F., and Rippe, K. (2018) Formation of chromatin
merase II clusters associate in transcription#dependent
subcompartments by phase separation, Biophys. J., 114,
condensates, Science, 361, 412#415, doi: 10.1126/science.
2262#2270, doi: 10.1016/j.bpj.2018.03.011.
aar4199.
7.
Boeynaems, S., Alberti, S., Fawzi, N. L., Mittag, T.,
20.
Hernandez#Verdun, D. (2006) The nucleolus: a model for
Polymenidou, M., Rousseau, F., Schymkowitz, J., Shorter, J.,
the organization of nuclear functions, Histochem. Cell.
Wolozin, B., Van Den Bosch, L., Tompa, P., and Fuxreiter, M.
Biol., 126, 135#148, doi: 10.1007/s00418#006#0212#3.
(2018) Protein phase separation: a new phase in cell biolo#
21.
Yao, R. W., Xu, G., Wang, Y., Shan, L., Luan, P. F.,
gy, Trends Cell. Biol., 28, 420#435, doi: 10.1016/j.tcb.
Wang, Y., Wu, M., Yang, L. Z., Xing, Y. H., Yang, L., and
2018.02.004.
Chen, L. L. (2019) Nascent pre#rRNA sorting via phase
8.
Uversky, V. N. (2017) Protein intrinsic disorder#based liq#
separation drives the assembly of dense fibrillar compo#
uid-liquid phase transitions in biological systems: complex
nents in the human nucleolus, Mol. Cell, 76, 767#783,
coacervates and membrane#less organelles, Adv. Coll.
e711, doi: 10.1016/j.molcel.2019.08.014.
Interface Sci., 239, 97#114, doi: 10.1016/j.cis.2016.05.012.
22.
Correll, C. C., Bartek, J., and Dundr, M. (2019) The
9.
Meng, F., Na, I., Kurgan, L., and Uversky, V. N. (2015)
nucleolus: a multiphase condensate balancing ribosome
Compartmentalization and functionality of nuclear disor#
synthesis and translational capacity in health, aging and
der: intrinsic disorder and protein-protein interactions in
ribosomopathies, Cells, 8, doi: 10.3390/cells8080869.
intra#nuclear compartments, Intern. J. Mol. Sci., 17,
23.
Ishov, A. M., Sotnikov, A. G., Negorev, D., Vladimirova, O. V.,
doi: 10.3390/ijms17010024.
Neff, N., Kamitani, T., Yeh, E. T., Strauss, J. F., 3rd, and
10.
Darling, A. L., Liu, Y., Oldfield, C. J., and Uversky, V. N.
Maul, G. G. (1999) PML is critical for ND10 formation
(2018) Intrinsically disordered proteome of human mem#
and recruits the PML#interacting protein daxx to this
brane#less organelles, Proteomics, 18, e1700193, doi:
nuclear structure when modified by SUMO#1, J. Cell.
10.1002/pmic.201700193.
Biol., 147, 221#234, doi: 10.1083/jcb.147.2.221.
11.
Uversky, V. N. (2017) Intrinsically disordered proteins in
24.
Lallemand#Breitenbach, V., and de The, H. (2010) PML
overcrowded milieu: membrane#less organelles, phase sep#
nuclear bodies, Cold Spring Harb. Perspect. Biol., 2,
aration, and intrinsic disorder, Curr. Opin. Struct. Biol., 44,
a000661.
18#30, doi: 10.1016/j.sbi.2016.10.015.
25.
Yamazaki, T., Nakagawa, S., and Hirose, T.
(2020)
12.
Turner, A. L., Watson, M., Wilkins, O. G., Cato, L.,
Architectural RNAs for membraneless nuclear body for#
Travers, A., Thomas, J. O., and Stott, K. (2018) Highly dis#
mation, Cold Spring Harb. Symp. Quant. Biol., doi:
ordered histone H1#DNA model complexes and their con#
10.1101/sqb.2019.84.039404.
densates, Proc. Natl. Acad. Sci. USA, 115, 11964#11969,
26.
Fox, A. H., and Lamond, A. I. (2010) Paraspeckles, Cold
doi: 10.1073/pnas.1805943115.
Spring Harb. Perspect. Biol., 2, a000687, doi: 10.1101/csh#
13.
Larson, A. G., Elnatan, D., Keenen, M. M., Trnka, M. J.,
perspect.a000687.
Johnston, J. B., Burlingame, A. L., Agard, D. A., Redding,
27.
Fox, A. H., Nakagawa, S., Hirose, T., and Bond, C. S.
S., and Narlikar, G. J. (2017) Liquid droplet formation by
(2018) Paraspeckles: where long noncoding RNA meets
HP1alpha suggests a role for phase separation in hete#
phase separation, Trends Biochem. Sci., 43, 124#135, doi:
rochromatin, Nature,
547,
236#240, doi:
10.1038/
10.1016/j.tibs.2017.12.001.
nature22822.
28.
Shin, Y., Berry, J., Pannucci, N., Haataja, M. P., Toettcher, J. E.,
14.
Tatavosian, R., Kent, S., Brown, K., Yao, T., Duc, H. N.,
and Brangwynne, C. P. (2017) Spatiotemporal control of
Huynh, T. N., Zhen, C. Y., Ma, B., Wang, H., and Ren, X.
intracellular phase transitions using light#activated opto#
(2019) Nuclear condensates of the polycomb protein chro#
droplets, Cell, 168, 159#171, doi: 10.1016/j.cell.2016.11.054.
mobox 2 (CBX2) assemble through phase separation, J.
29.
Zhou, J., Fan, J. Y., Rangasamy, D., and Tremethick, D. J.
Biol. Chem., 294, 1451#1463, doi: 10.1074/jbc.RA118.
(2007) The nucleosome surface regulates chromatin com#
006620.
paction and couples it with transcriptional repression, Nat.
15.
Boehning, M., Dugast#Darzacq, C., Rankovic, M.,
Struct. Mol. Biol., 14, 1070#1076.
Hansen, A. S., Yu, T., Marie#Nelly, H., McSwiggen, D. T.,
30.
Kalashnikova, A. A., Porter#Goff, M. E., Muthurajan, U. M.,
Kokic, G., Dailey, G. M., Cramer, P., Darzacq, X., and
Luger, K., and Hansen, J. C. (2013) The role of the nucle#
Zweckstetter, M. (2018) RNA polymerase II clustering
osome acidic patch in modulating higher order chromatin
БИОХИМИЯ том 85 вып. 6 2020
РАЗДЕЛЕНИЕ ЖИДКИХ ФАЗ И КОМПАРТМЕНТАЛИЗАЦИЯ ЯДРА
761
structure, J. Royal Soc. Interface/Royal Soc., 10, 20121022,
(2020) The interchromatin compartment participates in
doi: 10.1098/rsif. 2012.1022.
the structural and functional organization of the cell nucle#
31.
Sinha, D., and Shogren#Knaak, M. A. (2010) Role of
us, BioEssays, 42, e1900132, doi: 10.1002/bies.201900132.
direct interactions between the histone H4 tail and the
47.
Cremer, T., Cremer, M., and Cremer, C. (2018) The 4D
H2A core in long range nucleosome contacts, J. Biol.
nucleome: genome compartmentalization in an evolution#
Chem., 285, 16572#16581, doi: 10.1074/jbc.M109.091298.
ary context, Biochemistry (Moscow), 83, 313#325, doi:
32.
Pepenella, S., Murphy, K. J., and Hayes, J. J. (2014) Intra#
10.1134/S000629791804003X.
and inter#nucleosome interactions of the core histone
48.
Garcia#Jove Navarro, M., Kashida, S., Chouaib, R.,
tail domains in higher#order chromatin structure,
Souquere, S., Pierron, G., Weil, D., and Gueroui, Z.
Chromosoma, 123, 3#13, doi: 10.1007/s00412#013#0435#8.
(2019) RNA is a critical element for the sizing and the
33.
Luger, K., Mader, A. W., Richmond, R. K., Sargent, D. F.,
composition of phase#separated RNA#protein conden#
and Richmond, T. J. (1997) Crystal structure of the nucle#
sates, Nat. Commun., 10, 3230, doi: 10.1038/s41467#019#
osome core particle at 2.8 A resolution, Nature, 389, 251#
11241#6.
260, doi: 10.1038/38444.
49.
Fay, M. M., and Anderson, P. J. (2018) The role of RNA in
34.
Schalch, T., Duda, S., Sargent, D. F., and Richmond, T. J.
biological phase separations, J. Mol. Biol., 430, 4685#4701,
(2005) X#ray structure of a tetranucleosome and its impli#
doi: 10.1016/j.jmb.2018.05.003.
cations for the chromatin fibre, Nature, 436, 138#141, doi:
50.
Fedoriw, A. M., Starmer, J., Yee, D., and Magnuson, T.
10.1038/nature03686.
(2012) Nucleolar association and transcriptional inhibition
35.
Chodaparambil, J. V., Barbera, A. J., Lu, X., Kaye, K. M.,
through 5S rDNA in mammals, PLoS Genet., 8, e1002468,
Hansen, J. C., and Luger, K. (2007) A charged and con#
doi: 10.1371/journal.pgen.1002468.
toured surface on the nucleosome regulates chromatin
51.
Bersaglieri, C., and Santoro, R. (2019) Genome organiza#
compaction, Nat. Struct. Mol. Biol., 14, 1105#1107, doi:
tion in and around the nucleolus, Cells,
8, doi:
10.1038/nsmb1334.
10.3390/cells8060579.
36.
Chen, Q., Yang, R., Korolev, N., Liu, C. F., and
52.
Chen, Y., Zhang, Y., Wang, Y., Zhang, L., Brinkman, E. K.,
Nordenskiold, L. (2017) Regulation of nucleosome stack#
Adam, S. A., Goldman, R., van Steensel, B., Ma, J., and
ing and chromatin compaction by the histone H4 N#termi#
Belmont, A. S. (2018) Mapping 3D genome organization
nal tail#H2A acidic patch interaction, J. Mol. Biol., 429,
relative to nuclear compartments using TSA#Seq as a cyto#
2075#2092, doi: 10.1016/j.jmb.2017.03.016.
logical ruler, J. Cell. Biol., 217, 4025#4048, doi: 10.1083/
37.
Gibson, B. A., Doolittle, L. K., Schneider, M. W. G.,
jcb.201807108.
Jensen, L. E., Gamarra, N., Henry, L., Gerlich, D. W.,
53.
Quinodoz, S. A., Ollikainen, N., Tabak, B., Palla, A.,
Redding, S., and Rosen, M. K. (2019) Organization of
Schmidt, J. M., Detmar, E., Lai, M. M., Shishkin, A. A.,
chromatin by intrinsic and regulated phase separation,
Bhat, P., Takei, Y., Trinh, V., Aznauryan, E., Russell, P.,
Cell, 179, 470#484, doi: 10.1016/j.cell.2019.08.037.
Cheng, C., Jovanovic, M., Chow, A., Cai, L., McDonel, P.,
38.
Shakya, A., Park, S., Rana, N., and King, J. T. (2020)
Garber, M., and Guttman, M. (2018) Higher#order inter#
Liquid-liquid phase separation of histone proteins in cells:
chromosomal hubs shape 3D genome organization in the
role in chromatin organization, Biophys. J., 118, 753#764,
nucleus, Cell, 174, 744#757, doi: 10.1016/j.cell.2018.
doi: 10.1016/j.bpj.2019.12.022.
05.024.
39.
Strom, A. R., Emelyanov, A. V., Mir, M., Fyodorov, D. V.,
54.
Kim, J., Venkata, N. C., Hernandez Gonzalez, G. A.,
Darzacq, X., and Karpen, G. H. (2017) Phase separation
Khanna, N., and Belmont, A. S. (2020) Gene expression
drives heterochromatin domain formation, Nature, 547,
amplification by nuclear speckle association, J. Cell. Biol.,
241#245, doi: 10.1038/nature22989.
219, e201904046, doi: 10.1083/jcb.201904046.
40.
Strom, A. R., and Brangwynne, C. P. (2019) The liquid
55.
Dundr, M. (2012) Nuclear bodies: multifunctional com#
nucleome - phase transitions in the nucleus at a glance,
panions of the genome, Curr. Opin. Cell. Biol., 24, 415#422,
J. Cell. Sci., 132, jcs235093, doi: 10.1242/jcs.235093.
doi: 10.1016/j.ceb.2012.03.010.
41.
Plys, A. J., Davis, C. P., Kim, J., Rizki, G., Keenen, M. M.,
56.
Sawyer, I. A., Sturgill, D., and Dundr, M.
(2019)
Marr, S. K., and Kingston, R. E. (2019) Phase separation
Membraneless nuclear organelles and the search for phas#
of polycomb#repressive complex 1 is governed by a charged
es within phases, Wiley Interdiscip. Rev. RNA, 10, e1514,
disordered region of CBX2, Genes Dev., 33, 799#813, doi:
doi: 10.1002/wrna.1514.
10.1101/gad. 326488.119.
57.
Wang, Q., Sawyer, I. A., Sung, M. H., Sturgill, D.,
42.
Peng, A., and Weber, S. C. (2019) Evidence for and against
Shevtsov, S. P., Pegoraro, G., Hakim, O., Baek, S.,
liquid-liquid phase separation in the nucleus, Noncoding
Hager, G. L., and Dundr, M. (2016) Cajal bodies are linked
RNA, 5, doi: 10.3390/ncrna5040050.
to genome conformation, Nat. Commun., 7, 10966, doi:
43.
Boija, A., Klein, I. A., Sabari, B. R., Dall’Agnese, A.,
10.1038/ncomms10966.
Coffey, E. L., Zamudio, A. V., Li, C. H., Shrinivas, K.,
58.
Carter, D. R., Eskiw, C., and Cook, P. R.
(2008)
Manteiga, J. C., Hannett, N. M., Abraham, B. J., Afeyan, L. K.,
Transcription factories, Biochem. Soc. Trans., 36, 585#589,
Guo, Y. E., Rimel, J. K., Fant, C. B., Schuijers, J., Lee, T. I.,
doi: 10.1042/BST0360585.
Taatjes, D. J., and Young, R. A. (2018) Transcription fac#
59.
Hozak, P., Hassan, A. B., Jackson, D. A., and Cook, P. R.
tors activate genes through the phase#separation capacity
(1993) Visualization of replication factories attached to
of their activation domains, Cell, 175, 1842#1855, doi:
nucleoskeleton, Cell, 73, 361#373.
10.1016/j.cell.2018.10.042.
60.
Iborra, F. J., Pombo, A., Jackson, D. A., and Cook, P. R.
44.
Tarczewska, A., and Greb#Markiewicz, B. (2019) The sig#
(1996) Active RNA polymerases are localized within dis#
nificance of the intrinsically disordered regions for the
crete transcription “factories” in human nuclei, J. Cell.
functions of the bHLH transcription factors, Intern. J. Mol.
Sci., 109, 1427#1436.
Sci., 20, doi: 10.3390/ijms20215306.
61.
Jackson, D. A., Hassan, A. B., Errington, R. J., and Cook,
45.
Cremer, T., and Cremer, M. (2010) Chromosome territo#
P. R. (1993) Visualization of focal sites of transcription
ries, Cold Spring Harb. Perspect. Biol., 2, a003889, doi:
within human nuclei, EMBO J., 12, 1059#1065.
10.1101/cshperspect.a003889.
62.
Sutherland, H., and Bickmore, W. A. (2009) Transcription
46.
Cremer, T., Cremer, M., Hubner, B., Silahtaroglu, A.,
factories: gene expression in unions? Nat. Rev. Genet., 10,
Hendzel, M., Lanctot, C., Strickfaden, H., and Cremer, C.
457#466.
БИОХИМИЯ том 85 вып. 6 2020
762
РАЗИН, ГАВРИЛОВ
63.
Cook, P. R., and Marenduzzo, D. (2018) Transcription#
transcription complex assembly? BioEssays, 41, e1800164,
driven genome organization: a model for chromosome
doi: 10.1002/bies.201800164.
structure and the regulation of gene expression tested
72. Arnold, P. R., Wells, A. D., and Li, X. C. (2019) Diversity
through simulations, Nucl. Acids Res., 46, 9895#9906, doi:
and emerging roles of enhancer RNA in regulation of gene
10.1093/nar/gky763.
expression and cell fate, Front. Cell Develop. Biol., 7, 377,
64.
Osborne, C. S., Chakalova, L., Brown, K. E., Carter, D.,
doi: 10.3389/fcell.2019.00377.
Horton, A., Debrand, E., Goyenechea, B., Mitchell, J. A.,
73. Nair, S. J., Yang, L., Meluzzi, D., Oh, S., Yang, F.,
Lopes, S., Reik, W., and Fraser, P. (2004) Active genes
Friedman, M. J., Wang, S., Suter, T., Alshareedah, I.,
dynamically colocalize to shared sites of ongoing transcrip#
Gamliel, A., Ma, Q., Zhang, J., Hu, Y., Tan, Y., Ohgi, K. A.,
tion, Nat. Genet., 36, 1065#1071.
Jayani, R. S., Banerjee, P. R., Aggarwal, A. K., and
65.
Osborne, C. S., Chakalova, L., Mitchell, J. A., Horton, A.,
Rosenfeld, M. G. (2019) Phase separation of ligand#acti#
Wood, A. L., Bolland, D. J., Corcoran, A. E., and Fraser, P.
vated enhancers licenses cooperative chromosomal
(2007) Myc dynamically and preferentially relocates to a
enhancer assembly, Nat. Struct. Mol. Biol., 26, 193#203,
transcription factory occupied by Igh, PLoS Biol., 5, e192.
doi: 10.1038/s41594#019#0190#5.
66.
Ulianov, S. V., Doronin, S. A., Khrameeva, E. E., Kos, P. I.,
74. Hyman, A. A., Weber, C. A., and Julicher, F. (2014)
Luzhin, A. V., Starikov, S. S., Galitsyna, A. A., Nenasheva, V. V.,
Liquid-liquid phase separation in biology, Ann. Rev. Cell
Ilyin, A. A., Flyamer, I. M., Mikhaleva, E. A., Logacheva, M. D.,
Develop. Biol., 30, 39#58, doi: 10.1146/annurev#cellbio#
Gelfand, M. S., Chertovich, A. V., Gavrilov, A. A., Razin, S. V.,
100913#013325.
and Shevelyov, Y. Y. (2019) Nuclear lamina integrity is
75. Cramer, P. (2019) Organization and regulation of gene
required for proper spatial organization of chromatin in
transcription, Nature, 573, 45#54, doi: 10.1038/s41586#
Drosophila, Nat. Commun., 10, 1176, doi: 10.1038/s41467#
019#1517#4.
019#09185#y.
76. Guo, Y. E., Manteiga, J. C., Henninger, J. E., Sabari, B. R.,
67.
Arnold, C. D., Gerlach, D., Stelzer, C., Boryn, L. M.,
Dall’Agnese, A., Hannett, N. M., Spille, J. H., Afeyan, L. K.,
Rath, M., and Stark, A. (2013) Genome#wide quantitative
Zamudio, A. V., Shrinivas, K., Abraham, B. J., Boija, A.,
enhancer activity maps identified by STARR#seq, Science,
Decker, T. M., Rimel, J. K., Fant, C. B., Lee, T. I.,
339, 1074#1077, doi: 10.1126/science.1232542.
Cisse, I. I., Sharp, P. A., Taatjes, D. J., and Young, R. A.
68.
Consortium, E. P., Bernstein, B. E., Birney, E., Dunham, I.,
(2019) Pol II phosphorylation regulates a switch between
Green, E. D., Gunter, C., and Snyder, M. (2012) An inte#
transcriptional and splicing condensates, Nature, 572, 543#
grated encyclopedia of DNA elements in the human
548, doi: 10.1038/s41586#019#1464#0.
genome, Nature, 489, 57#74, doi: 10.1038/nature11247.
77. Erdel, F., Rademacher, A., Vlijm, R., Tunnermann, J.,
69.
Furlong, E. E. M., and Levine, M. (2018) Developmental
Frank, L., Weinmann, R., Schweigert, E., Yserentant, K.,
enhancers and chromosome topology, Science, 361, 1341#
Hummert, J., Bauer, C., Schumacher, S., Al Alwash, A.,
1345, doi: 10.1126/science.aau0320.
Normand, C., Herten, D. P., Engelhardt, J., and Rippe, K.
70.
Hnisz, D., Shrinivas, K., Young, R. A., Chakraborty, A. K.,
(2020) Mouse heterochromatin adopts digital compaction
and Sharp, P. A. (2017) A phase separation model for tran#
states without showing hallmarks of HP1#driven liquid-liquid
scriptional control, Cell, 169, 13#23, doi: 10.1016/j.cell.
phase separation, Mol. Cell, doi: 10.1016/j.molcel.2020.02.005.
2017.02.007.
78. Mir, M., Bickmore, W., Furlong, E. E. M., and Narlikar, G.
71.
Gurumurthy, A., Shen, Y., Gunn, E. M., and Bungert, J.
(2019) Chromatin topology, condensates and gene regula#
(2019) Phase separation and transcription regulation: are
tion: shifting paradigms or just a phase? Development, 146,
super#enhancers and locus control regions primary sites of
doi: 10.1242/dev.182766.
THE ROLE OF LIQUID-LIQUID PHASE SEPARATION
IN THE COMPARTMENTALIZATION OF CELL NUCLEUS
AND SPATIAL GENOME ORGANIZATION
Review
S. V. Razin1,2* and A. A. Gavrilov1
1 Institute of Gene Biology, Russian Academy of Sciences, 119334 Moscow, Russia; E&mail: sergey.v.razin@usa.net
2 Lomonosov Moscow State University, Faculty of Biology, 119991 Moscow, Russia
Received March 24, 2020
Revised April 7, 2020
Accepted April 9, 2020
Functional compartmentalization of the cell nucleus plays an important role in the regulation of genome activity by
providing accumulation of enzymes and auxiliary factors in the reaction centers, such as transcription factories,
Cajal bodies, speckles, etc. The mechanisms behind the nucleus functional compartmentalization are still poorly
understood. There are reasons to believe that the key role in the nucleus compartmentalization belongs to the process
of liquid-liquid phase separation. In this brief review, we analyze results of experimental studies demonstrating that
liquid-liquid phase separation not only governs functional compartmentalization of the cell nucleus but also con#
tributes to the formation of the 3D genomic architecture.
Keywords: liquid-liquid phase separation, chromatin, cell nucleus, transcription, nuclear compartment, spatial
genome organization
БИОХИМИЯ том 85 вып. 6 2020