БИОХИМИЯ, 2021, том 86, вып. 11, с. 1620 - 1634
УДК 577.17.05
ПРОТЕОЛИЗ IGFBP 4 ПОД ДЕЙСТВИЕМ PAPP A
В ПЕРВИЧНОЙ КУЛЬТУРЕ НЕОНАТАЛЬНЫХ
КАРДИОМИОЦИТОВ КРЫСЫ В НОРМЕ И ПРИ ГИПЕРТРОФИИ
© 2021
Д.В. Серебряная1*, Д.А. Адашева1, А.А. Конев2, М.М. Артемьева3,
И.А. Катруха1,2, А.Б. Постников1,2, Н.А. Медведева3, А.Г. Катруха1,2
1 Московский государственный университет имени М.В. Ломоносова, биологический факультет,
кафедра биохимии, 119234 Москва, Россия; электронная почта: dariaserebryanaya@gmail.com
2 HyTest Ltd, 20520 Турку, Финляндия
3 Московский государственный университет имени М.В. Ломоносова, биологический факультет,
кафедра физиологии человека и животных, 119234 Москва, Россия
Поступила в редакцию 06.08.2021
После доработки 03.09.2021
Принята к публикации 03.09.2021
Сердечно сосудистые заболевания (ССЗ) являются одной из главных причин смертности и инвалидизации
населения в мире. Белок А плазмы крови, ассоциированный с беременностью (PAPP A), представляет со
бой матриксную металлопротеиназу, локализованную на поверхности клеток. Одним из субстратов РАРР А
является IGFBP 4 (insulin like growth factor binding protein 4) - представитель семейства белков, связываю
щих IGF (insulin like growth factor). Протеолиз IGFBP 4 под действием РАРР А происходит по специфичес
кому участку с образованием двух протеолитических фрагментов - N концевого (NT IGFBP 4) и С конце
вого (CT IGFBP 4) - и приводит к высвобождению IGF, который активирует такие клеточные процессы,
как миграция, пролиферация и клеточный рост. Повышенный уровень протеолитических фрагментов
IGFBP 4 коррелирует с развитием осложнений и риском летального исхода у больных такими ССЗ, как
ишемическая болезнь сердца, острый коронарный синдром и сердечная недостаточность. Однако в литера
туре нет данных, демонстрирующих PAPP A зависимый протеолиз IGFBP 4 в сердечной ткани в норме и
при патологических состояниях. В настоящей работе на модели первичной культуры неонатальных карди
омиоцитов крысы нами было показано: 1) процесс протеолиза IGFBP 4 под действием PAPP A происходит
в кондиционированной среде кардиомиоцитов, 2) переход кардиомиоцитов в гипертрофированное состоя
ние сопровождается увеличением уровня PAPP A специфичного протеолиза IGFBP 4. Таким образом,
можно предположить, что усиление расщепления IGFBP 4 и гипертрофические изменения кардиомиоци
тов, сопровождающие некоторые ССЗ, взаимосвязаны, и PAPP A является одним из активаторов IGF за
висимых процессов в кардиомиоцитах в норме и особенно при гипертрофии.
КЛЮЧЕВЫЕ СЛОВА: сердечно сосудистые заболевания, сердечная недостаточность, кардиомиоциты,
первичная культура, протеолиз, PAPP A, IGFBP 4, гипертрофия, кардиомаркёр, эндотелин 1.
DOI: 10.31857/S0320972521110026
ВВЕДЕНИЕ
ганизма. При хронической форме СН снижает
ся способность сердечной мышцы к сокраще
На сегодняшний день сердечно сосудистые
нию и развивается патологическая гипертро
заболевания (ССЗ) являются главной причиной
фия - аномальное утолщение стенки миокарда,
летальных исходов и инвалидности во всем ми
возникающее вследствие увеличения кардиомио
ре [1]. Сердечная недостаточность (СН) - одно
цитов в размере и изменений во внеклеточном
из самых распространённых ССЗ, характеризу
матриксе сердечной ткани [2]. Гипертрофия так
ющееся изменениями в работе сердца, приводя
же сопровождает и другие ССЗ, такие как ише
щими к нарушению кровоснабжения всего ор
мическая болезнь сердца (ИБС), гипертония, а
Принятые сокращения: ИБС - ишемическая болезнь сердца; ОКС - острый коронарный синдром; ССЗ - сердеч
но сосудистые заболевания; СН - сердечная недостаточность; ФИА - флуороиммунный анализ; ЭТС - эмбриональная
телячья сыворотка; BNP - натрийуретический пептид типа B; CT IGFBP 4 - С концевой протеолитический фрагмент
IGFBP 4; DAPI - 4′,6 диамидино 2 фенилиндол; dPAPP A - димерная форма PAPP A; IGF - инсулиноподобный фак
тор роста; IGFBP 2-IGFBP 5 - белки, связывающие инсулиноподобный фактор роста; NT IGFBP 4 - N концевой про
теолитический фрагмент IGFBP 4; PAPP A - ассоциированный с беременностью белок плазмы А; proMBP - предшест
венник основного щелочного белка эозинофилов.
* Адресат для корреспонденции.
1620
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1621
также практически все известные на сегодняш
IGFBP 4 в крови до начала развития осложне
ний день типы врождённых и приобретенных
ний при различных ССЗ, в литературе нет пря
пороков сердца [3].
мых доказательств протекания dPAPP A специ
Белок А плазмы, ассоциированный с бере
фичного протеолиза IGFBP 4 в миокарде в нор
менностью (pregnancy associated plasma protein A,
ме или при патологических состояниях. Поэто
PAPP A), - матриксная металлопротеиназа, со
му данное исследование было проведено с
держащая в активном центре ионы цинка и ло
целью установить взаимосвязь между dPAPP A
кализованная на поверхности клеток [4, 5].
специфичным протеолизом IGFBP 4 и гипер
Большая часть РАРР A (~90%) в крови циркули
трофическими изменениями кардиомиоцитов,
рует в форме гетеротетрамера (htPAPP A), в сос
которые, как было упомянуто ранее, сопровож
тав которого входят димер РАРР А (dPAPP A) и
дают многие ССЗ. Для исследования протеоли
две субъединицы белка proMBP - предшествен
за IGFBP 4 в настоящей работе нами была раз
ника основного щелочного белка эозинофилов.
работана и охарактеризована клеточная модель
Тетрамерная форма PAPP A является протеоли
гипертрофии, основанная на первичной культу
тически неактивной [6]. Остальная часть PAPP A,
ре кардиомиоцитов крысы.
циркулирующего в крови, представлена его ди
мерной формой, которая обладает протеолити
ческой активностью [7]. Субстратами dРАРР А
МАТЕРИАЛЫ И МЕТОДЫ
в физиологических условиях являются белки,
связывающие инсулиноподобный фактор роста:
Все использованные биохимические реакти
IGFBP 2 [8], IGFBP 4 [9] и IGFBP 5 [10]. Дан
вы имели аналитическую чистоту и были приоб
ные белки связываются с инсулиноподобным
ретены в компаниях «Sigma Aldrich» (США),
фактором роста (IGF), ингибируя его актив
«Thermo Fisher Scientific» (США),
«ICN»
ность. В результате протеолиза комплекса
(США),
«AppliChem» (Германия),
«Merck»
IGFBP белков с IGF под действием dPAPP A
(США), «Диа М» (Россия) и «Bio Rad» (США).
IGF высвобождается из комплекса и активирует
Реактивы, использованные для проведения
такие процессы, как клеточный рост, пролифе
культурально биологических работ, были при
рация, миграция и ангиогенез [11]. В случае
обретены в компаниях
«HyClone» (США),
IGFBP 4 PAPP A является единственной проте
«Sigma Aldrich» и «Costar» (Нидерланды). Вто
азой, расщепляющей данный белок в физиоло
ричные антитела, специфичные к константной
гических условиях. Протеолиз IGFBP 4 под
части иммуноглобулинов G (Fc фрагментам)
действием dРАРР А происходит по специфи
антитела мыши, конъюгированные с флуорофо
ческому участку, расположенному между ами
ром Alexa 594, а также фаллоидин, конъюгиро
нокислотными остатками Met135 и Lys136, и в
ванный с флуорофором Alexa 488, и краситель
результате расщепления образуются два протео
DAPI (4′,6 диамидино 2 фенилиндол), были
литических фрагмента белка: N концевой (NT
приобретены в компании
«Thermo Fisher
IGFBP 4) и С концевой (CT IGFBP 4) [12].
Scientific». Моноклональные антитела, специ
Ранее было показано, что уровень экспрес
фичные к сердечной изоформе тропонина I
сии dPAPP A возрастает в атеросклеротической
(19С7, MF4), IGFBP 4 и его фрагментам (IBP3,
бляшке, а также, что dPAPP A является маркё
IBP180, IBP182, IBP163), рекомбинантные
ром риска развития острого коронарного синд
IGFBP 4, dPAPP A, NT IGFBP 4 и CT IGFBP 4,
рома (ОКС) [13]. В ряде исследований было по
а также эндогенный натрийуретический пептид
казано, что повышенный уровень протеолити
B типа (BNP) человека были любезно предос
ческих фрагментов IGFBP 4 (NT IGFBP 4 и
тавлены компанией «HyTest» (Финляндия).
CT IGFBP 4) ассоциирован с увеличением рис
Получение первичной культуры кардиомиоци
ка возникновения ОКС у пациентов с ИБС и
тов крысы. Получение первичной культуры кар
наступлением смерти от ССЗ у больных диабе
диомиоцитов крысы проводили в соответствии с
том 1 го типа [14, 15]. Недавно было обнаруже
методикой Степановой и соавт. [17] с некоторы
но, что повышенный уровень протеолитических
ми модификациями. Сердца двух/трёхдневных
фрагментов IGFBP 4 в крови у больных сердеч
крыс популяции Wistar очищали от соединитель
ной недостаточностью - состоянием, которое
ной ткани, крови и сосудов, помещали в охлаж
может развиваться вследствие ОКС и инфаркта
дённый раствор Кребса-Рингера (25 мМ NaCl,
миокарда, также ассоциирован с повышенным
2,5 мМ KCl, 1,25 мМ NaH2PO4, 2 мМ CaCl2,
риском летального исхода [16].
1 мМ MgCl2, 25 мМ NaHCO3, 25 мМ глюкоза,
Несмотря на значительное количество ис
pH 7,4) и измельчали, после чего обрабатывали
следований, демонстрирующих увеличение
коллагеназой («Gibco», США) в концентрации
концентрации dPAPP A и уровня протеолиза
5 мг/мл, приготовленной на растворе Кребса-
БИОХИМИЯ том 86 вып. 11 2021
1622
СЕРЕБРЯНАЯ и др.
Рингера, содержащем 50 мкМ CaCl2, в течение
телем разведениях и инкубировали в течение
10 мин при 37 °С. После инкубации ткань до
ночи при 4 °С. После промывки клетки инкуби
полнительно разрушали, пипетируя смесь
ровали в присутствии вторичных антител, спе
30-40 раз, и после оседания крупных фрагмен
цифичных к Fc фрагментам антител мыши и
тов ткани отбирали суспендированные клетки.
конъюгированных с флуоресцентной меткой
Данную процедуру повторяли 4-5 раз до полно
Alexa 594, в течение часа при комнатной темпе
го разрушения ткани и высвобождения клеток.
ратуре. Инкубации с фаллоидином, конъюгиро
Полученные суспензии клеток центрифугиро
ванным с флуорофором Alexa 488 и ядерным
вали 10 мин при 200 g, осадки клеток ресуспен
красителем DAPI, в указанных производителем
дировали в среде для культивирования
разведениях также проводили в течение часа
DMEM (модифицированная по способу Дуль
при комнатной температуре. После инкубации
бекко среда Игла), содержащей 10% эмбрио
клетки трижды промывали ФСБ. Полученные
нальной телячьей сыворотки (ЭТС, «HyClone»).
препараты визуализировали с использованием
Все фракции, кроме первой и второй, объединя
флуоресцентного инвертированного микроско
ли и повторно центрифугировали при тех же ус
па («EVOS FL Color», США).
ловиях для дополнительной очистки от коллаге
Протеолитическое расщепление IGFBP 4 под
назы. Осадок клеток ресуспендировали в куль
действием PAPP A в культурах клеток. Протеолиз
туральной среде и инкубировали в полистироль
IGFBP 4 в кондиционированной среде кардио
ном планшете в течение 20 мин при 37 °С в ат
миоцитов и примесных клеток проводили по
мосфере 5% CO2 для отделения фракции при
методике Laursen et al. [18] с некоторыми моди
месных клеток. Суспензию неприкрепившихся
фикациями. Для проведения протеолиза
клеток переносили в новый полистирольный
IGFBP 4 использовали 10 кратную субстратную
планшет и культивировали в течение 7 дней при
смесь, приготовленную на Tris солевом буфе
37 °С в атмосфере 5% CO2.
ре (20 мМ Tris HCl, 150 мМ NaCl, pH 7,4) и со
Определение площади кардиомиоцитов. Из
держащую 3 мкг/мл рекомбинантного IGFBP 4
мерение площади кардиомиоцитов проводили с
человека, 0,85 мкг/мл рекомбинантного IGF II
использованием программного обеспечения
человека («Sigma Aldrich») и 2 мМ CaCl2. После
ImageJ (Fiji). Указывали значение масштабной
приготовления субстратную смесь инкубирова
шкалы в пикселях и в мкм, после чего с исполь
ли 30 мин при комнатной температуре для фор
зованием программы рассчитывали значения
мирования комплекса IGFBP 4 с IGF II, после
площади отдельных клеток в мкм2. Для каждого
чего добавляли в кондиционированную среду к
снимка рассчитывали площадь 15 клеток с ис
кардиомиоцитам в лунки 24 луночного планше
пользованием последовательности команд
та (по 40 мкл в лунку) и инкубировали в термо
Analyse Measure, затем полученные значения
стате при 37 °С в атмосфере 5% CO2 в течение
использовали для расчёта среднего значения
30 мин, 3 или 24 ч. По окончании инкубации от
площади клетки.
бирали кондиционированную среду из лунок и
Определение частоты сокращений кардиомио
останавливали реакцию добавлением ЭДТА до
цитов. Частоту сокращений кардиомиоцитов
конечной концентрации 5 мМ. В полученных
определяли, фиксируя сокращение во времени в
образцах кондиционированной среды проводи
10 точках культуры, чтобы убедиться в равно
ли измерение концентраций NT IGFBP 4, CT
мерности и регулярности сокращений, после
IGFBP 4 и BNP методом флуороиммунного
чего проводили пересчёт на количество ударов в
анализа «сэндвич» типа, как описано ниже. По
минуту.
лученные значения концентраций NT IGFBP 4,
Иммуноцитохимическое окрашивание клеток.
CT IGFBP 4 и BNP нормировали на количест
Первичную культуру кардиомиоцитов и при
во клеток в каждой лунке. Для определения ко
месных клеток промывали фосфатно солевым
личества клеток культуру кардиомиоцитов в
буфером (ФСБ) от компонентов среды, после
каждой лунке трипсинизировали с использова
чего проводили фиксацию и пермеабилизацию
нием 0,25% ного раствора трипсин ЭДТА и
мембран клеток в присутствии 4% парафор
проводили подсчёт клеток в камере Горяева с
мальдегида и 0,1% (w/v) Triton X 100 соответ
использованием раствора трипанового синего.
ственно в течение 15 мин при комнатной темпе
Детекция NT IGFBP 4, CT IGFBP 4 и BNP
ратуре. Затем клетки промывали несколько раз
методом одностадийного флуороиммунного анали
ФСБ и инкубировали в присутствии 1% ЭТС в
за «сэндвич» типа (ФИА). Концентрации NT
течение 30 мин для блокирования неспецифи
IGFBP 4 и CT IGFBP 4 в культуральных средах
ческой сорбции антител. После промывки к
определяли методом неоэпитоп специфичного
клеткам добавляли первичные антитела, специ
флуороиммунного анализа «сэндвич» типа с ис
фичные к тропонину I, в указанных производи
пользованием пар антител IBP3 IBP180Eu3+
БИОХИМИЯ том 86 вып. 11 2021
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1623
(определение концентрации NT IGFBP 4) и
ми вносили водный раствор эндотелина 1
IBP182 IBP163Eu3+ (определение концентрации
(«Sigma Aldrich»») в диапазоне концентраций
CT IGFBP 4), как описано Konev et al. [15].
20-100 нМ. В контрольные лунки добавляли во
Концентрацию BNP определяли аналогичным
ду. Инкубировали клетки с эндотелином 1 в те
методом с использованием пары антител 24С5
чение 24 и 48 ч при 37 °С в атмосфере 5% CO2. О
AbBNP2Eu3+, как описано в статье Semenov et al.
наличии гипертрофии судили по увеличению
[19]. Для проведения ФИА антитела подложки
площади поверхности кардиомиоцитов (см. раз
(20 мкг/мл, 0,1 мл/лунка в ФСБ) сорбировали
дел «Определение площади кардиомиоцитов»),
на поверхность лунок 96 луночного полисти
инкубированных с эндотелином 1 по сравнению
рольного планшета при перемешивании в тече
с контрольными кардиомиоцитами.
ние 30 мин при комнатной температуре. Затем
Статистическую обработку результатов изме
лунки промывали 10 мМ Tris HCl, 150 мМ NaCl,
рений площади кардиомиоцитов и концентра
0,025% (v/v) Tween 20 и 0,05% NaN3, pH 7,8 (бу
ций NT IGFBP 4, CT IGFBP 4 и BNP в норме
фер А). После этого в каждую лунку планшета
и при гипертрофии проводили, используя t кри
вносили 0,05 мл образца, разведённого в буфере
терий Стьюдента. Данные представлены как
для анализа (50 мМ Tris HCl, 0,9% NaCl, 0,01%
среднее значение ± квадратичное отклонение.
(v/v) Tween 40, 0,5% бычьего сывороточного аль
Различия считали достоверными при p ≤ 0,05.
бумина, 0,05% NaN3, pH 7,7) и 0,05 мл детектор
ных антител (4 мкг/мл), конъюгированных со
стабильным хелатом европия (Eu3+). Планшеты
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ
инкубировали 30 мин при комнатной темпера
туре при постоянном перемешивании. После
Получение первичной культуры кардиомиоци
промывания буфером А в лунки планшета вно
тов из неонатальных крыс и ее характеристика.
сили по 0,2 мл раствора для усиления флуорес
Через 4 дня после выделения клеточная культу
ценции и затем детектировали флуоресценцию
ра, полученная из сердец неонатальных крыс,
на планшетном анализаторе Victor X («Perkin
приобретала соответствующий кардиомиоци
Elmer», США).
там фенотип (рис. 1, а) и демонстрировала сок
Индукция гипертрофии в культурах кардиомио
ращение с частотой ~11 ударов/мин. С 4 по
цитов под действием эндотелина 1. Перед прове
7 день культивирования кардиомиоцитов часто
дением эксперимента в лунках с клетками про
та сокращения не менялась. Процентное содер
водили смену культуральной среды на DMEM,
жание кардиомиоцитов в полученной культуре
содержащую 1% ЭТС. В лунки с кардиомиоцита
определяли иммуноцитохимически, проводя
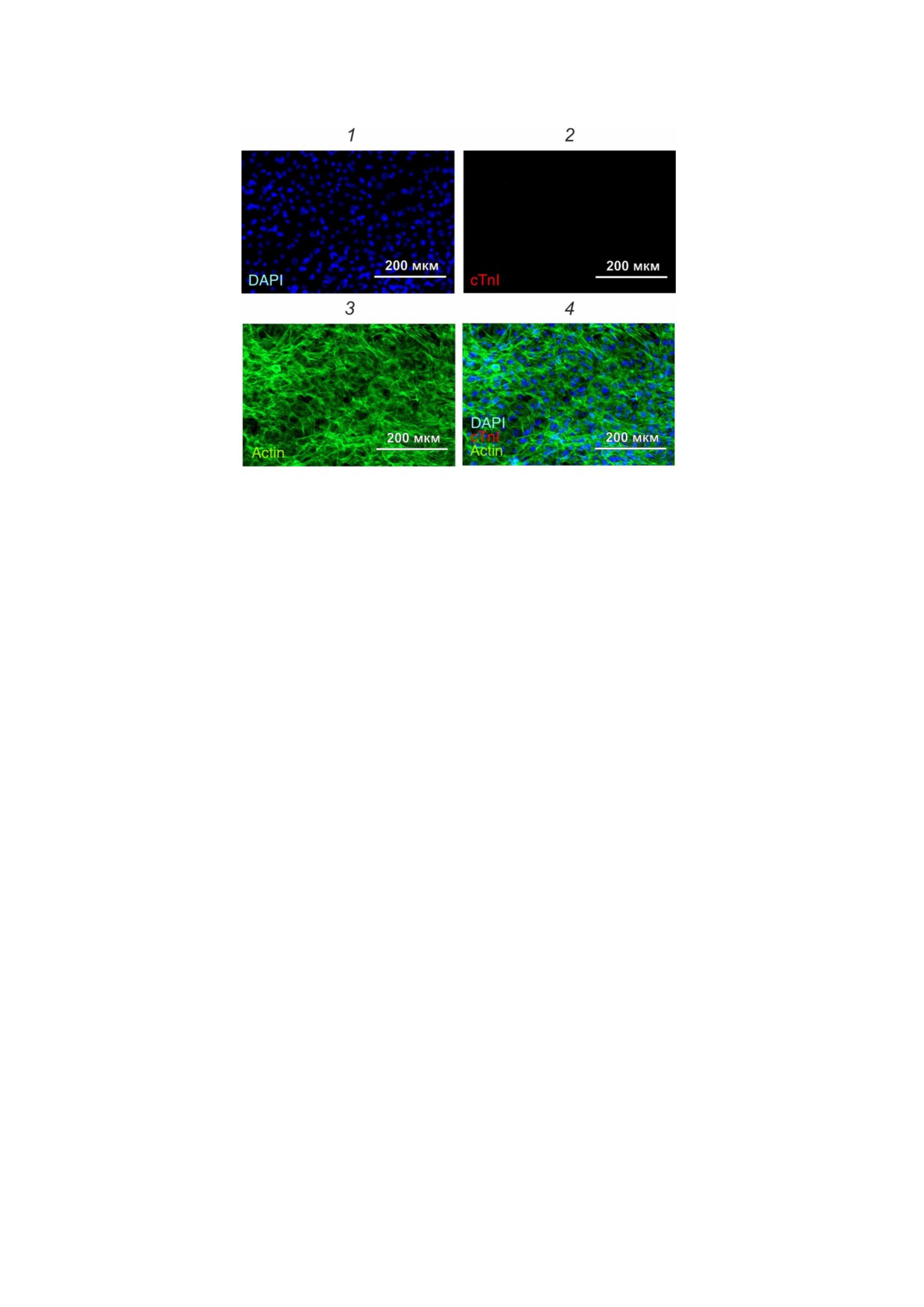
Рис. 1. Характеристика типичной первичной культуры кардиомиоцитов крысы. а - Микрофотографии кардиомиоцитов,
сделанные в режиме фазового контраста в процессе культивирования культуры в определенные промежутки времени:
1 - 1 день; 2 - 4 дня; 3 - 6 дней; 4 - 7 дней. б - Иммунофлуоресцентное окрашивание полученной культуры (7 дней) с ис
пользованием: флуоресцентного ядерного красителя DAPI (1); антител, специфичных к сердечной изоформе тропонина I
человека, конъюгированных с флуоресцентной меткой Alexa 594 (2); фаллоидина, конъюгированного с флуоресцентной
меткой Alexa 488 (3); наложение фотографий, сделанных в трёх флуоресцентных каналах при одинаковом увеличении (4)
БИОХИМИЯ том 86 вып. 11 2021
1624
СЕРЕБРЯНАЯ и др.
Рис. 2. Иммунофлуоресцентное окрашивание культуры примесных клеток с использованием: флуоресцентного ядерного
красителя DAPI (1); антител, специфичных к сердечной изоформе тропонина I человека, конъюгированных с флуоресцент
ной меткой Alexa 594 (2); фаллоидина, конъюгированного с флуоресцентной меткой Alexa 488 (3); наложение фотогра
фий, сделанных в трёх флуоресцентных каналах при одинаковом увеличении (4)
окрашивание моноклональными антителами,
клетки сосудов [23], клетки стромы эндомет
специфичными к сердечной изоформе тропо
рия [24], адипоциты сердечной ткани [25], клет
нина I (специфическому маркёру кардиомиоци
ки эндотелия коронарной артерии человека [26]
тов), и рассчитывая отношение клеток с детек
и клетки предшественники сердца челове
тированным тропонином I к общему числу кле
ка [27]. В качестве модели для исследования
ток для каждого снимка. Количество кардиоми
протеолиза IGFBP 4 в сердечной ткани в нашей
оцитов в полученных культурах составило
работе мы использовали первичную культуру
70-90% (рис. 1, б).
кардиомиоцитов крысы, содержание кардиомио
Остальные 10-30% клеток в полученных
цитов в которой составляло 70-90%. Протеоли
культурах, по всей видимости, были представле
тическое расщепление IGFBP 4 в кондициони
ны примесными клетками, содержащимися в
рованной среде кардиомиоцитов и определение
сердечной ткани. Для того чтобы в дальнейшем
концентраций NT IGFBP 4 и CT IGFBP 4
оценить суммарный вклад этих клеток в dPAPP
проводили, как описано в разделе «Материалы и
A специфическую протеолитическую деграда
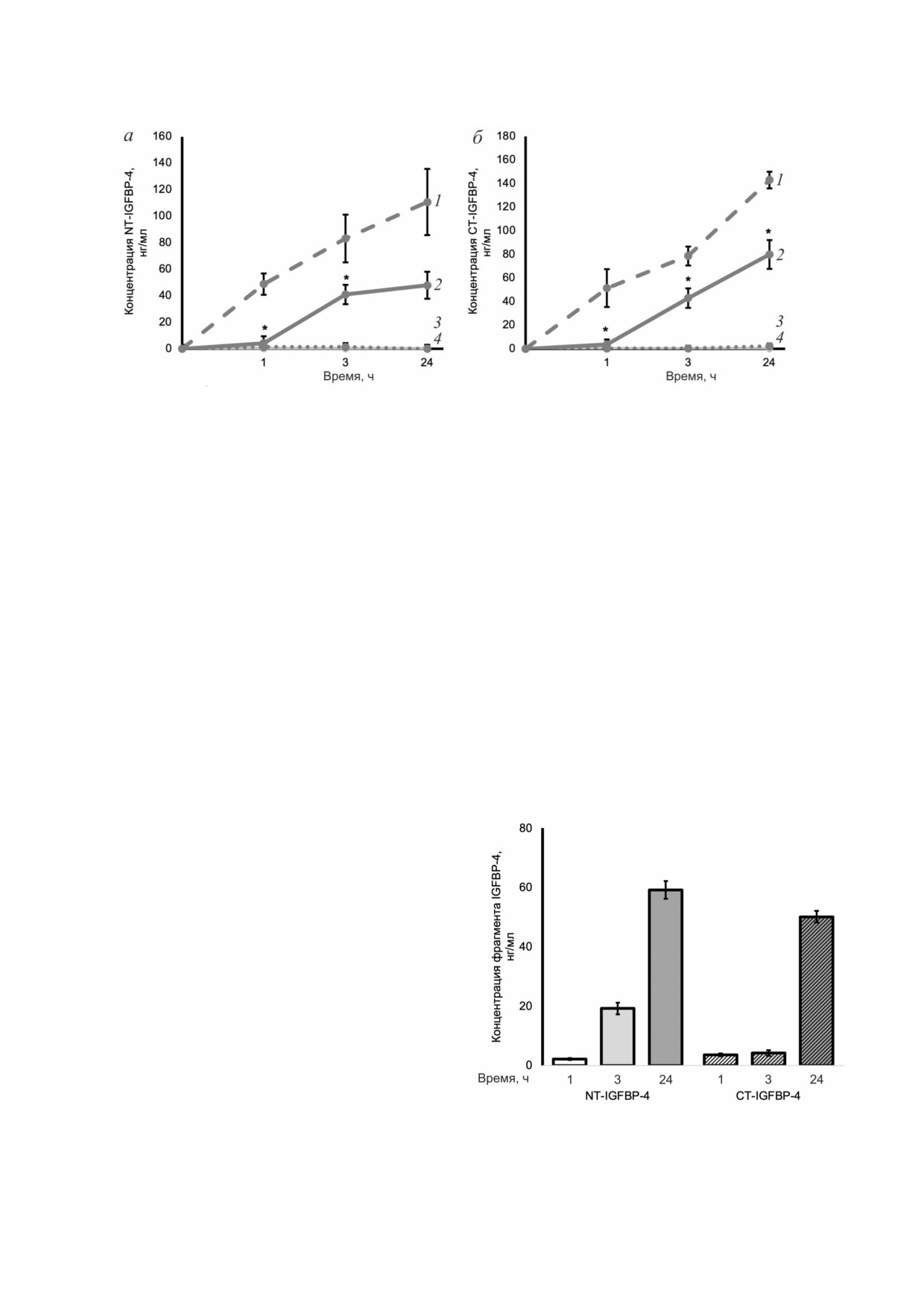
методы». Как видно на рис. 3, NT IGFBP 4
цию IGFBP 4 в сравнении с кардиомиоцитами,
(рис. 3, а) и СT IGFBP 4 (рис. 3, б) образуются
в ходе выделения мы также получили и охаракте
в ходе протеолиза IGFBP 4 в кондициониро
ризовали изолированную культуру примесных
ванной среде кардиомиоцитов.
клеток, не содержащую кардиомиоциты (рис. 2).
Концентрации фрагментов IGFBP 4 в конди
Получение культуры примесных клеток прово
ционированной среде (рис. 3, кривая 2) через 1, 3
дили, как описано в разделе «Материалы и ме
и 24 ч после начала реакции протеолиза составля
тоды». Результаты иммунофлуоресцентного ок
ли
5,3
± 4,2
нг/мл,
50,1
± 8,1
нг/мл и
рашивания культуры примесных клеток пред
98,3 ± 12,2 нг/мл (NT IGFBP 4) и 4,9 ± 4,2 нг/мл,
ставлены на рис. 2.
43,1 ± 8,3 нг/мл и 95,9 ± 15,4 нг/мл (CT IGFBP 4),
dPAPP A специфический протеолиз IGFBP 4
т.е. концентрация фрагментов IGFBP 4 в кон
в первичной культуре кардиомиоцитов крысы. Из
диционированной среде увеличивалась во вре
вестно, что dPAPP A расщепляет IGFBP 4 в
мени, в то время как в образцах стерильной
кондиционированной среде фибробластов [12]
культуральной среды образования фрагментов
и фолликулярной жидкости яичника челове
обнаружено не было (рис. 3, кривая 4). Также
ка [20], быка, свиньи и лошади [21], а также сек
NT IGFBP 4 и СT IGFBP 4 не были обнаруже
ретируется в среду такими типами клеток, как
ны в кондиционированной среде кардиомиоци
гранулезные клетки
[22], гладкомышечные тов в нулевой момент протеолитической реак
БИОХИМИЯ том 86 вып. 11 2021
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1625
Рис. 3. Динамика образования NT IGFBP 4 (а) и СT IGFBP 4 (б) в ходе протеолитической реакции IGFBP 4 в течение 1,
3 и 24 ч. Стерильная среда DMEM, проинкубированная с субстратной смесью в присутствии рекомбинантного dPAPP A
(кривая 1, пунктирная линия); кондиционированная клеточная среда, проинкубированная с субстратной смесью в при
сутствии первичной культуры кардиомиоцитов крысы (кривая 2, серая сплошная линия); стерильная среда DMEM про
инкубированная с субстратной смесью (кривая 3, линия из точек); стерильная среда DMEM, проинкубированная анало
гичные промежутки времени (кривая 4, светло серая сплошная линия); n = 12, * p < 0,05
ции. После инкубации стерильной среды
получили и охарактеризовали ранее (рис. 4), и
DMEM с субстратной смесью в течение анало
сравнили полученные значения со значениями
гичных промежутков времени образования NT
концентраций NT IGFBP 4 и CT IGFBP 4 в
IGFBP 4 и CT IGFBP 4 не было выявле
кондиционированной среде культуры с 70% ным
но (рис. 3, кривая 3). При этом при проведении
содержанием кардиомиоцитов, специально по
протеолитической реакции в стерильной сре
лученной для решения этой задачи.
де (рис. 3, кривая 1) в присутствии 500 нг/мл до
Как видно из представленных результатов, в
бавленного экзогенно dPAPP A концентрации
случае культуры примесных клеток (рис. 4) наб
NT IGFBP 4 и CT IGFBP 4, определенные ме
людается накопление NT IGFBP 4 и CT
тодом ФИА, через 1, 3 и 24 ч, были в 2 раза вы
IGFBP 4 в кондиционированной среде. Концен
ше, чем при отсутствии PAPP A, что говорит о
трации NT IGFBP 4 и CT IGFBP 4 в культуре
том, что dPAPP A проявляет протеолитические
примесных клеток через 3 и 24 ч после начала
свойства в данной среде, и данная модель под
протеолитической реакции составили
20
и
ходит для изучения протеолиза IGFBP 4 под
60 нг/мл и 5 и 50 нг/мл соответственно. В случае
действием dPAPP A.
культуры кардиомиоцитов уровень наблюдае
Однако, как уже упоминалось ранее, dPAPP A
и фрагменты IGFBP 4 обнаруживаются в куль
туральной среде фибробластов человека [12] и
эндотелиальных клетках коронарной артерии
человека [26]. Данные типы клеток широко
представлены в сердечной ткани [28] и могут со
очищаться при выделении культуры кардиомио
цитов из сердца, т.е. входить во фракцию при
месных клеток. Следовательно, можно ожидать,
что кардиофибробласты и эндотелиальные
клетки, присутствующие в полученной культуре
кардиомиоцитов в количестве 10-30% от обще
го числа клеток, потенциально могут вносить
вклад в наблюдаемую нами протеолитическую
деградацию IGFBP 4. Для вычисления вклада
dPAPP A, секретируемого примесными клетка
ми, в итоговый уровень протеолиза IGFBP 4 мы
измерили концентрации NT IGFBP 4 и CT
IGFBP 4 в кондиционированной среде изоли
Рис. 4. Накопление NT IGFBP 4 и СT IGFBP 4 в конди
рованной культуры примесных клеток, которую
ционированной среде культуры примесных клеток; n = 3
2 БИОХИМИЯ том 86 вып. 11 2021
1626
СЕРЕБРЯНАЯ и др.
мого нами dPAPP A специфичного протеолиза
ходить преимущественно в условиях, когда
IGFBP 4 оказался приблизительно в 2,5-3 раза
IGFBP 4 находится в комплексе с IGF II [29,
выше по сравнению с фракцией примесных кле
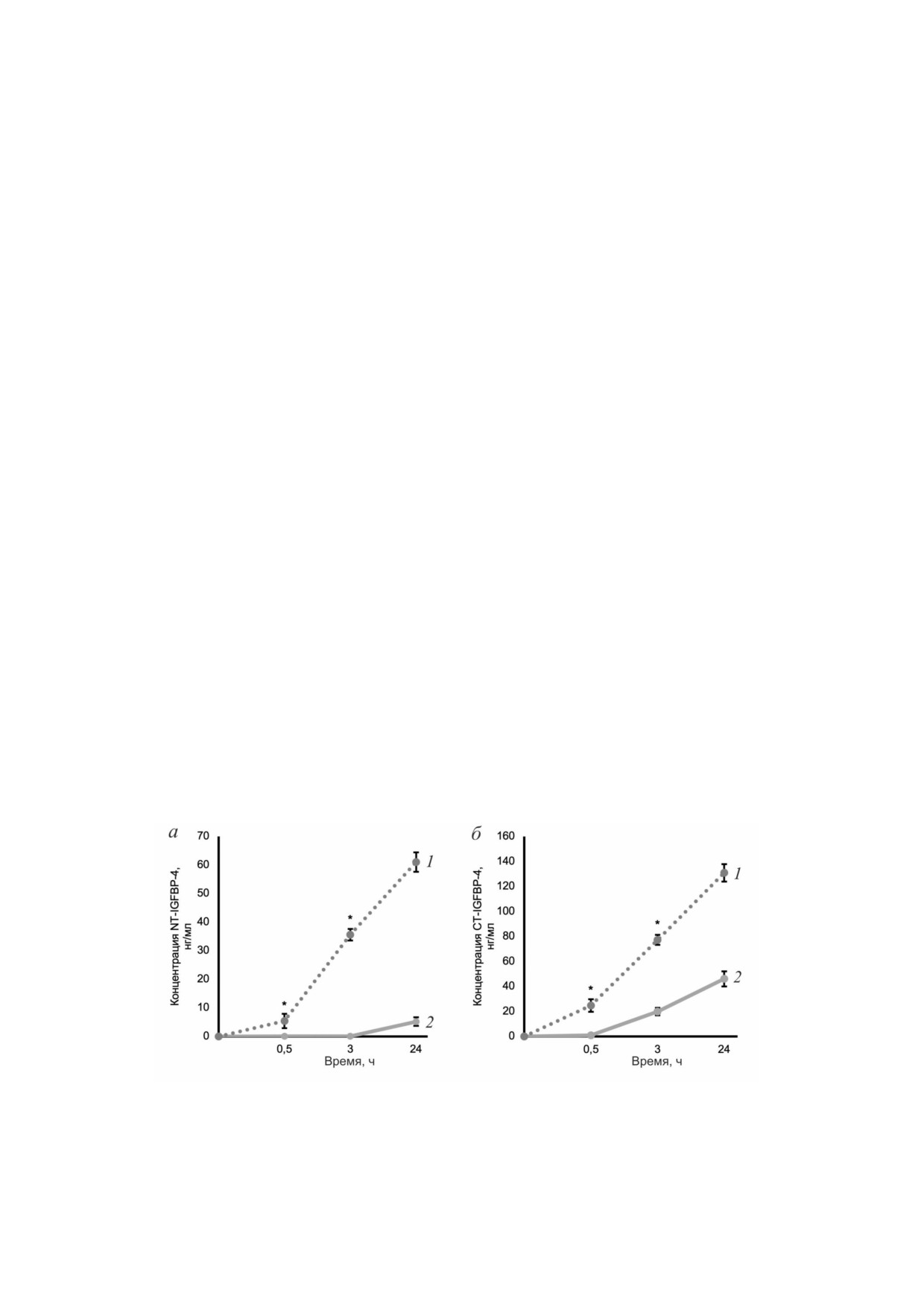
30]. Как видно на рис. 5, проведение протеоли
ток: концентрации NT IGFBP 4 и CT IGFBP 4
тической реакции IGFBP 4 в присутствии IGF
составляют 60 и 150 нг/мл и 20 и 110 нг/мл соот
II (рис. 5, а и б; кривая 1) приводит к возраста
ветственно.
нию концентраций NT IGFBP 4 и CT IGFBP 4
Далее, используя результаты иммунофлуо
в кондиционированной среде кардиомиоцитов
ресцентного окрашивания и учитывая концен
в 3-4 раза по сравнению с их концентрациями,
трации NT IGFBP 4 и CT IGFBP 4 в кондицио
определенными после проведения протеолиза в
нированной среде обеих культур, мы рассчитали
аналогичных условиях, но при отсутствии IGF
вклад фракции примесных клеток в протеоли
II (рис. 5, а и б; кривая 2).
тическую деградацию IGFBP 4 в полученной
Таким образом, суммируя полученные ре
культуре кардиомиоцитов. В том случае, когда
зультаты, представленные на рис. 3-5, можно
культура кардиомиоцитов имеет 70% ную чис
заключить: 1) протеолиз IGFBP 4 происходит в
тоту (содержит 30% примесных клеток), кон
кондиционированной среде первичной культу
центрации NT IGFBP 4 и CT IGFBP 4, кото
ры кардиомиоцитов и преимущественно ассо
рые образуются в результате секреции PAPP A
циирован именно с кардиомиоцитами, а не с
примесными клетками, будут в 3,3 раза ниже,
примесными клетками; 2) детекция NT IGFBP 4
чем в кондиционированной среде культуры,
и CT IGFBP 4 с использованием антител, спе
состоящей на 100% из примесных клеток. Таким
цифичных к неоэпитопу, образующемуся в ре
образом, вклад протеолитической деградации
зультате специфического расщепления IGFBP 4
IGFBP 4, осуществляемый dPAPP A, секрети
под действием dPAPP A, а также необходи
руемого примесными клетками, в итоговые кон
мость IGF II для реализации наблюдаемого
центрации NT IGFBP 4 и CT IGFBP 4 во всех
протеолиза позволяют предположить, что про
случаях составляет преимущественно 10-13%.
теолиз IGFBP 4 в кондиционированной среде
Следовательно, можно ожидать, что в случае
кардиомиоцитов происходит под действием
культуры кардиомиоцитов, имеющей чисто
PAPP A.
ту 90%, вклад примесных клеток в итоговый
Моделирование гипертрофического ответа
уровень dPAPP A специфичного протеоли
кардиомиоцитов крысы под действием эндотели
за IGFBP 4 будет ещё ниже и составит 3-4%.
на 1. Первичная культура кардиомиоцитов хо
Таким образом, полученные нами данные сви
рошо известна как in vitro модель для исследова
детельствуют о том, что наблюдаемый на
ния механизмов гипертрофии сердечной тка
ми dPAPP A специфичный протеолиз IGFBP 4
ни [31-33]. Одним из методов индукции гипер
в основном ассоциирован с кардиомиоцитами,
трофии является длительная (более 24 ч) инку
а не с примесными клетками.
бация кардиомиоцитов в присутствии эндоте
Известно, что специфический протеолиз
лина 1 в диапазоне концентраций 10-100 нМ
IGFBP 4 под действием dPAPP A может проис
[34-37].
Рис. 5. Образование NT IGFBP 4 (а) и CT IGFBP 4 (б) в ходе протеолитического расщепления IGFBP 4 в кондициони
рованной среде первичной культуры кардиомиоцитов в присутствии (кривая 1, линия из точек) и при отсутствии IGF
II (кривая 2, сплошная линия). Данные представлены как среднее значение ± квадратичное отклонение; n = 3, * p < 0,05
по сравнению с контролем без IGF II
БИОХИМИЯ том 86 вып. 11 2021
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1627
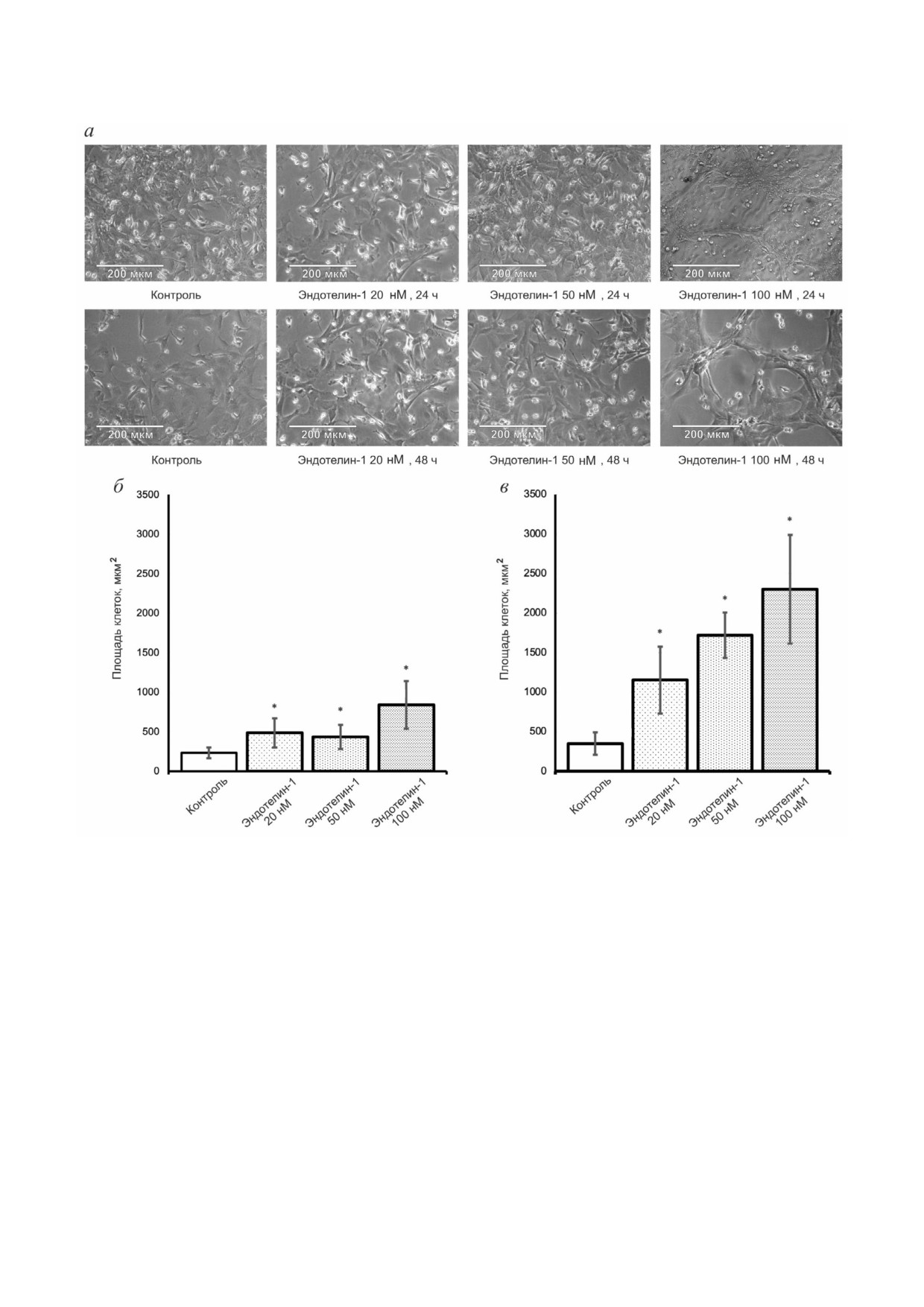
Рис. 6. Индукция гипертрофии в первичной культуре кардиомиоцитов крысы под действием эндотелина 1. а - Фотогра
фии кардиомиоцитов после инкубации с различными концентрациями эндотелина 1, сделанные в режиме фазового
контраста; б - зависимость площади кардиомиоцитов от концентрации эндотелина 1 при инкубации в течение 24 ч;
в - зависимость площади кардиомиоцитов от концентрации эндотелина 1 при инкубации в течение 48 ч; n = 15, * p < 0,05
по сравнению с контролем без эндотелина
Как видно из результатов (рис. 6), площадь
ции 20 нМ в кондиционированной среде наблю
поверхности кардиомиоцитов после инкубации
дается повышенное по сравнению с контроль
в культуральной среде, содержащей 20, 50 и
ными клетками содержание маркёра сердечной
100 нМ эндотелина 1, в течение 24 ч (рис. 6, б) и
недостаточности - натрийуретического пептида
48 ч (рис. 6, в) инкубации увеличивается в сред
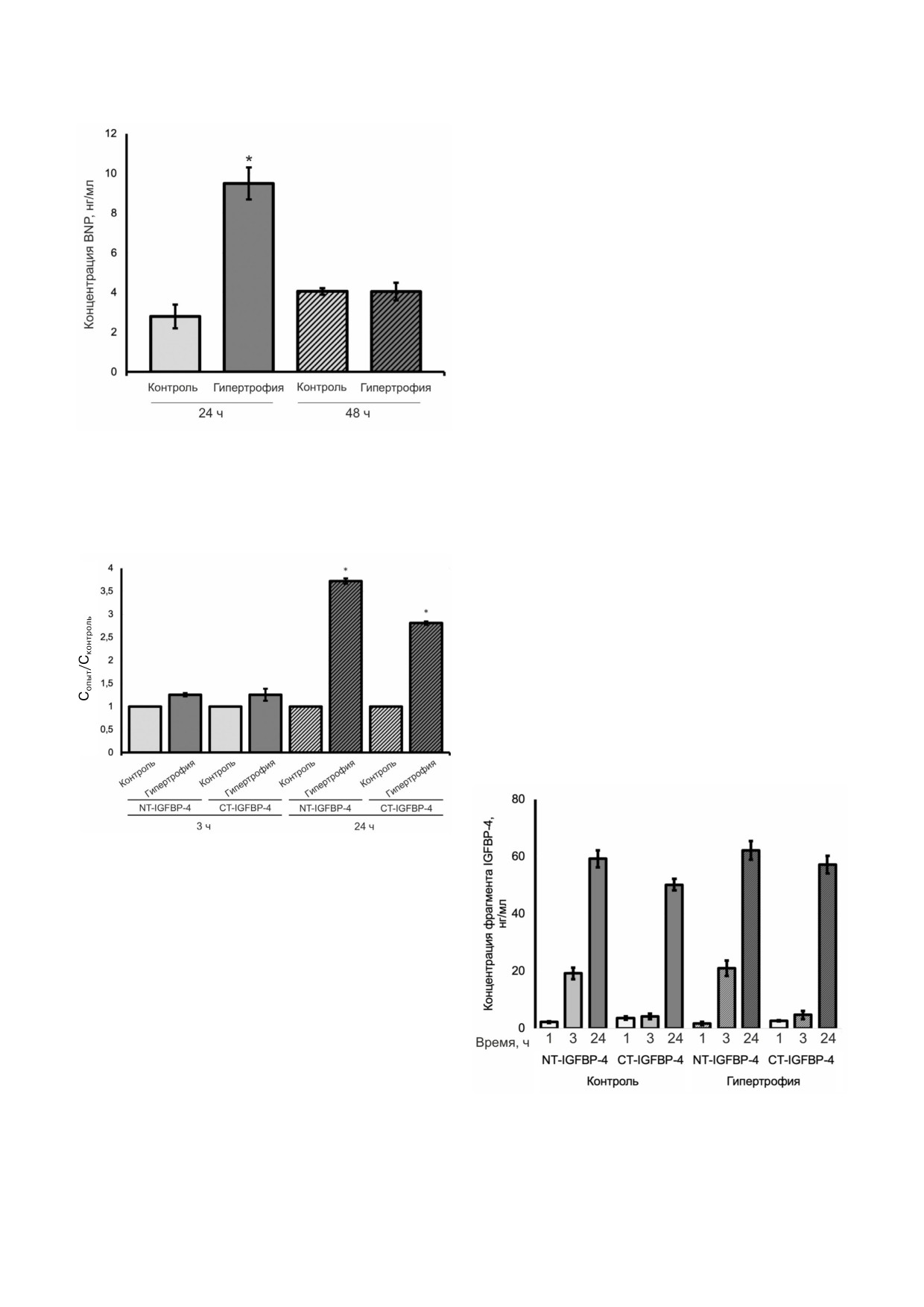
типа B (BNP) (рис. 7).
нем в 2, 1,8 и 4,5 раза и в 3,2, 4,4 и 6,4 раза соот
Кардиомиоциты инкубировали 24 и 48 ч в
ветственно по сравнению с площадью конт
присутствии или при отсутствии 20 нМ эндоте
рольных кардиомиоцитов (культивированных
лина 1, после чего определяли концентрацию
без добавления эндотелина 1).
BNP в культуральных средах методом флуоро
Мы также обнаружили, что после инкубации
иммунного анализа «сэндвич» типа с использо
кардиомиоцитов с эндотелином 1 в концентра ванием антител, специфичных к BNP. Из пред
БИОХИМИЯ том 86 вып. 11 2021
2*
1628
СЕРЕБРЯНАЯ и др.
связываем это с цитотоксическим влиянием эн
дотелина 1 при длительных инкубациях. Этот
эффект не был напрямую нами исследован, од
нако при подсчёте клеток после каждого экспе
римента мы наблюдали значительное уменьше
ние количества жизнеспособных кардиомиоци
тов в культуре, инкубированной с эндотелином 1
по сравнению с контрольными клетками.
Таким образом, инкубация первичной куль
туры кардиомиоцитов в присутствии эндотели
на 1 в концентрации 20 нМ в течение 24 ч под
ходит для моделирования гипертрофического
ответа кардиомиоцитов, и дальнейшие исследо
вания мы проводили при этой концентрации
эндотелина 1.
Исследование протеолиза IGFBP 4 в первич
ной культуре кардиомиоцитов при гипертрофии.
Чтобы исследовать, связано ли увеличение кон
Рис. 7. Концентрация BNP в кондиционированной среде
первичной культуры кардиомиоцитов после инкубации с
центраций фрагментов IGFBP 4 с гипертрофи
эндотелином 1 в концентрации 20 нМ. В кондициониро
ческим ответом кардиомиоцитов, мы измерили
ванную среду контрольных клеток добавляли воду; n = 5,
концентрацию протеолитических фрагментов
* p < 0,05
IGFBP 4 в культуре кардиомиоцитов при гипер
трофии. Концентрации NT IGFBP 4 и СТ
IGFBP 4, измеренные после протеолиза
IGFBP 4, проведённого в течение 3 и 24 ч в кон
диционированной среде гипертрофированных
кардиомиоцитов, превышали значения концен
траций фрагментов в контрольных клетках в 1,2
и 3,7 раза для NT IGFBP 4 и в 1,2 и 2,8 раза -
для CT IGFBP 4 соответственно (рис. 8).
Однако из данных литературы известно, что
инкубация в течение 24-48 ч в присутствии эн
дотелина 1 в концентрации 10-100 нМ приво
дит к активации пролиферации кардиофибро
бластов [38]. Поскольку кардиофибробласты с
Рис. 8. Концентрация NT IGFBP 4 и СT IGFBP 4 в кон
диционированной среде первичной культуры кардиомио
цитов крысы в норме и при гипертрофии. Отношение
Cопыт/Cконтроль соответствует отношению концентраций
фрагментов IGFBP 4, измеренных в кондиционирован
ной среде гипертрофированных кардиомиоцитов (Cопыт) и
контрольных кардиомиоцитов (Cконтроль); n = 7, * p < 0,05
ставленных результатов видно, что после 24 ча
совой инкубации с эндотелином 1 концентра
ция BNP в гипертрофированной культуре в 3 ра
за превышает концентрацию BNP в кондицио
нированной среде контрольных клеток (рис. 7).
Следует отметить, что инкубация кардиомиоци
тов с аналогичной концентрацией эндотелина 1
Рис. 9. Концентрация NT IGFBP 4 и СT IGFBP 4 в кон
в течение 48 ч не приводит к увеличению концен
диционированной среде культуры примесных клеток при
трации BNP в кондиционированной среде. Мы
гипертрофии; n = 3
БИОХИМИЯ том 86 вып. 11 2021
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1629
высокой вероятностью присутствуют во фрак
сопровождают различные ССЗ. В нашей работе
ции примесных клеток, это может способство
мы впервые продемонстрировали на модели
вать усилению PAPP A специфичной деграда
первичной культуры кардиомиоцитов крысы,
ции IGFBP 4, не связанной с кардиомиоцита
что dPAPP A специфичный протеолиз IGFBP 4
ми. Для того чтобы проверить, как влияет инку
протекает в кондиционированной среде кардио
бация с эндотелином 1 на количество примес
миоцитов. Мы также провели моделирование
ных клеток, мы провели подсчёт примесных
гипертрофического ответа кардиомиоцитов и
клеток до и после 24 часовой инкубации с
впервые установили, что гипертрофические из
20 нМ эндотелином 1. Мы обнаружили, что
менения кардиомиоцитов приводят к повыше
после инкубации изолированной культуры при
нию уровня протеолиза IGFBP 4 по сравнению
месных клеток с эндотелином 1 наблюдается
с контрольными негипертрофированными кар
увеличение их количества в 1,5 раза, что согла
диомиоцитами.
суется с литературными данными о стимулиру
Из литературных данных известно, что про
ющем эффекте эндотелина 1 на пролиферацию
теолиз IGFBP 4 под действием PAPP A проте
кардиофибробластов. Далее мы определили
кает в кондиционированной среде различных
уровень dPAPP A специфичного протеоли
клеточных линий [12, 21-27]. Однако на сегод
за IGFBP 4 в кондиционированной среде до
няшний день в литературе нет данных о том,
и после инкубации культуры примесных клеток
происходит ли протеолитическая деградация
с 20 нМ эндотелином 1 в течение 24 ч (рис. 9).
IGFBP 4 под действием PAPP A в кондициони
Из представленных результатов видно, что в
рованной среде кардиомиоцитов. В качестве
случае примесной клеточной фракции инкуба
модели для исследования протеолиза IGFBP 4 в
ция с эндотелином 1 не приводила к статисти
кардиомиоцитах мы использовали первичную
чески достоверному изменению уровня dPAPP
культуру кардиомиоцитов неонатальных крыс,
A специфичного протеолиза IGFBP 4. Получен
которая широко применяется для изучения раз
ные результаты подтверждают тот факт, что уси
личных процессов, протекающих в миокар
ление протеолитической деградации IGFBP 4
де [31-33, 40-42]. Несомненным преимущест
под действием dPAPP A при гипертрофии ассо
вом данной модельной системы является её
циировано именно с кардиомиоцитами, а не с
приближённость по физиологическим свой
примесными клетками.
ствам к ткани сердечной мышцы. Однако ис
Таким образом, в используемой модели при
пользование такой культуры сопряжено с рядом
гипертрофическом ответе кардиомиоцитов
сложностей, главной из которых является её ге
крысы наблюдается увеличение уровня протео
терогенность (содержание кардиомиоцитов в
лиза IGFBP 4 по сравнению с контрольными
ней составляет 70-90%, остальная часть клеток
клетками.
представлена кардиофибробластами и клетками
эндотелия). Контаминация культуры кардиомио
цитов другими типами клеток сердечной ткани
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
может вносить свой вклад в изучаемые молеку
лярные механизмы, влияя на исход экспери
Исследование прогностических маркёров
мента. Нам удалось впервые провести протеоли
ССЗ и установление причин, приводящих к воз
тическое расщепление IGFBP 4 в кондициони
растанию их концентраций в крови при разви
рованной среде кардиомиоцитов и детектиро
тии различных патологических состояний, яв
вать NT IGFBP 4 и CT IGFBP 4 с использова
ляется важной задачей как с фундаментальной
нием пар антител, специфичных к неоэпито
научной, так и с прикладной биомедицинской
пам, образующимся на N и С фрагментах в ре
точек зрения. В нашей работе мы исследовали
зультате протеолиза IGFBP 4 под действием
механизмы, приводящие к увеличению в крови
dPAPP A. Из литературных данных известно,
концентраций фрагментов IGFBP 4 - прогнос
что фибробласты и эндотелиальные клетки спо
тических маркёров развития таких ССЗ, как
собны секретировать dPAPP A [12, 26], следова
СН, ишемическая болезнь сердца и острый ко
тельно, присутствие таких типов клеток в итого
ронарный синдром [13-16], а также ассоцииро
вой первичной культуре кардиомиоцитов может
ванных с повышенным риском смертности пос
влиять на наблюдаемую нами протеолитичес
ле перенесенного инфаркта миокарда и при ост
кую деградацию IGFBP 4. В связи с этим мы
рой сердечной недостаточности [39]. Настоящее
оценили вклад суммарной фракции примесных
исследование было посвящено установлению
клеток в dPAPP A специфичную деградацию
взаимосвязи между уровнем протеолиза IGFBP 4
IGFBP 4, наблюдаемую нами в первичной куль
под действием PAPP A в кардиомиоцитах и их
туре кардиомиоцитов, который составил при
гипертрофическими изменениями, которые
мерно 10-13% от общего уровня итогового про
БИОХИМИЯ том 86 вып. 11 2021
1630
СЕРЕБРЯНАЯ и др.
теолиза IGFBP 4 в случае культуры кардиомио
циированы с риском развития таких ССЗ, как
цитов 70% ной чистоты. В случае, когда чистота
ИБС и ОКС, а также риском смертности у паци
культуры кардиомиоцитов достигала 90%, мож
ентов после перенесенного инфаркта миокарда
но предположить, что вклад суммарной фрак
и при острой СН [13-16, 39], однако механиз
ции примесных клеток в dPAPP A специфич
мы, лежащие в основе этих явлений, не исследо
ную деградацию IGFBP 4 будет состав
ваны. В этой связи важно было изучить возмож
лять 3-4%. Таким образом, мы впервые проде
ные причины увеличения уровня протеолиза
монстрировали, что PAPP A специфичный про
IGFBP 4 при ССЗ. В настоящем исследовании
теолиз IGFBP 4 протекает в первичной культуре
мы предположили, что одним из факторов, спо
неонатальных кардиомиоцитов крысы, и он ас
собствующих увеличению уровня протеолиза
социирован преимущественно с кардиомиоци
IGFBP 4, может быть гипертрофическое изме
тами, а не с примесными клетками. Интересным
нение сердечной мышцы, выражающееся в уве
фактом является то, что динамика накопления
личении размеров кардиомиоцитов и ускорении
NT IGFBP 4 и CT IGFBP 4 в кондициониро
в них белкового синтеза в ответ на физиологи
ванных средах кардиомиоцитов и примесных
ческие или патологические стимулы. В нашей
клеток различается. Вероятно, это связано с тем,
работе нам удалось смоделировать гипертрофи
что состав кондиционированных сред в случае
ческий ответ на первичной культуре кардиомио
обеих культур, которые представлены данными
цитов крысы с использованием эндотелина 1.
типами клеток, также может быть разным. Кон
Данный подход хорошо описан в ряде исследо
диционированные среды кардиомиоцитов и
ваний [35-37]. После 24 часовой инкубации с
примесных клеток могут содержать компоненты
20 нМ эндотелином 1 кардиомиоциты сущест
(например, различные протеазы), которые могут
венно увеличивались в размерах и демонстриро
по разному влиять на стабильность NT IGFBP 4
вали значительное увеличение секреции маркё
и CT IGFBP 4 (особенно при длительных инку
ра гипертрофии BNP, что согласуется с данны
бациях) и, как следствие, на их детекцию с ис
ми, описанными в литературе [36, 37]. Измерив
пользованием ФИА «сэндвич» типа. Мы также
концентрации NT IGFBP 4 и CT IGFBP 4 в
обнаружили, что для реализации протеолиза
кондиционированной среде кардиомиоцитов
IGFBP 4 в кондиционированной среде кардио
после индукции гипертрофии, мы обнаружили,
миоцитов необходимо присутствие IGF II, что
что уровень протеолиза IGFBP 4 в кондицио
согласуется с данными литературы [29, 30]. Та
нированной среде гипертрофированной культу
ким образом, мы впервые показали возмож
ры в несколько раз превышает таковой в конт
ность протекания dPAPP A специфичного про
рольных негипертрофированных кардиомиоци
теолиза IGFBP 4 в первичной культуре кардио
тах. При этом в условиях индукции гипертро
миоцитов крысы в норме и доказали, что наблю
фии (инкубация с 20 нМ эндотелином 1 в тече
даемая нами PAPP A специфичная деградация
ние 24 ч) в культуре кардиомиоцитов хоть и наб
IGFBP 4 ассоциирована именно с кардиомио
людается увеличение общего количества при
цитами, а не примесными клетками, что являет
месных клеток в 1,5 раза, усиления PAPP A спе
ся новыми данными, не представленными в ли
цифичного протеолиза IGFBP 4 при этом не
тературе. Основываясь на литературных дан
происходит. Таким образом, повышение уровня
ных [4, 7, 27], можно предположить, что расщеп
PAPP A специфичного протеолиза IGFBP 4
ление IGFBP 4 под действием dPAPP A будет
при гипертрофии связано исключительно с ги
приводить к разрушению комплекса IGFBP 4 с
пертрофическими изменениями кардиомиоци
IGF, высвобождению IGF и активации в мио
тов, а не с воздействием эндотелина 1 на при
карде таких процессов, как пролиферация, миг
месные клетки, содержащиеся в используемой
рация и клеточный рост. Регенеративные свой
культуре. Эти данные впервые позволяют обоз
ства IGF хорошо изучены и описаны для широ
начить взаимосвязь между возрастанием концен
кого спектра клеточных линий и активно ис
траций NT IGFBP 4 и CT IGFBP 4 и гипертро
пользуются для терапии различных заболева
фическими изменениями кардиомиоцитов, ко
ний [43-45]. Следовательно, по аналогии с пре
торые, как упоминалось выше, сопровождают
дыдущими исследованиями можно ожидать, что
многие ССЗ и проясняют функцию dPAPP A в
высвобождение IGF в результате dPAPP A зави
миокарде в норме и при его гипертрофических
симого протеолиза IGFBP 4 может быть важ
изменениях. По всей видимости, усиление
ным механизмом для поддержания жизнеспо
dPAPP A зависимого протеолиза IGFBP 4 при
собности кардиомиоцитов в норме.
гипертрофии будет приводить к повышенной по
В значительном количестве исследований
сравнению с нормой активации IGF. Данные о
было показано, что экспрессия dPAPP A и по
функциях IGF при патологиях миокарда доста
вышенный уровень протеолиза IGFBP 4 ассо
точно противоречивы. С одной стороны, в ряде
БИОХИМИЯ том 86 вып. 11 2021
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1631
исследований подробно описаны кардиопро
сит от экспрессии и ферментативной активнос
текторные свойства IGF при различных сердеч
ти PAPP A, что может играть роль в регуляции
но сосудистых патологиях, в том числе и при
жизнеспособности кардиомиоцитов. Во вто
гипертрофии [46-49]. В 2009 г. Vinciguerra et al.
рых, усиление dPAPP A зависимого протеолиза
[46] продемонстрировали, что оверэкспрессия
IGFBP 4 и, как следствие, высвобождения IGF
IGF I в неонатальных кардиомиоцитах, переве
при гипертрофии может быть как механизмом
дённых в гипертрофированное состояние, по
для компенсации негативных воздействий на
вышает экспрессию кардиопротекторных генов
клеточные процессы, вызванные гипертрофи
(генов, экспрессия которых ассоциирована с
ческими изменениями, так и стимулировать эти
низкой вероятностью возникновения ССЗ), та
изменения. И, наконец, результаты данной ра
ких, как гены адипонектина, разобщающего
боты позволяют установить взаимосвязь между
белка 1 (UCP 1) и металлотионеина 2. В 2018 г.
увеличением уровня протеолиза IGFBP 4 под
Yeves et al. [47] продемонстрировали, что IGF 1
действием dPAPP A и гипертрофическими из
обладает кардиопротекторным действием на
менениями кардиомиоцитов, сопровождающи
модели спонтанно гипертензивных крыс. В ис
ми некоторые ССЗ, которая раньше не была ис
следованиях, проведённых Sui et al. [48] и
следована, и частично проясняют роль dPAPP A
Lin et al. [49], оверэкспрессия IGF II и IGF I со
в миокарде в норме и при его патологических
ответственно улучшала функцию сердца после
изменениях. Активация dPAPP A зависимого
инфаркта миокарда у мышей. С другой стороны,
протеолитического расщепления IGFBP 4 при
в ряде исследований, напротив, показано, что
гипертрофии кардиомиоцитов открывает воз
IGF является индуктором патологической гипер
можности для исследования не изученных ранее
трофии кардиомиоцитов [50-53], т.е. можно
механизмов развития различных ССЗ.
предположить, что его высвобождение в резуль
тате dPAPP A специфичного протеолиза
IGFBP 4 при гипертрофии будет приводить к
Благодарности. Авторы выражают искрен
ещё большему развитию гипертрофии. Таким
нюю признательность д.б.н. профессору
образом, обнаруженное нами усиление dPAPP
Н.Б. Гусеву и В.Е. Адашеву за ценные замечания
A зависимого протеолиза и, как следствие, воз
и комментарии, которые позволили существен
можное высвобождение IGF при гипертрофи
но улучшить рукопись.
ческих изменениях кардиомиоцитов может, с
Конфликт интересов. Авторы заявляют об от
одной стороны, представлять собой потенци
сутствии конфликта интересов.
альный механизм для компенсации негативных
Соблюдение этических норм. Все примени
воздействий на клеточные процессы, вызван
мые международные, национальные и/или инс
ные гипертрофией, а с другой стороны, напро
титуциональные принципы ухода и использова
тив, усиливать гипертрофические изменения.
ния животных были соблюдены. В частности,
Очевидно, что данная проблема требует даль
все эксперименты с животными проводили
нейшего изучения.
с соблюдением этических норм, согласно «Пра
Таким образом, результаты, полученные в
вилам проведения работ с использованием экс
настоящей работе, свидетельствуют о протека
периментальных животных», утвержденным ди
нии процессов dPAPP A зависимого протеоли
рективой Евросоюза 2010/63/EU. Эксперимен
за IGFBP 4 в кардиомиоцитах в норме и их ак
ты были одобрены Комиссией по биоэтике МГУ
тивизации в гипертрофированной ткани. Во
имени М.В. Ломоносова. Настоящая статья
первых, это позволяет предположить, что в сер
не содержит описания каких либо исследова
дечной ткани в норме биодоступность IGF зави
ний с участием людей в качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1.
Bhatnagar, P., Wickramasinghe, K., Williams, J.,
4.
Hjortebjerg, R. (2018) IGFBP 4 and PAPP A in normal
Rayner, M., and Townsend, N. (2015) The epidemiology
physiology and disease, Growth Horm. IGF Res., 41, 7 22,
of cardiovascular disease in the UK 2014, Heart, 101,
doi: 10.1016/j.ghir.2018.05.002.
1182 1189, doi: 10.1136/heartjnl 2015 307516.
5.
Lin, T. M., Halbert, S. P., and Spellacy, W. N. (1974)
2.
Rame, J. E., and Dries, D. L. (2007) Heart failure and car
Measurement of pregnancy associated plasma proteins
diac hypertrophy, Curr. Treat. Options Cardiovasc. Med., 9,
during human gestation, J. Clin. Invest., 54, 576 582,
289 301, doi: 10.1007/s11936 007 0024 3.
doi: 10.1172/JCI107794.
3.
Shimizu, I., and Minamino, T. (2016) Physiological and
6.
Overgaard, M. T., Sorensen, E. S., Stachowiak, D., Boldt,
pathological cardiac hypertrophy, J. Mol. Cell Cardiol., 97,
H. B., Kristensen, L., Sottrup Jensen, L., and Oxvig, C.
245 262, doi: 10.1016/j.yjmcc.2016.06.001.
(2003) Complex of pregnancy associated plasma protein A
БИОХИМИЯ том 86 вып. 11 2021
1632
СЕРЕБРЯНАЯ и др.
and the proform of eosinophil major basic protein.
18.
Laursen, L. S., Overgaard, M. T., Søe, R., Boldt, H. B.,
Disulfide structure and carbohydrate attachment, J. Biol.
Sottrup Jensen, L., et al. (2001) Pregnancy associated
Chem., 278, 2106 2117, doi: 10.1074/jbc.M208777200.
plasma protein A (PAPP A) cleaves insulin like growth
7.
Oxvig, C. (2015) The role of PAPP A in the IGF system:
factor binding protein (IGFBP) 5 independent of IGF:
location, location, location, J. Cell. Commun. Signal., 9,
implications for the mechanism of IGFBP 4 proteolysis by
177 187, doi: 10.1007/s12079 015 0259 9.
PAPP A, FEBS Lett., 504, 36 40, doi: 10.1016/s0014
8.
Monget, P., Mazerbourg, S., Delpuech, T., Maurel, M. C.,
5793(01)02760 0.
Manière, S., et al. (2003) Pregnancy associated plasma
19.
Semenov, A. G., Tamm, N. N., Apple, F. S., Schulz, K. M.,
protein A is involved in insulin like growth factor binding
Love, S. A., et al. (2017) Searching for a BNP standard: gly
protein 2 (IGFBP 2) proteolytic degradation in bovine
cosylated proBNP as a common calibrator enables improved
and porcine preovulatory follicles: identification of cleav
comparability of commercial BNP immunoassays,
age site and characterization of IGFBP 2 degradation,
Clin. Biochem., 50, 181 185, doi: 10.1016/j.clinbiochem.
Biol. Reprod., 68, 77 86, doi: 10.1095/biolreprod.102.
2016.11.003.
007609.
20.
Conover, C. A., Oxvig, C., Overgaard, M. T.,
9.
Byun, D., Mohan, S., Yoo, M., Sexton, C., Baylink, D. J.,
Christiansen, M., and Giudice, L. C. (1999). Evidence that
and Qin, X. (2001) Pregnancy associated plasma protein
the insulin like growth factor binding protein 4 protease in
A accounts for the insulin like growth factor (IGF) bind
human ovarian follicular fluid is pregnancy associated plas
ing protein 4 (IGFBP 4) proteolytic activity in human
ma protein A, J. Clin. Endocrinol. Metab., 84, 4742 4745,
pregnancy serum and enhances the mitogenic activity of
doi: 10.1210/jcem.84.12.6342.
IGF by degrading IGFBP 4 in vitro, J. Clin. Endocrinol.
21.
Mazerbourg, S., Overgaard, M. T., Oxvig, C.,
Metab., 86, 847 854, doi: 10.1210/jcem.86.2.7223.
Christiansen, M., Conover, C. A., et al. (2001) Pregnancy
10.
Gyrup, C., and Oxvig, C. (2007) Quantitative analysis of
associated plasma protein A (PAPP A) in ovine, bovine,
insulin like growth factor modulated proteolysis of
porcine, and equine ovarian follicles: involvement in IGF
insulin like growth factor binding protein 4 and
5 by
binding protein 4 proteolytic degradation and mRNA
pregnancy associated plasma protein A, Biochemistry, 46,
expression during follicular development, Endocrinology,
1972 1980, doi: 10.1021/bi062229i.
142, 5243 5253, doi: 10.1210/endo.142.12.8517.
11.
Lindsay, C. R., and Evans, T. J. (2008) The insulin like
22.
Conover, C. A., Faessen, G. F., Ilg, K. E., Chandrasekher,
growth factor system and its receptors: a potential novel
Y. A., Christiansen, M., et al. (2001) Pregnancy associated
anticancer target, Biologics, 2, 855 864, doi: 10.2147/btt.
plasma protein A is the insulin like growth factor binding
s3841.
protein 4 protease secreted by human ovarian granulosa
12.
Lawrence, J. B., Oxvig, C., Overgaard, M. T., Sottrup
cells and is a marker of dominant follicle selection and the
Jensen, L., Gleich, G. J., et al. (1999) The insulin like
corpus luteum, Endocrinology, 142, 2155, doi: 10.1210/
growth factor (IGF) dependent IGF binding protein 4
endo.142.5.8286.
protease secreted by human fibroblasts is pregnancy asso
23.
Bayes Genis, A., Schwartz, R. S., Lewis, D. A., Overgaard,
ciated plasma protein A, Proc. Natl. Acad. Sci. USA, 96,
M. T., Christiansen, M., et al. (2001) Insulin like growth
3149 3153, doi: 10.1073/pnas.96.6.3149.
factor binding protein 4 protease produced by smooth
13.
Bayes Genis, A., Conover, C. A., Overgaard, M. T., Bailey,
muscle cells increases in the coronary artery after angio
K. R., Christiansen, M., et al. (2001) Pregnancy associat
plasty, Arterioscler. Thromb. Vasc. Biol., 21, 335341,
ed plasma protein A as a marker of acute coronary syn
doi: 10.1161/01.atv.21.3.335.
dromes, N. Engl. J. Med., 345, 1022 1029, doi: 10.1056/
24.
Giudice, L. C., Conover, C. A., Bale, L., Faessen, G. H.,
NEJMoa003147.
Ilg, K., et al. (2002) Identification and regulation of the
14.
Postnikov, A. B., Smolyanova, T. I., Kharitonov, A. V.,
IGFBP 4 protease and its physiological inhibitor in human
Serebryanaya, D. V., Kozlovsky, S. V., et al. (2012) N ter
trophoblasts and endometrial stroma: evidence for
minal and C terminal fragments of IGFBP 4 as novel bio
paracrine regulation of IGF II bioavailability in the pla
markers for short term risk assessment of major adverse
cental bed during human implantation, J. Clin. Endocrinol.
cardiac events in patients presenting with ischemia, Clin.
Metab., 87, 2359 2366, doi: 10.1210/jcem.87.5.8448.
Biochem.,
45,
519524, doi:
10.1016/j.clinbiochem.
25.
Conover, C. A., Bale, L. K., Frye, R. L., and Schaff, H. V.
2011.12.030.
(2019). Cellular characterization of human epicardial adi
15.
Hjortebjerg, R., Tarnow, L., Jorsal, A., Parving, H. H.,
pose tissue: highly expressed PAPP A regulates insulin like
Rossing, P., Bjerre, M., and Frystyk, J (2015) IGFBP 4
growth factor I signaling in human cardiomyocytes,
fragments as markers of cardiovascular mortality in type 1
Physiol. Rep., 7, doi: 10.14814/phy2.14006.
diabetes patients with and without nephropathy, J. Clin.
26.
Conover, C. A., Harrington, S. C., Bale, L. K. (2008)
Endocrin. Metab., 100, 3032-3040, doi: 10.1210/jc.2015
Differential regulation of pregnancy associated plasma
2196.
protein A in human coronary artery endothelial cells and
16.
Konev, A. A., Kharitonov, A. V., Rozov, F. N., Altshuler,
smooth muscle cells, Growth Horm. IGF Res., 18, 213 220,
E. P., Serebryanaya, D. V., et al. (2020) CT IGFBP 4 as a
doi: 10.1016/j.ghir.2007.09.001.
novel prognostic biomarker in acute heart failure, ESC
27.
D’Elia, P., Ionta, V., Chimenti, I., Angelini, F., Miraldi, F.,
Heart Fail., 7, 434 444, doi: 10.1002/ehf2.12590.
et al. (2013) Analysis of pregnancy associated plasma pro
17.
Степанова О. В., Чадин А.В., Куликова Т.Г., Масенко
tein A production in human adult cardiac progenitor cells,
В.П., Терещенко С.Н. (2012) Роль Rho ассоциирован
BioMed Res. Int., 2013, 190178, doi: 10.1155/2013/
ной киназы в формировании миофибрилл и сократи
190178.
мости кардиомиоцитов, Кардиологический вестник, 7,
28.
Banerjee, I., Fuseler, J. W., Price, R. L., Borg, T. K., and
10 14.
Baudino, T. A. (2007) Determination of cell types and
БИОХИМИЯ том 86 вып. 11 2021
PAPP A СПЕЦИФИЧНЫЙ ПРОТЕОЛИЗ IGFBP 4 В КАРДИОМИОЦИТАХ
1633
numbers during cardiac development in the neonatal and
rat cardiac myocyte cultures, Front. Physiol., 10, 1564,
adult rat and mouse, Am. J. Physiol. Heart Circ. Physiol.,
doi: 10.3389/fphys.2019.01564.
293, H1883 H1891, doi: 10.1152/ajpheart.00514.2007.
41.
Ariyasinghe, N. R., Lyra Leite, D. M., and McCain, M. L.
29.
Laursen, L. S., Kjaer Sorensen, K., Andersen, M. H., and
(2018) Engineering cardiac microphysiological systems to
Oxvig, C. (2007) Regulation of insulin like growth factor
model pathological extracellular matrix remodeling,
(IGF) bioactivity by sequential proteolytic cleavage of IGF
Am. J. Physiol. Heart Circ. Physiol., 315, H771 H789,
binding protein 4 and 5, Mol. Endocrinol., 21, 1246 1257,
doi: 10.1152/ajpheart.00110.2018.
doi: 10.1210/me.2006 0522.
42.
Belostotskaya, G. B., and Golovanova, T. A.
(2014)
30.
Laursen, L. S., Overgaard, M. T., Nielsen, C. G., Boldt,
Characterization of contracting cardiomyocyte colonies in
H. B., Hopmann, K. H., et al. (2002) Substrate specificity
the primary culture of neonatal rat myocardial cells: a
of the metalloproteinase pregnancy associated plasma pro
model of in vitro cardiomyogenesis, Cell Cycle, 13, 910
tein A (PAPP A) assessed by mutagenesis and analysis of
918, doi: 10.4161/cc.27768.
synthetic peptides: substrate residues distant from the scis
43.
Higashi, Y., Gautam, S., Delafontaine, P., and
sile bond are critical for proteolysis, Biochem. J., 367, 31
Sukhanov, S. (2019) IGF 1 and cardiovascular disease,
40, doi: 10.1042/BJ20020831.
Growth Horm. IGF Res., 45, 6 16, doi: 10.1016/j.ghir.
31.
Ryall, K. A., Saucerman, J. J. (2012) Automated imaging
2019.01.002.
reveals a concentration dependent delay in reversibility of
44.
Mohamed Ali, V., and Pinkney, J. (2002) Therapeutic
cardiac myocyte hypertrophy, J. Mol. Cell. Cardiol., 53,
potential of insulin like growth factor 1 in patients with
282 290, doi: 10.1016/j.yjmcc.2012.04.016.
diabetes mellitus, Treat. Endocrinol.,
1,
399410,
32.
Archer, C. R., Robinson, E. L., Drawnel, F. M.,
doi: 10.2165/00024677 200201060 00005.
and Roderick, H. L. (2017) Endothelin 1 promotes hyper
45.
Sádaba, M. C., Mart n Estal, I., Puche, J. E., and Castilla
trophic remodelling of cardiac myocytes by activating sus
Cortázar, I. (2016) Insulin like growth factor 1 (IGF 1)
tained signalling and transcription downstream of
therapy: mitochondrial dysfunction and diseases, Biochim.
endothelin type A receptors, Cell Signal., 36, 240 254,
Biophys. Acta, 1862, 1267 1278, doi: 10.1016/j.bbadis.
doi: 10.1016/j.cellsig.2017.04.010.
2016.03.010.
33.
Jen, H. L., Yin, W. H., Chen, J. W., and Lin, S. J. (2017)
46.
Vinciguerra, M., Santini, M. P., Claycomb, W. C.,
Endothelin 1 induced cell hypertrophy in cardiomyocytes
Ladurner, A. G., and Rosenthal, N. (2009) Local IGF 1
is improved by fenofibrate: possible roles of adiponectin,
isoform protects cardiomyocytes from hypertrophic and
J. Atheroscler. Thromb., 24, 508 517, doi: 10.5551/jat.
oxidative stresses via SirT1 activity, Aging (Albany NY), 2,
36368.
43 62, doi: 10.18632/aging.100107.
34.
Higazi, D. R., Fearnley, C. J., Drawnel, F. M., Talasila, A.,
47.
Yeves, A. M., Burgos, J. I., Medina, A. J., Villa Abrille,
Corps, E. M., et al. (2009) Ca2+ release is a nexus for
M. C., and Ennis, I. L. (2018) Cardioprotective role of
hypertrophic signaling in cardiac myocytes, Mol. Cell, 33,
IGF 1 in the hypertrophied myocardium of the sponta
472 482, doi: 10.1016/j.molcel.2009.02.005.
neously hypertensive rats: a key effect on NHE 1 activity,
35.
Yue, T. L., Gu, J. L., Wang, C., Reith, A. D., Lee, J. C.,
Acta Physiol. (Oxf), 224, doi: 10.1111/apha.13092.
et al. (2000) Extracellular signal regulated kinase plays an
48.
Sui, Y., Zhang, W., Tang, T., Gao, L., Cao, T., et al. (2020)
essential role in hypertrophic agonists, endothelin 1 and
Insulin like growth factor II overexpression accelerates
phenylephrine induced cardiomyocyte hypertrophy,
parthenogenetic stem cell differentiation into cardiomy
J. Biol. Chem., 275, 3789537901, doi: 10.1074/jbc.
ocytes and improves cardiac function after acute myocar
M007037200.
dial infarction in mice, Stem Cell Res. Ther., 11, 86,
36.
Yamazaki, T., Komuro, I., Kudoh, S., Zou, Y.,
doi: 10.1186/s13287 020 1575 4.
Shiojima, I., et al. (1996) Endothelin 1 is involved in
49.
Lin, M., Liu, X., Zheng, H., Huang, X., Wu, Y., et al.
mechanical stress induced cardiomyocyte hypertrophy,
(2020) IGF 1 enhances BMSC viability, migration, and
J. Biol. Chem., 271, 3221 3228, doi: 10.1074/jbc.271.
anti apoptosis in myocardial infarction via secreted friz
6.3221.
zled related protein 2 pathway, Stem Cell Res. Ther., 11, 22,
37.
Nakahashi, T., Fukuo, K., Inoue, T., Morimoto, S.,
doi: 10.1186/s13287 019 1544 y.
Hata, S., et al. (1995) Endothelin 1 enhances nitric oxide
50.
Adachi, S., Ito, H., Akimoto, H., Tanaka, M., Fujisaki, H.,
induced cytotoxicity in vascular smooth muscle,
et al. (1994) Insulin like growth factor II induces hyper
Hypertension, 25, 744 747, doi: 10.1161/01.hyp.25.4.744.
trophy with increased expression of muscle specific genes
38.
Piacentini, L., Gray, M., Honbo, N. Y., Chentoufi, J.,
in cultured rat cardiomyocytes, J. Mol. Cell. Cardiol., 26,
Bergman, M., Karliner, J. S. (2000) Endothelin 1 stimu
789 795, doi: 10.1006/jmcc.1994.1096.
lates cardiac fibroblast proliferation through activation of
51.
Carrasco, L., Cea, P., Rocco, P., Peña Oyarzún, D.,
protein kinase C, J. Mol. Cell Cardiol., 32, 565 576,
Rivera Mejias, P., et al. (2014) Role of heterotrimeric G
doi: 10.1006/jmcc.2000.1109.
protein and calcium in cardiomyocyte hypertrophy induced
39.
Hjortebjerg, R., Lindberg, S., Pedersen, S., Mogelvang, R.,
by IGF 1, J. Cell Biochem., doi: 10.1002/jcb.24712.
Jensen, J. S., et al. (2017) Insulin like growth factor bind
52.
Ito, H., Hiroe, M., Hirata, Y., Tsujino, M., Adachi, S., et al.
ing protein 4 fragments provide incremental prognostic
(1993) Insulin like growth factor I induces hypertrophy with
Information on cardiovascular events in patients with ST
enhanced expression of muscle specific genes in cultured rat
segment elevation myocardial infarction, J. Am. Heart
cardiomyocytes, Circulation, 87, doi: 10.1161/01.cir.87.5.1715.
Assoc., 6, doi: 10.1161/JAHA.116.005358.
53.
Huang, C. Y., Hao, L. Y., and Buetow, D. E. (2002)
40.
Makkos, A., Szántai, Á., Pálóczi, J., Pipis, J., Kiss, B.,
Insulin like growth factor II induces hypertrophy of adult
et al.
(2020) A Comorbidity model of myocardial
cardiomyocytes via two alternative pathways, Cell. Biol.
ischemia/reperfusion injury and hypercholesterolemia in
Int., 26, 737 739, doi: 10.1006/cbir.2002.0919.
БИОХИМИЯ том 86 вып. 11 2021
1634
СЕРЕБРЯНАЯ и др.
IGFBP 4 PROTEOLYSIS BY PAPP A IN A PRIMARY CULTURE
OF RAT NEONATAL CARDIOMYOCYTES IN NORMAL
AND HYPERTROPHIC CONDITIONS
D. V. Serebryanaya1*, D. A. Adasheva1, A. A. Konev2, M. M. Artemieva3,
I. A. Katrukha1,2, A. B. Postnikov1,2, N. A. Medvedeva3, and A. G. Katrukha1,2
1 Department of Biochemistry, Faculty of Biology, Lomonosov Moscow State University,
119234 Moscow, Russia; E>mail: dariaserebryanaya@gmail.com
2 HyTest Ltd, 20520 Turku, Finland
3 Department of Human and Animal Physiology, Faculty of Biology,
Lomonosov Moscow State University, 119234 Moscow, Russia
Cardiovascular disease (CVD) is one of the leading causes of death and disability worldwide. Pregnancy associated
plasma protein A (PAPP A) is a matrix metalloprotease localized on the cell surface. One of the substrates that
PAPP A cleaves is IGFBP 4 (insulin like growth factor binding protein 4), a member of the family of proteins that
bind IGF (insulin like growth factor). Proteolysis of IGFBP 4 by PAPP A occurs at a specific site, results in forma
tion of two proteolytic fragments - N terminal (NT IGFBP 4) and C terminal (CT IGFBP 4) - and leads to the
release of IGF, which activates various cellular processes including migration, proliferation, and cell growth. An
increased levels of proteolytic IGFBP 4 fragments correlate with the development of complications and the risk of
death of patients with such CVD as coronary heart disease, acute coronary syndrome, and heart failure. However,
there is no direct evidence of the PAPP A specific proteolysis of IGFBP 4 in cardiac tissue in normal and patholog
ical conditions. In the present study, using a model of a primary culture of rat neonatal cardiomyocytes, we have
demonstrated that (i) proteolysis of IGFBP 4 by PAPP A occurs in the conditioned medium of cardiomyocytes,
(ii) an increase of PAPP A specific IGFBP 4 proteolysis is observed when cardiomyocytes are transferred to a hyper
trophic state. Thus, it can be assumed that the enhancement of IGFBP 4 cleavage and hypertrophic changes in car
diomyocytes accompanying CVD are interrelated, and PAPP A appears to be the one of the activators of IGF depen
dent processes in normal and hypertrophic cardiomyocytes.
Keywords: cardiovascular diseases, heart failure, cardiomyocytes, primary culture, proteolysis, PAPP A, IGFBP 4,
hypertrophy, endothelin 1
БИОХИМИЯ том 86 вып. 11 2021