БИОХИМИЯ, 2022, том 87, вып. 1, с. 26 - 44
УДК 577.151.62
МУТАЦИИ В СУБЪЕДИНИЦЕ Cox12 ДРОЖЖЕЙ СНИЖАЮТ
АКТИВНОСТЬ МИТОХОНДРИАЛЬНОГО КОМПЛЕКСА IV
© 2022
S. Das, S. Mukherjee, M. Bedi, A. Ghosh*
Department of Biochemistry, University of Calcutta, 35 Ballygunge Circular Road,
Pin 700019, Kolkata, India; e mail: alok.caluni@gmail.com
Поступила в редакцию 11.04.2021
После доработки 25.10.2021
Принята к публикации 21.11.2021
Цитохром с оксидаза 6B1 (COX6B1) является одной из наименее изученных субъединиц комплекса IV (CIV)
митохондриальной электрон транспортной цепи. В настоящей работе мы изучали патобиохимические и
респираторные функции Cox12 (дрожжевой ортолог COX6B1 человека) с использованием клеток
Saccharomyces cerevisiae BY4741 (cox12Δ), дефицитных по белку Cox12. Эти клетки показывали серьёзные
затруднения в росте в аэробной (дыхательной) среде, содержащей глицерин и этанол, которые можно было
восстановить путём комплементации с генами COX12 дрожжей или COX6B1 человека. Cox12 с остатком ар
гинина 17, замещённым гистидином (R17H) или цистеином (R17C) (мутации, аналогичные тем, которые
наблюдаются у людей), не вызывал восполнение утраченной функции Cox12. Когда клетки cox12Δ выращи
вали в богатой дыхательной/ферментативной среде галактозы, изменений в экспрессии субъединиц дыха
тельной цепи не наблюдалось. Анализ с помощью метода голубого нативного электрофореза в полиакрила
мидном геле с последующим вестерн блоттингом с использованием антител против Rip1 и Cox1, которые
являются специфическими компонентами комплексов III (CIII) и IV (CIV) соответственно, не выявил за
метного снижения содержания нативных суперкомплексов (SC) CIII2CIV2 и CIII2CIV1. Однако ассоциация
фактора 2 респираторного суперкомплекса Rcf2 и субъединицы Cox2 с SC в клетках cox12Δ понижалась, а
специфическая активность CIV снижалась на 90%. Как базальное дыхание, так и стимулированное сукци
натом/АДФ дыхание в состоянии 3, а также мембранный потенциал митохондрий в клетках cox12Δ были
понижены. Кроме того, клетки cox12Δ и клетки, синтезирующие мутантные формы белка Cox12 (R17H и
R17C), показывали большую чувствительность к окислительному стрессу, индуцированному H2O2, по срав
нению с клетками дикого типа (WT). Моделирование in silico структуры SC дрожжей WT показало, что
Cox12 формирует сеть взаимодействий с Rcf2 и Cox2. В целом полученные нами результаты говорят о том,
что Cox12 необходим для проявления активности CIV.
КЛЮЧЕВЫЕ СЛОВА: цитохром с оксидаза 6B1, Cox12, комплекс IV, суперкомплексы.
DOI: 10.31857/S0320972522010031
ВВЕДЕНИЕ
логических видов - от одноклеточных пекарс
ких дрожжей Saccharomyces cerevisiae до челове
Цитохром с оксидаза (COX, EC 1.9.3.1) или
ка. CIV млекопитающих состоит из 14 различ
комплекс IV (CIV) митохондриальной элект
ных субъединиц [1, 2], 3 из которых кодируются
рон транспортной цепи (ЭТЦ) переносит
митохондриальной ДНК: большие каталитичес
электроны от восстановленного ферроцитохро
кие субъединицы COX1 и COX2, содержащие
ма c к молекулярному кислороду. Комплекс IV,
все окислительно восстановительные центры, и
который локализован на внутренней мембране
субъединица COX3, которая участвует в форми
митохондрий, является консервативным белко
ровании внутреннего ядра. Эти субъединицы
вым комплексом, присутствующим у всех био
собираются в холокомплекс CIV, образуя 3 мо
дуля вместе с 11 меньшими субъединицами
Принятые сокращения: АФК - активные формы (COX4, COX5A, COX5B, COX6A, COX6B,
кислорода; BN ПААГ - голубой нативный электрофорез в
COX6C, COX7A, COX7B, COX7C, COX8A и
полиакриламидном геле; ЭТЦ - электрон транспортная
цепь; CCCP - карбонилцианид м хлорфенилгидразон,
NDUFA4), которые кодируются ядерной ДНК
разобщитель; COX - цитохром с оксидаза; NAC - N аце
[3-7]. Биогенез CIV начинается с субъединицы
тилцистеин; OCR - скорость поглощения кислорода; COX1 (субкомплекс 1), к которой присоединя
R17H и R17C - мутантные формы гена COX12HA, кодирую
ются COX4 и COX5A, в результате чего образует
щие мутантные белки с заменами R17H или R17C; RFP -
ся субкомплекс 2. Затем модуль COX2 (COX2,
консервативный мотив Arg Phe Pro; SC - суперкомплекс;
TMPD - N,N,N′,N′ тетраметил p фенилендиамин; WT -
COX5B, COX6C, COX7B, COX7C и COX8A) и
дикий тип.
модуль COX3 (COX3, COX6A, COX6B и COX7A)
* Адресат для корреспонденции.
присоединяются к модулю COX1, в результате
26
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
27
чего образуется субкомплекс 3 [8, 9]. Наконец,
вносит вклад в антивозрастные эффекты огра
NDUFA4 присоединяется к субкомплексу 3,
ничения калорийности [14].
чтобы продуцировать холофермент CIV (рис. S1
Основные сведения о биохимической ро
в Приложении) [7].
ли COX6B1 были получены при изучении дрож
Далее CIV может взаимодействовать с други
жей S. cerevisiae. Клетки дрожжей - удобный
ми комплексами ЭТЦ с образованием суперком
объект для проведения генетических манипуля
плексов (SC). Например, CIV может объеди
ций. Кроме того, дрожжи с дефектной дыха
няться с комплексом I (CI) и димерным ком
тельной цепью могут расти на ферментативных
плексом III (CIII2) с образованием суперком
источниках углерода. Белок COX6B1 человека и
плексов I + III2 + IV2 и I + III2 + IV1. Дрожжи ли
его дрожжевой ортолог Cox12 демонстрируют
шены CI и образуют суперкомплексы III2 + IV1 и
идентичность последовательностей более чем
III2 + IV2 [10-12].
на 42%. Делеция Cox12 ассоциируется со сниже
Кодируемая ядерным геномом, субъедини
нием содержания цитохрома a+a3. В результате
ца COX6B встраивается в модуль COX3 на позд
эти клетки не могут расти в аэробной дыхатель
них этапах сборки CIV. COX6B содержит кон
ной среде [26]. Ранее мы продемонстрировали,
сервативный домен СНСН (coiled coil helix
что функции Coa6 - фактора сборки CIV, кото
coiled coil helix) с редокс активным и богатым
рый также содержит мотив Cx9CxnCx10C, пере
остатками цистеина мотивом Cx9CxnCx10C, ко
крываются с функциями Cox12 дрожжей
торый способствует транслокации этого белка в
[27, 28]. Клетки coa6Δ и cox12Δ не показывали
митохондрии через пути Mia40 erv1 [13-16].
ограниченный рост в аэробной/ферментацион
Другой консервативный мотив, Arg Phe Pro
ной среде, содержащей галактозу, при 30 °C.
(RFP), располагается на N концевом участ
Клетки coa6Δ cox12Δ (с двойным нокаутом) не
ке COX6B, но функция этого мотива пока не
могли расти в тех же условиях из за отсутствия
ясна. Обнаружены две изоформы COX6B.
субъединицы Cox2, и этот фенотип не мог быть
COX6B1 присутствует практически во всех тка
спасён при добавлении в среду экзогенной меди
нях за исключением опухолевых клеток семен
(в отличие от клеток coa6Δ) [27]. Было показано,
ников и поджелудочной железы, которые со
что Cox12 присоединяется к модулю Cox3 на
держат COX6B2 [17].
поздних стадиях сборки комплекса, а фак
COX6B1 является одной из шести субъеди
тор 2 (Rcf2) дыхательного SC обеспечивает
ниц CIV. Мутации в этой субъединице были вы
встраивание и стабильность Cox12 во время
явлены у пациентов с митохондриальными за
сборки модуля Cox3 [29-31]. Модули Cox1
болеваниями (MD). Мутации COX6B1 вызыва
и Cox2, которые содержат весь каталитический
ют различные патофизиологические проявле
гем a+a3 и центры меди, собираются до присое
ния, включая миопатию, тяжёлую детскую эн
динения Cox12 к комплексу IV. До сих пор оста
цефаломиопатию, гидроцефалию и кардиомио
ётся неясным, как мутации в Cox12 изменяют
патию. Пациенты с такими мутациями часто
дыхательную активность и процесс сборки CIV.
умирают в раннем возрасте из за отсутствия ак
В настоящей работе мы использовали клетки
тивности COX. Так, были идентифицированы
S. cerevisiae cox12Δ, чтобы изучить биохимичес
3 мутации COX6B: R20H, R20C и T81P. Интерес
кую и физиологическую роль Cox12 в биогенезе
но, что R20 является частью мотива RFP
и активности CIV.
[18-20]. Дефекты CIV, вызванные мутациями в
структурных субъединицах или факторах сбор
ки, представляют собой второй по частоте тип
МАТЕРИАЛЫ И МЕТОДЫ
наследственных MD после дефектов CI [21-24].
Кроме того, значение COX6B1 подчёркивается
Штаммы дрожжей, культивирование клеток и
тем фактом, что сверхэкспрессия COX6B1 ока
плазмиды. Клетки S. cerevisiae дикого типа (WT)
зывает защитное действие при вызванном ише
BY4741 (Mat a; his3Δ1; leu2Δ0; met15Δ0; ura3Δ0;
мией/реперфузией (I/R) повреждении нейро
лабораторные штаммы, полученные из штам
нов и окислительном стрессе, опосредованном
ма S288C) и клетки cox12Δ (Mat a; his3Δ1;
активными формами кислорода (АФК) в кардио
leu2Δ0; met15Δ0; ura3Δ0; YLR038C::kanMX4)
миоцитах крысы
[25]. Активная регуляция
(«Invitrogen», США) культивировали и поддер
COX6B1 и повышенная доля высокомолекуляр
живали в среде YPD (1% дрожжевого экстракта,
ных SC наблюдалась в печени животных, под
2% пептона и 2% декстрозы) при 30 °C. Делеция
вергшихся ограничению калорийности. В то же
гена cox12Δ была подтверждена проведением
время сверхэкспрессия COX6B1 в культуре кле
ПЦР колонии клеток (табл. S1 в Приложении);
ток 3T3 способствовала выживанию этих кле
coa6Δ, sco1Δ и клетки pet117Δ с известными де
ток, что позволяет предположить, что COX6B1
фектами CIV («Invitrogen») были использованы
БИОХИМИЯ том 87 вып. 1 2022
28
DAS и др.
в качестве отрицательных контролей [28]. Для
описано ранее [32]. Для приготовления цито
проверки восстановления роста клеток в среду
зольной фракции дрожжевые клетки обрабаты
YPD и YPGE добавляли 25 мМ N ацетилцисте
вали Zymolyase 20T («US Biological», США) и
ин (NAC).
гомогенизировали во льду в буфере, содержа
Клетки дрожжей культивировали в сре
щем 0,6 M сорбитол, 10 мМ Tris HCl (pH 7,4),
де YPD, затем их инокулировали в среду YPD,
1 мМ ЭДТА и 1 мМ PMSF. Обломки клеток уда
YPGal (2% галактозы) или YPGE (3% глицери
ляли центрифугированием при 3000 g в течение
на + 1% этанола). Чашки со средами YPD,
10 мин при 4 °C. Супернатант осветляли с по
YPGal и YPGE были приготовлены с добавлени
мощью ультрацентрифугирования при 150 000 g
ем 2% агара. Для проведения измерений роста
в течение 1 ч при 4 °C. К митохондриальной и
клеток на чашки со средами YPD, YPGal или
цитозольной фракциям добавляли смесь инги
YPGE наносили последовательные десятикрат
биторов протеаз («Roche cOmplete», Германия),
ные разведения ночных культур, и их инкубиро
и полученные препараты хранили при -80 °C.
вали при 30 °C и 37 °C в течение определенных
Концентрацию белка определяли с помощью
периодов времени. Рост дрожжей в жидкой сре
наборов BCA assay kit («Thermo Scientific»,
де измеряли спектрофотометрически при
США).
600 нм. Плазмиду pRS416 с низким числом ко
SDS<ПААГ, голубой нативный ПААГ и имму<
пий («Addgene», США) использовали для кло
ноблоттинг. Электрофорез в SDS полиакрила
нирования гена COX6B1 человека, дрожжево
мидном геле (SDS ПААГ) и голубой нативный
го COX12 и гена COX12, меченного C концевым
ПААГ (BN ПААГ) проводили для разделения
гемагглютинином (HA), под контролем промо
денатурированных и нативных белковых комп
тора GPD с использованием специфических
лексов соответственно [33]. Для SDS ПААГ ли
праймеров (табл. 1). Конструкцию дрожжевого
заты митохондрий (5-10 мкг) разделяли в
COX12HA использовали в качестве матрицы для
15% ном Tris глициновом геле. Для BN ПААГ
проведения сайт направленного мутагене
20 мкг митохондриальных белков солюбилизи
за («Agilent Technologies QuikChange Lightning»,
ровали в буфере, содержащем 50 мМ имида
США) для создания точечных мутантов R17C и
зол (pH 7,2), 500 мМ 6 аминогексаноевую кис
R17H с использованием праймеров, указанных
лоту,
1
мМ ЭДТА, 1× cOmpleteTM Protease
в табл. 1.
Inhibitor Cocktail («Roche») и 2% дигитонина, в
Все конструкции были подтверждены секве
течение 20 мин при 4 °C и центрифугировали
нированием ДНК. Дрожжевые клетки, транс
при 20 000 g в течение 30 мин при 4 °C. Перед на
формированные с помощью плазмиды pRS416
несением белков на нативный 3-13% Bis Tris
GPD, культивировали в средах без урацила
градиентный гель в супернатант добавляли кра
( URA): SCD (2% декстрозы) и SCGE (3% гли
ситель Кумасси голубой G 250 (0,01%). Для про
церина + 1% этанола).
ведения иммуноокрашивания разделённые бел
Получение митохондриальной и цитозольной
ки переносили на PVDF мембрану и зондирова
фракций. Клетки дрожжей (1 г.), выращенные
ли следующими антителами: анти Cox1
до достижения поздней лаг фазы, использова
(1 : 1000; «Abcam», Великобритания); анти Cox2
ли для получения митохондриальной и цито
(1
: 10 000; «Abcam»); анти Cox3 (1 : 5000;
зольной фракций. Митохондрии выделяли, как
«Abcam»); анти Cox4 (1 : 1500; «Abcam»); анти
Таблица 1. Праймеры, использованные в данной работе
Праймер
Последовательность (5′→3′)
pRS416 GPD COX12 прямой (EcoRI)
TAC CCG GAATTC CGG ATG GCT GAT CAA GAA AAC TCT CCA CT
pRS416 GPD COX12HA обратный (XhoI)
AGA CCG CTCGAG CGG TTA CGC ATA GTC AGG AAC ATC GTA TG
pRS416 GPD COX6B1 прямой (EcoRI)
CTG CCG GAATTC CGG ATG GCG GAA GAC ATG GAG ACC AAA AT
pRS416 GPD COX6B1 обратный (XhoI)
AGA CCG CTCGAG CGG TTA TCA GAT CTT CCC GGG AAA CGT
Cox12 R20H прямой
ACA GTT GGT TTC GAT GCT CAC TTT CCC CAA AAC CAA
Cox12 R20H обратный
TTG GTT TTG GGG AAA GTG AGC ATC GAA ACC AAC TGT
Cox12 R20C прямой
ACA GTT GGT TTC GAT GCT TGC TTT CCC CAA AAC CAA
Cox12 R20C обратный
TTG GTT TTG GGG AAA GCA AGC ATC GAA ACC AAC TGT
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
29
Cox12 (1 : 1500; любезно предоставлены сотруд
нием 2-3 мкг митопластов и проводили в тече
никами лаборатории доктора С. Мейсингера);
ние 5 мин. Чтобы рассчитать действительную
анти Coa6 (1 : 1500) и анти Rip1 (1 : 300 000)
активность CIV, из полученных данных вычита
(любезно предоставлены сотрудниками лабора
ли скорость этой реакции в присутствии
тории доктора В. Зара); анти Rcf1 (1 : 1000) и ан
100 мкМ азида натрия.
ти Rcf2 (1 : 1500) (любезно предоставлены сот
Скорость поглощения кислорода. Чтобы изме
рудниками лаборатории доктора М. Отта); ан
рить дыхательную активность на уровне клетки,
ти Vdac1 (1 : 10 000; «Abcam») и анти Pgk1
дрожжевые клетки выращивали в среде YPGal,
(1 : 5000; «Abcam»). Мембраны инкубировали со
собирали на поздней лаг фазе (A600 = 8) и ресус
вторичными антителами в разведении 1 : 5000 в
пендировали в свежей среде YPGal при концент
течение 1 ч при комнатной температуре и произ
рации 108 клеток/мл. Базальную скорость пот
водили окрашивание с использованием реаген
ребления кислорода (OCR) измеряли при 30 °C с
тов Clarity Western ECL («Bio Rad», США) или
помощью прибора Oxytherm («Hansatech», Вели
Super Signal West Femto («Thermo Scientific»).
кобритания), снабжённого электродом Кларка.
Все изображения гелей были получены с по
Клетки, трансформированные пустым векто
мощью системы «Bio Rad Chemidoc», США.
ром pRS416 GPD или плазмидами, несущими
Определение активности в геле. Нативные
гены COX12HA, R17H или R17C (R17H и R17C -
белковые комплексы разделяли с помощью чис
мутантные формы гена COX12HA, кодирующие
того нативного электрофореза в ПААГ (CN
мутантные белки с заменами R17H или R17C),
ПААГ), после чего проводили определение ак
культивировали в среде SCD ( URA) до A600 = 8
тивности в геле комплекса V (CV) и объединён
и ресуспендировали в свежей среде при концен
ной активности CIII + CIV [33]. Белки мембра
трации 108 клеток/мл, чтобы определить базаль
ны митохондрий получали, как было описано
ное значение OCR при 30 °C. Дыхание блокиро
выше перед проведением BN ПААГ. После
вали через
4
мин измерений добавлением
центрифугирования при 20 000 g в течение
1 мМ азида натрия (специфический ингиби
30 мин при 4 °C собирали прозрачный суперна
тор CIV). Среднее значение OCR (нмоль кисло
тант, и перед нанесением на 3-13% ный натив
рода/мин на 108 клеток) оценивали по данным
ный Bis Tris градиентный гель в него добавляли
как минимум трёх независимых экспериментов.
10% глицерина. Для определения активности
Исходный уровень и значения неспецифичес
CIII + CIV гель окрашивали 25 мМ диамино
кой OCR (после добавления азида натрия) были
бензидином (DAB), растворенным в 50 мМ нат
незначительными.
рий фосфатном буфере (pH 7,2), в течение 1 ч.
Чтобы измерить уровень митохондриально
Далее добавляли 60 мкМ цитохрома с из сердца
го дыхания, свежевыделенные митохондрии ре
лошади и инкубировали ещё 30 мин до появле
суспендировали в 1 мл дыхательной среды, со
ния полос, окрашенных в коричневый цвет. Ре
держащей
0,6
M маннитол,
2
мМ MgCl2,
акцию останавливали добавлением 50% метано
20 мМ HEPES KOH (pH 7,2), 1 мМ ЭДТА и
ла, содержащего 10% уксусной кислоты.
10 мМ K2HPO4. Для индукции дыхания исполь
Для измерения АТФ гидролизующей ак
зовали различные субстраты, специфичные к
тивности CV гель предварительно инкубирова
отдельным комплексам, такие как 10 мМ дву
ли при комнатной температуре в течение 2 ч в
натриевой соли янтарной кислоты (CII) или
буфере, содержащем 35 мМ Tris HCl (pH 8,3) и
12,5 мМ аскорбиновой кислоты + 1,4 мМ
270 мМ глицин. Затем гель переносили в бу
N,N,N′,N′ тетраметил p фенилендиамин (TMPD)
фер, содержащий 35 мМ Tris HCl (pH 8,3),
(CIV). Для индукции дыхательного состояния 3
270 мМ глицин, 14 мМ MgSO4, 0,2% Pb(NO3)2 и
добавляли АДФ (200 мкМ). Для блокировки ми
8 мМ АТФ, ещё на 1 ч. АТФ гидролизующую ак
тохондриального дыхания через 4 мин добавля
тивность определяли по появлению белого
ли 1 мМ азида натрия. Максимальное значение
осадка фосфата свинца. Реакцию останавливали
дыхательной ёмкости определяли путём добав
добавлением 50% метанола на 30 мин. Все изоб
ления 5 мкМ карбонилцианид м хлорфенил
ражения гелей получали с помощью системы
гидразона (CCCP, разобщитель) в присутствии
«Bio Rad Chemidoc».
10 мМ динатрий сукцината + 200 мкМ АДФ
Спектрофотометрическое определение актив<
(см. типичный график скорости для последова
ности комплекса IV. Активность CIV оценивали
тельности различных добавок на рисунках).
спектрофотометрически, отслеживая использо
В каждой серии определений концентрация мито
вание восстановленного цитохрома c при 550 нм
хондриального белка составляла 250-350 мкг/мл.
[34]. Реакционная смесь (1 мл) содержала 50 мМ
Среднее значение OCR (нмоль кислорода/мин
фосфата калия (pH 7,5) и 50 мкМ восстановлен
на мг митохондриального белка) оценивалось
ного цитохрома c. Реакцию запускали добавле
по данным как минимум трёх независимых экс
БИОХИМИЯ том 87 вып. 1 2022
30
DAS и др.
периментов. Исходный уровень и значения не
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
специфической OCR были незначительными.
Анализ чувствительности клеток к окисли<
Cox12/COX6B1 необходим для роста дрожжей
тельному стрессу. Клетки WT и cox12Δ выращи
в аэробной среде. Выравнивание аминокислот
вали до значения A600 = 3 в среде, содержащей
ной последовательности белков COX6B челове
2% ную декстрозу, при 30 °C, и затем их обраба
ка, крысы, рыбок Данио, мух и дрожжей с ис
тывали 2,5 мМ перекисью водорода в течение
пользованием программы ClustalW показало,
30 мин или использовали сразу. Приготовлен
что COX6B является эволюционно консерватив
ные серии разведений клеточных культур в сте
ным белком. Cox12 дрожжей имеет более чем 42
рильной воде высевали в чашки с YPD. Снимки
и 37% идентичности последовательности с изо
делали через каждые 2 дня. Клетки WT и cox12Δ,
формами COX6B1 и COX6B2 соответствен
трансформированные плазмидой pRS416 GPD,
но (рис. 1, a).
содержащей гены COX12HA, R17H или R17C, вы
Для определения биологической роли субъ
ращивали в среде SCD ( URA) при 30 °C до
единицы COX6B1 в сборке митохондриального
A600 = 3, а затем обрабатывали 2,5 мМ перекисью
дыхательного комплекса мы использовали
водорода в течение 30 мин или же использовали
дрожжевые клетки WT и cox12Δ S. cerevisiae. Мы
сразу. Десятикратные серийные разведения кле
регистрировали рост этих клеток на различных
ток наносили на чашки со средой SCD ( URA),
источниках углерода при различных температу
и клетки выращивали при 30 °C [35].
рах, чтобы оценить эффективность их дыхания.
Определение мембранного потенциала мито<
Оба типа клеток выращивали в течение
хондрий. Дрожжевые клетки выращивали в сре
2-3 дней в богатой ферментационной сре
де YPD до A600 = 3 и затем инкубировали с
де YPD, содержащей декстрозу, и в дыхательной
10 мкМ CCCP или без него в течение 30 мин при
среде YPGE, содержащей глицерин и этанол.
30 °C. Далее клетки центрифугировали при 300 g
Рост клеток WT и cox12Δ в среде YPD был со
в течение 5 мин. Полученные осадки ресуспен
поставим до 10 ч. После этого скорость роста
дировали в 500 мкл фосфатного солевого буфе
клеток cox12Δ снижалась без перехода в двух
ра (PBS) и трижды промывали в течение 5 мин
фазный рост, что свидетельствует об отсутствии
при комнатной температуре. К 500 мкл клеточ
способности использовать этанол (конечный
ной суспензии в PBS добавляли специфичный к
продукт ферментации), поскольку такая спо
мембранам митохондрий флуоресцентный кра
собность требует активную митохондриаль
ситель DiOC6 («Sigma Aldrich», США) в концен
ную ЭТЦ (рис. 1, b). Как и ожидалось, клетки
трации 20 нг/мл и инкубировали в течение
cox12Δ не росли в среде YPGE, что подтвердило
30 мин в темноте. Чтобы удалить избыток кра
наличие дефекта в дыхательной системе этих
сителя, клетки осаждали и промывали 3 ра
клеток (рис. 1, c). Мы также проанализировали
за PBS. Клетки изучали с помощью флуоресцент
рост клеток WT и cox12Δ на твёрдых средах YPD,
ной микроскопии («Olympus», Япония): воз
YPGE и YPGal (т.е. средах с различными источ
буждение при 485 нм и эмиссия при 520 нм.
никами углерода) при различных температурах.
Изображения анализировали с помощью прог
В качестве отрицательного контроля были ис
рамм FLUO VIEW
(«Olympus») и ImageJ
пользованы дрожжевые клетки с известными
(«NIH»).
дефектами CIV (coa6Δ, sco1Δ и pet117Δ)
Изучение белок<белковых взаимодействий с
(рис. 1, d) [28]. Как ожидалось, рост клеток
помощью программы PyMOL. In silico моделиро
cox12Δ на твёрдых средах YPD и YPGal был поч
вание проводили с использованием недавно
ти такой же, как рост клеток дикого типа, но
опубликованных структур дрожжевых суперком
был сильно понижен при культивировании в
плексов III2IV2 и III2IV1, полученных с помощью
среде YPGE как при 30 °C, так и при 37 °C
крио ЭМ (PDB IDs: 6T0B и 6T15) [29]. Ионные
(рис. 1, d).
взаимодействия Cox12 с другими субъединица
Далее мы трансформировали клетки cox12Δ
ми CIV были проанализированы с помощью
генами COX12HA или COX6B1 человека, клони
программы PyMOL.
рованными в низкокопийную плазмиду pRS416
Статистическая обработка данных. Получен
под контролем промотора GPD и определили
ные результаты представлены в виде среднего
способность этих генов восполнить недостаток
значения ± стандартная ошибка среднего. Ста
респираторного роста в дыхательной среде
тистическую обработку данных (t критерий
SCGE с глицерином/этанолом. Оба гена,
Стьюдента) проводили с использованием прог
COX12HA и COX6B1, способствовали восстанов
раммного обеспечения Microsoft Excel. * p < 0,05
лению дыхательного фенотипа клеток cox12Δ
и ** p < 0,001 считались статистически значи
(рис. 1, e). Ген COX12 дикого типа без гемагглю
мыми.
тининового тэга также восстанавливал дыха
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
31
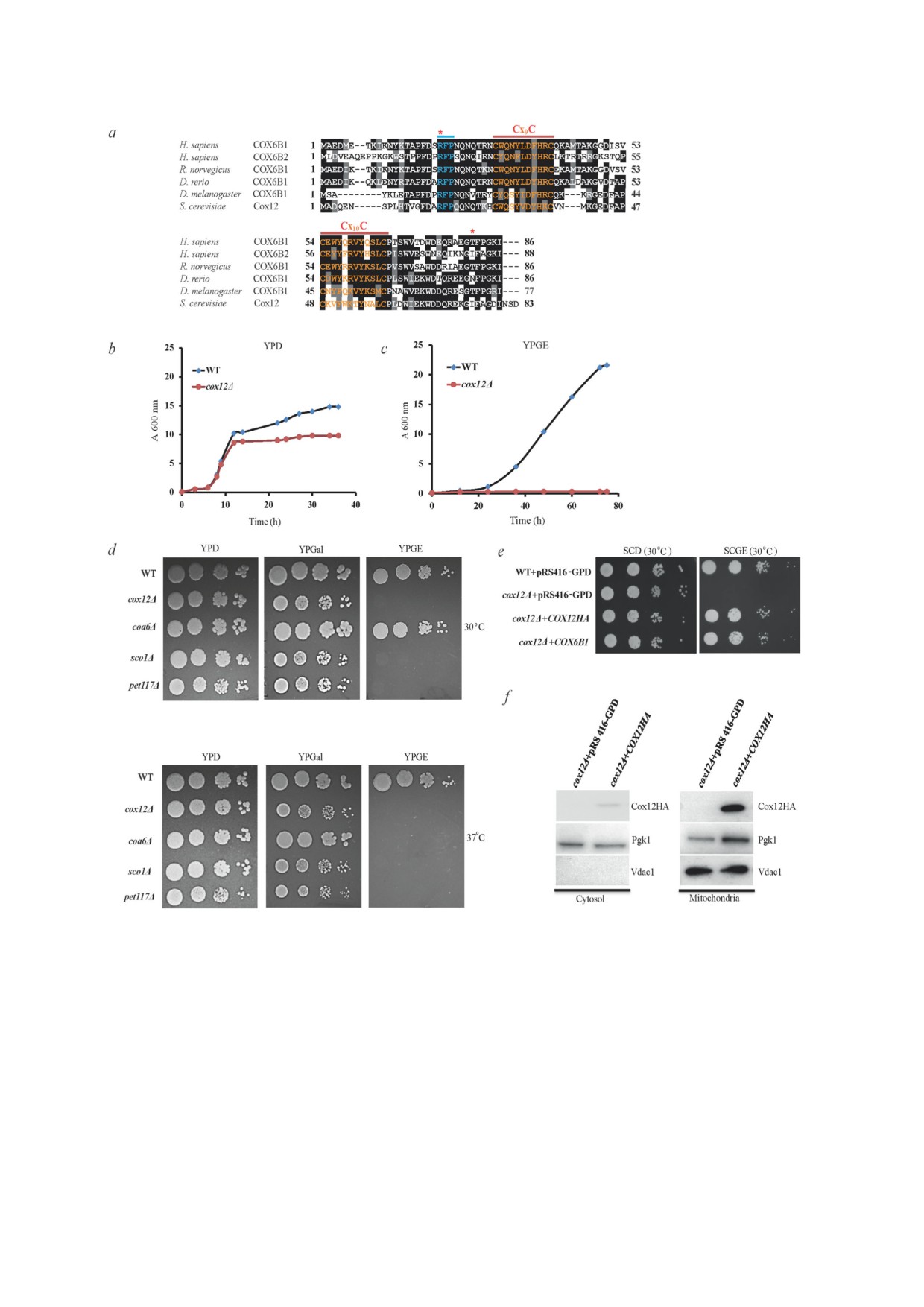
Рис. 1. Клетки cox12Δ дрожжей показывают сниженный рост на аэробной дыхательной среде. a - Выравнивание после
довательностей белка COX6B из различных видов (в клетках человека имеются 2 изоформы: COX6B1 и COX6B2). Гори
зонтальными линиями над последовательностью отмечены консервативные мотивы Cx9CxnCx10C и RFP. Звездочками по
казаны аминокислотные остатки, подвергающиеся мутациям у людей. b-c - При проведении анализа кривой роста клет
ки WT и cox12Δ культивировали в бульоне YPD, а затем инокулировали в свежей среде YPD (b) или YPGE (c) до A600 = 1.
Рост клеток регистрировали через указанные интервалы времени при 30 °C. d - Серийные десятикратные разведения кле
ток WT и cox12Δ, выращенных в течение ночи в среде YPD, наносили на чашки с YPD, YPGal и YPGE и инкубировали
при 30 или 37 °C. Снимки были сделаны через 2-5 дней роста. В качестве отрицательного контроля использовали клетки
с известными дефектами CIV (coa6Δ, sco1Δ и pet117Δ). e - Клетки WT и cox12Δ, трансформированные пустым векто
ром (pRS416 GPD) или векторами, экспрессирующими дрожжевой белок Cox12HA или COX6B1 человека, наносили на
чашки со средами без урацила ( URA) - SCD и SCGE - и выращивали при 30 °C. Снимки были сделаны через 2-5 дней
роста. f - SDS ПААГ и вестерн блот анализ уровней белка Cox12HA в митохондриальной и цитозольной фракциях кле
ток cox12Δ, трансформированных пустым вектором или геном COX12HA. Vdac1 и Pgk1 были использованы в качестве конт
роля нагрузки митохондриальной и цитозольной фракций соответственно. Все результаты блоттинга представляют по
крайней мере 3 независимых эксперимента
БИОХИМИЯ том 87 вып. 1 2022
32
DAS и др.
тельный фенотип в клетках cox12Δ (данные не
подтверждают то, что хотя Cox12 может быть не
показаны). Внутриклеточная локализация белка
заменим для частичного биогенеза CIV, его де
Cox12 была установлена с помощью метода
леция делает CIV неактивным.
SDS ПААГ и последующего иммуноблоттинга
OCR и максимальная дыхательная ёмкость
цитозольной и митохондриальной фракций ли
серьёзно нарушены в клетках cox12Δ. Чтобы оце
зата клеток cox12Δ, трансформированных пус
нить физиологическое влияние пониженной ак
тым вектором или COX12HA. Как ожидалось, бе
тивности CIV в клетках cox12Δ, мы измерили
лок Cox12HA экспрессировался и локализовал
OCR целых клеток и митохондрий с использо
ся в митохондриях (рис. 1, f). Следовательно,
ванием электрода Кларка для полярографичес
COX6B1 человека и Сox12 являются ортолога
кого определения содержания O2. Как и ожида
ми, и каждый из этих двух белков может восста
лось, клетки дефицитные по гену COX12, пока
навливать дефект роста в аэробной среде клеток
зывали значительное снижение (90%) базально
cox12Δ.
го уровня клеточной OCR по сравнению с клет
Делеция Cox12 вызывает снижение активнос<
ками WT, тогда как контрольные клетки coa6Δ
ти CIV. Чтобы выяснить биохимическую основу
показывали снижение уровня OCR на 45%
пониженного респираторного роста клеток
(рис. 3, a).
cox12Δ, нами была изучена стационарная
Затем измеряли OCR в стимулированном
экспрессия субъединиц ЭТЦ в митохондриаль
сукцинатом/ADP состоянии 3. Митохондрии из
ных экстрактах клеток WT, cox12Δ и coa6Δ, рас
клеток cox12Δ показали снижение OCR более
тущих в аэробной/ферментационной сре
чем на 80% по сравнению с клетками WT
де YPGal. SDS ПААГ и последующий вестерн
(рис. 3, b). Мы также измерили CIV опосредо
блоттинг не выявили значительных различий в
ванную OCR в присутствии высоких миллимо
содержании свободных CIII специфичных
лярных концентраций аскорбата и TMPD (ис
(Rip1) и CIV специфичных (Cox1-4) субъеди
кусственные субстраты дыхания). Удивительно,
ниц и факторов сборки SC (Rcf1 и Rcf2) в мито
но в клетках cox12Δ было обнаружено только
хондриях cox12Δ по сравнению с митохондрия
29% ное снижение управляемой CIV OCR, что
ми клеток WT и coa6Δ (рис. 2, a).
позволяет предположить, что есть некоторое
Был проведён BN ПААГ/вестерн блоттинг
восполнение OCR по сравнению с сукцинат
митохондрий, солюбилизированных 2% ным
опосредованным дыханием (рис. 3, c; см. раздел
дигитонином, чтобы выявить в образцах мито
«Обсуждение»). В присутствии 5 мкМ CCCP
хондрий нативные суперкомплексы. Интерес
значение максимальной дыхательной ёмкости
но, что аналогично данным, полученным для
митохондрий снижалось на 45% по сравнению с
стационарной экспрессии белка, наблюдалось
клетками WT (рис. 3, d). Запасная дыхательная
только частичное снижение количества
ёмкость (разница между OCR в состоянии 3 и
SC III2IV2 и III2IV1, когда использовались анти
максимальной OCR) была также значительно
тела против Cox1 и Rip1 (рис. 2, b). Это не уди
снижена в клетках cox12Δ (данные не показаны).
вительно, поскольку CIII2 может образовы
Следовательно, отсутствие правильной сбор
вать SC до того момента, когда будет полностью
ки CIV в клетках cox12Δ может серьёзно нару
сформирован CIV [29]. Однако встраивание
шить поток электронов через ETC.
Rcf2 и Cox2 в SC в клетках cox12Δ было в значи
Подавление мембранного потенциала митохон<
тельной степени снижено, в то время как воз
дрий в клетках cox12Δ. Мембранный потенци
растала ассоциация Rcf1 с SC (рис. 2, b) (см. раз
ал (Δψm) является основной силой в митохонд
дел «Обсуждение»). Далее мы провели CN ПААГ
риях, которая способствует переносу протонов
с последующим анализом активности в геле
через комплекс V, в результате чего образует
экстрактов митохондрий, солюбилизированных
ся АТФ. Чтобы выяснить, влияет ли снижение
дигитонином. В клетках cox12Δ было обнаруже
дыхания и дефекты ЭТЦ клеток cox12Δ на вели
но значительное снижение активности
чину Δψm, мы измерили Δψm в клетках WT и
C(III + IV) по сравнению с клетками WT, в то
cox12Δ, используя цианин содержащий флуо
время как объединённая активность CV (V1 + V2)
ресцентный краситель DiOC6, который на про
оставалась без изменений (рис. 2, c).
тяжении долгого времени применяется для оп
Мы также измерили специфическую актив
ределения митохондриального Δψm.
ность CIV в образцах митохондрий из клеток
Наши результаты показали, что отсутствие
WT, cox12Δ и coa6Δ. Удельная активность CIV в
Cox12 изменяет нормальное формирование по
митохондриях из клеток WT была равна
тенциала митохондриальной мембраны. Добав
148 нмоль/мин на мг белка. Лишь 18% этой ак
ление 10 мкМ CCCP рассеивало Δψm как в клет
тивности было обнаружено в митохондриях из
ках WT, так и в клетках cox12Δ (рис. 4, a). Совмест
клеток cox12Δ (рис. 2, d). В целом эти данные
ное ингибирование дыхания и Δψm может также
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
33
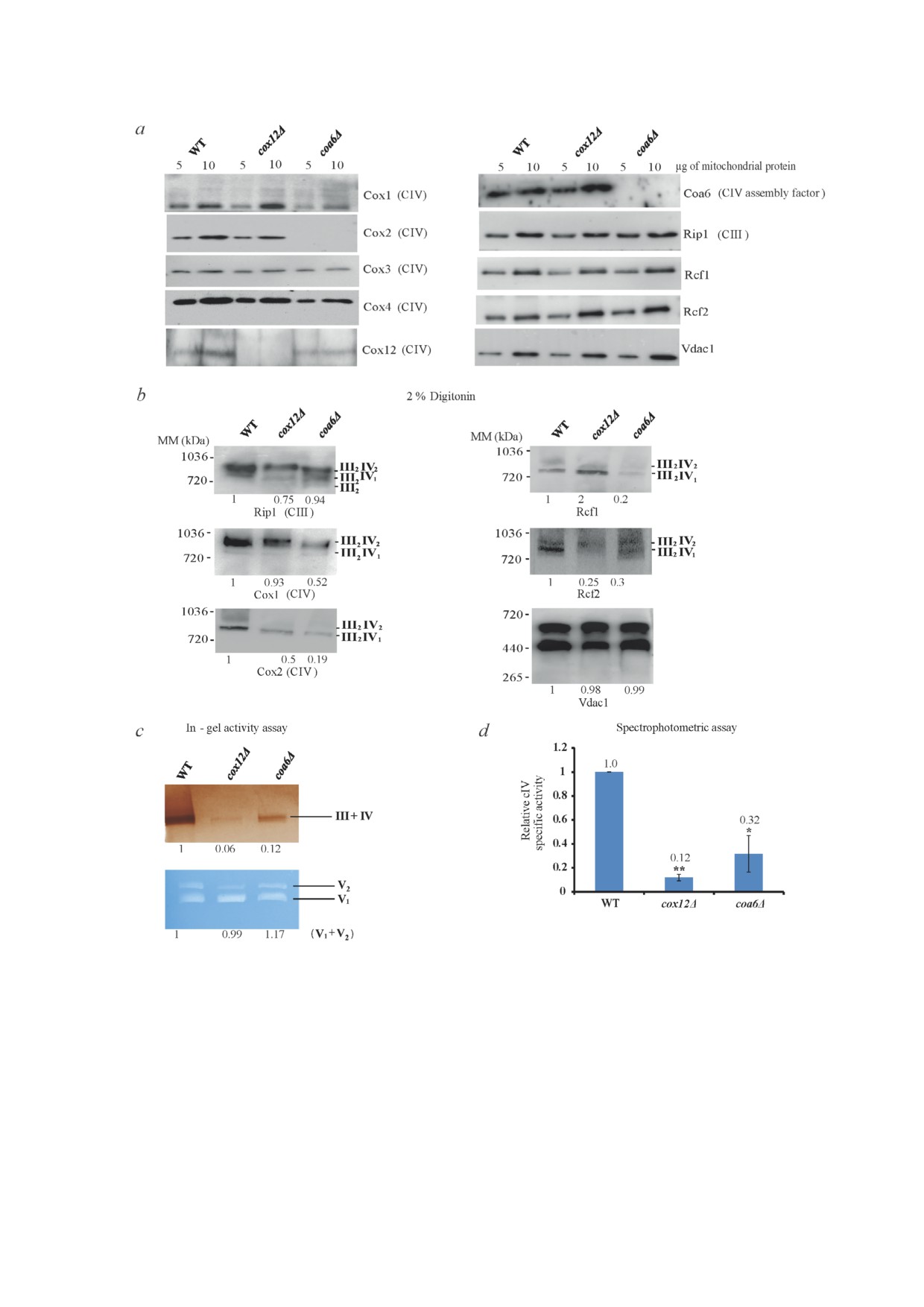
Рис. 2. Делеция Cox12 понижает активность CIV. a - SDS ПААГ/иммуноблоттинг митохондриальных лизатов из клеток
WT, cox12Δ и coa6Δ, выращенных в среде YPGal до A600 = 8. Далее 5-10 мкг белка митохондрий подвергались разделению
в 15% ном Tris глициновом геле с последующим иммуноблоттингом с использованием антител против CIII (Rip1),
CIV (Cox1-4 и Cox12), специфических субъединиц и факторов сборки (Coa6, Rcf1 и Rcf2). Vdac1 был использован в каче
стве контроля нагрузки. b - BN ПААГ/иммуноблоттинг образцов митохондрий (20 мкг белка), солюбилизированных
2% ным дигитонином и разделённых в 3-13% ном градиентном Bis Tris геле с последующим иммуноблоттингом с ис
пользованием антител против CIII, CIV и факторов сборки SC (Rcf1 и Rcf2). Vdac1 был использован в качестве контроля
нагрузки (денситометрически определённые комбинированные интенсивности полос для всех SC показаны под отдель
ными полосами). c - Окрашивание в геле активности C(III + IV) и CV содержащих SC в образцах митохондрий, солю
билизированных 2% ным дигитонином, из клеток WT, cox12Δ и coa6Δ. d - CIV специфичная активность в вышеупомяну
тых образцах митохондрий, измеренная спектрофотометрически при 550 нм. Полученные данные представлены в виде
среднего значения ± стандартная ошибка, n = 3 или более, * p < 0,05, ** p < 0,001. Все представленные результаты блот
тинга были получены при проведении по крайней мере трёх независимых экспериментов
3 БИОХИМИЯ том 87 вып. 1 2022
34
DAS и др.
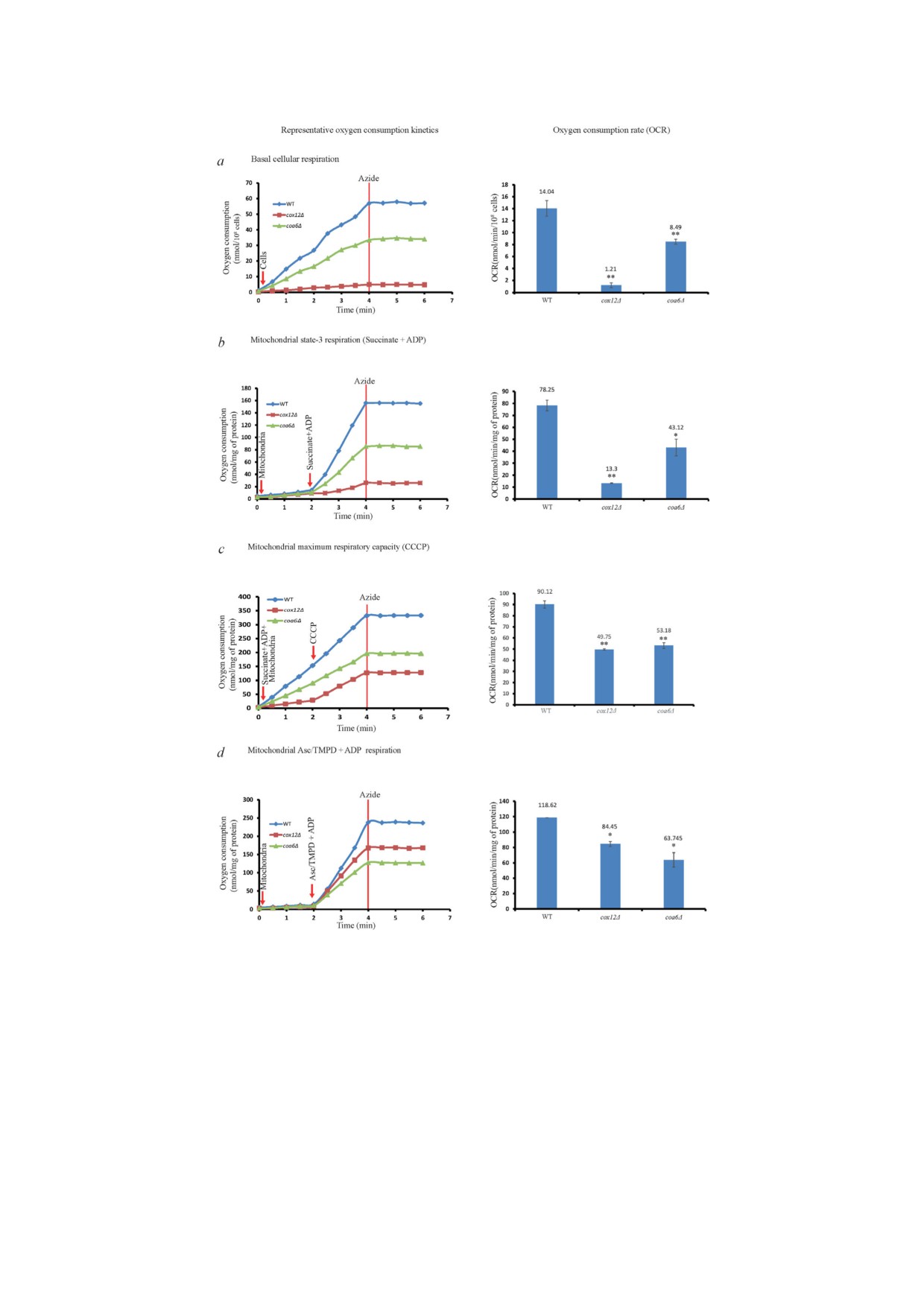
Рис. 3. Митохондриальное дыхание в клетках cox12Δ серьёзно нарушено. Левая часть рисунка - репрезентативная кине
тика потребления кислорода. Правая часть рисунка - значения OCR, рассчитанные на основании по крайней мере трёх
независимых экспериментов. Средние значения OCR определяли от 2 до 4 мин после добавления субстрата. a - Эндоген
ное дыхание клеток WT, cox12Δ и coa6Δ, измеренное при концентрации 108 клеток/мл, в среде YPGal при 30 °C с исполь
зованием электрода для определения O2. Через 4 мин для блокировки дыхания добавляли азид натрия (1 мМ) (вертикаль
ная линия). b - Кинетика потребления кислорода и OCR свежевыделенных митохондрий, измеренная в 1 мл респиратор
ного буфера, содержащего 0,6 M маннитол, 2 мМ MgCl2, 20 мМ HEPES KOH (pH 7,2), 1 мМ ЭДТА и 10 мМ K2HPO4. Уро
вень дыхания определяли в присутствии 10 мМ сукцината + 200 мкМ АДФ. c - Максимальную дыхательную ёмкость ми
тохондрий измеряли при добавлении 5 мкМ CCCP в присутствии 10 мМ сукцината + 200 мкМ АДФ при 30 °C. d - Уро
вень дыхания, измеренный с использованием 1,4 мМ TMPD/12,5 мМ аскорбата + 200 мкМ АДФ, при 30 °C при постоян
ном перемешивании. Во всех экспериментах стрелками показаны добавки, а вертикальные линии представляют добавку
азида натрия. Числа над отдельными столбиками показывают среднее значение OCR. Все результаты были получены с
помощью прибора Oxytherm, снабжённого электродом Кларка («Hansatech»). Значения OCR представлены в виде средне
го значения ± стандартная ошибка, n ≥ 3, * p < 0,05, ** p < 0,001
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
35
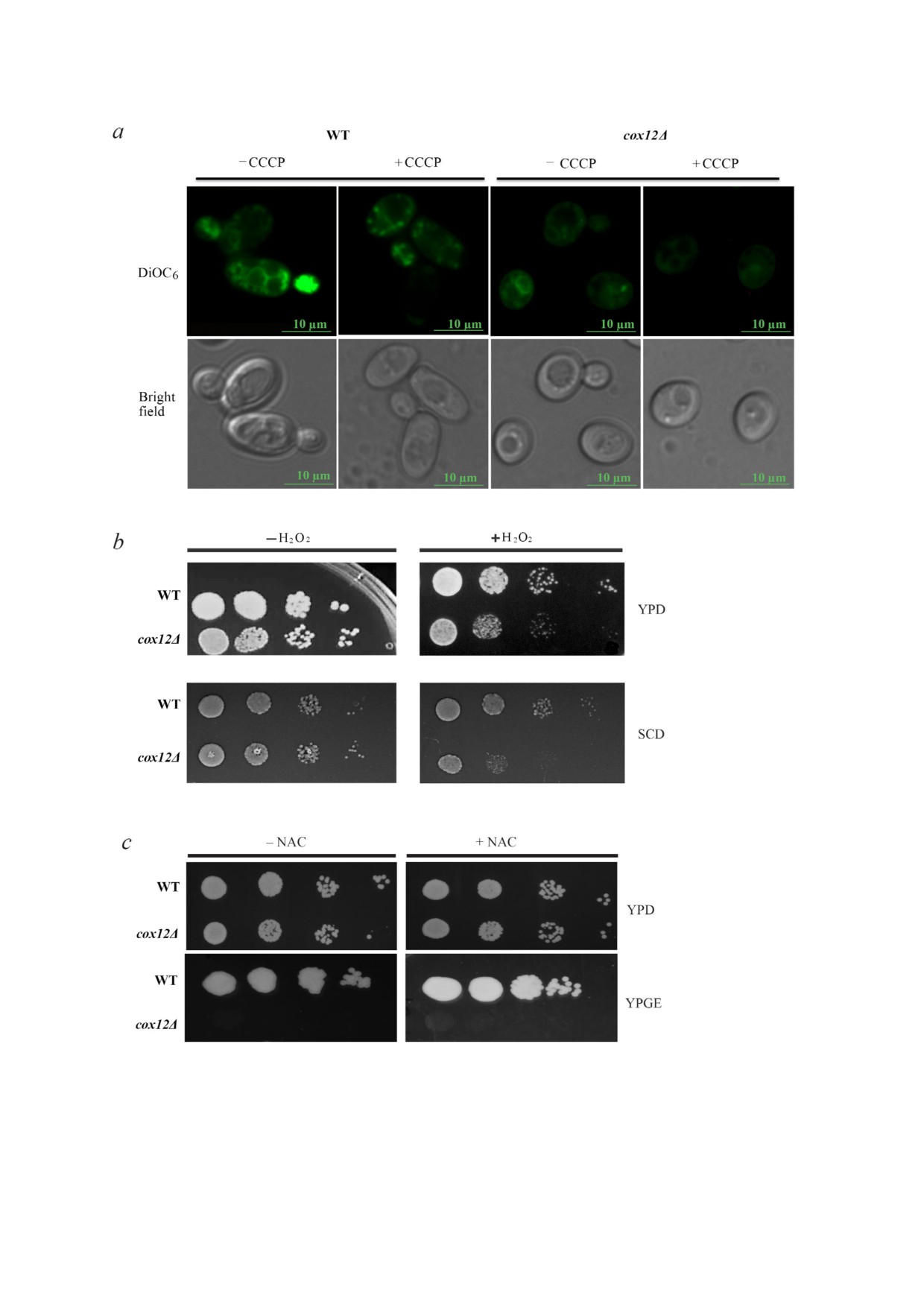
Рис. 4. Мембранный потенциал митохондрий в клетках cox12Δ был понижен. a - Клетки WT и cox12Δ, окрашенные спе
цифическим для мембранного потенциала митохондрий красителем DiOC6 (20 нг/мл). Флуоресцентные микрофотогра
фии и соответствующие фазово контрастные изображения клеток WT и cox12Δ были получены на флуоресцентном мик
роскопе («Olympus»). b - Для определения чувствительности к окислительному стрессу клетки WT и cox12Δ, обработан
ные 2,5 мМ H2O2, наносили на чашки со средами YPD и SCD. c - Аэробный рост клеток WT и cox12Δ в присутствии
25 мМ NAC в среде YPGE через 2-5 дней
БИОХИМИЯ том 87 вып. 1 2022
3*
36
DAS и др.
вызвать образование АФК [36]. Клетки, у кото
ных сайтов для каталитической субъедини
рых отсутствовал ген COX12, демонстрировали
цы Cox2. Среди них в Cox12 есть 4 консерватив
слабый рост на чашках со средами YPD и SCD в
ных а.о., которые также присутствуют в COX6B1
присутствии 2,5 мМ H2O2 (рис. 4, b), что предпо
человека (табл. 2). Однако эти остатки не взаи
лагает, что клетки cox12Δ чувствительны к окис
модействуют непосредственно с каталитичес
лительному стрессу, индуцированному H2O2.
ким центром CuA. Аминокислотные остатки Q21
Однако добавка тушителя активных форм кис
и Q23 Cox12 участвуют в формировании струк
лорода NAC (25 мМ) не привела к восстановле
турного микроокружения, которое стабилизи
нию роста клеток cox12Δ на аэробной среде
рует центр CuA Cox2 (рис. 5, c). Два других кон
YPGE (рис. 4, c).
тактных сайта предназначены для Cox1 и Cox13
Компьютерный анализ партнёров по взаимо<
соответственно. Предположительно, они ответ
действию Cox12. Чтобы получить более полное
ственны за правильное функционирование бел
представление o предполагаемой функции
ка (рис. 5, d, табл. 2). Cox12 также взаимодей
Cox12, мы выполнили in silico моделирование
ствует с C концевым участком Rcf2, располо
доступных структур SC из S. cerevisiae (PDB IDs
женным после домена белка индуцируемого ги
6T0B и 6T15) [29] для идентификации сети взаи
поксией гена (HIG) (рис. 5, e). Было показано,
модействий субъединицы Cox12. Было показа
что это взаимодействие необходимо для рекру
но, что Cox12 образует водородные связи с
тинга Cox12 в модуль Cox3 во время сборки
тремя субъединицами CIV (Cox1, Cox2 и
CIV (табл. 2) [29]. Анализ данных, полученных
Cox6a/Cox13) и одним фактором SC (Rcf2)
по SC III2IV2, показал, что сайт (K49) взаимо
(рис. 5, a-e; табл. 2), помимо уже известной
действия с Rcf2 (E199) находится внутри моти
субъединицы Cox3 [5]. Cox12 имеет 8 контакт
ва CX10C Cox12 (рис. 5, e и табл. 2). В суперком
Таблица 2. Аминокислотные остатки Cox12, взаимодействующие с другими субъединицами CIV и фактором сборки SC
Амино
кислот
Взаимодействующие
Образование
Обнаружены
ные
остатки
связей между
в суперкомплексах
Предполагаемые функции
остатки
субъединицы
цепями
Cox12
T11*
Cox2-A114
A114 с H174
III2IV1 (PDB ID: 6T15)
стабилизирует центр CuA
III2IV2 (PDB ID: 6T0B)
V12
Cox2-S112
III2IV2 (PDB ID: 6T0B)
стабилизирует центр CuA
G13
Cox2-R176
R176 с T116
III2IV1 (PDB ID: 6T15)
стабилизирует центр CuA
G13
Cox2-R176
R176 с M115 и I117
III2IV2 (PDB ID: 6T0B)
стабилизирует центр CuA
Q20
Cox2-Q206
III2IV1 (PDB ID: 6T15)
стабилизирует центр CuA
Q21*
Cox2-D108, Q206
III2IV2 (PDB ID: 6T0B)
стабилизирует центр CuA
Q21*
Cox1-R302
III2IV1 (PDB ID: 6T15)
стабилизирует микроокружение вблизи CuA и CuB
Cox2-Q206
Q23*
Cox2-L204
III2IV1 (PDB ID: 6T15)
стабилизирует центр CuA
III2IV2 (PDB ID: 6T0B)
Q29*
RCF2-R187
III2IV1 (PDB ID: 6T15)
стабилизирует COX содержащий SC
D33*
K49
RCF2-E199
III2IV2 (PDB ID: 6T0B)
стабилизирует COX содержащий SC
K53
Cox2-D132
III2IV2 (PDB ID: 6T0B)
стабилизирует центр CuA
N56
Cox2-S131
S131 с K118
III2IV1 (PDB ID: 6T15)
стабилизирует центр CuA
A57
Cox2-K118
K118 с E129 и S131
III2IV1 (PDB ID: 6T15)
стабилизирует центр CuA
A57
Cox2-S131
S131 с T116 и E129
III2IV2 (PDB ID: 6T0B)
стабилизирует центр CuA
D62
Cox2-Y122
Y122 с W124
III2IV2
(PDB ID: 6T0B)
стабилизирует центр CuA
F76*
Cox13/COX6A-Y96
III2IV2 (PDB ID: 6T0B)
стабилизирует мономерную структуру COX
Примечание. * Эволюционно консервативные а.о.
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
37
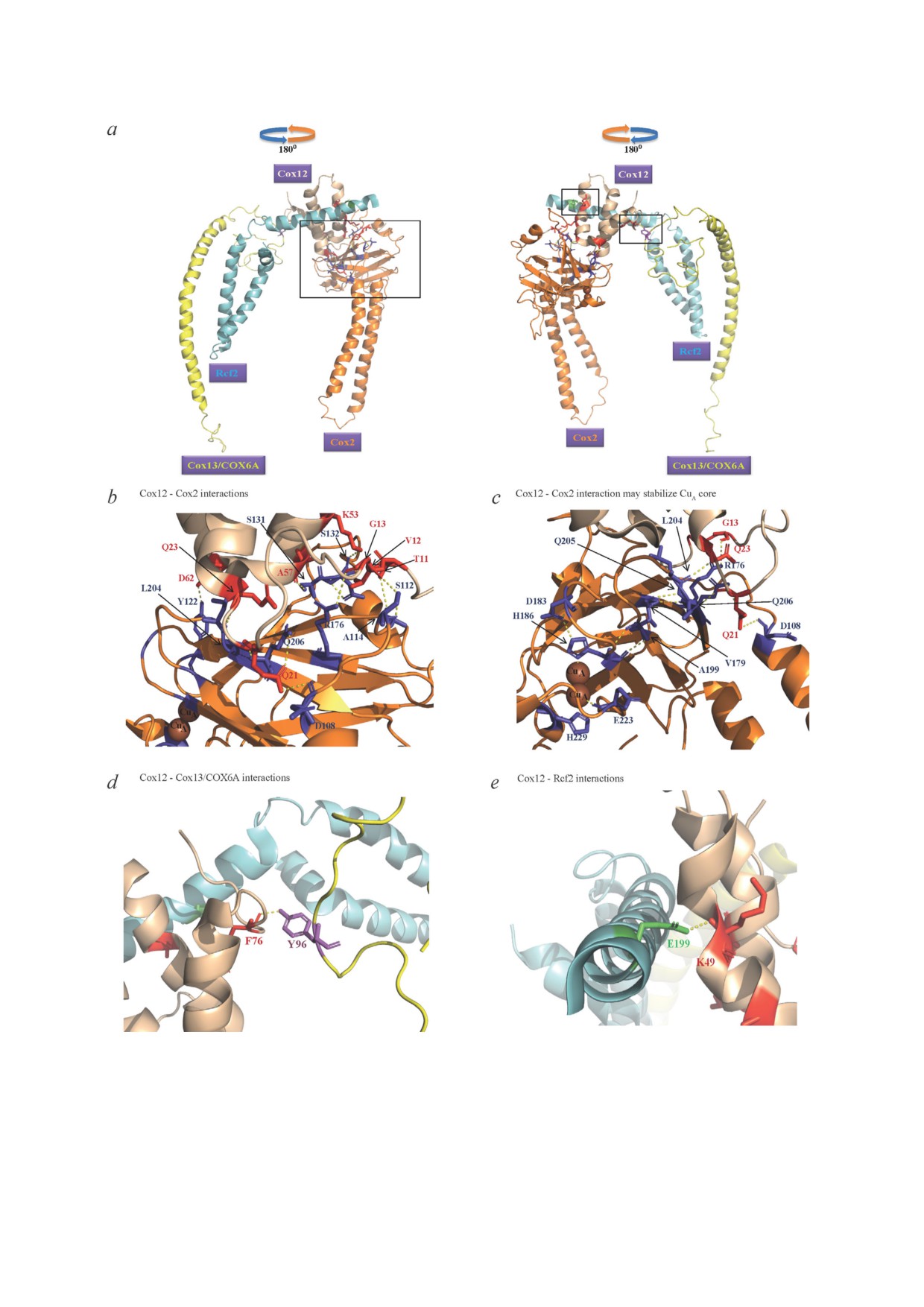
Рис. 5. Анализ in silico подтверждает, что взаимодействия Cox12 важны для функционирования CIV. a - Cox12 и 3 взаимо
действующих с ним партнёра (Cox2, Cox13 и Rcf2) смоделированы из структур крио ЭМ SC (идентификаторы PDB: 6T0B
и 6T15). Субъединицы CIV и фактор сборки суперкомплекса Rcf2 показаны различным цветом. b - Взаимодействия между
аминокислотными остатками Cox12 и Cox2 (показаны красным и фиолетовым цветом соответственно). c - Каталитичес
кий карман, образуемый между остатками Cox2 и Cox12, который может стабилизировать каталитическое микроокружение
на сайте CuA Cox2. Три а.о., окрашенных фиолетовым цветом (H186, E223, H229) являются сайтами Cox2, координируемы
ми по CuA. d-e - Взаимодействия Cox12 с Cox13 (показаны жёлтым цветом) (d) и с Rcf2 (показаны зелёным цветом) (e)
БИОХИМИЯ том 87 вып. 1 2022
38
DAS и др.
плексе III2IV сайт (Q49, D33) взаимодействия с
OCR более чем на 70% по сравнению с клетками
Rcf2 (R187) локализован внутри мотива CX9C
WT. OCR в клетках cox12Δ, экспрессирующих
Cox12 (табл. 2). В целом эти данные позволяют
Cox12, была схожа с OCR в клетках WT. OCR для
предположить, что Cox12 взаимодействует с
мутантных форм R17H и R17C была снижена
двумя каталитическими субъединицами и одной
на 56 и 30% соответственно по сравнению с
структурной субъединицей и также с одним
клетками WT (рис. 7, b и c). Кроме того, клетки
фактором SC, которые могут регулировать
cox12Δ, трансформированные пустым вектором,
функционирование CIV.
были чрезвычайно чувствительны к окислитель
Мутации R17H и R17C могут нарушить функ<
ному стрессу и не могли расти на чашках со сре
ционирование Cox12. Были сообщения о трёх му
дой SCD ( URA) после обработки H2O2. Сход
тациях двух а.о., R20 и T81, белка COX6B1чело
ная чувствительность к действию H2O2 наблю
века [18-20]. Среди этих остатков R20 консер
далась в клетках cox12Δ, трансформированных
вативен в дрожжах (R17 в Cox12 дрож
мутантами R17H и R17C. Однако экспрессия ге
жей) (рис. 1, a). Мы сконструировали два му
на COX12 дикого типа в клетках cox12Δ пол
танта, R17C и R17H (аналогично мутациям в
ностью подавляла фенотипы, чувствительные к
белках человека), в векторе pRS416 GPD и про
действию H2O2 (рис. 7, d). Следовательно, наши
тестировали их способность к восстановлению
результаты убедительно свидетельствуют о том,
аэробного роста клеток cox12Δ в дыхательной
что обе мутации, наблюдаемые у людей (R17H и
среде, содержащей глицерин и этанол. Мы об
R17C), могут быть причиной развития патогене
наружили, что оба мутанта лишь частично вос
за заболевания, уменьшая дыхание и вызывая
станавливают аэробный рост клеток cox12Δ.
окислительный стресс.
Наблюдаемая пролонгированная лаг фаза кри
вой роста клеток (рис. 6, a и b) позволяет пред
положить, что остаток R17 очень важен для
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
функционирования Cox12.
SDS ПААГ с последующим иммуноблоттин
Биогенез митохондриальной электрон
гом цитозольной и митохондриальной фракций
транспортной цепи является чрезвычайно слож
показали, что экспрессируемые в эписомах му
ным процессом, в котором задействовано более
тантные белки локализованы в митохондриях.
92 субъединиц [37]. Однако, помимо каталити
Однако мутация R17H значительно снижает
ческих субъединиц, содержащих редокс цент
стационарную митохондриальную экспрессию
ры, точная роль отдельных субъединиц остаётся
Cox12 по сравнению с клетками WT и трансфор
неясной. Это ограничивает не только наше по
мантами R17C, что может быть связано с дефек
нимание процесса образования энергии, но так
том импорта в митохондрии этого белка либо с
же является основным препятствием для прове
его пониженной стабильностью. Интересно, что
дения связи между структурными генами ЭТЦ,
мутация R17C не вызывала изменений в стацио
участвующими в развитии различных патоло
нарной экспрессии белка в митохондриях, но
гий, и их биологическими функциями. В этом
не устраняла дефект роста клеток cox12Δ
исследовании мы использовали дрожжевую мо
(рис. 6, c).
дель дефицита Cox12, чтобы установить патобио
Мутации R17H и R17C влияют на биоэнерге<
химическую и дыхательную роли этого белка.
тику митохондрий и чувствительность клеток к
Нами было показано, что делеция субъеди
окислительному стрессу. Используя BN ПААГ и
ницы CIV Cox12 приводит к заметной потере
последующий вестерн блоттинг, нами было по
дрожжевыми клетками способности к росту в
казано, что мутация R17H серьёзно нарушает
аэробных условиях (рис. 1, b-d). Гены COX12
сборку Cox12 в SC III2IV2 и III2IV1. В то же самое
дрожжей или COX6B1 человека, внедрённые в
время у мутантов R17C не наблюдалось значи
клетки cox12Δ, в полной мере восстанавливали
тельного снижения сборки SC (рис. 7, a). По
дыхательный фенотип этих клеток, подтверж
скольку антисыворотка против пептидов Cox12
дая, что белки, кодируемые этими генами, явля
не выявила Cox12 в нативных SC, мы использо
ются ортологами (рис. 1, e). Фенотипический
вали белок Cox12HA для изучения ассоциации
анализ также выявил, что мутантные формы
Cox12 с SC. Мы также измерили OCR в клетках
Cox12 (R17H и R17C) лишь частично дополня
cox12Δ, трансформированных геном COX12HA
ют функции Cox12 в клетках WT (рис. 6 и 7).
или его мутантными формами R17H и R17C с ис
При изучении причины снижения уровня
пользованием электрода Кларка для полярогра
дыхательного роста клеток cox12Δ мы обнару
фического определения O2. Как и ожидалось, в
жили, что в отличие от COX дефицитных клеток
клетках cox12Δ, трансформированных пустым
coa6Δ, стационарная экспрессия факторов
вектором, наблюдалось снижение базальной
SC (Rcf1 и Rcf2) и субъединиц CIII (Rip1) и
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
39
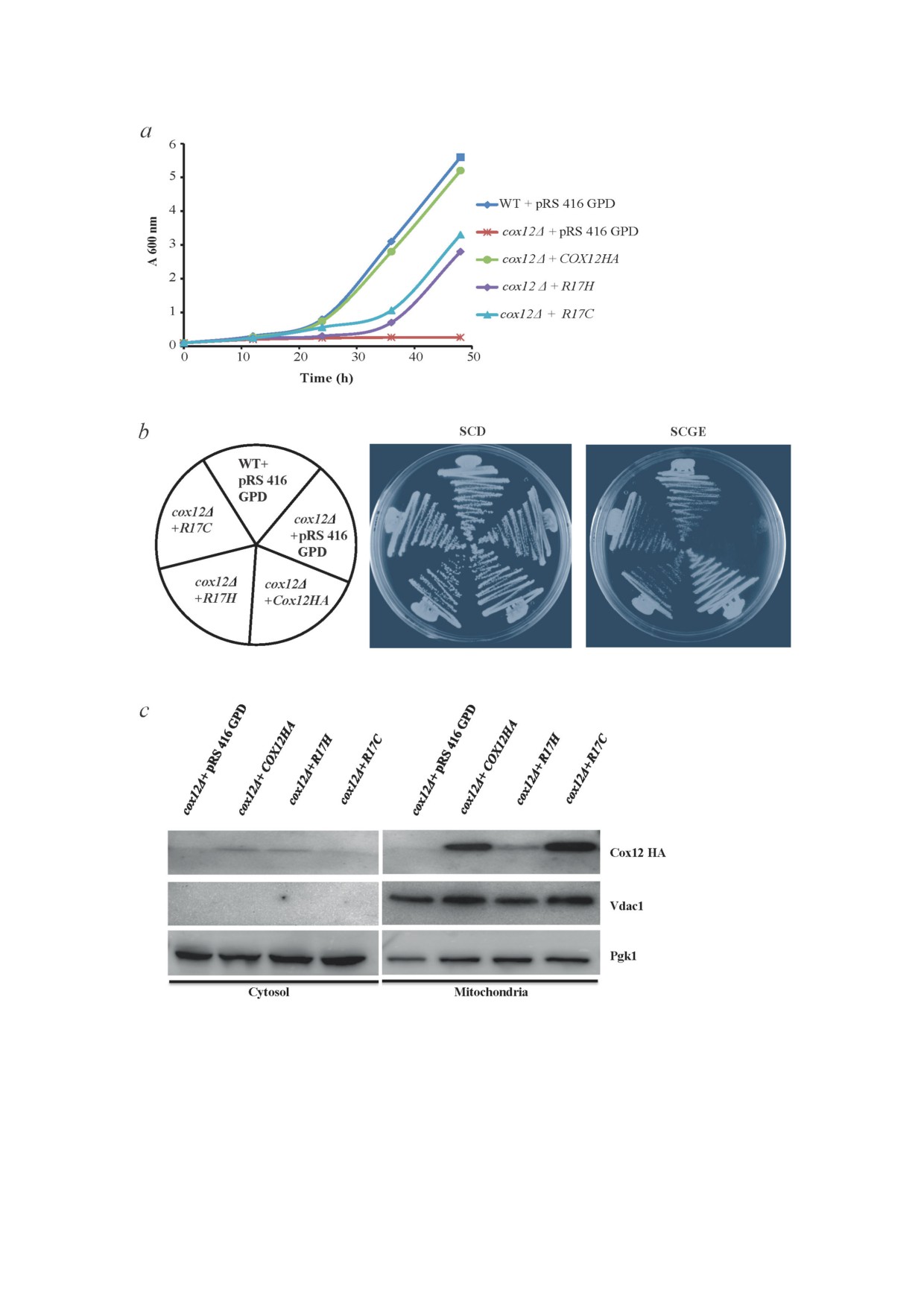
Рис. 6. Клетки cox12Δ из S. cerevisiae, экпрессирующие мутантные белки Cox12 с аминокислотными заменами R17H и
R17C, показывают замедленный аэробный рост. a - Кривые роста клеток cox12Δ, трансформированных пустым вектором
pRS416 GPD или векторами, несущими гены COX12HA, R17H или R17C. Клетки выращивали в среде SCD ( URA), затем
их инокулировали в свежую среду SCGE ( URA) до A600 = 0,1. Рост клеток при 30 °C регистрировали через обозначенные
интервалы времени. Клетки WT, трансформированные плазмидой pRS416 GPD, использовали в качестве контроля.
b - Трансформированные клетки помещали на чашки со средами SCD и SCGE и инкубировали в течение 2-5 дней перед
визуализацией. c - Иммуноблоттинг митохондриальных и цитозольных экстрактов клеток cox12Δ, трансформированных
пустым вектором, COX12HA и мутантными генами. Pgk1 и Vdac1 использовали как цитозольные и митохондриальные мар
кёры соответственно
БИОХИМИЯ том 87 вып. 1 2022
40
DAS и др.
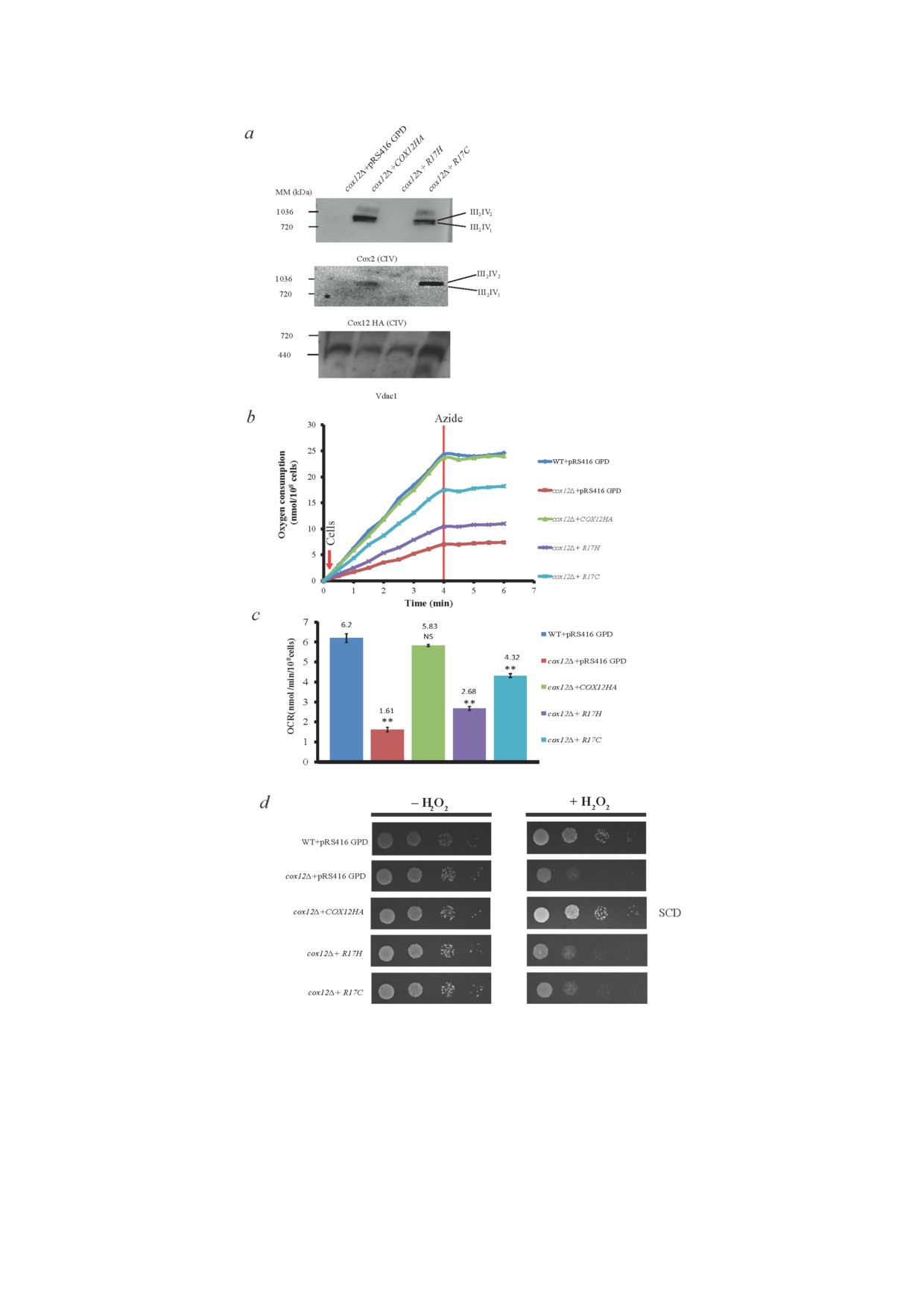
Рис. 7. Влияние мутаций R17H и R17C на митохондриальное дыхание и чувствительность клеток S. cerevisiae к окисли
тельному стрессу. a - BN ПААГ/иммуноблоттинг образцов митохондрий (20 мкг), солюбилизированных 2% ным диги
тонином и разделённых в 3-13% ном градиентном Bis Tris геле с последующим иммуноблоттингом с использованием
антител против Cox2 и Cox12HA. Vdac1 был использован в качестве контроля загрузки. b - Эндогенное клеточное дыха
ние WT + pRS416 GPD, cox12Δ + pRS416 GPD, cox12Δ + COX12HA, cox12Δ + R17H и cox12Δ + R17C, измеряемое при кон
центрации 108 клеток/мл в среде SCD ( URA) при 30 °C. Через 4 мин для блокировки дыхания добавляли азид нат
рия (1 мМ) (вертикальная линия). c - Значения OCR были рассчитаны как минимум по трём независимым эксперимен
там. d - Чувствительность к окислительному стрессу определяется обработкой вышеуказанных штаммов 2,5 мМ H2O2 и
последующим нанесением клеток на среду SCD ( URA). Изображения были получены через 2 дня роста клеток
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
41
CIV (Cox1-4) в клетках cox12Δ не отличалась от
аскорбате снижалась лишь на 29% (рис. 3, d).
клеток WT (рис. 2, a). BN ПААГ/вестерн блот
Это можно объяснить тем, что TMPD при более
тинг с использованием антител против Rip1 и
высоких концентрациях непосредственно пере
Cox1 не выявил заметного снижения количества
носит электроны на центр CuA/гем a в CIV в об
суперкомплексов III2IV2 и III2IV1 в клетках
ход цитохрома c [42]. Следовательно, возможно,
cox12Δ (рис. 2, b). Интересно, что количество
отсутствие Cox12 может вызывать дефекты в
субъединицы Cox2 в SC снижалось на 50% по
сайте стыковки цитохрома c CIV и препятство
сравнению с клетками WT. Делеция Cox12 не
вать потоку электронов от цитохрома c к цент
сказывается на синтезе и стабильности свобод
ру CuA.
ной субъединицы CIV (рис. 2, a). Следователь
Анализ с помощью программы PyMol пока
но, эти субъединицы могут образовывать непол
зал, что Cox12 располагается на противополож
ный холокомплекс CIV (без Cox12), который
ной стороне интерфейса CIV-CIII в обоих SC.
может далее связываться с CIII2 с образованием
Следовательно, отсутствие Cox12 не мешает
SC (рис. 2, b). Либо отсутствие Cox12 нарушает
формированию SC. Более того, анализ белок
включение на поздних стадиях субъедини
белковых взаимодействий показал, что Cox12
цы CIV (например, Cox2), либо стабилизация
взаимодействует с каталитическими субъедини
Cox12 в SC нарушается. В любом случае катали
цами CIV, регулирующими поток электро
тическая активность CIV в клетках cox12Δ суще
нов (рис. 5 и табл. 2). Мы обнаружили, что ос
ственно нарушена (рис. 2, c и d).
татки Q21 и Q23 в Cox12 обеспечивают стабиль
Интересно, что мы также выявили диффе
ность каталитического координационного сай
ренциальную экспрессию факторов дыхатель
та CuA через сеть непрямых взаимодействий с
ных SC (Rcf1 и Rcf2) в суперкомплексах III2IV2 и
остатками Q206 и L204 субъединицы Cox2 соот
III2IV1 клеток cox12Δ: уровень Rcf1 повышался,
ветственно (табл. 2). Эти остатки помогают ко
в то время как уровень Rcf2 был понижен
ординировать правильную ориентацию лиган
(рис. 2, b). Роль факторов Rcf1 и Rcf2 остаётся
дов CuA (H186, E223 и H229) Cox2. Было обнару
невыясненной. Было показано, что ортолог Rcf1
жено, что остаток D62, специфичный для
у человека (HIGD1A) необходим на поздних
Cox12 грибов, взаимодействовал с остатком
стадиях биогенеза CIII2 и на начальной стадии
Y122 Cox2, расположенным в непосредственной
биогенеза CIV. Человеческий ортолог
близости от одного из остатков (Y125) сайта до
Rcf2 (HIGD2A) крайне необходим на поздней
кинга цитохрома c (рис. 5, b). Cox12 также свя
стадии биогенеза CIV [38, 39]. Однако роли
зывается с Rcf2, который взаимодействует с дру
дрожжевых Rcf1 и Rcf2 в регуляции активнос
гими субъединицами CIV (Cox3 и Cox13), имею
ти CIV перекрываются [40]. Сейчас возникает
щими значение для сайта докинга цитохро
вопрос: почему уровни Rcf1 и Rcf2 изменились
ма c [29] (рис. 5, e). В целом эти данные говорят
в SC клеток cox12Δ по сравнению с клетками
о том, что Cox12 действует как «мост» между мо
WT? Может быть два ответа. Во первых, Rcf1
дулями Cox2 и Cox3. Следовательно, деле
может связываться с CIV на очень ранней ста
ция Cox12 может нарушить ассоциацию/ста
дии сборки CIV, тогда как Rcf2 участвует в при
бильность Cox2 в SC, что предотвращает фор
влечении или стабилизации Cox12 на поздней
мирование правильного кармана для связыва
стадии сборки CIV [29]. Следовательно, при от
ния цитохрома c в CIV.
сутствии Cox12 интеграция Rcf2 в SC нарушает
Дисфункции отдельных комплексов ЭТЦ и
ся. Альтернативная возможность состоит в том,
биогенеза SC часто связаны с активацией гене
что Rcf1 и Rcf2 являются положительным и от
рации АФК [43-45]. Митохондрии являются ос
рицательным модуляторами активности CIV со
новным источником образования АФК в клет
ответственно [41]. Следовательно, чтобы ком
ке [46]. Нами было показано, что отсутствие
пенсировать пониженную активность CIV в
Cox12 приводит к нарушения роста дрожжей в
клетках cox12Δ, уровень Rcf1 должен повышать
результате H2O2 индуцированного окислитель
ся, а уровень Rcf2 должен понижаться.
ного стресса (рис. 4, b) и приводит к деполяри
Анализ биоэнергетики клетки показал, что
зации митохондриальной мембраны (рис. 4, a).
потеря гена COX12 снижает базальную OCR клет
Пониженный мембранный потенциал митохон
ки на 90% и значительно снижает максимальную
дрий может вызвать запуск митофагии, что
респираторную ёмкость клеток (в присут
приводит к уменьшению числа митохондрий.
ствии CCCP) (рис. 3, a-d). Стимулируемое сук
Однако это предположение следует прове
цинатом комбинированное дыхание C(II + V)
рить [47]. Поскольку NAC не был способен вос
было затруднено на 84% по сравнению с дыха
становить дыхательный рост клеток cox12Δ
нием клеток WT (рис. 3, b). Интересно, что ды
(рис. 4, c), нарушение регуляции образования
хательная активность CIV при 1,4 мМ TMPD и
АФК может быть не единственной причиной
БИОХИМИЯ том 87 вып. 1 2022
42
DAS и др.
возникновения дефекта респираторного роста
бранный потенциал митохондрий в клетках
клеток cox12Δ.
cox12Δ, что может играть роль в возникновении
патологий, ассоциированных с дефици
В заключение, делеция гена COX12 приводит
том Cox12.
к нарушению респираторного роста клеток
дрожжей. Ортолог человека, COX6B1, может до
полнить функцию COX12 у дрожжей. Однако
Финансирование. Данная работа была под
белки Cox12 с аминокислотными заменами
держана DST SERB (ECR/2016/001127), прави
R17H и R17C (аналоги мутаций COX6B1, наблю
тельством Индии и грантами BI Калькуттского
даемые у людей) не смогли дополнить дыхатель
университета для AG; стипендией UGC JRF
ную функцию гена COX12 (рис. 6 и 7). Поскольку
(MAY2018 353734) для SM и стипендией CSIR
субъединица Cox12 встраивается лишь после
JRF (09/028 (1127)/2019 EMR I) для MB.
сборки модулей Cox1 и Cox2, мы показали, что в
Благодарности. Авторы выражают благодар
клетках cox12Δ синтезированный недостроен
ность докторам С. Мейсингеру, Мартину Отту и
ным CIV может связываться с CIII2 с образова
Винсенцо Зара за любезно предоставленные
нием суперкомплексов III2IV2 и III2IV1. Однако
ими препараты антител. Мы хотели бы выразить
эти SC ферментативно неактивны, предположи
благодарность доктору Каусику Чакраборти,
тельно, из за дестабилизации сайта докинга ци
IGIB, Индия за получение штаммов дрожжей с
тохрома c. В результате в клетках cox12Δ сукци
делециями. Мы также благодарны Д.К. Бозе и
нат стимулированная OCR митохондрий пони
Н. Сингху за техническую помощь в приготов
жена на 84%. Интересно, что добавка миллимо
лении текста настоящей статьи.
лярных концентраций TMPD/аскорбата частич
Конфликт интересов. Авторы заявляют об от
но восстанавливала потребление кислорода, ве
сутствии конфликта интересов.
роятно, за счёт усиления потока электронов че
Соблюдение этических норм. Данная статья не
рез недостроенные SC. In silico анализ белок
содержит результаты каких либо работ с участи
белковых взаимодействий показал, что Cox12
ем людей или лабораторных животных, выпол
встраивается в SC и образует контакты с Cox2 и
ненных с участием кого либо из её авторов.
Rcf2. Методом BN ПААГ было показано, что
Дополнительные материалы. Приложение к
отсутствие Cox12 затрудняет связывание Cox2 и
статье на английском языке опубликовано на
Rcf2 с суперкомплексами. Следовательно, эти
сайте журнала «Biochemistry» (Moscow) (http://
функционально дефектные недостроенные ды
protein.bio.msu.ru/biokhimiya/) и на сайте изда
хательные комплексы могут замедлять скорость
потока электронов через ЭТЦ и снижать мем
10541), том 86, вып. 12, 2021.
СПИСОК ЛИТЕРАТУРЫ
1.
Rak, M., Benit, P., Chretien, D., Bouchereau, J.,
7. Zong, S., Wu, M., Gu, J., Liu, T., Guo, R., and Yang, M.
Schiff, M., et al. (2016) Mitochondrial cytochrome c oxi
(2018) Structure of the intact
14 subunit human
dase deficiency, Clin. Sci. (Lond),
130,
393407,
cytochrome c oxidase, Cell Res.,
28,
10261034,
doi: 10.1042/CS20150707.
doi: 10.1038/s41422 018 0071 1.
2.
Soto, I. C., Fontanesi, F., Liu, J., and Barrientos, A. (2012)
8. Fornuskova, D., Stiburek, L., Wenchich, L., Vinsova, K.,
Biogenesis and assembly of eukaryotic cytochrome c oxi
Hansikova, H., et al. (2010) Novel insights into the assem
dase catalytic core, Biochim. Biophys. Acta, 1817, 883 897,
bly and function of human nuclear encoded cytochrome c
doi: 10.1016/j.bbabio.2011.09.005.
oxidase subunits 4, 5a, 6a, 7a and 7b, Biochem. J., 428,
3.
Barros, M. H., and McStay, G. P. (2020) Modular biogen
363 374, doi: 10.1042/BJ20091714.
esis
of
mitochondrial respiratory
complexes,
9. Tsukihara, T., Aoyama, H., Yamashita, E., Tomizaki, T.,
Mitochondrion, 50, 94114, doi: 10.1016/j.mito.2019.
Yamaguchi, H., et al. (1995) Structures of metal sites of
10.008.
oxidized bovine heart cytochrome c oxidase at 2.8 Å,
4.
Mukherjee, S., and Ghosh, A. (2020) Molecular mecha
Science, 269, 1069 1074, doi: 10.1126/science.7652554.
nism of mitochondrial respiratory chain assembly and its
10. Letts, J. A., Fiedorczuk, K., and Sazanov, L. A. (2016) The
relation to mitochondrial diseases, Mitochondrion, 53, 1
architecture of respiratory supercomplexes, Nature, 537,
20, doi: 10.1016/j.mito.2020.04.002.
644 648, doi: 10.1038/nature19774.
5.
Su, C. H., and Tzagoloff, A. (2017) Cox16 protein is phys
11. Timon Gomez, A., Nyvltova, E., Abriata, L. A., Vila, A. J.,
ically associated with Cox1p assembly intermediates and
Hosler, J., and Barrientos, A. (2018) Mitochondrial
with cytochrome oxidase, J. Biol. Chem., 292, 16277
cytochrome c oxidase biogenesis: recent developments,
16283, doi: 10.1074/jbc.M117.801811.
Semin. Cell Dev. Biol., 76, 163 178, doi: 10.1016/j.semcdb.
6.
Vidoni, S., Harbour, M. E., Guerrero Castillo, S.,
2017.08.055.
Signes, A., Ding, S., et al. (2017) MR 1S interacts with
12. Acin Perez, R., Fernandez Silva, P., Peleato, M. L.,
PET100 and PET117 in module based assembly of human
Perez Martos, A., and Enriquez, J. A. (2008) Respiratory
cytochrome c oxidase, Cell Rep.,
18,
17271738,
active mitochondrial supercomplexes, Mol. Cell, 32, 529
doi: 10.1016/j.celrep.2017.01.044.
539, doi: 10.1016/j.molcel.2008.10.021.
БИОХИМИЯ том 87 вып. 1 2022
Cox12 НЕОБХОДИМА ДЛЯ ФУНКЦИОНИРОВАНИЯ CIV
43
13.
Khalimonchuk, O., and Winge, D. R. (2008) Function and
27.
Ghosh, A., Pratt, A. T., Soma, S., Theriault, S. G., Griffin,
redox state of mitochondrial localized cysteine rich pro
A. T., et al. (2016) Mitochondrial disease genes COA6,
teins important in the assembly of cytochrome c oxidase,
COX6B and SCO2 have overlapping roles in COX2 biogen
Biochim. Biophys. Acta, 1783, 618 628, doi: 10.1016/
esis, Hum. Mol. Genet., 25, 660 671, doi: 10.1093/hmg/
j.bbamcr.2007.10.016.
ddv503.
14.
Kim, S. E., Mori, R., Komatsu, T., Chiba, T., Hayashi, H.,
28.
Ghosh, A., Trivedi, P. P., Timbalia, S. A., Griffin, A. T.,
et al. (2015) Upregulation of cytochrome c oxidase subunit
Rahn, J. J., et al. (2014) Copper supplementation restores
6b1 (Cox6b1) and formation of mitochondrial supercom
cytochrome c oxidase assembly defect in a mitochondrial
plexes: implication of Cox6b1 in the effect of calorie
disease model of COA6 deficiency, Hum. Mol. Genet., 23,
restriction, Age (Dordr), 37, 9787, doi: 10.1007/s11357
3596 3606, doi: 10.1093/hmg/ddu069.
015 9787 8.
29.
Hartley, A. M., Meunier, B., Pinotsis, N., and
15.
Modjtahedi, N., Tokatlidis, K., Dessen, P., and
Marechal, A. (2020) Rcf2 revealed in cryo EM structures
Kroemer, G. (2016) Mitochondrial proteins containing
of hypoxic isoforms of mature mitochondrial III IV super
coiled coil helix coiled coil helix (CHCH) domains in
complexes, Proc. Natl. Acad. Sci. USA, 117, 9329 9337,
health and disease, Trends Biochem. Sci., 41, 245 260,
doi: 10.1073/pnas.1920612117.
doi: 10.1016/j.tibs.2015.12.004.
30.
Strogolova, V., Furness, A., Robb McGrath, M.,
16.
Yang, S., Wu, P., Xiao, J., and Jiang, L.
(2019)
Garlich, J., and Stuart, R. A. (2012) Rcf1 and Rcf2, mem
Overexpression of COX6B1 protects against I/Rinduced
bers of the hypoxia induced gene 1 protein family, are crit
neuronal injury in rat hippocampal neurons, Mol. Med.
ical components of the mitochondrial cytochrome bc1
Rep., 19, 4852 4862, doi: 10.3892/mmr.2019.10144.
cytochrome c oxidase supercomplex, Mol. Cell. Biol., 32,
17.
Nie, K., Li, J., He, X., Wang, Y., Zhao, Q., et al. (2020)
1363 1373, doi: 10.1128/MCB.06369 11.
COX6B2 drives metabolic reprogramming toward oxidative
31.
Vukotic, M., Oeljeklaus, S., Wiese, S., Vogtle, F. N.,
phosphorylation to promote metastasis in pancreatic duc
Meisinger, C., et al. (2012) Rcf1 mediates cytochrome oxi
tal cancer cells, Oncogenesis, 9, 51, doi: 10.1038/s41389
dase assembly and respirasome formation, revealing het
020 0231 2.
erogeneity of the enzyme complex, Cell Metab., 15, 336
18.
Abdulhag, U. N., Soiferman, D., Schueler Furman, O.,
347, doi: 10.1016/j.cmet.2012.01.016.
Miller, C., Shaag, A., et al. (2015) Mitochondrial com
32.
Meisinger, C., Pfanner, N., and Truscott, K. N. (2006)
plex IV deficiency, caused by mutated COX6B1, is associ
Isolation of yeast mitochondria, Methods Mol. Biol., 313,
ated with encephalomyopathy, hydrocephalus and car
33 39, doi: 10.1385/1 59259 958 3:033.
diomyopathy, Eur. J. Hum. Genet.,
23,
159164,
33.
Wittig, I., Karas, M., and Schagger, H. (2007) High resolu
doi: 10.1038/ejhg.2014.85.
tion clear native electrophoresis for in gel functional assays
19.
Calvo, S. E., Compton, A. G., Hershman, S. G., Lim,
and fluorescence studies of membrane protein complexes,
S. C., Lieber, D. S., et al. (2012) Molecular diagnosis of
Mol. Cell Proteomics, 6, 1215 1225, doi: 10.1074/mcp.
infantile mitochondrial disease with targeted next genera
M700076 MCP200.
tion sequencing, Sci. Transl. Med.,
4,
118ra110,
34.
Spinazzi, M., Casarin, A., Pertegato, V., Salviati, L., and
doi: 10.1126/scitranslmed.3003310.
Angelini, C. (2012) Assessment of mitochondrial respira
20.
Massa, V., Fernandez Vizarra, E., Alshahwan, S.,
tory chain enzymatic activities on tissues and cultured
Bakhsh, E., Goffrini, P., et al. (2008) Severe infantile
cells, Nat. Protoc., 7, 1235 1246, doi: 10.1038/nprot.2012.
encephalomyopathy caused by a mutation in COX6B1, a
058.
nucleus encoded subunit of cytochrome c oxidase, Am. J.
35.
Jamar, N. H., Kritsiligkou, P., and Grant, C. M. (2017)
Hum. Genet., 82, 1281 1289, doi: 10.1016/j.ajhg.2008.
The non stop decay mRNA surveillance pathway is
05.002.
required for oxidative stress tolerance, Nucleic Acids Res.,
21.
Baertling, F., Brand, M. A. M., Hertecant, J. L., Al
45, 6881 6893, doi: 10.1093/nar/gkx306.
Shamsi, A., Heuvel, L. P., et al. (2015) Mutations in COA6
36.
Brand, M. D. (2010) The sites and topology of mitochon
cause cytochrome c oxidase deficiency and neonatal
drial superoxide production, Exp. Gerontol., 45, 466 472,
hypertrophic cardiomyopathy, Hum. Mutat., 36, 34 38,
doi: 10.1016/j.exger.2010.01.003.
doi: 10.1002/humu.22715.
37.
Chinnery, P. F., and Hudson, G. (2013) Mitochondrial
22.
Gorman, G. S., Chinnery, P. F., DiMauro, S., Hirano, M.,
genetics, Br. Med. Bull., 106, 135 159, doi: 10.1093/bmb/
Koga, Y., et al. (2016) Mitochondrial diseases, Nat. Rev.
ldt017.
Dis. Primers, 2, 16080, doi: 10.1038/nrdp.2016.80.
38.
Fernandez Vizarra, E., and Zeviani, M.
(2018)
23.
Pagliarini, D. J., Calvo, S. E., Chang, B., Sheth, S. A.,
Mitochondrial complex III Rieske Fe S protein processing
Vafai, S. B., et al. (2008) A mitochondrial protein com
and assembly, Cell Cycle, 17, 681 687, doi: 10.1080/
pendium elucidates complex I disease biology, Cell, 134,
15384101.2017.1417707.
112 123, doi: 10.1016/j.cell.2008.06.016.
39.
Timon Gomez, A., Garlich, J., Stuart, R. A., Ugalde, C.,
24.
Vondrackova, A., Vesela, K., Hansikova, H., Docekalova,
and Barrientos, A. (2020) Distinct roles of mitochondrial
D. Z., Rozsypalova, E., et al. (2012) High resolution melt
HIGD1A and HIGD2A in respiratory complex and super
ing analysis of 15 genes in 60 patients with cytochrome c
complex biogenesis, Cell Rep., 31, 107607, doi: 10.1016/
oxidase deficiency, J. Hum. Genet.,
57,
442448,
j.celrep.2020.107607.
doi: 10.1038/jhg.2012.49.
40.
Strogolova, V., Hoang, N. H., Hosler, J., and Stuart,
25.
Zhang, W., Wang, Y., Wan, J., Zhang, P., and Pei, F. (2019)
R. A. (2019) The yeast mitochondrial proteins Rcf1 and
COX6B1 relieves hypoxia/reoxygenation injury of neonatal
Rcf2 support the enzymology of the cytochrome c oxidase
rat cardiomyocytes by regulating mitochondrial function,
complex and generation of the proton motive force,
Biotechnol. Lett., 41, 59 68, doi: 10.1007/s10529 018
J. Biol. Chem., 294, 4867 4877, doi: 10.1074/jbc.RA118.
2614 4.
006888.
26.
LaMarche, A. E., Abate, M. I., Chan, S. H., and
41.
Dawitz, H., Schafer, J., Schaart, J. M., Magits, W.,
Trumpower, B. L. (1992) Isolation and characterization of
Brzezinski, P., and Ott, M. (2019) Rcf1 modulates
COX12, the nuclear gene for a previously unrecognized
cytochrome c oxidase activity especially under energy
subunit of Saccharomyces cerevisiae cytochrome c oxidase,
demanding conditions, Front. Physiol.,
10,
1555,
J. Biol. Chem., 267, 22473 22480.
doi: 10.3389/fphys.2019.01555.
БИОХИМИЯ том 87 вып. 1 2022
44
DAS и др.
42.
Hochman, J. H., Partridge, B., and Ferguson Miller, S.
45. Lopez Fabuel, I., Le Douce, J., Logan, A., James, A. M.,
(1981) An effective electron donor to cytochrome oxidase.
Bonvento, G., et al. (2016) Complex I assembly into
Purification, identification, and kinetic characterization of
supercomplexes determines differential mitochondrial
a contaminant of ruthenium red, hexaamineruthenium
ROS production in neurons and astrocytes, Proc. Natl.
II/III, J. Biol. Chem., 256, 8693 8698.
Acad. Sci. USA, 113, 13063 13068, doi: 10.1073/pnas.
43.
Diaz, F., Enriquez, J. A., and Moraes, C. T. (2012) Cells
1613701113.
lacking Rieske iron sulfur protein have a reactive oxygen
46. Dan Dunn, J., Alvarez, L. A., Zhang, X., and Soldati, T.
species associated decrease in respiratory complexes I and
(2015) Reactive oxygen species and mitochondria: a nexus
IV, Mol. Cell. Biol., 32, 415 429, doi: 10.1128/MCB.06051 11.
of cellular homeostasis, Redox Biol.,
6,
472485,
44.
Diaz, F., Fukui, H., Garcia, S., and Moraes, C. T. (2006)
doi: 10.1016/j.redox.2015.09.005.
Cytochrome c oxidase is required for the assembly/stabili
47. Knorre, D. A., and Severin, F. F. (2012) Longevity and
ty of respiratory complex I in mouse fibroblasts, Mol. Cell
mitochondrial membrane potential, Biochemistry
Biol., 26, 4872 4881, doi: 10.1128/MCB.01767 05.
(Moscow), 77, 793 794, doi: 10.1134/S0006297912070127.
MUTATIONS IN THE YEAST Cox12 SUBUNIT SEVERELY COMPROMISE
THE ACTIVITY OF THE MITOCHONDRIAL COMPLEX IV
S. Das, S. Mukherjee, M. Bedi, and A. Ghosh*
Department of Biochemistry, University of Calcutta, 35 Ballygunge Circular Road,
Pin 700019, Kolkata, India; e mail: alok.caluni@gmail.com
Cytochrome c oxidase 6B1 (COX6B1) is one of the less characterized subunits of the mitochondrial electron trans
port chain complex IV (CIV). Here, we studied the pathobiochemical and respiratory functions of Cox12 (yeast
ortholog of COX6B1) using Saccharomyces cerevisiae BY4741 (cox12Δ) cells deficient by the Cox12 protein. The
cells exhibited severe growth deficiency in the respiratory glycerol ethanol medium, which could be reverted by
complementation with the yeast COX12 or human COX6B1 genes. Cox12 with arginine 17 residue substituted by his
tidine (R17H) or cysteine (R17C) (mutations analogous to those observed in human patients) failed to complement
the loss of Cox12 function. When cox12Δ cells were grown in rich respiratory/fermentative galactose medium, no
changes in the expression of respiratory chain subunits were observed. Blue native PAGE/Western blotting analysis
using antibodies against Rip1 and Cox1, which are specific components of complexes III (CIII) and IV (CIV),
respectively, revealed no noticeable decrease in the native CIII2CIV2 and CIII2CIV1 supercomplexes (SCs).
However, the association of the respiratory SC factor 2 (Rcf2) and Cox2 subunit with the SCs in cox12Δ cells was
reduced, while the specific activity of CIV was downregulated by 90%. Both basal respiration and succinate ADP
stimulated respiration in state 3, as well as the mitochondrial membrane potential, were decreased in cox12Δ cells.
Furthermore, cox12Δ cells and cells synthesizing Cox12 mutants R17H and R17C showed higher sensitivity to the
H2O2 induced oxidative stress compared to the wild type (WT) cells. In silico structural modeling of the WT yeast
SCs revealed that Cox12 forms a network of interactions with Rcf2 and Cox2. Together, our results establish that
Cox12 is essential for the CIV activity.
Keywords: cytochrome c oxidase 6B1, Cox12, complex IV, supercomplexes
БИОХИМИЯ том 87 вып. 1 2022