БИОХИМИЯ, 2022, том 87, вып. 2, с. 216 - 229
УДК 577.352
МЕХАНИЗМ ЗАПАСАНИЯ И ТРАНСФОРМАЦИИ ЭНЕРГИИ
В МИТОХОНДРИЯХ НА МЕЖФАЗНОЙ ГРАНИЦЕ ВОДА МЕМБРАНА
Обзор
© 2022
С.В. Нестеров1,2, Е.Г. Смирнова3, Л.С. Ягужинский2,3,4*
1 НИЦ «Курчатовский институт», 123182 Москва, Россия
2 Московский физико!технический институт, 141701 Долгопрудный, Московская обл., Россия
3 НИИ физико!химической биологии им. А.Н. Белозерского, Московский государственный университет
им. М.В. Ломоносова, 119992 Москва, Россия; электронная почта: yag@genebee.msu.ru
4 НИИ цитохимии и молекулярной фармакологии, 115404 Москва, Россия
Поступила в редакцию 01.12.2021
После доработки 11.01.2022
Принята к публикации 13.01.2022
В данном аналитическом обзоре на модельных и природных системах рассмотрены разные способы гене
рации мембраносвязанных протонов, использующие различные внешние источники энергии. Анализ по
казал, что все три рассмотренных типа реакций содержат одинаковую ключевую стадию синтеза мембра
носвязанных протонов - диссоциацию электронейтральных кислот Бренстеда на межфазной границе при
переходе из гидрофобной фазы в воду с низкой диэлектрической постоянной. Особое внимание в работе
обращается на то, что на одной из анализируемых модельных систем мембраносвязанные протоны обес
печивают энергией реакцию синтеза ATP. В обзоре приводятся данные, показывающие, что аналогичный
механизм синтеза мембраносвязанных протонов в системе окислительного фосфорилирования осущест
вляется также на природных мембранах, в частности, на мембранах митопластов и митохондрий. Анализ
показал, что энергия окислительных реакций, которая обеспечивает синтез ATP, на промежуточной стадии
запасается не только в форме трансмембранного электрохимического потенциала ионов водорода, но так
же, и может быть даже в первую очередь, в форме фракции ионов водорода, лабильно связанных с поверх
ностью внутренней мембраны митохондрий. Процесс запасания энергии в митохондриях неразрывно свя
зан с переносом ионов водорода, которые одновременно исполняют две функции. Фракция ионов водоро
да на поверхности мембраны является переносчиком и носителем свободной энергии и в то же время не
посредственным субстратом (рабочим телом), обеспечивающими движение рабочих элементов сложной
биологической машины, которой является F1FO ATP синтаза.
КЛЮЧЕВЫЕ СЛОВА: мембраносвязанный протон, ион водорода, мембрана, митохондрии, окислитель
ное фосфорилирование, суперконденсатор.
DOI: 10.31857/S0320972522020063
ВВЕДЕНИЕ
свободной энергии Гиббса, то есть той энергии,
которая может быть использована для соверше
В настоящем обзоре проведён анализ дан
ния системой полезной работы. В работе на ос
ных об участии протона в начальной стадии за
нове имеющихся опубликованных эксперимен
пасания энергии в митохондриях. Акцент в об
тальных данных анализируются свойства мемб
зоре сделан на работах, выполненных ранее в
раносвязанных протонов и показывается их
нашей лаборатории, однако анализ данных осу
участие в реакциях синтеза ATP. Фракция
ществляется с учётом экспериментов других ис
мембраносвязанных протонов, согласно прове
следовательских групп. Показано, что запаса
дённому анализу, обладает свободной энергией
ние энергии в митохондриях осуществляется
в двух формах. Часть этой энергии обусловлена
путём реакции связывания ионов водорода с
локальным концентрационным потенциалом,
мембраной с образованием фракции мембра
создаваемым градиентом ионов водорода в при
носвязанных протонов, обладающих избытком
мембранном слое. Другая часть обусловлена
особенностями гидратной оболочки Н+ ионов,
образуемой в процессе их сольватации на меж
Принятые сокращения: БЛМ - бислойная липид
ная мембрана; ОКСФОС - окислительное фосфорилиро
фазной границе. Далее в тексте именно эти
вание.
компоненты энергии будут подразумеваться
* Адресат для корреспонденции.
под избытком свободной энергии фракции
216
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
217
мембраносвязанных протонов, а процессы,
лаборатории в НИИ физико химической био
приводящие к их формированию, подробно
логии им. А.Н. Белозерского, МГУ, совместно с
проанализированы.
лабораторией Института электрохимии РАН на
Как известно, П. Митчелл постулировал, что
модельной системе было показано, что энергия
первичным аккумулятором энергии окисли
ионов водорода, образующихся на межфазной
тельных реакций митохондрий является элект
границе, может быть использована ATP синта
рохимический потенциал ионов водорода, кото
зой в реакции синтеза ATP [9]. Дальнейшие ис
рый образуется при трансмембранном переносе
следования в ряде лабораторий показали, что
протонов [1]. Гипотеза Митчелла была много
связанные с мембраной ионы водорода облада
кратно экспериментально подтверждена, в част
ют высокой подвижностью и переносятся вдоль
ности, работами Skulachev et al.
[2],
мембранной границы гораздо быстрее, чем об
Liberman et al. [3] и Drachev et al. [4], которые до
мениваются с водной фазой [10-15]. Так как
казали присутствие электрического поля на
энергия мембранной фракции протонов доста
внутренней мембране митохондрий в процессе
точна для обеспечения синтеза ATP [9, 16, 17],
работы системы окислительного фосфорилиро
стадия транспорта протонов вдоль поверхности
вания (ОКСФОС). Одновременно с П. Митчел
мембраны, по видимому, включена в работу су
лом в 1961 г. Р. Вильямс предложил модель про
перкомплекса ОКСФОС, содержащего элект
тонного сопряжения, в которой начальной ста
рон транспортную систему (за исключением
дией запасания энергии является реакция пря
комплекса II) и ATP синтазу [18].
мого взаимодействия ионов водорода с полупро
Несмотря на значительный прогресс, точ
ницаемой мембраной [5]. Позднее Д. Келл
ный механизм удержания протонов на межфаз
в 1979 г. на основе модели П. Митчелла, соглас
ной границе до сих пор является предметом
но которой протон, не взаимодействуя с мемб
дискуссий [19, 20]. Первая часть настоящего
раной, пересекает её, предложил свою модель,
аналитического обзора посвящена в основном
согласно которой, напротив, протоны взаимо
описанию реакций мембраносвязанных прото
действуют с мембраной и накапливаются в не
нов на модельных системах и в митохондриях.
посредственной близости от неё. Это позволило
Во второй части дано описание реакций синте
ему объяснить наблюдаемый на алкалифильных
за ATP, протекающих с участием мембраносвя
бактериях эффект синтеза ATP при чрезвычайно
занных протонов.
низком градиенте ионов водорода [6]. Однако
следует отметить, что введение в модель Мит
челла дополнительной стадии торможения ио
ОБРАЗОВАНИЕ МЕМБРАНОСВЯЗАННЫХ
нов водорода при взаимодействии их с мембра
ПРОТОНОВ В МОДЕЛЬНЫХ СИСТЕМАХ
ной фактически трансформировало модель
Митчелла в модель Вильямса, согласно которой
В работе рассмотрены три способа синтеза
начальной стадией запасания энергии является
мембраносвязанных протонов, обладающих из
взаимодействие протона с мембраной. Важно
бытком свободной энергии, но при этом ис
указать, что в алкалифильных бактериях, соглас
пользующих разные внешние источники энер
но модели Келла, система ОКСФОС функцио
гии. Анализ показал, что все три типа реакций
нирует в полном согласии с моделью Вильямса,
протекают в одинаковых условиях - на меж
поскольку начальная стадия взаимодействия
фазной границе гидрофобной фазы с водой, то
протона с мембраной действительно контроли
есть в зоне, где вода, как известно, обладает
рует работу всей системы ОКСФОС. Интересно
сниженной диэлектрической постоянной [21].
отметить, что П. Митчелл в одной из своих позд
Во всех случаях мембраносвязанные ионы во
них работ тоже признал, что бóльшая часть про
дорода синтезируются из электронейтральных
тонов локализована в примембранных зонах и
кислот Бренстеда в процессе их диссоциации на
лишь незначительная часть протонного тока
границе раздела фаз при переходе из гидрофоб
обеспечивается протонами в объёмной фазе [7].
ной фазы в воду с низкой диэлектрической пос
Для того чтобы реализовалось прямое про
тоянной, в результате чего вновь образовавшая
тонное сопряжение по Вильямсу, ион водорода
ся гидратная оболочка протона имеет размер
должен некоторое время удерживаться на
меньший, чем в водной фазе. Первый способ -
мембране, образуя с ней лабильную связь.
перенос протона на межфазную границу в про
Впервые эффект связывания ионов водорода с
цессе К+/Н+ обмена на липидном бислое (за
поверхностью мембран был обнаружен на фо
счёт использования энергии градиента ионов
тосистемах: в работах Юнге на мембранах тила
калия). Второй способ - синтез мембраносвя
коидов (согласно [6]) и в работе Драчева и
занных протонов на межфазной границе октан
соавт. на родопсиновых бляшках [8]. В нашей
вода в условиях диссоциации кислоты Бренсте
5 БИОХИМИЯ том 87 вып. 2 2022
218
НЕСТЕРОВ и др.
да; регистрация синтеза ATP за счёт избытка
градиент ионов калия [26]. Полная схема пере
свободной энергии ионов водорода, связанных
носа протона через мембрану с помощью ниге
с межфазной границей. Третий способ - обра
рицина при наличии градиента ионов калия
зование мембраносвязанных протонов (сaged
представлена на рис. 1. На рисунке также пока
H+) в результате гидролиза электрофильных со
зано, что в этих условиях образуются две фрак
единений на гидрофобной поверхности на гра
ции ионов водорода - фракция мембраносвя
нице раздела. Все эти способы более подробно
занных протонов на поверхности липидного
будут рассмотрены далее.
бислоя и, как отмечалось выше, фракция ионов
Анализ показал, что во всех трёх случаях,
водорода в так называемом неперемешиваемом
независимо от источников энергии и природы
слое воды. Толщина неперемешиваемого слоя
исходной химической реакции, терминальная
водной фазы порядка 100 мкм, и его необходи
стадия синтеза энергизованных мембраносвя
мо отличать от межфазной границы вода мемб
занных протонов протекает по одинаковому
рана, где находятся мембраносвязанные прото
механизму, и энергия запасается в форме фрак
ны, и толщина которой составляет всего нес
ции энергизованных протонов. Энергия этой
колько ангстрем. При К+/Н+ обмене закисле
фракции распределена между мембраносвязан
ние неперемешиваемого слоя происходит в ре
ными ионами водорода и мембраной.
зультате протекания непрерывного процесса
Для регистрации и измерения величины
отрыва мембраносвязанных ионов водорода от
граничных потенциалов на мембране при обра
«cis» поверхности БЛМ.
зовании фракции мембраносвязанных ионов
На рис. 1 показано, что фракция мембрано
водорода наиболее часто используют метод
связанных протонов возникает и существует как
компенсации внутримембранного поля [22] и
стационарное состояние системы. При этом
метод регистрации изменений поверхностного
роль источника энергии выполняет градиент
заряда (ζ потенциала) [23, 24]. В последнем
ионов К+. Объём этой фракции определяется
случае часто используется прибор Malvern
соотношением скоростей подачи и отрыва Н+
Zetasizer, который сочетает метод электрофоре
ионов на «cis» поверхности БЛМ. Фракция
за в переменном электрическом поле с регист
мембраносвязанных протонов является стацио
рацией скорости движения объекта [23]. Выше
нарной (но неравновесной) энергозависимой
указанные методы дают различающиеся вели
структурой, возникающей в системе «БЛМ/ни
чины потенциалов, однако из ζ потенциала мо
герицин/градиент К+». Таким образом, весь
жет быть рассчитан граничный потенциал по
объём фракции мембраносвязанных протонов,
модели Гуи-Чепмена с учётом того, что рассто
пока существует градиент ионов калия, непре
яние от поверхности мембраны до плоскости
рывно обновляется. При этом в результате от
скольжения для липидных мембран составляет
рыва мембраносвязанных протонов от поверх
около 0,2 нм [25].
ности мембраны поддерживается низкое значе
Генерация мембраносвязанных протонов на
ние рН в неперемешиваемом водном слое. Пов
искусственных бислойных липидных мембранах
торная гидратация протонов на «cis» стороне
(БЛМ) с использованием градиента ионов калия.
мембраны происходит в гидрофобной фазе при
С помощью метода регистрации внутримемб
мембранного слоя с низкой диэлектрической
ранного поля было впервые зарегистрировано
постоянной [21]. При этом формируется новая
образование фракции мембраносвязанных про
гидратная оболочка меньших размеров. Свой
тонов на БЛМ из фосфолипидов [26]. Для наг
ства воды на заряженных межфазных границах
лядной демонстрации этих ключевых экспери
описаны в работе Gonella et al. [27]. Фракция
ментов на БЛМ они будут подробно описаны
мембраносвязанных протонов, образовавшаяся
далее и схематично проиллюстрированы на
в результате переноса нигерицин Н+ через
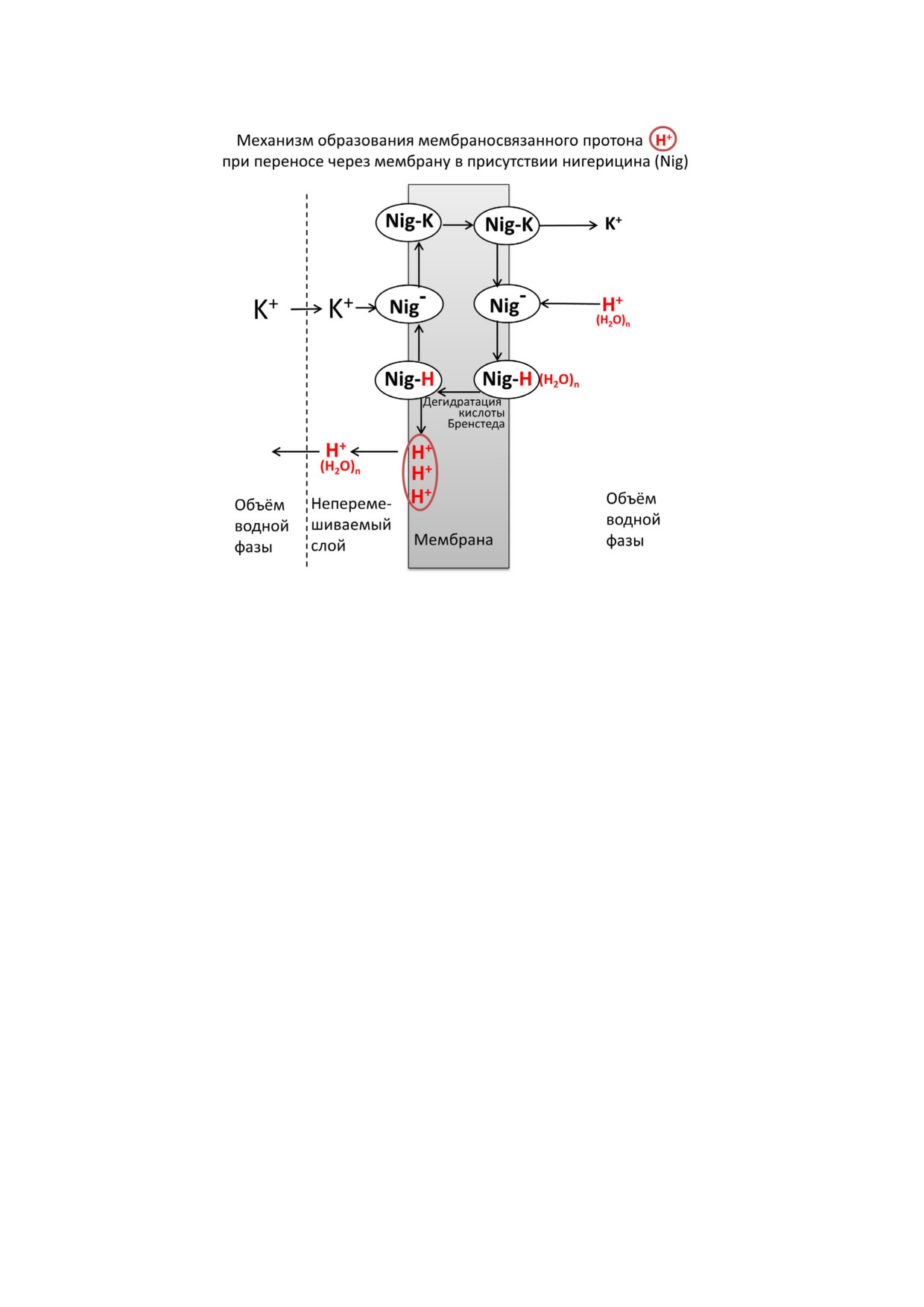
рис. 1 и 2. Эффект генерации фракции мембра
мембрану, на рис. 1 обведена красным овалом.
носвязанных протонов был зарегистрирован в
Для измерения закисления в неперемеши
условиях индукции К+/Н+ обмена на БЛМ. Для
ваемом слое у поверхности БЛМ был использо
этого был использован электронейтральный
ван разработанный метод [28], который позво
К+/Н+ обменник, нигерицин, со стехиометри
лил проводить регистрацию быстрых измене
ей 1 : 1. В молекуле нигерицина роль перенос
ний pH. В систему добавлялся разобщи
чика протона выполняет протонированная кар
тель (протонофор), который трансформировал
боксильная группа, диссоциация которой про
локальный градиент pH на БЛМ в электрохи
исходит на межфазной границе с образованием
мический потенциал ионов водорода, который
мембраносвязанного протона. В качестве ис
уже может быстро измеряться потенциометри
точника энергии для индукции потока ионов
ческим методом. Результаты таких измерений
водорода через мембрану был создан высокий
приведены на рис. 2. На рис. 2, б приведены
БИОХИМИЯ том 87 вып. 2 2022
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
219
Рис. 1. Схема генерации фракции мембраносвязанных протонов на БЛМ на межфазной границе при K+/H+ обмене на
нигерицине. Неравновесно связанные с мембраной протоны имеют изменённую гидратную оболочку (то есть в среднем
отличающуюся от таковой в объёме) и обладают избытком свободной энергии. На рисунке фракция этих протонов об
ведена красным овалом
кривые изменения потенциала, происходящие
тонов из неперемешиваемого слоя с помощью
при изменении активности H+ в примембран
ацетата позволило отдельно исследовать фрак
ном слое в присутствии разобщителя.
цию мембраносвязанных протонов, которая не
Такой подход позволил также отделить про
взаимодействует с ацетатом.
цесс закисления в примембранном слое от про
Важно указать ещё раз, что эффект образо
цессов на межфазной границе. Образующийся
вания мембраносвязанных протонов, представ
избыток протонов в неперемешиваемом вод
ленный на рис. 2, был получен в присутствии
ном слое препятствовал прямой регистрации
разобщителя. Этот результат показал, что ра
фракции мембраносвязанных протонов и ис
зобщитель в обычно используемых концентра
следованию её свойств. Для регистрации вклада
циях (1-10 мкМ) не рассеивает энергию мемб
фракции мембраносвязанных протонов в гра
раносвязанных протонов. Для взаимодействия
ничный потенциал на БЛМ закисление в непе
с этой фракцией протонов были синтезированы
ремешиваемом слое необходимо было устра
специальные поверхностно активные разоб
нить. Это было достигнуто за счёт создания
щители (более подробно эти соединения об
противоположно направленного потока прото
суждались в обзоре Eremeev и Yaguzhinsky [30]).
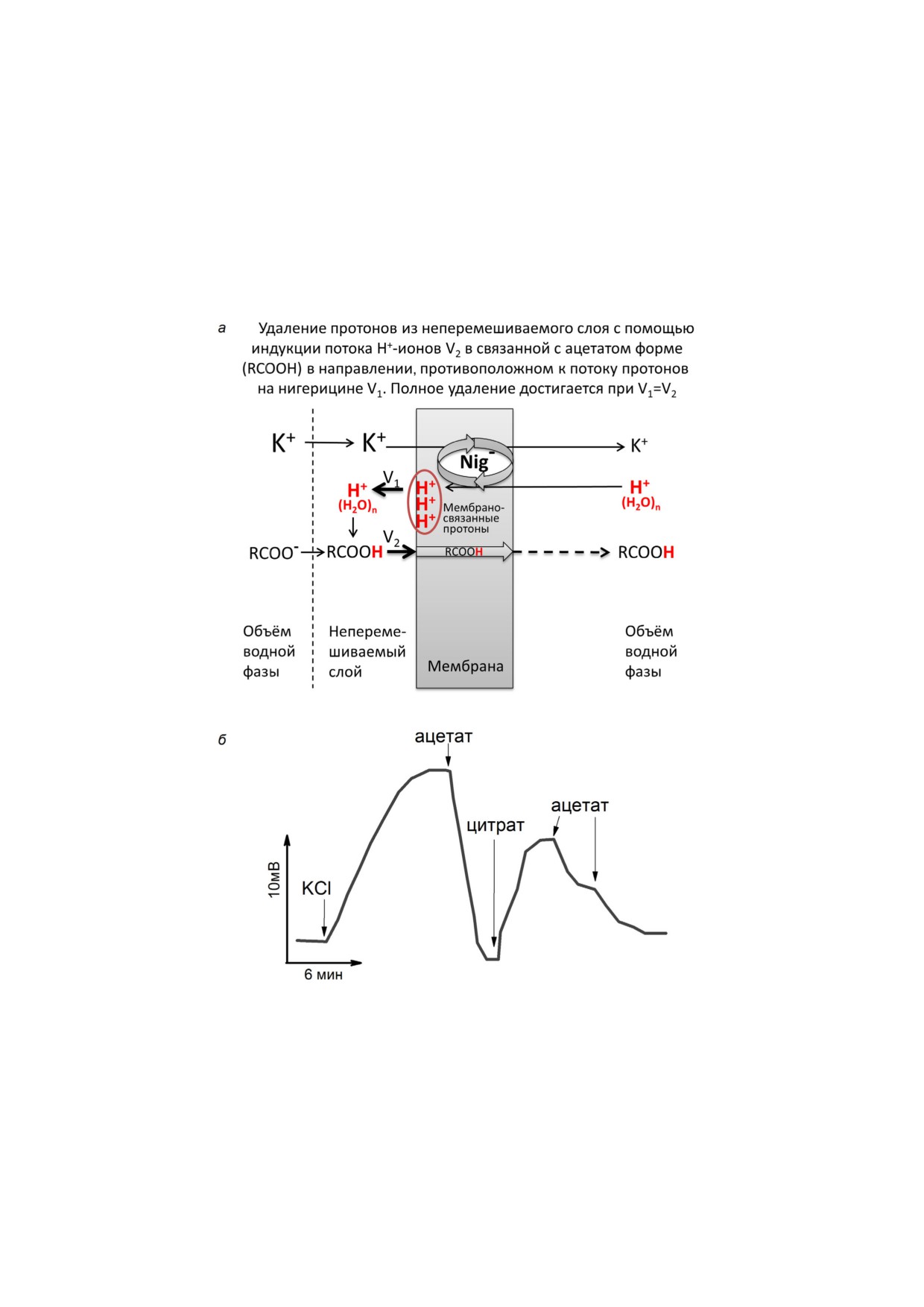
нов через мембрану на ацетате (рис. 2, а) [29].
Катализ реакции отрыва протона от поверх
Как показали эксперименты, отрицательно за
ности мембраны. Как было показано в работе
ряженный ацетат анион, как и разобщители, не
Antonenko et al. [26], в присутствии нигерицина
способен взаимодействовать с мембраносвя
и градиента К+ на БЛМ формируется фракция
занными протонами. Однако при этом ацетат
мембранных протонов, которая может быть
связывается с протонами в неперемешиваемом
удалена с поверхности добавлением слабых ос
слое, после чего в нейтральной форме перехо
нований Льюиса (в концентрации поряд
дит вместе с захваченным протоном через меж
ка 10 мМ). Поскольку слабые основания, как
фазную границу на другую сторону мембраны
известно, обладают буферными свойствами,
(рис. 2). Избирательное удаление избытка про
подобные эффекты многие авторы объясняют
БИОХИМИЯ том 87 вып. 2 2022
5*
220
НЕСТЕРОВ и др.
действием этих веществ в качестве буферов.
та, напротив, резко увеличивает градиент рН
Согласно такому объяснению, следовало ожи
(только в условиях K+/H+ обмена), что свиде
дать, что добавление буферов в систему, пред
тельствует об ускорении реакции отрыва мемб
ставленную на рис. 1, будет уменьшать скачок
раносвязанного протона от поверхности би
рН в примембранном слое при K+/H+ обмене.
слоя. Это полностью противоречит ожидаемо
Однако, как показал эксперимент, добавление в
му буферному эффекту цитрата, который дол
систему, представленную на рис. 2, б, слабого
жен проявляться как снижение градиента pH.
основания Льюиса (цитрата) вызывает прямо
Необходимо отметить, что при повышении
противоположный эффект. Добавление цитра
концентраций оснований Льюиса иногда мож
Рис. 2. Метод встречных потоков протонов. а - Схема удаления (путём титрования ацетатом) локального градиента pH,
возникающего в неперемешиваемом слое при переносе протонов через мембрану на нигерицине (Nig), с помощью соз
дания противоположно направленного потока протонов. б - Пример использования потенциометрического метода для
регистрации изменений pH в примембранном слое БЛМ в процессе его удаления нарастающими концентрациями аце
тата. Величина ΔpH пропорциональна величине мембранного потенциала, возникающего на мембране в присутствии
разобщителя (см. выше). Величина первой добавки ацетата, полностью снимающей градиент pH, определена путём тит
рования в предварительных экспериментах. После удаления «первичного» градиента pH в примембранном слое добавка
катализатора отрыва протона (цитрата) повторно создаёт рН градиент в примембранном слое БЛМ за счёт увеличения
скорости V1. Полное удаление вновь появившегося градиента pH достигается с помощью титрования небольшими пор
циями ацетата. Рисунок построен по данным работы [31]
БИОХИМИЯ том 87 вып. 2 2022
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
221
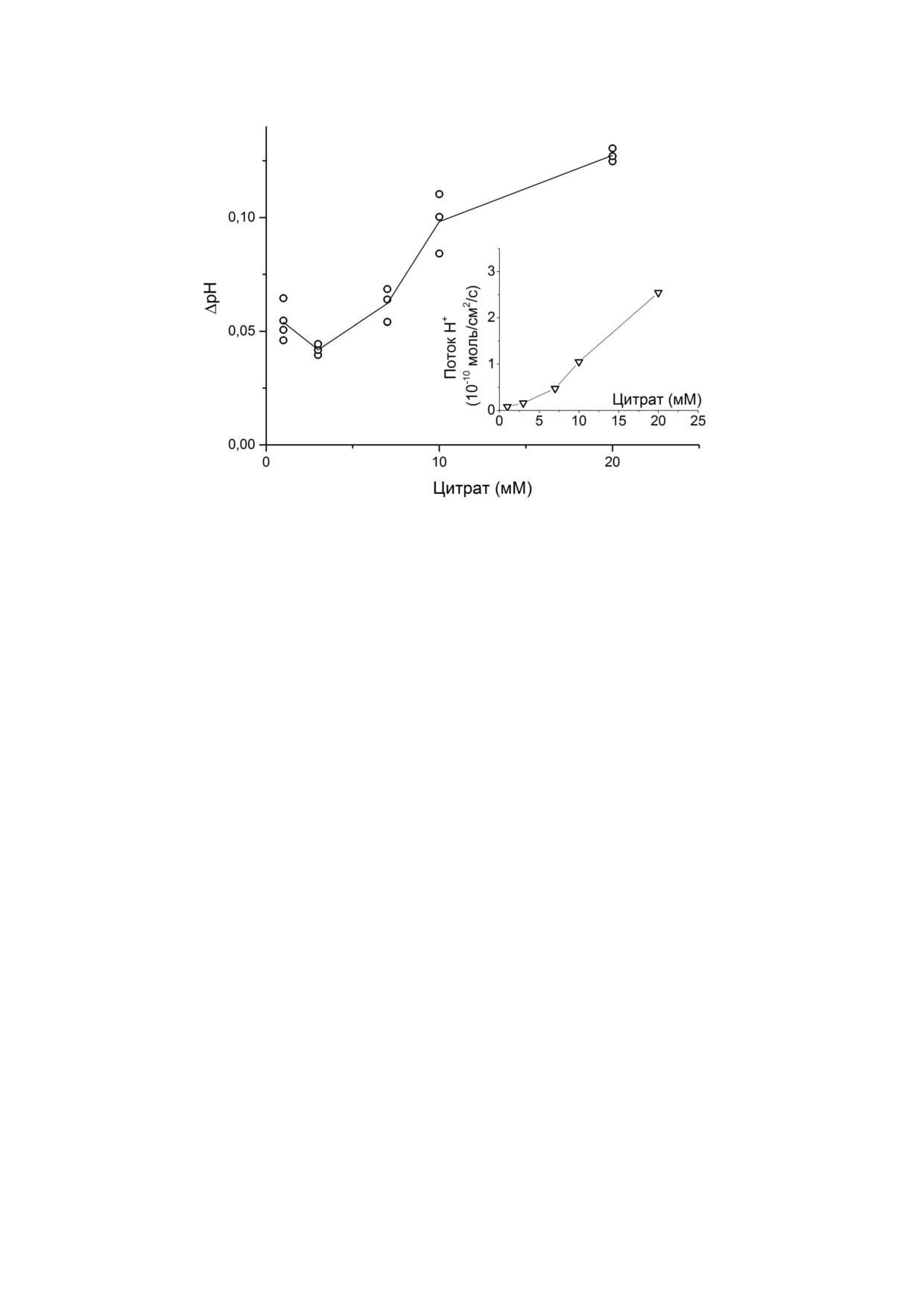
Рис. 3. Прямая регистрация с помощью pH микроэлектрода изменений pH в примембранном слое БЛМ при нарастаю
щей скорости отрыва мембранных протонов (прямое доказательство увеличения скорости отрыва мембранных протонов
под действием катализатора - слабого основания Льюиса). Измерения проводились в условиях генерации мембранных
протонов на «cis» стороне БЛМ в присутствии нигерицина и градиента ионов K+. Ускорение отрыва протонов с «cis»
стороны БЛМ достигалось за счёт увеличения концентрации катализатора отрыва протонов - цитрата. На вставке - воз
растание величины потока H+ ионов через мембрану (10-10 моль/см2/с) при увеличении концентрации цитрата. Рисунок
взят из работы [32] (с разрешения издательства Wiley)
но также наблюдать их слабый буферный эф
Синтез мембраносвязанных протонов в реак
фект. Таким образом, удаление градиента рН в
ции гидролиза электрофильных соединений
примембранном слое [26] позволило показать
(сaged H+) в зоне межфазной границы мембрана
присутствие граничного потенциала на БЛМ в
вода. Генерацию мембраносвязанных протонов
условиях К+/Н+ обмена и независимо доказать
можно осуществить за счёт высвобождения
каталитический механизм реакции отрыва ио
сильной кислоты при гидролизе caged H+ на
нов водорода от поверхности мембраны.
межфазной границе. Сaged H+ принято назы
Данные работы Evtodienko et al. [32] (рис. 3),
вать соединения, относящиеся к классу элект
в которой при помощи микроэлектрода было
рофильных веществ (например, эфиров суль
проведено прямое измерение рН в примемб
фокислот или галоидалкиламинов), которые на
ранном слое БЛМ, также показали, что слабые
поверхности мембран митохондрий и БЛМ мо
основания не только не снижают градиент рН,
гут гидролизоваться с выделением сильных Н+
но резко повышают концентрацию ионов водо
кислот. Высвобождающиеся при этом протоны,
рода в примембранном слое. В этой работе так
как и в случае трансмембранного переноса, ка
же была измерена скорость трансмембранного
кое то время удерживаются на межфазной гра
потока ионов водорода, которая увеличивалась
нице мембрана вода. Этот подход был реализо
при добавлении цитрата (вставка на рис. 3), что
ван в нашей лаборатории в начале 80 х гг.
явно свидетельствует не о буферном, а о катали
прошлого века с использованием электрофиль
тическом эффекте слабых оснований. Таким
ных соединений ряда β галоидалкиламинов,
образом, было надёжно зарегистрировано на
обладающих спонтанной реакционной способ
личие каталитической активности слабых осно
ностью, гидролиз которых эффективно проис
ваний Льюиса в реакции отрыва протона от
ходит на межфазной границе мембрана во
мембраны. Это является прямым доказатель
да [33]. В результате было показано, что генера
ством существования неравновесной фракции
ция избытка протонов на поверхности внутрен
связанных с мембраной протонов, которая в
ней мембраны митохондрий блокирует работу
форме граничного потенциала запасает энер
всех трёх протонных помп за счёт резкого повы
гию градиента ионов калия.
шения локальной активности ионов водорода.
БИОХИМИЯ том 87 вып. 2 2022
222
НЕСТЕРОВ и др.
Важность этих результатов в том, что они полу
бот, такая высокая энергия отрыва протонов от
чены на митохондриях. При этом очевидно, что
поверхности мембраны связана с необходи
мембраносвязанные протоны стабилизированы
мостью перестройки цепочек водородных свя
на поверхности митохондриальных мембран и
зей в больших кластерах молекул воды при уда
не подвергаются избыточной гидратации и от
лении протона с межфазной границы [15].
щеплению от мембраны митохондрий. Эти ре
О роли молекул воды в связывании протонов с
зультаты хорошо согласуются с более поздними
поверхностью искусственных мембран. С целью
работами на модельных мембранах, в том числе
выяснения участия молекул воды в образова
с теми, в которых был реализован более удоб
нии связи протонов с поверхностью мембран
ный и контролируемый вариант caged H+, в ко
были проведены эксперименты с использова
торых реакция освобождения ионов водорода
нием тяжёлой воды. В экспериментах на БЛМ с
индуцируется ультрафиолетовым (УФ) излуче
нигерицином, где скорость реакции отрыва
нием [34]. Результаты, полностью согласующие
мембраносвязанных протонов от поверхности
ся с выводами работ на БЛМ с нигерицином,
мембраны лимитировала скорость переноса
описанными выше, были независимо подтверж
протонов в объём водной фазы, было обнаруже
дены при генерации мембраносвязанных про
но, что в тяжёлой воде скорость потока прото
тонов с помощью высвобождения caged H+
нов через мембрану снижается [31]. При малых
(возбуждения УФ излучением молекул 2 ме
концентрациях катализатора отрыва прото
токси 5 нитрофенилсульфата) [22]. Во всех
нов (цитрата) изотопный эффект при заме
случаях регистрировалось образование фрак
не H2O на D2O составлял лишь 30%. Однако
ции мембраносвязанных протонов, которая ка
при высоких каталитических концентраци
талитически удалялась с поверхности мембра
ях (20-100 мМ) наблюдался очень высокий
ны слабыми основаниями Льюиса.
изотопный эффект, который достигал бо
Особенно необходимо отметить экспери
лее 400% [31]. Вышеприведённые результаты с
ментальные исследования кинетики диффузии
нигерицином находятся в согласии с экспери
протона вдоль плоской бислойной мембраны,
ментами на родопсине и цитохром с оксидазе, в
проведённые П. Полем и Ю. Антоненко с соавт.,
которых присутствовали высокие концентра
с использованием УФ активируемых caged
ции катализаторов отрыва протона. Лимитиру
H+ [35]. Связанные с мембраной caged H+ выс
ющая стадия отрыва протона от фермента в
вобождали с помощью УФ вспышек, и отсле
водную фазу [37] при замене H2O на D2O как в
живали их диффузию на различное расстояние
родопсине [38], так и в цитохром с оксида
в отдалённые области мембраны, которая реги
зе [39, 40] замедляется более чем в пять раз.
стрировалась по флуоресценции встроенного в
Наблюдаемые эффекты D2O однозначно указы
мембрану pH зонда. В результате удалось пока
вает на участие молекул воды в связывании ио
зать высокую подвижность протона на поверх
нов водорода с межфазной границей (вода ли
ности (одного порядка, но меньшую, чем в объ
пид или вода белок). Таким образом, было по
ёмной фазе дистиллированной воды), а также
казано, что эффективность катализатора по ус
то, что расстояние, преодолеваемое протоном
корению процесса переноса иона водорода от
вдоль поверхности, снижается при увеличении
поверхности границы раздела в объём водной
концентрации мобильных pH буферов (катали
фазы гораздо ниже в D2O по сравнению с Н2О.
заторов отрыва протонов) [35]. Исследование
Снижение скорости реакции отрыва прото
химически различных бислойных мембран поз
на в тяжёлой воде лимитировано свойствами
волило также показать, что быстрая диффузия
кластера тяжёлой воды, который определяет
протонов по поверхности происходит за счёт
прочность связи иона водорода с межфазной
движения протона по молекулам воды по меха
границей и его способность взаимодействовать
низму Гроттгуса [36], а не за счёт скачков между
с молекулой катализатора. Это предположение
закреплёнными на мембране участками связы
хорошо согласуется с результатами работы в мо
вания протонов (иммобилизованными pH бу
дельной системе межфазной границы n декана
ферами), как предполагалось до этого в ряде ра
с водой [41], где показали возможность удержа
бот (см. ссылки в [36]).
ния ионов водорода на межфазной границе и
Эксперименты по исследованию кинетики
снижение подвижности ионов водорода в тяжё
движения мембраносвязанных протонов позво
лой воде. Вывод об участии молекул воды в
лили также оценить энергию активации отрыва
удержании протонов на мембране также делает
протона от поверхности мембраны в водную фа
ся в работе по изучению латерального переноса
зу для различных липидов и показать, что она на
протона вдоль мембран [36].
порядок превышает тепловую энергию [15, 36].
Участие мембраносвязанных протонов в синте
Суммарно, согласно выводам авторов этих ра
зе ATP в модельной системе. Ещё в середине 70 х гг.
БИОХИМИЯ том 87 вып. 2 2022
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
223
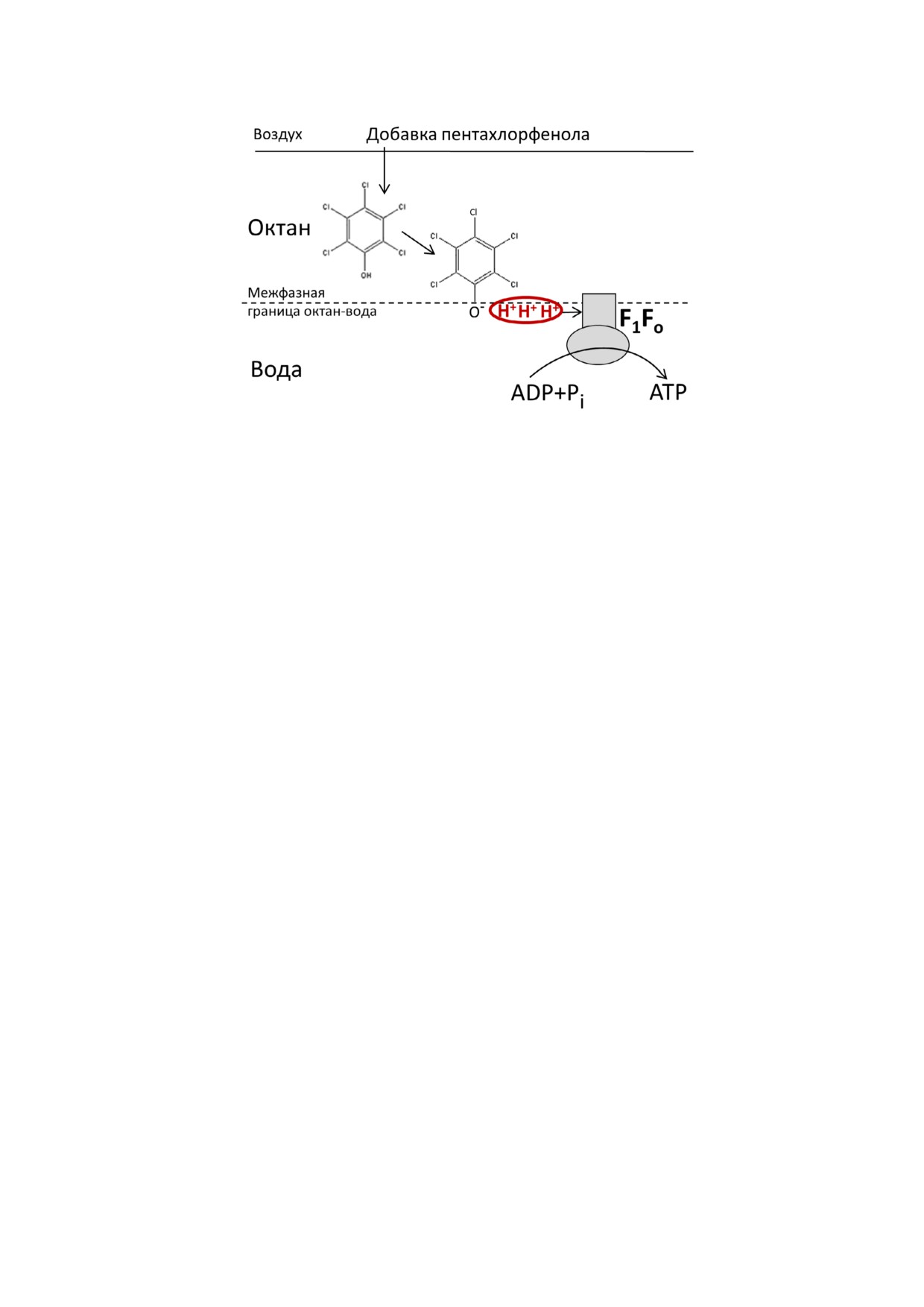
Рис. 4. Схема эксперимента по синтезу ATP на межфазной границе октан вода. Источником ионов водорода на межфаз
ной границе служила кислота Бренстеда (пентахлорфенол). Высвобождение протонов происходило при диссоциации
пентахлорфенола в момент контакта с водой. Синтез ATP наблюдался при отсутствии окислительных реакций и при от
сутствии трансмембранного потенциала
прошлого века в нашей лаборатории были по
связанных протонов, которые переносятся
ставлены эксперименты, в которых для синте
вдоль поверхности липосомальной мембраны от
за ATP использовалась сорбированная на меж
респирасом на ATP синтазу.
фазной границе октан вода (со стороны водной
фазы) F1FO ATPаза, выделенная из митохонд
рий сердца быка. В качестве источника энергии
ОБНАРУЖЕНИЕ ФРАКЦИИ
для синтеза ATP со стороны гидрофобной фазы
МЕМБРАНОСВЯЗАННЫХ ПРОТОНОВ
добавлялся безводный раствор электронейт
НА ПРИРОДНЫХ МЕМБРАНАХ
ральной Н+ кислоты Бренстеда - пентахлорфе
нола [9]. В этих экспериментах ионы водорода
Фракции мембраносвязанных протонов на по
на межфазной границе образовывались в резуль
верхности митопластов (митохондриях без внеш
тате диссоциации пентахлорфенола в момент
ней мембраны). Можно было ожидать, что при
контакта с водной фазой. Образование ионов
включении протонных помп положительный
водорода происходило в приграничном слое во
поверхностный заряд на поверхности мито
ды, имеющем низкую диэлектрическую посто
пластов повысится в результате образования
янную. В таких условиях, как отмечалось в пре
фракции мембраносвязанных протонов. Реги
дыдущих модельных экспериментах, на межфаз
страция изменений поверхностного заряда на
ной границе формируется фракция ионов водо
мембранах митопластов проводилась на прибо
рода (фракция мембраносвязанных протонов),
ре Malvern Zetasizer. Было показано, что поверх
обладающих избытком свободной энер
ность мембраны митопластов несёт на себе
гии (рис. 4). В этих условиях на межфазной гра
большой отрицательный заряд, но включение
нице осуществлялся синтез ATP при отсутствии
работы протонных помп практически не умень
трансмембранного электрохимического потен
шает его. Синтез фракции мембраносвязанных
циала ионов водорода. Эти эксперименты пока
протонов был достоверно продемонстрирован в
зали, что объёмные параметры гидратной обо
опытах с добавлением катализатора отрыва
лочки иона водорода, образовавшегося в воде с
протона (слабого основания HEPES 20 мМ).
низкой диэлектрической постоянной, действи
Включение протонных помп в присутствии ка
тельно невелики и соответствуют диаметру вход
тализатора приводило к достоверному сниже
ного протонного канала F1FO ATP синтазы.
нию величины отрицательного заряда, что ука
Приведённые выше результаты недавно получи
зывало на появление фракции мембраносвя
ли надёжное независимое экспериментальное
занных протонов на поверхности митоплас
подтверждение в работе Sjöholm et al. [17], в ко
тов [23]. Результаты действия катализатора на
торой на липосомах (со встроенными ATP син
заряд митопластов приведены на рис. 5. Наблю
тазой и комплексом IV) было показано, что син
даемый эффект катализа на митопластах пока
тез ATP происходит за счёт фракции мембрано
зал, что на природных мембранах связь протона
БИОХИМИЯ том 87 вып. 2 2022
224
НЕСТЕРОВ и др.
с мембраной качественно не отличается от свя
Наличие этой фракции тормозит работу про
зи мембраносвязанных протонов с БЛМ.
тонных помп по механизму обратной связи.
Важно отметить, что при выключенных про
Аналогичный эффект можно наблюдать также
тонных помпах добавление катализатора отры
при образовании мембраносвязанных протонов
ва протонов не оказывает влияния на поверхност
в результате гидролиза caged H+ [33]. Наблюдае
ный заряд митопластов. Это связано с тем, что
мый в этих экспериментах эффект торможения
при неработающих протонных помпах слой
дыхания избытком мембраносвязанных прото
противоионов на поверхности мембраны обра
нов показал, что природа их связи с поверх
зуется ионами калия (основными катионами в
ностью мембраны качественно отличается от
используемой среде измерения), а двойной
связи ионов калия с мембраной в равновесном
электрический слой находится в состоянии
состоянии. Скорее всего, связь ионов калия с
равновесия. При включении протонных помп
поверхностью митопласта определяется пря
ионы калия замещаются ионами водорода, при
мым электростатическим взаимодействием ка
этом система выходит из состояния равновесия.
тионов с отрицательным зарядом поверхности,
Состояние с избыточной концентрацией про
в то время как связь протонов с поверхностью
тонов на поверхности мембраны является ста
митопластов в энергизованной системе близка
ционарным и поддерживается работой протон
по своим свойствам к водородной связи. Имен
ных помп. Добавление катализатора увеличива
но этот тип связи, как показывает эксперимент,
ет скорость отрыва протонов в объёмную фазу
чувствителен к действию катализатора.
воды и смещает стационарное состояние, что и
Из данных рис. 5 и 6 видно, что разобщитель
наблюдается как увеличение отрицательного
не взаимодействует с мембраносвязанными
заряда мембраны. Этот эффект не наблюдается
протонами, но эффективно взаимодействует с
в равновесном состоянии (при отсутствии ис
ними после их отрыва от мембраны с помощью
точника энергии).
катализатора. Это обусловлено слабым взаимо
При исследовании функциональной роли
действием аниона разобщителя с ионами водо
фракции мембраносвязанных протонов было
рода, которые сорбированы на мембране. Этот
показано, что их удаление с поверхности мито
эффект наблюдается также при синтезе ATP [9].
пластов с помощью катализатора (HEPES 20 мМ)
Фракции мембраносвязанных протонов на по
увеличивало скорость работы протонных помп,
верхности митохондрий. Внешняя мембрана хо
оцениваемую по скорости дыхания митоплас
рошо проницаема для ионов водорода, и поэто
тов (рис. 6). Таким образом, было показано, что
му было необходимо ответить на вопрос о том,
фракция мембраносвязанных протонов, связан
существует ли перенос мембраносвязанных
ная с внутренней мембраной митохондрий, ис
протонов между внешней и внутренней мемб
полняет также роль регулятора активности элек
ранами. При этом было обнаружено, что поверх
трон транспортной цепи системы ОКСФОС.
ность фосфорилирующих митохондрий, так же,
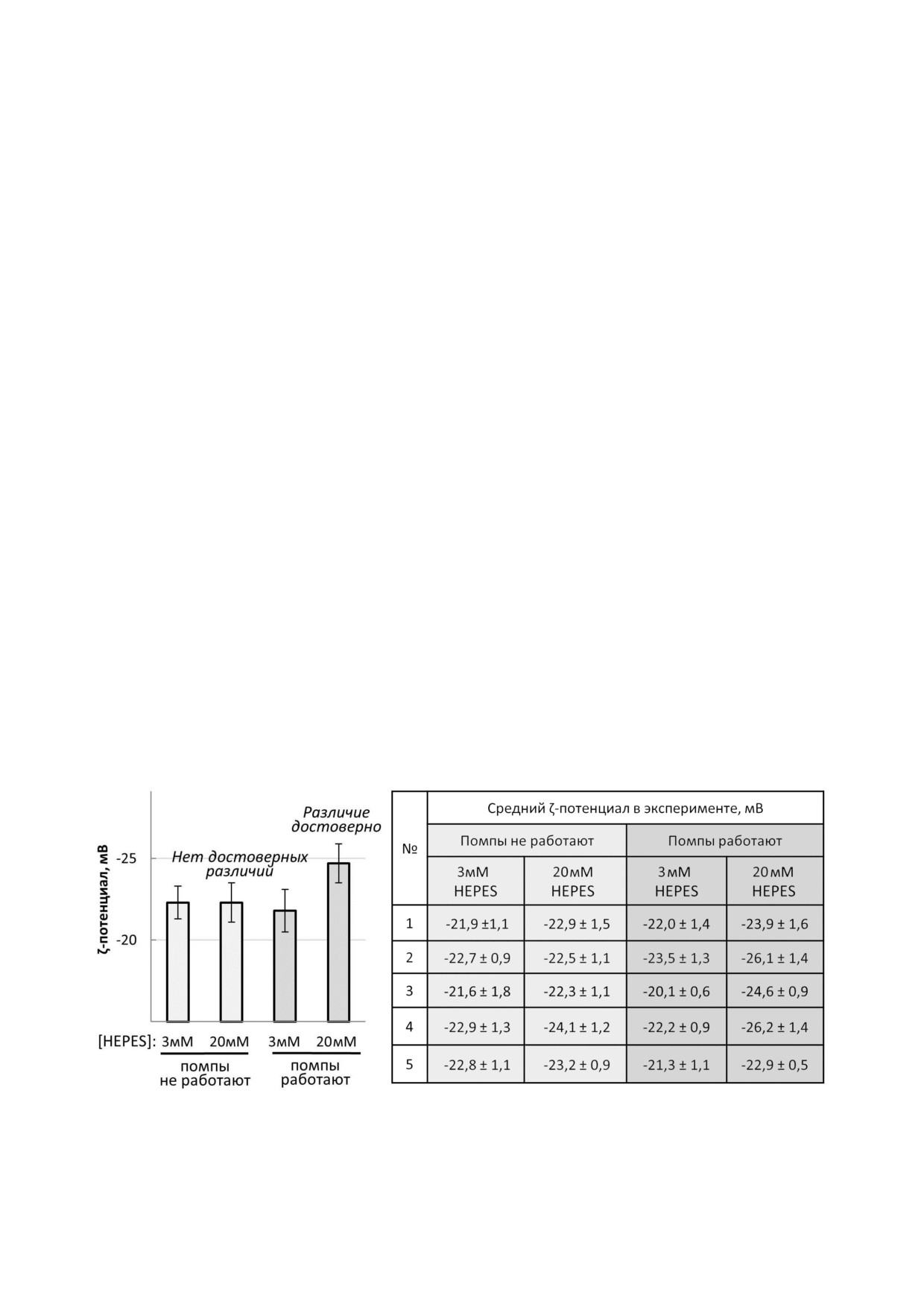
Рис. 5. Обнаружение мембраносвязанных протонов, обладающих избытком свободной энергии, на поверхности мито
пластов в условиях работы протонных помп. В таблице приведены ζ потенциалы в пяти экспериментах на разных пре
паратах митопластов по данным работы [23]. На диаграмме показаны усреднённые данные по всем пяти препаратам
БИОХИМИЯ том 87 вып. 2 2022
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
225
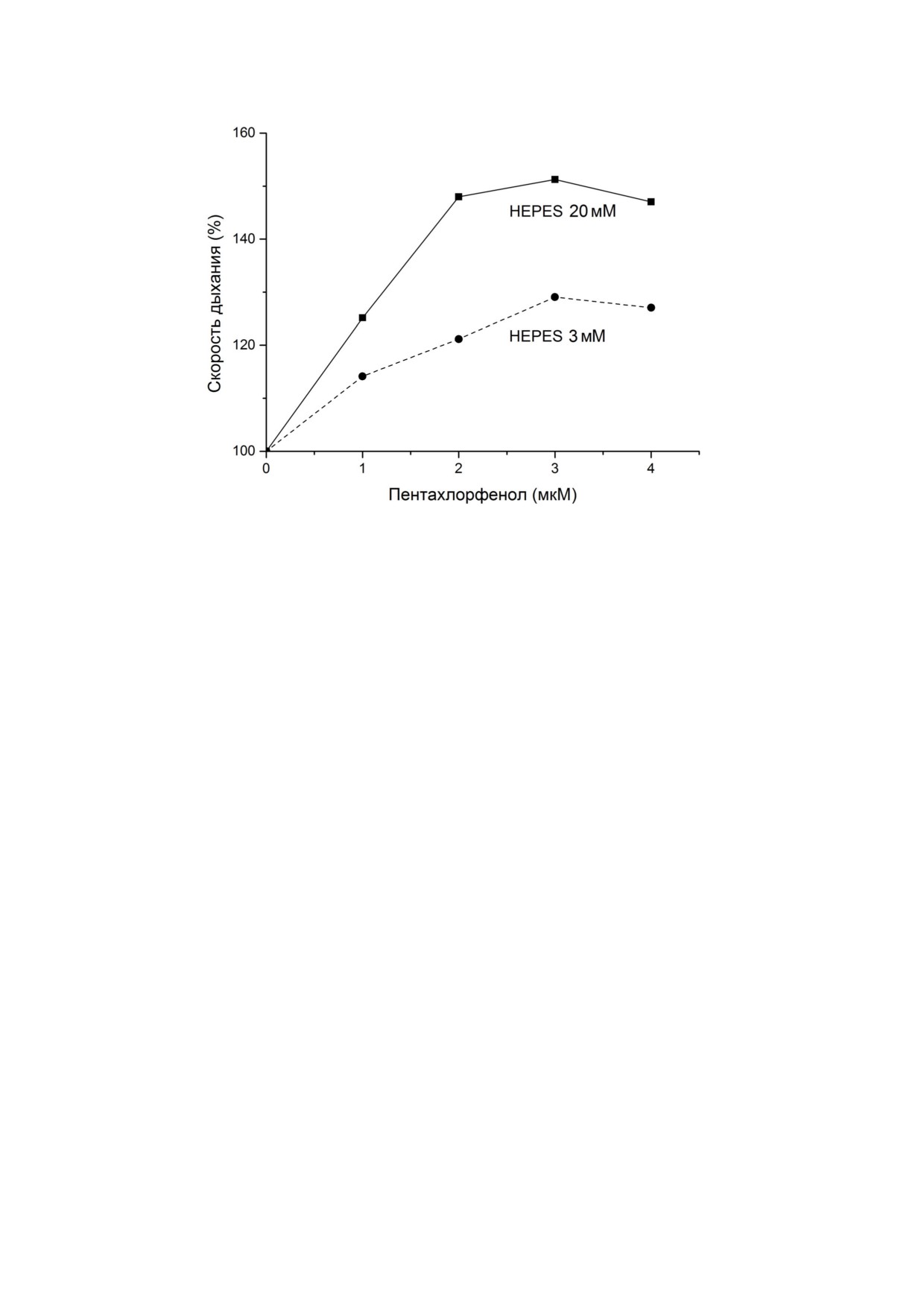
Рис. 6. Увеличение скорости дыхания митопластов (скорости функционирования протонных помп) в присутствии клас
сического разобщителя при повышении концентрации катализатора отрыва мембранных протонов HEPES. Рисунок мо
дифицирован по данным работы [23]
как и поверхность митопластов, может нести на
экспериментах он появлялся и в изотонических
себе значительный отрицательный заряд. Экс
условиях. Эти и ранее описанные данные поз
перименты показали, что перенос мембрано
воляют сделать заключение о том, что энергия
связанных протонов в нормальных изотоничес
фракции мембранных протонов используется в
ких условиях протекает малоэффективно. Од
реакции синтеза ATP при работе ОКСФОС.
нако межмембранный перенос активируется в
Неустойчивость эффекта вызвана тем, что то
условиях слабого осмотического стресса (при
ничность среды является не единственным
120 мОсм в среде инкубации митохондрий),
фактором, который контролирует слипание
когда, по данным электронной микроскопии,
мембран митохондрий и действие катализатора.
можно наблюдать стыковку внешней и внут
В связь между протонами и мембранами вклю
ренней мембран, обусловленную набуханием
чены, как было показано выше на модельных
матрикса [24]. Удаление мембраносвязанных
системах, молекулы воды, и такого рода связи
протонов с помощью катализатора (HEPES
могут меняться при небольших изменениях
20 мМ) увеличивает скорость работы протон
внешних условий.
ных помп в препаратах набухших митохонд
рий [42] аналогично тому, как это происходит
на митопластах.
МИТОХОНДРИИ КАК ПРОТОННЫЙ
Участие мембраносвязанных протонов в реак
СУПЕРКОНДЕНСАТОР (ИОНИСТОР)
циях синтеза ATP в митохондриях. Мембрано
связанные протоны напрямую участвуют в ре
Приведённые ранее данные показывают на
акциях синтеза ATP [43]. Опыты проводили на
копление ионов водорода в двойном электри
интактных митохондриях в гипотонических и
ческом слое на поверхности внутренней мемб
изотонических средах, в присутствии и при от
раны митохондрий. Это даёт возможность срав
сутствии катализатора реакции отрыва мембра
нить митохондрии с суперконденсатором (ио
носвязанных протонов (HEPES 20 мМ). Резуль
нистором) - техническим устройством, энергия
таты этих экспериментов приведены на рис. 7.
в котором запасается в двойном электрическом
Можно видеть, что катализатор резко снижает
слое на границе с электродом [44]. Недавние мо
эффективность функционирования ОКСФОС,
дельные исследования гидратации фосфолипи
уменьшая ADP/О на 20-40%. Эффект наблю
дов демонстрируют, что ионы на межфазной
дался в условиях гипотонии, но в некоторых
границе с фосфолипидным бислоем локализо
БИОХИМИЯ том 87 вып. 2 2022
226
НЕСТЕРОВ и др.
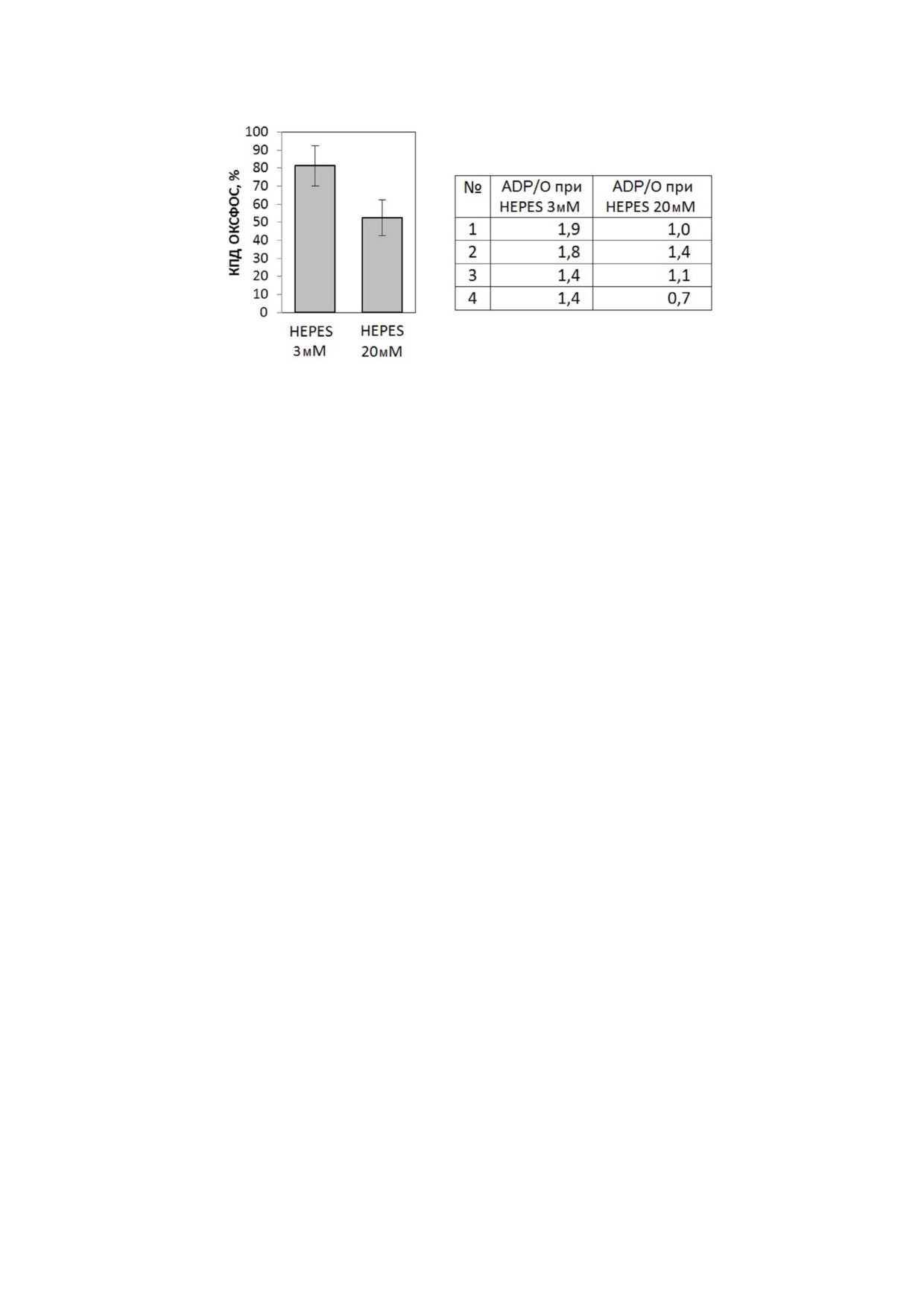
Рис. 7. Снижение коэффициента полезного действия (КПД) ОКСФОС при удалении фракции мембраносвязанных про
тонов с помощью катализатора (HEPES 20 мM). На диаграмме приведены усреднённые данные из работы [43], получен
ные на четырёх разных препаратах митохондрий. КПД оценивали по средней величине параметра ADP/О, отражающе
го количество атомов кислорода, используемое митохондриями для синтеза одной молекулы ATP из ADP и фосфата. За
100% принимали параметр ADP/О = 2, соответствующий теоретическому максимуму при окислении сукцината
ваны не только в слабосвязанном слое Гуи-Чеп
тохондрий, митопластов и на модельных систе
мена, но и адсорбируются в полярной зоне ли
мах: на БЛМ и на межфазной границе октан
пидного бислоя вблизи фосфатных групп [45].
вода. Важнейшей особенностью мембраносвя
Это даёт возможность для образования высоко
занных протонов является их способность при
устойчивых структур, аналогичных таковым в
отрыве от мембраны непосредственно участво
пористых электродах ионисторов. При этом
вать в работе ATP синтазы (ключевой биологи
электрический заряд протонов распределён на
ческой машины) в качестве рабочего тела. В ра
большой поверхности, а расстояние между раз
боте дано описание специфических свойств
ноимёнными зарядами очень мало (менее 3 Å).
мембраносвязанных протонов.
Важно отметить, что, в отличие от ионистора,
• Фракция мембраносвязанных протонов
где носителями заряда служат любые ионы
формируется в границах двойного электричес
электролита, в митохондриях идёт процесс
кого слоя и находится в плотном слое противо
трансмембранного переноса протонов (в ре
ионов (в пределах внешней плоскости Гельм
зультате функционирования комплексов дыха
гольца и плоскости скольжения). При работе
тельной цепи), в результате чего примембран
протонных помп сохраняется заряд первого
ный слой связанных катионов формируется
слоя противоионов (величина поверхностного
преимущественно из протонов. Последующий
заряда митохондрий не меняется), так как ионы
обмен протонов на другие ионы, приходящие из
водорода замещают в нём ионы калия.
водной фазы, возможен, однако имеет достаточ
• Фракция мембранных протонов является
но высокую энергию активации. Именно этот
неравновесной и обладает избытком свободной
процесс отрыва протонов от мембраны (или об
энергии. Она существует только в условиях ге
мена на другой ион) катализируется слабыми
нерации протонов на межфазной границе. Это
основаниями. Поскольку протоны, запасённые
принципиально отличает её от равновесной
на межфазной границе, могут использоваться
фракции противоионов слоя Штерна.
ATP синтазой для осуществления синте
• Высокие концентрации мембраносвязан
за ATP [9, 17], такие структуры с высокой элект
ных протонов ингибируют работу протонных
рической ёмкостью могут выполнять функцию
помп за счёт формирования запирающего слоя
промежуточного аккумулятора энергии в мито
из прочно удерживающихся на межфазной гра
хондриях.
нице ионов водорода.
• Мембраносвязанные протоны способны к
быстрому латеральному движению без отрыва в
О СВОЙСТВАХ МЕМБРАНОСВЯЗАННЫХ
водную фазу (подвижность одного порядка с
ПРОТОНОВ
подвижностью протона в объёме).
• Мембраносвязанные протоны обладают из
Эффект удержания протонов на межфазной
бытком свободной энергии, и поэтому могут
границе наблюдается в условиях связывания
быть удалены с мембраны добавлением катали
ионов водорода на поверхности мембраны ми
заторов отрыва протонов - высокими концент
БИОХИМИЯ том 87 вып. 2 2022
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
227
рациями слабых оснований (буферов HEPES,
нов водорода, которые одновременно исполня
Tris, MES) или анионов слабых кислот (цитрат).
ют две функции - переносчика и носителя сво
• Отрыв протонов от мембраны и их латераль
бодной энергии протонов и в то же время явля
ный перенос происходят с участием молекул
ются субстратами (рабочими телами), обеспе
воды.
чивающими направленное движение рабочих
• Протоны на межфазной границе обладают
элементов в сложной биологической машине,
избытком свободной энергии, которая исполь
которой является F1FO ATP синтаза.
зуется ATP синтазой в реакции синтеза ATP.
Финансирование. Работа выполнена при фи
нансовой поддержке Российского фонда фун
ЗАКЛЮЧЕНИЕ
даментальных исследований (грант № 19 04
00835), а также при поддержке НИЦ «Курчатов
Анализ показал, что энергия окислительных
ский институт» (тематический план «Изучение
реакций, которая используется в синтезе ATP,
процессов генерации, передачи и распределе
запасается не только в форме электрохимичес
ния энергии в живых организмах»).
кого потенциала ионов водорода на митохонд
Конфликт интересов. Авторы заявляют об от
риальной мембране, но также, а может быть и в
сутствии конфликта интересов.
первую очередь, в форме фракции ионов водо
Соблюдение этических норм. В рамках насто
рода, лабильно связанных с поверхностью
ящей статьи не проводилось каких либо экспе
мембраны. Процесс запасания энергии в мито
риментов с участием людей или животных в ка
хондриях неразрывно связан с переносом ио
честве объектов.
СПИСОК ЛИТЕРАТУРЫ
1. Mitchell, P. (1961) Coupling of phosphorylation to elec
membrane surface and retarded surface to bulk transfer,
tron and hydrogen transfer by a chemi osmotic type of
Nature, 370, 379 382, doi: 10.1038/370379a0.
mechanism, Nature, 191, 144 148.
11. Alexiev, U., Mollaaghababa, R., Scherrer, P., Khorana,
2. Skulachev, V. P., Sharaf, A. A., and Liberman, E. A. (1967)
H. G., and Heyn, M. P. (1995) Rapid long range proton
Proton conductors in the respirator chain and artificial
diffusion along the surface of the purple membrane and
membranes, Nature,
216,
718719, doi:
10.1038/
delayed proton transfer into the bulk, Proc. Natl. Acad. Sci.
216718a0.
USA, 92, 372 376.
3. Liberman, E. A., Topaly, V. P., Tsofina, L. M., Jasaitis, A.
12. Gopta, O. A., Cherepanov, D. A., Junge, W., and
A., and Skulachev, V. P. (1969) Mechanism of coupling of
Mulkidjanian, A. Y. (1999) Proton transfer from the bulk
oxidative phosphorylation and the membrane potential of
to the bound ubiquinone QB of the reaction center in
mitochondria, Nature, 222, 1076 1078, doi: 10.1038/
chromatophores of Rhodobacter sphaeroides: Retarded
2221076a0.
conveyance by neutral water, Proc. Natl. Acad. Sci. USA,
4. Drachev, L. A., Jasaitis, A. A., Kaulen, A. D.,
96, 13159 13164, doi: 10.1073/pnas.96.23.13159.
Kondrashin, A. A., Liberman, E. A., et al. (1974) Direct
13. Cherepanov, D. A., Junge, W., and Mulkidjanian, A. Y.
measurement of electric current generation by
(2004) Proton transfer dynamics at the membrane/water
cytochrome oxidase, H+ ATPase and bacteriorhodopsin,
interface: dependence on the fixed and mobile pH buffers,
Nature, 249, 321 324, doi: 10.1038/249321a0.
on the size and form of membrane particles, and on the
5. Williams, R. J. P. (1961) Possible functions of chains of
interfacial potential barrier, Biophys. J., 86, 665 680,
catalysts, J. Theor. Biol., 1, 1 17, doi: 10.1016/0022
doi: 10.1016/S0006 3495(04)74146 6.
5193(61)90023 6.
14. Medvedev, E., and Stuchebrukhov, A. (2012) Mechanism of
6. Kell, D. B. (1979) On the functional proton current path
long range proton translocation along biological mem
way of electron transport phosphorylation: An electrodic
branes, FEBS Lett., 587, doi: 10.1016/j.febslet.2012.12.010.
view, Biochim. Biophys. Acta, 9, 55 99, doi: 10.1016/0304
15. Weichselbaum, E., Österbauer, M., Knyazev, D. G.,
4173(79)90018 1.
Batishchev, O. V., Akimov, S. A., et al. (2017) Origin of
7. Mitchell, P. (1991) Foundations of vectorial metabolism
proton affinity to membrane/water interfaces, Sci. Rep., 7,
and osmochemistry, Biosci. Rep.,
11,
297346,
4553, doi: 10.1038/s41598 017 04675 9.
doi: 10.1007/BF01130212.
16. Toth, A., Meyrat, A., Stoldt, S., Santiago, R., Wenzel, D.,
8. Drachev, L. A., Kaulen, A. D., and Skulachev, V. P. (1984)
et al. (2020) Kinetic coupling of the respiratory chain with
Correlation of photochemical cycle, H+ release and
ATP synthase, but not proton gradients, drives ATP pro
uptake, and electric events in bacteriorhodopsin, FEBS
duction in cristae membranes, Proc. Natl. Acad. Sci. USA,
Lett., 178, 331 335, doi: 10.1016/0014 5793(84)80628 6.
117, 2412 2421, doi: 10.1073/pnas.1917968117.
9. Yaguzhinsky, L. S., Boguslavsky, L. I., Volkov, A. G., and
17. Sjöholm, J., Bergstrand, J., Nilsson, T., Šachl, R.,
Rakhmaninova, A. B. (1976) Synthesis of ATP coupled
Ballmoos, C., et al. (2017) The lateral distance between a
with action of membrane protonic pumps at the
proton pump and ATP synthase determines the ATP syn
octane-water interface, Nature,
259,
494496,
thesis rate, Sci. Rep., 7, 1 12, doi: 10.1038/s41598 017
doi: 10.1038/259494a0.
02836 4.
10. Heberle, J., Riesle, J., Thiedemann, G., Oesterhelt, D.,
18. Nesterov, S., Chesnokov, Y., Kamyshinsky, R., Panteleeva,
and Dencher, N. A. (1994) Proton migration along the
A., Lyamzaev, K., et al. (2021) Ordered clusters of the
БИОХИМИЯ том 87 вып. 2 2022
228
НЕСТЕРОВ и др.
complete oxidative phosphorylation system in cardiac
32.
Evtodienko, V. Y., Antonenko, Y. N., and Yaguzhinsky,
mitochondria, Int. J. Mol. Sci.,
22, doi:
10.3390/
L. S. (1998) Increase of local hydrogen ion gradient near
ijms22031462.
bilayer lipid membrane under the conditions of catalysis of
19.
Morelli, A. M., Ravera, S., Calzia, D., and Panfoli, I.
proton transfer across the interface, FEBS Lett., 425, 222
(2019) An update of the chemiosmotic theory as suggested
224, doi: 10.1016/s0014 5793(98)00233 6.
by possible proton currents inside the coupling membrane,
33.
Драгунова С. Ф., Красинская И. П., Ягужинский Л.
Open Biol., 9, doi: 10.1098/rsob.180221.
С. (1981) Регуляция переноса протона через двойной
20.
Lee, J. W. (2021) Mitochondrial energetics with trans
электрический слой на мембране митохондрий, Био!
membrane electrostatically localized protons: do we have
химия, 46, 1087 1095.
a thermotrophic feature? Sci. Rep.,
11,
14575,
34.
Geißler, D., Antonenko, Y. N., Schmidt, R., Keller, S.,
doi: 10.1038/s41598 021 93853 x.
Krylova, O. O., et al. (2005) (Coumarin 4 yl)methyl
21.
Teschke, O., Ceotto, G., and de Souza, E. F. (2001)
esters as highly efficient, ultrafast phototriggers for pro
Interfacial water dielectric permittivity profile measure
tons and their application to acidifying membrane sur
ments using atomic force microscopy, Phys. Rev. E, 64,
faces, Angew. Chem. Int. Ed., 44, 1195 1198, doi: 10.1002/
011605, doi: 10.1103/PhysRevE.64.011605.
anie.200461567.
22.
Ташкин В. Ю., Вишнякова В. Е., Щербаков А. А.,
35.
Serowy, S., Saparov, S. M., Antonenko, Y. N., Kozlovsky,
Финогенова О. А., Ермаков Ю. А., и др. (2019) Изме
W., Hagen, V., et al. (2003) Structural proton diffusion
нение емкости и граничного потенциала бислойной
along lipid bilayers, Biophys. J., 84, 1031 1037.
липидной мембраны при быстром освобождении
36.
Springer, A., Hagen, V., Cherepanov, D. A., Antonenko,
протонов на ее поверхности, Биол. Мемб., 36, 101 108.
Y. N., and Pohl, P. (2011) Protons migrate along interfa
23.
Моисеева В. С, Мотовилов К. А, Лобышева Н. В,
cial water without significant contributions from jumps
Орлов В. Н, Ягужинский Л. С. (2011) Образование
between ionizable groups on the membrane surface, Proc.
метастабильной связи ионов водорода с поверх
Natl. Acad. Sci. USA, 108, 14461 14466, doi: 10.1073/
ностью митопластов, Доклады Академии Наук, 438,
pnas.1107476108.
555558.
37.
Zaslavsky, D., Sadoski, R. C., Rajagukguk, S., Geren, L.,
24.
Eroshenko, L. V., Marakhovskaya, A. S., Vangeli, I. M.,
Millett, F., et al. (2004) Direct measurement of proton
Semenyuk, P. I., Orlov, V. N., et al. (2012) Bronsted acids
release by cytochrome c oxidase in solution during the
bounded to the mitochondrial membranes as a sub
F→O transition, Proc. Natl. Acad. Sci. USA, 101, 10544
strate for ATP synthase, Dokl. Biochem. Biophys., 444,
10547, doi: 10.1073/pnas.0401521101.
158161.
38.
Le Coutre, J., and Gerwert, K. (1996) Kinetic isotope
25.
Ermakov, Y. A., and Nesterenko, A. M. (2017) Boundary
effects reveal an ice like and a liquid phase type intramol
potential of lipid bilayers: Methods and interpretations,
ecular proton transfer in bacteriorhodopsin, FEBS Lett.,
J. Phys. Conf. Ser., 780, 012002, doi: 10.1088/1742
398, 333 336, doi: 10.1016/S0014 5793(96)01254 9.
6596/780/1/012002.
39.
Salomonsson, L., Brändén, G., and Brzezinski, P. (2008)
26.
Antonenko, Y. N., Kovbasnjuk, O. N., and Yaguzhinsky,
Deuterium isotope effect of proton pumping in
L. S. (1993) Evidence in favor of the existence of a kinetic
cytochrome c oxidase, Biochim. Biophys. Acta, 1777, 343
barrier for proton transfer from a surface of bilayer phos
350, doi: 10.1016/j.bbabio.2007.09.009.
pholipid membrane to bulk water, Biochim. Biophys. Acta,
40.
Salomonsson, L., Faxén, K., Adelroth, P., and Brzezinski,
1150, 45 50, doi: 10.1016/0005 2736(93)90119 K.
P. (2005) The timing of proton migration in membrane
27.
Gonella, G., Backus, E. H. G., Nagata, Y., Bonthuis, D.
reconstituted cytochrome c oxidase, Proc. Natl. Acad. Sci.
J., Loche, P., et al. (2021) Water at charged interfaces,
USA, 102, 17624 17629, doi: 10.1073/pnas.0505431102.
Nat. Rev. Chem., 5, 466 485, doi: 10.1038/s41570 021
41.
Zhang, C., Knyazev, D. G., Vereshaga, Y. A., Ippoliti, E.,
00293 2.
Nguyen, T. H., et al. (2012) Water at hydrophobic inter
28.
Antonenko, Yu. N., and Yaguzhinsky, L. S.
(1982)
faces delays proton surface to bulk transfer and provides a
Generation of potential in lipid bilayer membranes as a
pathway for lateral proton diffusion, Proc. Natl. Acad. Sci.
result of proton transfer reactions in the unstirred layers,
USA, 109, 9744 9749, doi: 10.1073/pnas.1121227109.
J. Bioenerg. Biomembr., 14, 457465, doi: 10.1007/
42.
Yurkov, V. I., Fadeeva, M. S. and Yaguzhinsky, L. S. (2005)
BF00743071.
Proton transfer through the membrane water interfaces in
29.
Antonenko, Y. N., and Yaguzhinsky, L. S. (1990) Effect of
uncoupled mitochondria, Biochemistry Moscow, 70, 195
changes in cation concentration near bilayer lipid mem
199, doi: 10.1007/s10541 005 0101 8.
brane on the rate of carrier mediated cation fluxes and on
43.
Солодовникова И. М., Юрков В. И., Тоньшин А. А.,
the carrier apparent selectivity, Biochim. Biophys. Acta,
Ягужинский Л. С. (2004) О локальном сопряжении
1026, 236 240, doi: 10.1016/0005 2736(90)90069 Z.
процессов дыхания и фосфорилирования в митохон
30.
Eremeev, S. A. and Yaguzhinsky, L. S. (2015) On local
дриях печени крысы, Биофизика, 49, 47 56.
coupling of electron transport and ATP synthesis system
44.
Conway, B. E. (1999) Electrochemical Supercapacitors:
in mitochondria. Theory and experiment, Biochemistry
Scientific Fundamentals and Technological Applications,
Moscow, 80, 576 581, doi: 10.1134/S0006297915050089.
Springer Science & Business Media, New York.
31.
Kovbasnjuk, O. N., Antonenko, Y. N., and Yaguzhinsky,
45.
Deplazes, E., White, J., Murphy, C., Cranfield, C. G., and
L. S. (1991) Proton dissociation from nigericin at the
Garcia, A. (2019) Competing for the same space: Protons
membrane-water interface, the rate limiting step of
and alkali ions at the interface of phospholipid bilayers,
K+/H+ exchange on the bilayer lipid membrane, FEBS
Biophys. Rev., 11, 483 490, doi: 10.1007/s12551 019
Lett., 289, 176 178, doi: 10.1016/0014 5793(91)81063 E.
00541 2.
БИОХИМИЯ том 87 вып. 2 2022
МЕМБРАНОСВЯЗАННЫЕ ПРОТОНЫ
229
MECHANISM OF ENERGY STORAGE AND TRANSFORMATION
IN MITOCHONDRIA AT THE WATER MEMBRANE INTERFACE
Review
S. V. Nesterov1,2, E. G. Smirnova3, and L. S. Yaguzhinsky2,3,4*
1 National Research Center “Kurchatov Institute”, 123182 Moscow, Russia
2 Moscow Institute of Physics and Techonology, 141701 Dolgoprudny, Moscow Region, Russia
3 Belozersky Research Institute of Physico!Chemical Biology, Lomonosov Moscow State University,
119992 Moscow, Russia; e!mail: yag@genebee.msu.ru
4 Institute of Cytochemistry and Molecular Pharmacology, 115404 Moscow, Russia
In this analytical review various methods for the generation of membrane bound protons with the use of different
energy sources were considered at model and natural systems. The analysis showed that all three considered types of
reactions contain the same key stage of membrane bound protons synthesis. It is the dissociation of electrically neu
tral Brønsted acids at the interface during the transition from hydrophobic phase to water with a low dielectric con
stant. Particular attention is paid to the fact that in one of the analyzed model systems, membrane bound protons
provide energy for the ATP synthesis reaction. The review provides data showing that a similar mechanism for the
synthesis of membrane bound protons was also carried out on natural membranes of the OXPHOS system, in par
ticular, on the membranes of mitoplasts and mitochondria. The analysis showed that the energy of oxidative reac
tions, which provides the synthesis of ATP, at the intermediate stage is stored not only in the form of the transmem
brane electrochemical potential of hydrogen ions. It is also and perhaps even primarily, stored in the form of hydro
gen ion fraction bounded to the inner mitochondrial membrane. The process of energy storage in mitochondria is
linked with the transfer of hydrogen ions, which simultaneously perform two functions. The fraction of hydrogen
ions on the membrane surface is a free energy carrier and, at the same time, a direct substrate (working body) pro
viding the movement of F1FO ATP synthase biological machine.
Keywords: membrane bound proton, hydrogen ion, membrane, mitochondria, oxidative phosphorylation, super
capacitor
БИОХИМИЯ том 87 вып. 2 2022