БИОХИМИЯ, 2022, том 87, вып. 8, с. 1118 - 1131
УДК 577
CRISPR-CAS9: ИСТОРИЯ ОТКРЫТИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
ПРИМЕНЕНИЯ В ГЕНОМНОМ РЕДАКТИРОВАНИИ
Обзор
© 2022 И. Гостимская
Манчестерский университет,
M1 7DN Манчестер, Великобритания; электронная почта: gostimskaya@gmail.com
Поступила в редакцию 11.05.2022
После доработки 07.07.2022
Принята к публикации 19.07.2022
Развитие метода геномного редактирования с использованием системы CRISPR-Cas9 было удостое-
но Нобелевской премии по химии в 2020 году, когда с момента открытия всех принципиальных мо-
лекулярных компонентов этой системы не прошло и 10 лет. Впервые в истории вручения премии её
получили две женщины, Эмманюэль Шарпантье и Дженнифер Даудна, сделавшие одни из ключе-
вых открытий в области манипулирования ДНК с помощью системы CRISPR-Cas9, так называемых
«генетических ножниц». Важность этой технологии сложно переоценить, так как она позволяет не
только направленно модифицировать геномы модельных организмов в научных исследованиях и из-
менять характеристики важных для человека растений и животных, но и несёт в себе потенциал ре-
волюционных изменений в медицинской науке, в особенности в области лечения генетических забо-
леваний. Изначальной биологической функцией системы CRISPR-Cas9 является защита прокариот
от мобильных генетических элементов, однако на момент написания данного обзора технологии,
основанные на использовании CRISPR-Cas9 и родственных систем, уже успешно применялись в
таких областях, как лечение опасных болезней человека, создание тестов для детекции коронавируса
и даже для геномной модификации человеческих эмбрионов с последующим рождением младенцев,
прошедших эту процедуру. Такое вмешательство в клетки зародышевой линии человека впоследствии
вызвало широкое осуждение по причине этического аспекта данного использования технологии и
даже призывы к мораторию на наследуемые геномные манипуляции. В данном обзоре рассматрива-
ется история открытия и изучения системы CRISPR-Cas9 с некоторыми современными аспектами её
последующего использования, включая этические вопросы применения системы на человеке.
КЛЮЧЕВЫЕ СЛОВА: CRISPR-Cas9, геномное редактирование, «генетические ножницы», этические
аспекты.
DOI: 10.31857/S0320972522080103, EDN: AYYPVK
ИСТОРИЯ ОТКРЫТИЯ ОСНОВНЫХ
несколько месяцев, однако ни их происхожде-
КОМПОНЕНТОВ СИСТЕМЫ CRISPR-Cas9
ние, ни значение в клетке не были предсказаны
их первооткрывателями. Несмотря на то что во
Короткие палиндромные повторы CRISPR
время ранних работ по этой тематике биологи-
(Clustered Regularly Interspaced Short Palindromic
ческая функция системы CRISPR ещё не была
Repeat) были впервые обнаружены в бактериях
выявлена, на тот момент учёными уже был пред-
Escherichia coli и описаны в 1987 г. в публикации
ложен способ использования закодированной в
Ishino et al. [1] из Осакского университета (Япо-
палиндромных повторах CRISPR информации
ния). Секвенирование этих сложных для изу-
в медицинских исследованиях, а именно, в об-
чения фрагментов ДНК на тот момент заняло ласти генотипировании различных штаммов
Принятые сокращения: cas - гены, ассоциированные с CRISPR (CRISPR-associated genes); CRISPR - равномерно рас-
пределённые короткие палиндромные повторы, собранные в кластеры (Clustered Regularly Interspaced Short Palindromic
Repeats); crRNA - CRISPR-ассоциированная РНК (CRISPR-RNA); PAM - мотив, соседствующий с протоспейсером
(Protospacer Adjacent Motif); sgRNA - единая направляющая РНК, «РНК-гид» (single guide RNA); SpCas9 - белок Cas9 из
Streptococcus pyogenes; tracrRNA - транс-активирующая CRISPR РНК (trans-activating CRISPR RNA).
1118
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1119
бактерий: изначально на примере Mycobacterium
тающих с йогуртовыми культурами бактерий
tuberculosis [2], а затем - Streptococcus pyogenes [3].
Streptococcus thermophilus в датской компании
Как оказалось, локусы CRISPR в разных штам-
«Даниско» [16]. Благодаря наличию у компа-
мах одного и того же вида патогенных бактерий
нии богатой коллекции штаммов бактерий,
обладали высокой степенью полиморфизма,
собранных начиная с 1980 гг., учёные смогли
что позволяло характеризовать разнообразие
проследить исторический ход приобретения
штаммов бактерий в клинических условиях.
бактериями спейсеров в локусе CRISPR в ответ
Важный прорыв в понимании биологиче-
на вирусные атаки бактериофагов. Добавление
ской функции палиндромных повторов CRISPR
дополнительных спейсеров в этой работе вы-
случился после того, как в 1995 г. Франсиско
зывало у клеток S. thermophilus приобретённый
Мохика из Университета г. Аликанте (Испания)
иммунитет к соответствующим новым видам
обнаружил подобные структуры в геноме архей
бактериофагов, что впоследствии привело к
Haloferax mediterranei [4]. Их наличие в эволю-
получению авторами одного из первых патен-
ционно удалённом домене жизни предполагало
тов в этой области [17] и началу «вакцинации»
функциональную значимость этих элементов и
бактериальных культур с помощью технологии
послужило толчком к дальнейшим исследова-
CRISPR компанией «Даниско» в 2005 г. [18].
ниям. Ф. Мохика заметил схожесть описанных
В настоящее время повторы CRISPR обна-
им элементов с ранее найденными ДНК-по-
ружены в большинстве геномов архей и почти
вторами в геноме бактерий и одним из первых
в половине изученных геномов бактерий, но не
выдвинул гипотезу, что эти необычные локусы
были найдены в последовательностях ДНК эу-
включают в себя фрагменты чужеродной ДНК
кариот и вирусов. Существование CRISPR-по-
и, по сути, являются частью иммунной защи-
второв в митохондриях было предположено в
ты бактерий и архей [5]. В том же году, что и
одной из самых ранних публикаций по темати-
Ф. Мохика, две другие лаборатории независимо
ке, в которой эта система также была впервые
пришли к подобным выводам [6, 7], оповещая о
описана у цианобактерий [19]. Авторы работы
начале эпохи активных исследований этого не-
использовали ранее опубликованные данные
обычайного явления природы. В соответствии
секвенирования митохондриальных плазмид
с вышеупомянутой теорией иммунной системы
из бобов Vicia faba L. [20], а их выводы были в
прокариот, фрагменты вирусной ДНК («спей-
дальнейшем процитированы Mojica et al. [21],
серы» длиной в 17-84 оснований), разделённые
однако не были подтверждены в более поздних
короткими палиндромными повторами (23-50
исследованиях [8].
оснований [8]) и сгруппированные в кластеры в
На начальном этапе исследований повто-
межгенных областях, представляют собой биб-
ров CRISPR различные научные группы для
лиотеку потенциально опасной для прокариот
их обозначения использовали разнообразные
генетической информации (для обзора по мик-
имена, что на нынешний момент осложняет по-
робному антивирусному арсеналу см. обзоры
иск ранних статей по этой тематике. Принятое
Isaev et al. [9, 10]). Изначально предполагалось,
на нынешний момент название CRISPR впер-
что такая система может работать по механиз-
вые появилось в публикации Jansen et al. [22]
му РНК-интерфeренции, однако в публикации
в 2002 г. (с подачи Ф. Мохики в корреспонден-
Марраффини и Сонтхаймера было впервые экс-
ции между двумя коллаборирующими научны-
периментально продемонстрировано, что ми-
ми группами). В этой же работе впервые было
шенью атаки иммунной системы прокариот яв-
описано наличие генов, ассоциированных с
ляется непосредственно чужеродная ДНК [11],
повторами CRISPR и получивших название
а не мРНК, и, следовательно, использование
cas1-4 (CRISPR-associated genes). Эти гены
такой системы в лаборатории может представ-
были обнаружены в непосредственной близо-
лять собой потенциальный инструмент геном-
сти от локусов CRISPR различных прокариот, а
ного редактирования. Однако в более поздних
два из них содержали мотивы, характерные для
исследованиях было показано, что некоторые
хеликазы и нуклеазы, что подкрепило гипотезу
из описанных систем CRISPR действительно
авторов о неслучайной связи группы генов cas
работают с молекулами РНК [12, 13] и, соот-
с системой CRISPR и их вовлечении в мета-
ветственно, могут быть использованы для из-
болизм ДНК. Также в 2002 г. эта группа генов
бирательной деактивации транскриптов внутри
была описана командой учёных под руковод-
клетки [14, 15].
ством Е.В. Кунина из института NCBI (Бетесда,
Первые экспериментальные сведения о ра-
США), однако её связь с повторами CRISPR не
боте системы CRISPR были получены в 2007 г.
была выявлена в их ранней работе [23]. С мо-
в исследованиях двух французских учёных,
мента первого открытия генов, ассоциирован-
Родольфа Баррангу и Филиппа Хорвата, рабо-
ных с системой CRISPR, по сегодняшний день
БИОХИМИЯ том 87 вып. 8 2022
1120
ГОСТИМСКАЯ
было обнаружено их поистине необычайное
выяснено впоследствии, в некоторых случаях -
множество и разнообразие в клетках прока-
РНК) - так называемые «генетические нож-
риот, включающее в себя представителей се-
ницы», среди которых наиболее изученной яв-
мейств хеликаз, нуклеаз, полимераз и др. Бел-
ляется нуклеаза Cas9. Впервые этот белок был
ки, ассоциированные с этой системой, можно
описан в связи с его ассоциацией с повторами
разделить на адаптационные (участвующие в
CRISPR в статье Bolotin et al. [6], где он изна-
приобретение иммунитета, главные предста-
чально был назван Cas5 (другие альтернатив-
вители - Cas1 и Cas2) и эффекторные (непо-
ные названия - Csn1 и Csx12), также авторами
средственно вовлечённые в уничтожение мо-
этой публикации было выявлено присутствие
бильных генетических элементов посредством
в нем мотива HNH (His-Asn-His), присущего и
их распознавания и расщепления), а также до-
другим нуклеазам. Ещё одно важное наблюде-
полнительные и регуляторные [24]. В настоя-
ние, сделанное авторами той же работы - об-
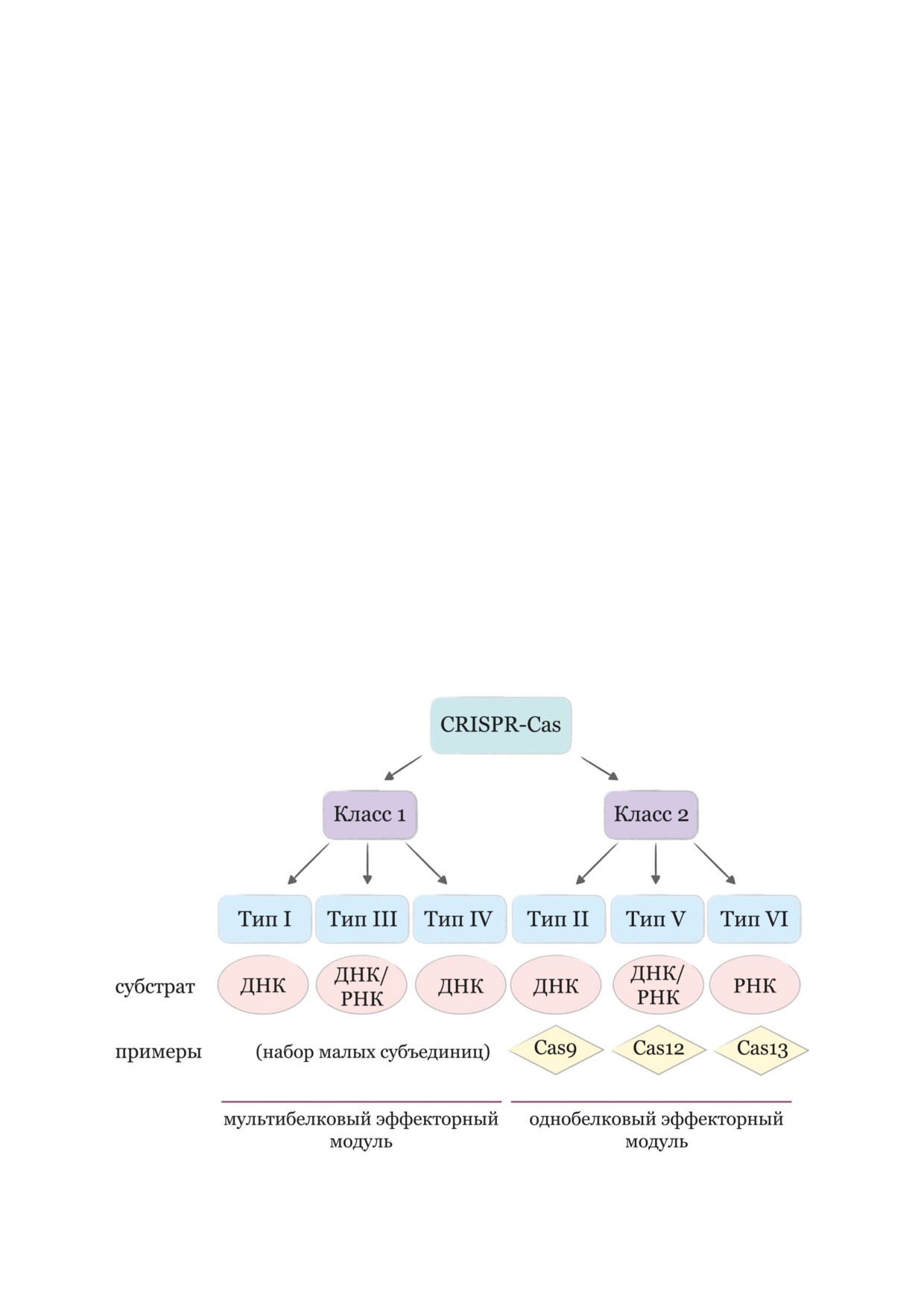
щий момент признана система классификации,
наружение определённой закономерности в
в которой все известные на сегодняшний день
последовательностях оснований по одну сто-
системы CRISPR-Cas разделены на 2 класса
рону от описанных спейсеров локусов CRISPR,
и 6 типов, которые также, в свою очередь, под-
однако понимание роли и название для этого
разделяются на многочисленные подтипы: на
явления пришло в более поздних исследовани-
момент написания обзора Makarova et al. [25]
ях. В настоящее время короткие мотивы, сосед-
было описано более 30 подтипов (рис. 1). Глав-
ствующие с протоспейсерами, но отсутствую-
ная разница между классами состоит в том, что
щие в изначальных спейсерах локуса CRISPR,
эффекторный модуль белков класса 1 представ-
носят название PAM - Protospacer Adjacent
лен комплексом из нескольких белков, тогда
Motifs (мотивы, соседствующие с протоспей-
как в классе 2 - одним мультидоменным бел-
серами)
[29]. Протоспейсерами называются
ком (Cas9, Cas12 или Cas13) [26-28].
фрагменты ДНК, атакуемые иммунной систе-
Наибольший интерес для биотехнологии,
мой прокариот и идентичные соответствующе-
медицины и других отраслей науки и инду-
му спейсеру в локусе CRISPR за исключением
стрии из всех известных молекул Cas представ-
вышеупомянутого мотива PAM. Эти мотивы
ляют собой белки системы направленного раз-
важны на этапе распознавания потенциально
резания молекул чужеродной ДНК (а как было
опасной генетической информации, их присут-
Рис. 1. Принятая классификация известных систем CRISPR-Cas
БИОХИМИЯ том 87 вып. 8 2022
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1121
Рис. 2. Исторический ход открытий компонентов системы CRISPR-Cas9. 1987 г. - короткие повторы ДНК, впослед-
ствии получившие название CRISPR, впервые замечены в бактериальных геномах, а в 1995 г. обнаружены и в геномах
архей. 2005 г. - предположена роль повторов CRISPR в защите прокариот от чужеродной генетической информации, а
также впервые описан белок Cas9 (изначальная информация о белках, ассоциированных с локусом CRISPR, появилась
в 2002 г.). Две молекулы РНК, crRNA и tracrRNA, обнаружены в составе комплекса в 2007 и 2011 гг. соответственно. Ра-
бота, в дальнейшем удостоенная Нобелевской премии, где все компоненты были собраны in vitro, а две молекулы РНК
объединены в одну для удобства использования системы, была опубликована в 2012 г.
ствие на конце последовательности сигналит о
ной активности комплекса CRISPR-Cas, даже
чужеродности фрагмента ДНК и необходимо-
если спейсер в локусе CRISPR представлен бо-
сти её расщепления, тогда как последователь-
лее длинной последовательностью нуклеоти-
ность ДНК, сохранённая в локусе CRISPR и
дов [31]. Эта публикация была одной из первых
не содержащая мотивов PAM, не подвергается
двух работ in vitro, проведённых параллельно и
атаке иммунной системы прокариот.
независимо в конкурирующих лабораториях и
Важным игроком в системе CRISPR-Cas9
описывающих, как в системе CRISPR фермент
оказалась также короткая РНК - процесси-
Cas9 использует crRNA для целенаправленного
рованный продукт транскрипции с локуса
разрезания чужеродной ДНК.
CRISPR, направляющая белки иммунной систе-
Последним недостающим звеном в голово-
мы прокариот к чужеродным молекулам с гене-
ломке, без которого невозможно собрать работаю-
тической информацией. Группа исследователей
щую систему CRISPR-Cas9 in vitro, оказалась
под руководством Дж. ван дер Уста (Вагенин-
ещё одна короткая молекула РНК, открытая в
генский университет, Нидерланды), описавших
связи с её участием в процессировании crRNA
существование таких молекул РНК, присвоила
группой Эмманюэль Шарпантье в 2011 г. [32].
им название crRNA (CRISPR RNA, CRISPR-ас-
Эта необходимая для работы нуклеазы молекула
социированная РНК). Также было замечено,
была названа tracrRNA (trans-activating CRISPR
что изначальным результатом транскрипции
RNA, транс-активирующая CRISPR RNA).
с локуса CRISPR является молекула-предше-
В последующей работе, позднее отмеченной Но-
ственница пре-crRNA, состоящая из несколь-
белевской премией 2020 г., была показана роль
ких фрагментов спейсеров и повторов, кото-
tracrRNA в непосредственном механизме разре-
рая в дальнейшем подвергается расщеплению
зания ДНК-мишени, а также предположено объ-
на индивидуальные фрагменты [30]. В работе
единение двух молекул РНК, crRNA и tracrRNA,
лаборатории под руководством В. Шикшниса
в одну химерную молекулу, что значительно об-
(Вильнюсский университет, Литва) было про-
легчило практическое использование системы
демонстрировано, что длина непосредственно
CRISPR-Cas9 в последующих применениях
«направляющей» последовательности crRNA в
(sgRNA - single guide RNA, единая направляю-
20 пар оснований, комплементарная ДНК-ми-
щая РНК, «РНК-гид» [33]). На рис. 2 показаны
шени, необходима и достаточна для нуклеаз-
временные рамки хода исторических событий
БИОХИМИЯ том 87 вып. 8 2022
1122
ГОСТИМСКАЯ
открытия компонентов системы CRISPR-Cas9:
сти гомологически направленную репарацию
изначально самого локуса CRISPR, затем бел-
двойного разрыва молекулы (последний шаг
ков, ассоциированных с ним, включая Cas9, а
был применён только в лаборатории Дж. Чёр-
позднее - и двух молекул РНК, необходимых
ча) [34, 35]. Также в январе 2013 г. вышли сход-
для образования рибонуклеопротеинового ком-
ные публикации из лабораторий Дж. Даудны
плекса и распознавания субстратной ДНК.
(Колледж Беркли, США) [36], Джин-Су Кима
(Сеульский университет, Южная Корея) [37]
и Дж. Кита Джоунга (Гарвардская школа ме-
ИСПОЛЬЗОВАНИЕ СИСТЕМЫ CRISPR-Cas9
дицины, США) [38]. В последней упомянутой
В ЭУКАРИОТИЧЕСКИХ КЛЕТКАХ
публикации работа была проведена на клетках
данио-рерио, а не человека, однако, что нема-
Открытие необходимых и достаточных ком-
ловажно, впервые было показано использова-
понентов системы CRISPR-Cas9 послужило
ние системы CRISPR-Cas9 на клетках зароды-
началом гонки конкурирующих лабораторий
шевой линии.
за титул первенства в применении системы для
генетического редактирования клеток человека
и животных. В январе 2013 г. практически одно-
ПЕРВЫЕ
временно появились пять публикаций авторов,
КРИСТАЛЛОГРАФИЧЕСКИЕ ДАННЫЕ
сообщавших о достижении этой цели. Две ра-
боты, напечатанные в одном выпуске журнала
Как было упомянуто выше, наиболее из-
Science и предложившие наиболее оптималь-
ученным белком из группы Cas является нук-
ный подход к решению этой задачи, были вы-
леаза Cas9, за ~20 лет с момента открытия ге-
полнены в лабораториях Джорджа Чёрча (Гар-
нов cas более 20 000 статей в системе PubMed
вардский университет, США) и Фэна Чжана
упоминают название Cas9 в том или ином
(Институт Броуд, США). В этих работах было
контексте. Следующим очевидным этапом
показано, что для успешного редактирования
исследований системы CRISPR-Cas9 послу-
ДНК в клетках человека необходимо провести
жили попытки получить детальную информа-
несколько шагов адаптации системы. К таким
цию о структуре этого белка с помощью мето-
шагам относятся оптимизация кодонов коди-
дов кристаллографии. Ситуация со многими
рующей части гена cas9 и добавление сигнала
другими ключевыми этапами исследований в
ядерной локализации, удлинение молекулы
данной области повторилась и в этом случае:
sgRNA (для улучшения эффективности работы
результаты кристаллографических работ кон-
системы), а также возможное добавление об-
курирующих лабораторий были опубликованы
разца ДНК, по которому клетка может прове-
практически одновременно. В феврале 2014 г. в
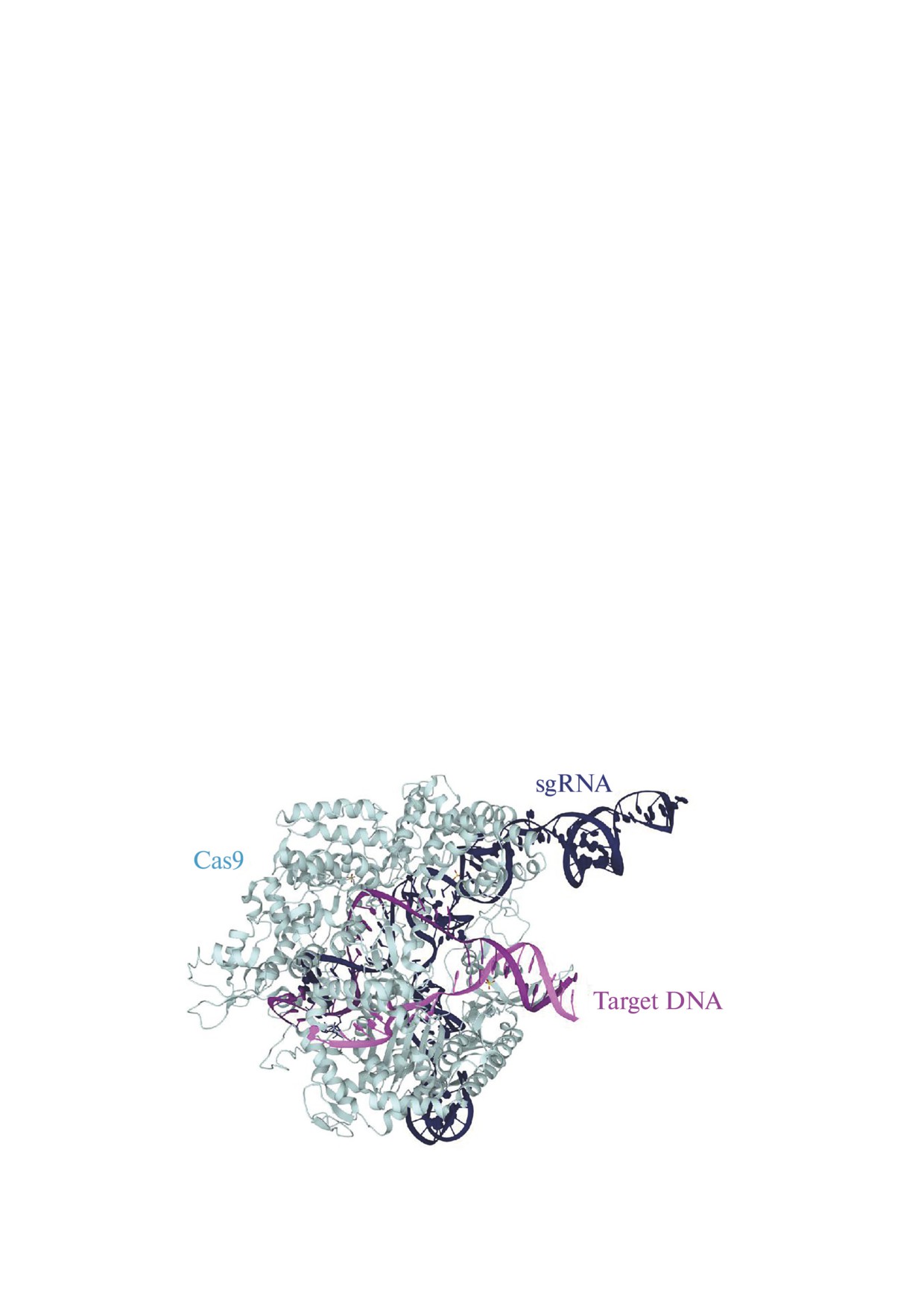
Рис. 3. Трёхмерная организация белка Cas9 в комплексе с РНК-«гидом» (sgRNA) и субстратной ДНК (Target DNA), кри-
сталлографические данные (PDB ID 5F9R, PDB DOI 10.2210/pdb5F9R/pdb)
БИОХИМИЯ том 87 вып. 8 2022
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1123
европейской базе данных PDBe («Protein Data
Ф. Чжана также отправил на рассмотрение за-
Bank in Europe») были размещены 2 структуры
явку на патент [43] одновременно с приняти-
кристаллов Cas9, а сопровождающие их пуб-
ем статьи Ф. Чжана по редактированию клеток
ликации были напечатаны в журналах Nature
человека к публикации в журнал Science [35].
и Cell [39, 40]. Структура, полученная в лабо-
Изначально именно заявка Ф. Чжана оказалась
ратории Дж. Даудны, состояла из апо-белка
успешной и привела к получению им патента в
(PDBe ID 4cmp, PDBe DOI 10.2210/pdb4cmp/
апреле 2014 г., тогда как заявка Дж. Даудны на
pdb), тогда как лаборатории О. Нуреки (Токий-
тот момент всё ещё была на рассмотрении. Ко-
ский университет, Япония) удалось закристал-
манда Дж. Даудны опротестовала такое реше-
лизовать белок в комплексе с «гидом»-РНК
ние, после чего последовал долгий диспут между
и «мишенью»-ДНК (PDBe ID 4oo8, PDBe
двумя сторонами, включавший в себя судебные
DOI 10.2210/pdb4oo8/pdb).
разбирательства, апелляции и т.п. и в итоге при-
Эти, как и многие последующие исследо-
ведший к неоднозначной ситуации в области
вания, использовали в качестве объекта бе-
биотехнологии. В связи с тем, что к 2019 г. обе
лок Cas9 из S. pyogenes, SpCas9, состоящий из
конкурирующие стороны обладали патентами в
1368 аминокислот и представляющий собой
этой области, часть компаний, использовавших
мультидоменную и мультифункциональную
систему CRISPR-Cas9 на клетках человека,
эндонуклеазу. Кристаллические структуры по-
получили лицензию от команды Дж. Даудны,
казали, что белок Cas9 пространственно раз-
а часть - от Ф. Чжана. Однако апелляционная
делён на 2 части: распознающую и непосред-
комиссия Ведомства по патентам и товарным
ственно нуклеазную, а связывание РНК-«гида»
знакам США в феврале 2022 г. опять подтвер-
и ДНК-«мишени» происходит в положительно
дила приоритет Ф. Чжана и Института Броуд в
заряженном желобке на границе этих двух ча-
позиции держателя патента по использованию
стей. Ключевыми структурами нуклеазной ча-
CRISPR-Cas9 в клетках человека, что вызвало
сти SpCas9 являются 2 домена: HNH и RuvC,
гнев и недоумение у противоположной стороны
каждый из которых расщепляет одну из цепо-
и финансовые осложнения для компаний, полу-
чек мишени ДНК. На рис. 3 показана общая
чивших лицензии у команды Дж. Даудны [44].
архитектура комплекса SpCas9-sgRNA-DNA,
Дж. Даудна и Э. Шарпантье, однако, выиграли
где видна сложная вторичная структура связан-
сходный диспут в Европе, а также являются дер-
ной молекулы РНК и «развёрнутая» конфор-
жателями основных патентов по использованию
мация двуцепочечной молекулы ДНК с обра-
технологии в Великобритании, Китае, Японии,
зованием ДНК-РНК-дуплекса (PDB ID 5F9R,
Австралии, Новой Зеландии и Мексике [18].
PDB DOI 10.2210/pdb5F9R/pdb, [41]). На мо-
мент написания обзора сотни кристаллических
структур белков семейства Cas9 размещены на
ГЕННАЯ ТЕРАПИЯ И ЭТИЧЕСКИЕ
сайтах баз данных PDB, PDBe и PDBj.
ВОПРОСЫ, СВЯЗАННЫЕ С НЕЙ
Спешка, с которой конкурирующие ла-
ПАТЕНТНЫЙ ДИСПУТ
боратории стремились вывести свои исследо-
вания на суд общественности, а также гонка
Закономерным желанием отдельных учё-
патентирования данной технологии были без-
ных, а также организаций, вовлечённых в ис-
условными индикаторами значимости выше-
следование системы CRISPR-Cas9, было воз-
означенного научного прорыва. Бесспорно,
можное получение финансовой прибыли от
одной из главных движущих сил, мотивиро-
использования этой многообещающей техно-
вавших многих учёных принять участие в ис-
логии. Одна из первых патентных заявок была
следованиях с использованием именно этой
подана совместно Калифорнийским универ-
технологии, была потенциальная возможность
ситетом в Беркли, представлявшим Дж. Дауд-
модификации клеток человека, как соматиче-
ну, Венским университетом (где работал один
ских, так и зародышевой линии. Однако, не-
из двух ведущих авторов в ключевой статье по
смотря на очевидные преимущества системы
CRISPR-Cas9 [33]), а также Э. Шарпантье в
CRISPR-Cas9, многочисленные этические и
качестве индивидуального изобретателя в со-
технические трудности стоят на пути иссле-
ответствии с правилами Университета Умео
дователей, желающих воплотить мечты об из-
(Швеция), где Шарпантье работала на момент
лечении жизненно-опасных заболеваний в
выхода статьи [18]. Эта заявка на патент была
реальность, особенно если генетические изме-
подана на рассмотрение в мае 2012 г. [42], тог-
нения, полученные в результате таких манипу-
да как в декабре 2012 г. Институт Броуд в лице
ляций, могут передаться по наследству.
БИОХИМИЯ том 87 вып. 8 2022
1124
ГОСТИМСКАЯ
Впервые генная терапия была примене-
клетками может оказать отрицательное влия-
на в сентябре 1990 г.: четырёхлетняя девочка,
ние на область генной терапии, в целом, и на
страдающая от дефицита аденозиндезамина-
годы отбросит назад работу исследователей в
зы, получила переливание генетически моди-
попытках лечения генетических и инфекци-
фицированных Т-лимфоцитов. Клетки, взятые
онных заболеваний в соматических клетках.
из крови девочки, были обработаны с помо-
Опубликованные в марте 2015 г. отчёт о конфе-
щью вирусного вектора - деактивированного
ренции в Напе и комментарий, призывавший
вируса, несущего здоровую копию гена. Как
не редактировать геном эмбрионов человека,
отмечали журналисты, освещавшие историю,
были выпущены в обстановке всё возрастаю-
«редко в современной медицине столько на-
щего волнения в научных кругах, вызванного
дежд возлагается на один эксперимент», а док-
просочившимися новостями о непосредствен-
тора, проводившего эту процедуру, У. Френча
ном совершении таких экспериментов. Группа
Андерсона, называли «отцом генной терапии».
учёных из Университета имени Сунь Ятсена
В дальнейшем, однако, стали накапливать-
(Гуанчжоу, Китай), после неудачных попыток
ся волнующие результаты отрицательных по-
публикации работы в журналах Nature и Science,
бочных эффектов некоторых попыток генной
в апреле 2015 г. напечатала соответствующую
терапии как на животных, так и на человеке.
статью по применению системы CRISPR-Cas9
Поистине трагическая история Джесси Гелсин-
на клетках человеческих эмбрионов [48]. Ис-
джера, американского подростка из Филадель-
следователи подчёркивали, что использовали
фии, умершего от последствий генной терапии
нежизнеспособные эмбрионы, полученные
в 1999 г., потрясла мировую общественность
в результате слияния двух сперматозоидов с
и повлекла за собой серьёзный скептицизм и
одной яйцеклеткой и отбракованные лабора-
значительную задержку в развитии этой тех-
ториями экстракорпорального оплодотворе-
нологии. В случае Гелсинджера масштабный
ния (ЭКО). Главный вывод статьи заключался
аутоиммуный ответ организма на вирусный
в том, что технология CRISPR-Cas9 на момент
вектор, несущий ген орнитинтранскарбамила-
исследования ещё не была готова к использо-
зы, привёл к резкому повышению температуры
ванию на эмбриональных клетках человека
тела, почечной и лёгочной недостаточности,
вследствие выявленных недостатков работы
желтухе, нарушению свёртываемости крови и
системы в отношении эффективности и специ-
последующей смерти в течение всего 4 дней с
фичности совершённых ей модификаций.
момента применения генной терапии [45].
Комментарий журнала Protein & Cell (Пекин,
Обширные дискуссии на тему безопасности
Китай), опубликовавшего эту работу, состоял в
и, что немаловажно, этичности потенциальной
том, что эта статья (помимо её научной ценно-
генной терапии с использованием CRISPR-
сти) способствует открытому обмену информа-
Cas9 начались вскоре после первых публика-
цией о текущих исследованиях, и несмотря на
ций, показавших возможность использования
неоднозначность вопроса и противоречивость
этой системы на клетках человека. Один из
мнений, должна по крайней мере послужить
первых шагов в инициации формальных пере-
началом необходимых дискуссий о геномном
говоров был совершён Дж. Даудной, созвавшей
редактировании клеток зародышевой линии.
конференцию по обсуждению научных, меди-
Заявка на публикацию была отправлена авто-
цинских, юридических и этических вопросов,
рами в редакцию Protein & Cell в совокупности
связанных с геномными модификациями, со-
с отзывами рецензентов, полученными во вре-
стоявшуюся в долине Напа в Калифорнии в
мя предыдущих попыток размещения работы,
январе 2015 г. Последующий отчёт по итогам
и принят редакцией к публикации в течение
конференции был опубликован в марте 2015 г.
2 дней с момента подачи заявки. Последующие
в журнале Science [46] и, по сути, призывал к
дебаты в научном сообществе были описаны
временному сдерживанию работы по внесению
как «эпические» [49] и спровоцировали инте-
наследуемых изменений в клетки эмбрионов
рес к этому сложному вопросу у более широкой
человека, по крайней мере, на время активных
публики, а также в правительственных и регу-
обсуждений социальных, экологических и эти-
ляторных кругах различных стран.
ческих последствий таких манипуляций. Прак-
Известные скандалы, вызванные проведе-
тически одновременно с этим отчётом в журна-
нием медицинских экспериментов на людях в
ле Nature также был опубликован комментарий
прошлом, привели к созданию общих между-
о серьёзных рисках создания наследуемых из-
народных рекомендаций по биоэтике. Наибо-
менений в эмбрионах человека [47]. Помимо
лее известными документами в этой области
прочего, авторы высказывали опасения, что
являются Нюрнбергский кодекс, разработан-
преждевременная работа над эмбриональными
ный после судебного процесса над врачами-на-
БИОХИМИЯ том 87 вып. 8 2022
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1125
цистами в 1947 г., и последующая Хельсинкская
ности к своей персоне. Оказалось, что Дз. Хэ
декларация 1964 г., расширяющая принципы
изучал физику в Университете науки и техноло-
кодекса и интерпретирующая применение этих
гии (Хэфей, Китай), а потом переехал в США,
принципов к клиническим исследованиям.
где получил степень PhD под руководством
Ещё один важный документ, Бельмонтский до-
профессора физики, астрономии и биоинжене-
клад, был выпущен Национальной комиссией
рии Майкла Дима в Университете Райса (Хью-
по защите человека при проведении биомеди-
стон, Техас), и в дальнейшем работал в Стэн-
цинских и поведенческих исследований в США
фордском университете (Калифорния) в
в 1978 г. Эта комиссия была создана в резуль-
лаборатории профессора Стивена Квейка.
тате шокирующего скандала, произошедшего
В группе М. Дима Дз. Хэ использовал методы
после утечки в прессу подробностей негуман-
теоретической биофизики, математического
ного исследования сифилиса в Таскиги с 1932
моделирования и компьютерных симуляций,
по 1972 г. («The Tuskegee Study of Untreated
опубликовав работы, посвящённые, помимо
Syphilis»). В течение десятилетий сотни муж-
прочего, вирусным штаммам гриппа и последо-
чин из бедного афроамериканского населения,
вательностям спейсеров в локусах CRISPR [50,
заражённых сифилисом, изучались врачами
51], тогда как в лаборатории под руководством
на предмет прогрессирования их заболевания.
С. Квейка он обучился методам молекулярной
И хотя пенициллин стал стандартным методом
биологии и заинтересовался инновационными
его излечения к 1947 г., участникам исследова-
технологиями силиконовой долины. Вернув-
ния лечение не было предложено, несмотря на
шись в Китай, Дз. Хэ продолжил сотрудниче-
очевидные физические страдания заражённых
ство с М. Димом, а также успешно воплотил в
и продолжение распространения инфекции в
жизнь инновационную идею в области метода
их семьях.
ДНК-секвенирования своего второго научного
Упомянутые выше Нюрнбергский кодекс,
руководителя, С. Квейка, создав успешную
Хельсинкская декларация и Бельмонтский до-
компанию «Direct Genomics» на основе его тех-
клад основаны на базовых этических принци-
нологии [18, 52]. В Китае он был достаточно
пах биомедицинских исследований, таких как
знаменит как молодой учёный и успешный
уважение личности, информированное согла-
предприниматель, вернувшийся из-за рубежа
сие пациента, понимание рисков и благ, добро-
по известной программе «Тысяча талантов»,
вольность участия, справедливость проведения
получивший позицию и лабораторию в Юж-
экспериментов, максимальный профессиона-
ном научно-технологическом университете
лизм исследователя и т.п. Эти принципы и их
(SUStech, г. Шэньджень) и участвовавший в
применение в медицинской практике стали
создании нескольких стартап-компаний [53].
чрезвычайно актуальны после событий ноября
Следующим шагом в его карьере, однако, стала
2018 г., когда китайский учёный Дзянкуй Хэ
сомнительная попытка внести вклад в историю
объявил о рождении младенцев, впервые про-
и совершить, по его мнению, научный прорыв,
шедших генную модификацию с помощью си-
способный изменить будущее человечества.
стемы CRISPR-Cas9. Инъекция этой системы
Вместо этого результатом его работы стал са-
в яйцеклетку матери была произведена на этапе
мый большой медицинский скандал как мини-
процедуры ЭКО непосредственно после слия-
мум десятилетия. В 2017 г. Дз. Хэ начал набор
ния с ней сперматозоида, и, соответственно,
добровольцев из числа семейных пар, желаю-
все изменения, потенциально привнесённые в
щих произвести на свет генетически модифи-
геном в течение этой процедуры, являлись на-
цированное потомство, резистентное к вирусу
следуемыми. Мировая научная общественность
иммунодефицита человека (ВИЧ). В числе ус-
была шокирована преждевременностью таких
ловий, например, было наличие высшего обра-
медицинских экспериментов и степенью риска,
зования у пары, желавшей участвовать в экспе-
принятого китайскими исследователями, по-
рименте, так, чтобы их участие происходило
шедшими на эксперимент. В особенности учё-
при адекватном уровне понимания ими основ
ных волновала возможность создания незапла-
науки и медицины. Следующим условием было
нированных («офф-таргет») мутаций в геноме
наличие в паре ВИЧ-положительного мужчины
будущих младенцев. Дз. Хэ (также известный в
и ВИЧ-отрицательной женщины: ситуация,
англоязычной среде под укороченным име-
при которой риск передачи вируса будущему
нем JK - Jiankui He) на момент проведения
младенцу был бы минимален (при условии
эксперимента не был известной фигурой в кру-
«промывания» спермы во время процеду-
гах исследователей CRISPR-Cas9, однако по-
ры ЭКО), однако мотивация пары участвовать в
сле заявления о его экспериментах привлёк
эксперименте была бы высока [53]. В планы
огромный интерес международной обществен-
Дз. Хэ входила генетическая модификация
БИОХИМИЯ том 87 вып. 8 2022
1126
ГОСТИМСКАЯ
гена CCR5, известного рецептора на поверхно-
что два эмбриона были подсажены в матку бу-
сти клеток, через связывание с которым проис-
дущей матери в надежде на то, что хотя бы один
ходит проникновение вируса иммунодефицита
из них приведёт к рождению младенца с геном-
человека в клетку. Около 300 человек отозва-
ной модификацией. Близнецы родились зна-
лись на объявление Дз. Хэ, из них - 20 пар
чительно раньше срока (на 31 неделе) и прове-
были отобраны для следующего этапа консуль-
ли первые недели своей жизни в инкубаторах
таций, на котором участникам объяснялась
неонатального отделения, однако в остальном
процедура и возможная степень риска. В ре-
были описаны как «здоровые» [53]. Учёные,
зультате этих консультаций 11 пар дали согла-
получившие доступ к неопубликованному ма-
сие на участие в исследованиях, из которых 7 в
нускрипту Дз. Хэ, также заметили, что несколь-
конечном итоге были отобраны исследователя-
ко клеток, отобранные для секвенирования на
ми для следующего этапа - непосредственного
ранних этапах развития эмбрионов, свидетель-
проведения процедуры ЭКО, включающего
ствовали о явлении мозаицизма - наблюдение,
этап геномного редактирования. Мотивацией
приведшее к усиленной критике работы Дз. Хэ.
отдельных участников было, судя по всему, не
В случае мозаицизма любая информация, по-
только возможность заведения детей (процеду-
лученная в ходе секвенирования отобранных
ра ЭКО в Китае запрещена при наличии
клеток, не может быть экстраполирована на
ВИЧ-инфекции у одного из родителей), но и
весь эмбрион в целом. Соответственно, на мо-
желание принятия участия в «историческом»
мент принятия ключевого решения о перенесе-
эксперименте, призванном принести благо бу-
нии эмбрионов в утробу матери исследователи
дущим поколениям как их страны, так и всего
не могли быть уверены в том, что система
человечества [53]. В конечном итоге после не-
CRISPR-Cas9 не произвела драматических не-
скольких неудачных попыток из отобранной
запланированных мутаций в остальных клет-
группы участников и после всех проведённых
ках эмбрионов, даже если результаты секвени-
процедур 2 беременности привели к рождению
рования показывали отсутствие таковых в
младенцев, прошедших процедуру геномной
отобранных клетках. Многие другие аспекты
модификации с помощью системы CRISPR-
проведения исследования также получили су-
Cas9. Достаточно много известно о первой бе-
ровую критику со стороны научной и медицин-
ременности, в результате которой родились две
ской общественности [54], включая сомни-
девочки-близнецы, Лулу и Нана (псевдонимы,
тельные обстоятельства получения разрешения
используемые в прессе и научной литературе).
от этического комитета одной из больниц горо-
Совсем незначительное количество информа-
да Шэньджень, уровень квалификации самого
ции доступно о второй беременности, в резуль-
Дз. Хэ для проведения клинических исследова-
тате которой родился ещё один ребёнок. Так
ний (отсутствие медицинского образования и
как это событие произошло уже после сканда-
достаточного опыта работы в этой области),
ла, вызванного рождением первых близнецов,
выбор гена, подвергшегося редактированию
то многие детали второй беременности оста-
(скорее социальные, чем медицинские причи-
лись в тайне. Манускрипт, написанный Дз. Хэ
ны обращений пациентов за помощью), воз-
по результатам первой беремeнности, «Рожде-
можные побочные эффекты отсутствия дей-
ние близнецов после геномного редактирова-
ствующей копии CCR5 и др. По словам
ния для ВИЧ-резистентности» («Birth of twins
американского кардиолога и профессора меди-
after genome editing for HIV resistance»), так и
цины Пенсильванского университета Кирана
остался неопубликованным, однако все же
Мусунуру, первые
«младенцы поколения
просочился в научное сообщество [54, 55]. Ста-
CRISPR», к сожалению, родились не в резуль-
ло известно, например, что в одном из эмбрио-
тате исторического научного достижения, а в
нов обе копии CCR5 были инактивирова-
результате исторического этического фиа-
ны (Нана), тогда как во втором - только
ско [56]. Пиар-кампания, проведённая Дз. Хэ и
одна (Лулу) [56]. Следовательно, при всех про-
его командой, обеспечила достаточно лестное
чих благоприятных обстоятельствах только
начальное освещение новостей о его работе в
Нана в будущем будет защищена от инфекции
газете Жэньминь Жибао (Народная ежедневная
ВИЧ (по крайней мере от основных вариантов
газета Китая), однако последующий междуна-
вируса, проникающих в клетку через связыва-
родный скандал привёл к помещению Дз. Хэ
ние с рецептором CCR5). В случае Лулу, к со-
под домашний арест, а затем и к тюремному за-
жалению, защиты от вируса не будет, так как
ключению сроком на 3 года. В настоящий мо-
одной копии гена CCR5 достаточно, чтобы
мент Дз. Хэ уже освобождён из тюрьмы, однако
произвести соответствующий рецептор на
мало что известно о его местонахождении и
мембране. Очевидцы происходящего полагают,
дальнейших планах [57].
БИОХИМИЯ том 87 вып. 8 2022
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1127
Спустя несколько месяцев после сканда-
межуточную или неопределившуюся позицию.
ла с Дз. Хэ российский учёный Д.В. Ребриков
Ситуация с внесением наследуемых геномных
повторно всколыхнул международное научное
изменений в эмбрионы, впоследствии исполь-
сообщество своими заявлениями о намерении
зуемые для репродуктивных целей, ещё более
стать вторым в мире учёным, создавшим ген-
сложная [44].
но-модифицированных младенцев. Профессор
Российского национального исследовательско-
го медицинского университета им. Пирогова и
МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ
заведующий лабораторией геномного редак-
НА СОМАТИЧЕСКИХ КЛЕТКАХ ЧЕЛОВЕКА
тирования в Центре акушерства, гинекологии
и перинатологии, Д.В. Ребриков сообщил о
Несмотря на повышенное внимание, при-
своей потенциальной готовности к пересадке
влечённое к внесению наследуемых изменений
модифицированных эмбрионов в утробу мате-
в клетках зародышевой линии, менее спор-
ри в июне 2019 г. [58]. Как и в экспериментах
ным и более распространённым на данный
Дз. Хэ, предполагалось редактирование гена
момент применением CRISPR-Cas9 в меди-
CCR5, а предварительная работа лаборатории
цинских целях является модификация сомати-
на нежизнеспособных эмбрионах ранее была
ческих клеток человека. Как уже было упомя-
опубликована в Вестнике РГМУ [59]. Реакция
нуто выше, в первых попытках генной терапии
научной общественности на заявление была
(1990 г.) использовался аденоассоциирован-
очень бурной и в большинстве своём крити-
ный вирусный вектор, доставлявший здоровую
ческой, а журналы Nature и Science в октябре
копию гена в клетки (в США эта технология
2019 г. опубликовали новостные ленты, сооб-
была окончательно одобрена к использованию
щавшие, что Д.В. Ребриков на тот момент уже
в клинике только в 2017 г. [63]). Дальнейшим
переключился на редактирование гена GJB2,
шагом в развитии генной инженерии стало
связанного с наследуемой глухотой, и подби-
возможное применение геномного редакти-
рал пары, согласные принять участие в экс-
рования с использованием хоуминг-эндону-
перименте [60, 61]. Однако в многочисленных
клеаз (HEs, Homing Endonucleases), нукле-
интервью журналистам Д.В. Ребриков подчёр-
аз с мотивом цинковых пальцев (ZFNs, Zinc
кивал, что обязательное получение всех необ-
Finger Nucleases) и эффекторных нуклеаз,
ходимых разрешений как от регуляторных ор-
подобных активатору транскрипции TALENs
ганов, так и этических является непременным
(Transcription Activator-Like Effector Nucleases),
условием проведением его экспериментов. Это
а в дальнейшем - и CRISPR-Cas9 [64]. Первые
радикально отличало подход Д.В. Ребрикова от
клинические исследования с использованием
ситуации с Дз. Хэ, который, по сути, сообщил
CRISPR-Cas9 на человеке начались в октябре
широкой научной общественности о рождении
2016 г. в Китае [65]. Ген PD-1 был инактивиро-
младенцев с модифицированным геномом пост-
ван в клетках крови ex vivo в надежде, что такие
фактум. Министерство здравоохранения РФ (в
клетки после возвращения в кровообращение
соответствии с рекомендацией Всемирной ор-
смогут побороть немелкоклеточный рак лёг-
ганизации здравоохранения) позднее сделало
кого, от которого страдал пациент. В США
заявление, что решение о выдаче разрешения
ex vivo терапия с использованием CRISPR-
на такое исследование было бы преждевремен-
Cas9 была впервые проведена в июле 2019 г.
ным и безответственным, что и приостанови-
на пациентке с серповидноклеточной анемией
ло дальнейшее развитие ситуации, по крайней
(компания «CRISPR Тherapeutics», основанная
мере, до изменения обстановки в регулятор-
Э. Шарпантье). Терапия значительно улучши-
ной сфере [62].
ла состояние пациентки по крайней мере на
На время написания обзора состояние
несколько месяцев после процедуры, однако,
правовой базы, обеспечивающeй регуляцию
к сожалению, цена такого лечения на момент
вопроса геномного редактирования эмбрио-
его проведения в США оценивалась в районе
нальных клеток человека, сильно различается в
0,5-1,5 млн долларов. Высокая цена терапии
разных государствах. Так, геномные модифика-
с использованием CRISPR-Cas9, естествен-
ции эмбрионов в целях, отличных от репродук-
но, может послужить препятствием на пути её
тивных, разрешены как минимум в 11 странах,
более широкого применения в будущем, даже
включающих Китай, США и Великобританию.
если клинические исследования подтвердят
Девятнадцать стран, включающих Беларусь,
эффективность и безопасность такого лече-
Канаду, Швецию и Швейцарию, запрещают
ния [18]. Интересно заметить, что самым доро-
проведение таких экспериментов. Многие дру-
гим лекарством на момент написания обзора
гие страны (Россия в их числе) занимают про-
является ещё один препарат генной терапии,
БИОХИМИЯ том 87 вып. 8 2022
1128
ГОСТИМСКАЯ
Золгенсма, использующийся для лечения спи-
необычных примеров применения системы
нальной мышечной атрофии (2,125 млн долла-
CRISPR-Cas9 стало выращивание мозгопо-
ров США за одну дозу лекарства). Золгенсма
добных органоидов, несущих различные ва-
непосредственно доставляет в клетки действую-
рианты важного гена NOVA1, характерного для
щую копию дефектного гена с помощью аде-
современного человека, неандертальца и дени-
ноассоциированного вируса - метод, отлич-
совского человека [69]. Разработка технологии
ный от геномного редактирования с помощью
применения CRISPR-Cas9 - один из нагляд-
нуклеаз [66].
ных примеров того, как находки, совершённые
Первый пример клинических исследова-
в ходе фундаментальных исследований, могут
ний in vivo, при котором клетки проходят ге-
изменить целые области науки и технологии,
номное редактирование с помощью нуклеаз
расширяя горизонты возможного. Можно
in situ, был проведён с использованием техно-
предположить, что развитие этой новаторской
логии ZFNs. Компания «Sangamo Therapeutics»
техники является достойным продолжением
впервые применила эту процедуру в июле
таких захватывающих событий в науке, как пуб-
2017 г. на пациенте, страдавшем от синдрома
ликация двуцепочечной структуры ДНК Уот-
Хантера (редкое генетическое заболевание,
соном и Криком в 1953 г., рождение первого
форма мукополисахаридоза). Пионерами в
ребёнка путём экстракорпорального оплодо-
применении CRISPR-Cas9 для геномного ре-
творения в 1978 г. и клонирование овечки Дол-
дактирования in vivo в марте 2020 г. стала ком-
ли в 1996 г. Научное сообщество в ближайшие
пания «Editas Medicine» [67]. Препарат под
годы будет с интересом наблюдать за развити-
названием EDIT-101 был введён локально в
ем законодательства и этических норм в при-
сетчатку пациенту, страдавшему от одной из
менении системы CRISPR-Cas9 в геномном
форм наследуемой слепоты, вызванной мута-
редактировании, а также за тем, в каких ещё
цией в гене CEP290. В настоящий момент ве-
областях познавательной деятельности сможет
дутся различные клинические исследования по
найти своё применение эта многообещающая
применению CRISPR-Cas9 для лечения таких
технология.
заболеваний, как, например, болезнь Альцгей-
мера, различные формы раковых изменений,
повышенный холестерол, ангиоэдема, острый
Благодарности. Автор с теплом и благодар-
миелоидный лейкоз и даже андрогенетическая
ностью вспоминает годы, проведённые в ла-
алопеция (облысение). Отдельным перспек-
боратории Андрея Дмитриевича Виноградова
тивным направлением для применения систе-
на кафедре биохимии МГУ имени М.В. Ломо-
мы CRISPR-Cas9 в будущем может послужить
носова. Эксперименты, задуманные Андреем
лечение инфекционных заболеваний, вызван-
Дмитриевичем, неизменно приносили инте-
ных такими патогенами как, например, вирус
ресные результаты, а его обширнейшие знания
иммунодефицита человека (ВИЧ) и вирус па-
в различных областях науки позволяли сотруд-
пилломы человека (ВПЧ) [64].
никам и студентам чувствовать уверенность в
том, что на любые вопросы будут даны ответы,
а время, проведённое в лаборатории, принесёт
ЗАКЛЮЧЕНИЕ
заслуженные плоды. Публикации результатов
работы, проведённой под руководством Андрея
Открытие CRISPR-Cas9 как иммунной
Дмитриевича, дали автору необходимый старт
системы прокариот на рубеже XX-XXI ве-
в научной жизни и возможность продолжения
ков - открытие, на первый взгляд, казалось
проведения исследований уже в других лабо-
бы, из разряда фундаментальной микробиоло-
раториях и в других областях знаний. Уникаль-
гии - привело к революционным изменениям
ная команда учёных, подобранная Андреем
в области совершения геномных манипуляций
Дмитриевичем: Вера Георгиевна Гривенникова,
за рекордно короткие сроки. Новые возможно-
Татьяна Вадимовна Жарова и Элеонора Влади-
сти открылись и в других областях биомедици-
мировна Гаврикова, - обеспечила семейную
ны, таких как молекулярная диагностика ин-
атмосферу доверия и поддержки в лаборато-
фекционных и неинфекционных заболеваний
рии, за что автор чрезвычайно благодарна.
(генотипирование бактериальных штаммов,
Конфликт интересов. Автор заявляет об от-
детекция вирусов и обнаружение генетиче-
сутствии конфликта интересов.
ских мутаций в циркулирующей внеклеточной
Соблюдение этических норм. Настоящая
ДНК у пациентов с раком лёгких [68]), а также
статья не содержит описания выполненных ав-
в разработке потенциально нового метода им-
тором исследований с участием людей или жи-
мунизации, ДНК-вакцин [18]. Одним из более
вотных в качестве объектов.
БИОХИМИЯ том 87 вып. 8 2022
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1129
СПИСОК ЛИТЕРАТУРЫ
1.
Ishino, Y., Shinagawa, H., Makino, K., Amemura,
of class 2 CRISPR-Cas systems, Nat. Rev. Microbiol.,
M., and Nakatura, A. (1987) Nucleotide sequence
15, 169-182, doi: 10.1038/nrmicro.2016.184.
of the iap gene, responsible for alkaline phosphatase
14.
Abudayyeh, O. O., Gootenberg, J. S., Konermann,
isoenzyme conversion in Escherichia coli, and identi-
S., Joung, J., Slaymaker, I. M., et al. (2016) C2c2 is a
fication of the gene product, J. Bacteriol., 169, 5429-
single-component programmable RNA-guided RNA-
5433, doi: 10.1128/jb.169.12.5429-5433.1987.
targeting CRISPR effector, Science, 353, aaf5573-
2.
Groenen, P. M., Bunschoten, A. E., van Soolingen,
aaf5573, doi: 10.1126/science.aaf5573.
D., and van Embden, J. D. (1993) Nature of DNA
15.
Abudayyeh, O. O., Gootenberg, J. S., Essletzbichler,
polymorphism in the direct repeat cluster of Myco-
P., Han, S., Joung, J., et al. (2017) RNA targeting with
bacterium tuberculosis; application for strain differen-
CRISPR-Cas13, Nature, 550, 280-284, doi: 10.1038/
tiation by a novel typing method, Mol. Microbiol., 10,
nature24049.
1057-1065, doi: 10.1111/j.1365-2958.1993.tb00976.x.
16.
Barrangou, R., Fremaux, C., Deveau, H., Richards, M.,
3.
Hoe, N., Nakashima, K., Grigsby, D., Pan, X.,
Boyaval, P., et al. (2007) CRISPR provides acquired
Dou, S. J., Naidich, S., et al.(1999) Rapid molecu-
resistance against viruses in prokaryotes, Science, 315,
lar genetic subtyping of serotype M1 group A Strep-
1709-1712.
tococcus strains, Emerg. Infect. Diseases, 5, 254-263,
17.
Horvath, P., Barrangou, R., Fremaux, C., Boyaval,
doi: 10.3201/eid0502.990210.
P., and Romero, D. (2007) Use of a Cas Gene in
4.
Mojica, F. J. M., Juez, G., and Rodriguez-Valera, F.
Combination with CRISPR Repeats for Modulating
(1993) Transcription at different salinities of Haloferax
Resistance in a Cell. US Patent Application No. PCT/
mediterranei sequences adjacent to partially modified
US2006/033167 (initially filed on 26.08.2005).
PstI sites, Mol. Microbiol., 9, 613-621, doi: 10.1111/
18.
Isaacson, W.
(2021) The Code Breaker: Jennifer
j.1365-2958.1993.tb01721.x.
Doudna, Gene Editing, and the Future of the Human
5.
Mojica, F. J. M., Díez-Villaseñor, C., García-
Race, Simon & Schuster (New York, USA).
Martínez, J., and Soria, E.
(2005) Intervening
19.
Masepohl, B., Görlitz, K., and Böhme, H. (1996)
sequences of regularly spaced prokaryotic repeats
Long tandemly repeated repetitive (LTRR) sequences
derive from foreign genetic elements, J. Mol. Evol., 60,
in the filamentous cyanobacterium Anabaena sp.
174-182, doi: 10.1007/s00239-004-0046-3.
PCC 7120, Biochim. Biophys. Acta Gene Struct. Expr.,
6.
Bolotin, A., Quinquis, B., Sorokin, A., and Dusko
1307, 26-30, doi: 10.1016/0167-4781(96)00040-1.
Ehrlich, S. (2005) Clustered regularly interspaced
20.
Flamand, M.-C., Goblet, J.-P., Duc, G., Briquet,
short palindrome repeats (CRISPRs) have spacers of
M., and Boutry, M. (1992) Sequence and transcrip-
extrachromosomal origin, Microbiology, 151, 2551-
tion analysis of mitochondrial plasmids isolated from
2561, doi: 10.1099/mic.0.28048-0.
cytoplasmic male-sterile lines of Vicia faba, Plant Mol.
7.
Pourcel, C., Salvignol, G., and Vergnaud, G. (2005)
Biol., 19, 913-923.
CRISPR elements in Yersinia pestis acquire new repeats
21.
Mojica, F. J. M., Díez-Villaseñor, C., Soria, E., and
by preferential uptake of bacteriophage DNA, and pro-
Juez, G. (2000) Biological significance of a family of
vide additional tools for evolutionary studies, Microbi-
regularly spaced repeats in the genomes of Archaea,
ology, 151, 653-663, doi: 10.1099/mic.0.27437-0.
Bacteria and mitochondria, Mol. Microbiol., 36, 244-
8.
Popkov, V. A., Zorova, L. D., Korvigo, I. O., Silachev,
246, doi: 10.1046/j.1365-2958.2000.01838.x.
D. N., Jankauskas, S. S., et al. (2016) Do mitochon-
22.
Jansen, R., van Embden, J. D. A., Gaastra, W., and
dria have an immune system? Biochemistry (Moscow),
Schouls, L. M. (2002) Identification of genes that
81, 1229-1236, doi: 10.1134/S0006297916100217.
are associated with DNA repeats in prokaryotes,
9.
Isaev, A. B., Musharova, O. S., and Severinov, K. V.
Mol. Microbiol., 43, 1565-1575, doi: 10.1046/j.1365-
(2021) Microbial arsenal of antiviral defenses. Part I,
2958.2002.02839.x.
Biochemistry (Moscow), 86, 319-337, doi: 10.1134/
23.
Makarova, K. S., Aravind, L., Grishin, N. V.,
S0006297921030081.
Rogozin, I. B., and Koonin, E. V. (2002) A DNA
10.
Isaev, A. B., Musharova, O. S., and Severinov, K. V.
repair system specific for thermophilic Archaea and
(2021) Microbial arsenal of antiviral defenses. Part II,
bacteria predicted by genomic context analysis,
Biochemistry (Moscow), 86, 449-470, doi: 10.1134/
Nucleic Acids Res.,
30,
482-496, doi:
10.1093/
S0006297921040064.
nar/30.2.482.
11.
Marraffini, L. A., and Sontheimer, E. J.
(2008)
24.
Shmakov, S. A., Makarova, K. S., Wolf, Y. I.,
CRISPR interference limits horizontal gene transfer
Severinov, K. V., and Koonin, E. V. (2018) Systematic
in staphylococci by targeting DNA, Science, 322,
prediction of genes functionally linked to CRISPR-
1843-1845, doi: 10.1126/science.1165771.
Cas systems by gene neighborhood analysis, Proc.
12.
Shmakov, S., Abudayyeh, O. O., Makarova, K. S.,
Natl. Acad. Sci. USA, 115, E5307-E5316, doi: 10.1073/
Wolf, Y. I., Gootenberg, J. S., et al. (2015) Discovery
pnas.1803440115.
and functional characterization of diverse class
2
25.
Makarova, K. S., Wolf, Y. I., Iranzo, J., Shmakov,
CRISPR-Cas systems, Mol. Cell,
60,
385-397,
S. A., Alkhnbashi, O. S., et al. (2020) Evolutionary
doi: 10.1016/j.molcel.2015.10.008.
classification of CRISPR-Cas systems: a burst of
13.
Shmakov, S., Smargon, A., Scott, D., Cox, D.,
class 2 and derived variants, Nat. Rev. Microbiol., 18,
Pyzocha, N., V. et al. (2017) Diversity and evolution
67-83, doi: 10.1038/s41579-019-0299-x.
9
БИОХИМИЯ том 87 вып. 8 2022
1130
ГОСТИМСКАЯ
26.
Makarova, K. S., Wolf, Y. I., and Koonin, E. V. (2013)
Cas9 in complex with guide RNA and target DNA,
The basic building blocks and evolution of CRISPR-
Cell, 156, 935-949, doi: 10.1016/j.cell.2014.02.001.
Cas systems, Biochem. Soc. Trans., 41, 1392-1400,
41.
Jiang, F., Taylor, D. W., Chen, J. S., Kornfeld, J. E.,
doi: 10.1042/BST20130038.
Zhou, K., et al. (2016) Structures of a CRISPR-Cas9
27.
Koonin, E. V., Makarova, K. S., and Zhang, F. (2017)
R-loop complex primed for DNA cleavage, Science,
Diversity, classification and evolution of CRISPR-
351, 867-871, doi: 10.1126/science.aad8282.
Cas systems, Curr. Opin. Microbiol.,
37,
67-78,
42.
Jinek, M., Doudna, J., Charpentier, E., and
doi: 10.1016/j.mib.2017.05.008.
Chylinski, K. (2013) Methods and Composition for
28.
Koonin, E. V., and Makarova, K. S. (2019) Origins
RNA-Directed Target DNA Modification and for
and evolution of CRISPR-Cas systems, Philos.
RNA-Directed Modulation of Transcription. US
Trans. R. Soc. B Biol. Sci., 374, 20180087-20180087,
Patent Application No. 61/652,086 (initially filed on
doi: 10.1098/rstb.2018.0087.
25.05.2012).
29.
Mojica, F. J. M., Díez-Villaseñor, C., García-
43.
Zhang, F.
(2014) CRISPR-Cas9 Systems and
Martínez, J., and Almendros, C. (2009) Short motif
Methods for Altering Expression of Gene Products.
sequences determine the targets of the prokaryotic
US Patent No. 8,697,359 (provisional application
CRISPR defence system, Microbiology, 155, 733-740,
No. 61/736,527 filed on 12.12.2012).
doi: 10.1099/mic.0.023960-0.
44.
Baylis, F., Darnovsky, M., Hasson, K., and Krahn,
30.
Brouns, S. J. J., Jore, M. M., Lundgren, M., Westra,
T. M. (2020) Human germline and heritable genome
E. R., Slij khuis, R. J., et al. (2008) Small CRISPR
editing: the global policy landscape, CRISPR J., 3,
RNAs guide antiviral defense in prokaryotes, Science,
365-377, doi: 10.1089/crispr.2020.0082.
321, 960-964, doi: 10.1126/science.1159689.
45.
Stolberg, S. G. (1999) The biotech death of Jesse
31.
Gasiunas, G., Barrangou, R., Horvath, P., and
Gelsinger, New York Times Magazine, 136-150.
Siksnys, V. (2012) Cas9-crRNA ribonucleoprotein
46.
Baltimore, D., Berg, P., Botchan, M., Carroll, D.,
complex mediates specific DNA cleavage for adaptive
Charo, R. A., et al. (2015) A prudent path forward for
immunity in bacteria, Proc. Natl. Acad. Sci. USA, 109,
genomic engineering and germline gene modification,
E2579-E2586, doi: 10.1073/pnas.1208507109.
Science, 348, 36-38, doi: 10.1126/science.aab1028.
32.
Deltcheva, E., Chylinski, K., Sharma, C. M.,
47.
Lanphier, E., Urnov, F., Haecker, S. E., Werner, M.,
Gonzales, K., Chao, Y., et al. (2011) CRISPR RNA
et al. (2015) Don’t edit the human germ line, Nature,
maturation by trans-encoded small RNA and host
519, 410-411, doi: 10.1038/519410a.
factor RNase III, Nature, 471, 602-607, doi: 10.1038/
48.
Liang, P., Xu, Y., Zhang, X., Ding, C., Huang, R.,
nature09886.
et al. (2015) CRISPR/Cas9-mediated gene editing in
33.
Jinek, M., Chylinski, K., Fonfara, I., Hauer, M.,
human tripronuclear zygotes, Protein Cell, 6, 363-372,
Doudna, J. A., et al. (2012) A programmable dual-
doi: 10.1007/s13238-015-0153-5.
RNA-guided DNA endonuclease in adaptive bacterial
49.
Cyranoski, D., and Reardon, S.
(2015) Embryo
immunity, Science,
337,
816-821, doi:
10.1126/
editing sparks epic debate, Nature, 520, 593-594,
science.1225829.
doi: 10.1038/520593a.
34.
Mali, P., Yang, L., Esvelt, K. M., Aach, J., Guell, M.,
50.
He, J., and Deem, M. W. (2010) Heterogeneous
et al. (2013) RNA-guided human genome engineering
diversity of spacers within CRISPR (clustered
via Cas9, Science,
339,
823-826, doi:
10.1126/
regularly interspaced short palindromic repeats),
science.1232033.
Phys. Rev. Lett.,
105,
128102, doi:
10.1103/
35.
Cong, L., Ran, F. A., Cox, D., Lin, S., Barretto,
PhysRevLett.105.128102.
R., et al.
(2013) Multiplex genome engineering
51.
He, J., and Deem, M. W. (2010) Low-dimensional clus-
using CRISPR/Cas systems, Science, 339, 819-823,
tering detects incipient dominant influenza strain clus-
doi: 10.1126/science.1231143.
ters, PEDS, 23, 935-946, doi: 10.1093/protein/gzq078.
36.
Jinek, M., East, A., Cheng, A., Lin, S., Ma, E., and
52.
Cyranoski, D.
(2016) Direct genomics revives
Doudna, J. (2013) RNA-programmed genome editing
Helicos sequencing system for China’s hospitals, Nat.
in human cells, eLife, 2, 1-9, doi: 10.7554/eLife.00471.
Biotechnol., 34, 122-123, doi: 10.1038/nbt0216-122b.
37.
Cho, S. W., Kim, S., Kim, J. M., and Kim, J. S.
53.
Kirksey, E. (2021) The Mutant Project. Inside the
(2013) Targeted genome engineering in human cells
Global Race to Genetically Modify Humans, Bristol
with the Cas9 RNA-guided endonuclease, Nat.
University Press, U.K.
Biotechnol., 31, 230-232, doi: 10.1038/nbt.2507.
54.
Regalado, A. (2019) China’s CRISPR babies: read
38.
Hwang, W. Y., Fu, Y., Reyon, D., Maeder, M. L.,
exclusive excerpts from the unseen original research,
Tsai, S. Q., et al. (2013) Efficient genome editing
MIT Technology Review. Biotechnology.
in zebrafish using a CRISPR-Cas system, Nat.
55.
Regalado, A. (2019) Why the paper on the CRISPR
Biotechnol., 31, 227-229, doi: 10.1038/nbt.2501.
babies stayed secret for so long, MIT Technology
39.
Jinek, M., Jiang, F., Taylor, D. W., Sternberg,
Review. Biotechnology.
S. H., Kaya, E., et al. (2014) Structures of Cas9
56.
Musunuru, K.
(2019) The CRISPR Generation:
endonucleases reveal RNA-mediated conformational
The Story of the World’s First Gene-Edited Babies,
activation,
Science,
343,
1247997-1247997,
BookBaby, N.J., U.S.A.
doi: 10.1126/science.1247997.
57.
Regalado, A. (2022) The creator of the CRISPR
40.
Nishimasu, H., Ran, F. A., Hsu, P. D., Konermann,
babies has been released from a Chinese prison, MIT
S., Shehata, S. I., et al. (2014) Crystal structure of
Technology Review. Biotechnology.
БИОХИМИЯ том 87 вып. 8 2022
CRISPR-CAS9: ИСТОРИЯ И ЭТИЧЕСКИЕ АСПЕКТЫ
1131
58. Cyranoski, D. (2019) Russian biologist plans more
63. Smalley, E. (2017) First AAV gene therapy poised for
CRISPR-edited babies, Nature,
570,
145-146,
landmark approval, Nat. Biotechnol., 35, 998-999,
doi: 10.1038/d41586-019-01770-x.
doi: 10.1038/nbt1117-998.
59. Kodyleva, T. A., Kirillova, A. O., Tyschik, E.
64. Porteus, M. H. (2019) A new class of medicines
A., Makarov, V. V., Khromov, A. V., et al. (2018)
through DNA editing, N. Engl. J. Med., 380, 947-959,
The efficacy of CRISPR-Cas9-mediated induc-
doi: 10.1056/NEJMra1800729.
tion of the CCR5delta32 mutation in the human
65. Cyranoski, D. (2016) CRISPR gene-editing tested
embryo, Bull. RSMU,
4,
70-74, doi:
10.24075/
in a person for the first time, Nature, 539, 479-479,
brsmu.2018.052.
doi: 10.1038/nature.2016.20988.
60. Cohen, J. (2019) Embattled Russian scientist sharpens
66. Editorial (2019) Gene therapy’s next installment, Nat.
plans to create gene-edited babies, Science. News.,
Biotechnol., 37, 697-697, doi: 10.1038/s41587-019-0194-z.
doi: 10.1126/science.aaz9337.
67. Ledford, H.
(2020) CRISPR treatment inserted
61. Cyranoski, D. (2019) Russian “CRISPR-baby” sci-
directly into the body for first time, Nature, 579, 185,
entist has started editing genes in human eggs with
doi: 10.1038/d41586-020-00655-8.
goal of altering deaf gene, Nature, 574, 465-466,
68. Chertow, D. S. (2018) Next-generation diagnostics with
doi: 10.1038/d41586-019-03018-0.
CRISPR, Science, 360, 381-382, doi: 10.1126/science.aat4982.
62. Meyer, M. (2020) The CRISPR babies controversy:
69. Remmel, A. (2021) Neanderthal-like “mini-brains”
responsibility and regulation in the spotlight, EMBO
created in lab with CRISPR, Nature, 590, 376-377,
Rep., 21, e50307, doi: 10.15252/embr.202050307.
doi: 10.1038/d41586-021-00388-2.
CRISPR-CAS9: A HISTORY OF ITS DISCOVERY AND ETHICAL
CONSIDERATIONS OF ITS USE IN GENOME EDITING
Review
I. Gostimskaya
The University of Manchester, M1 7DN, Manchester, United Kingdom; e-mail: gostimskaya@gmail.com
The development of a method for genome editing based on CRISPR-Cas9 technology was awarded The Nobel
Prize in Chemistry in 2020, less than a decade after the discovery of all principal molecular components of
the system. For the first time in history a Nobel prize was awarded to two women, Emmanuelle Charpentier
and Jennifer Doudna, who made key discoveries in the field of DNA manipulation with the CRISPR-Cas9
system, so-called “genetic scissors”. It is difficult to overestimate the importance of the technique as it enables
one not only to manipulate genomes of model organisms in scientific experiments, and modify characteristics
of important crops and animals, but also has the potential of introducing revolutionary changes in medicine,
especially in treatment of genetic diseases. The original biological function of CRISPR-Cas9 system is the
protection of prokaryotes from mobile genetic elements, in particular viruses. Currently, CRISPR-Cas9 and
related technologies have been successfully used to cure life-threatening diseases, make coronavirus detection
tests, and even to modify human embryo cells with the consequent birth of babies carrying the introduced
modifications. This intervention with human germplasm cells resulted in wide disapproval in the scientific
community due to ethical concerns, and calls for a moratorium on inheritable genomic manipulations. This
review focuses on the history of discovery of the CRISPR-Cas9 system with some aspects of its current
applications, including ethical concerns about its use in humans.
Keywords: CRISPR-Cas9, genome editing, “genetic scissors”, ethical considerations
БИОХИМИЯ том 87 вып. 8 2022
9*