БИОХИМИЯ, 2023, том 88, вып. 11, с. 2183 - 2205
УДК 577.218
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
ТЕРАПЕВТИЧЕСКИХ НУКЛЕИНОВЫХ КИСЛОТ.
МЕХАНИЗМЫ И ПОТЕНЦИАЛ ПРИМЕНЕНИЯ В МЕДИЦИНЕ
Обзор
© 2023 Е.Д. Тимотиевич*, И.П. Шиловский, М.Р. Хаитов
ФГБУ «ГНЦ Институт иммунологии» ФМБА России,
115522 Москва, Россия; электронная почта: ed0594@yandex.ru
Поступила в редакцию 31.03.2023
После доработки 13.09.2023
Принята к публикации 15.09.2023
В настоящее время разрабатывается значительное количество лекарственных и профилактиче-
ских средств, содержащих терапевтические нуклеиновые кислоты, для лечения онкологических,
воспалительных, инфекционных заболеваний, а также заболеваний, связанных с нарушением об-
мена веществ. Растёт число одобренных к использованию подобных препаратов, что демонстри-
рует перспективность генной терапии. Свой биологический эффект терапевтические нуклеиновые
кислоты реализуют в цитоплазме клетки, при этом плазматическая мембрана является основным
препятствием для их внутриклеточной доставки. Поэтому при разработке подобных препаратов
зачастую используют специально созданные носители. Оптимальный носитель должен не толь-
ко обеспечивать интернализацию нуклеиновых кислот, но и быть малотоксичным, стабильным,
а также несложным и незатратным в производстве. Всем этим требованиям соответствуют так
называемые проникающие пептиды (СРР), которые зарекомендовали себя как эффективные
и малотоксичные носители нуклеиновых кислот. CPP представляют собой основные пептиды
с положительным зарядом при физиологическом значении pH, которые способны формировать
наноструктуры с отрицательно заряженными нуклеиновыми кислотами. Многочисленные докли-
нические исследования, в которых CPP использовали в роли носителя, показали многообещающие
результаты, что в отдельных случаях обеспечило успешное прохождение клинических испытаний
и внедрение препарата в медицинскую практику. В данном обзоре мы рассматриваем многообра-
зие терапевтических нуклеиновых кислот, а также обобщаем опыт использования СРР для их внут-
риклеточной доставки. Кроме того, обсуждается классификация и механизмы поглощения CPP
клетками, понимание которых позволит ускорить разработку новых генно-терапевтических лекар-
ственные средств.
КЛЮЧЕВЫЕ СЛОВА: проникающие пептиды, пептидные средства доставки, средства доставки нуклеи-
новых кислот, миРНК.
DOI: 10.31857/S032097252311012X, EDN: MNWBMS
ВВЕДЕНИЕ
нуклеиновых кислот широкое распростране-
ние в медицине получают РНК- и ДНК-вак-
За последние два десятилетия существенно
цины [1]. Также создаются олигонуклеотидные
выросло количество разработок новых лекар-
препараты, в состав которых входят анти-
ственных средств, в составе которых в качестве
смысловые олигонуклеотиды (АСО), аптаме-
фармацевтических субстанций используются
ры, молекулы малых интерферирующих РНК
нуклеиновые кислоты. Среди терапевтических (миРНК) и другие [2].
Принятые сокращения: АСО - антисмысловые олигонуклеотиды; миРНК - малые интерферирующие РНК; CeNA-
нуклеотиды - циклогексеновые нуклеиновые кислоты; CPP - проникающие пептиды; DRBD - РНК-связывающий
домен; EGS - внешняя направляющая последовательность; HBV - вирус гепатита В человека; LNA-нуклеотиды -
замкнутые нуклеиновые кислоты; PIP2 - фосфатидилинозитол-4,5-дифосфат; PNA-нуклеотиды - нуклеотиды, моди-
фицированные с использованием пептидо-нуклеиновых кислот; PMO - фосфородиамидат-морфолиновый олигомер;
RISC - сайленсинговый комплекс, индуцируемый молекулами РНК.
* Адресат для корреспонденции.
2183
2184
ТИМОТИЕВИЧ и др.
Несмотря на огромный потенциал, ис-
клинических испытаний (NCT02508337).
пользование нуклеиновых кислот в качестве
Другие препараты на основе пептидов (KAI,
терапевтических средств сопряжено с рядом
POD, TAT-aFGF-His и TAT-μCL) находятся
сложностей; они подвержены разрушению нук-
в стадии разработки [13]. Использование CPP
леазами организма, могут элиминироваться
является потенциальным методом улучшения
фагоцитарной системой и ферментами пече-
биодоступности инсулина. Альтернативой под-
ни. Однако главной сложностью остаётся эф-
кожных инъекций является использование
фективная доставка терапевтических молекул
перорального инсулина, однако при таком
к месту действия [3]. Эта проблема частично
способе применения он имеет низкую биодо-
решена путём использования различных век-
ступность. Доставка инсулина с использова-
торов доставки как вирусной, так и невирус-
нием CPP является многообещающим под-
ной природы. Известны вирусные векторы на
ходом [11, 14]. Обширная область применения
основе лентивирусов и аденовирусов, однако,
СРР - это разработка новых подходов для те-
несмотря на высокую эффективность, вирус-
рапии и профилактики вирусных инфекций.
ные векторы обладают рядом существенных
К настоящему времени на основе СРР созда-
недостатков [4, 5]. Среди невирусных векторов
ют противовирусные препараты, а также вак-
широко распространены наночастицы (в том
цины [15] против таких патогенов как: вирус
числе липосомы, полимерные наночастицы) и
гепатита С, риновирус, коксакивирус, респи-
пептиды [6].
раторно-синцитиальный вирус, вирус Эбола,
В последние десятилетия активно разра-
грипп типа А, ВИЧ-1, папиллома вирус, гер-
батывают пептидные носители для доставки
песвирус, SARS-CoV-2 и др. [16].
различных терапевтических молекул в клетки-
В последние десятилетия активно развива-
мишени. К настоящему моменту изучается
ется область использования пептидных век-
возможность применения проникающих пеп-
торных систем для доставки терапевтических
тидов (cell penetrating peptides, СРР) в препара-
нуклеиновых кислот. К достоинствам СРР, в
тах для лечения онкологических заболеваний
сравнении с другими векторами, можно отнес-
(рак молочной железы, колоректальный рак,
ти биодеградируемость и биосовместимость,
рак лёгких и пр.), для чего используют пепти-
относительную простоту в получении, стан-
ды с собственной противоопухолевой (онко-
дартизации и хранении. Кроме того, в отличие
литической) активностью либо способных це-
от вирусных векторов, они не иммуногенны
ленаправленно доставлять противоопухолевый
и не приводят к мутациям [15]. В этом обзоре
препарат [7-9]. СРР способны доставлять те-
мы обобщаем последние разработки в области
рапевтические молекулы не только в опреде-
создания и использования векторов на основе
лённые клетки, но и органеллы. Например,
пептидов для доставки терапевтических нук-
пептид на основе TAT способен проникать в
леиновых кислот.
митохондрии клеток и доставлять в них анти-
оксидантный белок hMT1A, который умень-
шает образование активных форм кислорода и
ТЕРАПЕВТИЧЕСКИЕ
тем самым в экспериментальной модели пред-
НУКЛЕИНОВЫЕ КИСЛОТЫ
отвращает формирование проявлений болезни
Паркинсона [10, 11]. Широко исследуется воз-
Благодаря своей высокой специфичности,
можность применения СРР в целях ингиби-
функциональному разнообразию и низкой ток-
рования воспалительных процессов [9]. Из-
сичности терапевтические нуклеиновые кис-
вестны СРР, направленные против STAT3, ин-
лоты имеют огромные перспективы исполь-
гибирование которого значительно нивели-
зования в медицине. Главным образом эти
рует воспаление при псориазе. Противовос-
препараты способны специфично подавлять
палительные препараты на основе СРР часто
экспрессию целевых генов по различным ме-
применяют трансдермально, что является
ханизмам: АСО, рибозимы, ДНКзимы, внеш-
оправданным, т.к. некоторые их модификации
ние направляющие последовательности (EGS),
хорошо проникают через роговой слой кож-
миРНК и т.д. (табл. 1). В настоящее время для
ных покровов [11, 12]. Ряд исследований опи-
медицинского применения одобрено не менее
сывает применение СРР в офтальмологии,
15 препаратов, содержащих нуклеиновые кис-
т.к. их удобно использовать в форме глазных
лоты [2], 7 из которых в своём составе содер-
капель. Препарат XG-102, имеющий в своём
жат невирусные векторы доставки [2, 17].
составе пептид TAT, используется для умень-
АСО - это, как правило, одноцепочеч-
шения воспаления глаз после операции по
ные синтетические ДНК-олигонуклеотиды
удалению катаракты и успешно прошёл фазу 3
длиной 15-25 н. Их эффекты обусловлены
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2185
Таблица 1. Характеристика и молекулярные механизмы технологий специфического подавления генной экспрессии
Тип
Мишень
Характеристика агента
Механизм действия
данный тип АСО после связывания с мРНК-
мишенью способен рекрутировать клеточную
одноцепочечные синтетические
АСО
РНКазу Н, тем самым усиливать деградацию
ДНК-олигонуклеотиды,
первого
мРНК
мРНК-мишени, что в итоге увеличивает
состоящие из 15-25
поколения
супрессию гена;
фосфоротиоатных нуклеотидов
недостатки - неспецифический иммунный
ответ, токсичность
взаимодействуют с мРНК-мишенью
с увеличенной аффинностью, что приводит
одноцепочечные синтетические
к подавлению генной экспрессии за счёт
АСО
ДНК-олигонуклеотиды,
стерической блокады процесса трансляции;
второго
мРНК
состоящие из 15-25 2′MOE-
недостатки - не рекрутирует клеточный
поколения
нуклеотидов
фермент РНКаза Н, поэтому проявляет более
слабый эффект супрессии гена в сравнении
с АСО первого поколения
одноцепочечные синтетические
АСО
ДНК-олигонуклеотиды,
стерическая блокада процесса трансляции;
третьего
мРНК
состоящие из 15-25 PNA-,
длительность биологического эффекта
поколения
FANA-, CeNA-,
достигается за счёт устойчивости к ДНКазам
LNA-нуклеотидов
одноцепочечные синтетические
за счёт распознавания структуры с высокой
Аптамеры
белок
молекулы ДНК или РНК
аффинностью связываются с белковой
длиной 56-120 н.
мишенью
рибозимы комплементарно связываются
каталитически активные
Рибозимы
мРНК
с молекулами мРНК и самостоятельно
одноцепочечные молекулы РНК
катализируют её расщепление
ДНКзимы комплементарно связываются
с молекулами мРНК и в присутствии
каталитически активные
двухвалентных ионов магния самостоятельно
ДНКзимы
мРНК
одноцепочечные молекулы ДНК
катализируют расщепление мРНК в участке
между неспаренным пурином (R) и спаренным
пиримидином (Y) гетеродуплекса ДНК/РНК
EGS комплементарно связываются
синтетические одноцепочечные
с молекулой мРНК, после чего расщепляет
EGS
мРНК
молекулы РНК размером
её посредством клеточного фермента
15-20 н.
РНКазы Р
ДНК-ловушки имитируют участки
ДНК-
белок (факторы
двуцепочечные ДНК-
промоторов, тем самым конкурируют
ловушки
транскрипции)
олигонуклеотиды
с естественным геном за транскрипционные
факторы
в ядре клетки U1-адаптор за счёт целевого
участка специфически взаимодействует
с пре-мРНК-мишенью, а за счёт
консервативного U1-домена взаимодействует
синтетический олигонуклеотид,
с рибонуклеопротеиновым комплексом,
U1-
состоящий из 30-50 РНК, ДНК
пре-мРНК
который обеспечивает разрезание пре-мРНК-
адапторы
или модифицированных
мишени в области сайта полиаденилирования;
нуклеотидов
в результате этого пре-мРНК лишается
поли-А-хвоста, защищающего её от действия
РНКаз и быстро деградирует, что в итоге обес-
печивает подавление экспрессии гена в целом
при помощи комплекса RISC осуществляется
РНК-дуплексы
миРНК
мРНК
специфическое разрезание мРНК гена-
размером 21-25 п.н.
мишени в определённых участках
БИОХИМИЯ том 88 вып. 11 2023
2186
ТИМОТИЕВИЧ и др.
Таблица 1 (продолжение)
Тип
Мишень
Характеристика агента
Механизм действия
мРНК-
одноцепочечные
-
препараты
полноразмерные мРНК
напрямую вводятся в организм, кодируя
целевой белок (например, антигены вакцин)
ДНК-
рекомбинантные
-
препараты
ДНК-плазмиды
Примечание. PNA-нуклеотиды - нуклеотиды, модифицированные с использованием пептидо-нуклеиновых кислот;
FANA-нуклеотиды - 2′-дезокси-2′-фтор-β-D-арабинонуклеиновые кислоты; CeNA-нуклеотиды - циклогексеновые
нуклеиновые кислоты; LNA-нуклеотиды - замкнутые нуклеиновые кислоты; 2′MOE-модификация - модифициро-
ванные нуклеотиды, содержащие алкил-модификацию в 2′-позиции рибозы.
гибридизацией с мРНК-мишенью по прин-
торые практически не подвергаются деграда-
ципу комплементарности, в результате чего
ции нуклеазами. Два препарата на основе АСО
стерически затрудняется трансляция белка.
одобрены для медицинского применения:
Некоторые АСО проектируются таким обра-
фомивирсен - на основе АСО первого поко-
зом, чтобы при взаимодействии с мРНК-ми-
ления для лечения цитомегаловирусного рети-
шенью активировалась РНКаза Н, которая рас-
нита и мипомерсен - на основе АСО второго
щепляет целевую мРНК, что позволяет увели-
поколения для лечения гиперхолестеринемии.
чить активность. Разработано несколько поко-
Множество (более 50) подобных препаратов
лений АСО.
находится на стадии клинических исследова-
АСО первого поколения состоят из модифи-
ний [18].
цированных нуклеотидов (фосфоротиоатная
Аптамеры представляют собой одноцепо-
модификация), благодаря чему они приобре-
чечные синтетические молекулы ДНК или
тают устойчивость к воздействию нуклеаз.
РНК длиной 56-120 н., сходные по структуре
Данный тип АСО рекрутирует РНКазу Н для
с AСO. Аптамеры выступают в роли «ловушек»
деградации мРНК-мишени. Недостатками дан-
для белков; они могут с высокой аффинностью
ного поколения АСО являются возможность
связываться целевыми белками, нарушая их
запуска нежелательных иммунных реакций, а
функционирование. В отличие от АСО, аптаме-
также способность неспецифически взаимо-
ры осуществляют свой эффект не посредством
действовать с клеточными белками, что ока-
комплементарного взаимодействия оснований,
зывает токсический эффект.
а подобно антителам, взаимодействуя с белко-
АСО второго поколения состоят из модифи-
вой мишенью. Таким образом, они представ-
цированных нуклеотидов, содержащих алкил-
ляют собой привлекательную альтернативу мо-
модификацию в
2′-позиции рибозы
(2′-O-
ноклональным антителам, поскольку мало
methoxyethyl-oligonucleotides или так называе-
токсичны, неиммуногенны, хорошо проника-
мая 2′MOE-модификация). Данный тип АСО
ют в ткани, относительно просты в получении
устойчив к действию нуклеаз, а также взаимо-
и могут вводиться как внутривенно, так и под-
действует с мРНК-мишенью с увеличенной
кожно [3].
аффинностью. Однако этот тип АСО менее
Рибозимы - каталитически активные од-
эффективен в сравнении с первым поко-
ноцепочечные молекулы РНК, способствую-
лением, поскольку не привлекает клеточную
щие специфичному расщеплению мРНК-ми-
РНКазу Н, а подавление генной экспрессии
шеней. За счёт особой третичной структуры
происходит за счёт стерической блокады фер-
рибозимы формируют две петли, которые свя-
ментов трансляции.
зываются с мРНК-мишенью и образуют ката-
Третье поколение АСО состоит из нуклео-
литическое ядро, расщепляющее молекулы
тидов с иными модификациями нуклеотидов.
мРНК. Рибозимы имеют свои недостатки - они
Например, проектируются АСО на основе
малоустойчивы к РНКазам, и поэтому требуют
пептидо-нуклеиновых кислот (PNA - peptide
стабилизации, что увеличивает себестоимость
nucleic acids), 2′-дезокси-2′-фтор-β-D-араби-
синтеза.
нонуклеиновых кислот (FANA - 2′-deoxy-2′-
ДНКзимы - это каталитически активные
fluoro-β-D-arabinonucleic acids), «замкнутых»
одноцепочечные молекулы ДНК. Как и рибо-
нуклеиновых кислот (LNA - locked nucleic
зимы они имеют собственный каталитиче-
acids),
циклогексен-нуклеиновых кислот
ский центр, способный расщеплять молекулы
(CeNA - cyclohexene nucleic acids) и др. [3], ко-
мРНК без привлечения нуклеаз. ДНКзимы
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2187
более стабильны и менее затратны для про-
никшие, например, в результате вирусной
изводства, чем рибозимы, но в сравнении
инфекции, на короткие дуплексы - миРНК.
с миРНК обладают большими размерами и
На эффекторном этапе миРНК соединяются
сложны в синтезе.
с белковыми факторами, образуя мультисубъ-
EGS (External guide sequence) - это синте-
единичный комплекс RISC (RNA-induced si-
тические одноцепочечные РНК-олигонуклео-
lencing complex - сайленсинговый комплекс,
тиды размером 15-20 н. В цитоплазме клетки
индуцируемый молекулами РНК). В состав
EGS связываются с мРНК-мишенью по прин-
комплекса входит белок AGO, который обес-
ципу комплементарности, после чего мРНК
печивает специфичность взаимодействия с
разрезается в районе дуплекса посредством
мРНК-мишенью. После связывания с целе-
клеточного фермента РНКазы Р (RNAse P).
вой мРНК комплекс RISC осуществляет её
Благодаря активации этого фермента EGS эф-
первичное разрезание, а в дальнейшую дегра-
фективно подавляют ген-мишень, однако они
дацию вовлекаются экзонуклеазы клетки.
неустойчивы к действию РНКаз [19].
Введение в клетки искусственных миРНК необ-
ДНК-ловушки - это двуцепочечные ДНК-
ходимого размера (в среднем 21 п.н.) с заданной
олигонуклеотиды, имитирующие участки про-
последовательностью позволяет избежать про-
моторов. Благодаря такому сходству они свя-
цессинга ферментом Dicer, в результате чего
зываются с транскрипционными факторами,
они сразу же включаются в комплекс RISC
тем самым конкурируют с естественным ге-
и осуществляют специфическое подавление
ном, подавляя его активность [20].
экспрессии гена-мишени. В отличие от одно-
U1-адапторы - это синтетические олиго-
цепочечных рибозимов, EGS и U1-адапторов,
нуклеотиды, состоящие из 30-50 н. РНК, ДНК
двуцепочечные молекулы миРНК более устой-
или модифицированных нуклеотидов. Струк-
чивы к РНКазам, к тому же для увеличения
турно U1-адаптор состоит из двух участков;
их устойчивости и эффективности разрабо-
целевой участок - располагается на 5′-конце
таны разные способы модификации нуклео-
U1-адаптора, он проектируется комплемен-
тидов [24]. На сегодняшний день было ини-
тарным 3′-концевому экзону мРНК-мишени,
циировано более 30 клинических испытаний
благодаря чему U1-адаптор способен распо-
препаратов на основе миРНК. По данным на
знавать мРНК-мишень; второй участок пред-
2022 год, 6 препаратов на основе миРНК про-
ставляет собой консервативный U1-домен,
тив вируса гепатита B (HBV) проходят кли-
который способен гибридизоваться с малой
нические испытания: ARC-520, ARB-1467,
ядерной РНК (мяРНК), которая, в свою оче-
AB-729, RG-6346, VIR-2218 и JNJ-3989 [25].
редь, входит в состав рибонуклеопротеинового
Недавно было зарегистрировано первое ле-
комплекса, обладающего нуклеазной актив-
карственное средство - Inclesiran (разработ-
ностью. Процесс подавления экспрессии по-
чик Alnylam Pharmaceuticals, приобретена ли-
средством U1-адаптора происходит в ядре, а
цензия компанией
«Novartis») для лечения
не в цитоплазме. U1-адаптор за счёт таргент-
пациентов с атеросклеротическим сердечно-
ного участка специфически взаимодействует
сосудистым заболеванием и гиперхолестери-
с мРНК-предшественником (пре-мРНК), а за
немией [26]. Позднее FDA (Управление по
счёт консервативного U1-домена взаимодей-
санитарному надзору за качеством пище-
ствует с рибонуклеопротеиновым комплексом,
вых продуктов и медикаментов) одобрило
который обеспечивает разрезание пре-мРНК-
ещё 3 препарата на основе миРНК (patisiran,
мишени в области сайта полиаденилирования.
givosiran и lumasiran) [27], а в РФ был заре-
В результате этого пре-мРНК лишается поли-
гистрирован препарат МИР 19 для лечения
А-хвоста, защищающего её от действия РНКаз,
COVID-19 [17, 28].
и быстро деградирует, что в итоге обеспечива-
Препараты на основе мРНК. Основным
ет подавление экспрессии целевого гена [21].
классом препаратов, содержащих молекулы
миРНК - двуцепочечные молекулы РНК
мРНК, являются вакцины [29]. Преимущество
размером 21-25 п.н., способные специфично
мРНК заключается в способности одной та-
подавлять экспрессию генов по механизму
кой молекулы экспрессировать несколько
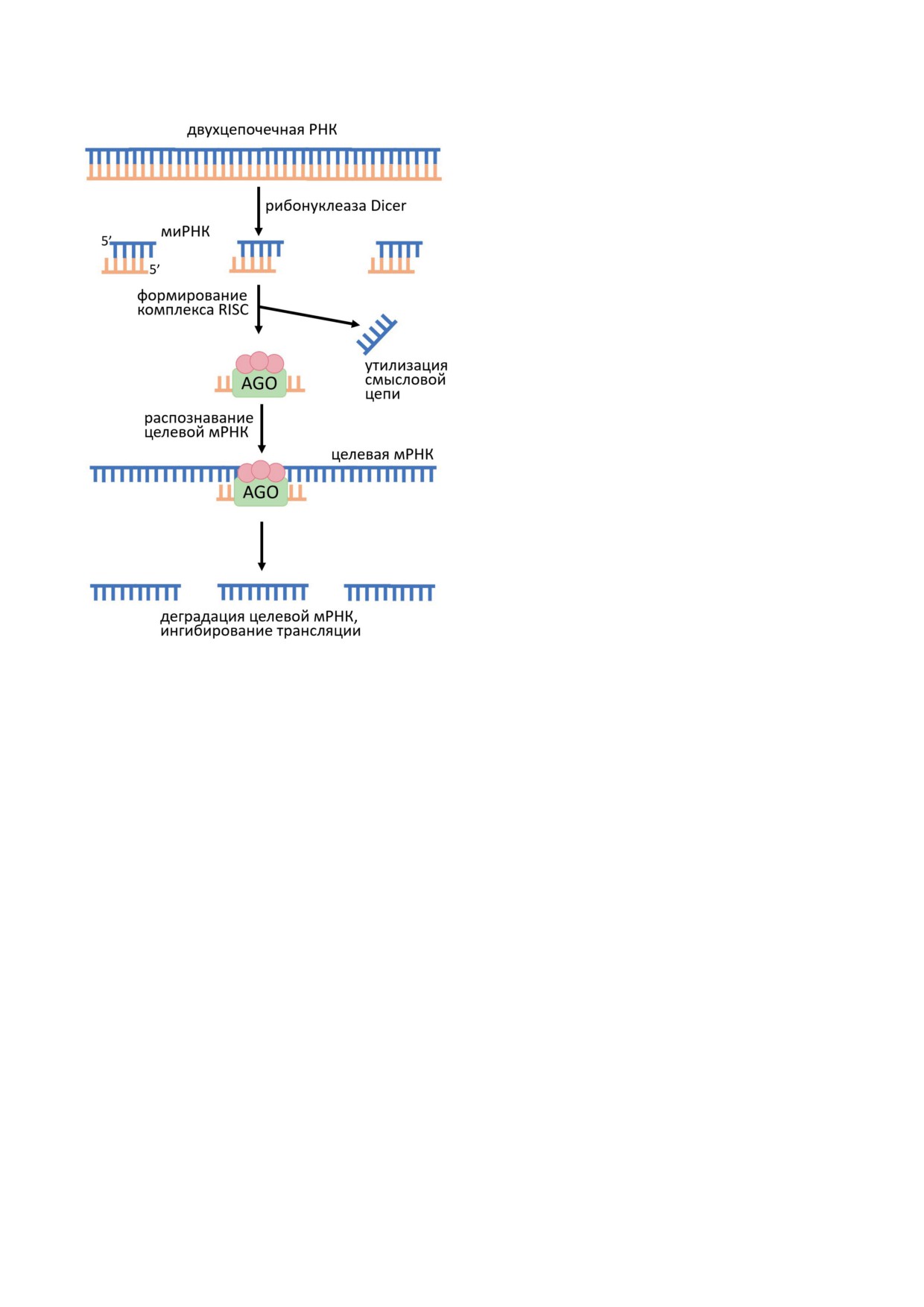
интерференции РНК [22] (рис. 1). Молекуляр-
целевых белков. К ограничениям мРНК-
ный механизм интерференции РНК включает
препаратов относят низкую стабильность и
два этапа: этап инициации и эффекторный
иммуногенность (т.к. часто мРНК содержат
этап [23]. На этапе инициации центральная
иммуностимулирующие последовательности).
роль принадлежит ферменту Dicer, который
К тому же, в отличии от относительно неболь-
находится в цитоплазме и фрагментирует
ших молекул миРНК и АСО, доставка крупных
крупные молекулы двуцепочечной РНК, про-
мРНК является более сложной задачей [3].
БИОХИМИЯ том 88 вып. 11 2023
2188
ТИМОТИЕВИЧ и др.
лизован при создании таких препаратов как:
Imlygic® (talimogene laherparepvec) на основе
вируса простого герпеса для терапии мела-
ном, Luxturna® (voretigene neparvovec) на ос-
нове аденоассоциированного вируса для ле-
чения ретинальной дистрофии и Zolgensma®
(onasemnogene abeparvovec) на основе аденоас-
социированного вируса для терапии спиналь-
ной мышечной атрофии и других [31].
Из вышеописанных технологий самой пер-
спективной с точки зрения эффективности и
экономической целесообразности является
технология РНК-интерференции. Сразу по-
сле открытия данного явления и выяснения
молекулярного механизма начаты попытки его
внедрения в медицинскую практику. Как уже
упоминалось выше, внедрению технологии
РНК-интерференции препятствует низкая ста-
бильность молекул миРНК в сыворотке крови
и отсутствие высокоэффективного и безопас-
ного агента для их адресной доставки в цито-
плазму клеток-мишеней. В настоящий момент
ведутся исследования по созданию невирус-
ных средств доставки на основе катионных
липосом, пептидов и полимеров, а также со-
здаются новые модификации молекул нуклеи-
новых кислот, устойчивых к действию РНКаз.
Все эти разработки в скором времени увели-
Рис. 1. Схема механизма РНК-интерференции. Моле-
чат возможности использования нуклеиновых
кулярный механизм интерференции РНК включает два
кислот в терапевтических целях.
этапа: этап инициации (I) и эффекторный этап (II).
На этапе I дцРНК расщепляется ферментом Dicer с обра-
зованием миРНК. На этапе II миРНК связываются с нук-
леазным комплексом RISC. Хеликаза, присутствующая в
НЕВИРУСНЫЕ СИСТЕМЫ
комплексе, расплетает молекулу миРНК, при этом анти-
ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ
смысловая цепь остаётся в комплексе. Она направляет
комплекс к родственной мРНК, что обеспечивает специ-
Среди невирусных векторов можно выде-
фичность взаимодействия с мРНК-мишенью и приводит
к её расщеплению
лить липосомы, экзосомы, наночастицы раз-
личной природы, катионные полимеры, пеп-
тиды и др. [4].
Тем не менее на основе этой технологии созда-
Липосомы - это один из наиболее часто
но более 60 препаратов, включая мРНК-вак-
используемых векторов для доставки нуклеи-
цины для профилактики COVID-19 от компа-
новых кислот. Они, как правило, состоят из
ний «Pfizer-BioNTech» и «Moderna» [3, 30].
катионных и/или амфифильных липидов и
ДНК-препараты представляют собой плаз-
холестерина. Их «популярность» объясняется
миды, несущие необходимый генетический ма-
относительной простотой формирования ком-
териал. Такие плазмидные ДНК-препараты на-
плекса с нуклеиновыми кислотами (часто
прямую вводятся в организм, где экспресси-
за счёт электростатического взаимодействия),
руют целевой белок (антиген) [3]. Активно раз-
высокой эффективностью доставки в целевые
рабатывались ДНК-вакцины, кодирующие бе-
клетки, а также тем фактом, что поверхность
лок-антиген. Однако они демонстрируют низ-
липосомы можно функционализировать раз-
кую эффективность, что побуждает множество
личными лигандами для увеличения троп-
научных коллективов по всему миру работать
ности к целевым клеткам и тканям. Однако
над оптимизацией состава и увеличением их
липосомы не лишены таких недостатков, как
иммуногенности. В настоящее время наиболее
низкая стабильность (из-за возможности се-
перспективным генотерапевтическим подхо-
диментации частиц), высокая токсичность,
дом для доставки ДНК является использо-
а также необходимость в дополнительных ме-
вание вирусных векторов. Этот подход реа-
тодах контроля качества при производстве.
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2189
В настоящее время зарегистрировано не ме-
чеством функциональных групп, которые
нее трёх РНК-препаратов на основе липо-
можно модифицировать и задавать необходи-
сом, включая Patisiran компании «Alnylam»,
мые биологические свойства. Однако у таких
BNT162b2 компании «Pfizer» и мРНК-1273 ком-
полимеров есть некоторые недостатки: корот-
пании «Moderna» [6].
кий период полувыведения и токсичность [4].
Экзосомы представляют собой природные
Основываясь на вышесказанном, можно
наночастицы (везикулы), инкапсулированные
сделать вывод, что для достижения терапев-
липидным бислоем, которые образуются в
тического эффекта системы доставки должны
результате отпочкования от эукариотических
быть нетоксичными, стабильными в биологи-
клеток. Считается, что экзосомы осущест-
ческих средах, успешно связываться нуклеи-
вляют межклеточную коммуникацию путём
новыми кислотами и проникать в клетки-ми-
транспорта макромолекул (нуклеиновых кис-
шени. Кроме того, при внедрении в широкую
лот, белков и липидов), по этой причине они
медицинскую практику важными аспектами
представляют интерес с точки зрения достав-
становятся относительная простота получе-
ки терапевтических олигонуклеотидов. Они,
ния и контроля качества, а также возможность
как правило, менее токсичны, в сравнении с
масштабирования производства. Большинству
липосомами, и способны проходить через био-
этих требований отвечают векторы для достав-
логические барьеры, например ГЭБ. Однако
ки терапевтических нуклеиновых кислот на
экзосомы менее эффективно (в сравнении с
основе СРР.
липосомами) связываются с транспортируе-
мыми нуклеиновыми кислотами. Тем не менее
несколько препаратов на их основе (производ-
СТРУКТУРА И КЛАССИФИКАЦИЯ
ства компаний «Codiak Biosciences» и «Evox
ТРАНСПОРТНЫХ ПЕПТИДОВ
Therapeutics») находятся на стадии доклиниче-
ских исследований [32].
CPP обычно имеют размер 5-30 а.о., при
Наночастицы различного рода также ис-
этом в их составе присутствует значительное
пользуют для доставки нуклеиновых кислот.
количество основных аминокислот (аргинин
Например, гибридные наночастицы, состоя-
и лизин), которые обеспечивают позитив-
щие из различных материалов (липиды, поли-
ный заряд молекулы в водных растворах при
меры и пептиды), объединяя преимущества
физиологическом значении рН. Зачастую CPP
каждого компонента [4]. Описаны также век-
имеют амфипатичную структуру, т.е. одна
торы на основе наночастиц золота [4], диок-
часть пептида обладает гидрофобными свой-
сида кремния и пр. материалов [6].
ствами, а другая - гидрофильными. СРР спо-
Векторы на основе полимеров имеют ряд
собны не только самостоятельно проникать
преимуществ в сравнении с липосомами.
внутрь клетки, но и транспортировать в цито-
В частности, они менее иммуногенны и легко
плазму различные терапевтические агенты [35,
поддаются модификации, за счёт чего можно
36], включая нуклеиновые кислоты [24].
формировать их физико-химические свойства
История исследований СРР началась с
(заряд, стабильность и молекулярную массу) и
открытия белка ВИЧ ТAT, который способен
тем самым регулировать растворимость, троп-
проникать и транспортировать различные со-
ность к тканям и фармакокинетику. Одним из
единения в клетки млекопитающих. На сего-
первых полимеров для доставки нуклеиновых
дняшний день база данных CPPsite 2.0 (http://
кислот начал использоваться полиэтиленимин
crdd.osdd.net/raghava/cppsite/) описывает более
и его производные. Однако широкое приме-
1700 уникальных пептидов с транспортной
нение этих соединений ограничено их ток-
активностью. Кроме того, описанию свойств
сичностью [33, 34]. Другой полимер - PLGA
и характеристик CPP посвящён ряд современ-
(поли-(D,L-лактид-ко-гликолид) - нетоксичен
ных обзоров [37-39].
и одобрен для использования в медицине. Од-
Существует несколько классификаций СРР.
нако ввиду отсутствия положительного заряда
Согласно классификации, учитывающей размер
он электростатически не взаимодействует с
и физико-химические свойства, CPP подразде-
нуклеиновыми кислотами. Тем не менее ве-
ляют на первичные амфипатические, вторичные
дутся работы по созданию его производных,
амфипатические и неамфипатические пептиды.
адаптированных для доставки терапевтических
Первичные амфипатические пептиды обыч-
нуклеиновых кислот [34]. Дендритные (раз-
но содержат более 20 а.о. и имеют в своей
ветвлённые) полимеры (например, поли(ами-
структуре гидрофильные и гидрофобные ами-
доамин) дендритные полимеры (ПАМАМ-
нокислоты. В эту группу входят MPG, пене-
полимеры)) характеризуются большим коли-
тратин, CADY, pVec и другие пептиды [40].
БИОХИМИЯ том 88 вып. 11 2023
2190
ТИМОТИЕВИЧ и др.
Вторичные амфипатические пептиды обыч-
идентифицировать компартменты клеток, в
но размером менее 20 а.о. и имеют вторичную
которых накапливаются СРР, а также оценить
структуру в форме α-спирали или β-слоя. Вто-
кинетику их накопления в клетке, что в итоге
ричные α-спиральные CPP, как правило, име-
позволяет выявлять молекулярные механизмы
ют гидрофобный участок на одном из концов,
интернализации.
тогда как другой конец пептида может быть
Согласно современным представлениям
гидрофильным (катионный или анионный).
[37, 40], выделяют несколько механизмов про-
Неамфипатические пептиды представляют
никновения СРР в клетки: энергонезависи-
собой относительно короткие пептиды (на-
мый (прямое проникновение) и энергозависи-
пример, HIV-TAT), которые имеют высокое
мый (различные виды эндоцитоза).
содержание положительно заряженных амино-
Энергонезависимое прямое проникновение
кислот, таких как аргинин или лизин. Иссле-
СРР. Энергонезависимое прямое проникно-
дования показывают, что для эффективного
вение включает два этапа: 1) взаимодействие
поглощения необходимо не менее восьми по-
CPP с мембраной клетки; 2) проникновение в
ложительных зарядов [40].
цитоплазму путём образования пор, адаптив-
Катионные дендримерные пептиды, отли-
ной транслокации или образования инверти-
чающиеся разветвлённой структурой и значи-
рованных мицелл (рис. 2, а). Такой механизм
тельной плотностью положительного заряда за
характерен для CPP, богатых аргинином и
счёт высокого содержания лизина или арги-
лизином [42], наличие которых обеспечивает
нина, можно выделить в отдельную группу. Та-
положительный заряд, что позволяет пептиду
кие соединения обладают значительными пре-
электростатически взаимодействовать с отри-
имуществами перед линейными пептидами,
цательно заряженными протеогликанами или
поскольку благодаря неприродным ε-амид-
гликозаминогликанами клеточной стенки и
ным связям более устойчивы к протеолизу,
тем самым накапливаться на поверхности
а наличие большого количества концевых заря-
мембраны. При достижении предельной кон-
женных групп обеспечивает эффективное свя-
центрации пептида происходит дестабилиза-
зывание с нуклеиновыми кислотами. Кроме
ция структуры липидов в бислое мембраны, в
того, дендримерные СРР также обладают го-
результате чего пептид проникает в цитоплаз-
раздо меньшей цитотоксичностью, чем линей-
му через сформированные поры (рис. 2, б).
ные, что имеет большое значение для их при-
Ввиду того, что в мембране образуются поры
менения в медицине.
на относительно короткие промежутки вре-
Таким образом, ввиду разнообразия струк-
мени, это позволяет пептиду проникать внутрь
тур и физико-химических свойств пептидные
клетки, не приводя к её лизису и гибели. Од-
носители представляют собой перспектив-
нако формирование пор в клеточной мембра-
ный класс соединений для внутриклеточной
не при высоких концентрациях CPP приводит
доставки терапевтических нуклеиновых кис-
к токсическим эффектам.
лот. Кроме того, такое разнообразие структур
Существует несколько молекулярных мо-
позволяет пептидам задействовать различные
делей формирования пор.
молекулярные механизмы для проникновения
Модель «бочка» (barrel-stave model) - мо-
внутрь клетки-мишени.
дель формирования пор (рис. 2, б), описываю-
щая проникновение амфипатических α-спи-
ральных пептидов. После взаимодействия с
МОЛЕКУЛЯРНЫЕ МЕХАНИЗМЫ
клеточной мембраной пептиды образуют клас-
ИНТЕРНАЛИЗАЦИИ СРР
теры, в центре которых образуются каналы.
Поры образованы обращёнными внутрь гид-
В настоящее время для изучения механиз-
рофильными поверхностями и взаимодействи-
мов интернализации СРР используется мно-
ем обращённых наружу гидрофобных остатков
жество различных методов, которые описаны в
с липидной мембраной.
обзоре Holm et al. [41]. В частности, использу-
Тороидальная модель (toroidal model) фор-
ют химические вещества - ингибиторы опре-
мирования пор применима к пептидам, спо-
делённых путей эндоцитоза; способность (или
собным образовывать α-спирали при контакте
неспособность) пептида проникать в эукарио-
с клеточными мембранами. Согласно этой мо-
тические клетки в присутствии таких инги-
дели, взаимодействие между положительными
биторов позволяет судить о механизмах его
боковыми цепями пептида и фосфатными
проникновения. Также СРР конъюгируют с
группами мембраны клетки приводит к на-
флюоресцентными метками, что даёт возмож-
коплению пептида на внешнем её слое. Затем
ность методом конфокальной микроскопии
пептиды вызывают изгиб липидного монослоя
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2191
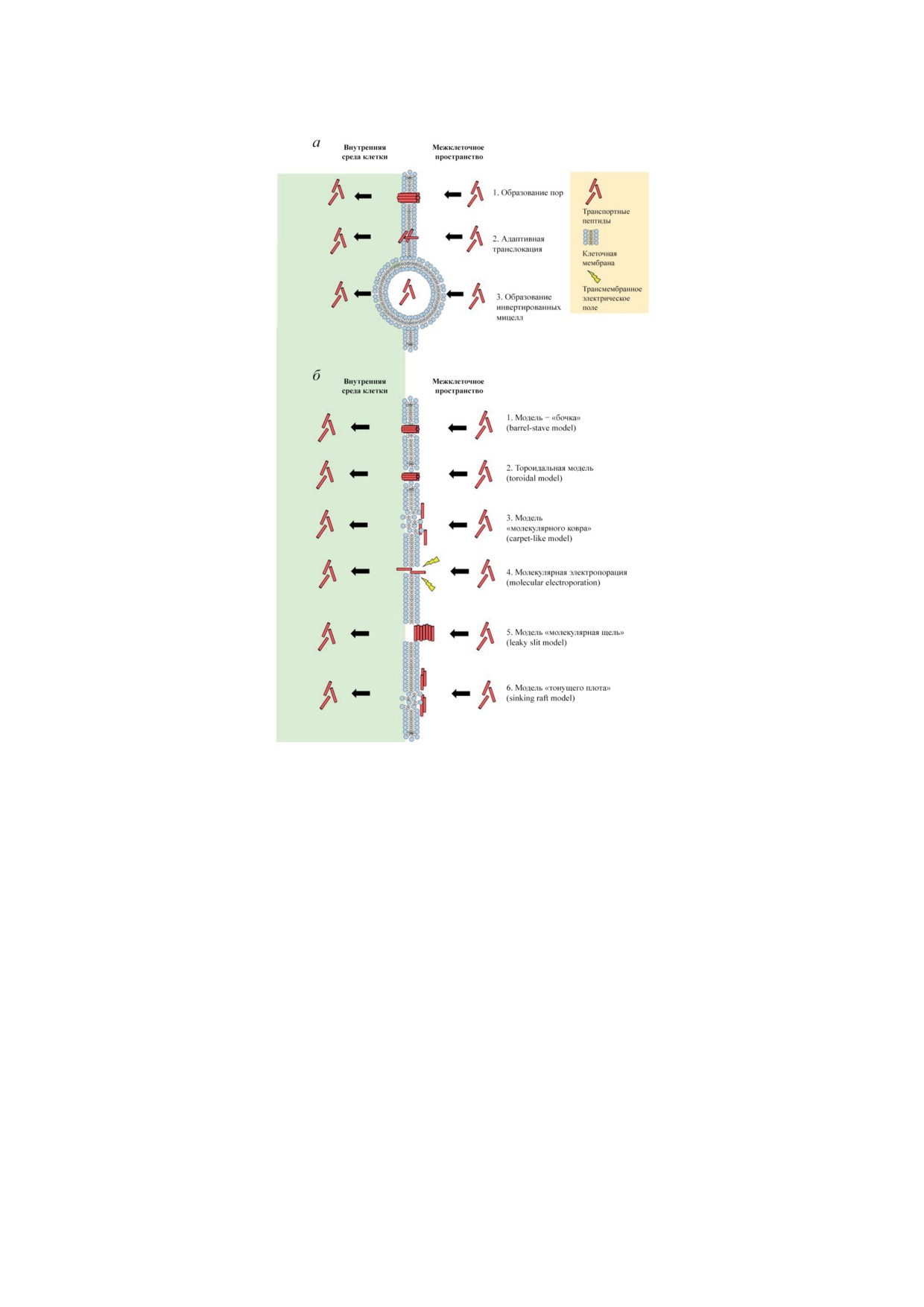
Рис. 2. Энергонезависимые механизмы проникновения CPP через клеточную мембрану. а - Пути энергонезависимо-
го проникновения положительно заряженных СРР позволяют пептиду электростатически взаимодействовать с отри-
цательно заряженной мембраной клетки с последующим проникновением путём: образования пор (1); адаптивной
транслокации (2), при которой СРР как бы «протискиваются» через фосфолипиды клеточной мембраны; образова-
ния инвертированных мицелл (3), сопряжённого с инвагинацией мембраны под воздействием положительно заря-
женных пептидов, и захватыванием их из внеклеточной среды внутрь клетки. б - Механизмы молекулярных моделей
формирования пор: модель «бочка» (1) предполагает образование пептидами кластеров, в центре которых образу-
ются каналы, через которые СРР проникают в цитозоль; тороидальная модель (2) основана на взаимодействии между
положительными цепями пептида и фосфатными группами мембраны клетки, что приводит к изгибанию липид-
ного монослоя внутрь с образованием гидрофильной щели в мембране и проникновению СРР внутрь клетки;
модель «молекулярного ковра» (3) предполагает накопление пептидов на поверхности клетки, которые образуют
слой наподобие «ковра», с последующей перегруппировкой отрицательных зарядов фосфолипидов мембраны в ре-
зультате их взаимодействия с катионными группами СРР, что вызывает снижение локального поверхностного натя-
жения и способствует интеркаляции СРР внутрь мембраны клетки; молекулярная электропорация (4) СРР внутрь
клетки возможна за счёт связывания сильно заряженного пептида с мембраной, образования локального электриче-
ского поля и разрыва клеточной мембраны; в модели «молекулярной щели» (5) пептиды ориентируются перпендику-
лярно мембране и агрегируют между собой боковыми поверхностями, образуя «ленту», которая проникает в клетку
через «щель» в фосфолипидах клеточной мембраны; модель «тонущего плота» (6) описывает процесс, при котором
пептиды образуют агрегаты, которые диффундируют через мембрану параллельно фосфолипидному бислою
внутрь, образуя гидрофильную щель в мем-
клетки, образуя слой наподобие
«ковра» с
бране, в которой находятся фосфолипидные
последующим искажением в результате взаи-
головки и пептиды.
модействия отрицательно заряженных липи-
В модели «молекулярного ковра» (carpet-like
дов наружного слоя мембраны и катионных
model) положительно заряженные пептиды
групп СРР. Это вызывает перегруппировку от-
накапливаются на поверхности мембраны
рицательных зарядов фосфолипидов и истон-
БИОХИМИЯ том 88 вып. 11 2023
2192
ТИМОТИЕВИЧ и др.
чение мембраны. Агрегация СРР на поверхно-
сти мембраны вызывает снижение локального
поверхностного натяжения и способствует ин-
теркаляции СРР внутрь мембраны клетки.
После интернализации пептида в цитоплазму
мембрана вновь восстанавливается [43].
Молекулярная электропорация (molecular
electroporation) - другой предполагаемый ме-
ханизм порообразования, при котором би-
слойная структура мембраны локально раз-
рывается трансмембранным электрическим
полем, образованным за счёт связывания за-
ряженного пептида с мембраной (рис. 2, б).
Модель
«молекулярная щель» (leaky slit).
В данной модели пептиды ориентируются пер-
пендикулярно мембране и агрегируют между
собой боковыми поверхностями, образуя так
называемую ленту. Затем другая сторона мем-
браны загибается сама на себя, образуя
щель [40] (рис. 2, б).
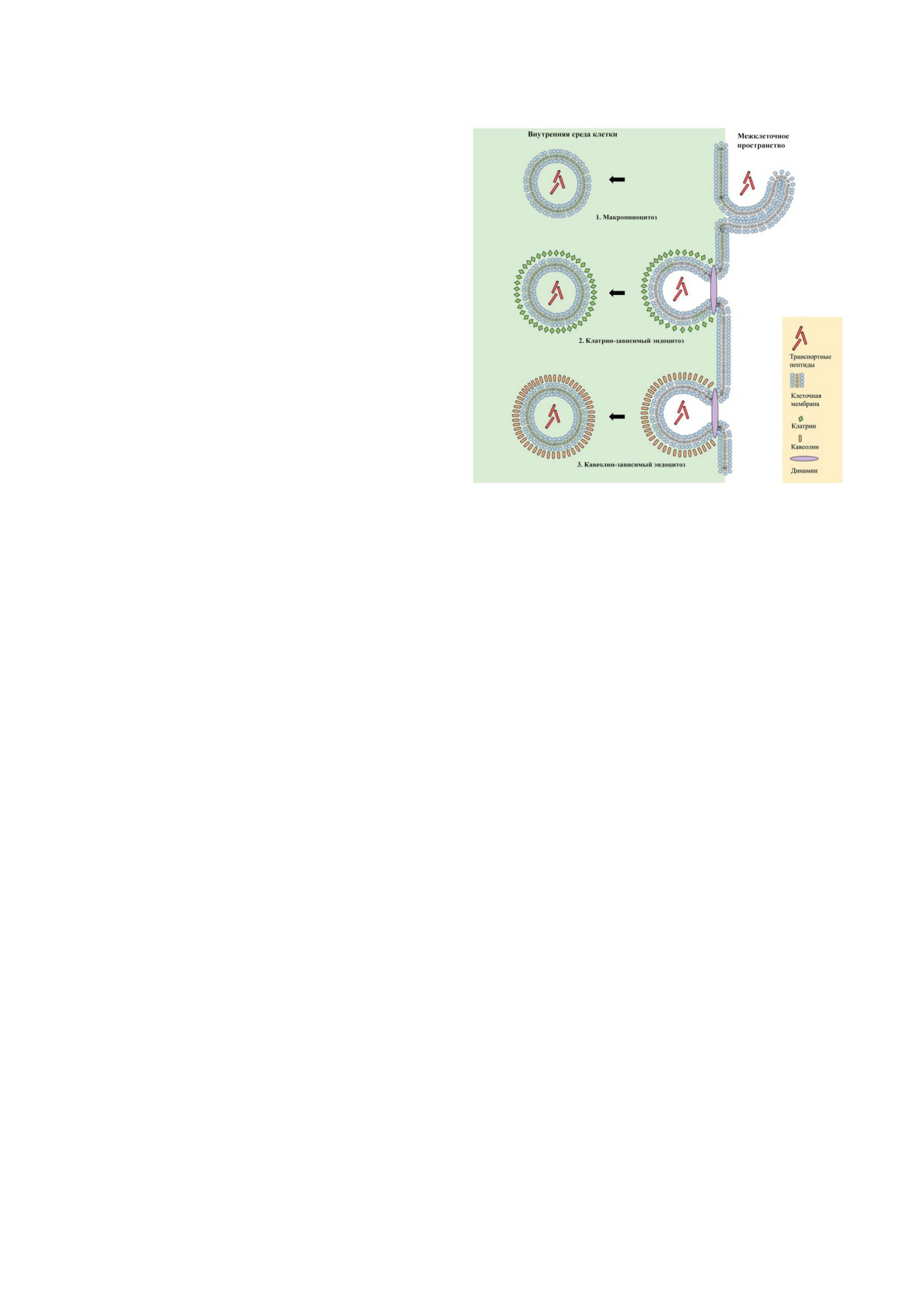
Рис.
3. Энергозависимые механизмы проникнове-
Модель «тонущего плота» (sinking raft mod-
ния CPP через клеточную мембрану за счёт гидро-
el) - альтернативная модель, описывающая
лиза ATP: в ходе рецептор-независимого макропино-
процесс, при котором пептиды образуют агре-
цитоза формируются выпячивания в мембране клетки,
которые сливаются с плазматической мембраной, обра-
гаты, способные диффундировать через мем-
зуя макропиносомы, в которых инкапсулированный CPP
брану (рис. 2, б).
взаимодействуют с протеогликанами на поверхности
При адаптивной транслокации положи-
мембраны (1); при клатрин-зависимом эндоцитозе про-
тельно заряженные CPP образуют переход-
исходит полимеризация клатрина и актинового цито-
скелета клетки, что приводит к инвагинации мембраны
ные ионные комплексы с отрицательно заря-
и формированию везикул с СРР, отделение которых от
женными компонентами мембраны (рис. 2, а).
донорской мембраны катализируется динамином, затем
Сформированные комплексы обладают сла-
происходит высвобождение везикулы в цитоплазму клет-
бым положительным зарядом (т.к. происходит
ки и деполимеризация клатрина (2); кавеолин-зависи-
частичная нейтрализация заряда CPP), что
мый эндоцитоз во многом сходен с клатрин-зависимым,
однако образование везикулы обеспечивается белками
позволяет пептиду адаптивно диффундировать
Cav-1, -2 и -3 и кавинами (3)
через клеточную мембрану, при этом «движу-
щей силой» диффузии служит мембранный
потенциал [44].
различные виды эндоцитоза (рис. 3). Эндо-
Образование инвертированных мицелл. Пря-
цитоз - это процесс транспорта веществ в
мое проникновение путём образования ин-
клетку, в котором задействованы различные её
вертированных мицелл первоначально было
органеллы (мембрана, микротрубочки и пр.).
описано для пенетратина (рис. 2, а). Первым
Эндоцитоз подразделяют на 2 категории: фа-
этапом процесса интернализации является
гоцитоз и пиноцитоз. Фагоцитоз используют
формирование электростатического взаимо-
специализированные виды клеток (макрофа-
действия между пептидом и клеточной мем-
ги, дендритные клетки и пр.) для поглощения
браной, что влияет на молекулярную организа-
из внеклеточного пространства крупных мак-
цию липидов и может приводить к изменению
ромолекул и частиц. Пиноцитоз используют
кривизны мембраны. Такие искривления или
все виды клеток для поглощения жидкостей из
инвагинации мембраны могут привести к
внеклеточного пространства. Он подразделя-
образованию инвертированных мицелл, ко-
ется на: макропиноцитоз, клатрин-, кавеолин-
торые захватывают пептид из внеклеточной
опосредованный эндоцитоз и клатрин/кавео-
среды. Гидрофильная среда внутри инверти-
лин-независимый эндоцитоз с привлечением
рованной мицеллы способствует накоплению
таких рецепторов, как нейропилин-1 и про-
пептида, после чего внутри клетки мицелла
теогликаны гепаран сульфата [40, 45]. Выше-
дестабилизируется и пептид высвобождается
указанные виды транспорта требуют затрат
в цитозоль [40].
энергии, обычно получаемой за счёт гидро-
Энергозависимое проникновение СРР. Виды
лиза ATP.
эндоцитоза. К энергозависимым способам
Макропиноцитоз - это рецептор-независи-
проникновения пептидов в клетки относят
мый вид транспорта, в котором важную роль
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2193
играют липидные рафты мембраны и актино-
вых кислот. Для повышения эффективности
вый цитоскелет клетки (рис. 3). Макропино-
транспорта используют вспомогательные со-
цитоз обычно индуцируется в ответ на стиму-
единения, которые инициируют ранний выход
ляцию клетки факторами роста (например,
транспортируемого вещества из эндосомы в
CSF-1, EGF и пр.). В ходе макропиноцитоза
цитоплазму клетки (см. ниже). Эксперимен-
формируются выпячивания в мембране клет-
тально показано, что многие СРР используют
ки, которые не «обволакивают» частицы (как в
данный механизм для проникновения в клет-
случае фагоцитоза), а сливаются с плазматиче-
ки, среди них ТАТ [47], MPGα, R8 [48] и др.
ской мембраной, образуя большие эндоцитар-
Кавеолин-зависимый эндоцитоз во многом
ные везикулы, называемые макропиносомами.
сходен с клатрин-зависимым, однако имеет
При макропиноцитозе CPP взаимодействуют
ряд отличительных особенностей (рис. 3). Ка-
с протеогликанами на поверхности мембраны
веолы представляют собой колбовидные инва-
и (после вовлечения Rac-белка и актина) мем-
гинации мембраны клетки диаметром около
брана реорганизуется, образуя макропино-
50-100 нм, присутствующие на многих типах
сомы, в которых инкапсулирован CPP. Пока-
клеток. Кавеолы формируются в участках мем-
зано, что посредством этого механизма внутрь
браны, которые богаты холестерином и сфин-
клеток проникают аргинин-богатые пепти-
голипидами; в этих участках также могут рас-
ды (R8, R9, R12) [40].
полагаться молекулярные рецепторы. Такие
Клатрин-зависимый эндоцитоз является
гидрофобные участки мембраны некоторые
наиболее изученным механизмом (рис. 3).
авторы называют липидными рафтами. Глав-
Формирование эндосомы происходит в опре-
ными молекулярными компонентами кавеол
делённых участках мембраны клетки - так
являются белки Cav-1, -2 и -3; из них первые
называемые «горячие точки» образования ве-
два экспрессируются совместно и представ-
зикул, которые обычно представляют собой
лены на широком спектре клеток. Cav-1 - это
участки клеточной мембраны, обогащенные
главный белок, определяющий форму кавеол,
фосфатидилинозитол-4,5-дифосфатом (PIP2).
гидрофобные аминокислоты которого встрое-
PIP2, в свою очередь, взаимодействует с адап-
ны в плазматическую мембрану. Вторая группа
терными белками, наиболее важный из них -
белков, необходимых для реализации кавео-
AP2, который связывается с PIP2 и рекрутирует
лин-опосредованного эндоцитоза, называется
каркасные белки плазматической мембраны,
кавинами; они локализуются на внутренней
что приводит к началу сборки клатрина в ико-
стороне мембраны клетки, обращенной к ци-
саэдрические структуры на внутренней сторо-
тозолю, и необходимы для взаимодействия с
не мембраны [44]. Далее, при накоплении CРР
цитоскелетом клетки. Показано, что кавин-1,
в
«горячих точках» формирования везикул
связываясь с кавеолинами, холестерином и
происходит инвагинация мембраны. Считает-
фосфатидилсерином, стабилизирует кривизну
ся, что полимеризация клатрина и актинового
мембраны и поддерживает колбовидную фор-
цитоскелета клетки способствует инвагинации
му кавеол. Другими важными молекулярными
и формированию везикулы размером
100-
компонентами кавеол являются актиновый
150 нм в диаметре [46]. Отделение везикул от
цитоскелет клетки и холестерин, а также дин-
донорской мембраны катализируется белком
амин, который взаимодействует непосред-
динамином. Динамин собирается в плотные
ственно с Cav-1 в основании кавеолы и обес-
олигомеры и сжимает мембрану наверху фор-
печивает её отпочковывание с последующим
мирующейся везикулы в тонкую перемычку
образованием внутриклеточной визикулы [40].
в виде «песочных часов», а затем полностью
Интернализация кавеол приводит к образо-
отделяет её. Далее происходит высвобожден-
ванию кавеосом - везикул с гетерогенной
ные везикулы в цитоплазму клетки и деполи-
морфологией и нейтральным рН внутри, что
меризация клатрина. В итоге формируются так
отличает их от поздних эндосом с низким рН.
называемые ранние эндосомы, которые созре-
По всей видимости, транспортируемое содер-
вают до поздних эндосом, характеризующихся
жимое кавеосом не подвергается деградации,
низким значением рН. Поздние эндосомы, в
как это происходит в лизосомах при кла-
свою очередь, транспортируют поглощённое
трин-опосредованном эндоцитозе. Однако
вещество в лизосомы - органеллы с ещё более
каким образом происходит высвобождение
низким рН и наличием ферментов деградации.
транспортируемого вещества в цитоплазму,
Ввиду деградации транспортируемых веществ
не известно [40]. Ряд СРР задействуют дан-
в лизосомах, клатрин-зависимый эндоцитоз
ный механизм для проникновения в клетки:
является менее предпочтительным механиз-
ТАТ-пептид, пролин-богатые пептиды
[49],
мом для доставки терапевтических нуклеино-
TP10 [50] и др.
11
БИОХИМИЯ том 88 вып. 11 2023
2194
ТИМОТИЕВИЧ и др.
Клатрин- и кавеолин-независимый эндоци-
образование ионных пар между CPP и отри-
тоз. Ещё одним путём энергозависимого входа
цательно заряженными липидами мембраны,
СРР в клетки является клатрин- и кавеолин-
после чего пептиды диффундируют через мем-
независимый эндоцитоз. В реализацию этого
брану. Это характерно для аргинин-богатых
механизма вовлечены липидные рафты
-
пептидов.
участки на поверхности мембраны клетки,
Фузогенные липиды. Выход из эндосомы
богатые стеринами и сфинголипидами, раз-
может быть индуцирован фузогенными липи-
мером 40-50 нм. Эти рафты могут содержать
дами (например, DOPE). Такие липиды при
не только клатрин и кавеолин, но и другие
низких значениях pH сливаются с мембраной
макромолекулы (например, белки-рецепторы),
эндосомы, что в итоге дестабилизирует её и
которые распознают транспортируемые ве-
приводит к высвобождению содержимого в
щества во внешней среде и способствуют их
цитозоль. Показано, что добавление DOPE к
поглощению. Было показано, что ряд СРР
комплексу СРР-нуклеиновая кислота значи-
проникает в клетки при помощи этого меха-
тельно увеличивало эффективность проник-
низма, например, азурин и его фрагменты р18
новения этого комплекса в цитозоль [33]. Эн-
и р28 [51], транспортан, транспортан-10 [50] и
досомальное ускользание также может быть
LMWP в комплексе с молекулами миРНК [52].
достигнуто за счёт использования рН-чув-
Примечательно, что ранее для транспортана и
ствительных полимеров и рН-чувствительных
транспортана-10 было показано проникнове-
липосом [54].
ние в клетки посредством кавеолин-зависи-
Модель «протонной губки» описывает выход
мого эндоцитоза. По всей видимости, пептиды
из эндосом полиплексов, содержащих поли-
могут задействовать одновременно несколько
этиленимин. Данный механизм подразумевает
путей проникновения в клетку.
присутствие в эндосоме протон-связывающих
В целом механизм проникновения СРР
молекул (рис. 4). Касаемо СРР, механизм «про-
зависит от физико-химических свойств пеп-
тонной губки», в частности, использует пеп-
тида и транспортируемой молекулы, а также
тиды, содержащие гистидин. Имидазольная
от концентрации и структурных особенно-
группа гистидина протонируется, а поскольку
стей плазматической мембраны. Например,
в эндосоме присутствует протонная помпа, то
при физиологических условиях и низкой кон-
в эндосому
«закачивается» дополнительное
центрации пептиды проникают в клетки при
количество протонов. Вслед за протонами в
помощи эндоцитоза, тогда как при высокой
эндосому проникают хлор-анионы. В резуль-
концентрации СРР непосредственно взаимо-
тате осмотическое давление разрушает мем-
действуют с клеточной мембраной и задей-
брану эндосомы, а её содержимое оказывается
ствуют энергонезависимые механизмы для по-
в цитозоли. Выход из эндосомы может быть
падания в клетки [40].
активирован эндосомолитическими агентами,
Выход СРР из эндосомы. После проникно-
например хлорохином, который представляет
вении внутрь клетки при помощи эндоцитоза
собой слабое основание. Находясь в эндосо-
СРР (и транспортируемые ими терапевтиче-
ме, хлорохин связывает протоны, тем самым
ские нуклеиновые кислоты) накапливаются в
препятствует её закислению, а в высокой кон-
эндосомах, которые созревают и превращают-
центрации хлорохин вызывает набухание и
ся в лизосомы, что приводит к деградации со-
разрушение. Ещё один способ задействовать
держимого эндосом гидролазами. Следователь-
эффект протонной губки для высвобождения
но, своевременный выход СРР из эндосомы
СРР из эндосом - применение протон-свя-
является необходимым условием эффективной
зывающих полимеров, например полиэтилен-
доставки переносимой молекулы в клетку [39].
имина. Такие полимеры могут быть присоеди-
Разрушение мембраны эндосомы. Выход
нены к CPP ковалентно (или использоваться
СРР из эндосом достигается при помощи раз-
в виде комплекса), что незначительно снижает
ных молекулярных механизмов. Один из воз-
их способность к интернализации, но облег-
можных механизмов - разрушение мембраны
чает выход из эндосомы, обеспечивая в итоге
эндосомы, что обеспечивается СРР с альфа-
более эффективную доставку [39].
спиральной структурой [44]. Позитивно за-
Модель
«зонтика» описывает выход из
ряженный СРР взаимодействует с негативно
эндосомы крупных полимерных соединений
заряженными фосфолипидами мембраны, что
(рис. 4). Согласно этой гипотезе, полимер-
приводит к образованию в ней пор и высво-
носитель образует комплексы с терапевтиче-
бождению содержимого в цитозоль [53].
скими нуклеиновыми кислотами за счёт элек-
Образование ионных пар. Другим возмож-
тростатических взаимодействий, в результате
ным механизмом выхода из эндосом является
происходит их уплотнение (конденсация ком-
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2195
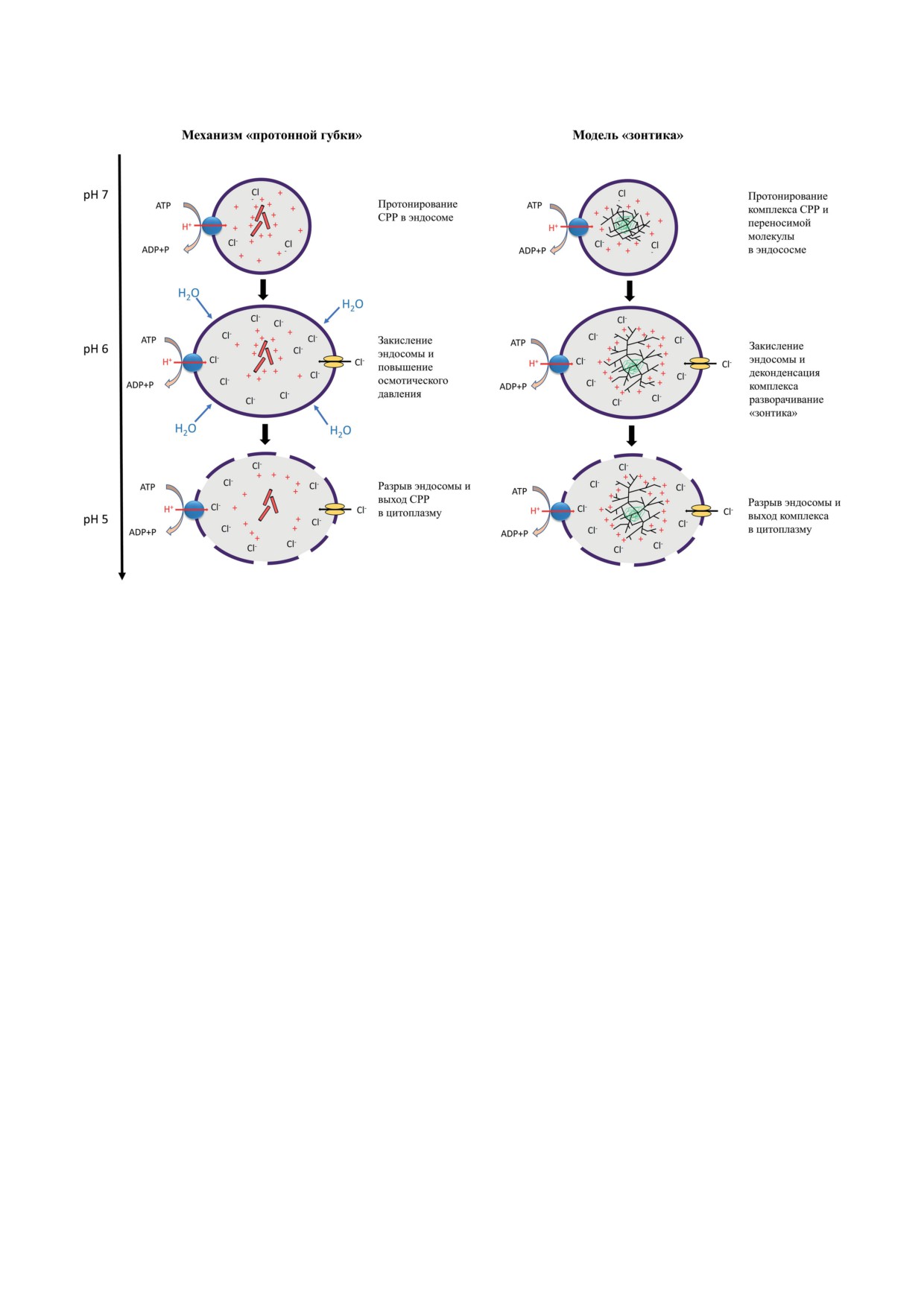
Рис. 4. Механизм выхода СРР из эндосомы
плекса). Находясь в эндосоме, при достижении
рование аминогрупп носителя, что приводит к
низких значений pH (pH = 5-6) происходит
его деконденсации и объёмному расширению
протонирование аминогрупп полимера-носи-
за счёт электростатического отталкивания со-
теля, что приводит к его деконденсации и
седних одноимённо заряженных аминогрупп,
объёмному расширению за счёт электроста-
увеличению объёма эндосомы и последующе-
тического отталкивания соседних одноименно
му разрыву её мембраны, что сопровождается
заряженных аминогрупп. Все эти процессы
попаданием содержимого в цитозоль.
приводят к увеличению объёма эндосомы и
Проникновение СРР в ядро. В некоторых
последующему разрыву её мембраны, что со-
случаях терапевтические нуклеиновые кисло-
провождается попаданием содержимого в ци-
ты следует доставлять в ядро клетки, для чего
тозоль. Данный механизм выхода из эндосомы
требуется преодолевать 2 барьера - клеточ-
присущ не только крупным полимерным но-
ную и ядерную мембраны. Некоторые СРР
сителям, но и СРР (например, разветвлённым
(ТАТ, полиаргинин и др.) способны проникать
пептидам).
в ядро клеток [54]. Для увеличения тропности
Модель «протонной губки» (рис. 4, слева)
к ядру СРР модифицируют путём конъюгации
подразумевает протонирование аминокислот в
с определёнными пептидными последователь-
составе СРР. Дополнительное количество про-
ностями (как правило, содержащими остатки
тонов попадает в эндосому при помощи про-
лизина, аргинина и пролина), распознающи-
тонной помпы. Вслед за протонами в эндосому
мися ядерными транспортными белками (им-
проникают хлор-анионы, в результате чего ос-
портин-α и импортин-β) [55]. Такая модифи-
мотическое давление разрушает мембрану эн-
кация усиливает ядерную локализацию СРР.
досомы, а её содержимое выходит в цитозоль.
Комплекс ядерных пор (КЯП) представля-
Модель «зонтика» (рис. 4, справа) описывает
ет собой цилиндрические структуры с внут-
выход из эндосомы крупных полимерных или
ренним диаметром около
30 нм и длиной
дендримерных соединений. СРР-носитель об-
50 нм, обеспечивающие транспорт веществ в
разует комплексы с переносимыми молеку-
ядро. Молекулы малого размера (вода, саха-
лами за счёт электростатических взаимодей-
ра и ионы) проникают через КЯП пассивно.
ствий, в результате происходит конденсация
Однако крупные молекулы (мРНК, белки,
комплекса. Находясь в эндосоме, при достиже-
пептиды и пр.) проходят через КЯП энерго-
нии низких значений pH происходит протони-
зависимым способом с помощью последова-
БИОХИМИЯ том 88 вып. 11 2023
11*
2196
ТИМОТИЕВИЧ и др.
тельностей ядерной локализации (NLS) [54].
механизм того, как структурные изменения в
Они представляют собой короткие последо-
локальных участках мембраны могут вызывать
вательности из 5-12 а.о., полученные из ядер-
транслокацию пептидов внутрь, ещё предстоит
ных белков эукариот и вирусов. СРР могут
выяснить. Новые знания о взаимодействии
быть конъюгированы с ними и таким образом
пептида и клетки необходимы для разработки
нацеливаться на проникновение в ядро. Наи-
эффективных векторных систем доставки те-
более известными NLS-пептидами являются:
рапевтических молекул.
большой Т-антиген SV40 и Xenopus из белка
нуклеоплазмина
[54], а также
29-членный
пептид белка pUL53 цитомегаловируса [56] и
СТРАТЕГИИ ПРИМЕНЕНИЯ СРР
др. [57]. Таким образом, разнообразие струк-
тур и физико-химических свойств СРР, а так-
Выделяют две основные стратегии приме-
же относительная простота их модификации
нения СРР для доставки терапевтических моле-
позволяет использовать пептидные векторы
кул (включая нуклеиновые кислоты) в клетки.
для доставки терапевтических нуклеиновых
Первая
- ковалентная стратегия подразу-
кислот в ядро.
мевает конъюгацию СРР с транспортируемым
Факторы, влияющие на интернализацию
соединением, что происходит при образова-
СРР. Во многих экспериментах было пока-
нии ковалентной химической связи между
зано, что применяемая концентрация СРР
соединениями. Такая стратегия подходит для
влияет на путь интернализации. Считается,
транспорта молекул с нейтральным зарядом,
что эндоцитоз обычно возникает при низкой
например, некоторых белков, пептидов, пеп-
концентрации пептида, а прямое проникно-
тидных нуклеиновых кислот и др. Перспектив-
вение возможно при более высокой концен-
ным направлением в ковалентной стратегии
трации [40]. Напротив, для пенетратина было
является использование так называемой де-
показано, что прямое проникновение про-
градируемой ковалентной связи между СРР и
исходит при низких концентрацих. Другим
транспортируемой молекулой. Такой конъюгат
фактором, влияющим на интернализацию,
способен проникать в клетку, после чего рас-
является заряд пептидов, особенно высо-
падаться внутри неё и высвобождать терапев-
кий положительный заряд, преимущественно
тическую молекулу в цитоплазму. Примером
обеспечивающийся наличием остатков арги-
служит деградируемый линкер с дисульфидной
нина. Амфипатичность - ещё один известный
связью между пептидом ТАТ и нуклеиновыми
фактор, влияющий на поглощение. Первич-
кислотами [59]. В ряде случаев ковалентная
ные и вторичные амфипатические пептиды
стратегия не оправдана, так как в результате
могут напрямую проникать через клеточную
конъюгации СРР и терапевтической молекулы
мембрану в низких концентрациях, в то время
происходит химическая модификация послед-
как неамфипатические СРР используют эндо-
ней, что приводит к уменьшению (или полной
цитоз. Температура, при которой проводится
утрате) её биологической активности. Кроме
эксперимент, также может влиять на механизм
того, ковалентная стратегия не подходит для
интернализации. При низких температурах
доставки кольцевых плазмидных ДНК ввиду
(4 °С) предпочтительна прямая транслокация,
отсутствия у них свободных валентностей для
однако при повышении (37 °С) - задейству-
конъюгации с СРР [60].
ется эндоцитоз. Переносимые молекулы могут
В соответствии со второй - не ковалентной
сильно влиять на путь поглощения. Размер
стратегией - пептид-носитель образует ком-
присоединяемого соединения влияет на раз-
плекс с транспортируемой молекулой, напри-
мер всего комплекса, что приводит к меха-
мер, за счёт электростатических или гидро-
низму поглощения, отличному от такового для
фобных взаимодействий. Данная стратегия
свободного СРР. Чем меньше размер, тем
хорошо подходит для доставки терапевтиче-
больше вероятность, что комплекс интернали-
ских нуклеиновых кислот, т.к. СРР чаще всего
зуется в клетку прямой транслокацией. Однако
обладают позитивным зарядом, а нуклеиновые
при больших размерах комплекса преобладает
кислоты - отрицательным.
эндоцитоз [40]. К настоящему моменту накап-
Применение СРР для доставки нуклеиновых
ливаются знания об эффективности доставки
кислот в доклинических исследованиях. Опуб-
CPP на различных линиях клеток [58].
ликовано множество работ, в которых опи-
Резюмируя вышесказанное, механизмы
саны СРР, доставляющие различные ну-
интернализации СРР разнообразны и зависят
клеиновые кислоты в клетки млекопитаю-
как от химического состава пептида, так и от
щих. Подавляющее большинство таких работ
свойств клеточной мембраны. Молекулярный
описывает эксперименты in vitro [43, 61, 62].
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2197
Применение СРР для доставки нуклеиновых
зован пептидный носитель. Применение ком-
кислот сопряжено с рядом сложностей, глав-
плекса PMO-пептид снижало репликацию
ные из которых
- относительно короткий
вируса на 70-98% in vitro. Местное нанесение
период полувыведения СРР и отсутствие спе-
10 мкг PMO-пептид на роговицу глаз мышей,
цифичности к тканям и органам. Тем не менее
инфицированных вирусом герпеса, снижало
регулярно публикуются работы, в которых
частоту заболевания на 37-50% [66].
СРР применяют для доставки терапевтических
Пептиды также применяются для доставки
нуклеиновых кислот лабораторным животным
ДНК-вакцин. В частности, иммунизация мы-
с индуцированной патологией (воспалением,
шей комплексом пептида MPG и плазмидных
опухолями или инфекцией). В данном разделе
ДНК, несущих антигены вируса гепатита С,
обобщён опыт применения СРР в экспери-
приводила к появлению специфических анти-
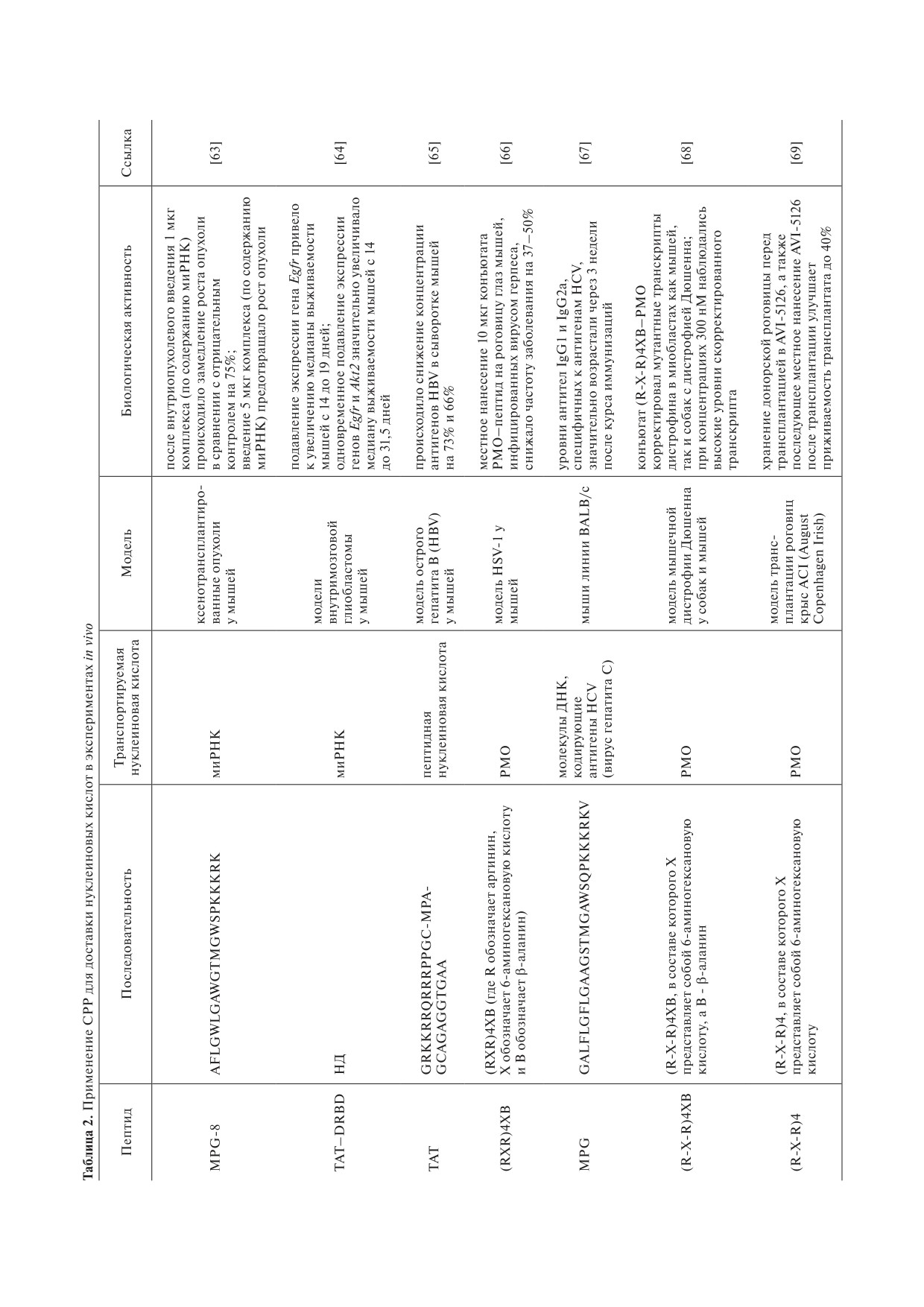
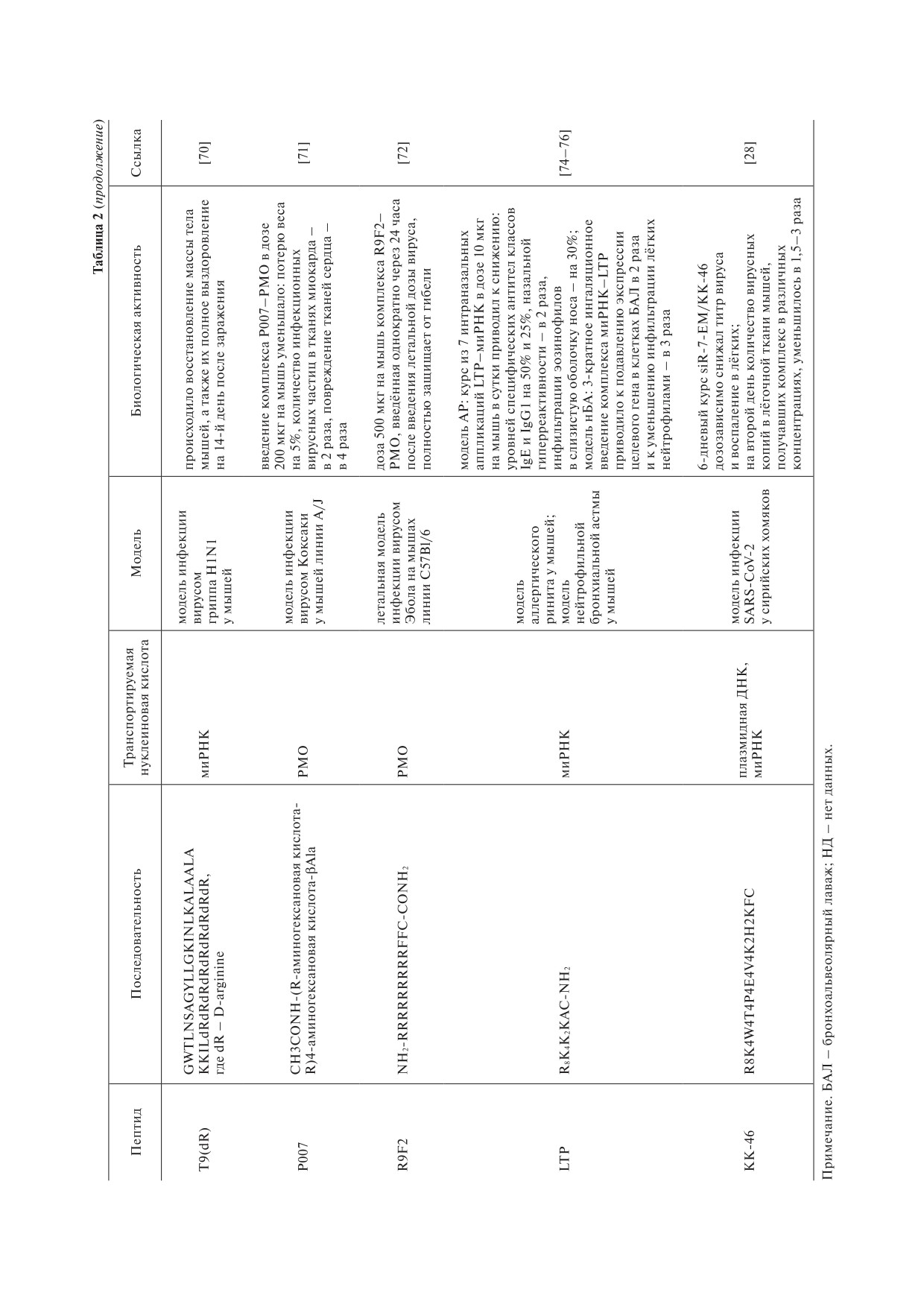
ментах in vivo (табл. 2).
тел классов IgG1 и IgG2a [67].
Укороченная версия амфипатического пеп-
В исследовании использовали пептид
тидного носителя MPG (MPG-8) была исполь-
(R-Х-R)4ХB (Х представляет собой 6-амино-
зована для доставки молекул миРНК против
гексановую кислоту, а B - β-аланин). Его конъ-
мРНК гена, кодирующего циклин B1. Этот ре-
югаты с молекулами PMO, направленными
гуляторный белок участвует в митозе и демон-
против гена, кодирующего дистрофин, были
стрирует повышенную экспрессию при раз-
успешно применены в модели мышечной дис-
личных формах рака. Показано, что MPG-8
трофии Дюшенна у мышей и собак (мышечная
образует наноразмерные комплексы с моле-
дистрофия золотистых ретриверов) [68].
кулами миРНК. Внутривенное ведение этих
Так как роговица глаза является одной из
комплексов мышам с ксенотрансплантирован-
наиболее часто трансплантируемых тканей,
ными опухолями приводило к значительному
то доклинические испытания безопасности и
уменьшению их размера [63].
эффективности препарата AVI-5126 проводи-
В исследовании Michiue et al. [64] для до-
ли на модели трансплантации роговиц крыс.
ставки молекул миРНК авторы использовали
Исследуемый препарат представляет собой
производное пептида TAT (пептид TAT-DRBD),
пептид (R-Х-R)4, конъюгированный с PMO,
который представлял собой пептид TAT, сли-
подавляющими экспрессию фактора тран-
тый с РНК-связывающим доменом - DRBD.
скрипции c-Myc, ключевого фактора отторже-
Такой гибридный пептид образовывал ком-
ния трансплантата. По результатам исследова-
плекс с миРНК за счёт домена DRBD и про-
ния выявлено, что отторжение трансплантата
никал внутрь клеток за счёт TAT-фрагмента,
происходило значительно хуже после хранения
при этом транспортируя связанную с ним
донорской роговицы перед трансплантацией в
миРНК. Такой подход был апробирован в экс-
AVI-5126 и последующего местного нанесения
перименте in vivo на модели внутримозговой
AVI-5126 после трансплантации [69].
глиобластомы у мышей. Пептид TAT-DRBD
Пептид T9(dR), являющийся производным
доставлял в клетки опухоли молекулы миРНК
транспортана, был использован для доставки
против генов Egfr и Akt2, которые вовлечены
миРНК, направленных против гена нуклео-
в онкогенез. В свою очередь, инактивация этих
протеина вируса гриппа. Данный комплекс
генов молекулами миРНК приводила к апоп-
снижал репликацию вируса как in vitro, так и в
тозу опухолевых клеток, что значительно увели-
модели у мышей, предотвращая случаи леталь-
чивало выживаемость модельных мышей [64].
ного исхода [70].
Был создан конъюгат пептида-носителя
Пептид P007, богатый аргинином, был
TAT и пептидной нуклеиновой кислоты (TAT-
конъюгирован с PMO, направленной против
PNA-DR), которая направлена против генома
генома вируса Коксаки B3. Для данного конъ-
вируса гепатита В. Конъюгат ингибировал ре-
югата показан противовирусный эффект в экс-
пликацию HBV в клетках HepG2.2.15, а также
периментах как in vitro, так и in vivo [71]. Дру-
на модели HBV у мышей происходило сни-
гой богатый аргинином пептид, R9F2, конъю-
жение вирусной нагрузки на 80%. Примеча-
гированный с молекулами PMO, направлен-
тельно, что TAT-PNA-DR показал низкую ток-
ными против генома вируса Эбола, обеспе-
сичность и иммуногенность, вместе с тем вы-
чивал полную защиту мышей после введения
сокую стабильность в сыворотке [65].
летальной дозы вируса [72].
Для доставки одноцепочечной ДНК - мо-
Нашим коллективом авторов выпущен
лекул фосфородиамидат-морфолинового оли-
ряд публикаций, посвящённых катионному
гомера (PMO, phosphorodiamidate morpholino
дендримерному пептиду LTP, богатому остат-
oligomer), направленных против генома герпес-
ками аргинина и лизина, за счёт чего он име-
вируса человека типа 1 (HSV-1) - также исполь-
ет высокий положительный заряд и способен
БИОХИМИЯ том 88 вып. 11 2023
2198
ТИМОТИЕВИЧ и др.
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2199
БИОХИМИЯ том 88 вып. 11 2023
2200
ТИМОТИЕВИЧ и др.
связывать отрицательно заряженные молекулы
Применение СРР для доставки нуклеино-
нуклеиновых кислот [73]. С помощью этого
вых кислот в клинических исследованиях. Ряд
пептида была осуществлена доставка молекул
СРР достиг клинических исследований, что
миРНК против генов, кодирующих провос-
свидетельствует о перспективности их приме-
палительные цитокины IL-4 и IL-13, в клетки
нения в медицинской практике. С их помо-
респираторного тракта мышей с индуцирован-
щью осуществляется доставка терапевтических
ным аллергическим ринитом. Интраназальное
молекул различной природы (белки, пептиды,
введение комплекса миРНК-LTP приводи-
циклоспорин, ботулин и пр.). Некоторые СРР-
ло к снижению продукции целевых цитоки-
содержащие препараты достигли клинических
нов клетками региональных лимфоузлов и к
исследований (см. обзоры Guidotti et al. [62] и
уменьшению основных проявлений патоло-
Stiltner et al. [77]). При этом в двух препаратах
гии: уменьшению уровня IgE-антител, выра-
СРР использовали для доставки терапевтиче-
женности инфильтрации верхних дыхательных
ских нуклеиновых кислот [27].
путей провоспалительными клетками и ре-
После успешного прохождения доклини-
моделирования респираторного тракта
[74].
ческих испытаний на модели трансплантации
В другой работе при помощи пептида LTP
роговиц крыс проведены клинические иссле-
доставляли молекулы миРНК, направленные
дования безопасности и эффективности пре-
против гена Stat3, который вовлечён в нейтро-
парата AVI-5126. Препарат представляет собой
фильное воспаление лёгких при бронхиальной
пептид (R-Ahx-R)4, конъюгированый с PMO,
астме. Показано, что 3-кратное ингаляцион-
нацеленным на фактор транскрипции c-Myc
ное введение этого комплекса миРНК-LTP
человека. Блокада данного транскрипцион-
приводило к подавлению экспрессии целевого
ного фактора помогает избежать отторжение
гена в клетках бронхоальвеолярного лаважа
трансплантированной вены после коронар-
(БАЛ) в 2 раза и к уменьшению инфильтрации
ного шунтирования сосудов сердца. В ходе
лёгких нейтрофилами - в 3 раза [75].
испытания после иссечения вены её погружа-
Ещё один разветвлённый (дендримерный)
ли в раствор, содержавший 10 мкМ AVI-5126,
пептид КК-46 был использован в качестве но-
а затем имплантировали в качестве шунта [78].
сителя молекул миРНК, направленных против
Однако клиническое исследование было терми-
геномной РНК вируса SARS-CoV-2. Нашим
нировано, а его результаты не опубликованы.
коллективом проведён скрининг библиотеки
На основе пептидных носителей был раз-
миРНК, специфичных к разным участкам
работан и одобрен для медицинского приме-
генома SARS-CoV-2, на предмет их способ-
нения первый в мире этиотропный препа-
ности подавлять репродукцию вируса. Наи-
рат (МИР 19) для терапии COVID-19, который
более активный вариант миРНК, направлен-
представляет собой комплекс LNA-модифици-
ный против участка генома, кодирующего
рованных молекул миРНК и пептида-носите-
РНК-зависимую РНК-полимеразу вируса, был
ля - КК-46. Проведены клинические иссле-
модифицирован путём замены пяти РНК-
дования фазы II, в ходе которых препарат
нуклеотидов на LNA-нуклеотиды, что суще-
вводили ингаляционно пациентам со средней
ственно (в 3,7 раза) повысило устойчивость
тяжестью COVID-19 в условиях стациона-
миРНК к ферментам деградации без потери
ра [17]. Пациенты контрольной группы (52 па-
антивирусной активности. В исследованиях
циента) получали стандартную терапию, со-
in vitro на культуре клеток комплекс миРНК-
гласно клиническим рекомендациям Мини-
КК-46 обеспечивал подавление вирусной
стерства здравоохранения РФ. Отдельная груп-
репликации до 10 000 раз. В модели инфек-
па пациентов со средней тяжестью COVID-19
ции SARS-CoV-2 сирийских хомячков инга-
(52 пациента) получала препарат МИР 19 ин-
ляционное введение препарата в дозах 0,7-
галяционно в дозе 3,7 и 11,1 мг в сутки (эти
5,6 мг на кг веса приводило к уменьшению
пациенты были лишены любой другой этио-
вирусной нагрузки в лёгких до 200 раз. Более
тропной терапии). Клинические исследования
того, снижение репликации вируса в лёг-
показали, что препарат безопасен, хорошо
ких приводило к улучшению их состояния,
переносится и значительно сокращает время
что выражалось в уменьшении уровня пери-
до клинического улучшения состояния паци-
бронхальной инфильтрации провоспалитель-
ентов, по сравнению со стандартной терапи-
ными клетками и уменьшении толщины стенок
ей, что выражалось в облегчении лихорадки,
бронхов. В ходе доклинических исследова-
нормализации частоты дыхания, уменьшении
ний безопасности установлено, что препарат
кашля и восстановлении сатурации кисло-
относится к классу малотоксичных соедине-
рода >95% [17]. По результатам исследования,
ний [28].
препарат показал свою клиническую эффек-
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2201
тивность и был зарегистрирован для медицин-
ности за счёт наличия неприродных ε-связей.
ского применения (рег. № ЛП-007720).
Более высокая стабильность может быть до-
Подводя итог, разработка безопасной и
стигнута за счёт использования неприродных
эффективной системы доставки нуклеиновых
аминокислот или энантиомеров D, которые
кислот на основе CPP, простота производства
менее чувствительны к ферментативной де-
и низкая стоимость имеют большой потенциал
градации, чем L-форма. Ведутся разработки
и значительные перспективы с точки зрения
в области улучшения специфичности CPP к
их клинического применения. В ближайшее
целевому сайту, такие как связывание CPP
время ожидается появление на рынке одоб-
со специфическими лигандами в форме ко-
ренных препаратов терапевтических нуклеи-
валентных или нековалентных комплексов.
новых кислот, доставляемых векторами на
Кроме того, направленности доставки можно
основе CPP.
достичь за счёт локального применения пеп-
тидов, например, ингаляционное применение
СРР-содержащих препаратов для доставки
ЗАКЛЮЧЕНИЕ
в лёгкие.
В итоге проведено множество доклини-
С момента открытия пептида TAT в
ческих исследований, в которых при помощи
1988 году было разработано большое количе-
СРР доставлялись различные терапевтические
ство CPP. Эти пептиды широко используются
молекулы, включая нуклеиновые кислоты.
для доставки различных видов терапевтиче-
Из них не менее девяти лекарственных пре-
ских средств. К настоящему времени накоп-
паратов достигли клинических исследований,
лен значительный опыт их применения как
при этом в двух из них при помощи СРР осу-
в исследованиях in vitro, так и in vivo.
ществляется доставка терапевтических нук-
Главные преимущества СРР состоят в от-
леиновых кислот. Один из таких препаратов
носительной простоте их получения и хране-
одобрен для медицинского применения. Всё
ния, хорошо разработанных методах очистки
это свидетельствует о перспективности ис-
и стандартизации. Кроме того, ввиду био-
пользования СРР для создания генно-терапев-
совместимости, СРР зачастую не обладают
тический лекарственных средств.
токсическими свойствами, а по причине не-
большого размера, как правило, не вызывают
Вклад авторов. М.Р. Хаитов - концепция
нежелательных иммунных реакций. Основны-
и руководство работой; Е.Д. Тимотиевич - на-
ми препятствиями для широкого применения
писание текста; И.П. Шиловский - написание
CPP в медицине являются низкая специфич-
текста, редактирование текста статьи.
ность к типу клеток и короткий период полу-
Финансирование. Исследование выпол-
выведения.
нено при поддержке Российского научного
Несмотря на вышеуказанные сложности,
фонда (грант
существуют способы их преодоления. В пер-
project/22-25-00182/).
вую очередь, это стабилизация структуры пеп-
Конфликт интересов. Авторы заявляют об
тидов за счёт введения точечных аминокис-
отсутствии конфликта интересов.
лотных замен или дополнительных хими-
Соблюдение этических норм. Настоящая
ческих связей. Также путём дендримериза-
статья не содержит описания каких-либо ис-
ции пептидов (синтез разветвлённых пепти-
следований с участием людей или животных
дов) можно добиться повышения их стабиль-
в качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1. Chaudhary, N., Weissman, D., and Whitehead, K. A.
3. Talap, J., Zhao, J., Shen, M., Song, Z., Zhou, H.,
(2021) mRNA vaccines for infectious diseases: princi-
Kang, Y., Sun, L., Yu, L., Zeng, S., and Cai, S. (2021)
ples, delivery and clinical translation, Nat. Rev. Drug
Recent advances in therapeutic nucleic acids and their
Discov., 20, 817-838, doi: 10.1038/S41573-021-00283-5.
analytical methods, J. Pharm. Biomed. Anal., 206,
2. Kulkarni, J. A., Witzigmann, D., Thomson, S. B.,
114368, doi: 10.1016/J.JPBA.2021.114368.
Chen, S., Leavitt, B. R., Cullis, P. R., and van der
4. Wang, Y., Zhang, R., Tang, L., and Yang, L. (2022)
Meel, R. (2021) The current landscape of nucleic
Nonviral delivery systems of mRNA vaccines for cancer
acid therapeutics, Nat. Nanotechnol., 16, 630-643,
gene therapy, Pharmaceutics, 14, 512, doi: 10.3390/
doi: 10.1038/s41565-021-00898-0.
PHARMACEUTICS14030512.
БИОХИМИЯ том 88 вып. 11 2023
2202
ТИМОТИЕВИЧ и др.
5.
Shirley, J. L., de Jong, Y. P., Terhorst, C., and Herzog,
17.
Khaitov, M., Nikonova, A., Kofiadi, I., Shilovskiy, I.,
R. W. (2020) Immune responses to viral gene therapy
Smirnov, V., Elisytina, O., Maerle, A., Shatilov, A.,
vectors, Mol. Ther.,
28,
709-722, doi:
10.1016/
Shatilova, A., Andreev, S., Sergeev, I., Trofimov, D.,
J.YMTHE.2020.01.001.
Latysheva, T., Ilyna, N., Martynov, A., Rabdano, S.,
6.
Yan, Y., Liu, X. Y., Lu, A., Wang, X. Y., Jiang, L. X.,
Ruzanova, E., Savelev, N., Pletiukhina, I., Safi, A.,
and Wang, J. C. (2022) Non-viral vectors for RNA
Ratnikov, V., Gorelov, V., Kaschenko, V., Kucheren-
delivery, J. Control. Rel., 342, 241, doi: 10.1016/
ko, N., Umarova, I., Moskaleva, S., Fabrichnikov, S.,
J.JCONREL.2022.01.008.
Zuev, O., Pavlov, N., Kruchko, D., Berzin, I.,
7.
Zou, Z., Shen, Q., Pang, Y., Li, X., Chen, Y.,
Goryachev, D., Merkulov, V., Shipulin, G., Udin, S.,
Wang, X., Luo, X., Wu, Z., Bao, Z., Zhang, J.,
Trukhin, V., Valenta, R., and Skvortsova, V. (2023)
Liang, J., Kong, L., Yan, L., Xiong, L., Zhu, T.,
Treatment of COVID-19 patients with a SARS-CoV-2-
Yuan, S., Wang, M., Cai, K., Yao, Y., Wu, J., Jiang, Y.,
specific siRNA-peptide dendrimer formulation,
Liu, H., Liu, J., Zhou, Y., Dong, Q., Wang, W.,
Allergy, 78, 1639-1653, doi: 10.1111/ALL.15663.
Zhu, K., Li, L., Lou, Y., Wang, H., Li, Y., and Lin, H.
18.
Sridharan, K., and Gogtay, N. J. (2016) Therapeutic
(2019) The synthesized transporter K16APoE enabled
nucleic acids: current clinical status, Br. J. Clin.
the therapeutic HAYED peptide to cross the blood-brain
Pharmacol., 82, 659-672, doi: 10.1111/BCP.12987.
barrier and remove excess iron and radicals in the brain,
19.
Davies-Sala, C., Soler-Bistué, A., Bonomo, R. A.,
thus easing Alzheimer’s disease, Drug Deliv. Transl. Res.,
Zorreguieta, A., and Tolmasky, M. E. (2015) External
9, 394-403, doi: 10.1007/s13346-018-0579-4.
guide sequence technology: a path to development of
8.
Matijass, M., and Neundorf, I. (2021) Cell-penetrat-
novel antimicrobial therapeutics, Ann. N. Y. Acad. Sci.,
ing peptides as part of therapeutics used in cancer re-
1354, 98-110, doi: 10.1111/NYAS.12755.
search, Med. Drug Discov., 10, 100092, doi: 10.1016/
20.
Gadgil, H., and Jarrett, H. W. (2002) Oligonucleotide
j.medidd.2021.100092.
trapping method for purification of transcription
9.
Derakhshankhah, H., and Jafari, S.
(2018) Cell
factors, J. Chromatogr. A, 966, 99-110, doi: 10.1016/
penetrating peptides: a concise review with emphasis
s0021-9673(02)00738-0.
on biomedical applications, Biomed. Pharmacother.,
21.
Vickers, T. A., Sabripour, M., and Crooke, S. T. (2011)
108, 1090-1096, doi: 10.1016/j.biopha.2018.09.097.
U1 adaptors result in reduction of multiple pre-mRNA
10.
Kang, Y. C., Son, M., Kang, S., Im, S., Piao, Y., Lim,
species principally by sequestering U1snRNP, Nucleic
K. S., Song, M. Y., Park, K. S., Kim, Y. H., and Pak,
Acids Res., 39, e71, doi: 10.1093/NAR/GKR150.
Y. K. (2018) Cell-penetrating artificial mitochon-
22.
Agrawal, N., Dasaradhi, P. V. N., Mohmmed, A.,
dria-targeting peptide-conjugated metallothionein 1A
Malhotra, P., Bhatnagar, R. K., and Mukherjee, S. K.
alleviates mitochondrial damage in Parkinson’s dis-
(2003) RNA interference: biology, mechanism, and
ease models, Exp. Mol. Med., 50, 1-13, doi: 10.1038/
applications, Microbiol. Mol. Biol. Rev.,
67,
657,
s12276-018-0124-z.
doi: 10.1128/MMBR.67.4.657-685.2003.
11.
Xie, J., Bi, Y., Zhang, H., Dong, S., Teng, L., Lee,
23.
Hammond, S. M., Boettcher, S., Caudy, A. A.,
R. J., and Yang, Z. (2020) Cell-penetrating peptides
Kobayashi, R., and Hannon, G. J. (2001) Argonaute 2,
in diagnosis and treatment of human diseases: from
a link between genetic and biochemical analyses
preclinical research to clinical application, Front.
of RNAi, Science,
293,
1146-1150, doi:
10.1126/
Pharmacol., 11, 697, doi: 10.3389/fphar.2020.00697.
science.1064023.
12.
Lopuszynski, J., Agrawal, V., and Zahid, M. (2022)
24.
Gangopadhyay, S., and Gore, K. R. (2022) Advanc-
Tissue-specific cell penetrating peptides for targeted
es in siRNA therapeutics and synergistic effect on
delivery of small interfering RNAs, Med. Res. Arch.,
siRNA activity using emerging dual ribose modifica-
doi: 10.18103/mra.v10i8.2998.
tions, RNA Biol., 19, 452-467, doi: 10.1080/15476286.
13.
Nhàn, N. T. T., Maidana, D. E., and Yamada, K. H.
2022.2052641.
(2023) Ocular delivery of therapeutic agents by cell-
25.
Wan-Hin Hui, R., Mak, L. Y., Seto, W. K., and Yuen,
penetrating peptides, Cells, 12, 1071, doi: 10.3390/
M. F. (2022) RNA interference as a novel treatment
cells12071071.
strategy for chronic hepatitis B infection, Clin. Mol.
14.
Zorko, M., Jones, S., and Langel, Ü. (2022) Cell-
Hepatol., 28, 408, doi: 10.3350/CMH.2022.0012.
penetrating peptides in protein mimicry and cancer
26.
Ray, K. K., Wright, R. S., Kallend, D., Koenig, W.,
therapeutics, Adv. Drug Deliv. Rev., 180, 114044,
Leiter, L. A., Raal, F. J., Bisch, J. A., Richardson, T.,
doi: 10.1016/J.ADDR.2021.114044.
Jaros, M., Wijngaard, P. L. J., and Kastelein, J. J. P.
15.
Jiang, J. (2021) Cell-penetrating peptide-mediated
(2020) Two phase 3 trials of inclisiran in patients with
nanovaccine delivery, Curr. Drug Targets, 22, 896-912,
elevated LDL cholesterol, New Eng. J. Med., 382,
doi: 10.2174/1389450122666210203193225.
1507-1519, doi: 10.1056/nejmoa1912387.
16.
Delcroix, M., and Riley, L. W. (2010) Cell-penetrating
27.
Zhang, M. M., Bahal, R., Rasmussen, T. P.,
peptides for antiviral drug development, Pharmaceuti-
Manautou, J. E., and Zhong, X.-Bo (2021) The growth
cals, 3, 448-470, doi: 10.3390/ph3030448.
of siRNA-based therapeutics: updated clinical studies,
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2203
Biochem. Pharmacol.,
189,
114432, doi:
10.1016/
41.
Holm, T., Andaloussi, S. El, and Langel, Ü. (2011)
J.BCP.2021.114432.
Comparison of CPP uptake methods, Methods
28.
Khaitov, M., Nikonova, A., Shilovskiy, I.,
Mol. Biol.,
683,
207-217, doi:
10.1007/978-1-
Kozhikhova, K., Kofiadi, I., Vishnyakova, L.,
60761-919-2_15.
Nikolskii, A., Gattinger, P., Kovchina, V., Barvin-
42.
Li, Z., Zhang, Y., Zhu, D., Li, S., Yu, X., Zhao, Y.,
skaia, E., Yumashev, K., Smirnov, V., Maerle, A.,
Ouyang, X., Xie, Z., and Li, L. (2017) Transporting
Kozlov, I., Shatilov, A., Timofeeva, A., Andreev, S.,
carriers for intracellular targeting delivery via non-
Koloskova, O., Kuznetsova, N., Vasina, D., Nikifo-
endocytic uptake pathways, Drug Deliv., 24, 45-55,
rova, M., Rybalkin, S., Sergeev, I., Trofimov, D.,
doi: 10.1080/10717544.2017.1391889.
Martynov, A., Berzin, I., Gushchin, V., Kovalchuk, A.,
43.
Sadeghian, I., Heidari, R., Sadeghian, S., Raee, M. J.,
Borisevich, S., Valenta, R., Khaitov, R., and Skvortso-
and Negahdaripour, M. (2022) Potential of cell-
va, V. (2021) Silencing of SARS-CoV-2 with modified
penetrating peptides (CPPs) in delivery of antiviral
siRNA-peptide dendrimer formulation, Allergy, 76,
therapeutics and vaccines, Eur. J. Pharm. Sci., 169,
2840-2854, doi: 10.1111/all.14850.
106094, doi: 10.1016/J.EJPS.2021.106094.
29.
Pardi, N., Hogan, M. J., and Weissman, D. (2020)
44.
Trabulo, S., Cardoso, A. L., Mano, M., and de
Recent advances in mRNA vaccine technology,
Lima, M. C. P. (2010) Cell-penetrating peptides -
Curr. Opin. Immunol., 65, 14-20, doi: 10.1016/J.COI.
mechanisms of cellular uptake and generation of
2020.01.008.
delivery systems, Pharmaceuticals,
3,
961-993,
30.
Ledford, H. (2020) Moderna COVID vaccine becomes
doi: 10.3390/PH3040961.
second to get US authorization, Nature, doi: 10.1038/
45.
Nath, A. (2021) Prediction for understanding the
D41586-020-03593-7.
effectiveness of antiviral peptides, Comput. Biol. Chem.,
31.
Blind, J. E., McLeod, E. N., Brown, A., Patel, H.,
95, 107588, doi: 10.1016/j.compbiolchem.2021.107588.
and Ghosh, S. (2020) Biosafety practices for in vivo
46.
Kaksonen, M., and Roux, A. (2018) Mechanisms of
viral-mediated gene therapy in the health care setting,
clathrin-mediated endocytosis, Nat. Rev. Mol. Cell
Appl. Biosaf., 25, 194, doi: 10.1177/1535676020942195.
Biol., 19, 313-326, doi: 10.1038/NRM.2017.132.
32.
Roberts, T. C., Langer, R., and Wood, M. J. A.
47.
Kawaguchi, Y., Takeuchi, T., Kuwata, K., Chiba, J.,
(2020) Advances in oligonucleotide drug delivery,
Hatanaka, Y., Nakase, I., and Futaki, S.
(2016)
Nat. Rev. Drug Discov., 19, 673, doi: 10.1038/S41573-
Syndecan-4 is a receptor for clathrin-mediated
020-0075-7.
endocytosis of arginine-rich cell-penetrating peptides,
33.
Chen, H., Ren, X., Xu, S., Zhang, D., and Han, T.
Bioconjug. Chem., 27, 1119-1130, doi: 10.1021/ACS.
(2022) Optimization of lipid nanoformulations for
BIOCONJCHEM.6B00082.
effective mRNA delivery, Int. J. Nanomed., 17, 2893-
48.
Futaki, S., and Nakase, I.
(2017) Cell-surface
2905, doi: 10.2147/IJN.S363990.
interactions on arginine-rich cell-penetrating peptides
34.
Paunovska, K., Loughrey, D., and Dahlman, J. E.
allow for multiplex modes of internalization, Acc.
(2022) Drug delivery systems for RNA therapeutics,
Chem. Res.,
50,
2449-2456, doi:
10.1021/ACS.
Nat. Rev. Genet.,
23,
265, doi:
10.1038/S41576-
ACCOUNTS.7B00221.
021-00439-4.
49.
Pujals, S., and Giralt, E.
(2008) Proline-rich,
35.
Khan, M. M., Filipczak, N., and Torchilin, V. P. (2021)
amphipathic cell-penetrating peptides, Adv. Drug Deliv.
Cell penetrating peptides: A versatile vector for co-
Rev., 60, 473-484, doi: 10.1016/J.ADDR.2007.09.012.
delivery of drug and genes in cancer, J. Controll. Rel.,
50.
Säälik, P., Padari, K., Niinep, A., Lorents, A.,
330, 1220-1228, doi: 10.1016/j.jconrel.2020.11.028.
Hansen, M., Jokitalo, E., Langel, Ü., and Pooga, M.
36.
Taylor, R. E., and Zahid, M. (2020) Cell penetrating
(2009) Protein delivery with transportans is mediated
peptides, novel vectors for gene therapy, Pharmaceutics,
by caveolae rather than flotillin-dependent pathways,
12, 225, doi: 10.3390/pharmaceutics12030225.
Bioconjug. Chem.,
20,
877-887, doi:
10.1021/
37.
Falato, L., Gestin, M., and Langel, Ü. (2021) Cell-
BC800416F.
penetrating peptides delivering siRNAs: An overview,
51.
Taylor, B. N., Mehta, R. R., Yamada, T., Lekmine, F.,
Methods Mol. Biol., 2282, 329-352, doi: 10.1007/
Christov, K., Chakrabarty, A. M., Green, A.,
978-1-0716-1298-9_18.
Bratescu, L., Shilkaitis, A., Beattie, C. W., and das
38.
Rádis-Baptista, G. (2021) Cell-penetrating peptides
Gupta, T. K. (2009) Noncationic peptides obtained
derived from animal venoms and toxins, Toxins (Basel),
from azurin preferentially enter cancer cells, Cancer
13, 147, doi: 10.3390/toxins13020147.
Res., 69, 537-546, doi: 10.1158/0008-5472.can-08-2932.
39.
Zorko, M., and Langel, Ü. (2022) Cell-penetrating
52.
Ye, J., Pei, X., Cui, H., Yu, Z., Lee, H., Wang, J.,
peptides, Methods Mol. Biol.,
2383,
3-32,
Wang, X., Sun, L., He, H., and Yang, V. C. (2018)
doi: 10.1007/978-1-0716-1752-6_1.
Cellular uptake mechanism and comparative in vitro
40.
Ruseska, I., and Zimmer, A. (2020) Internalization
cytotoxicity studies of monomeric LMWP-siRNA
mechanisms of cell-penetrating peptides, Beilstein J.
conjugate, J. Industr. Engineer. Chem., 63, 103-111,
Nanotechnol., 11, 101-123, doi: 10.3762/bjnano.11.10.
doi: 10.1016/J.JIEC.2018.02.005.
БИОХИМИЯ том 88 вып. 11 2023
2204
ТИМОТИЕВИЧ и др.
53.
Yang, S. T., Zaitseva, E., Chernomordik, L. V., and
65.
Zeng, Z., Han, S., Hong, W., Lang, Y., Li, F., Liu, Y.,
Melikov, K. (2010) Cell-penetrating peptide induces
Li, Z., Wu, Y., Li, W., Zhang, X., and Cao, Z. (2016)
leaky fusion of liposomes containing late endosome-
A Tat-conjugated peptide nucleic acid Tat-PNA-DR
specific anionic lipid, Biophys. J., 99, 2525-2533,
inhibits hepatitis B virus replication in vitro and
doi: 10.1016/J.BPJ.2010.08.029.
in vivo by targeting LTR direct repeats of HBV RNA,
54.
Cerrato, C. P., and Langel, Ü. (2022) An update on
Mol. Ther. Nucleic Acids, 5, e295, doi: 10.1038/
cell-penetrating peptides with intracellular organelle
MTNA.2016.11.
targeting, Expert Opin. Drug Deliv.,
19,
133-146,
66.
Moerdyk-Schauwecker, M., Stein, D. A., Eide, K.,
doi: 10.1080/17425247.2022.2034784.
Blouch, R. E., Bildfell, R., Iversen, P., and Jin, L.
55.
Wang, H. Y., Chen, J. X., Sun, Y. X., Deng, J. Z.,
(2009) Inhibition of HSV-1 ocular infection with mor-
Li, C., Zhang, X. Z., and Zhuo, R. X.
(2011)
pholino oligomers targeting ICP0 and ICP27, Antiviral
Construction of cell penetrating peptide vectors
Res., 84, 131-141, doi: 10.1016/J.antiviral.2009.07.020.
with N-terminal stearylated nuclear localization
67.
Mehrlatifan, S., Mirnurollahi, S. M., Motevalli, F.,
signal for targeted delivery of DNA into the cell
Rahimi, P., Soleymani, S., and Bolhassani, A. (2016)
nuclei, J. Control Rel., 155, 26-33, doi: 10.1016/
The structural HCV genes delivered by MPG cell
J.JCONREL.2010.12.009.
penetrating peptide are directed to enhance immune
56.
Alkhashrom, S., Kicuntod, J., Stillger, K., Lützen-
responses in mice model, Drug Deliv., 23, 2852-2859,
burg, T., Anzenhofer, C., Neundorf, I., Marschall, M.,
doi: 10.3109/10717544.2015.1108375.
and Eichler, J. (2022) A peptide inhibitor of the
68.
Moulton, H. M., Fletcher, S., Neuman, B. W.,
human cytomegalovirus core nuclear egress complex,
McClorey, G., Stein, D. A., Abes, S., Wilton, S. D.,
Pharmaceuticals, 15, 1040, doi: 10.3390/PH15091040.
Buchmeier, M. J., Lebleu, B., and Iversen, P. L.
57.
Huang, S., Zhu, Z., Jia, B., Zhang, W., and Song,
(2007) Cell-penetrating peptide-morpholino conju-
J. (2021) Design of acid-activated cell-penetrating
gates alter pre-mRNA splicing of DMD (Duchenne
peptides with nuclear localization capacity for
muscular dystrophy) and inhibit murine coronavirus
anticancer drug delivery, J. Pept. Sci., 27, e3354,
replication in vivo, Biochem. Soc. Trans., 35, 826-828,
doi: 10.1002/PSC.3354.
doi: 10.1042/BST0350826.
58.
Mueller, J., Kretzschmar, I., Volkmer, R., and
69.
Hosseini, A., Lattanzio, F. A., Samudre, S. S.,
Boisguerin, P. (2008) Comparison of cellular uptake
Disandro, G., Sheppard, J. D., and Williams, P. B.
using 22 CPPs in 4 different cell lines, Bioconjug.
(2012) Efficacy of a phosphorodiamidate morpholino
Chem., 19, 2363-2374, doi: 10.1021/BC800194E.
oligomer antisense compound in the inhibition of
59.
Chiu, Y. L., Ali, A., Chu, C. Y., Cao, H., and Rana,
corneal transplant rejection in a rat cornea transplant
T. M. (2004) Visualizing a correlation between siRNA
model, J. Ocul. Pharmacol. Ther.,
28,
194-201,
localization, cellular uptake, and RNAi in living cells,
doi: 10.1089/JOP.2011.0135.
Chem. Biol., 11, 1165-1175, doi: 10.1016/j.chembiol.
70.
Zhang, C., Ren, W., Liu, Q., Tan, Z., Li, J., and
2004.06.006.
Tong, C. (2019) Transportan-derived cell-penetrating
60.
Tai, W., and Gao, X. (2017) Functional peptides
peptide delivers siRNA to inhibit replication of
for siRNA delivery, Adv. Drug Deliv. Rev., 110-111,
influenza virus in vivo, Drug Des. Devel. Ther., 13,
157-168, doi: 10.1016/J.ADDR.2016.08.004.
1059-1068, doi: 10.2147/DDDT.S195481.
61.
Wang, F., Wang, Y., Zhang, X., Zhang, W., Guo, S.,
71.
Yuan, J., Stein, D. A., Lim, T., Qiu, D., Coughlin, S.,
and Jin, F. (2014) Recent progress of cell-penetrating
Liu, Z., Wang, Y., Blouch, R., Moulton, H. M.,
peptides as new carriers for intracellular cargo
Iversen, P. L., and Yang, D. (2006) Inhibition of
delivery, J. Control Rel., 174, 126-136, doi: 10.1016/
Coxsackievirus B3 in cell cultures and in mice by
J.JCONREL.2013.11.020.
peptide-conjugated morpholino oligomers targeting
62.
Guidotti, G., Brambilla, L., and Rossi, D. (2017) Cell-
the internal ribosome entry site, J. Virol., 80, 11510,
penetrating peptides: from basic research to clinics,
doi: 10.1128/JVI.00900-06.
Trends Pharmacol. Sci., 38, 406-424, doi: 10.1016/
72.
Enterlein, S., Warfield, K. L., Swenson, D. L., Stein,
J.TIPS.2017.01.003.
D. A., Smith, J. L., Gamble, C. S., Kroeker, A. D.,
63.
Crombez, L., Morris, M. C., Dufort, S., Aldrian-
Iversen, P. L., Bavari, S., and Mühlberger, E. (2006)
Herrada, G., Nguyen, Q., Mc Master, G., Coll, J. L.,
VP35 knockdown inhibits Ebola virus amplification
Heitz, F., and Divita, G. (2009) Targeting cyclin B1
and protects against lethal infection in mice,
through peptide-based delivery of siRNA prevents
Antimicrob. Agents Chemother., 50, 984, doi: 10.1128/
tumour growth, Nucleic Acids Res., 37, 4559-4569,
AAC.50.3.984-993.2006.
doi: 10.1093/NAR/GKP451.
73.
Kozhikhova, K. V., Shilovskiy, I. P., Shatilov, A. A.,
64.
Michiue, H., Eguchi, A., Scadeng, M., and Dowdy,
Timofeeva, A. V., Turetskiy, E. A., Vishniakova, L. I.,
S. F. (2009) Induction of in vivo synthetic lethal RNAi
Nikolskii, A. A., Barvinskaya, E. D., Karthikeyan, S.,
responses to treat glioblastoma, Cancer Biol. Ther., 8,
Smirnov, V. V., Kudlay, D. A., Andreev, S. M., and
2304-2311, doi: 10.4161/CBT.8.23.10271.
Khaitov, M. R. (2020) Linear and dendrimeric antiviral
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДНЫЕ НОСИТЕЛИ КАК СРЕДСТВА ДОСТАВКИ
2205
peptides: design, chemical synthesis and activity
Immunologiya, 42, 600-614, doi: 10.33029/0206-4952-
against human respiratory syncytial virus, J. Mater.
2021-42-6-600-614.
Chem. B, 8, 2607-2617, doi: 10.1039/c9tb02485a.
76. Shilovskiy, I., Sundukova,M., Korneev, A.,Nikolskii, A.,
74. Shilovskiy, I., Nikonova, A., Barvinskaia, E., Ka-
Barvinskaya, E., Kovchina, V., Vishniakova, L.,
ganova, M., Nikolskii, A., Vishnyakova, L.,
Turenko, V., Yumashev, K., Kaganova, M., Brilina, V.,
Kovchina, V., Yumashev, K., Korneev, A., Petukhova, O.,
Sergeev, I., Maerle, A., Kudlay, D., Petukhova, O.,
Kudlay, D., Smirnov, V., Andreev, S., Kozhikhova, K.,
Khaitov, M. (2022) The mixture of siRNAs targeted
Shatilov, A., Shatilova, A., Maerle, A., Sergeev, I.,
to IL-4 and IL-13 genes effectively reduces the airway
Trofimov, D., and Khaitov, M. (2022) Anti-inflam-
hyperreactivity and allergic inflammation in a mouse
matory effect of siRNAs targeted il-4 and il-13 in a
model of asthma, Int. Immunopharmacol.,
103,
mouse model of allergic rhinitis, Allergy, 77, 2829-
108432, doi: 10.1016/J.INTIMP.2021.108432.
2832, doi: 10.1111/ALL.15366.
77. Stiltner, J., McCandless, K., and Zahid, M. (2021)
75. Nikolskii, A. A., Shilovskiy, I. P., Yumashev, K. V.,
Cell-penetrating peptides: applications in tumor
Vishniakova, L. I., Barvinskaia, E. D., Kovchina, V. I.,
diagnosis and therapeutics, Pharmaceutics, 13, 890,
Korneev, A. V., Turenko, V. N., Kaganova, M. M.,
doi: 10.3390/PHARMACEUTICS13060890.
Brylina, V. E., Nikonova, A. A., Kozlov, I. B., Kofiadi,
78. Abes, R., Arzumanov, A. A., Moulton, H. M., Abes, S.,
I. A., Sergeev, I. V., Maerle, A. V., Petukhova, O. A.,
Ivanova, G. D., Iversen, P. L., Gait, M. J., and Lebleu, B.
Kudlay, D. A., and Khaitov, M. R. (2021) Effect of
(2007) Cell-penetrating-peptide-based delivery of
local suppression of Stat3 gene expression in a mouse
oligonucleotides: an overview, Biochem. Soc. Trans.,
model of pulmonary neutrophilic inflammation,
35, 775-779, doi: 10.1042/BST0350775.
PEPTIDE CARRIERS AS DELIVERY VEHICLES
FOR THERAPEUTIC NUCLEIC ACIDS.
MECHANISMS AND POTENTIAL APPLICATIONS IN MEDICINE
Review
E. D. Timotievich*, I. P. Shilovskiy, and M. R. Khaitov
Institute of Immunology, National Research Center, Federal Medical-Biological Agency of Russia
115522 Moscow, Russia; e-mail: ed0594@yandex.ru
Currently, a significant number of drugs based on therapeutic nucleic acids are being under development
for the treatment of oncological, inflammatory, infectious diseases, and metabolic disorders. A grow-
ing number of approved nucleic acid therapeutics demonstrate the potential of gene therapy approaches.
Therapeutic nucleic acids realize their biological effect in the cytoplasm, while plasma membrane is the
main barrier to their intracellular delivery. Therefore, specially designed carriers are often used during the
development of such drugs. The optimal carrier should not only facilitate the internalization of nucleic
acids, but also exhibit no toxic effects, provide stabilization, and must be suitable for large scale production
at low cost. Cell penetrating peptides (CPPs) match all these requirements. CPPs are effective and low-toxic
carriers of nucleic acids. They usually represent basic peptides with a positive charge at physiological pH
that capable to form nanostructures with negatively charged nucleic acids. Numerous preclinical studies
in which CPP has been used as a carrier have shown promising results. In some cases, CPP-containing
drugs successfully passed through clinical trials and the implemented into clinical practice. In this review,
we consider the variety of therapeutic nucleic acids and summarize the experience of using CPP for their
intracellular delivery. In addition, the classification and mechanisms of CPP cellular uptake are discussed,
the understanding of which will accelerate the development of new gene therapy drugs.
Keywords: cell penetrating peptides, peptide delivery systems, nucleic acid delivery vehicles, siRNA
БИОХИМИЯ том 88 вып. 11 2023