БИОХИМИЯ, 2023, том 88, вып. 11, с. 2221 - 2234
УДК 577.21
РАЗНООБРАЗИЕ И ЭВОЛЮЦИЯ
ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
Обзор
© 2023 М.В. Балева, У.Е. Пиунова, И.В. Чичерин, С.А. Левицкий, П.А. Каменский*
Московский государственный университет имени М.В. Ломоносова, биологический факультет,
119234 Москва, Россия; электронная почта: piotr.kamenski@gmail.com
Поступила в редакцию 18.07.2023
После доработки: 25.09.2023
Принята к публикации 26.09.2023
Эволюция митохондрий протекала независимо в разных эукариотических линиях, что отражается
в многообразии митохондриальных геномов и механизмов их экспрессии, наблюдаемых у разных
представителей эукариот. Митохондрии утратили подавляющее большинство генов своего бак-
териального предка, часть из которых была перенесена в ядро, а остальные - утрачены. Таким
образом, в митохондриях практически всех эукариотических клеток сохранились сравнительно
небольшие геномы, а также аппараты их репликации, транскрипции и трансляции. Зависимость
от ядерного генома, особенности митохондриальных транскриптов, необходимость синтеза вы-
сокогидрофобных мембранных белков привели к тому, что аппарат митохондриальной трансля-
ции, полученный от бактериального предка, претерпел ряд существенных изменений. Он сохранил
базовую структуру, необходимую для осуществления синтеза белка, но стал более специализиро-
ванным и лабильным. В данном обзоре мы рассматриваем изменения, произошедшие в процессе
инициации митохондриальной трансляции, а также то, как эволюция митохондрий отразилась
на функциях основных факторов инициации биосинтеза белка в этих органеллах.
КЛЮЧЕВЫЕ СЛОВА: митохондрии, факторы инициации трансляции, регуляция трансляции, трансляция.
DOI: 10.31857/S0320972523110143, EDN: MPXROI
ВВЕДЕНИЕ
мом, синтезируются в цитозоле, а затем им-
портируются в митохондрии.
Митохондрии - двумембранные органел-
Возникновение митохондрий предшество-
лы эукариотической клетки, предки которых
вало разделению общего эволюционного ство-
относятся к альфа-протеобактериям, родствен-
ла древних эукариот на ряд ветвей, давших
ным современной группе Rickettsiales [1]. Роль
начало новым типам. Этим может быть объ-
митохондрий в жизнедеятельности клетки
яснено и существующее разнообразие мито-
сложно переоценить: помимо дыхания, они
хондриальных геномов, отличающихся струк-
участвуют в метаболизме аминокислот и нук-
турой, размером, а также организацией про-
леотидов, в биогенезе липидов и железосер-
цессов экспрессии митохондриальных генов
ных (Fe/S) кластеров, являются ключевым
у разных групп эукариот. Большинство живот-
сигнальным пунктом клетки и регуляторами
ных, за исключением некоторых артропод, мол-
апоптоза [2-4]. В результате эволюции мито-
люсков и нематод, имеют исключительно ком-
хондрии утратили большую часть генов своего
пактные митохондриальные геномы (~16 тпн)
бактериального предка, которые либо были
в виде кольцевой молекулы с ограниченным
полностью утеряны, либо перенесены в ядер-
числом некодирующих последовательностей [6].
ный геном [5]. Подавляющее большинство бел-
В то же время митохондриальные геномы расте-
ков митохондрий кодируются ядерным гено- ний намного больше (до нескольких сотен тпн)
Принятые сокращения: 5′-НТО - 5′-нетранслируемая область; P-сайт - пептидильный участок; тпн - тысяча
пар нуклеотидов; mtIF - митохондриальные факторы инициации; PPR - семейство пентатрикопептидных белков;
SD - последовательности Шайна-Дальгарно.
* Адресат для корреспонденции.
2221
2222
БАЛЕВА и др.
и сильно отличаются по размеру даже у близ-
соме (1,4 МДа) [11]. Резкое уменьшение коли-
кородственных видов [7]. Так, митохондриаль-
чества митохондриальной рРНК в основном
ный геном Silene latifolia состоит из всего одной
характерно для билатеральных Metazoa, к ко-
хромосомы размером 253 тпн, в то время как у
торым относятся млекопитающие. Например,
Silene conica он состоит из 128 хромосом, раз-
миторибосомы млекопитающих на 25-30%
мер которых варьирует от 44 до 192 тпн. Инте-
состоят из РНК, в то время как бактериаль-
ресна организация митохондриального гено-
ные рибосомы - на 60-70% [11]. В отличие от
ма у представителей отряда Trypanosomatida.
бактериальных и цитоплазматических рибо-
Трипаносомная митохондриальная ДНК пред-
сом, миторибосомы большинства организмов
ставляет собой сеть из многочисленных макси-
утратили 5S рРНК, но у некоторых организ-
и мини-колец, связанных по типу катенанов,
мов она сохранилась. По данным структур-
причем основную генетическую информацию
ных исследований, 5S рРНК была обнаружена
содержат в себе макси-кольца, а в мини-
в составе миторибосом Arabidopsis thaliana [12],
кольцах закодированы малые РНК [8]. Мито-
также неканонические 5S рРНК обнаружи-
хондриальные ДНК могут кодировать транс-
ваются у Chlamydomonas reinhardtii [13] и Plas-
портные и рибосомные РНК, а также белки,
modium falciparum [14]. У млекопитающих в со-
участвующие в репликации и экспрессии ми-
став большой субъединицы миторибосом вхо-
тохондриального генома, митохондриальной
дят митохондриальные тРНКVal или тРНКPhe,
трансляции, а также субъединицы комплек-
занимающие место 5S рРНК [15].
сов цепи окислительного фосфорилирования.
Эволюция митохондриальных рРНК про-
Количество оставшихся белок-кодирующих
исходила в разных направлениях: как дегра-
генов также варьирует от двух (Сox1 и Сox3) -
дации, так и экспансии. Например, РНК боль-
у Chromera velia до 67 - у Reclimonas americans,
шой субъединицы дрожжевой рибосомы ха-
хотя большинство митохондриальных гено-
рактеризуется появлением значительных до-
мов содержат от 12 до 20 генов [5, 9]. Несмотря
полнительных участков по сравнению с бак-
на небольшое количество генов, оставшихся
териальной 16S рРНК. Все эти участки рас-
в составе митохондриальной ДНК, митохондрии
полагаются на периферии, некоторые из них
сохранили полностью функциональный ап-
участвуют в формировании «ножки» для ас-
парат для их транскрипции и трансляции,
социации миторибосомы дрожжей с поверх-
основанный на упрощенной бактериальной
ностью внутренней митохондриальной мем-
модели, дополненной в результате эволюции
браны [16]. Реорганизация рРНК в ходе эво-
новыми чертами и факторами, уникальными
люции привела к тому, что часть бактериаль-
для каждого вида эукариот.
ных белков была утрачена миторибосомой.
Так, редукция петель h8, h9 и h44 в 18S рРНК
малой субъединицы миторибосомы Arabidopsis
ЭВОЛЮЦИЯ
привела к потере рибосомного белка S20. Уда-
МИТОХОНДРИАЛЬНЫХ РИБОСОМ
ление 5S рРНК у дрожжей совпало с поте-
рей белков большой субъединицы bL25m и
Процесс трансляции в митохондриях осу-
uL18m [9]. В целом, в процессе эволюции мито-
ществляется особыми митохондриальными
хондриальная рибосома увеличила белковую
рибосомами (миторибосомами) - РНК-бел-
массу в большинстве эукариотических линий.
ковыми комплексами, которые преобразуют
Часть миторибосомных белков - гомо-
закодированную в мРНК генетическую ин-
логов рибосомных белков бактерий, имеют
формацию в белки. Подобно всем рибосомам,
значительно большую массу или характери-
миторибосомы состоят из двух субъединиц:
зуются наличием N- или C-концевых удли-
большой и малой. Данные структурного и
нений. Иногда это связано с компенсацией
филогенетического анализа миторибосомной
потери структурных доменов рРНК и необхо-
РНК и миторибосомных белков указывают
димостью стабилизации структуры рибосомы.
на то, что рибосомы митохондрий произошли
Многие эволюционно новые миторибосомные
от сходных органелл бактериального пред-
белки были рекрутированы из цитоплазмы.
шественника, альфа-протеобактериального
Чаще всего они не входят в состав кора мито-
предка митохондрий [10]. Миторибосомы край-
рибосомы, а располагаются преимущественно
не гетерогенны по содержанию рРНК. Общая
на периферии [11, 17]. Часть из этих белков,
масса рРНК в исследованных миторибосомах
например mS39, mL41 и mL46, являются кон-
колеблется от 0,5 МДа у Caenorhabditis elegans
сервативными среди эукариот, в то время как
до 1,6 МДа - у Neurospora crassa, что сопоста-
другие белки можно отнести к видоспеци-
вимо с массой рРНК в бактериальной рибо-
фичным [18]. Нередки примеры бифункцио-
БИОХИМИЯ том 88 вып. 11 2023
ЭВОЛЮЦИЯ ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
2223
нальности некоторых приобретенных мито-
кодон-антикодонового взаимодействия. Также
рибосомных белков. Например, белок малой
IF3 способствует диссоциации псевдо-ини-
субъединицы mS29 является участником апоп-
циаторных комплексов (содержащих отлич-
тоза, индуцируемого Dap3, а также способен
ную от инициаторной тРНК) и неканониче-
проявлять GTPазную активность [19].
ских инициаторных комплексов (содержащих
Вероятно, такое разнообразие митохон-
стартовый кодон, отличный от AUG, GUG
дриальных рибосом определяется описанным
и UUG). Формирование правильного кодон-
выше разнообразием геномов митохондрий и
антикодонового взаимодействия приводит к
отражает их специализацию к биосинтезу не-
ассоциации субъединиц 30S и 50S, диссоциа-
большого количества митохондриально коди-
ции IF3, гидролизу GTP фактором IF2 и выс-
руемых белков.
вобождению факторов IF2 и IF1 [21].
Помимо описанного канонического спо-
соба, у бактерий существует еще два меха-
СПЕЦИАЛИЗАЦИЯ ПРОЦЕССОВ
низма инициации трансляции (рис. 1). Один
ИНИЦИАЦИИ ТРАНСЛЯЦИИ
из них - «сквозное прочтение» («readthrough»),
заключается в том, что после терминации
Большинство митохондриальных белок-
трансляции первого цистрона на полици-
кодирующих генов несут в себе информацию
стронной мРНК рибосома не диссоциирует
о первичной структуре субъединиц комплек-
на субъединицы, а продолжает сканирование
сов цепи окислительного фосфорилирования.
мРНК до следующего стартового кодона [22].
Однако большая часть субъединиц этих ком-
Важную роль в инициации по данному меха-
плексов кодируется в ядре, синтезируется в
низму играет фактор IF3.
перимитохондриальных областях цитозоля и
Помимо мРНК с 5′-нетранслируемой об-
импортируется в митохондрии. Для коррект-
ластью (5′-НТО), в составе которой есть по-
ной сборки комплексов необходима четкая
следовательность SD, у бактерий есть и так
взаимная координация митохондриальной
называемые безлидерные мРНК, лишенные
трансляции и биосинтеза митохондриальных
5′-НТО [23]. У таких мРНК стартовый кодон
белков в цитозоле. По всей видимости, клю-
находится непосредственно на 5′-конце или
чевой стадией такой регуляции является ини-
на небольшом расстоянии от него. В этом слу-
циация трансляции, которая в митохондриях
чае трансляция начинается путем связывания
существенно отличается от бактериальной.
стартового кодона ассоциированной 70S-ри-
Трансляция у бактерий начинается с при-
босомой. Результаты in vitro исследований ука-
влечения мРНК к малой рибосомной субъ-
зывают на то, что при данном механизме фак-
единице и правильного позиционирования
торы инициации не играют важной роли, но
стартового кодона, за эти процессы отвечают
их наличие оказывает стимулирующее воз-
факторы инициации IF1, IF2 и IF3. Фактор
действие на инициацию трансляции, а в слу-
IF3 связывается с малой рибосомной субъ-
чае некоторых мРНК они все же оказываются
единицей, предотвращая ее реассоциацию
необходимыми [24].
с 50S-субъединицей и формируя пул свобод-
Отличительной особенностью митохондри-
ных 30S-субъединиц, необходимых для ини-
альных мРНК является использование стар-
циации трансляции [20]. Фактор IF1 блоки-
товых кодонов, отличных от AUG [25]. Так, в
рует А-cайт малой субъединицы рибосомы,
случае млекопитающих синтез субъединицы 2
способствуя позиционированию инициатор-
NADH-дегидрогеназы (ND2) начинается с AUU,
ной тРНК в пептидильный участок (P-сайт).
а синтез ND1, ND3 и ND5 - с AUA. Все мито-
Далее тройственный комплекс, состоящий из
хондриальные мРНК млекопитающих харак-
IF2, GTP и инициаторной аминоацил-тРНК
теризуются очень короткой, всего 1-3 нуклео-
(fMet-тРНК), связывается с малой рибосомной
тида, 5′НТО или полным ее отсутствием, в
субъединицей. Благодаря узнаванию последо-
то время как мРНК митохондрий дрожжей
вательности Шайна-Дальгарно (SD) в составе
и растений характеризуются протяженными
мРНК последовательностью анти-Шайна-
5′-концевыми удлинениями [26]. Кроме того,
Дальгарно (анти-SD) 16S рРНК происходит по-
все митохондриальные мРНК и рРНК малой
зиционирование стартового кодона в P-сайте
рибосомной субъединицы не содержат после-
рибосомы. IF2 в комплексе с GTP способству-
довательностей SD и анти-SD [27]. Все эти
ет установке инициаторной тРНК в P-сайт.
особенности митохондриальных мРНК ука-
При этом IF3 дискриминирует элонгаторную
зывают на то, что процесс инициации транс-
тРНК и стимулирует образование преини-
ляции в митохондриях должен отличаться от
циаторного комплекса, увеличивая скорость
канонического для бактерий.
БИОХИМИЯ том 88 вып. 11 2023
2224
БАЛЕВА и др.
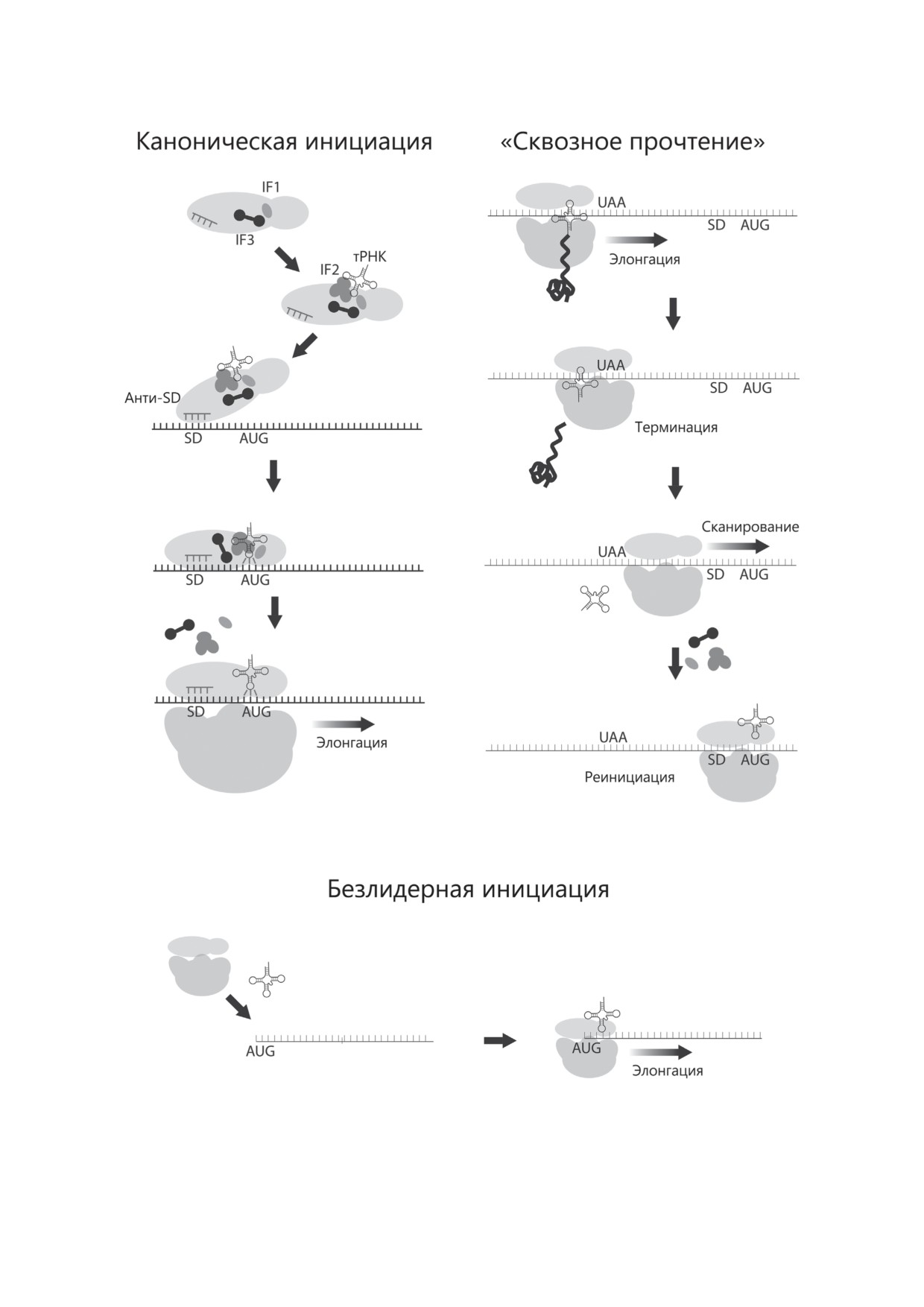
Рис. 1. Инициация трансляции у бактерий. У бактерий в основе инициации трансляции могут лежать три меха-
низма. При канонической инициации последовательность Шайна-Дальгарно (SD) узнается последовательностью
анти-Шайна-Дальгарно (anti-SD), входящей в состав 16S рРНК. Рибосома может не диссоциировать после прочтения
стоп-кодона (UAA) на субъединицы, а продолжить сканирование, пока не найдет следующий стартовый (AUG) кодон.
В случае безлидерных мРНК целая рибосома инициирует трансляцию, хотя механизм узнавания стартового кодона
не ясен
БИОХИМИЯ том 88 вып. 11 2023
ЭВОЛЮЦИЯ ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
2225
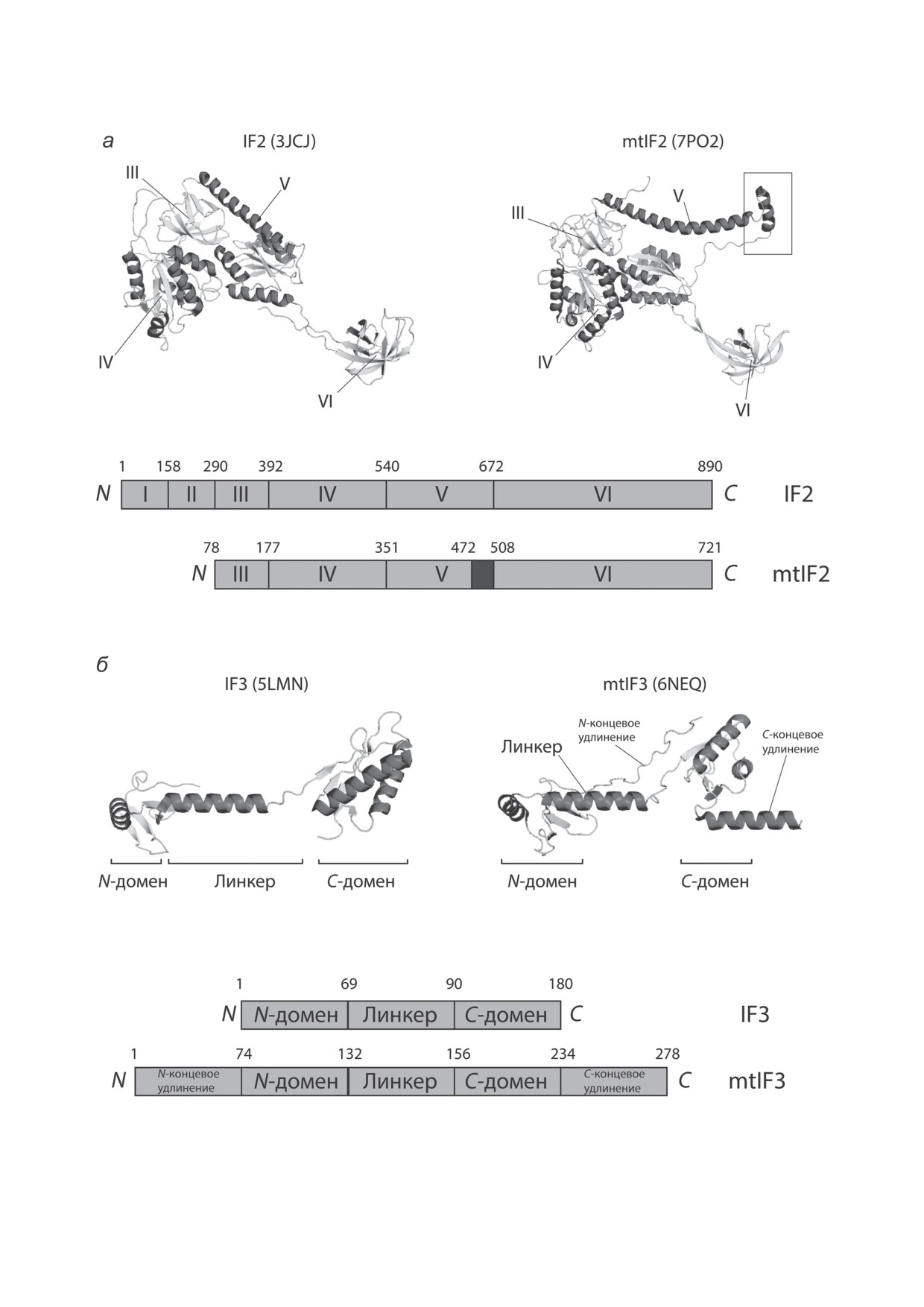
Рис. 2. Доменная организация и структура бактериальных факторов инициации и их гомологов из митохондрий
млекопитающих. а - Структуры бактериального IF2 (PDB ID: 3JCJ) и митохондриального mtIF2 (PDB ID: 7PO2).
Митохондриальный mtIF2 характеризуется отсутствием двух N-концевых доменов и наличием вставки между V и VI
доменами, взаимодействующей с A-сайтом рибосомы, подобно бактериальному IF1 (отмечена квадратным выделе-
нием). б - Структуры бактериального IF3 (PDB ID: 5MLN) и митохондриального mtIF3 (PDB ID: 6NEQ)
13
БИОХИМИЯ том 88 вып. 11 2023
2226
БАЛЕВА и др.
В первую очередь различия наблюдаются
варьировать в зависимости от вида. Напри-
в количестве факторов инициации и их функ-
мер, делеция гена mtIF2 у Schizosaccharomyces
циях. Роль фактора IF2 является ключевой в
pombe приводит к снижению эффективности
процессе инициации трансляции у бактерий.
трансляции всех мРНК [34], а у Saccharomyces
Он специфически связывает инициаторную
cerevisiae - всех, кроме Cytb и Atp9 [35].
fMet-тРНК и правильно позиционирует ее в
Митохондриальный фактор инициации
P-сайте малой субъединицы, увеличивая ско-
трансляции 3 (mtIF3) характеризуется низ-
рость и точность инициации трансляции [28].
кой степенью гомологии как между разными
Это единственный фактор инициации, для ко-
видами, так и по отношению к бактериаль-
торого были обнаружены гомологи в митохон-
ному IF3 (20-25% гомологии). Тем не менее
дриях всех эукариот. Бактериальный IF2 со-
данные in vitro исследований указывают на
стоит из дивергентных N-концевых доменов I
то, что mtIF3 функционально схож с бактери-
и II, участвующих в связывании с малой рибо-
альным IF3 [36]. Митохондриальный mtIF3,
сомной субъединицей, домена III, функция
подобно бактериальному IF3, состоит из двух
которого не ясна, высококонсервативного до-
доменов N и C, соединенных линкером, но име-
мена IV, обладающего GTPазной активностью,
ет дополнительные удлинения на обоих кон-
и двух С-концевых доменов (V и VI). Мито-
цах протяженностью приблизительно 30 а.о.
хондриальные факторы инициации 2 (mtIF2)
(рис. 2, б). В отличие от бактериального IF3, у
лишены первых двух доменов, однако сохра-
которого с 30S-рибосомой связывается только
нили в остальном схожую с бактериальным
C-домен [37], оба домена mtIF3 млекопитаю-
доменную структуру, имея в своем составе до-
щих связываются с 28S малой субъединицей
мены III-VI (рис. 2, а). Следует подчеркнуть,
миторибосомы, а концевые удлинения пре-
что в отличие от бактериального IF2, у кото-
пятствуют присоединению 39S большой субъ-
рого только два N-концевых домена влияют на
единицы [38, 39]. Удаление концевых удли-
связывание с малой субъединицей рибосомы,
нений влияет на функции mtIF3 млекопи-
для эффективного взаимодействия mtIF2
тающих: удаление С-концевого удлинения
c
28S-субъединицей миторибосомы млеко-
нарушает способность mtIF3 дестабилизиро-
питающих необходимо сохранение интакт-
вать неканонические или псевдо-инициатор-
ной мультидоменной структуры фактора [29].
ные комплексы в трансляционной системе
Также митохондриальные IF2 имеют вставку
E. coli, а удаление N-концевого удлинения
между доменами V и VI, длина и последова-
многократно увеличивает сродство фактора
тельность которой отличается у разных видов.
к 39S-субъединице.
Эта вставка взаимодействует с A-сайтом рибо-
У дрожжей Sac. cerevisiae удаление кон-
сомы подобно бактериальному IF1, гомологов
цевых удлинений у Aim23p, дрожжевого ми-
которого в митохондриях обнаружить не уда-
тохондриального гомолога IF3, приводит к
лось [30]. Таким образом, функции бактери-
потере, функциональной активности белка,
альных факторов IF1 и IF2 в митохондриях
вызывая фенотип, аналогичный полной деле-
выполняются mtIF2, что также подтвержда-
ции белка [40]. Подобные данные указывают
ется тем, что mtIF2 может заменить IF1 и IF2 в
на то, что механизмы действия белков Aim23p
клетках Escherichia coli [31], и данными струк-
и mtIF3 млекопитающих (гомологов IF3) от-
турных исследований взаимодействия mtIF2 с
личаются, несмотря на общность функций.
рибосомой E. coli [32]. Несмотря на функцио-
Доказательством этому могут служить и дан-
нальную и структурную схожесть, механизм
ные по исследованию делеций генов дан-
действия бактериального IF2 и митохондри-
ных белков. Делеция гена, кодирующего IF3
ального mtIF2 может отличаться. Так, в мито-
в бактериях E. coli, летальна [41]. Результаты
хондриях млекопитающих инициация транс-
делеции генов митохондриальных факторов,
ляции безлидерных мРНК, как и у бактерий,
гомологичных IF3, у различных организмов
может осуществляться целой рибосомой, но
разнятся. Так, делеция гена, кодирующего
mtIF2, вероятно, играет важную роль в этом
mtIF3 у дрожжей Sch. pombe, никак не влияет
процессе [33]. Так, делеция в гене, кодирую-
ни на рост клеток, ни на митохондриальную
щем mtIF2 в клетках линии HEK293T, при-
трансляцию [34]. В то же время делеция гена,
водит к полной остановке митохондриальной
кодирующего Aim23 в клетках дрожжей Sac.
трансляции.
cerevisiae, приводит к нарушению роста кле-
Совершенно отличная ситуация характер-
ток на средах с несбраживаемым источником
на для дрожжей. Хотя механизм инициации
углерода, что указывает на снижение мито-
трансляции в митохондриях дрожжей до сих
хондриальной функции. Однако возникно-
пор остается неясным, роль mtIF2 в нем может
вение митохондриальной дисфункции в этом
БИОХИМИЯ том 88 вып. 11 2023
ЭВОЛЮЦИЯ ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
2227
случае не связано со снижением эффектив-
СПЕЦИАЛИЗАЦИЯ МЕХАНИЗМОВ
ности трансляции, а определяется ее разба-
РЕКРУТИРОВАНИЯ мРНК
лансировкой: происходит значительное сни-
жение синтеза компонентов цитохром c-ок-
На первых этапах инициации трансляции
сидазного комплекса и увеличение синтеза
мРНК рекрутируется рибосомой для выбора
компонентов ATP-синтазы [42]. В дальней-
стартового кодона. У бактерий в основе это-
шем было показано, что, по крайней мере
го процесса лежит механизм комплементар-
в случае биосинтеза белка Cox2, подобный
ного взаимодействия между последователь-
эффект может быть объясним тем, что
ностью SD, расположенной перед стартовым
Aim23p взаимодействует с белком Pet111 [43],
кодоном, и последовательностью анти-SD
который усиливает эффективность трансля-
16S рРНК. Все митохондриальные мРНК эука-
ции мРНК Cox2. Делеция в гене, кодирую-
риот лишены последовательности SD, а у не-
шем mtIF3 в некоторых линиях клеток чело-
которых из них также нет и 5′-НТО, которые
века, также приводит к митохондриальной
могли бы участвовать в фактор-зависимой ре-
дисфункции в результате снижения синтеза
гуляции выбора стартового кодона.
белка Atp6 [33, 44]. Стоит отметить, что не-
Наличие у митохондриальных мРНК пе-
смотря на незначительное влияние mtIF3 на
карских дрожжей протяженных
5′-концевых
митохондриальную трансляцию в клеточ-
удлинений при отсутствии специфических сай-
ных линиях, делеция в гене mtIF3 на уровне
тов посадки рибосом должно создавать трудно-
организма у млекопитающих летальна: гомо-
сти при выборе стартового кодона. Подобная
зиготные мыши, нокаутные по гену mtIF3,
проблема в цитоплазматической трансляции
умирают на стадии эмбриона, в то время как
решается тем, что преинициаторный комплекс
гетерозиготные особи характеризуются раз-
связывается с кэпированным 5′-концом мРНК
витием у них прогрессирующей кардиомиопа-
и сканирует 5′-НТО в поисках стартового ко-
тии. Исследование профиля митохондриаль-
дона [46]. В митохондриях нет факторов для
ной трансляции в клетках сердечных мышц
реализации подобного сканирующего меха-
таких животных выявляет снижение уровня
низма, а мРНК не кэпированы. Вместо этого
синтеза белка ND3 [45]. Суммируя вышепри-
у дрожжей есть набор так называемых транс-
веденные данные, mtIF3 можно рассматривать
ляционных активаторов (см. таблицу), кото-
как тканеспецифический регулятор транс-
рые связываются с 5′-нетранслируемыми об-
ляции определенных мРНК в митохондриях
ластями и миторибосомными субъединица-
млекопитающих, хотя механизм его действия
ми [47, 48], способствуя выбору правильного
остается неясным. В случае бицистронной
стартового кодона. Данные криоэлектронной
мРНК Atp8-Atp6, mtIF3 может участвовать в
микроскопии указывают на то, что область
«readthrough» инициации, подобно бактери-
рядом с туннелем выхода пептида на митори-
альному IF3. В подтверждение этому предпо-
босоме дрожжей может служить некой общей
ложению недавно проведенный анализ рас-
платформой для различных активаторов [49].
пределения рибосом на митохондриальных
Большая часть этих трансляционных актива-
мРНК в клетках линии HEK293, нокаутной по
торов относится к семейству пентатрикопеп-
гену mtIF3, выявил изменение загрузки мРНК
тидных (PPR) белков, которые характеризуют-
миторибосомами на бицистронной матрице
ся РНК-связывающей способностью.
Atp8-Atp6: снижение количества рибосом на
Все закодированные в митохондриаль-
участке, соответствующем области кодиро-
ном геноме Sac. cerevisiae белки, за исключе-
вания белка Atp6, и увеличение - на участке
нием Var1, являются коровыми компонентами
кодирования белка Atp8 [33].
комплексов цепи окислительного фосфорили-
Таким образом, можно заключить, что
рования, необходимой для обеспечения энер-
митохондрии унаследовали от своего бакте-
гетических потребностей клетки [58]. Помимо
риального предшественника набор факто-
митохондриально закодированных белков, в
ров инициации трансляции. Они сохранили
состав комплексов цепи окислительного фос-
большинство своих изначальных «бактери-
форилирования входят продукты цитоплаз-
альных» функций, что подтверждается дан-
матической трансляции, поэтому сборка этих
ными различных исследований, проведенных
комплексов требует очень тонкой настройки,
преимущественно на гетерологичных систе-
с одной стороны, но и достаточной пластично-
мах. Тем не менее эти факторы могли приоб-
сти - с другой, чтобы обеспечить адаптацию к
рести дополнительные функции, связанные с
быстро меняющимся энергетическим потреб-
ходом эволюции мРНК, митохондриального
ностям клетки. Для этого некоторые трансля-
генетического кода и миторибосом.
ционные активаторы создают петли обратной
БИОХИМИЯ том 88 вып. 11 2023
13*
2228
БАЛЕВА и др.
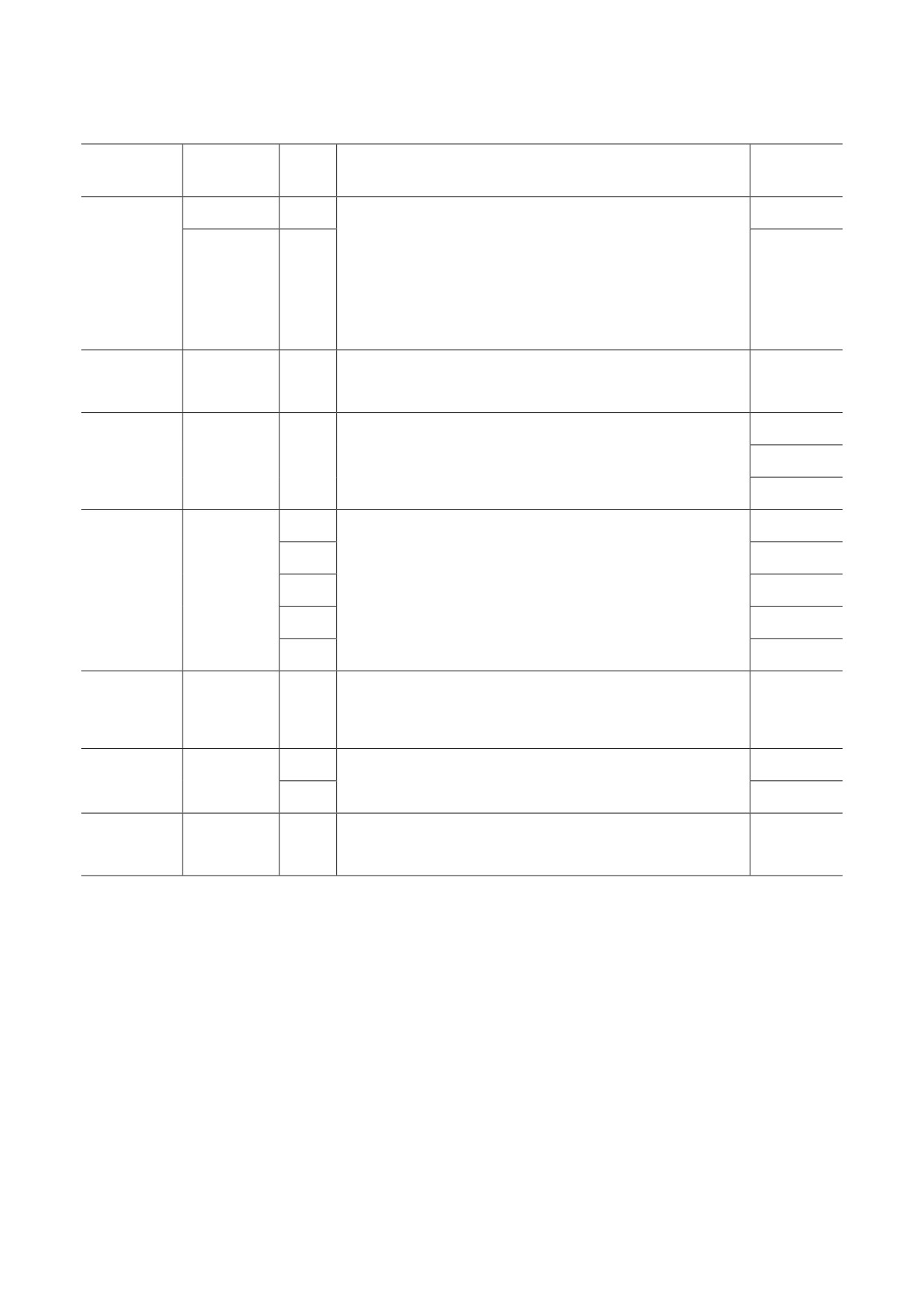
Трансляционные активаторы в митохондриях Saccharomyces cerevisiae
Регулируемая
Гомолог
Активатор
PPR
Механизм действия
мРНК
Homo sapiens
Pet309
PPR+
Pet309 связывает 5′-НТО мРНК Cox1, способствуя
LRPPRC
синтезу полноразмерного белка Сox1 [50];
делеция гена Pet309 приводит к прекращению синтеза
белка Сox1;
Cox1
правильное связывание рибосомы на мРНК регулирует
Mss51
PPR-
так же белок Mss51;
Zmynd17
делеция гена Mss51 приводит к изменению характера
взаимодействия Pet309 c мРНК и синтезу нового
белка (15 кДа) [51]
связывает мРНК Cox2 в двух сайтах (ближе к 5′-концу
Cox2
Pet111
PPR+
и недалеко от стартового кодона), предотвращая образование
-
вторичных структур, ингибирующих трансляцию [52]
-
Pet54 непосредственно связывается с 5′-НТО мРНК Сох3,
Pet54
PPR-
способствуя формированию «активационного» комплекса
Cox3
Pet122
PPR-
-
Pet122-Pet54-Pet494 для эффективного синтеза
Pet494
PPR-
белка Cox3 [53, 54]
-
PPR-
-
Cbs1 связывается с 5′-НТО мРНК Cytb, способствуя
Cbs1
PPR-
дальнейшему ее связыванию с большой субъединицей
–
Cbs2
рибосомы в присутствии Сbs2 и Cbp1;
Cytb
Cbp1
PPR+
при этом Cbs1 оказывает ингибирующее действие,
–
Cbp3
препятствуя началу трансляции;
Cbp6
PPR-
блок трансляции снимается тогда, когда Cbs1 вытесняется
UQCC1
из комплекса мРНК-рибосома белками Cbp3-Cbp6[55]
PPR-
UQCC2
хотя Atp6 и Atp8 находятся в составе бицистронного
транскрипта, делеция гена, кодирующего Atp22,
Atp6/8
Atp22
PPR+
-
влияет на синтез только белка Atp6 [56];
механизм влияния Atp22 на трансляцию мРНК Atp6 не ясен
PPR+
-
Aep1/Nca1
Atp9
механизм действия факторов неясен [56]
Aep2/Atp13
PPR+
-
Sov1 связывает мРНК Var1 благодаря наличию PPR-доменов,
Var1
Sov1
PPR+
обеспечивая ее эффективную трансляцию;
-
механизм действия неясен [57]
связи, которые координируют
синтез мито-
участвует в сборке комплекса коэнзим Q-ци-
хондриальных полипептидов и сборку функ-
тохром c редуктаза [55]. Подобным образом
ционально активных комплексов дыхательной
регулируется и синтез субъединицы цито-
цепи. Так, например, синтез апоцитохрома b
хром c-оксидазы Cox1 в пекарских дрожжах.
зависит сразу от пяти активаторов: Cbs1, Cbs2,
Так, трансляционный активатор Pet309 свя-
Cbp1, Cbp3 и Cbp6. При этом Cbs1, Cbs2 и Cbp1
зывает 5′-НТО мРНК Cox1 в присутствии бел-
связывают 5′-НТО мРНК Cytb и рекрутируют ее
ка Mss51. Далее, Mss51 в комплексе с другими
к большой субъединице миторибосомы, связы-
факторами связывает новосинтезированный
ваясь с выходным туннелем. Далее Cbs1, свя-
белок и участвует в сборке цитохром c-окси-
занный с 5′-НТО мРНК Cytb, вытесняется ком-
дазы [59]. При нарушениях сборки происходит
плексом Cbp3-Cbp6. Таким образом, 5′-НТО
накопление незрелых интермедиатов, ассо-
мРНК становится способной связаться с малой
циированных с Mss51, в результате чего умень-
субъединицей миторибосомы для инициации
шается пул свободного Mss51, что приводит,
трансляции. Новосинтезированный белок свя-
в свою очередь, к снижению эффективности
зывается с комплексом Cbp3-Cbp6, который
инициации трансляции мРНК Cox1 [60].
БИОХИМИЯ том 88 вып. 11 2023
ЭВОЛЮЦИЯ ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
2229
У млекопитающих митохондриальные
Подобно дрожжевым, мРНК растений
мРНК безлидерные: почти все они содержат
имеют выраженные 5′-НТО. Около полови-
стартовый кодон непосредственно на 5′-конце.
ны растительных мРНК имеет A-богатую по-
Согласно данным криоэлектронной микро-
следовательность (АхААА), расположенную
скопии, в связывании этих мРНК участвует
на
19 нуклеотидов выше стартового AUG.
белок малой рибосомной субъединицы mS39,
В узнавании данной последовательности мо-
расположенный у входа в туннель для мРНК.
жет участвовать миторибосомный белок mS83,
Своим пентатрикопептидным доменом mS39
относящийся к семейству PPR [12]. Тем не ме-
связывает мРНК в U-богатом участке в непо-
нее наличие ряда митохондриальных мРНК
средственной близости от седьмого кодо-
без последовательности АхААА предполагает
на мРНК. Подобный участок достаточно кон-
существование альтернативных механизмов
сервативен у большинства из 11 мРНК млеко-
рекрутирования мРНК в митохондриях расте-
питающих [30]. Кроме того, для эффективного
ний. Так, в состав митохондриальных рибо-
связывания мРНК митохондриальная рибо-
сом растений входят многочисленные PPR-
сома млекопитающих взаимодействует с ком-
белки, при том что у дрожжей нет ни одного
плексом белков LRPPRC-SLIRP. Этот комп-
миторибосомного белка, принадлежащего се-
лекс связывается с миторибосомным бел-
мейству PPR, а у млекопитающих их всего
ком mS39, обеспечивая рекрутирование мРНК
два - mS39 и mS27. Большинство митори-
и регулируя скорость ее трансляции. Таким
босомных PPR-белков растений выполняют
образом, комплекс LRPPRC-SLIRP может яв-
только структурную роль, за исключением
ляться универсальным активатором трансля-
рибосомного белка PPR1, делеция по гену ко-
ции в митохондриях млекопитающих [61, 62].
торого существенно влияет на трансляцию
Также более тонкую регуляцию трансляции
всех митохондриальных мРНК [66]. Тем не
у млекопитающих, как и у дрожжей, обес-
менее не исключено, что какие-то PPR-белки,
печивают специфические белки-активаторы.
входящие в состав миторибосомы, могут вы-
Первым найденным белком с такой функци-
полнять роль трансляционных активаторов,
ей стал TACO1. Мутации в гене этого белка,
подобно активаторам дрожжей и млекопита-
обнаруженные у некоторых пациентов, свя-
ющих. Вероятными кандидатами для роли
заны с развитием синдрома Лея и наруше-
трансляционных активаторов могут служить
нием функции цитохром c-оксидазного ком-
белки из семейства Rf-PPR, в частности, не-
плекса. Последнее связано со специфичным
давно описанный RFL8. Этот белок специфи-
влиянием TACO1 на синтез митохондриально
чески активирует трансляцию мРНК ccmFN2,
кодируемого белка Cox1 [63], корового ком-
кодирующую одну из цепей гем-лиазного ком-
понента цитохром c-оксидазы. Было пока-
плекса [67].
зано, что TACO1 имеет несколько участков
связывания в 5′-области мРНК Cox1, а также
имеет сродство к митохондриальной рибо-
СПЕЦИАЛИЗАЦИЯ ДЛЯ СИНТЕЗА
соме, преимущественно связываясь с малой
МЕМБРАННЫХ БЕЛКОВ
субъединицей, но в меньшей степени взаимо-
действуя и с ассоциированной миторибосо-
Гены, которые практически всегда при-
мой [64]. Таким образом, TACO1 может спо-
сутствуют в митохондриальной ДНК, кодиру-
собствовать рекрутированию мРНК Cox1 к
ют основные компоненты дыхательной цепи:
рибосоме, регулируя инициацию трансляции,
субъединицы ND1, ND2, ND3, ND4, ND4L,
а также может оказывать влияние и на стадию
ND5 и ND6 NADH-дегидрогеназы; апоцито-
элонгации.
хром b - коэнзим Q-цитохром c редуктазы;
Еще одним белком - активатором транс-
Cox1, Cox2 и Cox3 - цитохром c-оксидазы, а
ляции в митохондриях млекопитающих, яв-
также субъединицы Atp6 и Atp9 ATP-синта-
ляется PTCD2, для которого было показано,
зы. Тем не менее бывают исключения. Так, у
что он способен специфически регулировать
дрожжей произошла полная потеря комплекса
синтез субъединицы Cox3 цитохром с-окси-
NADH-дегидрогеназы и, следовательно, соот-
дазного комплекса [65]. Было показано, что
ветствующих митохондриальных генов [68].
PTCD2 ассоциирован с моносомой, что может
Митохондриально кодируемые субъеди-
указывать на то, что его механизм регуляции
ницы дыхательной цепи являются крайне
также основан на привлечении мРНК Cox3
гидрофобными белками, синтез которых тре-
к митохондриальной рибосоме. Активаторы
бует сопряжения со встройкой растущего по-
других мРНК в митохондриях млекопитаю-
липептида во внутреннюю митохондриальную
щих к настоящему времени не выявлены.
мембрану [69]. Эволюция митохондриального
БИОХИМИЯ том 88 вып. 11 2023
2230
БАЛЕВА и др.
генома шла по пути увеличения процента генов
Эволюция процессов регуляции привела
гидрофобных белков в его составе, что привело
к возникновению факторов, которые влияют
к соответствующей специализации миторибо-
на синтез конкретной мРНК. Наличие подоб-
сом. Ряд существенных изменений претерпел
ных факторов регуляции, располагающихся
туннель выхода растущего полипептида [70].
на периферии миторибосом, позволяет пред-
У миторибосом млекопитающих он выстлан
положить существование отдельных субпо-
белками с более гидрофобными, в сравнении с
пуляций миторибосом, специализированных
бактериальными рибосомами, аминокислотами
для бисинтеза конкретных митохондриально
в составе для создания условий корректного
кодируемых белков или их групп. Явление
фолдинга. Туннель большой субъединицы ми-
специализации известно для цитоплазмати-
торибосом пекарских дрожжей характеризуется
ческих рибосом [72, 73], хотя в этом случае оно
наличием двух уникальных адаптаций. Во-пер-
достигается либо внесением модификаций
вых, вход в туннель сужается из-за образования
в рРНК или рибосомные белки, либо исполь-
дополнительной пары оснований в 21S рРНК,
зованием различных паралогов рибосомных
а во-вторых, имеется митохондриально-специ-
белков.
фическое расширение белка uL23m, приводя-
Факторы регуляции трансляции митохон-
щее к изгибу выходного туннеля. Миторибо-
дриальных мРНК не только формируют петли
сомы связаны с внутренней мембраной мито-
обратной связи, но и участвуют в рекрутиро-
хондрий. У млекопитающих мембранным «яко-
вании мРНК к рибосоме, а также определяют
рем» выступает белок mL45 [30], расположен-
выбор стартового кодона. Возможно, расши-
ный в области выхода растущего пептида из
рение функций факторов регуляции привело
туннеля на большой субъединице рибосомы.
и к изменению роли факторов инициации
У дрожжей прикрепление миторибосом к мем-
трансляции: их универсальные функции ста-
бране осуществляет белок Mba1 и 96-й сегмент
ли менее востребованы.
рРНК большой субъединицы [71].
Тем не менее подобные предположения
можно сделать лишь для некоторых хорошо
изученных объектов, таких как дрожжи или
ЗАКЛЮЧЕНИЕ
млекопитающие. В то же время для большин-
ства организмов устройство аппарата митохон-
Все процессы в митохондриях зависят от
дриальной трансляции остается загадкой.
белков, которые кодируются ядерным геномом.
Кроме этого, процесс трансляции в митохон-
Вклад авторов. М.В. Балева, У.Е. Пиу-
дриях связан со сборкой и функционировани-
нова
- анализ литературы; М.В. Балева,
ем цепи окислительного фосфорилирования.
И.В. Чичерин - написание текста; С.А. Ле-
Резонно предполагать, что процессы митохон-
вицкий, П.А. Каменский - редактирование
дриальной трансляции должны были адапти-
текста статьи.
роваться к эволюционным изменениям как
Финансирование. Работа выполнена при
митохондриального, так и ядерного геномов, а
финансовой поддержке Российского научного
также эволюции дыхания [11]. Подобная адап-
фонда (грант № 21-14-00008).
тация привела к формированию особых мито-
Конфликт интересов. Авторы заявляют об
хондриальных рибосом, специализированных
отсутствии конфликта интересов.
для синтеза гидрофобных белков, а также воз-
Соблюдение этических норм. Настоящая
никновению особых процессов регуляции для
статья не содержит описания каких-либо ис-
обеспечения адаптации синтеза белка к мета-
следований с участием людей или животных
болическому статусу клетки.
в качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1. Andersson, S. G. E., Zomorodipour, A., Andersson,
2. Read, A. D., Bentley, R. ET., Archer, S. L., Dunham-
J. O., Sicheritz-Pontén, T., Alsmark, U. C. M.,
Snary, K. J. (2021) Mitochondrial iron-sulfur clusters:
Podowski, R. M., Näslund, A. K., Eriksson,
Structure, function, and an emerging role in vascular
A. S., Winkler, H. H., and Kurland, C. G. (1998)
biology, Redox Biol.,
47,
102164, doi:
10.1016/
The genome sequence of Rickettsia prowazekii and
j.redox.2021.102164.
the origin of mitochondria, Nature, 396, 133-140,
3. Kastaniotis, A. J., Autio, K. J., Kerätär, J. M.,
doi: 10.1038/24094.
Monteuuis, G., Mäkelä, A. M., Nair, R. R.,
БИОХИМИЯ том 88 вып. 11 2023
ЭВОЛЮЦИЯ ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
2231
Pietikäinen, L. P., Shvetsova, A., Chen, Z., and
falciparum, PLoS One, 7, e38320, doi: 10.1371/journal.
Hiltunen, J. K.
(2017) Mitochondrial fatty acid
pone.0038320.
synthesis, fatty acids and mitochondrial physiology,
15.
Chrzanowska-Lightowlers, Z., Rorbach, J., and
Biochim. Biophys. Acta Mol. Cell Biol. Lipids, 1862,
Minczuk, M. (2017) Human mitochondrial ribosomes
39-48, doi: 10.1016/j.bbalip.2016.08.011.
can switch structural tRNAs - but when and why?
4.
De Vitto, H., Arachchige, D. B., Richardson, B. C.,
RNA Biol., 14, 1668-1671, doi: 10.1080/15476286.
and French, J. B. (2021) The intersection of purine
2017.1356551.
and mitochondrial metabolism in cancer, Cells, 10,
16.
Amunts, A., Brown, A., Bai, X., Llácer, J. L.,
2603, doi: 10.3390/cells10102603.
Hussain, T., Emsley, P., Long, F., Murshudov, G.,
5.
Sloan, D. B., Warren, J. M., Williams, A. M., Wu, Z.,
Scheres, S. H. W., and Ramakrishnan, V.
(2014)
Abdel-Ghany, S. E., Nair, R. R., Pietikäinen, L. P.,
Structure of the yeast mitochondrial large ribosomal
Shvetsova, A., Chen, Z., and Hiltunen, J. K. (2018)
subunit, Science,
343,
1485-1489, doi:
10.1126/
Cytonuclear integration and co-evolution, Nat. Rev.
science.1249410.
Genet., 19, 635-648, doi: 10.1038/s41576-018-0035-9.
17.
Smits, P., Smeitink, J. A. M., van den Heuvel, L. P.,
6.
Boore, J. L. (1999) Animal mitochondrial genomes,
Huynen, M. A., and Ettema, T. J. G. (2007) Recon-
Nucleic Acids Res.,
27,
1767-1780, doi:
10.1093/
structing the evolution of the mitochondrial ribo-
nar/27.8.1767.
somal proteome, Nucleic Acids Res., 35, 4686-4703,
7.
Gualberto, J. M., Mileshina, D., Wallet, C., Niazi, A.
doi: 10.1093/nar/gkm441.
K., Weber-Lotfi, F., and Dietrich, A. (2014) The plant
18.
Scaltsoyiannes, V., Corre, N., Waltz, F., and Giegé, P.
mitochondrial genome: Dynamics and mainte-
(2022) Types and functions of mitoribosome-specific
nance, Biochimie, 100, 107-120, doi: 10.1016/j.biochi.
ribosomal proteins across eukaryotes, Int. J. Mol. Sci.,
2013.09.016.
23, 3474, doi: 10.3390/ijms23073474.
8.
Callejas-Hernández, F., Herreros-Cabello, A., del
19.
Koc, E. C., Ranasinghe, A., Burkhart, W., Black-
Moral-Salmoral, J., Fresno, M., and Gironès, N.
burn, K., Koc, H., Moseley, A., and Spremulli, L. L.
(2021) The complete mitochondrial DNA of
(2001) A new face on apoptosis: death-associated
Trypanosoma cruzi: maxicircles and minicircles, Front.
protein 3 and PDCD9 are mitochondrial ribosomal
Cell. Infect. Microbiol., 11, 672448, doi: 10.3389/
proteins, FEBS Lett., 492, 166-170, doi: 10.1016/
fcimb.2021.672448.
S0014-5793(01)02250-5.
9.
Petrov, A. S., Wood, E. C., Bernier, C. R., Norris,
20.
Hussain, T., Llácer, J. L., Wimberly, B. T., Kieft, J. S.,
A. M., Brown, A., and Amunts, A. (2019) Structural
and Ramakrishnan, V. (2016) Large-scale movements
patching fosters divergence of mitochondrial
of IF3 and tRNA during bacterial translation initiation,
ribosomes, Mol. Biol. Evol., 36, 207-2019, doi: 10.1093/
Cell, 167, 133-144.e13, doi: 10.1016/j.cell.2016.08.074.
molbev/msy221.
21.
Laursen, B. S., Sørensen, H. P., Mortensen, K. K.,
10.
Gray, M. W. (2015) Mosaic nature of the mitochon-
and Sperling-Petersen, H. U. (2005) Initiation of
drial proteome: implications for the origin and evolu-
protein synthesis in bacteria, Microbiol. Mol. Biol. Rev.,
tion of mitochondria, Proc. Natl. Acad. Sci. USA, 112,
69, 101-123, doi: 10.1128/mmbr.69.1.101-123.2005.
10133-10138, doi: 10.1073/pnas.1421379112.
22.
Yamamoto, H., Wittek, D., Gupta, R., Qin, B.,
11.
Van Der Sluis, E. O., Bauerschmitt, H., Becker, T.,
Ueda, T., Krause, R., Yamamoto, K., Albrecht, R.,
Mielke, T., Frauenfeld, J., Berninghausen, O.,
Pech, M., and Nierhaus, K. H. (2016) 70S-scanning
Neupert, W., Herrmann, J. M., and Beckmann, R.
initiation is a novel and frequent initiation mode
(2015) Parallel structural evolution of mitochondrial
of ribosomal translation in bacteria, Proc. Natl.
ribosomes and OXPHOS complexes, Genome Biol.
Acad. Sci. USA, 113, E1180-E1189, doi: 10.1073/
Evol., 7, 1235-1251, doi: 10.1093/gbe/evv061.
pnas.1524554113.
12.
Waltz, F., Soufari, H., Bochler, A., Giegé, P.,
23.
Zheng, X., Hu, G.-Q., She, Z.-S., and Zhu, H. (2011)
and Hashem, Y. (2020) Cryo-EM structure of the
Leaderless genes in bacteria: clue to the evolution of
RNA-rich plant mitochondrial ribosome, Nat. Plants,
translation initiation mechanisms in prokaryotes, BMC
6, 377-383, doi: 10.1038/s41477-020-0631-5.
Genomics, 12, 361, doi: 10.1186/1471-2164-12-361.
13.
Waltz, F., Salinas-Giegé, T., Englmeier, R.,
24.
Leiva, L. E., and Katz, A. (2022) Regulation of Lead-
Meichel, H., Soufari, H., Kuhn, L., Pfeffer, S.,
erless mRNA Translation in Bacteria, Microorganisms,
Förster, F., Engel, B. D., Giegé, P., Drouard, L., and
10, 723, doi: 10.3390/microorganisms10040723.
Hashem, Y. (2021) How to build a ribosome from RNA
25.
Temperley, R. J., Wydro, M., Lightowlers, R. N.,
fragments in Chlamydomonas mitochondria, Nat. Com-
and Chrzanowska-Lightowlers, Z. M. (2010) Human
mun., 12, 7176, doi: 10.1038/s41467-021-27200-z.
mitochondrial mRNAs - like members of all families,
14.
Feagin, J. E., Harrell, M. I., Lee, J. C., Coe, K. J.,
similar but different, Biochim. Biophys. Acta, 1797,
Sands, B. H., Cannone, J. J., Tami, G., Schnare,
1081-1085, doi: 10.1016/j.bbabio.2010.02.036.
M. N., and Gutell, R. R. (2012) The fragmented
26.
Kazama, T., Yagi, Y., Toriyama, K., and Nakamura, T.
mitochondrial ribosomal RNAs of Plasmodium
(2013) Heterogeneity of the 5′-end in plant mRNA
БИОХИМИЯ том 88 вып. 11 2023
2232
БАЛЕВА и др.
may be involved in mitochondrial translation, Front.
formation with natural mRNAs, J. Biol. Chem., 277,
Plant Sci., 4, 517, doi: 10.3389/fpls.2013.00517.
35541-35549, doi: 10.1074/jbc.M202498200.
27.
Soto, I., Couvillion, M., Hansen, K. G., McShane, E.,
37.
Ayyub, S. A., Dobriyal, D., and Varshney, U. (2017)
Moran, J. C., Barrientos, A., and Churchman, L. S.
Contributions of the N-and C-terminal domains
(2022) Balanced mitochondrial and cytosolic trans-
of initiation factor 3 to its functions in the fidelity
latomes underlie the biogenesis of human respirato-
of initiation and antiassociation of the ribosomal
ry complexes, Genome Biol., 23, 170, doi: 10.1186/
subunits, J. Bacteriol., 199, e00051-17, doi: 10.1128/
s13059-022-02732-9.
JB.00051-17.
28.
Marzi, S., Knight, W., Brandi, L., Caserta, E.,
38.
Koripella, R. K., Sharma, M. R., Haque, M. E.,
Soboleva, N., Hill, W. E., Gualerzi, C. O., and
Risteff, P., Spremulli, L. L., and Agrawal, R. K.
Lodmell, J. S.
(2003) Ribosomal localization of
(2019) Structure of human mitochondrial translation
translation initiation factor IF2, RNA, 9, 958-969,
initiation factor 3 bound to the small ribosomal subunit,
doi: 10.1261/rna.2116303.
iScience, 12, 76-86, doi: 10.1016/j.isci.2018.12.030.
29.
Spencer, A. C., and Spremulli, L. L. (2005) The inter-
39.
Haque, M. E., Grasso, D., and Spremulli, L. L. (2008)
action of mitochondrial translational initiation factor 2
The interaction of mammalian mitochondrial trans-
with the small ribosomal subunit, Biochim. Biophys.
lational initiation factor 3 with ribosomes: Evolution
Acta, 1750, 69-81, doi: 10.1016/j.bbapap.2005.03.009.
of terminal extensions in IF3mt, Nucleic Acids Res.,
30.
Kummer, E., Leibundgut, M., Rackham, O., Lee,
36, 589-597, doi: 10.1093/nar/gkm1072.
R. G., Boehringer, D., Filipovska, A., and Ban, N.
40.
Derbikova, K., Kuzmenko, A., Levitskii, S.,
(2018) Unique features of mammalian mitochondrial
Klimontova, M., Chicherin, I., Baleva, M., Krashenin-
translation initiation revealed by cryo-EM, Nature,
nikov, I., and Kamenski, P. (2018) Biological and
560, 263-267, doi: 10.1038/s41586-018-0373-y.
evolutionary significance of terminal extensions of
31.
Gaur, R., Grasso, D., Datta, P. P., Krishna, P. D. V.,
mitochondrial translation initiation factor 3, IJMS,
Das, G., Spencer, A., Agrawal, R. K., Spremulli, L.,
19, 3861, doi: 10.3390/ijms19123861.
and Varshney, U. (2008) A single mammalian mi-
41.
Springer, M., Graffe, M., and Grunberg-Manago, M.
tochondrial translation initiation factor functionally
(1977) Characterization of an E. coli mutant with a
replaces two bacterial factors, Mol. Cell, 29, 180-190,
thermolabile initiation factor IF3 activity, Mol. Gen.
doi: 10.1016/j.molcel.2007.11.021.
Genet., 151, 17-26, doi: 10.1007/BF00446908.
32.
Yassin, A. S., Haque, Md. E., Datta, P. P., Elmore, K.,
42.
Kuzmenko, A., Derbikova, K., Salvatori, R.,
Banavali, N. K., Spremulli, L. L., and Agrawal, R. K.
Tankov, S., Atkinson, G. C., Tenson, T., Ott, M.,
(2011) Insertion domain within mammalian mito-
Kamenski, P., and Hauryliuk, V. (2016) Aim-less
chondrial translation initiation factor 2 serves the role
translation: Loss of Saccharomyces cerevisiae mito-
of eubacterial initiation factor 1, Proc. Natl. Acad. Sci.
chondrial translation initiation factor mIF3/Aim23
USA, 108, 3918-3923, doi: 10.1073/pnas.1017425108.
leads to unbalanced protein synthesis, Sci. Rep.,
33.
Remes, C., Khawaja, A., Pearce, S. F., Dinan, A. M.,
6, 18749, doi: 10.1038/srep18749.
Gopalakrishna, S., Cipullo, M., Kyriakidis, V.,
43.
Chicherin, I., Levitskii, S., Baleva, M. V., Krashenin-
Zhang, J., Dopico, X. C., Yukhnovets, O., Atanas-
nikov, I. A., Patrushev, M. V., and Kamenski, P. (2020)
sov, I., Firth, A. E., Cooperman, B., and Rorbach, J.
Yeast mitochondrial translation initiation factor
3
(2023) Translation initiation of leaderless and poly-
interacts with pet111p to promote COX2 mRNA
cistronic transcripts in mammalian mitochon-
translation, Int. J. Mol. Sci., 21, 3414, doi: 10.3390/
dria, Nucleic Acids Res., 51, 891-907, doi: 10.1093/
ijms21103414.
nar/gkac1233.
44.
Chicherin, I. V., Baleva, M. V., Levitskii, S. A.,
34.
Luo, Y., Su, R., Wang, Y., Xie, W., Liu, Z., and
Dashinimaev, E. B., Krasheninnikov, I. A., and
Huang, Y. (2019) Schizosaccharomyces pombe Mti2
Kamenski, P. (2020) Initiation factor 3 is dispensable
and Mti3 act in conjunction during mitochondrial
for mitochondrial translation in cultured human cells,
translation initiation, FEBS J.,
286,
4542-4553,
Sci. Rep., 10, 7110, doi: 10.1038/s41598-020-64139-5.
doi: 10.1111/febs.15021.
45.
Rudler, D. L., Hughes, L. A., Perks, K. L., Richman,
35.
Ostojić, J., Panozzo, C., Bourand-Plantefol, A.,
T. R., Kuznetsova, I., Ermer, J. A., Abudulai, L. N.,
Herbert, C. J., Dujardin, G., and Bonnefoy, N. (2016)
Shearwood, A. M. J., Viola, H. M., Hool, L. C., Siira,
Ribosome recycling defects modify the balance be-
S. J., Rackham, O., and Filipovska, A. (2019) Fidelity
tween the synthesis and assembly of specific subunits
of translation initiation is required for coordinated
of the oxidative phosphorylation complexes in yeast
respiratory complex assembly, Sci. Adv., 5, eaay2118,
mitochondria, Nucleic Acids Res.,
44,
5785-5797,
doi: 10.1126/sciadv.aay2118.
doi: 10.1093/nar/gkw490.
46.
Gu, Y., Mao, Y., Jia, L., Dong, L., and Qian, S.-B.
36.
Koc, E. C., and Spremulli, L. L. (2002) Identification
(2021) Bi-directional ribosome scanning controls the
of mammalian mitochondrial translational initiation
stringency of start codon selection, Nat. Commun.,
factor 3 and examination of its role in initiation complex
12, 6604, doi: 10.1038/s41467-021-26923-3.
БИОХИМИЯ том 88 вып. 11 2023
ЭВОЛЮЦИЯ ТРАНСЛЯЦИОННЫХ АППАРАТОВ МИТОХОНДРИЙ
2233
47.
Herbert, C. J., Labarre-Mariotte, S., Cornu, D.,
mitoribosome biogenesis, Nucleic Acids Res., 48, 6759-
Sophie, C., Panozzo, C., Michel, T., Dujardin, G.,
6774, doi: 10.1093/nar/gkaa424.
and Bonnefoy, N. (2021) Translational activators and
58.
Tang, J. X., Thompson, K., Taylor, R. W., and
mitoribosomal isoforms cooperate to mediate mRNA-
Oláhová, M. (2020) Mitochondrial OXPHOS bio-
specific translation in Schizosaccharomyces pombe
genesis: co-regulation of protein synthesis, import,
mitochondria, Nucleic Acids Res., 49, 11145-11166,
and assembly pathways, Int. J. Mol. Sci., 21, 3820,
doi: 10.1093/nar/gkab789.
doi: 10.3390/ijms21113820.
48.
Haastrup, M. O., Vikramdeo, K. S., Singh, S.,
59.
Fontanesi, F., Clemente, P., and Barrientos, A. (2011)
Singh, A. P., and Dasgupta, S. (2023) The journey
Cox25 teams up with Mss51, Ssc1, and Cox14 to reg-
of mitochondrial protein import and the roadmap
ulate mitochondrial cytochrome c oxidase subunit 1
to follow, Int. J. Mol. Sci., 24, 2479, doi: 10.3390/
expression and Assembly in Saccharomyces cerevi-
ijms24032479.
siae, J. Biol. Chem., 286a, 555-566, doi: 10.1074/
49.
Desai, N., Brown, A., Amunts, A., and Ramakrish-
jbc.M110.188805.
nan, V. (2017) The structure of the yeast mitochondrial
60.
Barrientos, A., Zambrano, A., and Tzagoloff, A.
ribosome, Science, 355, 528-531, doi: 10.1126/science.
(2004) Mss51p and Cox14p jointly regulate mito-
aal2415.
chondrial Cox1p expression in Saccharomyces cer-
50.
Zamudio-Ochoa, A., Camacho-Villasana, Y., García-
evisiae, EMBO J.,
23,
3472-3482, doi:
10.1038/
Guerrero, A. E., and Pérez-Martínez, X.
(2014)
sj.emboj.7600358.
The Pet309 pentatricopeptide repeat motifs mediate
61.
Chujo, T., Ohira, T., Sakaguchi, Y., Goshima, N.,
efficient binding to the mitochondrial COX1 transcript
Nomura, N., Nagao, A., and Suzuki, T.
(2012)
in yeast, RNA Biol.,
11,
953-967, doi:
10.4161/
LRPPRC/SLIRP suppresses PNPase-mediated
rna.29780.
mRNA decay and promotes polyadenylation in human
51.
Zambrano, A., Fontanesi, F., Solans, A., de Oliveira,
mitochondria, Nucleic Acids Res., 40, 8033-8047,
R. L., Fox, T. D., Tzagoloff, A., and Barrientos, A.
doi: 10.1093/nar/gks506.
(2007) Aberrant translation of cytochrome c oxidase
62.
Lagouge, M., Mourier, A., Lee, H. J., Spåhr, H.,
subunit 1 mRNA species in the absence of Mss51p
Wai, T., Kukat, C., Ramos, E. C., Motori, E., Busch,
in the yeast Saccharomyces cerevisiae, Mol. Biol. Cell,
J. D., Siira, S., German Mouse Clinic Consortium,
18, 523-535, doi: 10.1091/mbc.e06-09-0803.
Kremmer, E., Filipovska, A., and Larsson, N.-G.
52.
Jones, J. L., Hofmann, K. B., Cowan, A. T.,
(2015) SLIRP regulates the rate of mitochondrial
Temiakov, D., Cramer, P., and Anikin, M. (2019)
protein synthesis and protects LRPPRC from
Yeast mitochondrial protein Pet111p binds directly
degradation, PLoS Genet., 11, e1005423, doi: 10.1371/
to two distinct targets in COX2 mRNA, suggesting a
journal.pgen.1005423.
mechanism of translational activation, J. Biol. Chem.,
63.
Weraarpachai, W., Antonicka, H., Sasarman, F.,
294, 7528-7536, doi: 10.1074/jbc.RA118.005355.
Seeger, J., Schrank, B., Kolesar, J. E., Lochmüller, H.,
53.
Brown, N. G., Costanzo, M. C., and Fox, T. D. (1994)
Chevrette, M., Kaufman, B. A., Horvath, R., and
Interactions among three proteins that specifically ac-
Shoubridge, E. A. (2009) Mutation in TACO1, encod-
tivate translation of the mitochondrial COX3 mRNA
ing a translational activator of COX I, results in cyto-
in Saccharomyces cerevisiae, Mol. Cell. Biol.,
14,
chrome c oxidase deficiency and late-onset Leigh syn-
1045-1053, doi: 10.1128/MCB.14.2.1045.
drome, Nat. Genet., 41, 833-837, doi: 10.1038/ng.390.
54.
Kaspar, B. J., Bifano, A. L., and Caprara, M. G.
64.
Richman, T. R., Spåhr, H., Ermer, J. A., Davies,
(2008) A shared RNA-binding site in the Pet54 protein
S. M. K., Viola, H. M., Bates, K. A., Papadimitriou, J.,
is required for translational activation and group I in-
Hool, L. C., Rodger, J., Larsson, N.-G., Rackham, O.,
tron splicing in yeast mitochondria, Nucleic Acids Res.,
and Filipovska, A. (2016) Loss of the RNA-binding
36, 2958-2968, doi: 10.1093/nar/gkn045.
protein TACO1 causes late-onset mitochondrial
55.
Salvatori, R., Kehrein, K., Singh, A. P., Aftab, W.,
dysfunction in mice, Nat. Commun.,
7,
11884,
Möller-Hergt, B. V., Forne, I., Imhof, A., and
doi: 10.1038/ncomms11884.
Ott, M. (2020) Molecular wiring of a mitochondrial
65.
Baleva, M. V., Chicherin, I., Piunova, U., Zgoda, V.,
translational feedback loop, Mol. Cell, 77, 887-900.e5,
Patrushev, M. V., Levitskii, S., and Kamenski, P.
doi: 10.1016/j.molcel.2019.11.019.
(2022) Pentatricopeptide protein PTCD2 Regulates
56.
Zeng, X., Hourset, A., and Tzagoloff, A.
(2007)
COIII translation in mitochondria of the HeLa
The Saccharomyces cerevisiae ATP22 gene codes for
cell line, Int. J. Mol. Sci., 23, 14241, doi: 10.3390/
the mitochondrial ATPase subunit 6-specific trans-
ijms232214241.
lation factor, Genetics, 175, 55-63, doi: 10.1534/
66.
Waltz, F., Nguyen, T.-T., Arrivé, M., Bochler, A.,
genetics.106.065821.
Chicher, J., Hammann, P., Kuhn, L., Quadrado, M.,
57.
Seshadri, S. R., Banarjee, C., Barros, M. H., and
Mireau, H., Hashem, Y., and Giegé, P. (2019) Small
Fontanesi, F. (2020) The translational activator Sov1
is big in Arabidopsis mitochondrial ribosome, Nat.
coordinates mitochondrial gene expression with
Plants, 5, 106-117, doi: 10.1038/s41477-018-0339-y.
БИОХИМИЯ том 88 вып. 11 2023
2234
БАЛЕВА и др.
67. Nguyen, T.-T., Planchard, N., Dahan, J., Arnal, N.,
proteins, Biochim. Biophys. Acta,
1803,
767-775,
Balzergue, S., Benamar, A., Bertin, P., Brunaud, V.,
doi: 10.1016/j.bbamcr.2009.11.010.
Dargel-Graffin, C., Macherel, D., Martin-Magniette,
70. Bieri, P., Greber, B. J., and Ban, N. (2018) High-
M.-L., Quadrado, M., Namy, O., and Mireau, H.
resolution structures of mitochondrial ribosomes and
(2021) A case of gene fragmentation in plant
their functional implications, Curr. Opin. Struct. Biol.,
mitochondria fixed by the selection of a compensatory
49, 44-53, doi: 10.1016/j.sbi.2017.12.009.
restorer of fertility-like PPR gene, Mol. Biol. Evol.,
71. Pfeffer, S., Woellhaf, M. W., Herrmann, J. M., and
38, 3445-3458, doi: 10.1093/molbev/msab115.
Förster, F. (2015) Organization of the mitochondrial
68. Matus-Ortega, M. G., Cárdenas-Monroy, C. A., Flores-
translation machinery studied in situ by cryoelectron
Herrera, O., Mendoza-Hernández, G., Miranda, M.,
tomography, Nat. Commun., 6, 6019, doi: 10.1038/
González-Pedrajo, B., Vázquez-Meza, H., and
ncomms7019.
Pardo, J. P. (2015) New complexes containing the
72. Ferretti, M. B., and Karbstein, K.
(2019) Does
internal alternative NADH dehydrogenase (Ndi1) in
functional specialization of ribosomes really exist?
mitochondria of Saccharomyces cerevisiae: mitochon-
RNA, 25, 521-538, doi: 10.1261/rna.069823.118.
drial complexes containing the alternative NADH
73. Shi, Z., Fujii, K., Kovary, K. M., Genuth, N. R.,
dehydrogenase, Yeast,
32,
629-641, doi:
10.1002/
Röst, H. L., Teruel, M. N., and Barna, M. (2017)
yea.3086.
Heterogeneous ribosomes preferentially translate
69. Ott, M., and Herrmann, J. M. (2010) Co-translational
distinct subpools of mRNAs genome-wide, Mol. Cell,
membrane insertion of mitochondrially encoded
67, 71-83.e7, doi: 10.1016/j.molcel.2017.05.021.
DIVERSITY AND EVOLUTION
OF MITOCHONDRIAL TRANSLATION APPARATUS
Review
M. V. Baleva, U. E. Piunova, I. V. Chicherin, S. A. Levitskii, and P. A. Kamenski*
Faculty of Biology, Lomonosov Moscow State University,
119234 Moscow, Russia; email: piotr.kamenski@gmail.com
The evolution of mitochondria proceeded independently in different eukaryotic lines, reflected in the diver-
sity of mitochondrial genomes and mechanisms of their expression observed in different eukaryotic species.
Mitochondria lost most of the genes of their bacterial ancestor, partially transferred them to the nucleus
or completely eliminated. However, the mitochondria of almost all eukaryotic cells retain relatively small
genomes, as well as their replication, transcription, and translation apparatuses. Dependence on the nuclear
genome, features of mitochondrial transcripts, and the necessity to synthesize highly hydrophobic mem-
brane proteins led to a number of significant changes in translation apparatus derived from the bacterial
ancestor. It retained the basic structure necessary for protein synthesis but became more specialized and
labile. In this review, we consider what changes take place during the initiation of mitochondrial translation,
and how the evolution of mitochondria affected the functions of the main factors initiating protein biosyn-
thesis in these organelles.
Keywords: mitochondria, translation initiation factors, regulation of translation, translation
БИОХИМИЯ том 88 вып. 11 2023