БИОХИМИЯ, 2023, том 88, вып. 11, с. 2251 - 2270
УДК 571.27;577.121
МЕТАБОЛИЧЕСКИЕ СВОЙСТВА Т-ЛИМФОЦИТОВ
И МЕТОДЫ ИХ РЕГУЛЯЦИИ
Обзор
© 2023 В.В. Власова*#, К.В. Шмагель#
Институт экологии и генетики микроорганизмов УрО РАН -
филиал ФГБУН «Пермский федеральный исследовательский центр УрО РАН»,
614081 Пермь, Россия; электронная почта: violetbaudelaire73@gmail.com
Поступила в редакцию 28.04.2023
После доработки 21.07.2023
Принята к публикации 27.08.2023
Т-Лимфоциты играют ведущую роль в реализации иммунного ответа. В ходе жизнедеятельности
Т-клетки проходят через целый ряд функциональных состояний: покой, активация, пролифера-
ция, дифференцировка, реализация эффекторных и регуляторных функций, апоптоз и формиро-
вание памяти. Метаболизм поддерживает все функции Т-лимфоцитов, обеспечивая их энергией,
биосинтетическими субстратами и сигнальными молекулами. Поэтому переход Т-клеток из одно-
го функционального состояния в другое, как правило, сопровождается перестройкой обменных
процессов. Тесная связь между метаболизмом и функцией Т-лимфоцитов дает основания пола-
гать, что, воздействуя на обменные процессы в Т-клетках, можно управлять иммунным ответом.
Настоящий обзор призван осветить ключевые метаболические адаптации, поддерживающие функ-
ции Т-лимфоцитов, а также возможности воздействия на обменные процессы в Т-клетках для
регуляции работы иммунной системы.
КЛЮЧЕВЫЕ СЛОВА: Т-лимфоциты, метаболизм, гликолиз, ЦТК, окислительное фосфорилирование,
митохондрии, пролиферация, дифференцировка, иммунологическая память, истощение.
DOI: 10.31857/S0320972523110167, EDN: MMRMGN
ВВЕДЕНИЕ
Среди иммунокомпетентных клеток наи-
более сложной и гетерогенной популяцией
В настоящий момент общепризнанно, что
являются Т-лимфоциты. Принято выделять
функции всех эукариотических клеток обес-
две крупные субпопуляции Т-клеток - CD4-
печиваются метаболизмом [1]. Клетки иммун-
позитивные Т-хелперы и цитотоксические
ной системы не являются исключением. Для
CD8+ Т-лимфоциты. Обе субпопуляции состо-
поддержания гомеостаза организма иммуно-
ят из клеток различной степени дифференци-
компетентные клетки выполняют множество
ровки: наивных Т-лимфоцитов, Т-эффекторов
функций: продуцируют цитотоксические гра-
и Т-клеток памяти [3]. CD4+ Т-клетки, обладаю-
нулы, антимикробные пептиды и цитокины,
щие эффекторными функциями, могут быть
фагоцитируют чужеродные объекты и погиб-
разделены на Th1-, Th2- и Th17-лимфоциты [4].
шие клетки, презентируют антигены и про-
Кроме того, существуют регуляторные Т-лим-
изводят антитела. Реализация этих задач тре-
фоциты (Трег), выполняющие важную роль в
бует энергии, биосинтетических субстратов и
подавлении иммунных реакций [5]. Перечис-
сигнальных молекул, образуемых в ходе мета-
ленные субпопуляции Т-клеток различаются
болизма. Поэтому за каждой функцией имму-
не только по функциональной направленности
нокомпетентных клеток, как правило, стоит
и экспрессии поверхностных маркеров, но
уникальный метаболический профиль [2].
и по метаболическим характеристикам [6, 7].
Принятые сокращения: Трег - регуляторные Т-лимфоциты; AMPK - AMP-активируемая протеинкиназа; mTOR -
мишень рапамицина млекопитающих; PD-1 - рецептор программируемой клеточной гибели 1; PD-L - лиганды PD-1.
* Адресат для корреспонденции.
# Авторы внесли равный вклад в работу.
2251
2252
ВЛАСОВА, ШМАГЕЛЬ
Иммунный ответ, реализуемый Т-лимфоци-
с дефицитом липидов [13], нуклеотидов [14] и
тами, также требует включения целого ряда
аминокислот [15] подвергаются аресту клеточ-
фундаментальных процессов, характерных для
ного цикла. Скорость и эффективность им-
большинства клеток организма: пролиферации,
мунного ответа во многом определяются про-
дифференцировки, апоптоза
[8]. При этом
лиферативным потенциалом Т-лимфоцитов.
наблюдается выраженная перестройка метабо-
Поэтому в делящихся Т-клетках метаболиче-
лизма. При хронических инфекциях или дли-
ские пути всегда адаптированы к активному
тельной персистенции антигена Т-лимфоциты
биосинтезу.
могут подвергаться истощению [9, 10]. Дру-
При пролиферации Т-лимфоцитов важ-
гими словами, при иммунном ответе Т-клет-
ным источником биосинтеза и энергии явля-
ки проходят через множество функциональ-
ется глюкоза. Процесс окисления глюкозы -
ных состояний, требующих для их реализации
гликолиз - представляет собой комплекс из
установления оптимального метаболического
десяти последовательных ферментативных
статуса.
реакций, промежуточные продукты которых
Тесная связь между метаболизмом и функ-
нередко выступают субстратами в побочных
цией Т-лимфоцитов дает основания полагать,
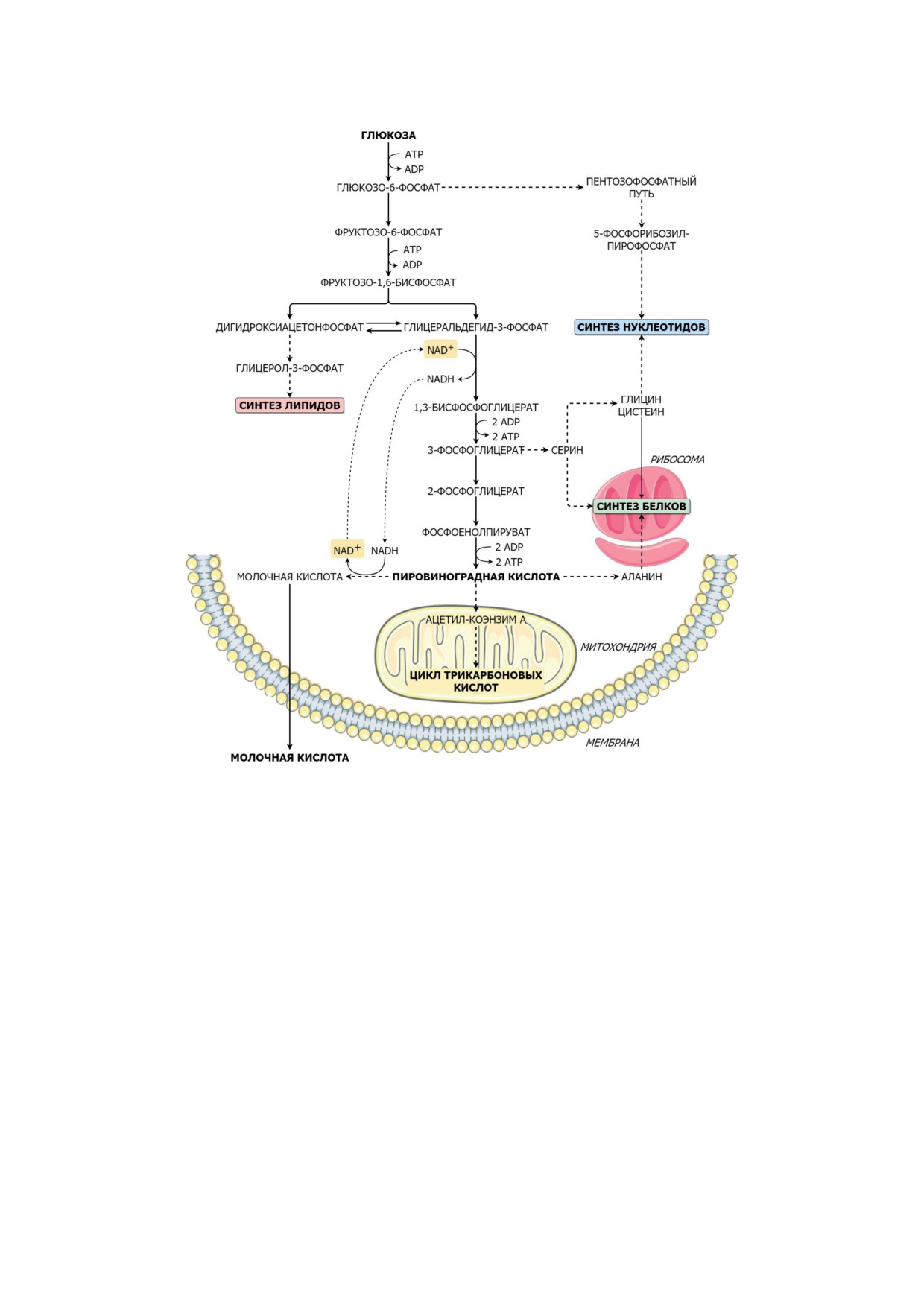
биосинтетических путях (рис. 1). Так, глю-
что через обменные процессы можно объектив-
козо-6-фосфат может служить источником
но воздействовать на Т-клеточный иммунный
углерода в пентозофосфатном пути, обеспе-
ответ. Развитие этого вектора исследований
чивающим клетку 5-фосфорибозилпирофос-
может привести к появлению терапевтических
фатом
- важным компонентом пуриновых
препаратов с известным и точным механиз-
и пиримидиновых нуклеотидов [16]. Другой
мом действия, изменяющих иммунный ответ
промежуточный продукт гликолиза - 3-фос-
в нужном направлении. Разработка подобных
фоглицерат - может быть предшественником
препаратов актуальна для целого ряда заболе-
цистеина, серина и глицина, участвующих в
ваний: онкологических, аутоиммунных, ин-
синтезе белков и нуклеотидов [17]. Кроме того,
фекционных. Настоящий обзор призван осве-
конечный продукт гликолиза
- пировино-
тить ключевые метаболические адаптации,
градная кислота - может преобразовываться
поддерживающие функции Т-лимфоцитов, а
в аминокислоту аланин [18]. Третьим классом
также возможности воздействия на обменные
соединений, продуцируемых из метаболитов
процессы в Т-клетках для регуляции работы
гликолитического пути, являются глицеро-
иммунной системы.
липиды [19]. Их источником служит дигид-
роксиацетонфосфат - предшественник глице-
рол-3-фосфата.
МЕТАБОЛИЧЕСКОЕ ОБЕСПЕЧЕНИЕ
Углерод, поступающий с глюкозой, необ-
ПРОЛИФЕРАЦИИ Т-ЛИМФОЦИТОВ
ходим для протекания многих биосинтети-
ческих процессов, поэтому ее потребление и
Ключевым этапом Т-клеточного иммун-
окисление в пролиферирующих Т-лимфоцитах
ного ответа является клональная экспансия,
существенно усиливается [20]. Полное окис-
то есть пролиферация антигенспецифичных
ление глюкозы завершается формированием
клеток. Необходимость в делении продикто-
двух молекул ATP и двух молекул пировино-
вана клональной природой Т-лимфоцитов:
градной кислоты, которые могут подвергаться
при проникновении антигена в организм
либо окислению, либо восстановлению. Как
число специфичных к нему клеток слишком
правило, в присутствии кислорода пировино-
мало для реализации эффективного иммун-
градная кислота окисляется под действием
ного ответа [11]. Лимфоциты, распознавшие
пируватдегидрогеназного мультиферментного
презентированный им чужеродный пептид,
комплекса и формирует ацетил-коэнзим А
преодолевают данное ограничение путем мно-
(ацетил-КоА) [21]. Образованный ацетил-КоА
гократного митотического деления. Как пра-
служит источником углерода в цикле три-
вило, митоз сопровождается метаболической
карбоновых кислот (ЦТК), функционирова-
ассимиляцией, в ходе которой усиливается
ние которого сопряжено с синтезом 36 моле-
синтез энергии, а также нуклеиновых кислот,
кул ATP на одну молекулу глюкозы. Однако
белков и липидов - «строительных материа-
данное правило не распространяется на деля-
лов» для генетического аппарата, органелл и
щиеся Т-лимфоциты [22]: несмотря на нали-
мембран дочерней клетки [12]. При этом спо-
чие кислорода в среде, такие клетки преоб-
собность клетки активно производить макро-
разуют большую часть глюкозы в молочную
молекулы прямо влияет на возможность завер-
кислоту (рис. 1). В этом случае энергетический
шения деления: в большинстве случаев клетки
выход гликолиза на одну молекулу глюкозы
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2253
Рис. 1. Продукты гликолитических реакций и их роль в биосинтетических процессах при делении Т-лимфоцитов
существенно снижается и составляет две моле-
В покоящемся состоянии Т-лимфоциты под-
кулы ATP. В литературе данный феномен обо-
держивают гликолитическую активность, пре-
значается термином «аэробный гликолиз».
имущественно окисляя этот продукт в ЦТК.
Использование аэробного гликолиза в ка-
Однако количество пировиноградной кисло-
честве основного пути метаболизма глюкозы
ты, которую можно реализовать таким спосо-
при пролиферации на первый взгляд кажется
бом, ограничено дыхательной емкостью мито-
контрпродуктивным. В таком случае только
хондрий [27]. Пролиферирующие клетки сни-
около 7% углерода, поступающего с глюкозой,
мают данное ограничение, преобразуя избы-
вовлечены в образование макромолекул [23].
ток пировиноградной кислоты в молочную и
Более 90% расходуется на продукцию молоч-
транспортируя ее во внеклеточное простран-
ной кислоты, которая экскретируется во вне-
ство [26]. Другим фактором, ограничивающим
клеточное пространство [24]. Тем не менее
гликолитическую активность, является со-
делящиеся Т-лимфоциты используют такой
держание окисленной формы никотинамид-
«расточительный» тип метаболизма для до-
адениндинуклеотида (NAD+) в цитоплазме.
стижения важной цели - увеличения интен-
Полное окисление одной молекулы глюкозы
сивности гликолиза [25]. Существует целый
требует двух молекул NAD+, служащих ко-
ряд факторов, способных ограничить ско-
ферментами при превращении глицеральде-
рость гликолиза в клетке. Одним из основ-
гид-3-фосфата в 1,3-бисфосфоглицериновую
ных является накопление конечного продукта
кислоту [28]. В ходе реакции NAD+ переходит
гликолиза - пировиноградной кислоты [26].
в восстановленную форму (NADН), поэтому
БИОХИМИЯ том 88 вып. 11 2023
2254
ВЛАСОВА, ШМАГЕЛЬ
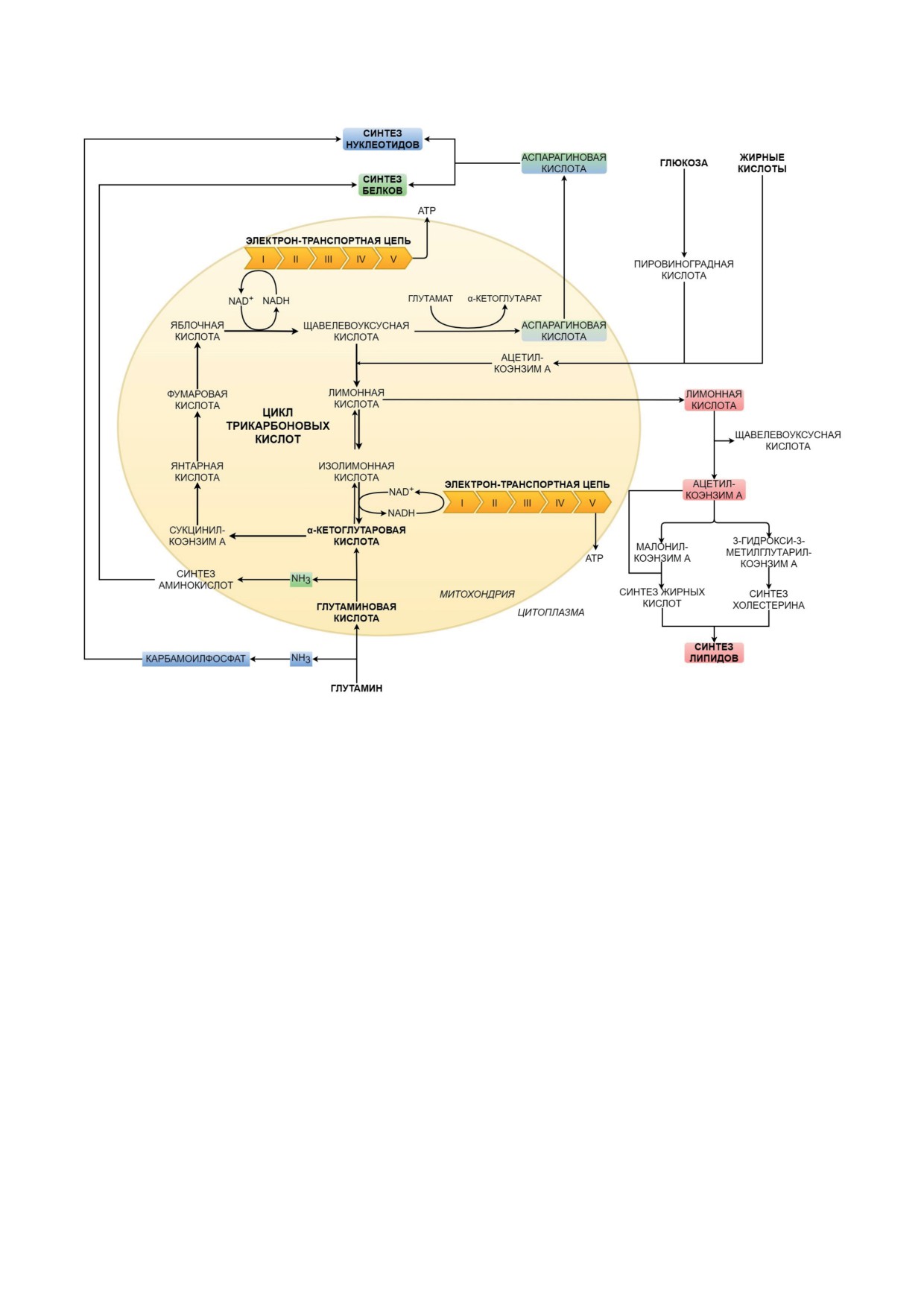
Рис. 2. Промежуточные продукты цикла трикарбоновых кислот и их роль в биосинтетических процессах
повторение гликолиза требует окисления ко-
страты - производные глюкозы, глутамина и
фермента. В пролиферирующих клетках реге-
жирных кислот - участвуют в восстановлении
нерация цитозольного NAD+ происходит при
доноров электронов для дыхательной цепи.
окислении NADН в ходе реакции восстанов-
Помимо этого, ЦТК является важным источ-
ления пировиноградной кислоты [29]. Таким
ником метаболических субстратов, необходи-
образом, аэробный гликолиз исключает воз-
мых для синтеза аминокислот, липидов и ну-
действие двух факторов, ограничивающих ско-
клеотидов (рис. 2) [33]. Так, лимонная кислота,
рость окисления глюкозы: избытка пирувата
формируемая в первой реакции ЦТК при взаи-
и дефицита NAD+. В результате в пролифери-
модействии щавелевоуксусной кислоты и аце-
рующих Т-лимфоцитах увеличивается продук-
тил-КоА, участвует в de novo синтезе жирных
ция ATP вне митохондрий, а поток углерода
кислот. Образованная в митохондрии лимон-
через гликолитический путь и сопряженные с
ная кислота транспортируется в цитоплазму,
ним биосинтетические процессы существенно
где подвергается ферментативному расщепле-
возрастает [30].
нию на исходные соединения: ацетил-КоА и
Активность митохондрий при пролифе-
щавелевоуксусную кислоту [34]. В цитоплазме
рации Т-клеток также существенно усилива-
ацетил-КоА превращается в малонил-КоА,
ется и дополняет гликолиз при синтезе макро-
осуществляющий удлинение углеродной цепи
молекул и энергии [31]. Так, в Т-лимфоцитах
жирных кислот [35]. Помимо этого, цитоплаз-
уже через 4 часа митогенной стимуляции воз-
матический ацетил-КоА может участвовать в
растает концентрация промежуточных про-
формировании
3-гидрокси-3-метилглутарил-
дуктов ЦТК [32]. ЦТК представляет собой узел
КоА - предшественника мевалоновой кисло-
пересечения большинства метаболических пу-
ты и, соответственно, холестерина [36]. Упомя-
тей, в котором разнообразные углеродные суб-
нутая выше щавелевоуксусная кислота также
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2255
поддерживает процессы биосинтеза в деля-
ной цепи митохондрий связывали исключи-
щихся клетках. В реакции трансаминирования
тельно с потребностью делящихся клеток в
данный субстрат преобразуется в аспарагино-
энергии. Тем не менее последние исследо-
вую кислоту, используемую при построении
вания показывают, что именно способность
белков и нуклеотидов [37].
дыхательной цепи восстанавливать пул NAD+
В пролиферирующих клетках промежуточ-
является фактором, лимитирующим пролифе-
ные продукты ЦТК активно используются в
рацию [46]. Так, было установлено, что инги-
побочных биосинтетических реакциях, поэто-
биторы митохондриального дыхания вызы-
му для поддержания данного метаболического
вают в опухолевых клетках арест клеточного
пути необходим постоянный приток углерода.
цикла, снижение соотношения NAD+/NADН,
Его основным источником в делящихся клет-
а также падение концентрации промежуточ-
ках является самая распространенная в орга-
ных продуктов ЦТК и их производных, в част-
низме аминокислота - глутамин. В условиях
ности - аспарагиновой кислоты. Аспарагино-
пролиферации ее потребление в Т-лимфоци-
вая кислота имеет большое значение в синтезе
тах возрастает в 5-10 раз [38]. Углеродный ске-
пуриновых нуклеотидов, поэтому ее дефицит
лет глутамина включается в ЦТК в виде α-кето-
при недостатке NAD+ приводит к остановке
глутаровой кислоты (рис. 2), которая способна
деления на стадии репликации ДНК. Таким
преобразовываться в продукты нисходящих
образом, при пролиферации клетки метаболи-
реакций цикла либо пополнять пул лимонной
ческие пути, сопряженные с продукцией энер-
кислоты. В структуре глутамина присутствуют
гии, активно поддерживают процессы био-
две азотсодержащие группы, поэтому его пре-
синтеза.
вращение в α-кетоглутаровую кислоту пред-
Помимо промежуточных продуктов гли-
ставляет собой две последовательные реакции
колиза и ЦТК, важным источником биосин-
дезаминирования [39]. Продуктами первой ре-
тетических молекул также являются продукты
акции являются глутаминовая кислота и ам-
метаболизма одноуглеродных остатков (one-
миак. В пролиферирующих клетках аммиак
carbon metabolism) [31]. Метаболизм одноугле-
участвует в образовании карбамоилфосфата -
родных остатков объединяет фолатный цикл
основы пиримидинового кольца [40]. Азот,
и цикл метионина и представляет собой свое-
высвобождающийся при дезаминировании глу-
образный
«распределительный центр» угле-
таминовой кислоты, также участвует в био-
рода. Источником углерода в данном случае
синтетических процессах, в частности - в пре-
является аминокислота серин, а акцепторами
вращении кетокислот в аминокислоты. Так,
выступают метаболические продукты, соеди-
глутаминовая кислота является донором азота
няющие фолатный цикл и цикл метионина
для пировиноградной, 3-фосфоглицериновой
с путями биосинтеза нуклеотидов, белков и
и щавелевоуксусной кислот, образующих со-
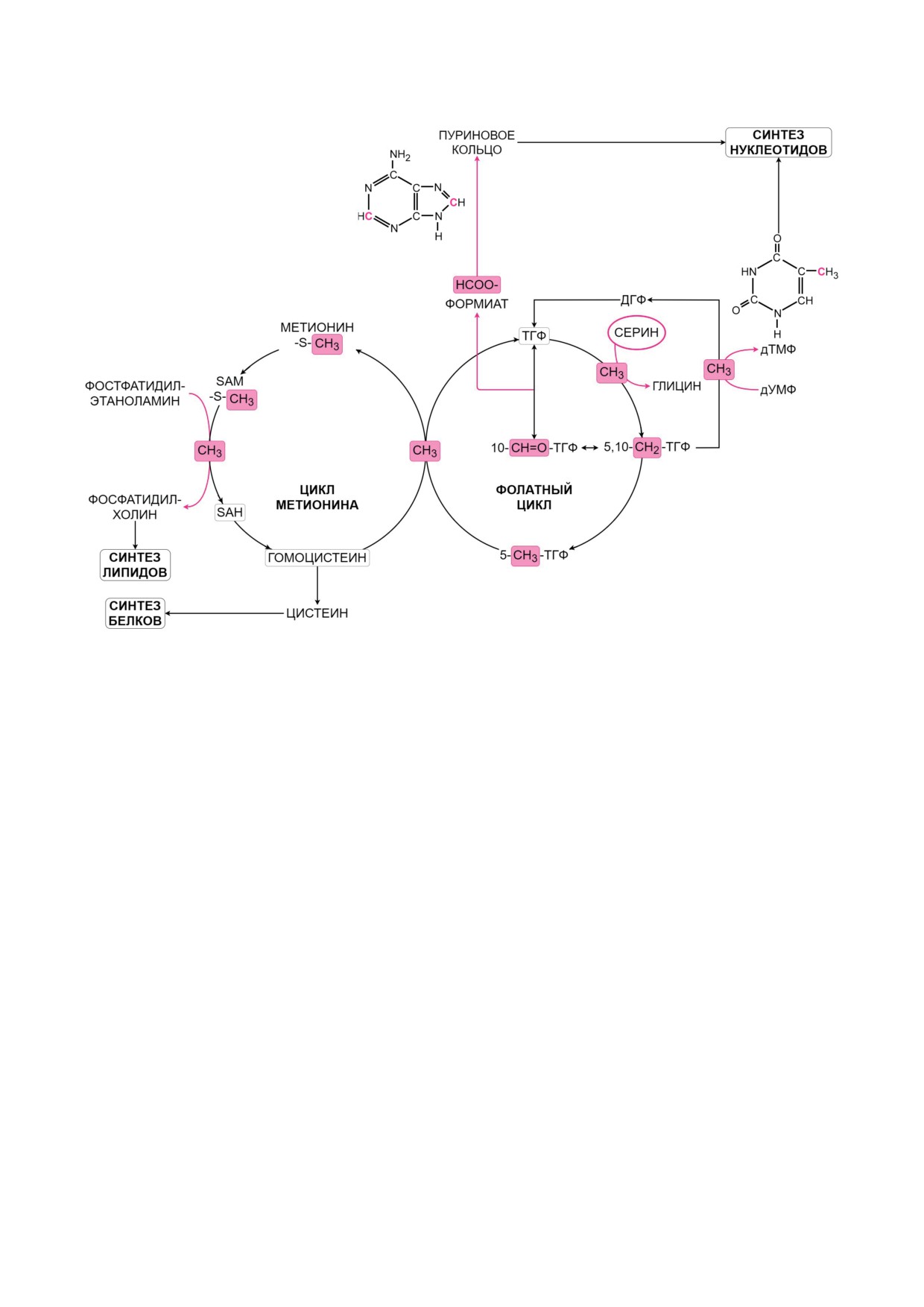
липидов (рис. 3) [47]. Так, производное фо-
ответственно аланин, серин и аспарагиновую
лиевой кислоты
- 5,10-метилентетрагидро-
кислоту [41].
фолат - переносит метильную группу серина
По аналогии с гликолизом, функциони-
на дезоксиуридинмонофосфат, что приводит
рование ЦТК существенно зависит от баланса
к образованию дезокситимидинмонофосфа-
между окисленной и восстановленной фор-
та [48]. В свою очередь, 10-формилтетрагид-
мой NAD. NAD+ является коферментом при
рофолат участвует в биосинтезе пуриновых
превращении α-кетоглутаровой кислоты в
нуклеотидов [49]. Кроме того, при участии
сукцинил-КоА [42], а также яблочной кис-
одноуглеродных остатков протекает формиро-
лоты в щавелевоуксусную [43]. В ходе дан-
вание фосфатидилхолина - основного компо-
ных реакций NAD переходит из окисленной
нента всех клеточных мембран [50]. Наконец,
формы в восстановленную (NADН) и стано-
функционирование фолатного цикла и цикла
вится потенциальным донором электронов
метионина также сопряжено с образованием
для дыхательной цепи митохондрий [43]. При
ряда аминокислот, в том числе глицина, гомо-
отсутствии кофермента дегидрирование α-ке-
цистеина и цистеина [51]. В связи с этим при
тоглутаровой и яблочной кислот не проис-
пролиферации интенсивность метаболизма
ходит, поэтому повторение цикла всегда тре-
одноуглеродных остатков существенно воз-
бует восполнения пула NAD+ [44]. В связи с
растает [52].
этим в пролиферирующих клетках усиление
Представленные данные демонстрируют,
работы ЦТК, как правило, сопровождается
что переход покоящихся лимфоцитов к деле-
повышением активности дыхательной цепи,
нию сопровождается усилением большинства
окисляющей NADН [45]. Стоит отметить, что
биосинтетических процессов, каждый из кото-
ранее усиление работы электрон-транспорт-
рых вносит уникальный вклад в образование
БИОХИМИЯ том 88 вып. 11 2023
2256
ВЛАСОВА, ШМАГЕЛЬ
Рис. 3. Метаболизм одноуглеродных остатков и его роль в биосинтетических процессах. Примечания: одноуглеродные
остатки выделены на рисунке розовым цветом; ДГФ - дигидрофолат; ТГФ - тетрагидрофолат; дУМФ - дезоксиури-
динмонофосфат; дТМФ - дезокситимидинмонофосфат; SAM - S-аденозилметионин; SAH - S-аденозилгомоцистеин
нуклеотидов, белков и липидов, необходимых
воздействуя на эти метаболические пути, мож-
для воспроизведения материнской клетки.
но подавить Т-клеточный иммунный ответ на
В частности, в ответ на стимуляцию в Т-клет-
начальном этапе - на стадии клональной экс-
ках усиливаются аэробный гликолиз, окисли-
пансии.
тельное фосфорилирование и глутаминолиз,
В настоящий момент известен целый ряд
активность ЦТК, пентозофосфатного и мева-
препаратов, подавляющих анаболизм в клет-
лонового путей, а также метаболизм одноугле-
ках млекопитающих. К ним относятся 2-дез-
родных остатков. В результате, спустя 24 часа
оксиглюкоза и дихлорацетат, подавляющие
после стимуляции, размер Т-лимфоцитов зна-
аэробный гликолиз [56, 61], метформин, сни-
чительно увеличивается
[53], а содержание
жающий интенсивность окислительного фос-
клеточных белков удваивается [54]. Через 30-
форилирования [62], AR-C141990, подавляю-
48 часов с момента активации метаболическая
щий активность транспортера лактата [63],
перестройка Т-лимфоцитов завершается гене-
а также ингибиторы синтеза жирных кислот
рацией первой дочерней популяции [55].
и глутаминолиза - сорафен А [64] и диазо-
Исходя из важной роли метаболизма в про-
норлейцин [58]. Следует отметить, что при-
лиферации Т-лимфоцитов, закономерно, что
веденные данные получены преимущественно
ингибиторы анаболических процессов явля-
экспериментальным путем. Способность дан-
ются перспективными агентами для борьбы с
ных препаратов ограничивать пролиферацию
нежелательными иммунными реакциями. По-
Т-лимфоцитов показана исключительно в
казано, что Т-лимфоциты, в которых подавле-
системах in vitro и на модельных организмах.
на активность гликолиза [56], транспортеров
Применение ингибиторов анаболизма для ре-
глюкозы [57], глутаминолиза [58], ЦТК [59],
гуляции иммунных реакций в организме чело-
окислительного фосфорилирования [56] либо
века потребует расширения спектра исполь-
метаболизма одноуглеродных остатков
[52,
зуемых препаратов и проведения длительных
60], пролиферируют слабо. Следовательно,
клинических испытаний.
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2257
МЕТАБОЛИЧЕСКАЯ РЕГУЛЯЦИЯ
щих), напротив, стимулирует образование
Т-КЛЕТОЧНОЙ ДИФФЕРЕНЦИРОВКИ
Th17-клеток [74]. Еще одной особенностью
Th17-лимфоцитов является активный синтез
За экспансией лимфоцитов следует ста-
жирных кислот de novo. Об этом свидетель-
дия дифференцировки, в ходе которой
ствует высокий уровень экспрессии в данных
CD8+ Т-лимфоциты преобразуются в эффек-
клетках фермента ацетил-КоА карбоксилазы I,
торные клетки, а CD4+ Т-лимфоциты поляри-
катализирующего лимитирующую реакцию
зуются в Th1, Th2, Th17 или Трег. Среди них
биосинтеза жирных кислот [64]. Подавление
Th17-лимфоциты и Трег чаще всего являются
активности данного фермента в Т-лимфо-
объектом исследований при различных забо-
цитах также препятствует их поляризации в
леваниях: данные субпопуляции обладают ан-
направлении Th17 и стимулирует образова-
тагонистическими функциями и представ-
ние Трег [64].
ляют собой две крайности спектра между
Метаболизм Трег, в свою очередь, отли-
про- и противовоспалительным фенотипом.
чается высокой активностью окислительного
Th17-лимфоциты в норме участвуют в защите
фосфорилирования. Эти клетки, в сравнении
слизистых барьеров от внеклеточных пато-
с конвенциональными лимфоцитами, актив-
генов: продуцируют цитокины IL-17, IL-22 и
нее экспрессируют цитохром c и комплексы I,
IL-23, привлекают нейтрофилы в очаг инфек-
II и V электронно-транспортной цепи, а также
ции и стимулируют локальное воспаление [65].
имеют большую резервную дыхательную ем-
Функции Трег направлены на поддержание
кость митохондрий [68]. При этом уровень ми-
толерантности к собственным антигенам и
тохондриального дыхания в Трег влияет на их
предотвращение аутоиммунных реакций [5].
супрессорную активность [75]. Показано, что
Эти клетки продуцируют цитокины IL-10 и
добавление рапамицина (ингибитора mTOR)
TGF-β, подавляют активность множества им-
к наивным Т-лимфоцитам, культивируемым в
мунных клеток и, следовательно, угнетают
присутствии активационных частиц и TGF-β,
воспалительные реакции [64]. Нарушение ба-
приводит к усилению окислительного фос-
ланса между Th17-лимфоцитами и Трег неиз-
форилирования в данных клетках и увеличе-
бежно приводит к развитию заболеваний.
нию доли индуцированных Трег [76]. Другой
Так, преобладание активности Th17-лимфо-
ингибитор mTOR - эмпаглифлозин - показал
цитов характерно для ревматоидного артрита
аналогичный эффект в культурах CD4+ Т-кле-
и системной красной волчанки [66]. Усиление
ток, полученных от пациентов с иммунной
функции Трег, в свою очередь, связывают с
тромбоцитопенией [77]. Важным источником
развитием и прогрессией опухолей [67].
углерода для митохондрий Трег являются про-
Принято считать, что за антагонистиче-
дукты β-окисления жирных кислот. Об этом
скими функциями Th17-клеток и Трег стоят
свидетельствует повышенное содержание аце-
два различных метаболических профиля [7].
тилкарнитина и гидроксибутирилкарнитина,
Так, метаболизм Th17-лимфоцитов отлича-
а также высокий уровень экспрессии в дан-
ется высокой активностью гликолиза. В цито-
ных клетках транспортера жирных кислот -
плазме Th17-лимфоцитов содержится боль-
карнитин-пальмитоилтрансферазы I [68]. По-
шое количество пировиноградной и молочной
казано, что индукция AMP-активируемой про-
кислот, а также промежуточных продуктов
теинкиназы (англ. AMP-activated protein ki-
пентозофосфатного пути [68]. Кроме того, такие
nase - AMPK), стимулирующей потребление
клетки отличаются от Трег усиленной экспрес-
и окисление липидов, приводит к поляриза-
сией транспортера глюкозы Glut1 и начально-
ции Т-лимфоцитов в направлении Трег [78],
го фермента гликолиза - гексокиназы II [68].
в то время как блокада липолиза подавляет
Показано, что подавление гликолиза путем за-
дифференцировку Трег [75, 79] и угнетает суп-
мещения глюкозы 2-деоксиглюкозой [69], га-
рессорную активность данных клеток [75, 80].
лактозой [70] или маннозой [71] препятствует
Из вышесказанного следует, что в популя-
поляризации активированных лимфоцитов в
ции Т-клеток про- и противовоспалитель-
направлении Th17-клеток и стимулирует фор-
ный фенотипы поддерживаются гликолизом
мирование Трег. Кроме того, формирование
и окислительным фосфорилированием соот-
Th17-лимфоцитов нарушается при подавлении
ветственно. При этом на дифференцировку
активности гликолитических ферментов - пи-
Т-лимфоцитов также существенно влияет
руваткиназы [72] и лактатдегидрогеназы [73].
баланс между анаболическими и катаболиче-
Усиление гликолиза на фоне активации
скими процессами в липидном обмене: поля-
фактора mTOR (англ. mammalian target of
ризация в направлении Th17 в значительной
rapamycin - мишень рапамицина млекопитаю-
степени зависит от синтеза жирных кислот,
15
БИОХИМИЯ том 88 вып. 11 2023
2258
ВЛАСОВА, ШМАГЕЛЬ
в то время как образование Трег поддержива-
противовоспалительных Трег и формирование
ется их β-окислением.
толерантности.
Необходимо отметить, что в дифференци-
Наиболее перспективной метаболической
рованных Т-клетках дихотомия «гликолиз ↔
мишенью для терапии аутоиммунных заболева-
↔ окислительное фосфорилирование» или «син-
ний в настоящий момент считается mTOR [87].
тез ↔ окисление жирных кислот» носит неабсо-
Эффективность его ингибиторов была дока-
лютный характер. Вероятнее всего, Th17-лим-
зана целым рядом клинических исследова-
фоциты и Трег в разной степени задействуют
ний. Так, в двойном слепом контролируемом
как анаболические, так и катаболические
исследовании было показано, что назначение
процессы для поддержания своей жизнедея-
N-ацетилцистеина пациентам с системной
тельности. Основные свидетельства в пользу
красной волчанкой приводит к снижению ак-
этой гипотезы были получены в эксперимен-
тивности mTOR в CD4+ Т-клетках, увеличению
тах с генетически модифицированными Трег.
экспрессии характерного для Трег транскрип-
В частности, было показано, что Трег, не спо-
ционного фактора Forkhead box P3 (FoxP3) и
собные экспрессировать один из основных
снижению проявления симптомов заболева-
транскрипционных регуляторов гликолиза -
ния [88]. Помимо этого, было показано, что
HIF-1α (англ. hypoxia-inducible factor-1α
-
N-ацетилцистеин может снижать проявление
гипоксией индуцированный фактор-1α) - от-
симптомов синдрома Шегрена [89]. Другой
личаются низкой супрессорной активностью
ингибитор mTOR - рапамицин - обладает
в модели экспериментального язвенного ко-
доказанной эффективностью при лечении си-
лита [81]. Кроме того, было установлено, что
стемной красной волчанки у пациентов со сла-
в Трег делеция гена RPTOR, кодирующего
бым ответом на традиционную терапию [90].
адаптерный белок для mTOR, приводит к
Еще один препарат этой группы - эвероли-
нарушению синтеза жирных кислот и холе-
мус - повышает эффективность терапии мето-
стерина, угнетению пролиферации, а также
трексатом у пациентов с ревматоидным артри-
снижению экспрессии индуцируемого кости-
том [91]. Возможно, более продолжительные и
мулятора Т-лимфоцитов (англ. inducible T-cell
масштабные исследования, подтверждающие
costimulator - ICOS) и ингибиторного рецеп-
безопасность и эффективность данных препа-
тора CTLA-4 (CD152) [82]. Из вышесказанного
ратов, позволят внедрить ингибиторы mTOR в
следует, что, хотя химические ингибиторы гли-
общую практику лечения аутоиммунных забо-
колиза и синтеза жирных кислот стимулируют
леваний.
образование Трег, полное подавление анабо-
лических путей угнетает супрессорную функ-
цию регуляторных клеток.
РОЛЬ МЕТАБОЛИЗМА В ФОРМИРОВАНИИ
Представленные сведения позволяют за-
ИММУНОЛОГИЧЕСКОЙ ПАМЯТИ
ключить, что направление дифференцировки
Т-лимфоцитов определяется тем, какие мета-
После элиминации патогена большинство
болические процессы преобладают в данных
антигенспецифичных Т-лимфоцитов, сформи-
клетках: анаболические или катаболические.
рованных в процессе иммунного ответа, по-
Более того, метаболизм можно использовать
гибает путем апоптоза, а выжившие клетки
в качестве переключателя, направляющего
сохраняют иммунологическую память о пере-
Т-клетки к про- или противовоспалительному
несенном контакте с антигеном. Сохранив-
фенотипу. Ожидается, что препараты, подав-
шиеся Т-клетки памяти, при их сравнении с
ляющие процессы гликолиза и синтеза жир-
наивными Т-лимфоцитами, обладают суще-
ных кислот в Т-лимфоцитах, найдут широ-
ственным преимуществом при вторичном им-
кое применение при терапии аутоиммунных
мунном ответе: такие клетки быстрее вступают
заболеваний и предотвращении отторжения
в пролиферацию и начинают продуцировать
трансплантата [83]. В настоящий момент для
цитокины значительно раньше [92]. Способ-
коррекции этих состояний применяются им-
ность Т-лимфоцитов памяти к ускоренному и
муносупрессанты, такие как метотрексат [84],
усиленному иммунному ответу на вновь рас-
циклоспорин, азатиоприн и такролимус [85].
познанный антиген лежит в основе создания
Однако данные соединения обладают невысо-
вакцин.
кой специфичностью и подавляют активность
Преобразование эффекторных Т-лимфо-
всех Т-лимфоцитов, в том числе Трег [86].
цитов в Т-клетки памяти сопряжено с оче-
Ингибиторы анаболизма, в свою очередь, по-
редной метаболической перестройкой: анабо-
зволят не подавлять, а модулировать иммун-
лический процесс аэробного гликолиза сменя-
ный ответ, то есть стимулировать образование
ется катаболическим окислением липидов [93].
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2259
В соответствии с этим, было показано, что
В отличие от клеток крови, лимфатических
подавление активности mTOR [94], угнете-
узлов и селезенки, резидентные CD8+ Т-лим-
ние гликолиза [95] и блокада митохондри-
фоциты памяти, населяющие базальную мем-
ального переносчика пирувата [96] приводят
брану эпидермиса, преимущественно исполь-
к усилению β-окисления жирных кислот в
зуют жирные кислоты экзогенного проис-
CD8+ Т-лимфоцитах и стимулируют фор-
хождения. Так, делеция генов Fabp4 и Fabp5,
мирование клеток памяти. К накоплению
кодирующих транспортеры жирных кислот,
Т-клеток памяти in vitro приводит снижение
существенно снижает срок жизни резидент-
концентрации глюкозы в среде: данный эф-
ных CD8+ Т-клеток памяти кожи [102]. В то же
фект обусловлен активацией фактора AMPK
время делеция Fabp4 и Fabp5 в CD8+ Т-лимфо-
в Т-лимфоцитах [97]. При этом индуциро-
цитах центральной памяти, населяющих лим-
ванная экспрессия мишени AMPK - тран-
фатические узлы, не приводит к изменению их
скрипционного коактиватора PGC-1α (англ.
жизнеспособности. Потребление экзогенных
peroxisome proliferator-activated receptor-gamma
липидов также характерно для CD8+ Т-кле-
coactivator-1-alpha - коактиватор-1-альфа гамма-
ток памяти, расположенных в жировой ткани.
рецептора, активируемого пролифератором
Показано, что такие клетки потребляют суще-
пероксисом) - усиливает формирование Т-кле-
ственно больше экзогенных жирных кислот,
ток памяти в модели меланомы мыши [98].
чем CD8+ Т-лимфоциты памяти селезенки
Подавление β-окисления на уровне адаптер-
и лимфоидной ткани желудочно-кишечного
ного белка TRAF6 (англ. TNF receptor-asso-
тракта [103]. Однако их роль в обеспечении
ciated factor 6 - фактор 6, ассоциированный с
жизнеспособности и эффективного функцио-
рецептором фактора некроза опухолей), свя-
нирования CD8+ Т-клеток памяти жировой
зывающего AMPK, напротив, препятствует
ткани до конца не ясна.
формированию CD8+ Т-лимфоцитов памяти у
Как отмечалось ранее, ключевой функ-
иммунизированных мышей [99]. При этом вве-
циональной особенностью Т-лимфоцитов па-
дение мышам индуктора AMPK метформина
мяти является способность реализовывать
восстанавливает способность CD8+ Т-лимфо-
ускоренный и усиленный иммунный ответ
цитов дифференцироваться в клетки памяти.
при повторной встрече с патогеном. При этом
Важно отметить, что метформин также являет-
механизмы, позволяющие клеткам памяти
ся сильным индуктором формирования клеток
вступать в иммунный ответ быстрее наивных
памяти у мышей, не подвергшихся делеции
клеток, остаются малоизученными. Послед-
гена TRAF6. Авторы показали, что введение
ние экспериментальные данные позволяют
метформина мышам дикого типа с бактериаль-
предположить, что эта особенность Т-лимфо-
ной инфекцией или опухолью приводит к зна-
цитов памяти, по крайней мере отчасти, свя-
чительному увеличению числа CD8+ Т-лимфо-
зана с метаболическими адаптациями. Так,
цитов памяти в их организме [99].
было показано, что CD4+ и CD8+ Т-клетки
Жирные кислоты, используемые CD8+
памяти, при их сравнении с наивными клет-
Т-клетками памяти в ходе β-окисления, могут
ками, характеризуются большей активностью
иметь различное происхождение. Так, показа-
окислительного фосфорилирования
[6,
32],
но, что CD8+ Т-лимфоциты памяти из крови,
повышенной резервной дыхательной емко-
селезенки или лимфоузлов мыши используют
стью митохондрий [104, 105] и повышенным
жирные кислоты эндогенного происхождения:
гликолитическим резервом [6, 104]. При этом
они регулярно синтезируются de novo из угле-
высокая дыхательная и гликолитическая ем-
рода, поступающего с глюкозой, и запасаются
кость CD8+ Т-лимфоцитов памяти связана с
в форме триацилглицеридов [100, 101]. В этом
их способностью вступать в деление быстрее
случае метаболизм липидов характеризует-
наивных клеток [6]. Окислительное фосфори-
ся выражением «futile cycle» («бесполезный»
лирование и гликолиз являются магистраль-
цикл), поскольку антагонистические процес-
ными метаболическими путями, обеспечиваю-
сы синтеза и окисления жирных кислот, обыч-
щими биосинтез в пролиферирующих клетках.
но разобщенные, протекают одновременно.
В связи с этим можно предположить, что вы-
Многочисленные исследования показали, что
сокий дыхательный и гликолитический потен-
данный цикл имеет большое значение для
циал Т-лимфоцитов памяти позволяет им бы-
формирования [99] и выживания CD8+ Т-лим-
стрее завершить метаболическую перестройку,
фоцитов памяти [100, 101]. Однако механизм,
предшествующую делению.
связывающий «futile cycle» с формировани-
Обобщая вышесказанное, можно заклю-
ем иммунологической памяти, остается неиз-
чить, что формирование и функционирова-
вестным.
ние Т-клеток памяти зависит от определенных
БИОХИМИЯ том 88 вып. 11 2023
15*
2260
ВЛАСОВА, ШМАГЕЛЬ
метаболических адаптаций: перехода к β-окис-
зитол-3-киназу (phosphatidylinositol-3-kinase -
лению жирных кислот и усиления дыхательно-
PI3K) и протеинкиназу B, также известную
го и гликолитического потенциала. Что более
как Akt [112]. Блокада этого сигнального пути,
важно, вмешательства в метаболизм Т-лимфо-
с одной стороны, снижает уровень потребле-
цитов достаточно, чтобы усилить или ослабить
ния и метаболизма глюкозы и аминокислот, а
формирование клеток памяти. Связь между
с другой - усиливает экспрессию карнитин-
метаболизмом и иммунологической памятью
пальмитоилтрансферазы I, липолиз и β-окис-
позволяет предположить, что регуляция об-
ление жирных кислот [113]. Таким образом,
менных процессов станет ключом к усилению
Т-лимфоцит, получивший сигнал через рецеп-
поствакцинального иммунитета. В этом кон-
тор PD-1, не способен индуцировать анабо-
тексте большой интерес для исследователей
лические обменные процессы, необходимые
представляют иммуносупрессант рапамицин и
для активации, пролиферации и эффекторных
антидиабетический препарат метформин, ми-
функций.
шенью которых являются mTOR и AMPK соот-
Лиганды PD-1 - PD-L1 и PD-L2 - могут
ветственно [106]. Эти лекарственные средства
быть представлены на многих клетках чело-
способны усиливать формирование клеток
веческого организма. Так, PD-L1 может экс-
памяти у мышей после иммунизации [94, 99]
прессироваться на поверхности большинства
и трансплантации опухоли [107]. Эффектив-
иммуноцитов, в том числе на самих Т-лимфо-
ность рапамицина также была продемонстри-
цитах [114]. Кроме того, PD-L1 может присут-
рована на нечеловеческих приматах [99]. Од-
ствовать на поверхности неиммунных клеток,
нако влияние метформина и рапамицина на
таких как клетки эпителия и эндотелия, мио-
механизмы формирования иммунологической
циты, гепатоциты и астроциты [115]. Наконец,
памяти у человека остается малоизученным.
экспрессия PD-L1 также характерна для неко-
торых иммунно-привилегированных органов:
плаценты и глаза [115]. Экспрессия PD-L2,
МЕТАБОЛИЧЕСКИЕ МЕХАНИЗМЫ
напротив, ограничена иммунным клетками:
ЭФФЕКТОВ ИНГИБИТОРНЫХ
макрофагами, дендритными клетками и моно-
РЕЦЕПТОРОВ Т-ЛИМФОЦИТОВ
цитами [114, 116]. Поверхностная экспрессия
обоих лигандов, как правило, строго регулиру-
Иммунный ответ включает в себя не толь-
ется цитокиновым окружением. Показано, что
ко процессы, направленные на уничтожение
интерфероны типа 1 и 2, а также TNF-α стиму-
патогена, но и защитные реакции, обеспечи-
лируют экспрессию PD-L1 на поверхности Т-
вающие разрешение воспаления и восстанов-
и В-лимфоцитов, моноцитов, дендритных кле-
ление гомеостаза. Эффективным средством
ток, а также клеток эпителия и эндотелия [114,
контроля иммунных реакций выступает сиг-
117, 118]. Гемопоэтические цитокины IL-2, IL-7
нализация через ингибиторные рецепторы
и IL-15 также усиливают экспрессию PD-L1
Т-лимфоцитов
[108]. Ингибиторные рецеп-
на Т-клетках [119]. Экспрессию PD-L2 на по-
торы начинают экспрессироваться на поверх-
верхности дендритных клеток и макрофагов
ности Т-клеток уже в момент их активации и
индуцируют цитокины IL-4 и IFN-γ [116]. При
обеспечивают баланс между эффективным
отсутствии лиганда ингибирующий сигнал с
иммунным ответом, с одной стороны, и защи-
PD-1 не поступает, и Т-клетки, распознавшие
той тканей от избыточного воспаления и пов-
чужеродный пептид, активируются, пролифе-
реждения - с другой [109].
рируют и реализуют эффекторные функции.
Среди ингибиторных рецепторов наиболее
Наиболее активно PD-1 и PD-L1 (его наи-
изучен рецептор программируемой клеточной
более изученный лиганд) экспрессируются
гибели 1 (англ. Programmed death-1 - PD-1).
в ситуациях, когда иммунная система стал-
Сигнал, поступающий с PD-1 при его взаи-
кивается с персистирующим антигеном: хро-
модействии с лигандами PD-L1 или PD-L2,
нические вирусные инфекции [120], развитие
подавляет пролиферацию, продукцию цито-
опухолей [116] и сепсис [121]. При этих забо-
кинов и цитолитическую функцию Т-лимфо-
леваниях прекращения иммунного ответа не
цитов, а также повышает их чувствительность к
происходит, Т-клетки продолжают контакти-
апоптозу [110, 111]. Угнетение функции Т-лим-
ровать с антигеном, а защитный механизм,
фоцитов вследствие сигнализации через PD-1
реализуемый ингибиторными рецепторами,
во многом обусловлено ее влиянием на кле-
приобретает патологический характер. Про-
точный метаболизм. Установлено, что после
должительный контакт с антигеном приводит
взаимодействия PD-1 с лигандом подавляется
к тому, что специфичные Т-лимфоциты на-
прохождение сигнала через фосфатидилино-
чинают экспрессировать как рецептор PD-1,
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2261
так и другие ингибиторные молекулы - Tim-3,
дит к снижению их пролиферативного потен-
Lag-3, CTLA-4 и TIGIT [27]. Вместе с тем та-
циала, угнетению продукции эффекторных
кие клетки постепенно утрачивают способ-
цитокинов и повышению экспрессии инги-
ность производить цитокины (в частности,
биторных молекул PD-1 и LAG-3 [129]. Кроме
IFN-γ) и делиться [122]. В литературе Т-лим-
того, экспериментально вызванное нарушение
фоциты, утратившие функции вследствие про-
функции митохондрий в CD8+ Т-лимфоцитах
должительного контакта с антигеном, называ-
приводит к изменению структуры хромати-
ют истощенными. При хронических вирусных
на [129]. При этом эпигенетические измене-
инфекциях [9], сепсисе [123] и развитии опу-
ния, протекающие в этих клетках, сходны с
холей [124] количество истощенных Т-клеток
таковыми в истощенных CD8+ Т-лимфоцитах.
значительно возрастает. При этом накопление
Представленные данные свидетельствуют о
малофункциональных Т-лимфоцитов, специ-
том, что CD8+ Т-клетки с нарушением функ-
фичных к антигену, нередко способствует про-
ции митохондрий могут переходить в исто-
грессии заболевания [125].
щенное состояние даже при отсутствии перси-
Помимо конститутивной экспрессии ин-
стирующего антигена.
гибиторных рецепторов, истощенные Т-клет-
Механизм, приводящий к истощению кле-
ки также отличаются от функционально ак-
ток с митохондриальной дисфункцией, до сих
тивных Т-лимфоцитов нарушением работы
пор неизвестен. Тем не менее предполагается,
митохондрий. Установлено, что в истощенных
что влияние митохондрий на эпигенетический
CD8+ Т-клетках аккумулируются деполяри-
ландшафт клеток имеет определяющее значе-
зованные митохондрии с низкой интенсив-
ние в развитии данного процесса [10]. В на-
ностью окислительного фосфорилирования
стоящий момент общепризнано, что митохон-
и продукции ATP [126]. Кроме того, в исто-
дрии могут активно влиять на генетический
щенных CD8+ Т-лимфоцитах нарушается про-
аппарат клетки [132]. При этом существенную
цесс слияния митохондрий [127], подавляют-
роль в регуляции со стороны митохондрий
ся процессы, связанные с активностью тран-
играют продукты ЦТК, задействованные в
скрипционного фактора PGC-1α [128], и ми-
модификации ДНК и гистонов [133]. Так, для
тофагия [129]. В совокупности эти изменения
процессов ацетилирования необходим ацетил-
приводят к угнетению антиоксидантных про-
КоА, источником которого являются ацетил-
цессов и накоплению активных форм кисло-
карнитин и лимонная кислота, транспорти-
рода (АФК). Предполагается, что аккумуля-
руемые из митохондрий [134]. В связи с этим
ция АФК прямо связана с изменениями в
нарушение функции митохондрий способно
структуре хроматина, которые приводят к тер-
привести к сокращению пула ацетил-КоА,
минальному истощению Т-лимфоцитов [130].
гипоацетилированию гистонов и изменению
Так, было показано, что интратуморальное
профиля экспрессируемых генов [135]. Пока-
или пероральное введение никотинамид ри-
зано, что недостаток ацетил-КоА нарушал
бозида - предшественника NAD - стиму-
ацетилирование гистона H3 в локусе Ifng и
лирует митофагию, снижает уровень АФК в
блокировал продукцию IFN-γ в CD4+ Т-лим-
CD8+ Т-клетках, инфильтрирующих опухоль,
фоцитах [136]. Как отмечалось ранее, утрата
а также повышает их активность против рака
способности продуцировать IFN-γ является
прямой кишки и меланомы мыши [129]. При-
одним из основных признаков истощения
менение метформина для снижения уровня
Т-клеток.
АФК в CD8+ Т-лимфоцитах, находящихся
Помимо ацетилирования, митохондрии
в гипоксическом микроокружении опухоли,
также способны влиять на уровень метили-
также приводит к повышению их функцио-
рования ДНК и гистонов. Показано, что на-
нальной активности и снижению экспрессии
рушение функции митохондрий приводит
рецептора PD-1 [131].
к существенному изменению расположе-
Примечательно, что угнетение функции
ния метильных групп и уровня транскрип-
митохондрий не только является неотъемле-
ции целого ряда генов
[137]. Связь между
мой чертой истощенных CD8+ Т-клеток, но
митохондриями и метилированием генетиче-
и само по себе может привести к истощению
ского материала обусловлена тем, что фермен-
Т-лимфоцитов. Так, было показано, что инду-
ты-деметилазы Jmjd3 (англ. Jumonji domain-
цированное накопление деполяризованных
containing protein-3
- белок 3, содержащий
митохондрий в CD8+ Т-клетках, инкубиро-
домен Jumonji) и TET (англ. ten-eleven translo-
ванных в присутствии олигомицина и Mdivi-1
cation - белки с транслокацией десять-один-
(англ. mitochondrial division inhibitor 1 - инги-
надцать) требуют присутствия α-кетоглутаро-
битор митохондриального деления 1), приво-
вой кислоты для своей активности [138, 139].
БИОХИМИЯ том 88 вып. 11 2023
2262
ВЛАСОВА, ШМАГЕЛЬ
При этом другие производные ЦТК - янтарная
ли. Таким образом, терапевтические стратегии
и фумаровая кислоты - угнетают активность
для лечения опухолей, совмещающие анти-
данных ферментов
[140, 141]. Примечатель-
тела анти-PD-1/PD-L1 и фармакологические
но, что CD8+ Т-лимфоциты, культивируемые
регуляторы клеточного метаболизма, требуют
при отсутствии глутамина или в присутствии
дальнейшего детального изучения.
ингибиторов глутаминолиза, сохраняют свою
функциональную активность даже при пер-
систирующем контакте с антигеном: такие
ЗАКЛЮЧЕНИЕ
клетки активно пролиферируют и оказыва-
ют противоопухолевую активность, а также
Сведения, представленные в настоящей
экспрессируют PD-1 на относительно низ-
работе, демонстрируют, что на всех этапах
ком уровне [142]. Добавление α-кетоглутарата
жизненного цикла - с момента активации до
в среду с дефицитом глутамина возвращает
формирования иммунологической памяти -
CD8+ Т-клеткам истощенный фенотип [143].
метаболизм и функции Т-лимфоцитов взаимо-
По-видимому, снижение внутриклеточного пу-
связаны. Эта связь сохраняется и в том случае,
ла α-кетоглутаровой кислоты препятствует
когда функциональная активность Т-клеток
изменению экспрессии генов, регулирующих
снижается для завершения иммунного ответа
процесс истощения Т-лимфоцитов.
или вследствие истощения. Препараты, на-
Таким образом, установлено, что ингиби-
правленные на изменение обменных процес-
торные рецепторы и PD-1, в частности, изме-
сов, активно применяются при лечении сер-
няют метаболизм Т-клеток, что отражается
дечно-сосудистых заболеваний [147]. Кроме
на их функции: подавляется активация, про-
того, в последние годы значительно возросло
лиферация и продукция цитокинов. Но спра-
число ингибиторов, агонистов метаболических
ведливо и обратное - метаболические сдвиги
путей и антиметаболитов, которые проходят
индуцируют экспрессию PD-1 и, таким обра-
клинические испытания в качестве противо-
зом, ингибируют функциональную активность
опухолевых препаратов либо уже используют-
Т-клеток. Двусторонняя связь между нару-
ся для терапии рака [148]. Вместе с тем пред-
шением работы митохондрий и истощением
ставленные сведения требуют повышенного
Т-лимфоцитов указывает на то, что нормализа-
внимания к побочным эффектам, которые ре-
ция Т-клеточного метаболизма может усилить
гуляторы метаболизма могут оказывать на им-
иммунный ответ на персистирующий антиген.
мунную систему. Возможные эффекты данных
Представленные сведения могут быть осо-
препаратов на метаболизм и функциональную
бенно актуальны для разработки противоопу-
активность иммунных клеток (как позитив-
холевых препаратов. В настоящий момент для
ные, так и негативные) требуют дальнейшего
снижения уровня истощения в пуле Т-лимфо-
детального изучения.
цитов, инфильтрирующих опухоль, приме-
Важно отметить, что обратной стороной
няют различные виды терапии, основанной
зависимости между функцией Т-лимфоцитов
на антителах анти-PD-1/PD-L1. Преимуще-
и их метаболизмом является возможность на-
ствами ингибиторов сигнального пути PD-1/
правлять функциональную активность Т-кле-
PD-L1 являются относительная безопасность
ток путем изменения обменных процессов.
и эффективность в отношении прогрессирую-
Так, было показано, что ингибиторы и агони-
щих опухолей [144]. Тем не менее в ряде случа-
сты метаболических путей способны подав-
ев вероятность полной ремиссии при приеме
лять пролиферацию Т-клеток, изменять на-
антител анти-PD-1 или анти-PD-L1 остается
правление их дифференцировки, угнетать или
невысокой и значительно зависит от типа опу-
стимулировать формирование иммунологиче-
холи и индивидуальных характеристик паци-
ской памяти, а также препятствовать истоще-
ента [145]. Можно предположить, что норма-
нию специфичных к антигену клеток. В сово-
лизация функции митохондрий Т-лимфоцитов
купности эти данные указывают на то, что
дополнит действие ингибиторов данного сиг-
препараты, воздействующие на метаболизм
нального пути и сделает лечение более эффек-
Т-лимфоцитов, обладают большим потенциа-
тивным. К настоящему моменту известна одна
лом в контроле иммунных реакций [149].
работа, проверяющая и подтверждающая эту
Дальнейшее развитие этого направления,
гипотезу. Chowdhury et al. [146] показали, что
безусловно, потребует проведения большого
агонист транскрипционного фактора PGC-1α
количества широкомасштабных исследований.
безафибрат усиливает функцию митохондрий
До сих пор мало известно о том, как ингиби-
в CD8+ Т-лимфоцитах и повышает активность
торы и агонисты метаболических путей воз-
антител анти-PD-1 в модели мышиной опухо-
действуют на неиммунные клетки организма,
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2263
в том числе эпителий кишечника, клетки пе-
мирование концепции обзора, руководство,
чени, миоциты и β-клетки поджелудочной
редактирование текста статьи.
железы, отличающиеся высокой активностью
Финансирование. Исследование выпол-
обменных процессов. Более того, неизвестно,
нено в рамках государственного задания
какие компенсаторные реакции эти препараты
«Роль метаболизма CD4+ Т-клеток памя-
вызовут в самих клетках-мишенях. Изучение
ти в нарушении регенерации иммунитета у
неспецифических, перекрестных и компен-
ВИЧ-инфицированных пациентов на фоне
саторных эффектов соединений, способных
антиретровирусной терапии» (номер гос-
воздействовать на метаболизм Т-лимфоцитов,
регистрации темы: 121112500044-9) и государ-
потребует усилий большого количества иссле-
ственного задания
«Механизмы регуляции
дователей. Тем не менее эта большая работа
иммунной системы» (номер госрегистрации
откроет многообещающую перспективу - ре-
темы: АААА-А19-119112290007-7).
альный путь к терапевтическому воздействию
Конфликт интересов. Авторы заявляют об
на отдельные звенья иммунной системы.
отсутствии конфликта интересов.
Соблюдение этических норм. Настоящая
Вклад авторов: Власова В.В. - анализ ли-
статья не содержит описания каких-либо ис-
тературных данных, написание текста статьи,
следований с участием людей или животных
подготовка рисунков; Шмагель К.В. - фор-
в качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1.
Ghosh-Choudhary, S., Liu, J., and Finkel, T. (2020)
9.
Barili, V., Fisicaro, P., Montanini, B., Acerbi, G.,
Metabolic regulation of cell fate and function, Trends
Filippi, A., Forleo, G., Romualdi, C., Ferracin, M.,
Cell Biol., 30, 201-212, doi: 10.1016/j.tcb.2019.12.005.
Guerrieri, F., Pedrazzi, G., Boni, C., Rossi, M.,
2.
Gerriets, V. A., and Rathmell, J. C. (2012) Metabolic
Vecchi, A., Penna, A., Zecca, A., Mori, C.,
pathways in T cell fate and function, Trends Immunol.,
Orlandini, A., Negri, E., Pesci, M., Massari, M.,
33, 168-173, doi: 10.1016/j.it.2012.01.010.
Missale, G., Levrero, M., Ottonello, S., and Ferrari, C.
3.
Sallusto, F., Lanzavecchia, A., Araki, K., and
(2020) Targeting p53 and histone methyltransferases
Ahmed, R.
(2010) From vaccines to memory
restores exhausted CD8+ T cells in HCV infection, Nat.
and back, Immunity,
33,
451-463, doi:
10.1016/
Commun., 11, 604, doi: 10.1038/s41467-019-14137-7.
j.immuni.2010.10.008.
10.
Franco, F., Jaccard, A., Romero, P., Yu, Y.-R., and
4.
Bettelli, E., Korn, T., and Kuchroo, V. K. (2007)
Ho, P.-C. (2020) Metabolic and epigenetic regulation
Th17: the third member of the effector T cell trilogy,
of T-cell exhaustion, Nat. Metab.,
2,
1001-1012,
Curr. Opin. Immunol., 19, 652-657, doi: 10.1016/
doi: 10.1038/s42255-020-00280-9.
j.coi.2007.07.020.
11.
Burnet, F. M.
(1976) A modification of Jerne’s
5.
Sakaguchi, S.
(2004) Naturally arising CD4+
theory of antibody production using the concept of
regulatory T cells for immunologic self-tolerance
clonal selection, CA Cancer J. Clin., 26, 119-121,
and negative control of immune responses, Annu.
doi: 10.3322/canjclin.26.2.119.
Rev. Immunol., 22, 531-562, doi: 10.1146/annurev.
12.
Wang, R., and Green, D. R.
(2012) Metabolic
immunol.21.120601.141122.
checkpoints in activated T cells, Nat. Immunol., 13,
6.
Van der Windt, G. J. W., O’Sullivan, D., Everts, B.,
907-915, doi: 10.1038/ni.2386.
Huang, S. C.-C., Buck, M. D., Curtis, J. D., Chang,
13.
Patel, D., Salloum, D., Saqcena, M., Chatterjee, A.,
C. H., Smith, A. M., Ai, T., Faubert, B., Jones, R. G.,
Mroz, V., Ohh, M., and Foster, D. A. (2017) A late
Pearce, E. J., and Pearce, E. L. (2013) CD8 memory
G1 lipid checkpoint that is dysregulated in clear cell
T cells have a bioenergetic advantage that underlies
renal carcinoma cells, J. Biol. Chem., 292, 936-944,
their rapid recall ability, Proc. Natl. Acad. Sci. USA,
doi: 10.1074/jbc.M116.757864.
110, 14336-14341, doi: 10.1073/pnas.1221740110.
14.
Pelletier, J., Riaño-Canalias, F., Almacellas, E.,
7.
Barbi, J., Pardoll, D., and Pan, F. (2013) Metabolic
Mauvezin, C., Samino, S., Feu, S., Menoyo, S.,
control of the Treg/Th17 axis, Immunol. Rev., 252,
Domostegui, A., Garcia-Cajide, M., Salazar, R.,
52-77, doi: 10.1111/imr.12029.
Cortés, C., Marcos, R., Tauler, A., Yanes, O., Agell, N.,
8.
Pennock, N. D., White, J. T., Cross, E. W., Cheney,
Kozma, S. C., Gentilella, A., and Thomas, G.
E. E., Tamburini, B. A., and Kedl, R. M. (2013) T cell
(2020) Nucleotide depletion reveals the impaired
responses: naive to memory and everything in between,
ribosome biogenesis checkpoint as a barrier against
Adv. Physiol. Educ.,
37,
273-283, doi:
10.1152/
DNA damage, EMBO J., 39, e103838, doi: 10.15252/
advan.00066.2013.
embj.2019103838.
БИОХИМИЯ том 88 вып. 11 2023
2264
ВЛАСОВА, ШМАГЕЛЬ
15.
Pardee, A. B. (1974) A restriction point for control of
27.
Catakovic, K., Klieser, E., Neureiter, D., and
normal animal cell proliferation, Proc. Natl. Acad. Sci.
Geisberger, R.
(2017) T cell exhaustion: from
USA, 71, 1286-1290, doi: 10.1073/pnas.71.4.1286.
pathophysiological basics to tumor immunotherapy,
16.
Ge, T., Yang, J., Zhou, S., Wang, Y., Li, Y., and
Cell Commun. Signal., 15, 1, doi: 10.1186/s12964-
Tong, X. (2020) The role of the pentose phosphate
016-0160-z.
pathway in diabetes and cancer, Front. Endocrinol.,
28.
Trentham, D. R. (1971) Rate-determining processes
11, 365, doi: 10.3389/fendo.2020.00365.
and the number of simultaneously active sties of
17.
Reid, M. A., Allen, A. E., Liu, S., Liberti, M. V., Liu, P.,
D-glyceraldehyde
3-phosphate
dehydrogenase,
Liu, X., Lai, L., and Locasale, J. W. (2018) Serine syn-
Biochem. J., 122, 71-77, doi: 10.1042/bj1220071.
thesis through PHGDH coordinates nucleotide levels
29.
Lemire, J., Mailloux, R. J., and Appanna, V. D. (2008)
by maintaining central carbon metabolism, Nat. Com-
Mitochondrial lactate dehydrogenase is involved in
mun., 9, 5442, doi: 10.1038/s41467-018-07868-6.
oxidative-energy metabolism in human astrocytoma
18.
Grassian, A. R., Metallo, C. M., Coloff, J. L.,
cells (CCF-STTG1), PLoS One, 3, e1550, doi: 10.1371/
Stephanopoulos, G., and Brugge, J. S. (2011) Erk
journal.pone.0001550.
regulation of pyruvate dehydrogenase flux through
30.
Wang, R., Dillon, C. P., Shi, L. Z., Milasta, S.,
PDK4 modulates cell proliferation, Genes Dev., 25,
Carter, R., Finkelstein, D., McCormick, L. L.,
1716-1733, doi: 10.1101/gad.16771811.
Fitzgerald, P., Chi, H., Munger, J., and Green,
19.
Lee, J., and Ridgway, N. D.
(2020) Substrate
D. R. (2011) The transcription factor Myc con-
channeling in the glycerol-3-phosphate pathway
trols metabolic reprogramming upon T lympho-
regulates the synthesis, storage and secretion of
cyte activation, Immunity, 35, 871-882, doi: 10.1016/
glycerolipids, Biochim. Biophys. Acta Mol. Cell Biol.
j.immuni.2011.09.021.
Lipids, 1865, 158438, doi: 10.1016/j.bbalip.2019.03.010.
31.
Chapman, N. M., Boothby, M. R., and Chi, H.
20.
Dimeloe, S., Burgener, A.-V., Grählert, J., and
(2020) Metabolic coordination of T cell quiescence
Hess, C. (2017) T-cell metabolism governing activa-
and activation, Nat. Rev. Immunol.,
20,
55-70,
tion, proliferation and differentiation; a modular view,
doi: 10.1038/s41577-019-0203-y.
Immunology, 150, 35-44, doi: 10.1111/imm.12655.
32.
Jones, N., Vincent, E. E., Cronin, J. G., Panetti, S.,
21.
Adeva-Andany, M., López-Ojén, M., Funcasta-
Chambers, M., Holm, S. R., Owens, S. E., Francis,
Calderón, R., Ameneiros-Rodríguez, E., Donapetry-
N. J., Finlay, D. K., and Thornton, C. A. (2019)
García, C., Vila-Altesor, M., and Rodríguez-Seijas, J.
Akt and STAT5 mediate naïve human CD4+ T-cell
(2014) Comprehensive review on lactate metabolism
early metabolic response to TCR stimulation, Nat.
in human health, Mitochondrion,
17,
76-100,
Commun., 10, 2042, doi: 10.1038/s41467-019-10023-4.
doi: 10.1016/j.mito.2014.05.007.
33.
Czibik, G., Steeples, V., Yavari, A., and Ashrafian, H.
22.
Grist, J. T., Jarvis, L. B., Georgieva, Z., Thompson, S.,
(2014) Citric acid cycle intermediates in cardioprotec-
Kaur Sandhu, H., Burling, K., Clarke, A., Jackson, S.,
tion, Circ. Cardiovasc. Genet., 7, 711-719, doi: 10.1161/
Wills, M., Gallagher, F. A., and Jones, J. L. (2018)
CIRCGENETICS.114.000220.
Extracellular lactate: a novel measure of T cell prolif-
34.
Palmieri, F. (2004) The mitochondrial transporter
eration, J. Immunol., 200, 1220-1226, doi: 10.4049/
family (SLC25): physiological and pathological
jimmunol.1700886.
implications, Pflug. Arch. Eur. J. Physiol.,
447,
23.
Hume, D. A., Radik, J. L., Ferber, E., and Weide-
689-709, doi: 10.1007/s00424-003-1099-7.
mann, M. J. (1978) Aerobic glycolysis and lympho-
35.
Saggerson, D. (2008) Malonyl-CoA, a key signaling
cyte transformation, Biochem. J.,
174,
703-709,
molecule in mammalian cells, Annu. Rev. Nutr., 28,
doi: 10.1042/bj1740703.
253-272, doi: 10.1146/annurev.nutr.28.061807.155434.
24.
DeBerardinis, R. J., Mancuso, A., Daikhin, E.,
36.
Huang, B., Song, B.-L., and Xu, C. (2020) Cholesterol
Nissim, I., Yudkoff, M., Wehrli, S., and Thompson,
metabolism in cancer: mechanisms and therapeutic
C. B. (2007) Beyond aerobic glycolysis: transformed
opportunities, Nat. Metab., 2, 132-141, doi: 10.1038/
cells can engage in glutamine metabolism that exceeds
s42255-020-0174-0.
the requirement for protein and nucleotide synthesis,
37.
Ahn, C. S., and Metallo, C. M. (2015) Mitochondria
Proc. Natl. Acad. Sci. USA,
104,
19345-19350,
as biosynthetic factories for cancer proliferation,
doi: 10.1073/pnas.0709747104.
Cancer Metab., 3, 1, doi: 10.1186/s40170-015-0128-2.
25.
Lunt, S. Y., and Vander Heiden, M. G. (2011) Aerobic
38.
Carr, E. L., Kelman, A., Wu, G. S., Gopaul, R.,
glycolysis: meeting the metabolic requirements of cell
Senkevitch, E., Aghvanyan, A., Turay, A. M., and
proliferation, Annu. Rev. Cell Dev. Biol., 27, 441-464,
Frauwirth, K. A.
(2010) Glutamine uptake and
doi: 10.1146/annurev-cellbio-092910-154237.
metabolism are coordinately regulated by ERK/
26.
Vander Heiden, M. G., Cantley, L. C., and Thompson,
MAPK during T lymphocyte activation, J. Immunol.,
C. B. (2009) Understanding the Warburg effect: the
185, 1037-1044, doi: 10.4049/jimmunol.0903586.
metabolic requirements of cell proliferation, Science,
39.
DeBerardinis, R. J., and Cheng, T. (2010) Q’s next:
324, 1029-1033, doi: 10.1126/science.1160809.
the diverse functions of glutamine in metabolism,
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2265
cell biology and cancer, Oncogene,
29,
313-324,
Rabinowitz, J. D., Sharpe, A. H., and Haigis, M. C.
doi: 10.1038/onc.2009.358.
(2016) Mitochondrial biogenesis and proteome
40.
Skaper, S. D., O’Brien, W. E., and Schafer, I. A. (1978)
remodeling promote one-carbon metabolism for T cell
The influence of ammonia on purine and pyrimidine
activation, Cell Metab., 24, 104-117, doi: 10.1016/
nucleotide biosynthesis in rat liver and brain in vitro,
j.cmet.2016.06.007.
Biochem. J., 172, 457-464, doi: 10.1042/bj1720457.
53.
Grumont, R., Lock, P., Mollinari, M., Shannon,
41.
Young, V. R., and Ajami, A. M. (2001) Glutamine:
F. M., Moore, A., and Gerondakis, S. (2004) The mi-
the emperor or his clothes? J. Nutr., 131, 2449-2459,
togen-induced increase in T cell size involves PKC
doi: 10.1093/jn/131.9.2449S.
and NFAT activation of Rel/NF-kappaB-dependent
42.
Tretter, L., and Adam-Vizi, V.
(2005) Alpha-
c-myc expression, Immunity, 21, 19-30, doi: 10.1016/
ketoglutarate dehydrogenase: a target and generator of
j.immuni.2004.06.004.
oxidative stress, Philos. Trans. R. Soc., 360, 2335-2345,
54.
Obst, R. (2015) The timing of T cell priming and
doi: 10.1098/rstb.2005.1764.
cycling, Front. Immunol., 6, 563, doi: 10.3389/fimmu.
43.
Xie, N., Zhang, L., Gao, W., Huang, C., Huber,
2015.00563.
P. E., Zhou, X., Li, C., Shen, G., and Zou, B. (2020)
55.
Hommel, M., and Kyewski, B.
(2003) Dynamic
NAD+ metabolism: pathophysiologic mechanisms and
changes during the immune response in T cell-
therapeutic potential, Signal Transduction Targeted
antigen-presenting cell clusters isolated from lymph
Ther., 5, 227, doi: 10.1038/s41392-020-00311-7.
nodes, J. Exp. Med., 197, 269-280, doi: 10.1084/
44.
Akie, T. E., Liu, L., Nam, M., Lei, S., and Cooper,
jem.20021512.
M. P.
(2015) OXPHOS-mediated induction of
56.
Tan, S. Y., Kelkar, Y., Hadjipanayis, A., Shipstone, A.,
NAD+ promotes complete oxidation of fatty ac-
Wynn, T. A., and Hall, J. P. (2020) Metformin and
ids and interdicts non-alcoholic fatty liver disease,
2-deoxyglucose collaboratively suppress human CD4+
PLoS One, 10, e0125617, doi: 10.1371/journal.pone.
T cell effector functions and activation-induced
0125617.
metabolic reprogramming, J. Immunol., 205, 957-967,
45.
Yao, C.-H., Wang, R., Wang, Y., Kung, C.-P., Weber,
doi: 10.4049/jimmunol.2000137.
J. D., and Patti, G. J. (2019) Mitochondrial fusion
57.
Macintyre, A. N., Gerriets, V. A., Nichols, A. G.,
supports increased oxidative phosphorylation during
Michalek, R. D., Rudolph, M. C., Deoliveira, D.,
cell proliferation, ELife, 8, e41351, doi: 10.7554/
Anderson. S. M., Abel, E. D., Chen, B. J., Hale, L. P.,
eLife.41351.
and Rathmell, J. C. (2014) The glucose transporter
46.
Birsoy, K., Wang, T., Chen, W. W., Freinkman, E.,
Glut1 is selectively essential for CD4 T cell activation
Abu-Remaileh, M., and Sabatini, D. M.
(2015)
and effector function, Cell Metab.,
20,
61-72,
An essential role of the mitochondrial electron
doi: 10.1016/j.cmet.2014.05.004.
transport chain in cell proliferation is to enable
58.
Nian, Y., Iske, J., Maenosono, R., Minami, K.,
aspartate synthesis, Cell, 162, 540-551, doi: 10.1016/
Heinbokel, T., Quante, M., Liu, Y., Azuma, H.,
j.cell.2015.07.016.
Yang, J., Abdi, R., Zhou, H., Elkhal, A., and Tullius,
47.
Pan, S., Fan, M., Liu, Z., Li, X., and Wang, H. (2021)
S. G. (2021) Targeting age-specific changes in CD4+
Serine, glycine and one-carbon metabolism in cancer,
T cell metabolism ameliorates alloimmune responses
Int. J. Oncol., 58, 158-170, doi: 10.3892/ijo.2020.5158.
and prolongs graft survival, Aging Cell, 20, e13299,
48.
Tong, X., Zhao, F., and Thompson, C. B. (2009)
doi: 10.1111/acel.13299.
The molecular determinants of de novo nucleotide
59.
Chen, X., Sunkel, B., Wang, M., Kang, S., Wang, T.,
biosynthesis in cancer cells, Curr. Opin. Genet. Dev.,
Gnanaprakasam, J. N. R., Liu, L., Cassel, T. A., Scott,
19, 32-37, doi: 10.1016/j.gde.2009.01.002.
D. A., Muñoz-Cabello, A. M., Lopez-Barneo, J.,
49.
Baggott, J. E., and Tamura, T.
(2015) Folate-
Yang, J., Lane, A. N., Xin, G., Stanton, B. Z., Fan,
dependent purine nucleotide biosynthesis in humans,
T. W., and Wang, R. (2022) Succinate dehydrogenase/
Adv. Nutr., 6, 564-571, doi: 10.3945/an.115.008300.
complex II is critical for metabolic and epigenetic
50.
Van der Veen, J. N., Kennelly, J. P., Wan, S., Vance,
regulation of T cell proliferation and inflammation,
J. E., Vance, D. E., and Jacobs, R. L. (2017) The crit-
Sci. Immunol., 7, eabm8161, doi: 10.1126/sciimmunol.
ical role of phosphatidylcholine and phosphatidy-
abm8161.
lethanolamine metabolism in health and disease,
60.
Ma, E. H., Bantug, G., Griss, T., Condotta, S.,
Biochim. Biophys. Acta Biomembr., 1859, 1558-1572,
Johnson, R. M., Samborska, B., Mainolfi, N.,
doi: 10.1016/j.bbamem.2017.04.006.
Suri, V., Guak, H., Balmer, M. L., Verway, M. J.,
51.
Finkelstein, J. D.
(1990) Methionine metabo-
Raissi, T. C., Tsui, H., Boukhaled, G., Henriques da
lism in mammals, J. Nutr. Biochem., 1, 228-237,
Costa, S., Frezza, C., Krawczyk, C. M., Friedman, A.,
doi: 10.1016/0955-2863(90)90070-2.
Manfredi, M., Richer, M. J., Hess, C., and Jones,
52.
Ron-Harel, N., Santos, D., Ghergurovich, J. M.,
R. G. (2017) Serine is an essential metabolite for
Sage, P. T., Reddy, A., Lovitch, S. B., Dephoure, N.,
effector T cell expansion, Cell Metab., 25, 345-357,
Satterstrom, F. K., Sheffer, M., Spinelli, J. B., Gygi, S.,
doi: 10.1016/j.cmet.2016.12.011.
БИОХИМИЯ том 88 вып. 11 2023
2266
ВЛАСОВА, ШМАГЕЛЬ
61.
Caro-Maldonado, A., Wang, R., Nichols, A. G.,
Th17 cells by fatty acid synthesis and glycolysis, Front.
Kuraoka, M., Milasta, S., Sun, L. D., Gavin, A. L.,
Immunol., 10, 115, doi: 10.3389/fimmu.2019.00115.
Abel, E. D., Kelsoe, G., Green, D. R., and Rathmell,
71.
Wang, H., Teng, X., Abboud, G., Li, W., Ye, S., and
J. C. (2014) Metabolic reprogramming is required for
Morel, L. (2021) D-mannose ameliorates autoimmune
antibody production that is suppressed in anergic but
phenotypes in mouse models of lupus, BMC Immunol.,
exaggerated in chronically BAFF-exposed B cells,
22, 1, doi: 10.1186/s12865-020-00392-7.
J. Immunol., 192, 3626-3636, doi: 10.4049/jimmunol.
72.
Angiari, S., Runtsch, M. C., Sutton, C. E., Palsson-
1302062.
McDermott, E. M., Kelly, B., Rana, N., Kane, H.,
62.
Kim, J., Kim, Y.-S., and Park, S.-H. (2021) Metformin
Papadopoulou, G., Pearce, E. L., Mills, K. H. G., and
as a treatment strategy for Sjögren’s syndrome, Int. J.
O’Neill, L. A. J. (2020) Pharmacological activation of
Mol. Sci., 22, 7231, doi: 10.3390/ijms22137231.
pyruvate kinase M2 inhibits CD4+ T cell pathogenicity
63.
Påhlman, C., Qi, Z., Murray, C. M., Ferguson, D.,
and suppresses autoimmunity, Cell Metab.,
31,
Bundick, R. V., Donald, D. K., and Ekberg, H. (2013)
391-405, doi: 10.1016/j.cmet.2019.10.015.
Immunosuppressive properties of a series of novel
73.
Xu, K., Yin, N., Peng, M., Stamatiades, E. G.,
inhibitors of the monocarboxylate transporter MCT-1,
Chhangawala, S., Shyu, A., Li, P., Zhang, X., Do,
Transplant Int., 26, 22-29, doi: 10.1111/j.1432-2277.
M. H., Capistrano, K. J., Chou, C., Leslie, C. S.,
2012.01579.x.
and Li, M. O. (2021) Glycolytic ATP fuels phos-
64.
Berod, L., Friedrich, C., Nandan, A., Freitag, J.,
phoinositide 3-kinase signaling to support effector
Hagemann, S., Harmrolfs, K., Sandouk, A.,
T helper 17 cell responses, Immunity, 54, 976-987,
Hesse, C., Castro, C. N., Bähre, H., Tschirner, S. K.,
doi: 10.1016/j.immuni.2021.04.008.
Gorinski, N., Gohmert, M., Mayer, C. T., Huehn, J.,
74.
Pandit, M., Timilshina, M., and Chang, J.-H.
Ponimaskin, E., Abraham, W. R., Müller, R.,
(2021) LKB1-PTEN axis controls Th1 and Th17 cell
Lochner, M., and Sparwasser, T. (2014) De novo fatty
differentiation via regulating mTORC1, J. Mol. Med.,
acid synthesis controls the fate between regulatory
99, 1139-1150, doi: 10.1007/s00109-021-02090-2.
T and T helper 17 cells, Nat. Med., 20, 1327-1333,
75.
Miska, J., Lee-Chang, C., Rashidi, A., Muroski,
doi: 10.1038/nm.3704.
M. E., Chang, A. L., Lopez-Rosas, A., Zhang, P.,
65.
Littman, D. R., and Rudensky, A. Y. (2010) Th17
Panek, W. K., Cordero, A., Han, Y., Ahmed, A. U.,
and regulatory T cells in mediating and restraining
Chandel, N. S., and Lesniak, M. S. (2019) HIF-1α
inflammation, Cell,
140,
845-858, doi:
10.1016/
is a metabolic switch between glycolytic-driven mi-
j.cell.2010.02.021.
gration and oxidative phosphorylation-driven immu-
66.
Singh, R. P., Hasan, S., Sharma, S., Nagra, S.,
nosuppression of Tregs in glioblastoma, Cell Rep., 27,
Yamaguchi, D. T., Wong, D. T., Hahn, B. H., and
226-237, doi: 10.1016/j.celrep.2019.03.029.
Hossain, A. (2014) Th17 cells in inflammation and
76.
Chen, X., Li, S., Long, D., Shan, J., and Li, Y. (2021)
autoimmunity, Autoimmun. Rev.,
13,
1174-1181,
Rapamycin facilitates differentiation of regulato-
doi: 10.1016/j.autrev.2014.08.019.
ry T cells via enhancement of oxidative phosphor-
67.
Ohue, Y., and Nishikawa, H.
(2019) Regulatory
ylation, Cell. Immunol., 365, 104378, doi: 10.1016/
T (Treg) cells in cancer: Can Treg cells be a new
j.cellimm.2021.104378.
therapeutic target? Cancer Sci.,
110,
2080-2089,
77.
Qin, J., Liu, Q., Liu, A., Leng, S., Wang, S., Li, C.,
doi: 10.1111/cas.14069.
Ma, J., Peng, J., and Xu, M. (2022) Empagliflozin
68.
Gerriets, V. A., Kishton, R. J., Nichols, A. G.,
modulates CD4+ T-cell differentiation via metabolic
Macintyre, A. N., Inoue, M., Ilkayeva, O., Winter,
reprogramming in immune thrombocytopenia, British
P. S., Liu, X., Priyadharshini, B., Slawinska,
Br. J. Haematol., 198, 765-775, doi: 10.1111/bjh.18293.
M. E., Haeberli, L., Huck, C., Turka, L. A., Wood,
78.
Gualdoni, G. A., Mayer, K. A., Göschl, L.,
K. C., Hale, L. P., Smith, P. A., Schneider, M. A.,
Boucheron, N., Ellmeier, W., and Zlabinger, G. J.
MacIver, N. J., Locasale, J. W., Newgard, C. B.,
(2016) The AMP analog AICAR modulates the Treg/
Shinohara, M. L., and Rathmell, J. C. (2015) Met-
Th17 axis through enhancement of fatty acid oxidation,
abolic programming and PDHK1 control CD4+
FASEB J., 30, 3800-3809, doi: 10.1096/fj.201600522R.
T cell subsets and inflammation, J. Clin. Invest., 125,
79.
Field, C. S., Baixauli, F., Kyle, R. L., Puleston,
194-207, doi: 10.1172/JCI76012.
D. J., Cameron, A. M., Sanin, D. E., Hippen, K. L.,
69.
Shi, L. Z., Wang, R., Huang, G., Vogel, P., Neale, G.,
Loschi, M., Thangavelu, G., Corrado, M., Edwards-
Green, D. R., and Chi, H.
(2011) HIF1alpha-
Hicks, J., Grzes, K. M., Pearce, E. J., Blazar, B. R.,
dependent glycolytic pathway orchestrates a metabolic
and Pearce, E. L. (2020) Mitochondrial integrity
checkpoint for the differentiation of TH17 and Treg
regulated by lipid metabolism is a cell-intrinsic
cells, J. Exp. Med., 208, 1367-1376, doi: 10.1084/
checkpoint for Treg suppressive function, Cell Metab.,
jem.20110278.
31, 422-437, doi: 10.1016/j.cmet.2019.11.021.
70.
Cluxton, D., Petrasca, A., Moran, B., and Fletcher,
80.
Zhu, H., Liu, Z., An, J., Zhang, M., Qiu, Y., and
J. M. (2019) Differential regulation of human Treg and
Zou, M.-H. (2021) Activation of AMPKα1 is essential
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2267
for regulatory T cell function and autoimmune liver
in patients with systemic lupus erythematosus, Arthritis
disease prevention, Cell. Mol. Immunol., 18, 2609-
Rheum., 54, 2983-2988, doi: 10.1002/art.22085.
2617, doi: 10.1038/s41423-021-00790-w.
91.
Bruyn, G. A. W., Tate, G., Caeiro, F., Maldonado-
81.
Clambey, E. T., McNamee, E. N., Westrich, J. A.,
Cocco, J., Westhovens, R., Tannenbaum, H.,
Glover, L. E., Campbell, E. L., Jedlicka, P., de Zoeten,
Bell, M., Forre, O., Bjorneboe, O., Tak, P. P.,
E. F., Cambier, J. C., Stenmark, K. R., Colgan, S. P.,
Abeywickrama, K. H., Bernhardt, P., van Riel, P. L.,
and Eltzschig, H. K. (2012) Hypoxia-inducible factor-1
and RADD Study Group (2008) Everolimus in patients
alpha-dependent induction of FoxP3 drives regulatory
with rheumatoid arthritis receiving concomitant
T-cell abundance and function during inflammatory
methotrexate: a 3-month, double-blind, randomised,
hypoxia of the mucosa, Proc. Natl. Acad. Sci. USA,
placebo-controlled, parallel-group, proof-of-concept
109, 2784-2793, doi: 10.1073/pnas.1202366109.
study, Ann. Rheum. Dis., 67, 1090-1095, doi: 10.1136/
82.
Zeng, H., Yang, K., Cloer, C., Neale, G., Vogel, P.,
ard.2007.078808.
and Chi, H. (2013) mTORC1 couples immune signals
92.
Bachmann, M. F., Barner, M., Viola, A., and Kopf, M.
and metabolic programming to establish T(reg)-
(1999) Distinct kinetics of cytokine production and
cell function, Nature, 499, 485-490, doi: 10.1038/
cytolysis in effector and memory T cells after viral
nature12297.
infection, Eur. J. Immunol., 29, 291-299, doi: 10.1002/
83.
Allocco, J. B., and Alegre, M.-L. (2020) Exploiting
(SICI)1521-4141(199901)29:01<291::AID-IMMU291>
immunometabolism and T cell function for solid
3.0.CO;2-K.
organ transplantation, Cell. Immunol., 351, 104068,
93.
Park, B. V., and Pan, F. (2015) Metabolic regulation
doi: 10.1016/j.cellimm.2020.104068.
of T cell differentiation and function, Mol. Immunol.,
84.
Lopez-Olivo, M. A., Siddhanamatha, H. R., Shea, B.,
68, 497-506, doi: 10.1016/j.molimm.2015.07.027.
Tugwell, P., Wells, G. A., and Suarez-Almazor, M. E.
94.
Araki, K., Turner, A. P., Shaffer, V. O., Gangappa, S.,
(2014) Methotrexate for treating rheumatoid arthritis,
Keller, S. A., Bachmann, M. F., Larsen, C. P.,
Cochrane Database Syst. Rev.,
2014, CD000957,
and Ahmed, R. (2009) mTOR regulates memory
doi: 10.1002/14651858.CD000957.pub2.
CD8 T-cell differentiation, Nature, 460, 108-112,
85.
Lee, J.-U., Kim, L.-K., and Choi, J.-M. (2018) Revis-
doi: 10.1038/nature08155.
iting the concept of targeting NFAT to control T cell
95.
Sukumar, M., Liu, J., Ji, Y., Subramanian, M.,
immunity and autoimmune diseases, Front. Immunol.,
Crompton, J. G., Yu, Z., Roychoudhuri, R., Palmer,
9, 2747, doi: 10.3389/fimmu.2018.02747.
D. C., Muranski, P., Karoly, E. D., Mohney, R. P.,
86.
Gao, W., Lu, Y., El Essawy, B., Oukka, M., Kuchroo,
Klebanoff, C. A., Lal, A., Finkel, T., Restifo, N. P.,
V. K., and Strom, T. B. (2007) Contrasting effects of
and Gattinoni, L.
(2013) Inhibiting glycolytic
cyclosporine and rapamycin in de novo generation
metabolism enhances CD8+ T cell memory and
of alloantigen-specific regulatory T cells, Am. J.
antitumor function, J. Clin. Invest., 123, 4479-4488,
Transplant., 7, 1722-1732, doi: 10.1111/j.1600-6143.
doi: 10.1172/JCI69589.
2007.01842.x.
96.
Wenes, M., Jaccard, A., Wyss, T., Maldonado-
87.
Xu, T., Sun, D., Chen, Y., and Ouyang, L. (2020)
Pérez, N., Teoh, S. T., Lepez, A., Renaud, F.,
Targeting mTOR for fighting diseases: a revisited
Franco, F., Waridel, P., Yacoub Maroun, C.,
review of mTOR inhibitors, Eur. J. Med. Chem., 199,
Tschumi, B., Dumauthioz, N., Zhang, L., Donda, A.,
112391, doi: 10.1016/j.ejmech.2020.112391.
Martín, F., Migliorini, D., Lunt, S. Y., Ho, P. C., and
88.
Lai, Z.-W., Hanczko, R., Bonilla, E., Caza, T. N.,
Romero, P. (2022) The mitochondrial pyruvate carrier
Clair, B., Bartos, A., Miklossy, G., Jimah, J.,
regulates memory T cell differentiation and antitumor
Doherty, E., Tily, H., Francis, L., Garcia, R.,
function, Cell Metab., 34, 731-746, doi: 10.1016/
Dawood, M., Yu, J., Ramos, I., Coman, I., Faraone,
j.cmet.2022.03.013.
S. V., Phillips, P. E., and Perl, A. (2012) N-acetylcys-
97.
He, J., Shangguan, X., Zhou, W., Cao, Y., Zheng, Q.,
teine reduces disease activity by blocking mammalian
Tu, J., Hu, G., Liang, Z., Jiang, C., Deng, L.,
target of rapamycin in T cells from systemic lupus ery-
Wang, S., Yang, W., Zuo, Y., Ma, J., Cai, R.,
thematosus patients: a randomized, double-blind, pla-
Chen, Y., Fan, Q., Dong, B., Xue, W., Tan, H., Qi, Y.,
cebo-controlled trial, Arthritis Rheum., 64, 2937-2946,
Gu, J., Su, B., Eugene Chin, Y., Chen, G., Wang, Q.,
doi: 10.1002/art.34502.
Wang, T., and Cheng, J. (2021) Glucose limitation
89.
Walters, M. T., Rubin, C. E., Keightley, S. J.,
activates AMPK coupled SENP1-Sirt3 signalling in
Ward, C. D., and Cawley, M. I. (1986) A double-
mitochondria for T cell memory development, Nat.
blind, cross-over, study of oral N-acetylcysteine in
Commun., 12, 4371, doi: 10.1038/s41467-021-24619-2.
Sjögren’s syndrome, Scand. J. Rheumatol. Suppl., 61,
98.
Dumauthioz, N., Tschumi, B., Wenes, M., Marti, B.,
253-258.
Wang, H., Franco, F., Li, W., Lopez-Mejia, I. C.,
90.
Fernandez, D., Bonilla, E., Mirza, N., Niland, B., and
Fajas, L., Ho, P. C., Donda, A., Romero, P., and
Perl, A. (2006) Rapamycin reduces disease activity and
Zhang, L.
(2021) Enforced PGC-1α expression
normalizes T cell activation-induced calcium fluxing
promotes CD8 T cell fitness, memory formation
БИОХИМИЯ том 88 вып. 11 2023
2268
ВЛАСОВА, ШМАГЕЛЬ
and antitumor immunity, Cell. Mol. Immunol., 18,
cancer prevention and treatment, Biomaterials, 270,
1761-1771, doi: 10.1038/s41423-020-0365-3.
120678, doi: 10.1016/j.biomaterials.2021.120678.
99. Pearce, E. L., Walsh, M. C., Cejas, P. J., Harms,
108. Riva, A., and Chokshi, S. (2018) Immune checkpoint
G. M., Shen, H., Wang, L.-S., Jones, R. G., and
receptors: homeostatic regulators of immunity,
Choi, Y. (2009) Enhancing CD8 T-cell memory
Hepatol. Int.,
12,
223-236, doi:
10.1007/s12072-
by modulating fatty acid metabolism, Nature, 460,
018-9867-9.
103-107, doi: 10.1038/nature08097.
109. Fife, B. T., and Pauken, K. E. (2011) The role of
100. O’Sullivan, D., van der Windt, G. J. W., Huang,
the PD-1 pathway in autoimmunity and peripheral
S. C.-C., Curtis, J. D., Chang, C.-H., Buck, M. D.,
tolerance, Ann. N. Y. Acad. Sci.,
1217,
45-59,
Qiu, J., Smith, A. M., Lam, W. Y., DiPlato, L. M.,
doi: 10.1111/j.1749-6632.2010.05919.x.
Hsu, F. F., Birnbaum, M. J., Pearce, E. J., and Pearce,
110. Chemnitz, J. M., Parry, R. V., Nichols, K. E., June,
E. L. (2014) Memory CD8+ T cells use cell-intrinsic
C. H., and Riley, J. L. (2004) SHP-1 and SHP-2 asso-
lipolysis to support the metabolic programming
ciate with immunoreceptor tyrosine-based switch mo-
necessary for development, Immunity,
41,
75-88,
tif of programmed death 1 upon primary human T cell
doi: 10.1016/j.immuni.2014.06.005.
stimulation, but only receptor ligation prevents T cell
101. Cui, G., Staron, M. M., Gray, S. M., Ho, P.-C.,
activation, J. Immunol., 173, 945-954, doi: 10.4049/
Amezquita, R. A., Wu, J., and Kaech, S. M. (2015)
jimmunol.173.2.945.
IL-7-induced glycerol transport and TAG synthesis
111. Riley, J. L.
(2009) PD-1 signaling in primary
promotes memory CD8+ T cell longevity, Cell,
T cells, Immunol. Rev., 229, 114-125, doi: 10.1111/
161, 750-761, doi: 10.1016/j.cell.2015.03.021.
j.1600-065X.2009.00767.x.
102. Pan, Y., Tian, T., Park, C. O., Lofftus, S. Y., Mei, S.,
112. Francisco, L. M., Sage, P. T., and Sharpe, A. H.
Liu, X., Luo, C., O’Malley, J. T., Gehad, A., Teague,
(2010) The PD-1 pathway in tolerance and autoim-
J. E., Divito, S. J., Fuhlbrigge, R., Puigserver, P.,
munity, Immunol. Rev., 236, 219-242, doi: 10.1111/
Krueger, J. G., Hotamisligil, G. S., Clark, R. A.,
j.1600-065X.2010.00923.x.
and Kupper, T. S. (2017) Survival of tissue-resident
113. Patsoukis, N., Bardhan, K., Chatterjee, P., Sari, D.,
memory T cells requires exogenous lipid uptake and
Liu, B., Bell, L. N., Karoly, E. D., Freeman, G. J.,
metabolism, Nature,
543,
252-256, doi:
10.1038/
Petkova, V., Seth, P., Li, L., and Boussiotis, V. A.
nature21379.
(2015) PD-1 alters T-cell metabolic reprogramming by
103. Han, S.-J., Glatman Zaretsky, A., Andrade-
inhibiting glycolysis and promoting lipolysis and fatty
Oliveira, V., Collins, N., Dzutsev, A., Shaik, J., Morais
acid oxidation, Nat. Commun., 6, 6692, doi: 10.1038/
da Fonseca, D., Harrison, O. J., Tamoutounour, S.,
ncomms7692.
Byrd, A. L., Smelkinson, M., Bouladoux, N., Bliska,
114. Keir, M. E., Butte, M. J., Freeman, G. J., and
J. B., Brenchley, J. M., Brodsky, I. E., and Belkaid, Y.
Sharpe, A. H. (2008) PD-1 and its ligands in tolerance
(2017) White adipose tissue is a reservoir for memory
and immunity, Ann. Rev. Immunol., 26, 677-704,
T cells and promotes protective memory responses
doi: 10.1146/annurev.immunol.26.021607.090331.
to infection, Immunity, 47, 1154-1168, doi: 10.1016/
115. Sharpe, A. H., Wherry, E. J., Ahmed, R., and
j.immuni.2017.11.009.
Freeman, G. J. (2007) The function of programmed
104. Dimeloe, S., Mehling, M., Frick, C., Loeliger, J.,
cell death 1 and its ligands in regulating autoimmunity
Bantug, G. R., Sauder, U., Fischer, M., Belle, R.,
and infection, Nat. Immunol., 8, 239-245, doi: 10.1038/
Develioglu, L., Tay, S., Langenkamp, A., and
ni1443.
Hess, C. (2016) The immune-metabolic basis of
116. Ohaegbulam, K. C., Assal, A., Lazar-Molnar, E.,
effector memory CD4+ T cell function under hypoxic
Yao, Y., and Zang, X. (2015) Human cancer immu-
conditions, J. Immunol., 196, 106-114, doi: 10.4049/
notherapy with antibodies to the PD-1 and PD-L1
jimmunol.1501766.
pathway, Trends Mol. Med., 21, 24-33, doi: 10.1016/
105. Van der Windt, G. J. W., Everts, B., Chang, C.-H.,
j.molmed.2014.10.009.
Curtis, J. D., Freitas, T. C., Amiel, E., Pearce, E. J.,
117. Antonangeli, F., Natalini, A., Garassino, M. C., Sica, A.,
and Pearce, E. L. (2012) Mitochondrial respiratory
Santoni, A., and Di Rosa, F. (2020) Regulation of
capacity is a critical regulator of CD8+ T cell memory
PD-L1 expression by NF-κB in cancer, Front. Immu-
development, Immunity,
36,
68-78, doi:
10.1016/
nol., 11, 584626, doi: 10.3389/fimmu.2020.584626.
j.immuni.2011.12.007.
118. Brown, J. A., Dorfman, D. M., Ma, F.-R., Sullivan,
106. Prlic, M., and Bevan, M. J. (2009) Immunology: a
E. L., Munoz, O., Wood, C. R., Greenfield, E. A.,
metabolic switch to memory, Nature, 460, 41-42,
and Freeman, G.J. (2003) Blockade of programmed
doi: 10.1038/460041a.
death-1 ligands on dendritic cells enhances T cell
107. Luo, L., Li, X., Zhang, J., Zhu, C., Jiang, M., Luo, Z.,
activation and cytokine production, J. Immunol., 170,
Qin, B., Wang, Y., Chen, B., Du, Y., Lou, Y., and
1257-1266, doi: 10.4049/jimmunol.170.3.1257.
You, J. (2021) Enhanced immune memory through
119. Kinter, A. L., Godbout, E. J., McNally, J. P., Sereti, I.,
a constant photothermal-metabolism regulation for
Roby, G. A., O’Shea, M. A., and Fauci, A. S. (2008)
БИОХИМИЯ том 88 вып. 11 2023
МЕТАБОЛИЗМ Т-ЛИМФОЦИТОВ
2269
The common gamma-chain cytokines IL-2, IL-7,
Genolet, R., Cheng, W. C., Jandus, C., Coukos, G.,
IL-15, and IL-21 induce the expression of pro-
Jiang, Y. F., Locasale, J. W., Zippelius, A., Liu,
grammed death-1 and its ligands, J. Immunol., 181,
P. S., Tang, L., Bock, C., Vannini, N., and Ho, P. C.
6738-6746, doi: 10.4049/jimmunol.181.10.6738.
(2020) Disturbed mitochondrial dynamics in CD8+
120. Blackburn, S. D., Crawford, A., Shin, H., Polley, A.,
TILs reinforce T cell exhaustion, Nat. Immunol.,
Freeman, G. J., and Wherry, E. J. (2010) Tissue-
21, 1540-1551, doi: 10.1038/s41590-020-0793-3.
specific differences in PD-1 and PD-L1 expression
130. Li, W., Cheng, H., Li, G., and Zhang, L. (2020)
during chronic viral infection: implications for
Mitochondrial damage and the road to exhaustion, Cell
CD8 T-cell exhaustion, Virol. J., 84, 2078-2089,
Metab., 32, 905-907, doi: 10.1016/j.cmet.2020.11.004.
doi: 10.1128/JVI.01579-09.
131. Finisguerra, V., Dvorakova, T., Formenti, M.,
121. Zhang, Y., Zhou, Y., Lou, J., Li, J., Bo, L., Zhu, K.,
Van Meerbeeck, P., Mignion, L., Gallez, B., and
Wan, X., Deng, X., and Cai, Z. (2010) PD-L1 block-
Van den Eynde, B. J. (2023) Metformin improves
ade improves survival in experimental sepsis by inhibit-
cancer immunotherapy by directly rescuing tumor-
ing lymphocyte apoptosis and reversing monocyte dys-
infiltrating CD8 T lymphocytes from hypoxia-induced
function, Critical Care, 14, R220, doi: 10.1186/cc9354.
immunosuppression, J. Immunother. Cancer,
11,
122. Alfei, F., and Zehn, D. (2017) T cell exhaustion:
e005719, doi: 10.1136/jitc-2022-005719.
an epigenetically imprinted phenotypic and func-
132. Haws, S. A., Leech, C. M., and Denu, J. M.
tional makeover, Trends Mol. Med., 23, 769-771,
(2020) Metabolism and the epigenome: a dynamic
doi: 10.1016/j.molmed.2017.07.006.
relationship, Trends Biochem. Sci.,
45,
731-747,
123. He, W., Xiao, K., Xu, J., Guan, W., Xie, S., Wang, K.,
doi: 10.1016/j.tibs.2020.04.002.
Yan, P., Fang, M., and Xie, L. (2021) Recurrent sepsis
133. Martínez-Reyes, I., Diebold, L. P., Kong, H.,
exacerbates CD4+ T cell exhaustion and decreases
Schieber, M., Huang, H., Hensley, C. T., Mehta, M. M.,
antiviral immune responses, Front. Immunol., 12,
Wang, T., Santos, J. H., Woychik, R., Dufour, E.,
627435, doi: 10.3389/fimmu.2021.627435.
Spelbrink, J. N., Weinberg, S. E., Zhao, Y.,
124. Philip, M., and Schietinger, A. (2019) Heterogeneity
DeBerardinis, R. J., and Chandel, N. S. (2016) TCA
and fate choice: T cell exhaustion in cancer and
cycle and mitochondrial membrane potential are
chronic infections, Curr. Opin. Immunol., 58, 98-103,
necessary for diverse biological functions, Mol. Cell,
doi: 10.1016/j.coi.2019.04.014.
61, 199-209, doi: 10.1016/j.molcel.2015.12.002.
125. Fenwick, C., Joo, V., Jacquier, P., Noto, A.,
134. Madiraju, P., Pande, S. V., Prentki, M., and Madiraju,
Banga, R., Perreau, M., and Pantaleo, G. (2019) T-cell
S. R. M. (2009) Mitochondrial acetylcarnitine pro-
exhaustion in HIV infection, Immunol. Rev., 292,
vides acetyl groups for nuclear histone acetylation,
149-163, doi: 10.1111/imr.12823.
Epigenetics, 4, 399-403, doi: 10.4161/epi.4.6.9767.
126. Vardhana, S. A., Hwee, M. A., Berisa, M., Wells,
135. Lozoya, O. A., Wang, T., Grenet, D., Wolfgang,
D. K., Yost, K. E., King, B., Smith, M., Herrera,
T. C., Sobhany, M., Ganini da Silva, D., Riadi, G.,
P. S., Chang, H. Y., Satpathy, A. T., van den Brink,
Chandel, N., Woychik, R. P., and Santos, J. H. (2019)
M. R. M., Cross, J. R., and Thompson, C. B. (2020)
Mitochondrial acetyl-CoA reversibly regulates locus-
Impaired mitochondrial oxidative phosphorylation
specific histone acetylation and gene expression,
limits the self-renewal of T cells exposed to persistent
Life Sci. Alliance,
2, e201800228, doi:
10.26508/
antigen, Nat. Immunol., 21, 1022-1033, doi: 10.1038/
lsa.201800228.
s41590-020-0725-2.
136. Peng, M., Yin, N., Chhangawala, S., Xu, K., Leslie,
127. Liu, Y.-N., Yang, J.-F., Huang, D.-J., Ni, H.-H.,
C. S., and Li, M. O. (2016) Aerobic glycolysis promotes
Zhang, C.-X., Zhang, L., He, J., Gu, J. M.,
T helper 1 cell differentiation through an epigenetic
Chen, H. X., Mai, H.Q., Chen, Q.Y., Zhang,
mechanism, Science,
354,
481-484, doi:
10.1126/
X.S., Gao, S., and Li, J. (2020) Hypoxia induces
science.aaf6284.
mitochondrial defect that promotes T cell exhaustion
137. Delsite, R., Kachhap, S., Anbazhagan, R., Gabriel-
in tumor microenvironment through MYC-regulated
son, E., and Singh, K. K. (2002) Nuclear genes
pathways, Front. Immunol., 11, 1906, doi: 10.3389/
involved in mitochondria-to-nucleus communication
fimmu.2020.01906.
in breast cancer cells, Mol. Cancer, 1, 6, doi: 10.1186/
128. Scharping, N. E., Rivadeneira, D. B., Menk, A. V.,
1476-4598-1-6.
Vignali, P. D. A., Ford, B. R., Rittenhouse, N. L.,
138. Carey, B. W., Finley, L. W. S., Cross, J. R., Allis,
Peralta, R., Wang, Y., Wang, Y., DePeaux, K., Poholek,
C. D., and Thompson, C. B. (2015) Intracellular
A. C., and Delgoffe, G. M. (2021) Mitochondrial stress
α-ketoglutarate maintains the pluripotency of
induced by continuous stimulation under hypoxia
embryonic stem cells, Nature,
518,
413-416,
rapidly drives T cell exhaustion, Nat. Immunol.,
doi: 10.1038/nature13981.
22, 205-215, doi: 10.1038/s41590-020-00834-9.
139. Liu, P.-S., Wang, H., Li, X., Chao, T., Teav, T.,
129. Yu, Y.-R., Imrichova, H., Wang, H., Chao, T.,
Christen, S., Di Conza, G., Cheng, W. C., Chou,
Xiao, Z., Gao, M., Rincon-Restrepo, M., Franco, F.,
C. H., Vavakova, M., Muret, C., Debackere, K.,
БИОХИМИЯ том 88 вып. 11 2023
2270
ВЛАСОВА, ШМАГЕЛЬ
Mazzone, M., Huang, H. D., Fendt, S. M., Ivanise-
The tumor suppressor menin prevents effector CD8
vic, J., and Ho, P. C.
(2017) α-ketoglutarate
T-cell dysfunction by targeting mTORC1-dependent
orchestrates macrophage activation through metabolic
metabolic activation, Nat. Commun.,
9,
3296,
and epigenetic reprogramming, Nat. Immunol., 18,
doi: 10.1038/s41467-018-05854-6.
985-994, doi: 10.1038/ni.3796.
144. Sun, L., Zhang, L., Yu, J., Zhang, Y., Pang, X.,
140. Xu, W., Yang, H., Liu, Y., Yang, Y., Wang, P., Kim,
Ma, C., et al. (2020) Clinical efficacy and safety of
S.-H., Ito, S., Yang, C., Wang, P., Xiao, M. T., Liu,
anti-PD-1/PD-L1 inhibitors for the treatment of
L. X., Jiang, W. Q., Liu, J., Zhang, J. Y., Wang, B.,
advanced or metastatic cancer: a systematic review
Frye, S., Zhang, Y., Xu, Y. H., Lei, Q. Y., Guan, K. L.,
and meta-analysis, Sci. Rep., 10, 2083, doi: 10.1038/
Zhao, S. M., and Xiong, Y. (2011) Oncometabolite
s41598-020-58674-4.
2-hydroxyglutarate is a competitive inhibitor of
145. Seidel, J. A., Otsuka, A., and Kabashima, K. (2018)
α-ketoglutarate-dependent dioxygenases, Cancer Cell,
Anti-PD-1 and anti-CTLA-4 therapies in cancer:
19, 17-30, doi: 10.1016/j.ccr.2010.12.014.
mechanisms of action, efficacy, and limitations, Front.
141. Sciacovelli, M., Gonçalves, E., Johnson, T.I.,
Oncol., 8, 86, doi: 10.3389/fonc.2018.00086.
Zecchini, V. R., da Costa, A. S. H., Gaude, E.,
146. Chowdhury, P. S., Chamoto, K., Kumar, A., and
Drubbel, A. V., Theobald, S. J., Abbo, S. R., Tran,
Honjo, T. (2018) PPAR-induced fatty acid oxidation
M. G., Rajeeve, V., Cardaci, S., Foster, S., Yun, H.,
in T cells increases the number of tumor-reactive
Cutillas, P., Warren, A., Gnanapragasam, V.,
CD8+ T cells and facilitates anti-PD-1 therapy, Cancer
Gottlieb, E., Franze, K., Huntly, B., Maher, E. R.,
Immunol. Res., 6, 1375-1387, doi: 10.1158/2326-6066.
Maxwell, P. H., Saez-Rodriguez, J., and Frezza, C.
CIR-18-0095.
(2016) Fumarate is an epigenetic modifier that elicits
147. Abdul-Rahman, T., Bukhari, S. M. A., Herrera, E. C.,
epithelial-to-mesenchymal transition, Nature,
537,
Awuah, W. A., Lawrence, J., and de Andrade, H.
544-547, doi: 10.1038/nature19353.
(2022) Lipid lowering therapy: an era beyond statins,
142. Nabe, S., Yamada, T., Suzuki, J., Toriyama, K.,
Curr. Probl. Cardiol.,
47,
101342, doi:
10.1016/j.
Yasuoka, T., Kuwahara, M., Shiraishi, A., Take-
cpcardiol.2022.101342.
naka, K., Yasukawa, M., and Yamashita, M. (2018)
148. Lemberg, K. M., Gori, S. S., Tsukamoto, T., Rais, R.,
Reinforce the antitumor activity of CD8+ T cells via
and Slusher, B. S. (2022) Clinical development of
glutamine restriction, Cancer Sci., 109, 3737-3750,
metabolic inhibitors for oncology, J. Clin. Invest., 132,
doi: 10.1111/cas.13827.
e148550, doi: 10.1172/JCI148550.
143. Suzuki, J., Yamada, T., Inoue, K., Nabe, S., Kuwa-
149. Peng, M., and Li, M. O. (2023) Metabolism along the
hara, M., Takemori, N., Matsuda, S., Kanoh, M.,
life journey of T cells, Life Metab., 2, 1-9, doi: 10.1093/
Imai, Y., Yasukawa, M., and Yamashita, M. (2018)
lifemeta/load002.
T-LYMPHOCYTE METABOLIC FEATURES
AND TECHNIQUES TO MODULATE THEM
Review
V. V. Vlasova*# and K. V. Shmagel#
Institute of Ecology and Genetics of Microorganisms,
Perm Federal Research Center of the Ural Branch of the Russian Academy of Sciences,
614081 Perm, Russia; e-mail: violetbaudelaire73@gmail.com
T cells demonstrate a high degree of complexity and a broad range of functions which distinguish them
from other immune cells. Throughout life, T lymphocytes experience several functional states: quiescence,
activation, proliferation, differentiation, performance of effector and regulatory functions, memory for-
mation, and apoptosis. Metabolism supports all the T cell functions, providing lymphocytes with energy,
biosynthetic substrates, and signaling molecules. Therefore, T cells usually restructure their metabolism
as they transition from one functional state to another. The strong association between metabolism and T cell
function implies that the immune response can be controlled by manipulating metabolic processes within
T lymphocytes. This review aims to highlight the main metabolic adaptations necessary for T cell function,
as well as the recent progress in techniques to modulate the lymphocyte metabolic features.
Keywords: T lymphocytes, metabolism, glycolysis, TCA, oxidative phosphorylation, mitochondria, proliferation,
differentiation, immunological memory, exhaustion
БИОХИМИЯ том 88 вып. 11 2023