БИОХИМИЯ, 2023, том 88, вып. 11, с. 2271 - 2288
УДК 615, 616-05
C-КОНЦЕВЫЕ ФРАГМЕНТЫ АПЕЛИНА:
БИОЛОГИЧЕСКИЕ СВОЙСТВА И ТЕРАПЕВТИЧЕСКИЙ ПОТЕНЦИАЛ
Обзор
© 2023 О.И. Писаренко*, И.М. Студнева
ФГБУ «НМИЦ кардиологии им. академика Е.И. Чазова» Минздрава России,
121552 Москва, Россия; электронная почта: olpi@live.ru
Поступила в редакцию 30.05.2023
После доработки 10.09.2023
Принята к публикации 11.09.2023
В последние годы показано, что адипокин апелин - эндогенный лиганд рецептора APJ - участвует
в регуляции сердечно-сосудистой, гипоталамо-гипофизарной, желудочно-кишечной и иммунной
системах человека. В обзоре представлены данные литературы о системе апелин/APJ, ее влиянии
на сосудистую систему, пищеварение, жировую ткань и водно-электролитный обмен. Обсуждается
действие пептидов апелина при ожирении, диабете и сердечно-сосудистых заболеваниях, а также
их кардиопротекторные эффекты, связанные с активацией реперфузионных киназ и проявлением
антиоксидантных свойств. Обобщены результаты собственных экспериментов по влиянию апели-
на-13, [Pyr1]апелина-13, апелина-12 и их химически модифицированных аналогов на сердце в нор-
ме и при моделировании патофизиологических состояний in vitro и in vivo. Показано, что спектр
действия С-концевых фрагментов апелина на поврежденный миокард охватывает уменьшение
гибели кардиомиоцитов от некроза, снижение повреждения клеточных мембран, улучшение мета-
болического состояния миокарда, снижение образования активных форм кислорода и продуктов
перекисного окисления липидов. Сделан вывод о перспективности молекулярного конструирова-
ния фармакологических агонистов рецептора APJ, обладающих протеолитической устойчивостью
и стабильностью при хранении, которые могут служить основой для разработки нового класса ле-
карственных средств.
КЛЮЧЕВЫЕ СЛОВА: апелин, структурные аналоги, сердце, экспериментальная патология, метаболизм,
мембраны кардиомиоцитов, перекисное окисление липидов, активные формы кислорода, антиоксидант-
ные ферменты.
DOI: 10.31857/S0320972523110179, EDN: MMSYTE
ВВЕДЕНИЕ
взаимодействуя с гормонами гипофиза, инсу-
лином, катехоламинами. Адипокины влияют
Хорошо установлено, что жировая ткань
на обмен липидов, гомеостаз глюкозы, про-
является не только хранилищем запасенной
цессы ангиогенеза, иммунитета, воспаления,
энергии, но и активным эндокринным орга-
свертывания крови, образования костной
ном, в котором продуцируются пептидные гор-
ткани, опухолевого роста и др. Одним из наи-
моны - адипокины [1]. Они обладают разно-
более активно изучающихся адипокинов явля-
образными биологическими эффектами и ока-
ется апелин - лиганд сопряженного с G-бел-
зывают свое влияние во многих органах пря-
ком семидоменного трансмембранного рецеп-
мо или через нейроэндокринные механизмы, тора APJ [2]. Апелин активно экспрессируется
Принятые сокращения: АФК - активные формы кислорода; ИМ - инфаркт миокарда; ЛЖ - левый желудочек
сердца; ПЭГ - полиэтиленгликоль; ACE2 - ангиотензин-превращающий фермент 2; Akt - протеинкиназа В; APJ -
рецептор апелина (APLNR), связанный с G-белком; CAT - каталаза; CD10 - неприлизин; MEK1/2 - киназа мито-
ген-активируемой протеинкиназы (MAP2K); mitoK+ATP-каналы - митохондриальные ATP-зависимые К+-каналы;
mPTP - митохондриальная пора; MDA - малоновый диальдегид; PI3K - фосфатидилинозитол-3-киназа; PKC - про-
теинкиназа С; PLCβ - фосфолипаза Сβ; PRCP - пролилкарбоксипептидаза; [Pyr1]апелин-13 - пироглутаминиро-
ванный по N-концевому глутамину апелин-13; RISK-киназа - киназы спасения от реперфузионного повреждения;
SOD - супероксиддисмутаза; О2• - супероксидный анион-радикал; ONOO• - пероксинитрит.
* Адресат для корреспонденции.
2271
2272
ПИСАРЕНКО, СТУДНЕВА
различными тканями, включая эндотелиаль-
лин не был обнаружен в качестве родствен-
ные и гладкомышечные клетки коронарных
ного лиганда после выделения из экстрактов
сосудов и кардиомиоциты. Активация систе-
желудка крупного рогатого скота в 1998 г. [9].
мы апелин/APJ оказывает мощное регулятор-
Рецептор APJ широко распространен в орга-
ное действие на сердечно-сосудистую систему.
низме, включая скелетную мышцу, сердце,
С-концевые фрагменты апелина способны сни-
легочную ткань, молочную железу, яичники,
жать метаболические и функциональные пов-
головной мозг, почки, поджелудочную железу
реждения сердца при различной эксперимен-
и надпочечники [10]. Это указывает на роль
тальной патологии [3]. Это указывает на целе-
системы апелин/APJ в регуляции ряда физио-
сообразность использования таких пепти-
логически важных показателей - жидкостного
дов в качестве потенциальных лекарственных
гомеостаза [11], артериального давления [12],
средств. В настоящем обзоре рассмотрены
метаболического контроля [13] и других. Не-
структурные и функциональные свойства при-
давно в эмбриональных стволовых клетках че-
родных и модифицированных пептидов апе-
ловека был идентифицирован эндогенный ли-
лина и молекулярные механизмы их действия.
ганд рецептора APJ, названный ELABELA.
ELABELA - это пептид, состоящий из 32 а.о.,
который играет роль в эмбриональном разви-
БИОЛОГИЧЕСКИЕ СВОЙСТВА АПЕЛИНА
тии сердца [14].
Ген апелина локализован в Х-хромосоме
Апелин и его рецептор APJ. Сопряженный
(локус Xq25-q26.1) [15] и кодирует препробе-
с G-белком рецептор APJ, расположенный
лок, состоящий из 77 а.о., с сигнальной по-
в 11 хромосоме (локус 11q12), был обнару-
следовательностью в N-концевой области.
жен O’Dowd et al. [4] в 1933 г. Он имеет высо-
После транслокации в эндоплазматический
кую гомологичность с рецептором ангиотен-
ретикулум и отделения сигнального пептида
зина II 1-го типа AT1 (до 50% по гидрофобным
образуется пробелок из 55 а.о. Первоначально
трансмембранным областям), но не связыва-
апелин-55 считался неактивным пробелком,
ется с ангиотензином II. Рецептор APJ был
а апелин-36 - предшественником биологиче-
идентифицирован у большого числа различ-
ски активных изоформ: апелина-17 и апели-
ных видов животных и человека, он состоит из
на-13 [9, 10, 16]. Это было связано с наличием
377-380 а.о. и содержит 7 трансмембранных
в апелине-36 фрагментов Arg-Arg - типич-
доменов. На мембране рецептор существует
ного сайта расщепления трипсиноподобной
в форме мономера, димера или олигомера с
эндопептидазой [17]. Апелин-13 может под-
возможными взаимными превращениями [5],
вергаться посттрансляционному пироглутами-
которые могут быть важными для дальней-
нированию, катализируемому глутаминилцик-
шей трансдукции сигнала. Рецептор APJ спо-
лазой (QC), на уровне N-концевого остатка
собен к интернализации [6] и ассоциации с
глутамина в [Pyr1]апелин-13. Удаление остатка
другими рецепторами [7, 8]. Его долгое время
Gln в апелине-13 приводит к образованию наи-
считали «орфановым» рецептором, пока апе-
более короткого из биоактивных фрагментов
Таблица 1. Препробелок апелина и его С-концевые фрагменты
Пептид
Аминокислотная последовательность
MNLRLCVQALLLLWLSLTAVCGGSLMPLPDGNGLEDGNVRHLVQPRGSRNGPGPWQGGRRKFRRQ
Препроапелин
RPRLSHKGPMPF
Апелин-55
GSLMPLPDGNGLEDGNVRHLVQPRGSRNGPGPWQGGRRKFRRQRPRLSHKGPMPF
Апелин-36
LVQPRGSRNGPGPWQGGRRKFRRQRPRLSHKGPMPF
Апелин-17
KFRRQRPRLSHKGPMPF
Апелин-13
QRPRLSHKGPMPF
[Pyr1]апелин-13
(pGlu)RPRLSHKGPMPF
Апелин-12
RPRLSHKGPMPF
Примечание. Жирным шрифтом показаны остатки Cys6 и Cys21, обеспечивающие стабильность димера препроапелина.
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2273
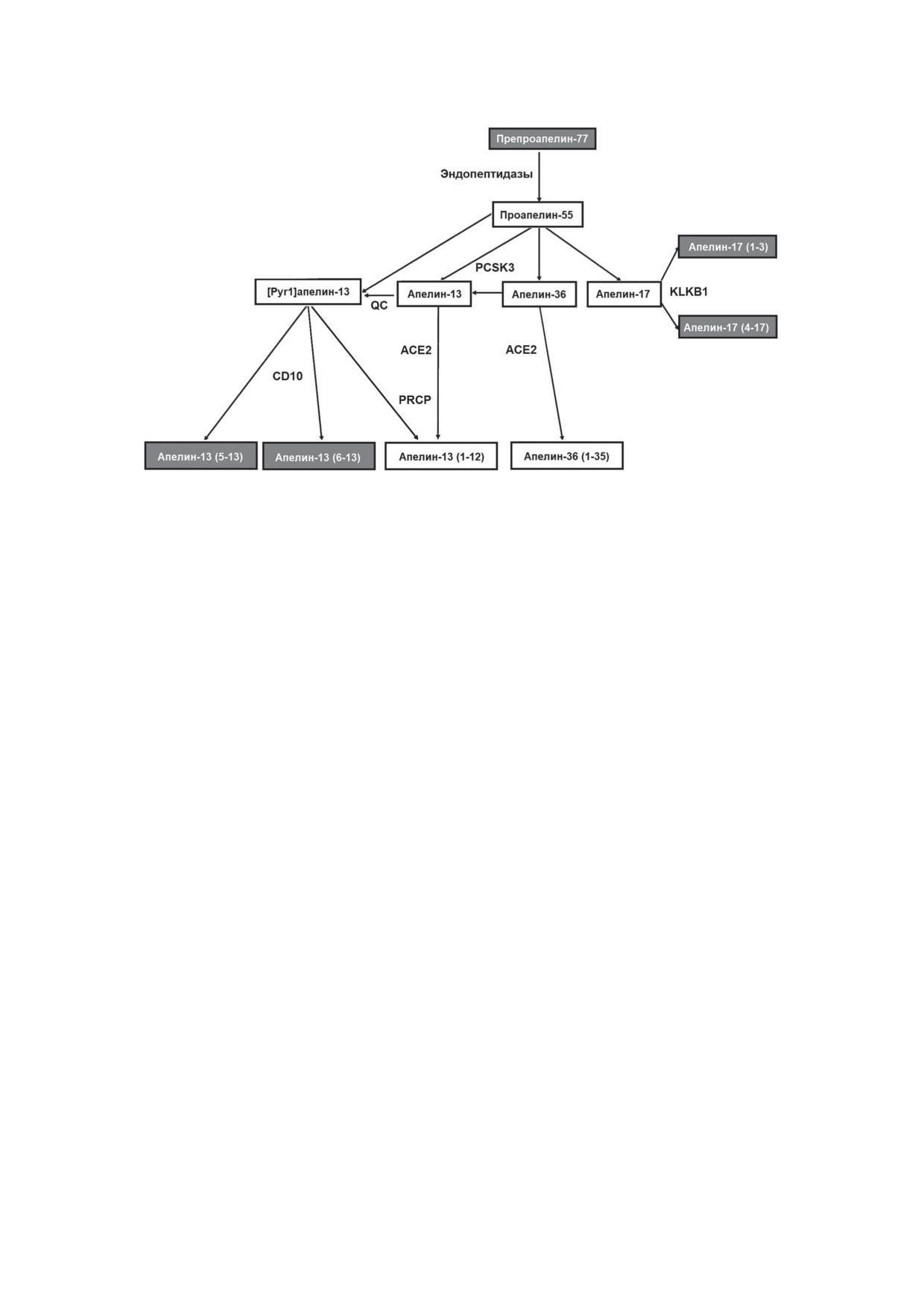
Рис. 1. Ферментативное расщепление пептидов апелина. ACE2 - ангиотензин-превращающий фермент 2; CD10 -
неприлизин; KLKB1 - калликреин; PRCP - пролилкарбоксипептидаза; PCSK3 - пропротеинконвертаза субтили-
зин/кексин 3; QC - глутаминилциклаза. Темным цветом показаны пептиды, не способные связываться с рецепто-
ром APJ (апелин-13 (5-13) и апелин-13 (6-13)) или активировать внутриклеточную сигнализацию (апелин-17 (1-3)
и апелин-17 (4-17))
апелина-12 (табл. 1). Короткие C-концевые
[22-25]. Металлопротеаза CD10 расщепляет
фрагменты апелина ответственны за связыва-
[Pyr1]апелин-13 между остатками Arg4 и Leu5
ние с рецептором и биологическую активность
и Leu5 и Ser6, создавая фрагменты 5-13 и 6-13
пептида [16, 18]. Было обнаружено, что пре-
соответственно. Образующиеся при этом пеп-
проапелин в нативной ткани существует как
тиды лишены способности активировать ре-
димер, стабилизированный дисульфидными
цептор APJ [22]. ACE2, цинксодержащая кар-
мостиками остатков Cys6 и Суs21, а апелин-36
боксимонопептидаза, отвечает за отщепление
и апелин-13 являются мономерами [15].
С-концевого Phe в апелине-13 и -36 [23]. В ре-
Недавние исследования показали, что про-
зультате расщепления ACE2 апелина-13 и -36
цессинг апелина сложен. Выяснено, что апе-
образуются два фрагмента - апелин-13 (1-12)
лин-55 не является биологически неактивным
и апелин-36 (1-35). Оба фрагмента способны
пробелком и может активировать рецептор
связываться с APJ и активировать внутрикле-
APJ, хотя и с меньшей эффективностью, чем
точную сигнализацию. PRCP способна сход-
более короткие С-концевые фрагменты апе-
ным образом c ACE2 гидролизовать апелин-13
лина [19]. В дополнение Shin et al. [20] обнару-
и [Pyr1]апелин-13, но с более низкой скоро-
жили способность пропротеинконвертазы суб-
стью [24]. Сериновая протеаза калликреин
тилизин/кексин 3 (PCSK3) расщеплять апе-
расщепляет апелин-17 между Arg3 и Arg4 на
лин-55 с образованием апелина-13 без образо-
две изоформы - апелин-17 (1-3) и апелин-17
вания других изоформ, что представляет но-
(4-17). Эти фрагменты связываются с рецеп-
вый путь деградации апелина. Кроме того, не
тором APJ с высоким сродством, но не могут
ясными остаются процессы, связанные с обра-
активировать передачу сигнала и мобилиза-
зованием апелина-13 и -12 из апелина-36 [21].
цию ионов Са2+ [25]. Пути деградации пепти-
Чувствительность пептидов апелина к протео-
дов апелина могут быть представлены следую-
литической деградации значительно ограни-
щей схемой (рис. 1).
чивает продолжительность и эффективность
Связывание с рецептором. С-концевые фраг-
их действия в биологических средах. Период
менты апелина различаются аффинностью по
полувыведения апелина у человека составляет
отношению к APJ. Инкубация 125I-меченных
около 5 минут [17]. Нестабильность апелинов
пептидов апелина на мембранах клеток яич-
объясняется ферментативной активностью
ника китайского хомячка CHO-A10 показала,
неприлизина (CD10), ангиотензин-превраща-
что короткие апелины связываются с рецепто-
ющего фермента 2 (ACE2), пролилкарбокси-
ром прочнее более длинных [16]. Апелин-13,
пептидазы (PRCP) и калликреина (KLKB1)
[Pyr1]апелин-13 и апелин-12, являющиеся наи-
16
БИОХИМИЯ том 88 вып. 11 2023
2274
ПИСАРЕНКО, СТУДНЕВА
более биологически активными изоформами
демонстрируя важность жесткости конструк-
[9, 15], характеризуются более высокими зна-
ции и расстояния между двумя эпитопами [30].
чениями аффинности (1/Kd) и максимального
Таким образом, показано значение последо-
связывания (Bmax), чем апелин-17, -19 и -36 [10].
вательности аминокислот Arg-Pro-Arg-Leu в
В то же время апелин-36 может связываться с
структуре апелина и С-концевого Phe для свя-
рецептором APJ дольше, чем более короткие
зывания с рецептором APJ.
изоформы [16]. Это увеличение занятости ре-
Распределение в организме. мРНК апелина
цепторов можно объяснить наличием отри-
и рецептора APJ экспрессируются практи-
цательно заряженной области рецептора APJ,
чески во всех тканях и органах организма и
которая взаимодействует с положительно за-
в центральной нервной системе. Особенно
ряженными аминокислотами в более длин-
высоки их концентрации в мозжечке, сосуди-
ном пептиде апелин-36 [26].
стом эндотелии, сердце, легких, почках, пече-
Работы по изучению структуры и актив-
ни, надпочечниках и жировой ткани [9, 16, 31].
ности апелина обнаружили, что последова-
Рецепторы APJ в сердце обнаруживаются в
тельности аминокислотных остатков Arg-Pro-
эндотелии, гладкомышечных клетках и кар-
Arg-Leu и Lys-Gly-Pro-Met являются наиболее
диомиоцитах, так же как и рецептор AT1 [32].
существенными для связывания апелина-13
Обширная «география» синтеза апелина в ор-
с рецептором APJ, а замены Gln1, His7, Pro12
ганизме свидетельствует о широком спектре
и Phe13 незначительно ухудшают сродство с
его регуляторного влияния на физиологиче-
рецептором [27]. В работе Medhurst et al. [27]
ские и биохимические процессы. Таким обра-
было также показано, что два С-концевых
зом, апелин является не только гормоноподоб-
фрагмента апелина, N-ацетил-Leu-Ser-His-Lys-
ным веществом, циркулирующим в крови, но
Gly-Pro-Met-Pro-Phe-COOH и N-ацетил-Lys-
и аутопаракринным, и паракринным факто-
Gly-Pro-Met-Pro-Phe-COOH, проявляют низ-
ром в целом ряде тканей-мишеней. Считается,
кое сродство к рецептору APJ. Кроме того,
что апелин оказывает значимую часть своего
замена в структуре апелина-13 Leu5 или Arg2
влияния паракринным путем, хотя и эндо-
на Ala приводит к значительному (более чем
кринный путь является очень важным [33].
50-кратному) снижению способности связы-
ваться с рецептором. Таким образом, после-
довательность Arg-Pro-Arg-Leu в структуре
ФИЗИОЛОГИЧЕСКАЯ РОЛЬ
апелина играет ключевую роль для взаимо-
СИСТЕМЫ АПЕЛИН/APJ
действия с рецептором APJ. Эта гипотеза под-
тверждается результатами 1Н-ЯМР-исследова-
В последние годы подтверждена суще-
ний апелина-17 (NH2-Lys-Phe-Arg-Arg-Gln-Arg-
ственная роль апелина в физиологии человека
Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Met-Pro-
как регуляторного пептида в сердечно-сосу-
Phe-COOH), которые показали, что последо-
дистой, гипоталамо-гипофизарной, желудоч-
вательность Arg-Pro-Arg-Leu образует четко
но-кишечной и иммунной системах
[34].
определенный тип β-поворота в растворе [28],
Многочисленные работы демонстрируют, что
играющего, как полагают, решающую роль
активация рецептора APJ апелинами вовле-
в узнавании и связывании эндогенных пеп-
чена в регуляцию тонуса сосудов, сердеч-
тидов с рецепторами, сопряженными с G-бел-
ной сократимости, водного баланса, метабо-
ком [29].
лизма, клеточной пролиферации, апоптоза и
В работе Murza et al. [30] была продемон-
воспаления [35].
стрирована исключительная важность про-
Влияние на сосудистую систему. Апелин-13
странственной ориентации некоторых амино-
и [Pyr1]апелин-13 влияют на сосудистый тонус
кислотных остатков апелина-13, в особенности
in vivo, вызывая снижение артериального дав-
Arg2, Pro3, Arg4 и в меньшей степени Pro12. Так-
ления у крыс [15, 36] и вазодилатацию рези-
же было изучено влияние на связывание с ре-
стивных сосудов предплечья у человека [37].
цептором модификации С-концевой части мо-
In vitro апелин-13 вызывает вазодилатацию вис-
лекулы, состоящей в замене Phe13 на различные
церальной артерии человека [38] преимуще-
типы ароматических групп. Оно подтвердило
ственно благодаря NO-зависимому механизму.
связь С-концевого Phe с электрон-насыщен-
Под действием образующегося в эндотелиаль-
ными аминокислотными остатками кармана
ных клетках oксида азота (NO) происходит
связывания APJ-рецептора. Была предприня-
активация растворимой гуанилатциклазы в
та попытка модификации центральной части
гладкомышечных клетках, которая приводит
молекулы заменой аминокислот на различные
к образованию циклического гуанозинмоно-
линкеры (полиэтиленгликоль (ПЭГ), аланин),
фосфата (cGMP) и расслаблению этих кле-
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2275
ток, вызывая вазодилатацию. Однако апелин
около 40 пМ в ткани сердца человека [48] и
может вызвать и вазоконстрикторный эффект
33 пМ - в ткани сердца крысы [49]. Пожилые
при контакте с дисфункциональным эндо-
нокаутные по генам апелина и рецептора APJ
телием. Показано, что [Pyr1]апелин-13 вызы-
мыши показывают прогрессивное ухудшение
вает вазоконстрикцию подкожной вены [39] и
сердечной сократимости независимо от внут-
грудной артерии [40] человека in vitro. В этом
риклеточного транспорта ионов Ca2+, поте-
случае пептид действует напрямую на глад-
рю способности к укорочению саркомеров и
комышечные клетки сосуда, которые также
уменьшение скорости сокращения и расслаб-
экспрессируют APJ-рецептор, увеличивая кон-
ления миофибрилл [51].
центрацию внутриклеточного Ca2+ и вызы-
Регуляция жидкостного гомеостаза. Экс-
вая их сокращение. Работы, проведенные на
прессия апелина и его рецептора, подобно
нокаутных по гену апелинового рецептора
антидиуретическому гормону (вазопрессину),
мышах, показали присутствие баланса между
происходит также в магноцеллюлярных ней-
сигнальным путем ангиотензина II, который
ронах супраоптического и паравентрикуляр-
повышает кровяное давление, и сигналь-
ного ядер гипоталамуса, т.е. в областях мозга,
ным путем апелина, который снижает дав-
включенных в регуляцию потребления пищи
ление [35].
и воды [15]. Введение апелина-13 увеличивает
Активация рецептора APJ участвует в фор-
потребление воды, а также уменьшает в гипо-
мировании новых кровеносных сосудов [35].
таламусе секрецию вазопрессина. Показано,
Ангиогенная активность - это последствие
что интрацеребровентрикулярная инъекция
действия апелина на пролиферацию и мигра-
апелина-13 мышам ингибирует активность
цию эндотелиальных клеток. Показано, что
вазопрессиновых нейронов и высвобождение
апелин-13 является мощным ангиогенным
вазопрессина, уменьшая его концентрацию в
фактором [41, 42] и митогеном эндотелиаль-
плазме и усиливая диурез [52]. Обезвожива-
ных [40, 43] и гладкомышечных [44] клеток со-
ние усиливает экспрессию апелина и умень-
судов. Он активирует внутри клетки сигналь-
шает экспрессию вазопрессина у крыс [53].
ные каскады (фосфорилирование ERK, Akt
Этот диуретический эффект апелина вместе
(протеинкиназы B) и p70S6-киназ), которые
с его гипотензивным эффектом принимает
приводят к пролиферации эндотелиальных
глобальное участие в гомеостатической регу-
клеток и формированию новых кровеносных
ляции жидкостей тела.
сосудов. Исследования на клетках микросо-
Пищеварение. Рецептор APJ экспрессиру-
судов мозга мышей показали, что апелин дей-
ется в желудочных энтерохромаффиноподоб-
ствует как митогенный, хемотаксический и
ных клетках, некоторых клетках поджелу-
антиапоптотический агент для эндотелиаль-
дочной железы, эпителиальных клетках ки-
ных клеток. Было продемонстрировано, что
шечника [54]. В желудке активация рецепто-
нокаут по гену апелина у мышей связан со
ров APJ на энтерохромаффиноподобных клет-
снижением развития ретинальных сосудов, а
ках апелином, секретируемым париеталь-
нокаут по гену апелинового рецептора приво-
ными клетками, может ингибировать высво-
дит к дефектам развития сердечно-сосудистой
бождение энтерохромаффиноподобными клет-
системы [45]. Подобно многим другим ангио-
ками гистамина, который, в свою очередь,
генным факторам, экспрессия APJ возрастает
уменьшает секрецию кислоты париетальны-
в условиях гипоксии [42].
ми клетками. В поджелудочной железе апе-
Инотропное действие. Рецептор APJ экс-
лин ингибирует секрецию инсулина, инду-
прессируется на начальных стадиях форми-
цированную глюкозой. Предполагается суще-
рования сердца в эмбриональном периоде, где
ствование функциональной взаимозависимо-
он регулирует миграцию прогениторных кле-
сти между сигнальными путями апелина и
ток, дифференцирующихся в сократитель-
инсулина на уровне адипоцитов, где инсулин
ные клетки - кардиомиоциты [46]. Экспрес-
стимулирует продукцию апелина [35].
сия APJ также обнаружена в кардиомиоцитах
Влияние на жировую ткань. Адипоциты, се-
взрослых животных, где апелин является
кретирующие апелин, являются возможными
мощным стимулятором сердечной сократи-
источниками плазматического апелина [35].
мости [47, 48]. Показано, что [Pyr1]апелин-13
На экспрессию апелина в жировой ткани влия-
и апелин-16 оказывают положительный ино-
ют многие факторы, в том числе голодание,
тропный эффект на сердце лабораторных жи-
гипоксия [36, 55] и инсулин [56]. В то время
вотных и человека in vivo благодаря прямому
как инсулин стимулирует экспрессию апелина
действию [49, 50]. При этом полумаксимальная
жировой тканью [35, 56], апелин ингибирует
эффективная концентрация EС50 составляет
секрецию инсулина [57], демонстрируя взаи-
БИОХИМИЯ том 88 вып. 11 2023
16*
2276
ПИСАРЕНКО, СТУДНЕВА
мозависимость этих двух систем. Активация
матического апелина возрастает на ранних
системы апелин/APJ также принимает уча-
стадиях сердечной недостаточности [64], но
стие в усвоении глюкозы благодаря активации
возвращается к исходному уровню или сни-
АМP-активируемой протеинкиназы (AMPK)
жается на более поздних стадиях [65, 66]. Было
и Akt [58]. Апелин может быть также вовлечен
установлено, что экспрессия мРНК APJ сни-
в васкуляризацию жировой ткани [55].
жается в левом желудочке (ЛЖ) у пациентов с
идиопатической дилатационной кардиомио-
патией [67]. Эти данные позволяют предпо-
ДЕЙСТВИЕ ПЕПТИДОВ АПЕЛИНА
ложить, что увеличение уровня экспрессии
ПРИ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЯХ
апелина на ранних стадиях заболевания мо-
жет быть компенсаторным действием, повы-
Ожирение и диабет. Данные, имеющиеся
шающим силу сокращения сердца. Уровень
в современной литературе, указывают, что
экспрессии апелина и его рецептора затем
плазматический апелин положительно кор-
может подавляться на более поздних стадиях
релирует с индексом массы тела человека, а
сердечной недостаточности, когда положи-
увеличенная экспрессия апелина в плазме
тельное инотропное действие апелина начнет
и жировой ткани у пациентов с ожирением
ухудшать состояние сердца в связи с увели-
может быть снижена благодаря низкокало-
чением потребности в кислороде. Уровень
рийной диете, приводящей к потере веса [59].
[Pyr1]апелина-13 в сердце возрастает в ответ
Однако на моделях ожирения у мышей было
на гипоксию через гипоксия-индуцибельный
показано, что не ожирение, а уровень инсули-
фактор-1 [68]. Кроме того, уровень экспрес-
на является основным фактором, определяю-
сии апелина и его рецептора повышается при
щим повышение экспрессии апелина [35]. Это
ишемической сердечной недостаточности у
означает, что экспрессия апелина увеличи-
крыс [66, 69].
вается не просто при ожирении, а в ответ на
В ряде исследований были предприняты
гиперинсулинемию, связанную с ожирением,
попытки изучить роль системы апелин/APJ
хотя исследование влияния плазматического
в патогенезе атеросклероза. Так, в 2007 г. с
апелина на сахарный диабет 2-го типа дает
помощью трансгенных моделей у мышей
разрозненные результаты [60, 61]. Регуляция
Hashimoto et al. [70]) показали, что апелин-13
экспрессии апелина при ожирении может
стимулирует
экспрессию субъединицы
быть полезной при метаболическом синдроме,
NADPН-оксидазы и индуцирует связанную
потому что периферийное введение апелина
с окислительным стрессом пролиферацию в
снижает толерантность к глюкозе и улучшает
гладкомышечных клетках сосудов, а рецеп-
ее утилизацию при ожирении у инсулин-ре-
тор APJ может участвовать в развитии ате-
зистентных мышей [58]; и наоборот, нокаут-
росклероза, связанного с гиперхолестерине-
ные по гену апелина мыши обладают сни-
мией. У человека уровень экспрессии апелина
женной чувствительностью к инсулину [62].
увеличивается в атеросклеротической коро-
Апелин также уменьшает количество жиро-
нарной артерии [71]. Кроме того, уровни экс-
вой ткани у мышей с ожирением, не изменяя
прессии апелина и APJ увеличиваются при
потребление пищи, путем увеличения экс-
стенозе аортального клапана - процессе, ко-
прессии разобщающего белка UCP1 и рас-
торый отражает некоторые признаки атеро-
хода энергии [63]. Очевидно, что регуляция
склероза
[72], демонстрируя вовлеченность
метаболизма апелином при ожирении может
апелиновой системы в атеросклероз у челове-
также оказать благоприятное действие на
ка. Апелин также предотвращает образование
сердечно-сосудистую систему, снижая арте-
аневризмы аорты у мышей [73].
риальное давление и повышая сократимость
Предполагается участие системы апелин/
сердца.
APJ при патофизиологическом ангиогенезе, ко-
Сердечно-сосудистые заболевания. В ис-
торый способствует портосистемной коллате-
следованиях Chen et al. [64], Chong et al. [65]
рализации и висцеральной неоваскуляриза-
и Miettinen et al. [66] были отмечены изме-
ции у портальных гипертензивных крыс [74],
нения уровня апелина в плазме крови чело-
неоангиогенезу при циррозе печени [75] и
века в условиях сердечной дисфункции с
неоангиогенезу опухоли [76, 77]. Тем не менее
довольно противоречивыми результатами и
ангиогенное действие апелина [78, 79] может
очень широким диапазоном концентраций
вносить серьезный вклад в восстановление
(20-4000 пг/мл) в зависимости от уровня
сердца после ишемии. Таким образом, апелин
патологии и метода определения пептида.
очень важен для сохранения функции повреж-
В основном предполагается, что уровень плаз-
денного сердца.
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2277
Защитное действие апелина при ишемиче-
МЕХАНИЗМЫ ЗАЩИТНОГО
ском и реперфузионном повреждении сердца.
ДЕЙСТВИЯ АПЕЛИНА
Имеющиеся в современной литературе дан-
ные показывают, что под действием апелина
Запуск каскада реперфузионных киназ
происходит уменьшение ишемического и ре-
(RISK-сигнализация). Кардиопротекторное
перфузионного (И/Р) повреждения миокар-
действие апелина включает стимуляцию ме-
да in vitro и in vivo. В работе Zeng et al. [80] на
ханизмов запрограммированного клеточно-
модели изолированного сердца крысы было
го выживания, которые запускаются репер-
показано, что глобальная ишемия приводит
фузионными киназами (RISK) [87, 88]. Свя-
к значительному увеличению экспрессии
зывание пептидов апелина с рецептором APJ
APJ-рецептора на уровне мРНК и продукции
активирует сигналинг через Gi/o-белок с
белка, а также к ухудшению функции сердца,
дальнейшим фосфорилированием PI3K и
которая существенно улучшается после пер-
Akt-киназы [34, 89] (рис. 2). В пользу акти-
фузии раствором, содержащим апелин-13.
вации Gi/o-белков свидетельствует то, что
Кроме того, эти же авторы на модели анок-
апелин снижает стимулированную форско-
сии/реоксигенации неонатальных кардио-
лином и гормонами активность аденилат-
миоцитов крысы продемонстрировали, что
циклазы в клетках, где экспрессируется ре-
апелин-13 уменьшает апоптоз и генерацию
цептор APJ [90]. Существенно, что данный
активных форм кислорода (АФК), увеличи-
путь включает образование NO в результа-
вает активность супероксиддисмутазы (SOD)
те активации eNOS протеинкиназой В (Akt).
и снижает образование малонового диальде-
Последующая активация гуанилатциклазы
гида (MDA) [80]. На модели изолированного
под действием NO приводит к образованию
сердца крысы Rastaldo et al. [81] показали от-
сGMP, который, в свою очередь, активирует
сутствие достоверного влияния апелина-13 на
протеинкиназу G (PKG) и ε-изоформу проте-
снижение размера инфаркта миокарда (ИМ)
инкиназы С (PKC). Следствием этого явля-
и повреждение клеточных мембран при вве-
ется открытие митохондриальных ATP-зави-
дении пептида до ишемии. Однако перфузия
симых К+-каналов (mitoK+ATP-каналов), ини-
апелином-13 по окончании периода глобаль-
циирующих закрытие митохондриальной
ной ишемии приводила к уменьшению ИМ
поры (mPTP) [88, 91]. Участие mitoK+ATP-ка-
вдвое, по сравнению с контролем, и ограни-
налов в механизмах защитного действия апе-
чению реперфузионной контрактуры, а так-
линов было подтверждено тем, что 5-гидрок-
же к снижению активности лактатдегидро-
сидеканоат (5-HD) - ингибитор mitoK+ATP-
геназы (LDH) в миокардиальном эффлюенте.
каналов - отменял/снижал влияние С-кон-
Существенно, что эти эффекты отменялись
цевых фрагментов апелина-12 на разме-
в присутствии ингибитора NO-синтазы NG-
ры ИМ [92]. Еще одной мишенью Akt явля-
нитро-L-аргинина (L-NNA), демонстрируя
ется киназа гликогенсинтазы-3β (GSK-3β).
NO-зависимый механизм кардиозащитного
В результате ингибирования GSK-3β проис-
действия апелина. Кроме того, было показано,
ходит блокирование открытия митохондри-
что ишемический период увеличивает экс-
альной поры и, как следствие, - защита клет-
прессию APJ-рецептора на уровне белка [81].
ки от гибели [88, 93].
Simpkin et al. [82] провели сравнительное ис-
Другие сигнальные пути связаны с ак-
следование эффективности действия двух
тивацией Ras-белков [89, 94], приводящей к
С-концевых фрагментов: апелина-13 и апе-
запуску митоген-активируемого протеинки-
лина-36. На модели изолированного сердца
назного (MAP-киназного) каскада. Так, со-
крысы и острого ИМ у мышей in vivo под дей-
пряжение APJ с Gi/o может стимулировать
ствием апелина-13 уменьшение размеров ИМ
передачу сигнала через PKC - активатор мало-
происходило в большей степени, чем под дей-
го G-белка Ras. Ras затем активирует МАP-
ствием апелина-36. В хронических экспери-
киназный каскад Raf-1 → MEK1/2 → ERK1/2.
ментах in vivo пятидневное введение крысам
Данные МАР-киназы подавляют проапопто-
[Pyr1]апелина-13 после окклюзии коронарной
тические белки BAX и BAD либо напрямую,
артерии уменьшало размеры ИМ к оконча-
либо посредством дистальных сигнальных
нию двухнедельного периода реперфузии [83].
компонентов, таких как рибосомальные p70S6-
В ряде работ показано, что кардиозащитное
и p90RS-киназы, что, в свою очередь, приво-
действие пептидов апелина при И/Р-повреж-
дит к ингибированию высвобождения цито-
дении связано с активацией PI3K → Akt → NO
хрома с (Сyt c), препятствуя открытию mPTP
и MEK1/2 → ERK1/2 сигнальных путей в кар-
(рис. 2). Сопряжение APJ с Gq/11 может сти-
диомиоцитах [81, 84-86].
мулировать передачу сигнала через фосфо-
БИОХИМИЯ том 88 вып. 11 2023
2278
ПИСАРЕНКО, СТУДНЕВА
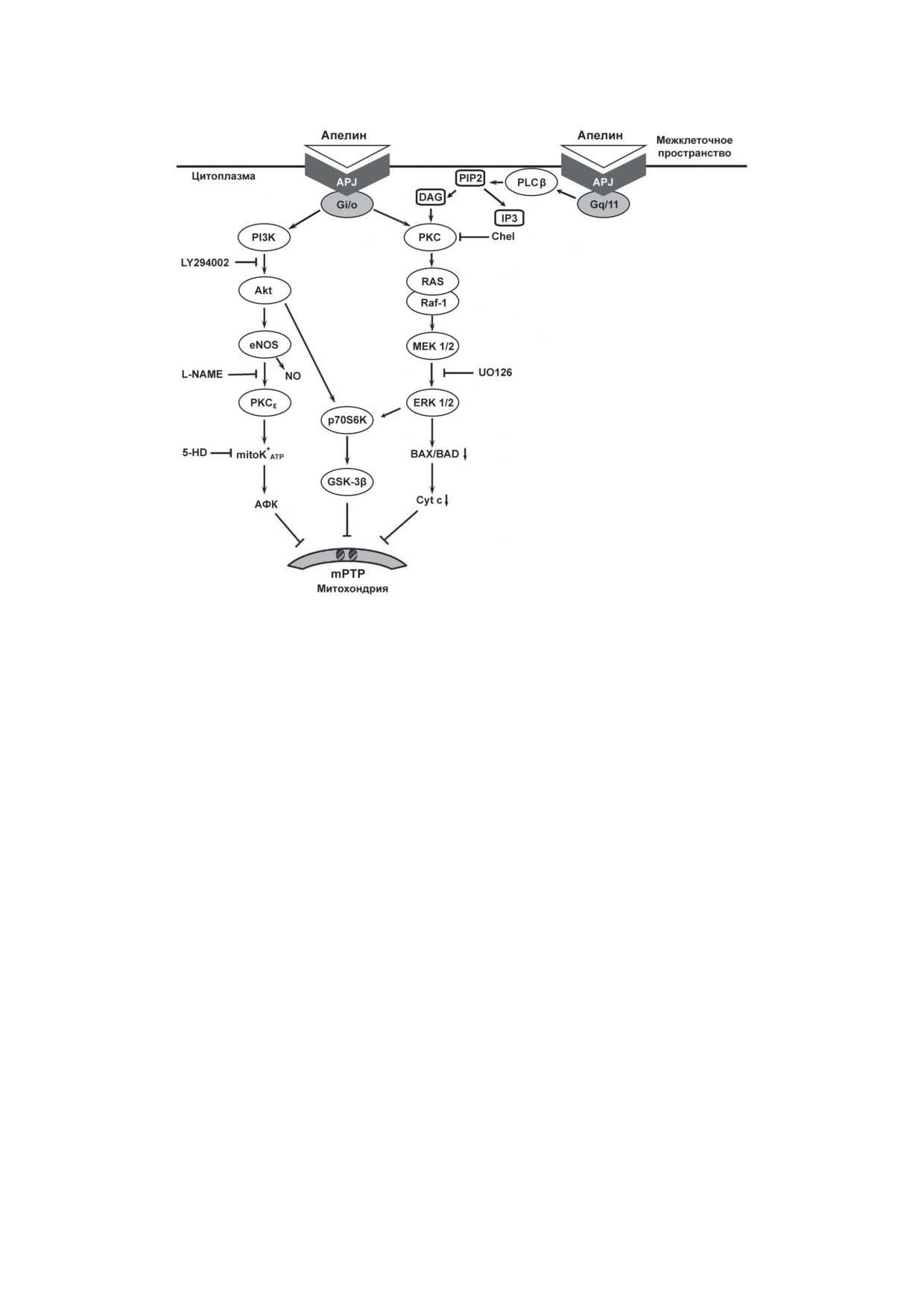
Рис. 2. Активация RISK-сигнализации системой апелин/рецептор APJ в ишемизированном кардиомиоците пред-
упреждает открытие митохондриальной поры (mPTP). Ras - семейство малых G-белков; MEK1/2 - киназа ми-
тоген-активируемой протеинкиназы (MAP2K); ERK1/2
- киназа, регулируемая внеклеточными сигналами;
BAX/BAD - проапоптотические белки; Cyt c - цитохром c; PI3K - фосфатидилинозитол-3-киназа; Akt - протеин-
киназа В; eNOS - эндотелиальная NO-синтаза; PKCε - ε-изоформа протеинкиназы С; mitoK+ATP-каналы - мито-
хондриальные ATP-зависимые К+-каналы; GSK-3β - киназа гликогенсинтазы 3β; p70S6K - рибосомная протеиновая
киназа S6 β1; Chel - хелеритрин; PLCβ - фосфолипаза Сβ; PIP2 - фосфатидилинозитол-4,5-биcфосфат; IP3 - ино-
зитол-1,4,5-трисфосфат; DAG - диацилглицерол; АФК - активные формы кислорода; LY294002 - селективный ин-
гибитор PI3К; Raf-1 - серин/треониновая протеинкиназа
липазу Сβ (PLCβ), включающую гидролиз
биторами ERK1/2 (UO126 или PD098059) [44]
фосфатидилинозитол-4,5-биcфосфата (PIP2)
или ингибитором p70S6-киназы рапамици-
до инозитол-1,4,5-триcфосфата (IP3) и диацил-
ном [90] отменяет действие апелина-13 на
глицерола (DAG). DAG далее активирует про-
митохондриальную пору и приводит к гибели
теинкиназу С (PKC). В результате активации
кардиомиоцитов, усиливая некроз и апоптоз.
RAS под действием PKC происходит запуск
Механизмы антиоксидантной защиты. По-
МАP-киназного каскада Raf-1 → MEK1/2 →
мимо ингибирования открытия mPTP, умень-
→ ERK1/2. Наконец, Gq/11 может сигнализиро-
шение реперфузионного повреждения мио-
вать независимо от PLCβ и PKC через Ras и
карда под действием апелина может быть свя-
этот каскад MAPK [93]. (Этот путь не пред-
зано с антиоксидантными свойствами NO.
ставлен на рис. 2.)
В культуре кардиомиоцитов при моделирова-
Активация MAP-киназных каскадов свя-
нии гипоксии и реоксигенации экзогенный
зана с реперфузионным повреждением и нару-
апелин-13 уменьшал образование вторичного
шениями сердечного ритма. Было показано,
продукта свободнорадикального окисления
что изменения в сигнальных путях МАР-ки-
липидов MDA и супероксидного анион-ради-
наз у больных после кардиохирургических
кала (О•-), а также увеличивал экспрессию
вмешательств, кардиоплегии и искусственно-
антиоксидантного фермента SOD, утилизи-
го кровообращения, участвуют в коронарной
рующей О•- [80]. Было показано, что при вве-
микроциркуляционной дисфункции с нега-
дении апелина-13 отмечаются меньшие нару-
тивными последствиями для перфузии мио-
шения структуры мембран кардиомиоцитов и
карда [95]. Блокирование RISK-сигнализации
снижение продукции MDA в поврежденном
(рис. 2) селективными ингибиторами PI3К
изопротеренолом миокарде крыс in vivo [96].
(LY294002 или вортманнином) [80, 82], инги-
Подавление окислительного стресса, инду-
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2279
цированного пероксидом водорода (Н2О2) в
изолированных неонатальных кардиомиоци-
тах крысы, с помощью [Pyr1]апелина-13 со-
провождалось повышением уровня мРНК и
активности каталазы (CAT) [97]. Также у мы-
шей in vivo под действием диеты, обогащен-
ной [Pyr1]апелином-13, снижение гипертро-
фии ЛЖ сопровождалось уменьшением кон-
центрации липогидропероксидов в плазме и
увеличением активности CAT в миокарде [97].
Таким образом, действие апелина может быть
связано со снижением генерирования АФК,
вызванным возрастанием экспрессии генов,
кодирующих SOD и CАТ и увеличением про-
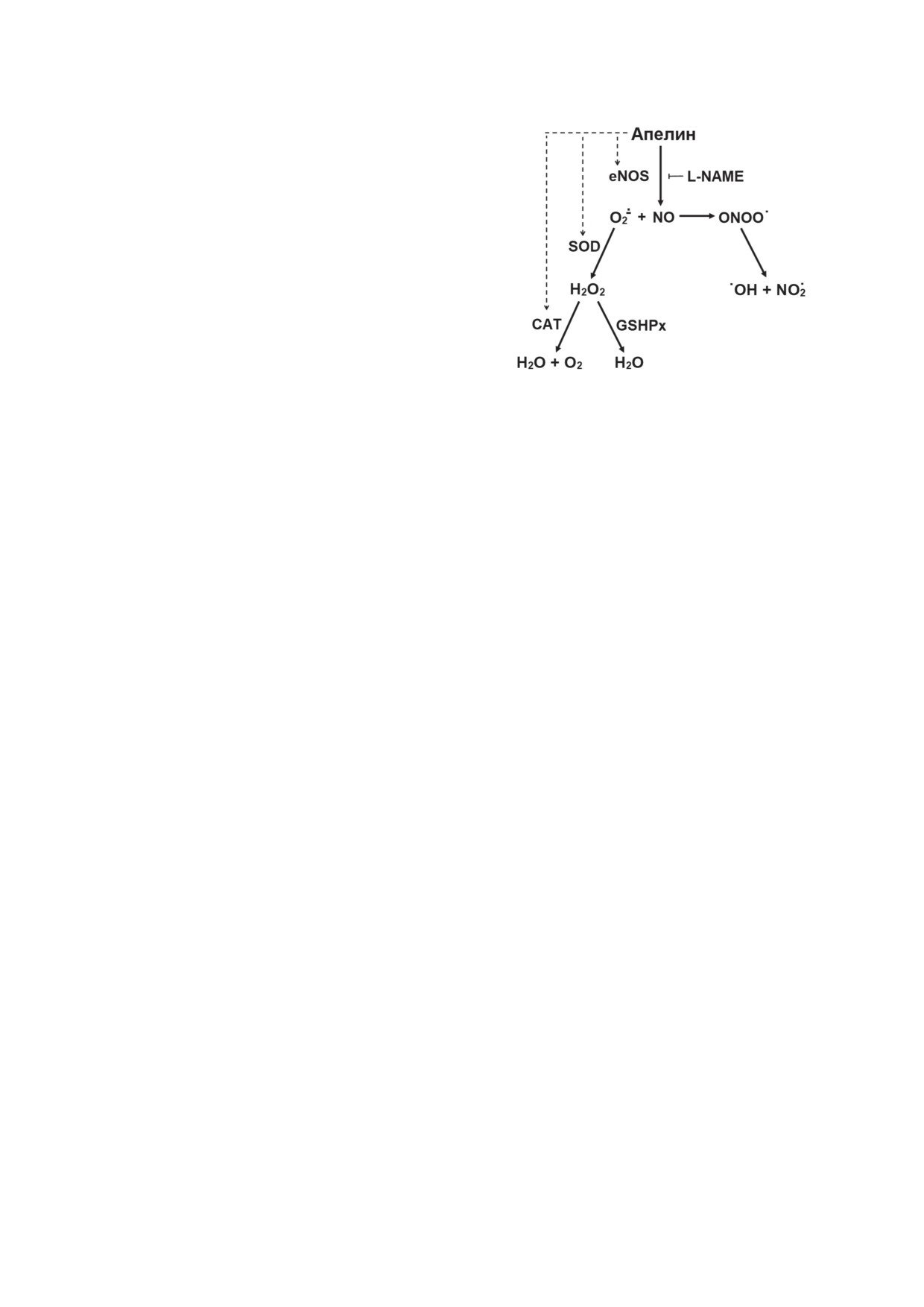
Рис. 3. Антиоксидантное действие апелина. eNOS - эн-
дукции NO.
дотелиальная NO-синтаза; SOD
- супероксиддисму-
В присутствии NO О•- образует перокси-
таза; CAT - каталаза; GSHPx - глутатионпероксидаза;
нитрит (ONOO•), который расщепляется на
L-NAME - ингибитор eNOS метиловый эфир N-нитро-
высокоактивный цитотоксичный гидроксиль-
L-аргинина
ный радикал (•ОН) и радикал диоксида азо-
та (NО•) (рис. 3) [98]. Наличие АФК и азота
(О•-, ONOO•, •ОН, NО•) приводит к дисфунк-
тидов апелина по отношению к действию ами-
ции и гибели клеток. Можно предположить,
но- и карбоксипептидаз в биологических си-
что удаление избытка супероксида за счет
стемах [18] обусловила новое направление ра-
повышения активности SOD под влиянием
бот, связанных с синтезом фармакологических
апелина должно уменьшать окислительный
агонистов APJ-рецептора. Было показано, что
стресс. В то же время увеличение активности
циклические аналоги апелина (рис. 4) связы-
SOD способствует образованию Н2О2, менее
ваются с апелиновым рецептором и обладают
токсичного соединения, но также способного
функциональной активностью, обусловленной
инициировать повреждения миокарда. Как
запуском внутриклеточной сигнализации [99,
известно, Н2О2 разлагается на воду и кисло-
100]. В работе Macaluso et al. [99] по оценке
род под действием CАТ [97], активность кото-
возможностей конкурентного связывания с
рой может возрастать под действием апелина.
APJ циклических фрагментов апелина-13 раз-
Также пероксид водорода может быть транс-
личной длины (рис. 4) было выяснено, что
формирован в воду под действием глутатион-
соединения, содержащие последовательность
пероксидазы (GSHPx) в результате окисления
Arg-Pro-Arg-Leu, демонстрируют четко опре-
восстановленного глутатиона до дисульфида
деленный β-поворот, необходимый для свя-
глутатиона. Поскольку апелин активирует эн-
зывания с рецептором. Циклические аналоги
дотелиальную NO-синтазу, то образующийся
апелина-12 показали дозозависимый ингиби-
вследствие этого NO способен конкурировать
торный эффект по отношению к форсколин-
с SOD за супероксид-анион О•-. Вероятно, уве-
индуцированному накоплению сAMP. Кроме
личения активности SOD под действием апе-
того, они, аналогично природному пептиду,
лина достаточно для того, чтобы предупре-
могут влиять на пути внутриклеточной сигна-
ждать образование цитотоксичного ONOO•
лизации [100].
и тем самым снижать нежелательные послед-
Модификации апелина-13 и апелина-36.
ствия окислительного стресса.
В работе Wang et al. [101] было изучено влияние
Этот гипотетический механизм частично
двух структурных аналогов [Pyr1]апелина-13,
объясняет, каким образом С-концевые фраг-
включающих бромирование С-концевого фе-
менты апелина могут участвовать в регуляции
нилаланина, на И/Р-повреждение сердца у мы-
свободнорадикального окисления и улучшать
шей in vivo. При этом наиболее оптимальная
антиоксидантный потенциал ишемизирован-
модификация пептида не приводила к ухуд-
ного сердца при реперфузии.
шению кардиопротекторных свойств по срав-
нению с природным [Pyr1]апелином-13. Вве-
дение этой структуры уменьшало размер ИМ
СТРУКТУРНЫЕ АНАЛОГИ АПЕЛИНА
у мышей, по сравнению с контролем, более
чем в 2 раза. Одновременно наблюдалась мень-
Циклические аналоги апелина-12 и
-13.
шая деградация модифицированной структуры
Необходимость повышения устойчивости пеп-
под действием ACE2. Влияние модификации
БИОХИМИЯ том 88 вып. 11 2023
2280
ПИСАРЕНКО, СТУДНЕВА
105] показали, что замена или удаление С-кон-
цевого Phe снижает гипотензивные свойства
апелина-13 и ингибирует интернализацию
апелинового рецептора. Кроме того, Iturrioz
et al. [105] продемонстрировали наличие гид-
рофобной полости в нижней части кармана
связывания рецептора APJ, в которую вклады-
вается С-концевой Phe пептидов апелина-13
или апелина-17 благодаря Trp152, Trp259 и Phe255,
которые, как было установлено с помощью мо-
лекулярного моделирования, являются ключе-
выми аминокислотными остатками для ин-
тернализации рецептора. Однако имеются дан-
ные, свидетельствующие о том, что удаление
или замена С-концевого Phe влияет только
на интернализацию рецептора APJ, но не
оказывает влияния на связывание апелина
с рецептором или сопряжение с G-белком.
Так, Pitkin et al. [106] показали, что структура,
аналогичная [Pyr1]апелин-13, без С-концево-
го Phe обнаруживала сродство к апелиновому
рецептору и проявляла активность агониста
в опытах in vitro на подкожной вене человека.
Macaluso et al. [107] удалось создать антагонист
рецептора APJ со свойствами конкурентного
ингибитора, состоящий из двух циклизован-
ных последовательностей Arg-Pro-Leu-Arg, со-
единенных между собой линкерным участком
Рис. 4. Циклические аналоги апелина-13 и апелина-12.
Lys-His. Работы Murza et al. [30] по изучению
Апелин-13 - линии обозначают амидные связи между N-
возможности связывания соединений пептид-
и C-концами (циклизация «от головы к хвосту»). Затем-
ненные кружки обозначают аминокислотные остатки с
ной природы с APJ-рецептором привели к со-
наименьшим влиянием на связывание с рецептором АPJ.
зданию ряда синтетических агонистов с бо-
Апелин-12 - линии обозначают связи между аминокис-
лее высоким сродством и протеолитической
лотными остатками; СО - карбонильная группа
устойчивостью в плазме по сравнению с при-
родным [Pyr1]апелином-13.
апелина-36 по N-концу полиэтиленгликолем
Структурные аналоги апелина-12. С целью
(ПЭГ, 40 кДа) было изучено на крысах в ра-
повышения протеолитической устойчивости
боте Jia et al. [102]. Инфузия конъюгата ПЭГ-
природного апелина-12 и стабильности при
апелин-36 в течение 20 минут поддерживала
хранении были синтезированы его структур-
более высокий уровень апелина-36 в плазме
ные аналоги (табл. 2) [108, 109].
крови в течение 2 часов и обеспечивала увели-
Одна из модификаций апелина-12 заклю-
чение фракции выброса сердца по сравнению
чалась в метилировании N-концевого Arg
с инфузией немодифицированного апелина-36
(пептиды AII и AIII). Показано, что введение
после моделирования ИМ у крыс.
в пептидную цепь Nα-метиламинокислот су-
Также впервые был синтезирован не-
щественно повышает устойчивость этих со-
пептидный агонист апелинового рецептора
единений к ферментативной биодеградации,
Е339-3D6, который проявил себя как частич-
в том числе к действию аминопептидаз [110,
ный агонист в отношении образования cAMP
111]. Кроме того, С-концевая часть молекул
и как полный агонист в отношении интерна-
пептидов AIII и AIV была защищена от дей-
лизации рецептора APJ [103]. Это соединение
ствия карбоксипептидаз амидной группой.
более эффективно препятствовало вазокон-
Модификация AIV заключалась также во вве-
стрикции колец аорты крысы, вызванной нор-
дении нитрогруппы в гуанидиновую группу
адреналином, по сравнению с природным апе-
остатка Arg для увеличения продукции NO.
лином-17.
Стабильность этих структурных аналогов апе-
Результаты исследований по влиянию мо-
лина-12 при хранении была повышена за
дификации С-концевой части молекулы апе-
счет замены легко окисляющегося Met на
лина на связывание с APJ-рецептором [18, 104,
Nle - природную аминокислоту небелкового
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2281
Таблица 2. Апелин-12 и его структурные аналоги
Структура
М, г/моль
Обозначения пептидов
H-Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Met-Pro-Phe-OH
1422,7
Апелин-12
H-(NαMe)Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Nle-Pro-Phe-OH
1418,7
AII
H-(NαMe)Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Nle-Pro-Phe-NH2
1417,7
AIII
H-(NGNO2)Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Nle-Pro-Phe-NH2
1448,7
AIV
H-Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-Pro-Met-Pro-dAla-OH
1346,6
AV
Примечание. Модификации в структуре природного апелина-12 выделены жирным шрифтом.
происхождения, устойчивую к окислению кис-
Pro-Nle-Pro-Phe-OH (AII). Роль сигнальных ме-
лородом. Для оценки роли С-концевого Phe
ханизмов, участвующих в посткондициониро-
в кардиопротекторном действии апелина-12
вании сердца с AII, была изучена на анестези-
при ишемии и реперфузии сердца эта амино-
рованных крысах in vivo, подвергнутых окклю-
кислота была заменена на d-Ala в модифика-
зии коронарной артерии и восстановлению ко-
ции AV. Полученные аналоги апелина-12 были
ронарного кровотока [85]. Ингибиторы MEK1/2
исследованы на моделях различного физио-
и PI3K (UO126 и LY294002 соответственно)
логического уровня при ишемии и реперфузии
снижали защитную эффективность AII. Об этом
сердца.
свидетельствовала отмена ограничения разме-
Было показано, что синтезированные на
ров ИМ, ослабление метаболического восста-
основе апелина-12 агонисты рецептора APJ
новления зоны риска ЛЖ сердца и наруше-
способны подавлять процессы свободноради-
ния целостности сарколеммы при совмест-
кального окисления в культуре кардиомиоци-
ном введении АII с этими ингибиторами. Это
тов в изолированном перфузируемом сердце и
показывает, что MEK1/2 и PI3K являются
в целом организме [112]. Их действие включает
принципиально важными внутриклеточными
перехват супероксид-аниона, снижение про-
молекулами, участвующими в эффектах AII,
дукции пероксида водорода в митохондриях
так же, как и в случае природного апелина-13
кардиомиоцитов, а также уменьшение образо-
и апелина-36 [80, 82]. Дополнительно было
вания АФК в ишемизированном миокарде при
выяснено, что ингибирование NO-синтазы
реперфузионном стрессе. Снижение генерации
(NOS) с помощью метилового эфира N-нитро-
короткоживущих АФК под действием этих пеп-
L-аргинина (L-NAME) снижает полезные эф-
тидов сочетается с уменьшением образования
фекты АII при посткондиционировании серд-
продуктов свободнорадикального окисления
ца крыс in vivo [85]. Как известно, образование
липидов в моделях ex vivo и in vivo и уменьше-
NO приводит к открытию mitoK+ATP-каналов,
нием Cu2+-индуцированного окисления липо-
препятствуя открытию mPTP [117, 118]. Введе-
протеидов низкой плотности в плазме крови
ние блокатора mitoK+ATP-каналов (5-HD) со-
человека in vitro [113, 114]. Антиоксидантные
вместно с АII отменяло влияние пептида на
эффекты аналогов апелина-12 в реперфузиро-
снижение размера ИМ, уменьшение активно-
ванном миокарде проявляются увеличением
сти маркеров некроза и ухудшало метаболиче-
активности Cu,Zn-SOD, CAT и GSHPx [113],
ское восстановление зоны риска к окончанию
которое, вероятно, связано с экспрессией ге-
реперфузии [92], указывая на участие агони-
нов этих ферментов под влиянием пепти-
ста AII в этом механизме защиты. Недавно
дов [97]. Существенно, что защита миокарда от
была завершена разработка новой технологии
реперфузионного повреждения на различных
синтеза структурного аналога АII с использо-
экспериментальных моделях фармакологиче-
ванием Fmoc-методологии в сочетании с вре-
скими агонистами APJ, состоящими из 12 а.о.,
менной защитой гуанидиновых остатков Arg
включает уменьшение повреждения мембран
протонированием (солеобразованием) на ста-
кардиомиоцитов и улучшение энергетического
дии образования амидной связи [119]. Она
состояния кардиомиоцитов [109, 114-116].
позволила исключить образование побочных
В нашей лаборатории было показано, что
продуктов и повысить целевой выход пептида.
одним из наиболее эффективных структур-
Существенно, что изучение биоактивности по-
ных аналогов апелина-12 является пептид
лученного по новой схеме агониста АII на
H-(NαMe)Arg-Pro-Arg-Leu-Ser-His-Lys-Gly-
кроликах с хронической сердечной недоста-
БИОХИМИЯ том 88 вып. 11 2023
2282
ПИСАРЕНКО, СТУДНЕВА
точностью (ХСН), вызванной длительным
Gly-Pro-Nle-Pro-Phe-OH (AII), оказывающий
введением доксорубицина, подтвердило его
мощное влияние на сердце в условиях дефи-
способность уменьшать дисфункцию ЛЖ при
цита кислорода и энергетических субстратов.
инфузии. Очевидно, что эта технология может
Он обеспечивает меньшее повреждение функ-
быть использована для синтеза фармакологи-
ции сердца при окислительном стрессе, сни-
ческих лигандов рецептора АРJ с метилиро-
жает необратимые повреждения кардиомио-
ванным N-концевым аргинином, которые мо-
цитов и улучшает метаболическое состояние
гут иметь терапевтический потенциал.
миокарда после ишемии и реперфузии, а так-
же обладает выраженными антиоксидантными
свойствами. Структурный аналог АII не усту-
ЗАКЛЮЧЕНИЕ
пает по эффективности кардиозащиты при-
родным пептидам апелину-12, апелину-13 и
Результаты исследований, выполненных в
[Pуr1]апелину-13. Мы полагаем, что это соеди-
различных лабораториях в течение последнего
нение, доклиническое исследование которого
двадцатилетия, показали, что система апелин/
завершается в настоящее время, может найти
рецептор APJ является важным регулятором
применение при терапии целого ряда заболе-
сердечно-сосудистой системы в нормальных и
ваний, связанных с сердечной патологией.
патологических условиях. Создание фармако-
логических лигандов рецептора APJ, которые
Вклад авторов. О.И. Писаренко - концеп-
обладают повышенной устойчивостью к воз-
ция и руководство работой, И.М. Студнева -
действию протеолитических ферментов и ста-
анализ данных литературы. Оба автора под-
бильностью при хранении, указывает на воз-
готовили рукопись к печати.
можность разработки новых лекарственных
Финансирование. Работа выполнена при
средств для применения при реперфузионном
финансовой поддержке Российского фонда
повреждении сердца, сердечной недостаточ-
фундаментальных исследований (гранты
ности и окислительном стрессе. Наши рабо-
№№ 18-015-0008-а и 18-015-0009-а).
ты показывают, что одним из перспективных
Благодарности. Авторы признательны
подходов к созданию таких лигандов является
М.В. Сидоровой и Ю.А. Пелогейкиной за цен-
модификация С- и N-концевых остатков ами-
ные советы при обсуждении этого обзора.
нокислот в молекуле апелина-12, обладающего
Конфликт интересов. Авторы заявляют об
высокой биологической активностью, и замена
отсутствии конфликта интересов.
остатка легко окисляющегося Met на Nle [108].
Соблюдение этических норм. Настоящая
Это позволило синтезировать устойчивый к
статья не содержит описания каких-либо ис-
действию протеаз аналог природного апели-
следований с участием людей или животных
на-12 H-(NαMe)Arg-Pro-Arg-Leu-Ser-His-Lys-
в качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1. Coelho, M., Oliveira, T., and Fernandes, R. (2013) Bio-
tensin receptor is located on chromosome 11, Gene,
chemistry of adipose tissue: an endocrine organ, Arch.
136, 355-360, doi: 10.1016/0378-1119(93)90495-o.
Med. Sci., 9, 191-200, doi: 10.5114/aoms.2013.33181.
5. Cai, X., Bai, B., Zhang, R., Wang, Ch., and Chen, J.
2. Castan-Laurell, I., Masri, B., and Valet, P. (2019)
(2017) Apelin receptor homodimer-oligomers revealed
The apelin/APJ system as a therapeutic target in
by single-molecule imaging and novel G protein-
metabolic diseases, Expert. Opin. Ther. Targets, 23,
dependent signaling, Sci. Rep., 7, 40335, doi: 10.1038/
215-225, doi: 10.1080/14728222.2019.1561871.
srep40335.
3. Kinjo, T., Higash, H., Un, K., and Kuramoto, N.
6. Charo, D. N., Ho, M., Fajardo, G., Kawana, M.,
(2021) Apelin/apelin receptor system molecular char-
Kundu, R. K., Sheikh, A. Y., Finsterbach, Th. P.,
acteristics, physiological roles, and prospects as a
Leeper, N. J., Ernst, K. V., Chen, M. M., Ho, Y. D.,
target for disease prevention and pharmacothera-
Chun, H. J., Bernstein, D., Ashley, E. A., and
py, Curr. Mol. Pharmacol., 14, 210-221, doi: 10.2174/
Quertermous, Th. (2009) Endogenous regulation of
1874467213666200602133032.
cardiovascular function by apelin-APJ, Am. J. Physi-
4. O’Dowd, B. F., Heiber, M., Chan, A., Heng, H. H.,
ol. Heart Circ. Physiol., 297, 1904-1913, doi: 10.1152/
Tsui, L. C., Kennedy, J. L., Shi, X., Petronis, A.,
ajpheart.00686.2009.
George, S. R., and Nguyen, T. (1993) A human gene
7. Li, Y., Chen, J., Bai, B., Du, H., Liu, Y., and Liu, H.
that shows identity with the gene encoding the angio-
(2012) Heterodimerization of human apelin and kappa
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2283
opioid receptors: roles in signal transduction, Cell
Dupré, D. J., and Rainey, J. K. (2017) Bioactivi-
Signal., 24, 991-1001, doi: 10.1016/j.cellsig.2011.12.012.
ty of the putative apelin proprotein expands the rep-
8.
Abbasloo, E., Najafipour, H., and Esmaeili-Mahani, S.
ertoire of apelin receptor ligands, Biochim. Biophys.
(2016) Induction of antinociceptive tolerance to the
Acta Gen. Sub.,
1861,
1901-1912, doi:
10.1016/j.
chronic intrathecal administration of apelin-13 in
bbagen.2017.05.017.
rat, Neuropeptides,
60,
7-12, doi:
10.1016/j.npep.
20.
Shin, K., Pandey, A., Liu, X. Q., Anini, Y., and
2016.08.001.
Rainey, J. K. (2013) Preferential apelin-13 production
9.
Tatemoto, K., Hosoya, M., Habata, Y., Fujii, R.,
by the proprotein convertase PCSK3 is implicated in
Kakegawa, T., Zou, M. X., Kawamata, Y., Fukusumi, S.,
obesity, FEBS Open Bio., 3, 328-333, doi: 10.1016/
Hinuma, S., Kitada, C., Kurokawa, T., Onda, H., and
j.fob.2013.08.001.
Fujino, M. (1998) Isolation and characterization of a
21.
Adam, F., Khatib, A. M., Lopez, J. J., Vatier, C.,
novel endogenous peptide ligand for the human APJ
Turpin, S., Muscat, A., Soulet, F., Aries, A., Jardin, I.,
receptor, Biochem. Biophys. Res. Commun., 251, 471-
Bobe, R., Stepanian, A., de Prost, D., Dray, C.,
476, doi: 10.1006/bbrc.1998.9489.
Rosado, J. A., Valet, P., Feve, B., and Siegfried, G.
10.
Kawamata, Y., Habata, Y., Fukusumi, S., Hosoya, M.,
(2016) Apelin: an antithrombotic factor that inhibits
Fujii, R., Hinuma, S., Nishizawa, N., Kitada, C.,
platelet function, Blood, 127, 908-920, doi: 10.1182/
Onda, H., Nishimura, O., and Fujino, M. (2001)
blood-2014-05-578781.
Molecular properties of apelin: tissue distribution and
22.
McKinnie, S. M., Fischer, C., Tran, K. M., Wang, W.,
receptor binding, Biochim. Biophys. Acta, 1538, 162-
Mosquera, F., Oudit, G. Y., and Vederas, J. C. (2016)
171, doi: 10.1016/s0167-4889(00)00143-9.
The metalloprotease neprilysin degrades and inac-
11.
Roberts, E. M., Newson, M. J. F., Pope, G. R.,
tivates apelin peptides, Chem. Bio. Chem., 17, 1495-
Landgraf, R., Lolait, S. J., and O’Carroll, A. M.
1498, doi: 10.1002/cbic.201600244.
(2009) Abnormal fluid homeostasis in apelin recep-
23.
Vickers, C., Hales, P., Kaushik, V., Dick, L., Gavin, J.,
tor knockout mice, J. Endocrinol., 202, 453-462,
Tang, J., Godbout, K., Parsons, T., Baronas, E.,
doi: 10.1677/JOE-09-0134.
Hsieh, F., Acton, S., Patane, M., Nichols, A., and
12.
Mughal, A., and O’Rourke, S. T. (2018) Vascular ef-
Tummino, P. (2002) Hydrolysis of biological peptides
fects of apelin: mechanisms and therapeutic poten-
by human angiotensin-converting enzyme-related
tial. Pharmacol. Ther., 190, 139-147, doi: 10.1016/
carboxypeptidase, J. Biol. Chem., 277, 14838-14843,
j.pharmthera.2018.05.013.
doi: 10.1074/jbc.M200581200.
13.
Bertrand, C., Valet, P., and Castan-Laurell, I. (2015)
24.
Kehoe, K., Elzen, R., Verkerk, R., Sima, Y., van
Apelin and energy metabolism, Front. Physiol., 6,
der Veken, P., Lambeir, A. M., and De Meester, I.
115, doi: 10.3389/fphys.2015.00115.
(2016) Prolyl carboxypeptidase purified from human
14.
Chung, S. C., Ho, L., Tian, J., and Reversade, B.
placenta: its characterization and identification as an
(2013) ELABELA: a hormone essential for heart
apelin-cleaving enzyme, Biochim. Biophys. Acta, 1864,
development signals via the Apelin receptor, Dev. Cell.,
1481-1488, doi: 10.1016/j.bbapap.2016.07.004.
27, 672-680, doi: 10.1016/j.devcel.2013.11.002.
25.
Fischer, C., Lamer, T., Wang, W., McKinnie, S. M. K.,
15.
Lee, D. K., Cheng, R., Nguyen, T., Fan, T.,
Iturrioz, X., Llorens-Cortes, C., Oudit, G. Y., and
Kariyawasam, A. P., Liu, Y., Osmond, D. H., George,
Vederas, J. C. (2019) Plasma kallikrein cleaves and
S. R., and O’Dowd, B. F. (2000) Characterization of
inactivates apelin-17: palmitoyl- and PEG-extended
apelin, the ligand for the APJ receptor, J. Neurochem.,
apelin-17 analogs as metabolically stable blood
74, 34-41, doi: 10.1074/jbc.M908417199.
pressure-lowering agents, Eur. J. Med. Chem., 166,
16.
Hosoya, M., Kawamata, Y., Fukusumi, S., Fujii, R.,
119-124, doi: 10.1016/j.ejmech.2019.01.040.
Habata, Y., Hinuma, S., Kitada, C., Honda, S.,
26.
Ma, Y., Yue, Y., Ma, Y., Zhang, Q., Zhou, Q., Song, Y.,
Kurokawa, T., Onda, H., Nishimura, O., and Fujino, M.
Shen, Y., Li, X., Ma, X., Li, C., Hanson, M. A.,
(2000) Molecular and functional characteristics of
Han, G. W., Sickmier, E. A., Swaminath, G., Zhao, S.,
APJ. Tissue distribution of mRNA and interaction
Stevens, R. C., Hu, L. A., Zhong, W., Zhang, M.,
with the endogenous ligand apelin, J. Biol. Chem.,
and Xu, F. (2017) Structural basis for apelin control of
275, 21061-21067, doi: 10.1074/jbc.M908417199.
the human apelin receptor, Structure, 25, 858-866.e4,
17.
Kleinz, M. J., and Davenport, A. P. (2005) Emerging
doi: 10.1016/j.str.2017.04.008.
roles of apelin in biology and medicine, Pharmacol.
27.
Medhurst, A. D., Jennings, C. A., Robbins, M. J.,
Ther.,
107,
198-211, doi:
10.1016/j.pharmthera.
Davis, R. P., Ellis, C., Winborn, K. Y., Lawrie, K. W.,
2005.04.001.
Hervieu, G., Riley, G., Bolaky, J. E., Herrity, N. C.,
18.
Japp, A. G., and Newby, D. E. (2016) Unlocking the
Murdock, P., and Darker, J. G. (2003) Pharmaco-
therapeutic potential of apelin, Hypertension, 68, 307-
logical and immunohistochemical characterization
309, doi: 10.1161/HYPERTENSIONAHA.116.07057.
of the APJ receptor and its endogenous ligand apelin,
19.
Shin, K., Chapman, N. A., Sarker, M., Kenward, C.,
J. Neurochem., 84, 1162-1172, doi: 10.1046/j.1471-4159.
Huang, S. K., Weatherbee-Martin, N., Pandey, A.,
2003.01587.x.
БИОХИМИЯ том 88 вып. 11 2023
2284
ПИСАРЕНКО, СТУДНЕВА
28.
Langelan, D. N., Bebbington, E. M., Reddy, T., and
S. R., and Davenport, A. P.
(2001)
[125I]-(Pyr1)
Rainey, J. K. (2009) Structural insight into G-protein
Apelin-13 is a novel radioligand for localizing the APJ
coupled receptor binding by apelin, Biochemistry, 48,
orphan receptor in human and rat tissues with evidence
537-548, doi: 10.1021/bi801864b.
for a vasoconstrictor role in man, Br. J. Pharmacol.,
29.
Tyndall, J. D., Pfeiffer, B., Abbenante, G., and Fairlie,
132, 1255-1260, doi: 10.1038/sj.bjp.0703939.
D. P. (2005) Over one hundred peptide-activated
40.
Maguire, J. J., Kleinz, M. J., Pitkin, S. L., and
G protein-coupled receptors recognize ligands with
Davenport, A. P. (2009) [Pyr1]apelin-13 identified
turn structure, Chem. Rev., 105, 793-826, doi: 10.1021/
as the predominant apelin isoform in the human
cr040689g.
heart: vasoactive mechanisms and inotropic action
30.
Murza, A., Parent, A., Besserer-Offroy, E., Tremblay, H.,
in disease, Hypertension, 54, 598-604, doi: 10.1161/
Karadereye, F., Beaudet, N., Leduc, R., Sarret, P., and
HYPERTENSIONAHA.109.134619.
Marsault, É. (2012) Elucidation of the structure-activ-
41.
Kasai, A., Shintani, N., Oda, M., Kakuda, M.,
ity relationships of apelin: influence of unnatural ami-
Hashimoto, H., Matsuda, T., Hinuma, S., and Baba, A.
no acids on binding, signaling, and plasma stability,
(2004) Apelin is a novel angiogenic factor in retinal
Chem. Med. Chem., 7, 318-325, doi: 10.1002/cmdc.
endothelial cells, Biochem. Biophys. Res. Commun.,
201100492.
325, 395-400, doi: 10.1016/j.bbrc.2004.10.042.
31.
Kleinz, M. J., and Davenport, A. P. (2004) Immu-
42.
Cox, C. M., D’Agostino, S. L., Miller, M. K.,
nocytochemical localization of the endogenous va-
Heimark, R. L., and Krieg, P. A. (2006) Apelin, the
soactive peptide apelin to human vascular and endo-
ligand for the endothelial G-protein-coupled receptor,
cardial endothelial cells, Regul. Pept., 118, 119-125,
APJ, is a potent angiogenic factor required for normal
doi: 10.1016/j.regpep.2003.11.002.
vascular development of the frog embryo, Dev. Biol.,
32.
Kleinz, M. J., Skepper, J. N., and Davenport, A. P.
296, 177-189, doi: 10.1016/j.ydbio.2006.04.452.
(2005) Immunocytochemical localization of the apelin
43.
Masri, B., Morin, N., Cornu, M., Knibiehler, B.,
receptor, APJ, to human cardiomyocytes, vascular
and Audigier, Y.
(2004) Apelin
(65-77) activates
smooth muscle and endothelial cells, Regul. Pept., 126,
p70S6 kinase and is mitogenic for umbilical endo-
233-240, doi: 10.1016/j.regpep.2004.10.019.
thelial cells, FASEB J., 18, 1909-1911, doi: 10.1096/
33.
Barnes, G., Japp, A. G., and Newby, D. E. (2010)
fj.04-1930fje.
Translational promise of the apelin-APJ system, Heart,
44.
Li, F., Li, L., Qin, X., Pan, W., Feng, F., Chen, F.,
96, 1011-1016, doi: 10.1136/hrt.2009.191122.
Zhu, B., Liao, D., Tanowitz, H., Albanese, C., and
34.
Chapman, N. A., Dupré, D. J., and Rainey, J. K.
Chen, L. (2008) Apelin-induced vascular smooth
(2024) The apelin receptor: physiology, pathology,
muscle cell proliferation: the regulation of cyclin D1,
cell signalling, and ligand modulation of a peptide-
Front. Biosci., 13, 3786-3792, doi: 10.2741/2967.
activated class A GPCR, Biochem. Cell Biol., 92, 431-
45.
Kasai, A., Shintani, N., Kato, H., Matsuda, S.,
440, doi: 10.1139/bcb-2014-0072.
Gomi, F., Haba, R., Hashimoto, H., Kakuda, M.,
35.
Pitkin, S. L., Maguire, J. J., Bonner, T. I., and Daven-
Tano, Y., and Baba, A. (2008) Retardation of retinal
port, A. P. (2010) International union of basic and clin-
vascular development in apelin deficient mice,
ical pharmacology. LXXIV. Apelin receptor nomencla-
Arterioscler. Thromb. Vasc. Biol.,
28,
1717-1722,
ture, distribution, pharmacology, and function, Pharma-
doi: 10.1161/ATVBAHA.108.163402.
col. Rev., 62, 331-342, doi: 10.1124/pr.110.002949.
46.
Zhang, Q., Shen, Y., Niloy, S. I., O'Rourke, S. T.,
36.
Tatemoto, K., Takayama, K., Zou, M. X., Kumaki, I.,
and Sun, C. (2023) Chronic effects of apelin on
Zhang, W., Kumano, K., and Fujimiya, M. (2001)
cardiovascular regulation and angiotensin II-induced
The novel peptide apelin lowers blood pressure via a
hypertension, Pharmaceuticals (Basel), 16, 600, doi:
nitric oxide-dependent mechanism, Regul. Pept., 99,
10.3390/ph16040600.
87-92, doi: 10.1016/s0167-0115(01)00236-1.
47.
Berry, M. F., Pirolli, T. J., Jayasankar, V., Burdick, J.,
37.
Japp, A. G., Cruden, N. L., Amer, D. A., Li, V. K.,
Morine, K. J., Gardner, T. J., and Woo, Y. J. (2004)
Goudie, E. B., Johnston, N. R., Sharma, S., Neilson, I.,
Apelin has in vivo inotropic effects on normal
Webb, D. J., Megson, I. L., Flapan, A. D., and Newby,
and failing hearts, Circulation,
110, II187-II193,
D. E. (2008) Vascular effects of apelin in vivo in man,
doi: 10.1161/01.CIR.0000138382.57325.5c.
Am. Coll. Cardiol., 52, 908-913, doi: 10.1016/j.jacc.
48.
Aydin, S., Eren, M. N., Sahin, I., and Aydin, S.
2008.06.013.
(2014) The role of apelins in the physiology of the
38.
Salcedo, A., Garijo, J., Monge, L., Fernandez, N.,
heart, Protein Pept. Lett.,
21,
2-9, doi:
10.2174/
Luis García-Villalon, A., Sánchez Turrión, V.,
09298665113209990083.
Cuervas-Mons, V., and Diéguez, G. (2007) Apelin
49.
Szokodi, I., Tavi, P., Földes, G., Voutilainen-Myllylä, S.,
effects in human splanchnic arteries. Role of nitric
Ilves, M., Tokola, H., Pikkarainen, S., Piuhola, J.,
oxide and prostanoids, Regul. Pept.,
144,
50-55,
Rysä, J., Tóth, M., and Ruskoaho, H. (2002) Apelin,
doi: 10.1016/j.regpep.2007.06.005.
the novel endogenous ligand of the orphan receptor
39.
Katugampola, S. D., Maguire, J. J., Matthewson,
APJ, regulates cardiac contractility, Circ. Res., 91,
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2285
434-440, doi: 10.1161/01.res.0000033522.37861.69.
Kováciková, M., Kovacova, Z., Hejnova, J., Stich, V.,
50.
Ashley, E. A., Powers, J., Chen, M., Kundu, R.,
and Valet, P. (2008) Effect of hypocaloric diet-in-
Finsterbach, T., Caffarelli, A., Deng, A., Eichhorn, J.,
duced weight loss in obese women on plasma ape-
Mahajan, R., Agrawal, R., Greve, J., Robbins, R.,
lin and adipose tissue expression of apelin and APJ,
Patterson, A. J., Bernstein, D., and Quertermous, T.
Eur. J. Endocrinol.,
158,
905-910, doi:
10.1530/
(2005) The endogenous peptide apelin potently
EJE-08-0039.
improves cardiac contractility and reduces cardiac
60.
Li, L., Yang, G., Li, Q., Tang, Y., Yang, M., Yang, H.,
loading in vivo, Cardiovasc. Res.,
65,
73-82,
and Li, K. (2006) Changes and relations of circulating
doi: 10.1016/j.cardiores.2004.08.018.
visfatin, apelin, and resistin levels in normal, impaired
51.
Scimia, M. C., Hurtado, C., Ray, S., Metzler, S., Wei, K.,
glucose tolerance, and type 2 diabetic subjects, Exp.
Wang, J., Woods, C. E., Purcell, N. H., Catalucci, D.,
Clin. Endocrinol. Diab., 114, 544-548, doi: 10.1055/
Akasaka, T., Bueno, O. F., Vlasuk, G. P., Kaliman, P.,
s-2006-948309.
Bodmer, R., Smith, L. H., Ashley, E., Mercola, M.,
61.
Castan-Laurell, I., Dray, C., Knauf, C., Kunduzova, O.,
Brown, J. H., and Ruiz-Lozano, P. (2012) APJ acts as
and Valet, P. (2012) Apelin, a promising target for
a dual receptor in cardiac hypertrophy, Nature, 488,
type 2 diabetes treatment? Trends. Endocrinol. Metab.,
394-398, doi: 10.1038/nature11263.
23, 234-241, doi: 10.1016/j.tem.2012.02.005.
52.
De Mota, N., Reaux-Le Goazigo, A., El Messari, S.,
62.
Yue, P., Jin, H., Aillaud, M., Deng, A. C., Azuma, J.,
Chartrel, N., Roesch, D., Dujardin, C., Kordon, C.,
Asagami, T., Kundu, R. K., Reaven, G. M.,
Vaudry, H., Moos, F., and Llorens-Cortes, C. (2004)
Quertermous, T., and Tsao, P. S. (2010) Apelin is
Apelin, a potent diuretic neuropeptide counteracting
necessary for the maintenance of insulin sensitivity,
vasopressin actions through inhibition of vasopressin
Am. J. Physiol. Endocrinol. Metab., 298, E59-E67,
neuron activity and vasopressin release, Proc. Natl.
doi: 10.1152/ajpendo.00385.2009.
Acad. Sci. USA, 101, 10464-10469, doi: 10.1073/
63.
Higuchi, K., Masaki, T., Gotoh, K., Chiba, S.,
pnas.0403518101.
Katsuragi, I., Tanaka, K., Kakuma, T., and Yoshimat-
53.
Reaux-Le Goazigo, A., Morinville, A., Burlet, A.,
su, H. (2007) Apelin, an APJ receptor ligand, regulates
Llorens-Cortes, C., and Beaudet, A. (2004) Dehy-
body adiposity and favors the messenger ribonucleic
dration-induced cross-regulation of apelin and vaso-
acid expression of uncoupling proteins in mice, Endo-
pressin immunoreactivity levels in magnocellular hy-
crinology, 148, 2690-2697, doi: 10.1210/en.2006-1270.
pothalamic neurons, Endocrinology, 145, 4392-4400,
64.
Chen, M. M., Ashley, E. A., Deng, D. X., Tsalenko, A.,
doi: 10.1210/en.2004-0384.
Deng, A., Tabibiazar, R., Ben-Dor, A., Fenster, B.,
54.
Huang, Zh., Luo, X., Liu, M., and Chen, L. (2019)
Yang, E., King, J. Y., Fowler, M., Robbins, R.,
Function and regulation of apelin/APJ system in
Johnson, F. L., Bruhn, L., McDonagh, T., Dargie, H.,
digestive physiology and pathology, J. Cell. Physiol.,
Yakhini, Z., Tsao, P. S., and Quertermous, T. (2003)
234, 7796-7810, doi: 10.1002/jcp.27720.
Novel role for the potent endogenous inotrope apelin
55.
Kunduzova, O., Alet, N., Delesque-Touchard, N.,
in human cardiac dysfunction, Circulation, 108, 12,
Millet, L., Castan-Laurell, I., Muller, C., Dray, C.,
1432-1439, doi: 10.1161/01.CIR.0000091235.94914.75.
Schaeffer, P., Herault, J. P., Savi, P., Bono, F., and
65.
Chong, K. S., Gardner, R. S., Morton, J. J., Ashley,
Valet, P. (2008) Apelin/APJ signaling system: a po-
E. A., and McDonagh, T. A. (2006) Plasma concen-
tential link between adipose tissue and endotheli-
trations of the novel peptide apelin are decreased in
al angiogenic processes, FASEB J., 22, 4146-4153,
patients with chronic heart failure, Eur. J. Heart. Fail.,
doi: 10.1096/fj.07-104018.
8, 355-360, doi: 10.1016/j.ejheart.2005.10.007.
56.
Wei, L., Hou, X., and Tatemoto, K. (2005) Regulation
66.
Miettinen, K. H., Magga, J., Vuolteenaho, O.,
of apelin mRNA expression by insulin and glucocorti-
Vanninen, E. J., Punnonen, K. R., Ylitalo, K.,
coids in mouse 3T3-L1 adipocytes, Regul. Pept., 132,
Tuomainen, P., and Peuhkurinen, K. J.
(2007)
27-32, doi: 10.1016/j.regpep.2005.08.003.
Utility of plasma apelin and other indices of cardiac
57.
Sorhede Winzell, M., Magnusson, C., and Ahren, B.
dysfunction in the clinical assessment of patients with
(2005) The APJ receptor is expressed in pancreat-
dilated cardiomyopathy, Regul. Pept., 140, 178-184,
ic islets and its ligand, apelin, inhibits insulin secre-
doi: 10.1016/j.regpep.2006.12.004.
tion in mice, Regul. Pept., 131, 12-17, doi: 10.1016/
67.
Foldes, G., Horkay, F., Szokodi, I., Vuolteenaho, O.,
j.regpep.2005.05.004.
Ilves, M., Lindstedt, K. A., Mäyränpää, M., Sármán, B.,
58.
Dray, C., Knauf, C., Daviaud, D., Waget, A., Boucher, J.,
Seres, L., Skoumal, R., Lakó-Futó, Z., deChâtel, R.,
Buléon, M., Cani, P. D., Attané, C., Guigné, C.,
Ruskoaho, H., and Tóth, M. (2003) Circulating and
Carpéné, C., Burcelin, R., Castan-Laurell, I., and
cardiac levels of apelin, the novel ligand of the orphan
Valet, P. (2008) Apelin stimulates glucose utilization in
receptor APJ, in patients with heart failure, Biochem.
normal and obese insulin-resistant mice, Cell. Metab.,
Biophys. Res. Commun., 308, 3, 480-485, doi: 10.1016/
8, 437-445, doi: 10.1016/j.cmet.2008.10.003.
s0006-291x(03)01424-4.
59.
Castan-Laurell, I., Vítkova, M., Daviaud, D., Dray, C.,
68.
Ronkainen, V. P., Ronkainen, J. J., Hanninen, S. L.,
БИОХИМИЯ том 88 вып. 11 2023
2286
ПИСАРЕНКО, СТУДНЕВА
Leskinen, H., Ruas, J. L., Pereira, T., Poellinger, L.,
doi: 10.1038/sj.onc.1210573.
Vuolteenaho, O., and Tavi, P.
(2007) Hypoxia
78.
Eyries, M., Siegfried, G., Ciumas, M., Montagne, K.,
inducible factor regulates the cardiac expression
Agrapart, M., Lebrin, F., and Soubrier, F. (2008) Hy-
and secretion of apelin, FASEB J., 21, 1821-1830,
poxia-induced apelin expression regulates endothe-
doi: 10.1096/fj.06-7294com.
lial cell proliferation and regenerative angiogenesis,
69.
Sheikh, A. Y., Chun, H. J., Glassford, A. J., Kundu,
Circ. Res.,
103,
432-440, doi:
10.1161/circresaha.
R. K., Kutschka, I., Ardigo, D., Hendry, S. L.,
108.179333.
Wagner, R. A., Chen, M. M., Ali, Z. A., Yue, P.,
79.
Kidoya, H., Naito, H., and Takakura, N.
(2010)
Huynh, D. T., Connolly, A. J., Pelletier, M. P., Tsao,
Apelin induces enlarged and nonleaky blood vessels
P. S., Robbins, R. C., and Quertermous, T. (2008)
for functional recovery from ischemia, Blood, 115,
In vivo genetic profiling and cellular localization
3166-3174, doi: 10.1182/blood-2009-07-232306.
of apelin reveals a hypoxia-sensitive, endothelial-
80.
Zeng, X. J., Zhang, L. K., Wang, H. X., Lu, L. Q., Ma,
centered pathway activated in ischemic heart failure,
L. Q., and Tang, C. S. (2009) Apelin protects heart
Am. J. Physiol. Heart Circ. Physiol., 294, H88-H98,
against ischemia/reperfusion injury in rat, Peptides,
doi: 10.1152/ajpheart.00935.2007.
30, 1144-1152, doi: 10.1016/j.peptides.2009.02.010.
70.
Hashimoto, T., Kihara, M., Imai, N., Yoshida, S.,
81.
Rastaldo, R., Cappello, S., Folino, A., Berta, G. N.,
Shimoyamada, H., Yasuzaki, H., Ishida, J., Toya, Y.,
Sprio, A. E., Losano, G., Samaja, M., and Pagliaro, P.
Kiuchi, Y., Hirawa, N., Tamura, K., Yazawa, T.,
(2011) Apelin-13 limits infarct size and improves
Kitamura, H., Fukamizu, A., and Umemura, S. (2007)
cardiac postischemic mechanical recovery only if given
Requirement of apelin-apelin receptor system for
after ischemia, Am. J. Physiol. Heart Circ. Physiol.,
oxidative stress-linked atherosclerosis, Am. J. Pathol.,
300, H2308-H2315, doi: 10.1152/ajpheart.01177.2010.
171, 1705-1712, doi: 10.2353/ajpath.2007.070471.
82.
Simpkin, J. C., Yellon, D. M., Davidson, S. M., Lim,
71.
Pitkin, S. L., Maguire, J. J., Kuc, R. E., and
S. Y., Wynne, A. M., and Smith, C. C. (2007) Ape-
Davenport, A. P. (2010) Modulation of the apelin/
lin-13 and apelin-36 exhibit direct cardioprotective ac-
APJ system in heart failure and atherosclerosis in man,
tivity against ischemia- reperfusion injury, Basic Res.
Br. J. Pharmacol., 160, 1785-1795, doi: 10.1111/j.1476-
Cardiol., 102, 518-528, doi: 10.1007/s00395-007-0671-2.
5381.2010.00821.x.
83.
Azizi, Y., Faghihi, M., Imania, A., Roghanib, M.,
72.
Peltonen, T., Napankangas, J., Vuolteenaho, O.,
and Nazari, A. (2013) Post-infarct treatment with
Ohtonen, P., Soini, Y., Juvonen, T., Satta, J.,
[Pyr1]-apelin-13 reduces myocardial damage through
Ruskoaho, H., and Taskinen, P. (2009) Apelin and its
reduction of oxidative injury and nitric oxide en-
receptor APJ in human aortic valve stenosis, J. Heart
hancement in the rat model of myocardial infarction,
Valve Dis., 18, 644-652.
Peptides, 46, 76-82, doi: 10.1016/j.peptides.2013.05.006.
73.
Leeper, N. J., Tedesco, M. M., Kojima, Y., Schultz,
84.
Yang, S., Li, H., Tang, L., Ge, G., Ma, J., Qiao, Z.,
G. M., Kundu, R. K., Ashley, E. A., Tsao, P. S.,
Liu, H., and Fang, W. (2015) Apelin-13 Protects the
Dalman, R. L., and Quertermous, T. (2009) Apelin pre-
Heart against Ischemia-Reperfusion Injury through
vents aortic aneurysm formation by inhibiting macro-
the RISK-GSK-3-MPTP Pathway, Arch. Med. Sci.,
phage inflammation, Am. J. Physiol. Heart Circ. Physiol.,
11, 1065-1073, doi: 10.5114/aoms.2015.54863.
296, H1329-H1335, doi: 10.1152/ajpheart.01341.2008.
85.
Pisarenko, O. I., Shulzhenko, V. S., Studneva, I. M.,
74.
Tiani, C., Garcia-Pras, E., Mejias, M., de Gottardi, A.,
Serebryakova, L. I., Pelogeykina, Y. A., and Veselova,
Berzigotti, A., Bosch, J., and Fernandez, M. (2009)
O. M. (2015) Signaling pathways of a structural ana-
Apelin signaling modulates splanchnic angiogenesis
logue of apelin-12 involved in myocardial protection
and portosystemic collateral vessel formation in rats
against ischemia/reperfusion injury, Peptides, 73, 67-
with portal hypertension, J. Hepatol., 50, 296-305,
76, doi: 10.1016/j.peptides.2015.09.001.
doi: 10.1016/j.jhep.2008.09.019.
86.
An, S., Wang, X., Shi, H., Zhang, X., Meng, H.,
75.
Principe, A., Melgar-Lesmes, P., Fernandez-Varo, G.,
Li, W., Chen, D., and Ge, J. (2020) Apelin protects
del Arbol, L. R., Ros, J., Morales-Ruiz, M., Bernar-
against ischemia-reperfusion injury in diabetic myo-
di, M., Arroyo, V., and Jiménez, W. (2008) The hepatic
cardium via Inhibiting apoptosis and oxidative stress
apelin system: a new therapeutic target for liver disease,
through PI3K and P38-MAPK signaling pathways,
Hepatology, 48, 1193-1201, doi: 10.1002/hep.22467.
Aging, 12, 25120-25137, doi: 10.18632/aging.104106.
76.
Kalin, R. E., Kretz, M. P., Meyer, A. M., Kispert, A.,
87.
Kleinz, M. J., and Baxter, G. F. (2008) Apelin reduces
Heppner, F. L., and Brändli, A. W. (2007) Paracrine
myocardial reperfusion injury independently of PI3K/
and autocrine mechanisms of apelin signaling govern
Akt and P70S6 kinase, Regul. Pept., 146, 271-277,
embryonic and tumor angiogenesis, Dev. Biol., 305,
doi: 10.1016/j.regpep.2007.10.002.
599-614, doi: 10.1016/j.ydbio.2007.03.004.
88.
Smith, C. C., Mocanu, M. M., Bowen, J., Wynne,
77.
Sorli, S. C., Le Gonidec, S., Knibiehler, B., and
A. M., Simpkin, J. C., Dixon, R. A., Cooper, M. B.,
Audigier, Y. (2007) Apelin is a potent activator of
and Yellon, D. M. (2007) Temporal changes in myo-
tumour neoangiogenesis, Oncogene, 26, 7692-7699,
cardial salvage kinases during reperfusion following
БИОХИМИЯ том 88 вып. 11 2023
ПЕПТИДЫ АПЕЛИНА И ПОВРЕЖДЕННОЕ СЕРДЦЕ
2287
ischemia: studies involving the cardioprotective adipo-
Morishita, S., Ichihara, S., and Fukamizu, A. (2008)
cytokine apelin, Cardiovasc. Drugs Ther., 21, 409-414,
Evaluation of novel cyclic analogues of apelin, Int. J.
doi: 10.1007/s10557-007-6054-y.
Mol. Med., 22, 547-552, doi: 10.3892/ijmm_00000054.
89.
O’Carroll, A-M., Lolait, S. J., Harris, L. E., and Pope,
101. Wang, W., McKinnie, S. M., Patel, V. B., Haddad, G.,
G. R. (2013) The apelin receptor APJ: journey from
Wang, Z., Zhabyeyev, P., Das, S. K., Basu, R.,
an orphan to a multifaceted regulator of homeostasis,
McLean, B., Kandalam, V., Penninger, J. M., Kassiri, Z.,
J. Endocrinol., 219, R13-R35, doi: 10.1530/joe-13-0227.
Vederas, J. C., Murray, A. G., and Oudit, G. Y.
90.
Masri, B., Morin, N., Pedebernade, L., Knibiehler, B.,
(2013) Loss of apelin exacerbates myocardial infarc-
and Audigier, Y. (2006) The apelin receptor is coupled
tion adverse remodeling and ischemia-reperfusion
to Gi1 or Gi2 protein and is differentially desensitized
injury: therapeutic potential of synthetic apelin ana-
by apelin fragments, J. Biol. Chem., 281, 18317-18326,
logues, J. Am. Heart. Assoc., 2, e000249, doi: 10.1161/
doi: 10.1074/jbc.M600606200.
JAHA.113.000249.
91.
Kennedy, S. G., Kandel, E. S., Cross, T. K., and
102. Jia, Z. Q., Hou, L., Leger, A., Wu, I., Kudej, A. B.,
Hay, N. (1999) Akt/Protein kinase B inhibits cell
Stefano, J., Jiang, C., Pan, C. Q., and Akita, G. Y.
death by preventing the release of cytochrome c
(2012) Cardiovascular effects of a PEGylated ape-
from mitochondria, Mol. Cell. Biol., 19, 5800-5810,
lin, Peptides, 38, 181-188, doi: 10.1016/j.peptides.
doi: 10.1128/MCB.19.8.5800.
2012.09.003.
92.
Pisarenko, O., Shulzhenko, V., Studneva, I.,
103. Iturrioz, X., Alvear-Perez, R., DeMota, N., Franchet, C.,
Serebryakova, L., and Veselova, O.
(2017)
Guillier, F., Leroux, V., Dabire, H., Le Jouan, M.,
5-Hydroxydecanoate abolishes cardioprotective effects
Chabane, H., Gerbier, R., Bonnet, D., Berdeaux, A.,
of a structural analogue of apelin-12 in ischemia/
Maigret, B., Galzi, J. L., Hibert, M., and Llorens-
reperfusion injury, Int. J. Pept. Res. Ther., 23, 333-341,
Cortes, C. (2010) Identification and pharmacological
doi: 10.1007/s10989-016-9565-1.
properties of E339-3D6, the first nonpeptidic
93.
Miura, T., Tanno, M., and Sato, T. (2010) Mitochon-
apelin receptor agonist, FASEB J., 24, 1506-1517,
drial kinase signaling pathways in myocardial protec-
doi: 10.1096/fj.09-140715.
tion from ischaemia/reperfusion-induced necrosis,
104. Murali, S., and Aradhyam, G. K. (2023) Structure-
Cardiovasc. Res., 88, 7-15, doi: 10.1093/cvr/cvq206.
function relationship and physiological role of apelin
94.
Chapman, N. A., Dupré, D. J., and Rainey, J. K.
and its G protein coupled receptor, Biophys. Rev.,
(2014) The apelin receptor: physiology, pathology,
15, 127-143, doi: 10.1007/s12551-023-01044-x.
cell signalling, and ligand modulation of a peptide-
105. Iturrioz, X., Gerbier, R., Leroux, V., Alvear-Perez, R.,
activated class A GPCR, Biochem. Cell Biol., 92, 431-
Maigret, B., and Llorens-Cortes, C. (2010) By inter-
440, doi: 10.1139/bcb-2014-0072.
acting with the C-terminal Phe of apelin, Phe255 and
95.
Khan, T. A., Bianchi, C., Ruel, M., Voisine, P., and
Trp259 in helix VI of the apelin receptor are critical
Sellke, F. W. (2004) Mitogen-activated protein kinase
for internalization, J. Biol. Chem., 285, 32627-32637,
pathways and cardiac surgery, J. Thorac. Cardiovasc.
doi: 10.1074/jbc.M110.127167.
Surg., 127, 806-811, doi: 10.1016/j.jtcvs.2003.04.001.
106. Pitkin, S., Macaluso, N., Maguire J., Glen, R., and
96.
Jia, Y. X., Pan, C. S., Zhang, J., Geng, B., Zhao, J.,
Davenport, A. (2009) Role for apelin in human athero-
Gerns, H., Yang, J., Chang, J. K., Tang, C. S., and Qi,
sclerosis and discovery of novel agonist for its recep-
Y. F. (2006) Apelin protects myocardial injury induced
by isoproterenol in rats, Regul. Pept., 133, 147-154,
pa2online.org/abstracts/Vol7Issue4abst027P.pdf.
doi: 10.1016/j.regpep.2005.09.033.
107. Macaluso, N. J., Pitkin, S. L., Maguire, J. J.,
97.
Foussal, C., Lairez, O., Calise, D., Pathak, A., Guilbeau-
Davenport, A. P., and Glen, R. C. (2011) Discovery
Frugieret, C., Valet, P., Parini, A., and Kunduzova, O.
of a competitive apelin receptor (APJ) antagonist,
(2010) Activation of catalase by apelin prevents oxida-
Chem. Med. Chem., 6, 1017-1023, doi: 10.1002/cmdc.
tive stress-linked cardiac hypertrophy, FEBS Lett., 584,
201100069.
2363-2370, doi: 10.1016/j.febslet.2010.04.025.
108. Sidorova, M. V., Azmuko, A. A., Pal’keeva, M. E.,
98.
Rastaldo, R., Cappello, S., Folino, A., and Losano, G.
Molokoedov, A. S., and Bushuev, V. N.
(2012)
(2011) Effect of apelin-apelin receptor system in pos-
Synthesis and cardioprotective properties of apelin-12
tischaemic myocardial protection: a pharmacological
and its structural analogs [in Russian], Bioorg. Khim.,
postconditioning tool? Antioxid. Redox Signal., 14,
38, 40-51, doi: 10.1134/s1068162012010177.
909-922, doi: 10.1089/ars.2010.3355.
109. Молокоедов А. С., Беспалова Ж. Д., Пелогейкина
99.
Macaluso, N. J., and Glen, R. C. (2010) Exploring
Ю. А., Азьмуко А. А., Масенко В. П., Писаренко
the ‘RPRL’ motif of apelin-13 THROUGH molecular
О. И., Шульженко В. С., Терещенко С. Н., Сидо-
simulation and biological evaluation of cyclic
рова М. В., Палькеева М. Е. (2012) Додекапеп-
peptide analogues, Chem. Med. Chem., 5, 1247-1253,
тиды, обладающие кардиопротекторными свой-
doi: 10.1002/cmdc.201000061.
ствами, Патент РФ № 2457216 (27.07.2012).
100. Hamada, J., Kimura, J., Ishida, J., Kohda, T.,
110. Филатова М. П., Крит Н. А., Комарова О. М.,
БИОХИМИЯ том 88 вып. 11 2023
2288
ПИСАРЕНКО, СТУДНЕВА
Орехович В. И., Рейссманн З., Лиепиня И. Т.,
s10517-015-3024-4.
Никифорович Г. В. (1986) Синтез и исследование
115. Pisarenko, O. I., Shulzhenko, V. S., Pelogeykina, Y. A.,
конформационно ограниченных аналогов пеп-
and Studneva, I. M. (2015) Enhancement of crys-
тидных ингибиторов ангиотензинпревращающего
talloid cardioplegic protection by structural analogs
фермента, Биоорг. Хим., 12, 59-70.
of apelin-12, J. Surg. Res., 194, 18-24, doi: 10.1016/
111. Janecka, A., Kruszynski, R., Fichna, J., Kosson, P.,
j.jss.2014.11.007.
and Janecki, T.
(2006) Enzymatic degradation
116. Pisarenko, O. I., and Studneva, I. M. (2023) Modified
studies of endomorphin-2 and its analogs containing
APJ receptor peptide ligands as postconditioning drugs
N-methylated amino acids, Peptides., 27, 131-135,
in myocardial ischaemia/reperfusion injury, Int. J. Pept.
doi: 10.1016/j.peptides.2005.06.015.
Res. Ther., 29, 23, doi: 10.1007/s10989-023-10498-2.
112. Pisarenko, O., Shulzhenko, V., Studneva, I.,
117. Tao, J., Zhu, W., Li, Y., Xin, P., Li, J., Liu, M., Li, J.,
Pelogeykina, Yu., Timoshin, A., Anesia, R., Valet, P.,
Redington, A. N., and Wei, M. (2011) Apelin-13 pro-
Parini, A., and Kunduzova, O. (2015) Structural
tects the heart against ischemia-reperfusion injury
apelin analogues: mitochondrial ROS inhibition and
through inhibition of ER-dependent apoptotic path-
cardiometabolic protection in myocardial ischaemia-
ways in a time-dependent fashion, Am. J. Physiol.
reperfusion injury, Br. J. Pharmacol., 172, 2933-2945,
Heart Circ. Physiol., 301, H1471-H1486, doi: 10.1152/
doi: 10.1111/bph.13038.
ajpheart.00097.2011.
113. Pisarenko, O. I., Lankin, V. Z., Konovalova, G. G.,
118. Hausenloy, D. J., and Yellon, D. M. (2007) Precon-
Serebryakova, L. I., Shulzhenko, V. S., Timoshin, A. A.,
ditioning and postconditioning: united at reperfu-
Tskitishvili, O. V., Pelogeykina, Y. A., and Studneva,
sion, Pharmacol. Ther., 116, 173-191, doi: 10.1016/
I. M. (2014) Apelin-12 and its structural analog en-
j.pharmthera.2007.06.005.
hance antioxidant defense in experimental myocardi-
119. Sidorova, M., Studneva, I., Bushuev, V., Pal’keeva, M.,
al ischemia and reperfusion, Mol. Cell. Biochem., 391,
Molokoedov, A., Veselova, O., Ovchinnikov, M., and
241-250, doi: 10.1007/s11010-014-2008-4.
Pisarenko, O.
(2020)
[MeArg1, NLe10]-apelin-12:
114. Pelogeykina, Y. A., Konovalova, G. G., Pisarenko,
Optimization of solid-phase synthesis and evaluation
O. I., and Lankin, V. Z. (2015) Antioxidant action of
of biological properties in vitro and in vivo, Peptides,
apelin-12 peptide and its structural analog in vitro,
129, 170320, doi: 10.1016/j.peptides.2020.170320.
Bull. Exp. Biol. Med.,
159, 604-606, doi: 10.1007/
APELIN C-TERMINAL FRAGMENTS:
BIOLOGICAL PROPERTIES AND THERAPEUTIC POTENTIAL
Review
O. I. Pisarenko* and I. M. Studneva
National Medical Research Center of Cardiology named after Academician E. I. Chazov,
121552 Moscow, Russia; e-mail: olpi@live.ru
The creation of bioactive molecules for the treatment of cardiovascular diseases based on natural peptides
stimulates intensive experimental research. In recent years, it has been established that the C-terminal frag-
ments of apelin, an endogenous ligand of the APJ receptor, reduce metabolic and functional disorders in ex-
perimental heart damage. The review presents literature data and generalized results of our own experiments
on the effect of apelin-13, [Pyr]apelin-13, apelin-12, and their chemically modified analogues on the heart
in normal conditions and when modeling pathophysiological conditions in vitro and in vivo. It has been
shown that the spectrum of action of apelin peptides on the damaged myocardium covers a decrease in the
death of cardiomyocytes from necrosis, a decrease in cardiomyocyte membrane damage, an improvement in
the metabolic state of the myocardium, and a decrease in the formation of reactive oxygen species and lipid
peroxidation products. The mechanisms of the protective action of these peptides associated with the acti-
vation of the APJ receptor and the manifestation of antioxidant properties are discussed. The data presented
in the review indicate the promise of molecular design of pharmacological APJ receptor agonists, which can
serve as the basis for the development of cardioprotectors that affect the processes of free radical oxidation
and metabolic adaptation.
Keywords: apelin, structural analogs, heart, experimental pathology, metabolism, cardiomyocyte membranes, lipid
peroxidation, reactive oxygen species, antioxidant enzymes
БИОХИМИЯ том 88 вып. 11 2023