БИОХИМИЯ, 2023, том 88, вып. 11, с. 2326 - 2339
УДК 577.175.6
ИЗУЧЕНИЕ ЭФФЕКТОВ ПРОГЕСТЕРОНА
И СЕЛЕКТИВНЫХ ЛИГАНДОВ МЕМБРАННЫХ
РЕЦЕПТОРОВ ПРОГЕСТЕРОНА В КЛЕТКАХ HepG2
ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ ЧЕЛОВЕКА
© 2023 Т.А. Щелкунова1*, И.С. Левина2, И.А. Морозов3, П.М. Рубцов3,
А.И. Гончаров1, Ю.В. Кузнецов2, И.В. Заварзин2, О.В. Смирнова1
1 Московский государственный университет имени М.В. Ломоносова, биологический факультет,
119991 Москва, Россия; электронная почта: schelkunova-t@mail.ru
2 Институт органической химии им. Н.Д. Зелинского РАН, 117913 Москва, Россия
3 Институт молекулярной биологии им. В.А. Энгельгардта РАН, 117913 Москва, Россия
Поступила в редакцию 02.12.2022
После доработки 13.09.2023
Принята к публикации 22.09.2023
Прогестерон оказывает множественные эффекты в разных тканях через ядерные рецепторы (nPR)
и через мембранные рецепторы семейства адипонектиновых и прогестиновых рецепторов (mPR).
Через разные типы рецепторов действие прогестерона на клетки может значительно различаться.
При этом он влияет на процессы пролиферации и апоптоза в нормальных и опухолевых тканях
двойственно: стимулируя пролиферацию и канцерогенез в одних тканях, подавляя их и стимулируя
гибель клеток - в других. В данной работе мы показали наличие высокого уровня мРНК и белка
mPRβ в опухолевых клетках HepG2 гепатоцеллюлярной карциномы человека. Экспрессия дру-
гих мембранных и классических ядерных рецепторов не была обнаружена. Можно предположить,
что mPRβ выполняет важную функцию в клетках HepG2. Главной целью работы явилось изуче-
ние функции этого белка и механизмов его действия в клетках гепатоцеллюлярной карциномы
человека. Ранее нами были выявлены селективные лиганды mPR - соединения LS-01 и LS-02,
не взаимодействующие с ядерными рецепторами. Их применение позволяет дифференцировать
эффекты прогестинов, опосредуемые разными типами рецепторов. В работе изучалось действие
прогестерона, LS-01 и LS-02 на пролиферацию и гибель клеток HepG2, а также активирующее
фосфорилирование двух киназ, р38 МАРК и JNK, под действием трех стероидов. Показано, что
все три прогестина через 72 ч инкубации с клетками подавляли их жизнеспособность и стимули-
ровали появление фосфатидилсерина на наружной поверхности мембран, выявляемое по связыва-
нию с аннексином V, но они не влияли на фрагментацию ДНК ядер клеток. Прогестерон достовер-
но снижал экспрессию генов маркеров пролиферации и стимулировал экспрессию гена белка р21,
но на экспрессию генов некоторых проапоптотических факторов действовал подавляюще. Все три
стероида активировали JNK в этих клетках, но на активность р38 МАРК действия не оказывали.
Эффекты прогестерона и селективных лигандов mPR в клетках HepG2 были одинаковыми в отно-
шении подавления пролиферации и стимуляции апоптотических изменений в наружных мембра-
нах, следовательно, они осуществлялись через взаимодействие с mPRβ. Участником сигнального
каскада, активируемого в этих клетках изучаемыми стероидами, является JNK.
КЛЮЧЕВЫЕ СЛОВА: прогестерон, селективные лиганды мембранных рецепторов прогестерона, про-
лиферация, апоптоз, ядерный рецептор прогестерона, мембранный β-рецептор прогестерона, клеточная
линия HepG2 гепатоцеллюлярной карциномы человека.
DOI: 10.31857/S0320972523110210, EDN: MNJPKA
ВВЕДЕНИЕ
процессы в женском организме. Значительно
менее исследованы его эффекты на ткани и
Наиболее изученной функцией прогесте-
органы нерепродуктивной сферы. Однако по-
рона является его действие на репродуктивные казано влияние прогестерона и его синтети-
Принятые сокращения: ВхРС3 - линия клеток аденокарциномы поджелудочной железы человека; HepG2 - ли-
ния клеток гепатоцеллюлярной карциномы человека; nPR и mPR - ядерные и мембранные рецепторы прогестерона;
PI - йодид пропидия.
* Адресат для корреспонденции.
2326
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2327
ческих аналогов на процессы пролиферации,
линиях клеток человека [13]. Можно пред-
гибели клеток и канцерогенез в целом ряде
положить, что данный рецептор принимает
изученных тканей [1]. Такое влияние проге-
важное участие в регуляции функций этих
стинов часто бывает разнонаправленным: сти-
клеток. Функции субтипа β мембранных ре-
мулирующим или ингибирующим в зависи-
цепторов и сигнальные пути, активируемые
мости от состава рецепторов прогестерона и
через него прогестероном, изучены мало в
фенотипа конкретной клетки [2-4]. Действие
сравнении с субтипом mPRα. В нейрональ-
прогестерона обусловлено активацией его ядер-
ных клетках РС12 его функция связана с ро-
ных рецепторов (nPR) и мембранных рецеп-
стом аксонов, а сигнальный путь включает
торов семейства адипонектиновых и проге-
фосфорилирование ERK [17], в миометрии ак-
стиновых рецепторов пяти субтипов (mPRs).
тивация этого рецептора, наряду с mPRα, при-
Из последних наиболее широко представлены
водит к фосфорилированию легких цепей мио-
в тканях субтипы mPRα, mPRβ и mPRγ. Уча-
зина и усилению сократительной активности,
стие ядерных рецепторов в процессах репро-
при этом показана активация р38 МАРК, но
дукции у особей женского пола, в поведенче-
не ERK1/2 [18], экспрессия mPRβ в клетках
ских реакциях, а также в функционировании
рака эндометрия связана с благоприятным
некоторых тканей и органов нерепродуктив-
прогнозом в течение заболевания [19]. Главной
ной сферы и опухолевых клетках изучается с
целью данной работы было выяснение функ-
конца 60-х гг. прошлого века [5]. Мембранные
ции mPRβ в клетках гепатоцеллюлярной кар-
рецепторы изучаются последние 20 лет [6-8].
циномы человека HepG2 и изучение сигналь-
Много работ посвящено исследованию разли-
ных каскадов, активируемых при его взаимо-
чий в лигандной специфичности связывания
действии с прогестинами. Для подтверждения
nPR и mPRs с целью поиска для последних
участия mPRβ в исследуемых эффектах мы ис-
селективных агонистов и антагонистов [9-12],
пользовали выявленные нами селективные ли-
поскольку часто оба типа рецепторов обна-
ганды mPRs. В работе исследовалось действие
руживаются одновременно в одних и тех же
прогестерона, LS-01 и LS-02 на пролиферацию
клетках. Функция mPRs в разных тканях, а
и гибель опухолевых клеток HepG2, а также на
также их роль в процессе канцерогенеза оста-
активирующее фосфорилирование двух ки-
ются под вопросом. Мы изучили экспрессию
наз - возможных посредников действия этих
генов разных типов рецепторов прогестерона
стероидов. Изучалось влияние трех стероидов
более чем в 16 опухолевых культурах и выяви-
на жизнеспособность клеток с помощью ХТТ-
ли клеточную линию ВхРС3 аденокарцино-
теста, на процесс апоптоза и некроза путем
мы поджелудочной железы человека с макси-
изучения фрагментации ядерной ДНК, экс-
мальной экспрессией mPRα и mPRγ, низкой
понирования на наружной мембране клеток
экспрессией mPRβ и отсутствием nPR [13].
фосфатидилсерина, проницаемости к йодиду
В клетках ВхРС3 мы изучили связывание про-
пропидия. Также исследовалось действие про-
гестерона и его производных, синтезированных
гестерона и селективных лигандов его мем-
в ИОХ имени Н.В. Зелинского, и обнаружи-
бранных рецепторов на экспрессию генов бел-
ли 2 соединения, взаимодействующие с mPRs,
ков, связанных с процессами пролиферации и
но не имеющие сродства к nPR [14, 15]. Эффек-
апоптоза, и возможность участия р38 МАРК
ты этих новых селективных лигандов мем-
и JNK в сигнальных путях, активируемых ре-
бранных рецепторов прогестерона
- LS-01
цептором при взаимодействии с гормонами.
(19-гидроксипрегн-4-ен-20-он) и LS-02 (19-гид-
рокси-5β-прегн-3-ен-20-он) - были изучены в
опухолевых клетках ВхРС3 [16]. В них обнару-
МАТЕРИАЛЫ И МЕТОДЫ
жилось цитотоксическое действие изучаемых
соединений, причем эффекты LS-02 значи-
Материалы. В исследованиях исполь-
тельно отличались от действия прогестерона
зовали следующие реактивы: среда DMEM
и LS-01. В данной работе мы нашли еще одну
с феноловым красным, раствор Версена,
культуру клеток, в которой также не обнару-
100× L-глютамин, 0,05%-ный раствор трип-
живались nPR, но наблюдалась высокая экс-
сина-ЭДТА в сбалансированном солевом рас-
прессия гена PAQR8 мембранного β-рецептора
творе Хэнка («ПанЭко», Россия); фетальная
прогестерона. Это культура клеток гепатоцел-
бычья сыворотка (FBS) и фетальная бычья
люлярной карциномы человека HepG2. Уро-
сыворотка, обработанная декстран-покрытым
вень мРНК белка mPRβ в клетках HepG2 зна-
углем (DFBS) («HyClone», США); 100× смесь
чительно превосходил уровень мРНК этого
антибиотиков (пенициллин, стрептомицин) и
белка в других изученных нами 16 опухолевых
антимикотиков, среда DMEM без фенолового
БИОХИМИЯ том 88 вып. 11 2023
2328
ЩЕЛКУНОВА и др.
красного («Gibco», США); прогестерон («Sigma-
фотометре Multiscan EX («Thermo electron cor-
Aldrich Corporation», США); реагенты для
poration», США).
иммуноблоттинга и электрофореза («Thermo
TUNEL-анализ. Клетки HepG2 рассеи-
Scientific», США и «GE Healthcare», Велико-
вали в 6-луночные планшеты («Corning») по
британия); антитела козы к IgG (H + L) кро-
(5-7) × 105 клеток на лунку. На следующий
лика и антитела козы к IgG (H + L) мыши,
день среду в лунках заменяли на среду с про-
конъюгированные с пероксидазой хрена HRP
гестероном, LS-01 или LS-02 в разных концен-
(«Wuhan Elabscience Biotechnology», Китай);
трациях. После инкубации клетки снимали
19-гидроксипрегн-4-ен-20-он (LS-01) и 19-гид-
раствором трипсина, промывали, фиксиро-
рокси-5β-прегн-3-ен-20-он (LS-02) были синте-
вали в 1%-ном (w/v) растворе параформаль-
зированы в ИОХ имени Н.Д. Зелинского [14, 15].
дегида в течение 15 мин на льду, промывали
Культивирование клеток и обработка гормо-
физиологическим раствором на фосфатном
нами. Клетки HepG2 гепатоцеллюлярной кар-
буфере (PBS) и заливали 70%-ным этанолом,
циномы человека («ATCC», США) культиви-
после чего оставляли на ночь при -20 °C.
ровали в среде DMEM с феноловым красным,
На следующий день проводили анализ TUNEL
cодержащей 10% FBS, 0,365 г/литр глютамина
с помощью набора APO-BrdU™ TUNEL Assay
и раствор смеси антибиотика и антимикотика,
Kit, with Alexa Fluor® 488 Anti-BrdU («In-
в стандартных условиях при 37 °C в инкуба-
vitrogen», A23210) в соответствии с инструк-
торе в атмосфере 5% CO2. После третьего пас-
цией производителя. Клетки промывали, ин-
сажа клетки рассеивали в среду DMEM без
кубировали в течение ночи при комнатной
фенолового красного, содержащую 10% DFBS
температуре в растворе, содержащем BrdUTP,
и раствор антибиотиков. После трех пасса-
терминальную дезоксинуклеотидилтрансферазу,
жей в среде без стероидов клетки рассажи-
реакционный буфер. После инкубации клет-
вали в планшеты или чашки Петри, растили
ки отмывали промывочным буфером и об-
до 50-70% конфлюэнтности и обрабатывали
рабатывали час в темноте антителами Alexa
гормонами или растворителем - этанолом (не
Fluor™ 488 dye-labeled anti-BrdU, разведен-
больше 0,2% v/v) в течение 24-72 ч. Затем куль-
ными в 20 раз. Затем в пробирки добавляли
туральную среду удаляли, клетки использова-
буфер с йодистым пропидием и РНКазой А,
лись для анализов. В разных анализах исполь-
через 30 мин измерялось количество клеток,
зовались концентрации стероидов от 10 нМ
провзаимодействовавших с мечеными анти-
до 20 мкМ. Высокие концентрации позволяют
телами, на LSR Fortessa («BD Biosciences»,
лучше выявить эффект, поскольку сродство
США) методом проточной цитометрии.
прогестерона к mPRs в 5-30 раз ниже, чем
Окраска конъюгатом аннексин V. Клетки
его сродство к nPR [13, 14]. По-видимому, ак-
рассеивали на 24-луночный планшет по 7 × 104
тивация mPRs происходит при беременно-
клеток на лунку. На следующий день клетки
сти и вблизи мест синтеза прогестерона, где
обрабатывали гормонами. После инкубации
локально наблюдаются концентрации этого
клетки снимали раствором трипсина, про-
гормона в 10-100 раз выше, чем в кровенос-
мывали холодным PBS и определяли апоп-
ном русле [20]. В экспериментальных условиях
тотические и некротические клетки с ис-
подобные концентрации наблюдались в сыво-
пользованием набора Annexin V-FITC conjugate
ротке животных при дополнительном введе-
(«Invitrogen», A13199). Апоптотическую и не-
нии стероида, но выживаемость, активность и
кротическую гибель клеток анализировали с
прибавка веса у таких животных сохранялись
помощью двойного окрашивания с аннекси-
неизмененными в сравнении с контрольными
ном V и йодидом пропидия (PI). Аннексин V
животными [21].
связывается с апоптотическими клетками с
ХТТ-тест. Клетки HepG2 рассевали в
экспонированным фосфатидилсерином, в то
96-луночный планшет («Corning», США) по
время как PI метит клетки с повреждением
(5-6) × 103 клеток на лунку. На следующий
мембраны. Окрашивание производили соглас-
день проводили замену среды на среду с про-
но рекомендациям производителя, как было
гестероном или одним из селективных ли-
описано ранее [16]. Процент апоптотических
гандов в разных концентрациях. После окон-
и некротических клеток определяли проточ-
чания инкубации проводили ХТТ-тест с помо-
ной цитофлуориметрией на каналах «FITC» и
щью набора Cell Proliferation Kit («Biological
«PerCP-cy5-5 A» на приборе LSR Fortessa.
Industries», США) в соответствии с рекомен-
Определение экспрессии генов. После обра-
дациями производителя. Измерение погло-
ботки клеток HepG2 гормонами из лунок уда-
щения в лунках проводили через час и через
ляли культуральную среду, из клеток выделяли
2 ч при 450 и 620 нм на планшетном спектро-
общую РНК, используя TRIzol («Invitrogen»).
БИОХИМИЯ том 88 вып. 11 2023
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2329
Синтез кДНК проводили с помощью набо-
Anti-GAPDH antibody G9545 («Sigma-Aldrich
ра ImProm-II™ Reverse Transcription System
Corporation») с повторением описанной выше
(«Promega»), согласно инструкции произво-
процедуры.
дителя. ПЦР в реальном времени проводили
Для определения активирующего фосфо-
на приборе LightCycler 96 («Roche», Герма-
рилирования киназ под действием гормонов
ния) с использованием реагентов, вклю-
клетки подвергали воздействию прогестерона
чающих интеркалирующий краситель SYBR
и селективных лигандов mPRs в концентрации
Green I («Синтол», Россия). Используемые для
20 мкM в течение 40 мин. Далее их лизировали
ПЦР специфические праймеры приведены в
в реагенте, описанном ранее. Белки перед на-
таблице в Приложении. Праймеры подбира-
несением на 13,5%-ный ПААГ прогревали при
лись с учетом экзон-интронной структуры ге-
50 °C 15 мин, разделяли электрофорезом и пе-
нов так, чтобы не образовывалось ампликонов
реносили на мембраны. После обработки бло-
на геномной ДНК в выбранных условиях ПЦР.
кирующим раствором, содержащим 5% блоки-
В случае, когда ген имел только один экзон,
рующего агента на ТBSТ (физиологический
препарат РНК перед синтезом кДНК обраба-
раствор на основе Tris-буфера, содержащий
тывали RQ1 RNase-Free DNase («Promega»).
0,1% (v/v) Tween 20), мембраны инкубировали
Были использованы следующие условия ам-
с первичными антителами либо к активи-
плификации: инкубация при 95 °C - 5 мин; да-
рованным изоформам JNK (monoclonal anti-
лее 40 циклов: 95 °C - 10 с, 58 °C - 15 с, 72 °C -
JNK, activated (diphosphorylated JNK), J4750),
20 с; плавление 72-95 °C. Каждый образец ана-
либо ко всем изоформам JNK (Anti-JNK anti-
лизировали в трех повторах. Уровень экспрес-
body, SAB4200176), либо к фосфо-p38 MAPK
сии мРНК изучаемых генов нормировался на
[Phospho-p38 MAPK (Thr180, Tyr182), S.417.1,
уровень мРНК референсного гена глицер-
(«Invitrogen»), либо к p38 MAPK (Anti-p38
альдегид-3-фосфатдегидрогеназы (GAPDH), а
MAPK antibody SAB4500490)] при 4 °C в тече-
затем - на контрольный образец для относи-
ние ночи. Затем мембраны промывали TBST,
тельного количественного определения с ис-
инкубировали (60 мин) со вторичными анти-
пользованием метода ΔΔCt [16].
телами козы к IgG (H + L) кролика или мыши
Иммуноблоттинг. Для определения рецеп-
в разведении 10 000, опять промывали TBST
торов клетки HepG2 лизировали с помощью
и измеряли хемилюминесценцию на приборе
реагента CelLytic™ M («Sigma-Aldrich Corpo-
ChemiDoc MP system.
ration») с добавлением ингибитора MS-SAFE
Статистическая обработка результатов.
Protease and Phosphatase inhibitor
(«Sigma-
Статистический обсчет данных проводился
Aldrich Corporation»). Белки прогревали в бу-
в программе GraphPad Prism 6.01 («GraphPad
фере с SDS и разделяли в 13,5%-ном ПААГ,
Software», США). Результаты измерений на
переносили на мембраны
(«GE Healthcare
гистограммах даны как среднее ± стандартное
Life Sciences», США и «Amersham», Герма-
отклонение. Оценку проводили с использова-
ния), которые обрабатывали 60 мин раствором
нием однофакторного дисперсионного ана-
PBS-T (PBS и 0,1% (v/v) Tween 20), содержа-
лиза (one-way ANOVA) с поправкой на мно-
щим 5% блокирующего агента (ECL Advance
жественные сравнения Даннетта. Различия
Blocking Agent, «GE Healthcare Life Sciences»).
считались достоверными при р <0 ,05.
Затем мембраны инкубировали с антитела-
ми к mPRα (ab75508), к mPRβ (ab123693) и
к mPRγ (ab79517) («Abcam», США), разведен-
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
ными соответственно в 500, 100 и 500 раз.
Инкубацию проводили в течение ночи, за-
Экспрессия рецепторов прогестерона в клет-
тем мембраны промывали и обрабатывали
ках HepG2 гепатоцеллюлярной карциномы чело-
(60 мин) вторичными антителами козы к IgG
века. В клетках HepG2 была изучена экспрессия
(H + L) кролика в разведении 10 000, после
генов PGR ядерных рецепторов прогестерона
чего промывали PBS-Т. Хемилюминесценцию
и PAQR 7, PAQR 8 и PAQR 5 трех мембранных
измеряли на приборе ChemiDoc MP system
рецепторов: mPRα, mPRβ, mPRγ. Результаты
(«Bio-Rad», США) с использованием реагента
экспериментов представлены на рис. 1, а. Сред-
ECL SuperSignal™ West Femto Maximum Sensi-
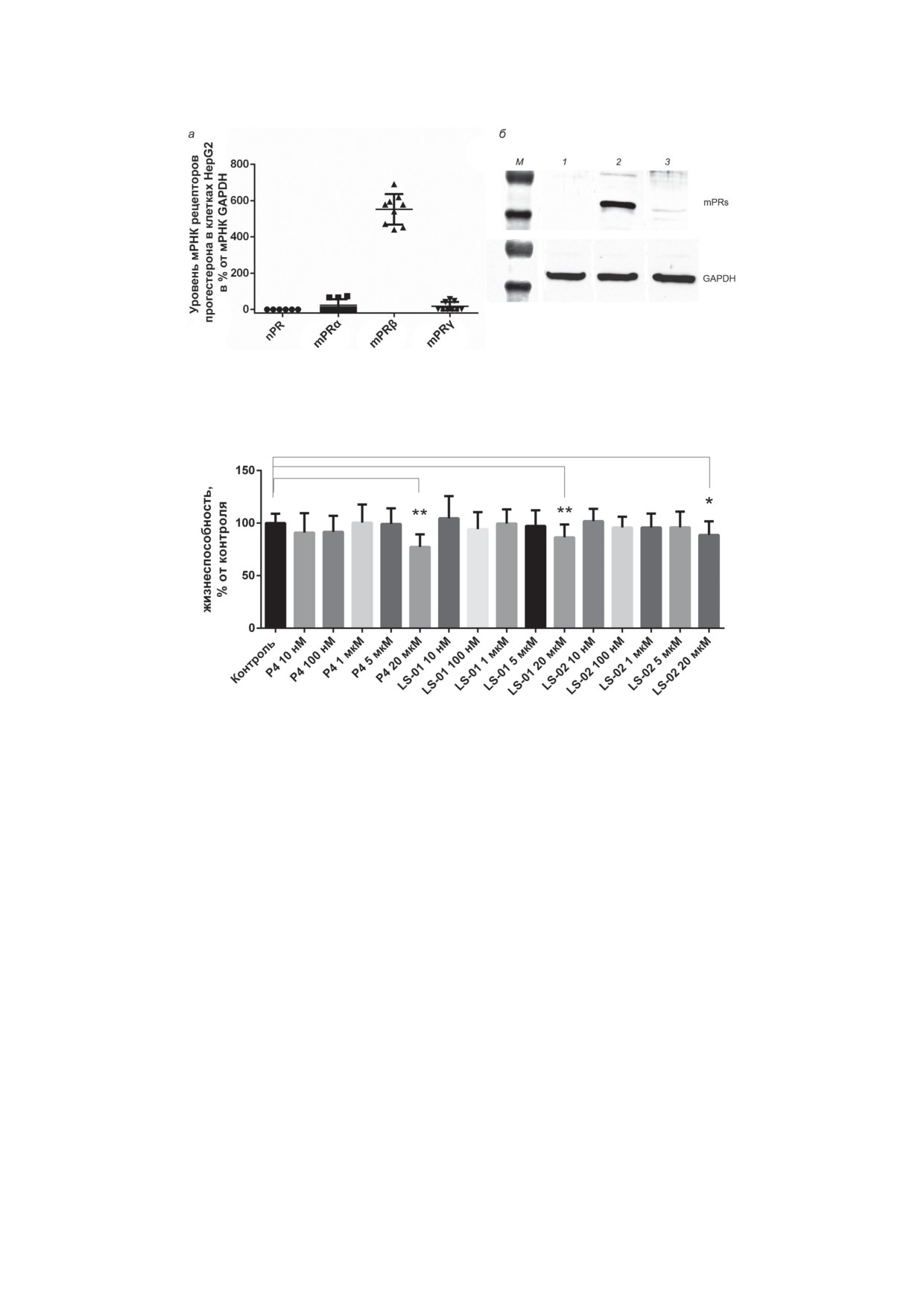
ние значения уровня мРНК PAQR 7 (mPRα)
tivity Substrate («Thermo Scientific»). Для по-
составляли 23% от уровня мРНК референсно-
вторного использования мембраны обраба-
го гена GAPDH, мРНК PAQR 8 (mPRβ) - 579%,
тывали в соответствии с протоколом «Western
мРНК PAQR 5 (mPRγ) - 17%, мРНК PGR (nPR)
blot membrane stripping for restaining proto-
практически не выявлялась. Таким образом, в
col» («Abcam») и инкубировали с антителами
клетках HepG2 преимущественно экспресси-
БИОХИМИЯ том 88 вып. 11 2023
2330
ЩЕЛКУНОВА и др.
Рис. 1. Изучение экспрессии генов и содержания белков, рецепторов прогестерона, в HepG2-клетках. а - Содержа-
ние мРНК PGR (nPR) и мРНК PAQR 7, PAQR 8 и PAQR 5 (mPRα, mPRβ, mPRγ) в клетках HepG2 в процентах от
мРНК GAPDH. б - Иммуноблоттинг лизатов клеток HepG2 после инкубации: 1 - с первичными антителами (АТ)
к mPRα, 2 - с первичными АТ к mPRβ, 3 - с первичными АТ к mPRγ и АТ к референсному белку (GAPDH).
mPRs - 40 кДа; GAPDH - 36 кДА; М - маркеры 50 кДа и 34 кДа
Рис. 2. Действие разных концентраций прогестерона (Р4) и селективных лигандов LS-01 и LS-02 на жизнеспособность
клеток HepG2, определенную с помощью теста ХТТ. Результаты измерений представлены как среднее ± стандартное
отклонение. Отмечено достоверное отличие от контрольных значений: * р = 0,0011; ** р < 0,0001
руется субтип mPRβ. Результаты иммуноблот-
На рис. 3 представлена гистограмма статисти-
тинга, приведенные на рис. 1, б, подтверждают
ческого обсчета результатов экспериментов
этот вывод.
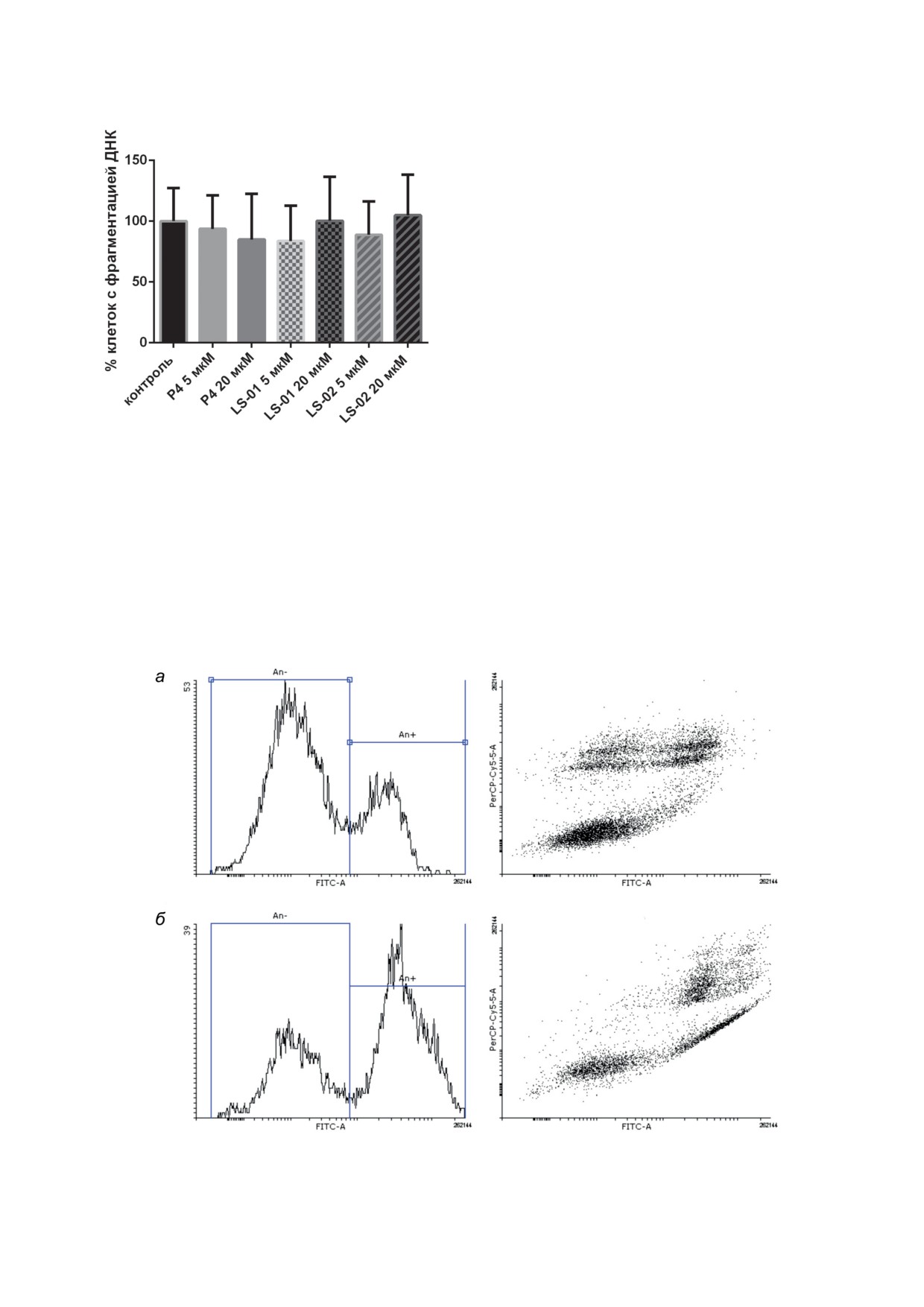
исследования клеток с фрагментацией ДНК
Действие прогестерона и селективных лиган-
методом TUNEL-анализа. Можно видеть, что
дов mPRs на жизнеспособность клеток HepG2
через 72 ч инкубации достоверных эффектов
в ХТТ-тесте. Клетки HepG2 были обработа-
гормонов в сравнении с контролем не обнару-
ны прогестероном и селективными лигандами
жено (по результатам 7 независимых экспери-
в течение 24, 48 и 72 ч. В экспериментах с ин-
ментов).
кубацией 24 и 48 ч достоверного эффекта гор-
Эффект прогестерона и селективных лиган-
монов выявлено не было (данные не представ-
дов LS-01 и LS-02 на связывание клетками
лены). На рис. 2 продемонстрированы резуль-
HepG2 аннексина V и проницаемость к йодиду
таты статистической обработки ХТТ-теста
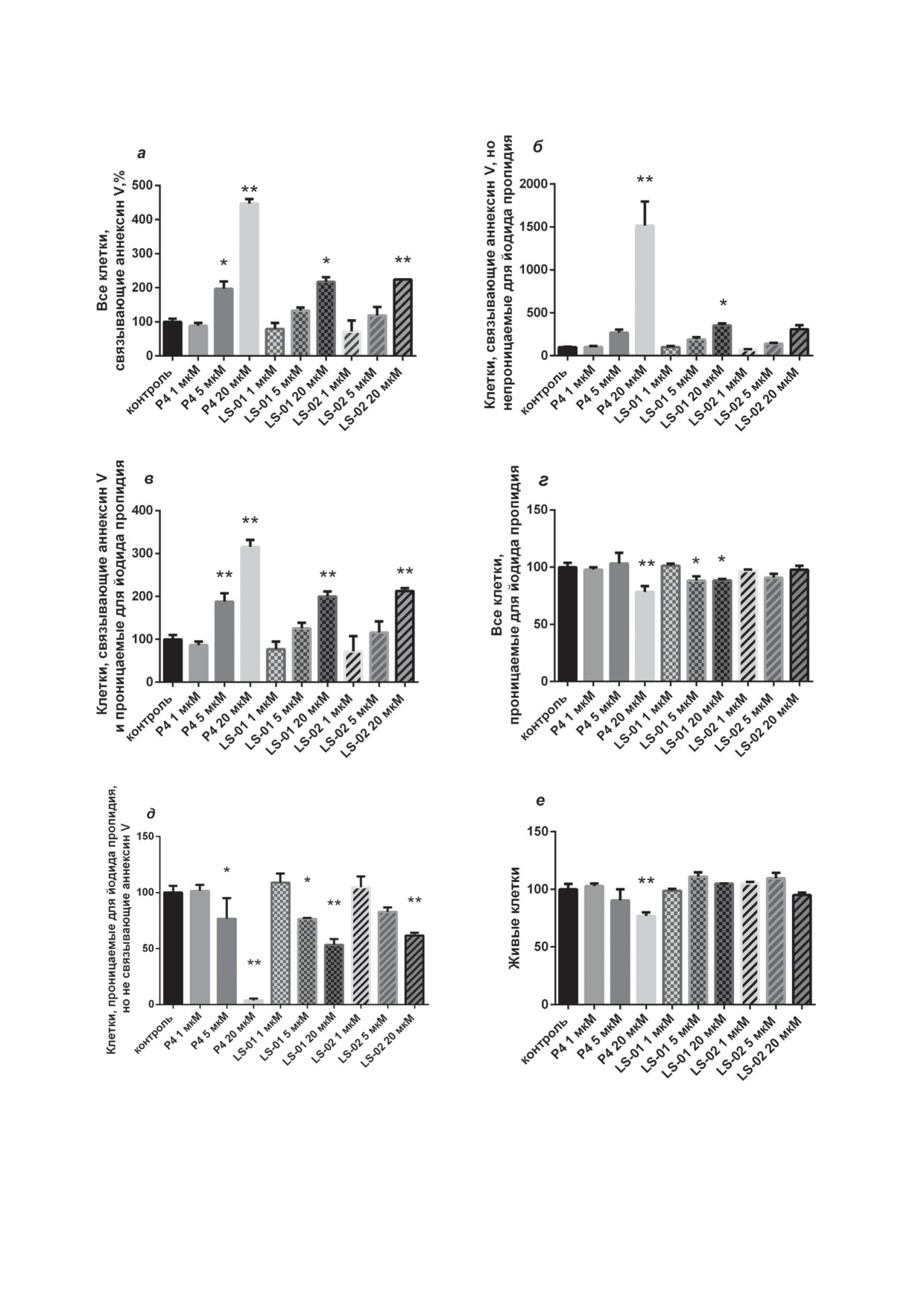
пропидия. Через 72 ч инкубации прогестерон
шести независимых экспериментов: проге-
достоверно вызывал повышение связывания
стерон (Р4) снижал жизнеспособность клеток
аннексина V клетками HepG2, но при этом сни-
HepG2 на 23% (р < 0,0001), LS-01 - на 14%
жал количество клеток, проницаемых для PI
(р < 0,0001), LS-02 - на 12% (р = 0,0011) при
(рис. 4 и 5). Селективные лиганды обладали
концентрациях 20 мкМ через 72 ч инкубации
таким же, но менее выраженным действием
с гормонами.
(рис. 5 и 6). В сравнении с контролем коли-
Действие прогестерона и селективных лиган-
чество всех клеток, которые связывали ан-
дов mPRs на фрагментацию ДНК клеток HepG2
нексин V, в присутствии 5 мкМ прогестерона
в TUNEL-тесте. В работе изучалось дей-
увеличивалось в 2 раза (р = 0,044), в при-
ствие трех стероидов на фрагментацию ДНК.
сутствии 20 мкМ - в 4,5 раза (р < 0,0001).
БИОХИМИЯ том 88 вып. 11 2023
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2331
клеток, связывающих аннексин V, под дей-
ствием прогестерона увеличивалось количе-
ство тех из них, которые были непроницаемы
для PI (рис. 5, б), при 5 мкМ - в 2,7 раза и
при 20 мкМ - в 15 раз (р < 0,0001); а тех, ко-
торые одновременно связывали аннексин V
и были проницаемы для PI (рис. 5, в), при
5 мкМ - в 1,9 раза (р = 0,0005) и при 20 мкМ -
в 3,2 раза (р < 0,0001). Под действием LS-01
среди всех клеток, связывающих аннексин V,
увеличивалось количество тех из них, которые
были непроницаемы для PI (рис. 5, б), при
5 мкМ - в 1,9 раза и при 20 мкМ - в 3,5 раза
(р = 0,0302); а тех, которые одновременно свя-
зывали аннексин V и были проницаемы для PI
(рис. 5, в), при 5 мкМ - в 1,3 раза и при 20 мкМ -
в 2 раза (р = 0,0002). Наконец, под действием
Рис. 3. Действие прогестерона (Р4) и селективных лиган-
дов LS-01 и LS-02 на фрагментацию ДНК клеток HepG2,
LS-02 среди всех клеток, связывающих ан-
определенную с помощью TUNEL-теста. Результаты из-
нексин V, увеличивалось количество тех из
мерений представлены как среднее ± стандартное откло-
них, которые были непроницаемы для PI, при
нение
5 мкМ - в 1,4 раза и при 20 мкМ - в 3,1 раза
(р = 0,0839); а тех, которые одновременно свя-
LS-01 в концентрации 5 мкМ повышал коли-
зывали аннексин V и были проницаемы для PI,
чество таких клеток в 1,3 раза, в концентрации
при 5 мкМ - в 1,2 раза и при 20 мкМ -
20 мкМ - в 2,2 раза (р = 0,0136). LS-02 в кон-
в 2,1 раза (р < 0,0001) (рис. 5, б и в). Наоборот,
центрации 5 мкМ повышал количество таких
количество всех клеток, проницаемых для PI,
клеток в 1,2 раза, в концентрации 20 мкМ -
снижалось под действием 20 мкМ прогестеро-
в 2,2 раза (р < 0,0001) (рис. 5, а). Среди всех
на на 22% (р = 0,0004), под действием LS-01
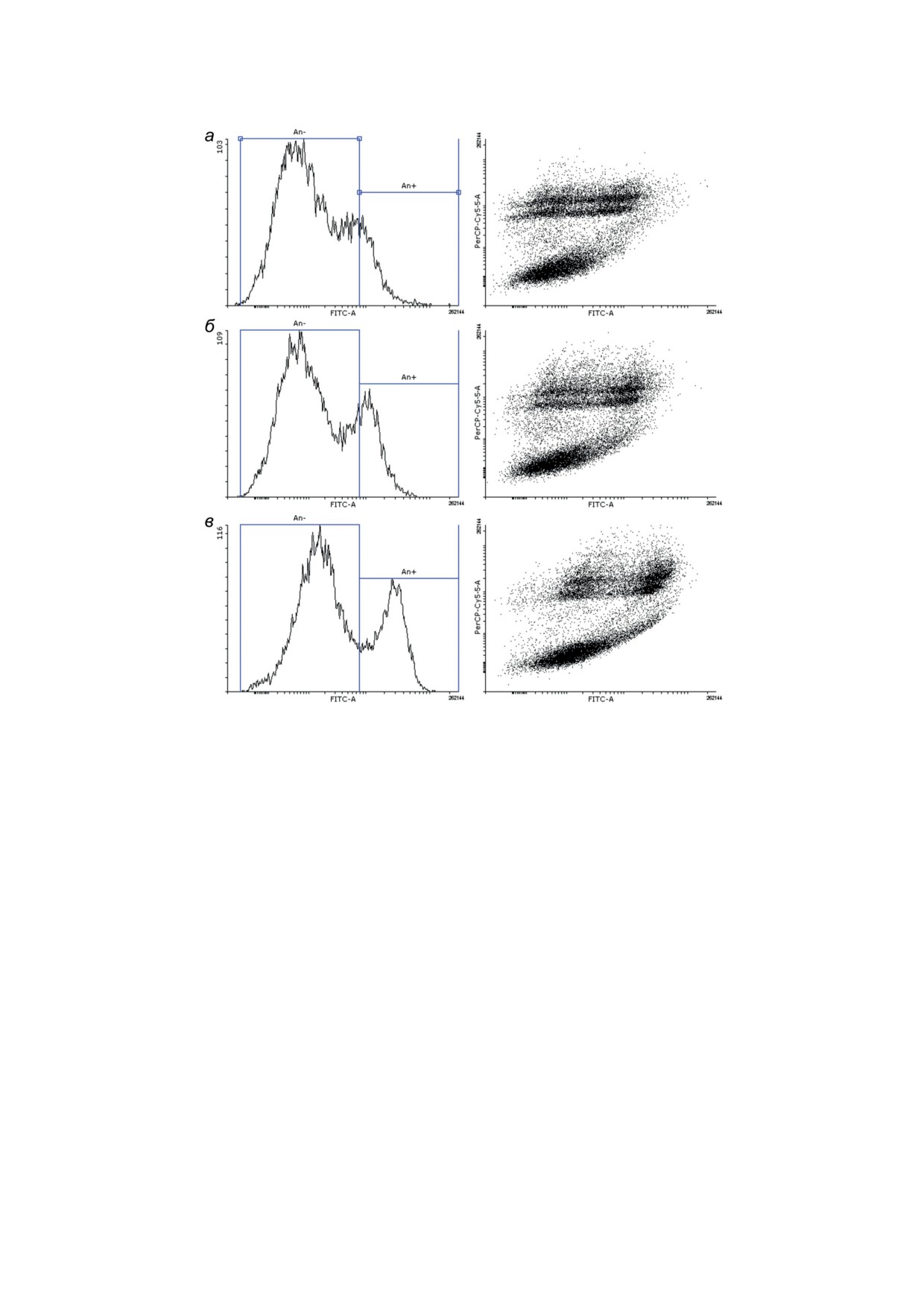
Рис. 4. Графики и точечные диаграммы распределения клеток HepG2 в эксперименте по связыванию меченого аннек-
сина V и окраске их PI в контроле (а) и после инкубации с 20 мкМ прогестерона в течение 72 ч (б). An- - пик клеток,
не взаимодействующих с аннексином V; An+ - пик клеток, связывающих аннексин V
БИОХИМИЯ том 88 вып. 11 2023
2332
ЩЕЛКУНОВА и др.
Рис. 5. Действие прогестерона (Р4) и селективных лигандов LS-01 и LS-02 в разных концентрациях на все клетки,
связывающие аннексин V (а); на клетки, связывающие аннексин V, но непроницаемые для PI (б); на клетки, одновре-
менно связывающие аннексин V и проницаемые для PI (в); на все клетки, проницаемые для PI (г); на клетки, которые
не связывают аннексин V, но проницаемы для PI (д); на живые, незатронутые апоптозом и некрозом клетки (е).
Результаты даны в процентах от количества соответствующих клеток в контроле и представлены как среднее ± стан-
дартное отклонение. Отмечено достоверное отличие от контрольных значений: * 0,014 ≤ р ≤ 0,044; ** р ≤ 0,0005
БИОХИМИЯ том 88 вып. 11 2023
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2333
Рис. 6. Графики и точечные диаграммы распределения клеток HepG2 в эксперименте по связыванию меченого аннек-
сина V и окраске их PI в контроле (а), после инкубации с 5 мкМ (б) и с 20 мкМ (в) LS-01 в течение 72 ч. An- - пик
клеток, не взаимодействующих с аннексином V; An+ - пик клеток, связывающих аннексин V
в концентрации 5 мкМ - на 12% (р = 0,0358),
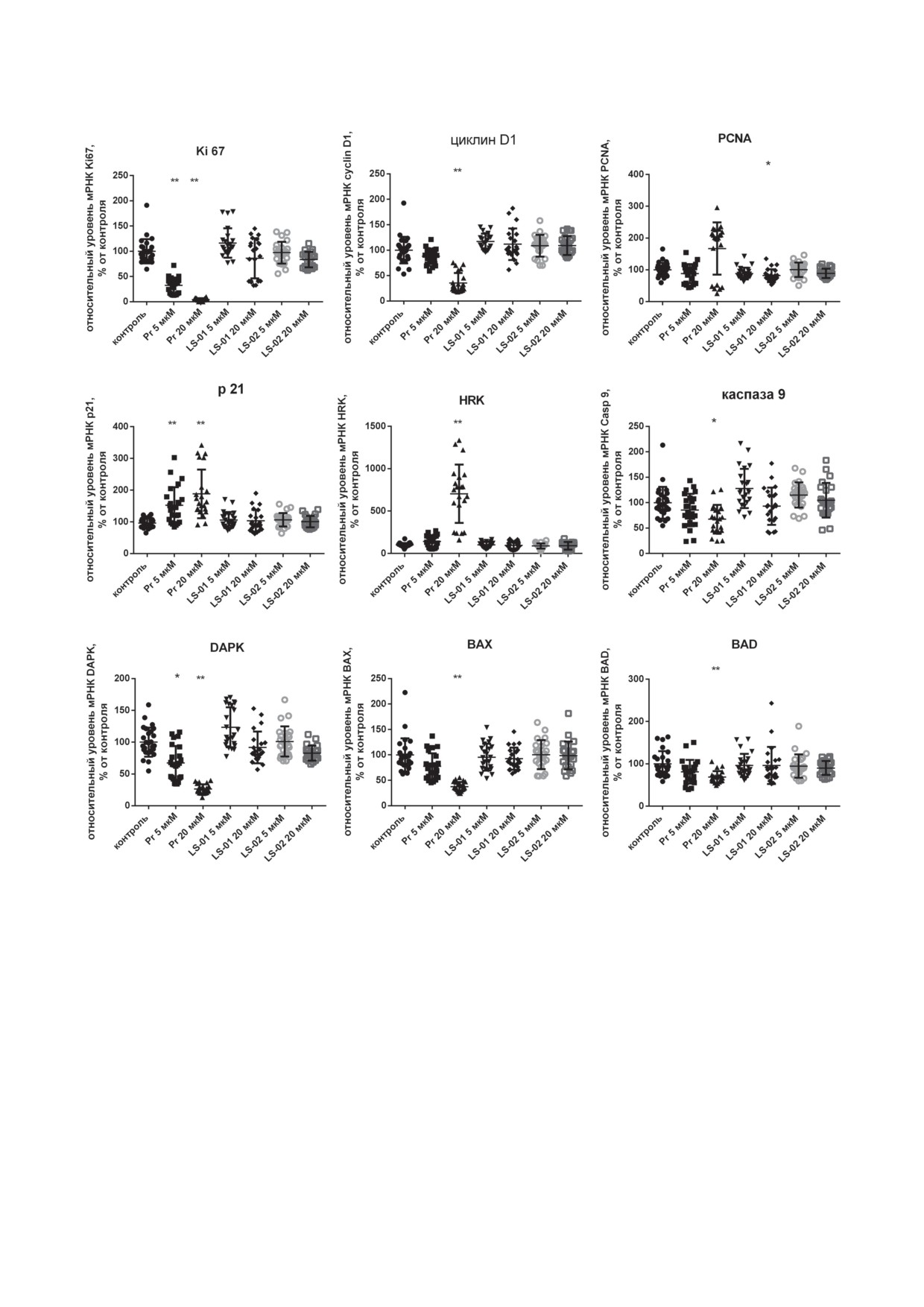
стерон (рис. 7). Исключением является ген, ко-
в концентрации 20 мкМ - на 12% (р = 0,0403)
дирующий PCNA, экспрессия которого досто-
(рис. 5, г). Такое снижение происходило за счет
верно ингибируется только LS-01 в концентра-
клеток, которые не связывали аннексин V,
ции 20 мкМ - на 18% от значений в контроле
но были проницаемы для PI. Под действием
(р = 0,0463). Прогестерон в двух изученных кон-
5 мкМ прогестерона количество таких клеток
центрациях (5 и 20 мкМ) снижает уровень
снижалось на 23% (р = 0,0226), под действием
мРНК белка Ki67 на 67% (р < 0,0001) и 96%
20 мкМ прогестерона - на 96% (р < 0,0001), под
(р < 0,0001) соответственно, повышает мРНК
действием 5 мкМ LS-01 - на 24% (р = 0,0215),
белка р21 на 52% (р = 0,0002) и 88% (р < 0,0001)
20 мкМ LS-01 - на 47% (р = 0,0001), а под дей-
соответственно; в концентрации 20 мкМ про-
ствием 5 мкМ LS-02 - на 17%, 20 мкМ LS-02 -
гестерон снижает уровень мРНК белка ци-
на 38% (р = 0,0005) (рис. 5, д). В результате ко-
клин D1 - на 64% (р < 0,0001). На экспрессию
личество живых, незатронутых апоптозом и
факторов апоптоза прогестерон оказывает пре-
некрозом клеток достоверно снижалось толь-
имущественно ингибирующее действие, за ис-
ко под действием 20 мкМ прогестерона на 23%
ключением гена белка HRK (Harakiri), экспрес-
(р = 0,0003) (рис. 5, е).
сия которого повышается в 7 раз (р < 0,0001)
Определение изменения экспрессии генов
в присутствии 20 мкМ этого стероида. В этой
в клетках HepG2 под действием прогестерона,
концентрации прогестерон подавляет экспрес-
LS-01 и LS-02. На экспрессию генов выбран-
сию проапоптотических факторов: каспазы 9 -
ных маркеров пролиферации и факторов апоп-
на 33% (р = 0,0164), ВАХ - на 62% (р < 0,0001),
тоза достоверное влияние оказывает проге-
BAD - на 31% (р = 0,0001). Снижение экс-
БИОХИМИЯ том 88 вып. 11 2023
2334
ЩЕЛКУНОВА и др.
Рис. 7. Регуляция прогестероном (Р4) и соединениями LS-01и LS-02 уровня экспрессии генов факторов, связанных
с пролиферацией и апоптозом, в клетках HepG2. Определение содержания мРНК проводилось методом обратной
транскрипции и ПЦР в реальном времени, приведено значение среднего ± среднего отклонения. Отмечено достовер-
ное отличие от контрольных значений: * 0,013 ≤ р ≤ 0,046; ** р ≤ 0,0002
прессии гена проапоптотического факто-
вание р38 МАРК и JNK. На рис. 8 представле-
ра DAPK происходит уже при 5 мкМ - на 33%
ны репрезентативные данные одного из трех
(р = 0,0013), при 20 мкМ - на 73% (р < 0,0001).
экспериментов по изучению активирующе-
Селективные лиганды на экспрессию генов
го фосфорилирования двух киназ под дей-
факторов апоптоза не оказывали достоверного
ствием 20 мкМ прогестерона, LS-01 и LS-02.
действия. В работе изучалась также экспрес-
По результатам денситометрии соотношение
сия гена фактора Bcl2A1. Все три исследуемых
фосфо-р38/р38 МАРК в контроле (рис. 8, до-
стероида не оказывали влияния на уровень
рожка 1) и под действием всех трех стерои-
мРНК этого антиапоптотического белка (дан-
дов (рис. 8, дорожки
2-4) практически не
ные не показаны).
менялось. Соотношение фосфо-JNK/JNK по-
Действие прогестерона и селективных ли-
вышалось для первой изоформы в 1,9 раза
гандов mPRs на активирующее фосфорилиро- под действием прогестерона (2), в 1,5 раза -
БИОХИМИЯ том 88 вып. 11 2023
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2335
ВхРС3 аденокарциномы поджелудочной же-
лезы человека с преимущественной экспрес-
сией mPRα и mPRγ (270% и 283% от уровня
мРНК референсного гена соответственно) и
отсутствием nPRs. Оно было ниже, чем срод-
ство прогестерона к этим рецепторам [14].
Как было показано в этой работе, в линии
HepG2 содержание mPRα и mPRγ очень мало,
мРНК nPRs не была обнаружена. Сродство се-
лективных лигандов к mPRβ не определялось.
Важно было выяснить, могут ли наши селек-
тивные лиганды регулировать функции клеток
через mPRβ. Клетки HepG2 оказались наибо-
лее подходящими для этой цели. Было обнару-
жено, что взаимодействие LS-01и LS-02 с этим
Рис. 8. Эффект прогестерона, LS-01и LS-02 на активи-
субтипом mPRs происходит, судя по эффектам
рующее фосфорилирование р38 МАРК и JNK в клет-
этих соединений на активацию JNK, стиму-
ках HepG2. Дорожки: 1 - контроль, 2 - действие 20 мкМ
прогестерона, 3 - действие 20 мкМ LS-01, 4 - действие
ляцию связывания клетками меченого аннек-
20 мкМ LS-02
сина V и на торможение некротических изме-
нений, вызывающих проницаемость мембран.
под действием LS-01 (3) и в 1,7 раза - под
Поскольку прогестерон действует сильнее, чем
действием LS-02; для второй и третьей изо-
селективные лиганды, можно предположить,
форм суммарно - в 2 раза (2), в 1,7 раза (3) и
что и к субтипу mPRβ сродство прогестерона
в 2,2 раза (4) соответственно. Таким образом,
выше, чем сродство его производных. Дей-
все изучаемые соединения в клетках HepG2
ствие изучаемых стероидов в клетках HepG2
активировали все изоформы JNK, но не влия-
было антипролиферативным и проапоптоти-
ли на активность р38 МАРК.
ческим. Изучаемые соединения подавляли жиз-
неспособность клеток (рис. 2), стимулирова-
ли апоптотические изменения в их мембра-
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
нах (рис. 4-6). Действие всех трех стероидов
приводило к активации всех изоформ JNK,
Действие прогестерона и его производных
при этом активирующего фосфорилирования
в значительной мере определяется составом
р38 МАРК обнаружено не было (рис. 8).
рецепторов прогестерона, а также фенотипом
Интересно было сравнить действие изучае-
данной конкретной клетки. В настоящей ра-
мых стероидов в клетках HepG2 с преимуще-
боте было изучено действие прогестерона и
ственной экспрессией mPRβ с их эффектами
селективных лигандов mPRs (LS-01 и LS-02)
в клетках ВхРС3, где наблюдалась преимуще-
в клетках гепатоцеллюлярной карциномы че-
ственная экспрессия mPRα и mPRγ. В обоих
ловека HepG2. Это действие осуществляется
типах клеток мРНК nPR не была обнаружена.
преимущественно через субтип mPRβ, по-
В результате исследования мы показали, что
скольку уровень мРНК mPRβ составлял 579%
эффекты изучаемых соединений разнятся в
от мРНК референсного гена, в то время как
клеточных линиях HepG2 и ВхРС3, но имеют
для других мембранных рецепторов он не пре-
общую направленность [16]. В клетках HepG2
вышал 23%, а уровень мРНК nPR был равен
достоверное снижение жизнеспособности на-
нулю (рис. 1, а). Следует отметить, что такого
блюдалось при максимальных используемых
высокого уровня экспрессии гена PAQR8 мы
концентрациях всех трех стероидов, тогда как
не обнаружили ни в одной из 16 исследован-
жизнеспособность клеток ВхРС3 подавлялась
ных ранее клеточных культур, максимальны-
достоверно только под действием прогесте-
ми были значения 154% - в клетках LN229 и
рона и LS-01, а LS-02 не влиял на жизнеспо-
112% - в клетках U87MG, в других линиях уро-
собность клеток ВхРС3 в ХТТ-тесте. Наличие
вень мРНК составлял 10-50% от мРНК рефе-
одного субтипа mPR приводит к более универ-
ренсного гена [13]. Методом иммуноблоттинга
сальному действию изучаемых прогестинов.
также были выявлены белки этого рецептора,
В линии HepG2 нет такого разнообразного
в то время как белки mPRα и mPRγ практиче-
действия трех стероидов, которое наблюдалось
ски не были обнаружены (рис. 1, б).
в ВхРС3-клетках. Там эффекты LS-02 суще-
Сродство LS-01 и LS-02 к мембранным ре-
ственно отличались от эффектов прогесте-
цепторам изучалось с использованием клеток
рона и соединения LS-01, видимо, из-за очень
БИОХИМИЯ том 88 вып. 11 2023
2336
ЩЕЛКУНОВА и др.
высокой экспрессии сразу двух субтипов
ружили в клетках ВхРС3 на уровне транскрип-
mPRs, к которым три изучаемых стероида мо-
ции. В линии HepG2 прогестерон подавлял
гут иметь разное сродство.
экспрессию гена маркера пролиферации бел-
Значительно отличалось действие прогес-
ка Ki67, циклина D1, повышал экспрессию ин-
терона и селективных лигандов mPRs в клеточ-
гибитора 1А циклин-зависимой киназы - р21.
ных линиях HepG2 и ВхРС3 и на фрагмента-
Аналогично он действовал и в клетках ВхРС3.
цию ДНК ядер. В линии ВхРС3 прогестерон и
Однако эффектов LS-01 и LS-02 не было обна-
LS-01 достоверно и значительно (в 3-3,5 раза)
ружено. Возможно, активация mPRβ под дей-
увеличивали количество клеток с фрагмен-
ствием лигандов, взаимодействующих с мень-
тацией ДНК ядер, а LS-02 - в 2,2 раза. Глав-
шим сродством, оказалась недостаточной для
ным посредником в этом действии оказалась
проявления этого действия. Эффекты проге-
р38 МАРК. В клетках HepG2 мы не обнаружи-
стерона на экспрессию генов факторов, свя-
ли ни достоверного изменения этого парамет-
занных с апоптотическим процессом в клет-
ра, ни активации р38 МАРК под действием изу-
ках, оказались неожиданными. В клетках HepG2
чаемых соединений.
этот гормон повышал экспрессию гена про-
Действие прогестерона и селективных
апоптотического белка HRK (Harakiri) - бел-
лигандов было, наоборот, более выраженным
ка, взаимодействующего с Bcl2, но снижал
в клетках HepG2 на ранние стадии апоптоза,
экспрессию генов других проапоптотических
выявляемые по связыванию меченого аннек-
факторов - ВАХ, ВАD, каспазы 9 и DAPK -
сина V. В клетках ВхРС3 через 72 ч после ин-
протеинкиназы 1, ассоциированной со смер-
кубации с гормонами не было достоверных
тью (Death-associated protein kinase 1), притом
изменений в количестве апоптотических кле-
что суммарный эффект на процесс апоптоза
ток и клеток с признаками некроза в сравне-
был стимулирующим. Можно предположить,
нии с контролем. Наоборот, в линии HepG2
что на экспрессию некоторых генов прогесте-
все 3 стероида, а особенно мощно прогесте-
рон в высоких концентрациях может действо-
рон, увеличивали количество клеток с фос-
вать, активируя ядерные рецепторы глюко-
фатидилсерином на наружной мембране, свя-
кортикоидов. Глюкокортикоиды действуют на
зывающим аннексин V. Но при этом все 3 сте-
гепатоциты человека и крысы, ингибируя про-
роида, а особенно сильно прогестерон, снижа-
цесс апоптоза и способствуя их выживаемо-
ли количество некротических клеток, мембра-
сти [22, 23]. Прогестерон через глюкокорти-
ны которых проницаемы для йодида пропи-
коидные рецепторы может влиять на экспрес-
дия. Клетки линии HepG2 растут кластерами,
сию генов, чувствительных к этим гормонам.
не формируя монослой, в отличие от клеток
Селективные лиганды не взаимодействуют с
линии ВхРС3. При отсутствии гормонов в те-
ядерными рецепторами стероидных гормонов,
чение 72 ч в среде с бесстероидной сыворот-
поскольку у них отсутствует 3-кето/3-гидрокси
кой (DFBS) среди клеток HepG2 появлялась
группа в структуре А-кольца, принципиально
значительная популяция с признаками некро-
важная для такого взаимодействия [9, 24, 25].
тической гибели (т.е. клетки, мембраны кото-
Результирующее действие селективных лиган-
рых проницаемы для PI). Возможно, это про-
дов и самого прогестерона в клетках HepG2 на
исходило за счет кластерного роста клеток,
жизнеспособность и апоптоз, выявляемый по
снижения доступности питательных веществ
появлению фосфатидилсерина на наружной
и/или кислорода для нижних слоев. В присут-
мембране клеток, противоположно действию
ствии изучаемых стероидов рост клеток суще-
глюкокортикоидов на гепатоциты. Можно
ственно замедлялся, особенно в присутствии
предположить, что в данном случае главное
прогестерона. Через 72 ч инкубации с гормо-
действие этих соединений направлено не на
нами клеток в лунках было значительно мень-
изменение транскрипции генов, а на посттран-
ше, чем в контроле. Поэтому нижние слои
скрипционную активирующую модификацию
страдали меньше от недостатка питательных
самих белков - факторов апоптоза, которая
веществ или гипоксии, некроз был выражен
описана в литературе [26-29]. По-видимому,
слабее. При этом стероиды вызывали в клет-
это действие на посттранскрипционном уров-
ках процесс апоптотической гибели, ранние
не перекрывает побочный эффект активации
стадии которой выявлялись через 72 ч по свя-
прогестероном других стероидных рецепторов.
зыванию с меченым аннексином V.
На основании полученных результатов
Для изучения экспрессии генов под дей-
можно сделать заключение, что в клетках ге-
ствием прогестерона и селективных лигандов
патоцеллюлярной карциномы человека HepG2
были выбраны маркеры пролиферации и фак-
с высоким уровнем mPRβ прогестерон и се-
торы апоптоза, регуляцию которых мы обна-
лективные лиганды, активируя сигнальный
БИОХИМИЯ том 88 вып. 11 2023
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2337
каскад с участием JNK, действуют подавля-
ния LS-01 и LS-02 регулируют функции этих
юще на процесс пролиферации клеток, сти-
клеток, но для усиления этого действия необ-
мулируют экспонирование фосфатидилсери-
ходимы дальнейшие поиски эффективного ли-
на на наружной мембране клеток HepG2,
ганда, обладающего сродством к данным ре-
что является ранней стадией апоптотических
цепторам, сопоставимым со сродством про-
изменений. При этом замедляются процессы
гестерона, но при этом не взаимодействую-
некротических изменений в изучаемых клет-
щего с ядерными рецепторами прогестерона
ках, возможно, за счет подавления пролифе-
и других стероидов.
рации и снижения давления на нижние слои
верхних клеток в формируемых ими класте-
Вклад авторов. Щелкунова Т.А. - концеп-
рах. На более поздние стадии апоптоза влия-
ция и руководство работой; Щелкунова Т.А.,
ния LS-01, LS-02 и прогестерона выявлено
Морозов И.А., Гончаров А.И. - проведение
не было в изученном промежутке времени.
экспериментов; Левина И.С., Кузнецов Ю.В.,
Поскольку перечисленные эффекты были вы-
Заварзин И.В. - химический синтез соедине-
званы не только прогестероном, но и селек-
ний LS-01 и LS-02; Щелкунова Т.А., Леви-
тивными лигандами mPRs, действие это об-
на И.С., Морозов И.А., Рубцов П.М., Смир-
условлено активацией mPRβ. В изучаемых
нова О.В. - обсуждение результатов исследо-
HepG2-клетках все стероиды действовали од-
вания; Щелкунова Т.А. - написание текста;
нотипно, в отличие от клеток ВхРС3, что так-
Щелкунова Т.А., Левина И.С., Морозов И.А.,
же подтверждает их взаимодействие только с
Рубцов П.М., Смирнова О.В. - редактирова-
одним типом рецепторов. Действие прогести-
ние текста статьи.
нов на клетки HepG2, по-видимому, является
Финансирование. Исследование выпол-
специфическим именно для данного фено-
нено при финансовой поддержке Российского
типа, поскольку в первичной культуре клеток
фонда фундаментальных исследований (грант
миометрия, например, действие гормона че-
№ 20-015-00092-а) и Российского научного
рез mPRα и mPRβ сопровождалось активаци-
фонда (грант
ей р38 МАРК и приводило к фосфорилирова-
project/23-25-00071/).
нию легких цепей миозина и сократительной
Конфликт интересов. Авторы заявляют об
активности миометрия [18].
отсутствии конфликта интересов.
Таким образом, мы показали, что mPRβ в
Соблюдение этических норм. Настоящая
клетках гепатоцеллюлярной карциномы при
статья не содержит описания каких-либо ис-
взаимодействии с лигандами активируют сиг-
следований с участием людей или животных
нальный каскад, в котором принимает уча-
в качестве объектов.
стие JNK, что приводит к снижению пролифе-
Дополнительные материалы. Приложе-
ративной активности и стимуляции апопто-
ние к статье опубликовано на сайте журнала
тических процессов в этих клетках. Соедине-
СПИСОК ЛИТЕРАТУРЫ
1. Щелкунова Т. А., Морозов И. А. (2015) Молекуляр-
4. Diep, C. H., Daniel, A. R., Mauro, L. J., Knutson,
ные основы и тканевая специфичность действия
T. P., and Lange, C. A. (2015) Progesterone action
прогестинов, Мол. Биол., 49, 728-748, doi: 10.7868/
in breast, uterine, and ovarian cancers, J. Mol.
S0026898415050158.
Endocrinol., 54, R31-R53, doi: 10.1530/jme-14-0252.
2. González-Orozcoa, J. C., Hansberg-Pastorb, V.,
5. Gustafsson, J. A.,
(2016) Historical overview of
Valadez-Cosmesa, P., Nicolas-Ortegaa, W., Bastida-
nuclear receptors, J. Steroid Biochem. Mol. Biol., 157,
Beristaina, Y., Fuente-Granada, M., González-
3-6, doi: 10.1016/j.jsbmb.2015.03.004.
Arenas, A., and Camacho-Arroyo, I. (2018) Activation
6. Zhu, Y., Bond, J., and Thomas, P. (2003) Identifica-
of membrane progesterone receptor-alpha increas-
tion, classification, and partial characterization of genes
es proliferation, migration, and invasion of human
in humans and other vertebrates homologous to a fish
glioblastoma cells, Mol. Cell. Endocrinol., 477, 81-89,
membrane progestin receptor, Proc. Natl. Acad. Sci.
doi: 10.1016/j.mce.2018.06.004.
USA, 100, 2237-2242, doi: 10.1073/pnas.0436133100.
3. Xiao, J., Chen, X., Lu, X., Xie, M., He, B., He, S,
7. Thomas, P., Pang, Y., Camilletti, M. A., and Castel-
You, S, and Chen, Q. (2020) Progesterone/Org inhibits
novo, L. F. (2022) Functions of membrane proges-
lung adenocarcinoma cell growth via membrane
terone receptors (mPRs, PAQRs) in nonreproductive
progesterone receptor alpha, Thorac. Cancer,
11,
tissues, Endocrinology, 163, bqac147, doi: 10.1210/
2209-2223, doi: 10.1111/1759_7714.13528.
endocr/bqac147.
20
БИОХИМИЯ том 88 вып. 11 2023
2338
ЩЕЛКУНОВА и др.
8.
Thomas, P. (2022) Membrane progesterone recep-
ВхРС3 аденокарциномы поджелудочной железы
tors (mPRs, PAQRs): review of structural and sig-
человека, Биохимия, 86, 1702-1718, doi: 10.31857/
naling characteristics, Cells, 11, 1785, doi: 10.3390/
S0320972521110087.
cells11111785.
17.
Kasubuchi, M., Watanabe, K., Hirano, K., Inoue, D.,
9.
Kelder, J., Pang, Y., Dong, J., Schaftenaar, G., and
Li, X., Terasawa, K., Konishi, M., Itoh, N., and
Thomas, P. (2022) Molecular modeling, mutational
Kimura, I. (2017) Membrane progesterone receptor
analysis and steroid specificity of the ligand binding
beta (mPRβ/Paqr8) promotes progesterone-dependent
pocket of mPRα (PAQR7): shared ligand binding
neurite outgrowth in PC12 neuronal cells via non-G
with AdipoR1 and its structural basis, J. Steroid
protein-coupled receptor (GPCR) signaling, Sci. Rep.,
Biochem. Mol. Biol.,
219,
106082, doi:
10.1016/
7, 5168, doi: 10.1038/s41598-017-05423-9.
j.jsbmb.2022.106082.
18.
Karteris, E., Zervou, S., Pang, Y., Dong, J., Hill-
10.
Jyoti, M. M. S., Rana, M. R., Ali, M. H., and
house, E. W., Randeva, H. S., and Thomas, P. (2006)
Tokumoto, T.
(2022) Establishment of a steroid
Progesterone signaling in human myometrium through
binding assay for membrane progesterone recep-
two novel membrane G protein-coupled receptors:
tor alpha (PAQR7) by using graphene quantum dots
potential role in functional progesterone withdrawal
(GQDs), Biochem. Biophys. Res. Commun., 592, 1-6,
at term, Mol. Endocrinol., 20, 1519-1534, doi: 10.1210/
doi: 10.1016/j.bbrc.2022.01.002.
me.2005-0243.
11.
Acharjee, M., Ali, M. H., Jyoti, M. M. S., Rezanuj-
19.
Sinreih, M., Knific, T., Thomas, P., Grazio, S. F., and
jaman, M., Hassan, M. M., Rana, M. R., Hossain,
Rižner, T. L. (2018) Membrane progesterone receptors
M. F., Kodani, S., and Tokumoto, T. (2022) The an-
β and γ have potential as prognostic biomarkers of
tagonistic activity of Padina arborescens extracts on
endometrial cancer, J. Steroid. Biochem. Mol. Biol.,
mPRα, Nat. Prod. Res., 37, 1872-1876, doi: 10.1080/
178, 303-311, doi: 10.1016/j.jsbmb.2018.01.011.
14786419.2022.2120873.
20.
Büscher, U., Chen, F. C., Kentenich, H., and
12.
Levina, I. S., Kuznetsov, Y. V., Shchelkunova, T. A.,
Schmiady, H. (1999) Cytokines in the follicular fluid
and Zavarzin, I. V. (2021) Selective ligands of mem-
of stimulated and nonstimulated human ovaries; is
brane progesterone receptors as a key to studying their
ovulation a suppressed inflammatory reaction? Hum.
biological functions in vitro and in vivo, J. Steroid Bio-
Reprod., 14, 162-166, doi: 10.1093/humrep/14.1.162.
chem. Mol. Biol., 207, 105827, doi: 10.1016/j.jsbmb.
21.
Atif, F., Yousuf, S., and Stein, D. G. (2015) Anti-
2021.105827.
tumor effects of progesterone in human glioblastoma
13.
Goncharov, A. I., Maslakova, A. A., Polikarpova, A. V.,
multiforme: role of PI3K/Akt/mTOR signaling, J. Ste-
Bulanova, E. A., Guseva, A. A., Morozov, I. A.,
roid Biochem. Mol. Biol., 146, 62-73, doi: 10.1016/
Rubtsov, P. M., Smirnova, O. V., and Shchelkunova,
j.jsbmb.2014.04.007.
T. A. (2017) Progesterone inhibits proliferation and
22.
Bailly-Maitre, B., Souse, G., Boulukos, K., Gugen-
modulates expression of proliferation-Related genes
heim, J., and Rahmani, R. (2001) Dexamethasone
in classical progesterone receptor-negative human
inhibits spontaneous apoptosis in primary cultures
BxPC3 pancreatic adenocarcinoma cells, J. Steroid
of human and rat hepatocytes via Bcl-2 and Bcl-xL
Biochem. Mol. Biol., 165, 293-304, doi: 10.1016/
induction, Cell Death Differ., 8, 279-288, doi: 10.1038/
j.jsbmb.2016.07.007.
sj.cdd.4400815.
14.
Polikarpova, A. V., Maslakova, A. A., Levina, I. S.,
23.
Oh, H.-Y., Namkoong, S., Lee, S.-J., Por, E., Kim,
Kulikova, L. E., Kuznetsov, Y. V., Guseva, A. A.,
C.-K., Billiar, T. R., Han, J. A., Ha, K. S., Chung,
Shchelkunova, T. A., Zavarzin, I. V., and Smirnova, O. V.
H. T., Kwon, Y. G., Lee, H., and Kim, Y. M. (2006)
(2017) Selection of progesterone derivatives specific to
Dexamethasone protects primary cultured hepato-
membrane progesterone receptors, Biochemistry (Mos-
cytes from death receptor-mediated apoptosis by up-
cow), 82, 140-148, doi: 10.1134/S0006297917020055.
regulation of cFLIP, Cell Death Differ., 13, 512-523,
15.
Левина И. С., Щелкунова Т. А., Поликарпова А. В.,
doi: 10.1038/sj.cdd.4401771.
Кузнецов Ю. В., Заварзин И. В. (2021) Синтез
24.
Williams, S. P., and Sigler, P. B. (1998) Atomic
19-гидроксипрегн-4-ен-20-она и 19-гидрокси-5β-
structure of progesterone complexed with its receptor,
прегн-3-ен-20-она, селективно связывающихся
Nature, 393, 392-396, doi: 10.1038/30775.
с мембранными рецепторами прогестерона, и
25.
Tanenbaum, D. M., Wang, Y., Williams, S. P., and
оценка их иммуномодуляторных эффектов, Изв.
Sigler, P. B. (1998) Crystallographic comparison of the
АН Сер. Хим., 11, 2227-2232, doi: 10.1007/s11172-021-
estrogen and progesterone receptor’s ligand binding
3337-6.
domains, Proc. Natl. Acad. Sci. USA, 95, 5998-6003,
16.
Гончаров А. И., Левина И. С., Шляпина В. Л.,
doi: 10.1073/pnas.95.11.5998.
Морозов И. А., Рубцов П. М., Заварзин И. В.,
26.
Moldoveanu, T., and Czabotar, P. E. (2020) BAX,
Смирнова О. В., Щелкунова Т. А. (2021) Цито-
BAK, and BOK: a coming of age for the BCL-2 family
токсические эффекты селективных лигандов
effector proteins, Cold Spring Harb. Perspect. Biol., 12,
мембранных рецепторов прогестерона в клетках
a036319, doi: 10.1101/cshperspect.a036319.
БИОХИМИЯ том 88 вып. 11 2023
ЭФФЕКТЫ ПРОГЕСТЕРОНА, LS-01 И LS-02 В КЛЕТКАХ HepG2
2339
27. Kale, J., Osterlund, E. J., and Andrews, D. W. (2018)
preapoptotic phase, Cell Death Differ., 12, 571-584,
BCL-2 family proteins: changing partners in the
doi: 10.1038/sj.cdd.4401591.
dance towards death, Cell Death Differ., 25, 65-80,
29. Roberts, J. Z., Crawford, N., and Longley, D. B.
doi: 10.1038/cdd.2017.186.
(2022) The role of ubiquitination in apoptosis
28. Morley, S. J., Coldwell, M. J., and Clemens,
and necroptosis, Cell Death Differ., 29, 272-284,
M. J. (2005) Initiation factor modifications in the
doi: 10.1038/s41418-021-00922-9.
EFFECTS OF PROGESTERONE AND SELECTIVE LIGANDS
OF MEMBRANE PROGESTERONE RECEPTORS IN HepG2 CELLS
OF HUMAN HEPATOCELLULAR CARCINOMA
T. A. Shchelkunova1*, I. S. Levina2, I. A. Morozov3, P. M. Rubtsov3, A. I. Goncharov1,
Yu. V. Kuznetsov2, I. V. Zavarzin2, and O. V. Smirnova1
1 Faculty of Biology, Lomonosov Moscow State University,
119234 Moscow, Russia; e-mail: Schelkunova-t@mail.ru
2 Zelinsky Institute of Organic Chemistry, Russian Academy of Sciences, 119991 Moscow, Russia
3 Engelhardt Institute of Molecular Biology, Russian Academy of Sciences, 119991 Moscow, Russia
Progesterone exerts multiple effects in different tissues through nuclear receptors (nPRs) and through mem-
brane receptors of the adiponectin and progestin receptor (mPRs) family. The effect of progesterone on
cells through different types of receptors can vary significantly. At the same time, it affects the processes
of proliferation and apoptosis in normal and tumor tissues in a dual way, stimulating proliferation and car-
cinogenesis in some tissues, suppressing them and stimulating cell death in others. In this study, we have
shown the presence of a high level of mRNA and mPRβ protein in HepG2 tumor cells of human hepa-
tocellular carcinoma. Expression of other membrane and classical nuclear receptors was not detected.
May be mPRβ has an important function in HepG2 cells. The main goal of the work was to study the func-
tion of this protein and the mechanisms of its action in human hepatocellular carcinoma cells. Previously,
we have identified selective mPRs ligands, compounds LS-01 and LS-02, which do not interact with nuclear
receptors. Their employment allows differentiating the effects of progestins mediated by different types
of receptors. The work studied the effects of progesterone, LS-01 and LS-02 on the proliferation and death
of HepG2 cells, as well as the activating phosphorylation of two kinases, p38 MAPK and JNK, under the
action of three steroids. It was shown that all three progestins after 72 hours of incubation with cells sup-
pressed their viability and stimulated the appearance of phosphatidylserine on the outer surface of mem-
branes, which was detected by binding to V-FITC annexin, but they did not affect DNA fragmentation of
cell nuclei. Progesterone significantly reduced the expression of proliferation marker genes and stimulated
the expression of the p21 protein gene, but had a suppressive effect on the expression of some proapoptotic
factor genes. All three steroids activated JNK in these cells, but had no effect on p38 MAPK activity.
The effects of progesterone and selective mPRs ligands in HepG2 cells were the same in terms of suppres-
sion of proliferation and stimulation of apoptotic changes in outer membranes, therefore, they were medi-
ated through interaction with mPRβ. JNK is a member of the signaling cascade activated in these cells by
the studied steroids.
Keywords: progesterone, selective ligands of membrane progesterone receptors, proliferation, apoptosis, nuclear
progesterone receptor, membrane progesterone receptor β, human HepG2 hepatocellular carcinoma cells
БИОХИМИЯ том 88 вып. 11 2023
20*