БИОХИМИЯ, 2023, том 88, вып. 5, с. 693 - 724
УДК 612.822
ГЛЮКОКОРТИКОИДЫ - РЕГУЛЯТОРЫ ПЛАСТИЧНОСТИ ВЗРОСЛОГО
ГИППОКАМПА: ТОЧКИ РОСТА И ТРАНСЛЯЦИОННЫЕ АСПЕКТЫ*
Обзор
© 2023 Н.В. Гуляева1,2
1 ФГБУН Институт высшей нервной деятельности и нейрофизиологии РАН,
117485 Москва, Россия; электронная почта: nata_gul@ihna.ru
2 ГБУЗ Научно-практический психоневрологический центр им. З.П. Соловьева
Департамента здравоохранения города Москвы, 115419 Москва, Россия
Поступила в редакцию 27.03.2023
После доработки 10.04.2023
Принята к публикации 10.04.2023
В обзоре проанализированы современные представления о контроле глюкокортикоидами раз-
личных механизмов пластичности гиппокампа взрослых млекопитающих и человека. Глюкокор-
тикоидные гормоны обеспечивают согласованное функционирование ключевых компонентов
и механизмов гиппокампальной нейропластичности: нейрогенеза, глутаматергической нейро-
трансмиссии, микроглии и астроцитов, систем нейротрофических факторов, нейровоспаления,
протеаз, метаболических гормонов, нейростероидов. Регуляторные механизмы многообразны:
наряду с прямым действием глюкокортикоидов через специфические рецепторы, описаны опо-
средованные глюкокортикоид-зависимые воздействия, а также многочисленные взаимодействия
между различными системами и компонентами, опосредующими нейропластичность. Несмотря
на то что многие связи в этой сложной регуляторной схеме до сих пор не установлены, изучение
рассмотренных в работе факторов и механизмов формирует точки роста в области исследований
регулируемых глюкокортикоидами процессов в мозге и в первую очередь в гиппокампе. Эти ис-
следования принципиально важны для трансляции в клинику и потенциального лечения/преду-
преждения распространенных заболеваний эмоциональной и когнитивной сфер и коморбидных
им состояний.
КЛЮЧЕВЫЕ СЛОВА: нейропластичность, гиппокамп, глюкокортикоиды, гипоталамо-гипофизарно-над-
почечниковая ось, синаптическая пластичность, стресс, нейрогенез, нейровоспаление, глутаматергиче-
ская трансмиссия, протеазы, BDNF, инсулинорезистентность, депрессия, болезнь Альцгеймера, старение.
DOI: 10.31857/S0320972523050019, EDN: AXHRHM
ВВЕДЕНИЕ.
изменение нервной системы в ответ на изме-
ГИППОКАМП - МИШЕНЬ
нение внешних сигналов, охватывает множе-
ГЛЮКОКОРТИКОИДОВ
ство процессов и механизмов их реализации,
В НОРМЕ И ПРИ ПАТОЛОГИИ
от рождения, выживания, миграции и инте-
грации новых нейронов, роста нейритов, си-
Пластичность нейронов и глиальных кле-
наптогенеза и модуляции зрелых синапсов до
ток играет жизненно важную роль в передаче
формирования и трансформации нейронных
и интеграции сигналов в центральной нерв-
сетей. Фундаментальным механизмом плас-
ной системе. Нейропластичность, адаптивное тичности взрослого мозга является зависимая
Принятые сокращения: ACTH - адренокортикотропный гормон; AMPAR - рецепторы α-амино-3-гидрокси-
5-метил-4-изоксазолпропионовой кислоты (АМРА); APP - белок-предшественник амилоида; BACE1 - β-секретаза 1;
BDNF - нейротрофический фактор головного мозга; CRH - кортикотропин-рилизинг-гормон; GR - глюкокортико-
идные рецепторы; MAPK - митоген-активируемая протеинкиназа; mGluR - метаботропные глутаматные рецепторы;
ММР - металлопротеиназы; MR - минералокортикоидные рецепторы; NMDAR - N-метил-D-аспартатные рецепторы;
TrkB - тропомиозиновый тирозинкиназный рецептор B; БА - болезнь Альцгеймера; ГГНО - гипоталамо-гипофизарно-
надпочечниковая ось; ГК -глюкокортикоиды.
* Статья опубликована в рамках специального выпуска «Биохимические аспекты разных уровней нейропластичности:
молекулы, гены, синапсы, клетки, когнитивные процессы» (том 88, №№ 3-4, 2023).
693
694
ГУЛЯЕВА
от активности нейронов реорганизация пред-
Стресс как адаптивная реакция на изме-
существующей структуры, и именно пластич-
няющиеся условия окружающей среды необ-
ность мозга взрослого человека позволяет ему
ходим для выживания организма. ГК, сте-
учиться на протяжении всей жизни. Исследо-
роидные «гормоны стресса», секретируемые
вания последних десятилетий позволили оха-
фасцикулярной зоной коры надпочечников,
рактеризовать не только пластические струк-
имеют решающее значение для успешной
турно-функциональные перестройки мозга,
адаптации к стрессорам, и в реализация этой
но и несколько форм синаптической пластич-
важной для выживания организма функ-
ности, определив их как ключевые процессы,
ции ГК ключевое место принадлежит именно
которые позволяют мозгу работать динамично
способности этих гормонов регулировать бы-
и осуществлять обучение, запоминание и ис-
струю и долговременную пластичность мозга.
пользование памяти [1]. Нейропластичность
Воздействие стресса вызывает активацию
является основой адаптации мозга к изменяю-
ключевой нейрогуморальной системы орга-
щимся условиям внешней и внутренней среды,
низма, гипоталамо-гипофизарно-надпочечни-
а аберрантные изменения пластичности ассо-
ковой оси (ГГНО) и связанных с ней нейрохи-
циированы с патологическими состояниями.
мических реакций после высвобождения ГК из
Глюкокортикоиды (ГК), оказывая влияние
надпочечников, что и лежит в основе быстрых
согласованно с катехоламинами, контролиру-
физиологических реакций. Стимуляция ГГНО
ют поведенческую адаптацию к стрессу и улуч-
приводит к активации определенных областей
шают сохранение значимой эмоциональной
мозга, включая гиппокамп, миндалевидное
информации; они динамично регулируют си-
тело и префронтальную кору, в которых высо-
наптическую функцию и синаптическую плас-
ка плотность рецепторов ГК [5].
тичность, лежащие в основе формирования
Действуя через специфические внутрикле-
эмоциональной памяти [2]. Формирование и
точные рецепторы в головном мозге и на пери-
использование памяти - сложный процесс, в
ферии, ГК регулируют поведение, а также мета-
котором участвуют несколько структур мозга,
болическую, сердечно-сосудистую, иммунную
такие как гиппокамп, миндалевидное тело и
и нейроэндокринную активности. ГК связы-
прилегающие области коры, обычно опреде-
ваются с двумя подтипами рецепторов: мине-
ляемые как медиальные структуры височной
ралокортикоидными рецепторами (MR) и глю-
доли. Считают, что после обучения многие
кокортикоидными рецепторами (GR), отлича-
формы памяти первоначально кодируются в
ющимися по своей аффинности к ГК. Как MR,
гиппокампе, но впоследствии энграммы дли-
так и GR могут быть локализованы внутри-
тельно сохраняются и в других областях мозга,
клеточно или на мембране. MR и GR акти-
таких как неокортекс (этот процесс известен
вируются под действием ГК и опосредуют их
как консолидация системной памяти). Синап-
эффекты, в т.ч. на быстрые и долговремен-
тическая пластичность является основным
ные события синаптической пластичности.
клеточным механизмом, лежащим в основе
GR присутствуют в каждой клетке нервной
обучения и памяти, и поэтому считается клю-
системы, но уровень экспрессии варьируется,
чевой в этом процессе [3]. Во взрослом гиппо-
поэтому разные типы клеток по-разному реа-
кампе, лимбической структуре, отвечающей
гируют на активацию GR [6]. Классически ГК
как за когнитивные функции, так и за эмоции,
оказывают свое влияние на мозг через геном-
синаптическая пластичность важна для обра-
ные механизмы, включающие внутриклеточ-
ботки информации, обучения и кодирования
ные MR и GR, непосредственно связываю-
памяти. Зубчатая извилина взрослого гиппо-
щиеся с ДНК. В последние годы было показано
кампа постоянно генерирует когорты нейро-
наличие мембранных MR и GR, связанных с
нов, часть из которых выживает, созревает и
G-белками, активация которых запускает сиг-
интегрируется в существующие нейронные
нальные каскады и, как полагают, реализует
цепи, и этот процесс регулируется как гло-
быстрые эффекты ГК также через негеномные
бальной, так и локальной нейронной актив-
механизмы [7] (рис. 1).
ностью, обеспечивая уникальную клеточную
Эффекты ГК могут сильно различаться в
и синаптическую пластичность гиппокампа.
зависимости от типа рецептора, а также от об-
По-видимому, возникновение новых нейро-
ласти мозга, типа клеток и физиологического
нов гиппокампа на протяжении всей жизни
контекста. Эти различия в конечном счете за-
позволяет постоянно
«омолаживать» мозг
висят от дифференциальных взаимодействий
взрослых млекопитающих, включая челове-
MR и GR с другими белками, которые опре-
ка, и поддерживать адаптивные пластические
деляют связывание лиганда, ядерную транс-
свойства мозга [4].
локацию и транскрипционную активность.
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
695
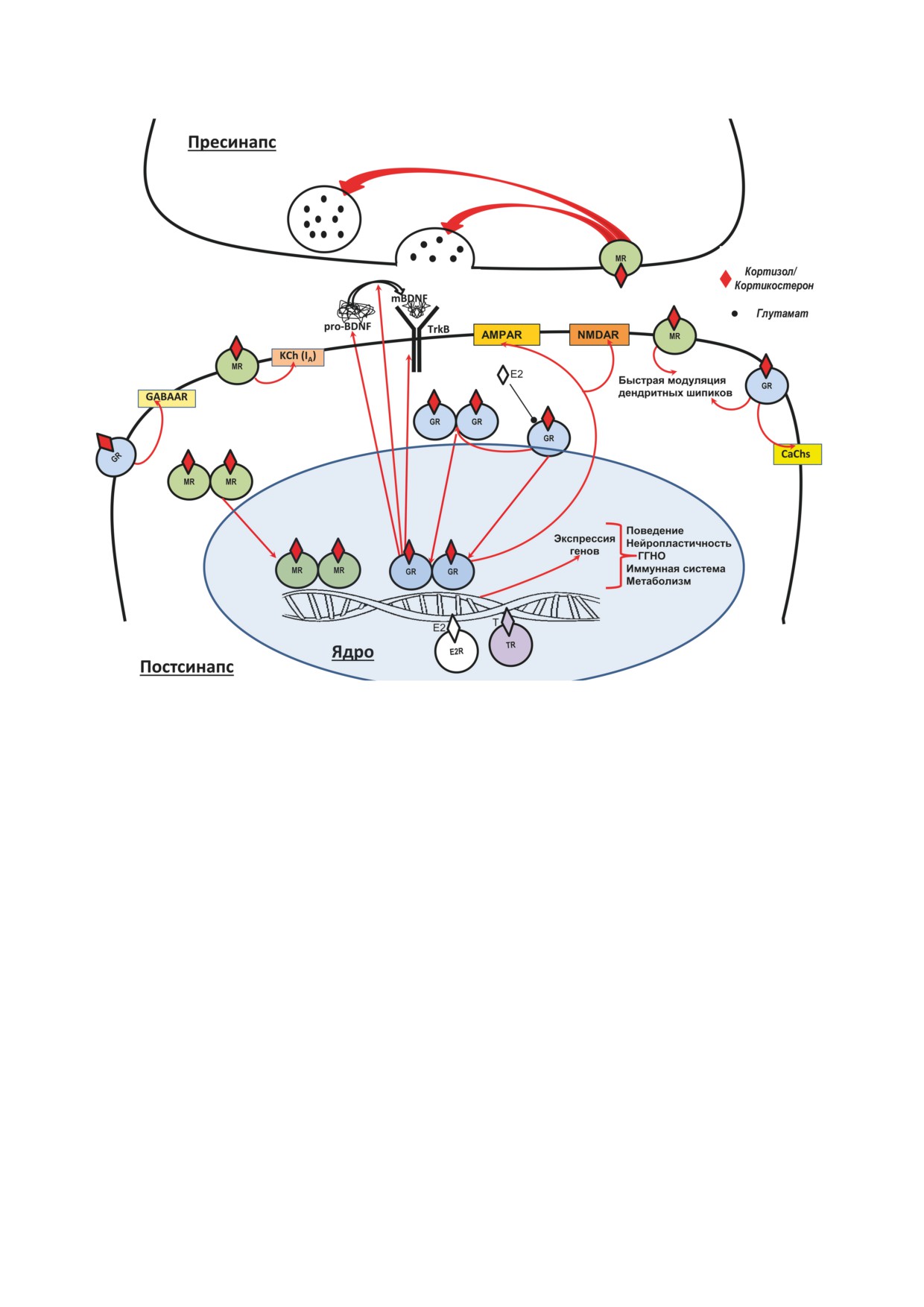
Рис. 1. Рецепторы глюкокортикоидов (ГК) в глутаматергическом синапсе (схема составлена по данным, представлен-
ным в опубликованных недавно работах [7-11]). Кортикостерон (у грызунов) или кортизол (у человека) высвобожда-
ются из надпочечников в кровоток. Как липидорастворимые молекулы, ГК могут свободно проникать через клеточную
мембрану. Когда ГК связывается с цитозольными глюкокортикоидными рецепторами (GR) и минералокортикоидными
рецепторами (MR), это приводит к высвобождению регуляторных комплексов, таких как HSP90, FKBP5 и BAG1,
с последующей димеризацией рецепторов и транслокацией их в ядро. Связывание димеризованных GR (MR) с пред-
полагаемыми элементами глюкокортикоидного ответа (GRE), присутствующими в промоторных областях, инду-
цирует активацию факторов транскрипции. Половые стероидные гормоны эстрадиол (E2) и тестостерон (Т) могут
модулировать экспрессию GR-зависимых генов (Е2R, TR - рецепторы эстрадиола и тестостерона соответственно).
Контролируемые ГК гены регулируют экспрессию ионотропных рецепторов глутамата (NMDAR, AMPAR), системы
трофических факторов (BDNF), включая синтез про-BDNF (pro-BDNF), протеолитическое превращение его в зре-
лый BDNF (mBDNF), и синтез рецептора BDNF TrkB. Экспрессия ГК-зависимых генов контролирует функциони-
рование гипоталамо-гипофизарно-надпочечниковой оси (ГГНО), нейропластичность, поведение, иммунную систему
и метаболизм. В отличие от классических цитозольных/ядерных рецепторов, мембранные GR и MR реализуют бы-
стрые эффекты ГК, модулируя высвобождение глутамата в пресинапсе, а в постсинаптической мембране - активность
рецепторов γ-аминомасляной кислоты (GABAAR), катионных каналов: нескольких типов кальциевых (CaCh) и ка-
лиевого KCh (IA), а также быстрые изменения дендритных шипиков. Эстрадиол (Е2) конкурирует с кортикостероном
за ингибирование передачи сигналов GR
MR и GR головного мозга могут опосредовать
ное распределение MR и GR зависит от равно-
очень разные, а иногда и противоположные
весия между ядерным импортом и экспортом.
эффекты. Экспрессия MR в мозге гораздо бо-
Это равновесие, по-видимому, зависит от типа
лее ограничена в сравнении с GR. MR наи-
клеток [9, 10].
более распространен в гиппокампе грызу-
ГК взаимодействуют (как геномно, так и
нов и человека, где экспрессия MR равна
негеномно) с нейромедиаторами, нейротро-
или превышает экспрессию GR в пирамид-
фическими факторами, половыми гормонами и
ных клетках CA3 [8]. Известно, что MR и GR
другими медиаторами стресса, формируя настоя-
перемещаются между цитоплазматическими и
щие и будущие реакции организма на стресс.
ядерными компартментами, а внутриклеточ-
В гиппокампе и других стресс-реактивных
БИОХИМИЯ том 88 вып. 5 2023
696
ГУЛЯЕВА
областях мозга аллостатическая перегрузка,
рилизинг-гормона (CRH) вазопрессина, основ-
возникающая в результате хронического стрес-
ных регуляторов гипофизарного адренокорти-
са, может изменить функционирование ГГНО
котропного гормона (ACTH). Механизмы бы-
и посредством эпигенетической модифика-
строй обратной связи, включающие негеном-
ции [7]. В многочисленных экспериментах на
ные действия ГК, опосредуют немедленное
животных показано, что в базовых условиях с
ингибирование гипоталамической секреции
низкой секрецией ГК занятость MR близка к
CRH и ACTH, а более медленные механизмы,
насыщению. Когда уровни ГК повышаются во
опосредованные геномом, включают модуля-
время стресса или пика циркадианного цикла
цию лимбических сетей и периферических ме-
этих гормонов, MR становится полностью за-
таболических мессенджеров [14].
нятым, и связывание ГК происходит главным
Избыток ГК может иметь негативные эф-
образом с GR. Важная роль ГК в нейроплас-
фекты особенно в гиппокампе, в котором вы-
тичности была постулирована несколько деся-
сока плотность MR и GR [15]. Эти эффекты
тилетий назад [12], однако конкретные меха-
включают нарушение синаптической пластич-
низмы регуляторной функции ГК до конца не
ности, атрофию дендритов, нарушение спо-
расшифрованы. Широкая распространенность
собности нейронов выживать при действии
GR в различных популяциях нервных и глиаль-
различных повреждающих факторов и в ко-
ных клеток также за пределами классических
нечном итоге гибель нейронов [16]. Избира-
областей мозга, отвечающих за реализацию
тельная уязвимость гиппокампа к стрессу,
стресс-реакции, подтверждают представление
опосредованная рецепцией выделяемых при
о том, что в ЦНС ГК могут действовать как
стрессе ГК, является ценой высокой функцио-
дирижер, организующий и контролирующий
нальной пластичности и плейотропности этой
мозговой оркестр, состоящий из различных
лимбической структуры [17]. Общие молеку-
клеток, включенных в специфические сети.
лярные и клеточные механизмы нарушения
Плейотропность эффектов ГК непосредствен-
пластичности гиппокампа включают дисфунк-
но связана с множественными механизмами,
цию GR, систем нейротрансмиттеров и нейро-
которые они запускают и/или контролируют
трофических факторов, развитие нейровос-
на всех уровнях от молекулярного до сетевого
паления, приводящее к нейродегенерации и
и организменного.
гибели нейронов гиппокампа, а также наруше-
Стресс посредством ГК индуцирует струк-
ния нейрогенеза в субгранулярной нейроген-
турную пластичность нейронов, шванновских
ной нише и формирование аберрантных ней-
клеток, микроглии, олигодендроцитов и астро-
ронных сетей.
цитов, а также влияет на нейротрансмиссию,
Нормальная пластичность нервной систе-
изменяя высвобождение и обратный захват
мы необходима для адаптации, обучения и
глутамата. Воздействие стрессоров вызывает
памяти, а пластичность, вызванная стрессом,
спектр реакций, которые варьируются от по-
часто является неадекватной и способству-
тенциально адаптивных до дезадаптивных по-
ет развитию нейропсихических расстройств
следствий на структурном, клеточном и фи-
и других патологий мозга [18]. Структурная
зиологическом уровнях. Эти ответы особенно
пластичность гиппокампа играет ключевую
выражены в гиппокампе, где они также влияют
роль в этиопатогенезе нейродегенеративных
на гиппокамп-зависимую когнитивную функ-
заболеваний [19]. Влияние ГК на мозг имеет
цию и эмоциональность [13]. В отличие от хро-
решающее значение для поддержания гомео-
нически повышенных уровней, циркадианные
стаза, поэтому эти гормоны вовлечены и в про-
и острые стресс-индуцированные периоды уве-
цесс старения, которое определяется как пе-
личения ГК необходимы для выживания ней-
риод онтогенеза со сниженной способностью
ронов гиппокампа, приобретения и консоли-
поддерживать гомеостаз, повышенной лабиль-
дации памяти, облегчения глутаматергической
ностью ГГНО после стресса и нарушением
нейротрансмиссии и образования возбуждаю-
поведенческой адаптации [20]. По-видимому,
щих синапсов, индукции немедленных ранних
дисфункция ГК-зависимых процессов ассо-
генов и образования дендритных шипиков.
циирована практически со всеми патологиями
Отрицательная обратная связь со стороны ГК
мозга, поэтому неполное понимание соответ-
включает несколько механизмов, ведущих к
ствующих механизмов не позволяет в полной
ограничению активации ГГНО и предотвра-
мере использовать потенциальные возмож-
щению вредных эффектов чрезмерной гене-
ности предотвращения и терапии заболева-
рации ГК. Адекватная секреция ГК регули-
ний мозга.
руется нервной системой, контролирующей
В данном обзоре проанализированы совре-
секрецию гипоталамического кортикотропин-
менные представления о ключевых механизмах
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
697
гиппокампальной нейропластичности, находя-
постоянно, другие со временем изменяются,
щихся под контролем ГК. Это механизмы, из-
и это позволяет предположить, что представ-
учение которых формирует точки роста в обла-
ленные воспоминания также могут быть пре-
сти изучения регулируемых посредством ГК
образованы. Наиболее вероятно, что нейро-
процессов в мозге, принципиально важные для
генез во взрослом гиппокампе представляет
трансляции в клинику и потенциального лече-
собой один из процессов, который постоянно
ния/предупреждения распространенных забо-
перестраивает нейронные сети гиппокампа,
леваний эмоциональной и когнитивной сфер,
предположительно, включая сохраненные эн-
в том числе депрессивных расстройств, болез-
граммы [22]. Считают, что нейронные цепи
ни Альцгеймера (БА) и других.
зубчатой извилины - области СА3 взрослого
гиппокампа постоянно модифицируются за
счет интеграции рожденных в результате ней-
НЕЙРОГЕНЕЗ
рогенеза гранулярных клеток зубчатой извили-
КАК ФОРМА РЕГУЛИРУЕМОЙ
ны. Эти клетки проходят длительный период
ГЛЮКОКОРТИКОИДАМИ
созревания, в течение которого они прояв-
ПЛАСТИЧНОСТИ ГИППОКАМПА
ляют повышенную синаптическую пластич-
ность, эффективные электрофизиологические
Нервная система взрослого организма не
свойства и коннективность. Предполагается,
статична; она подвергается морфологическим
что нейрогенез взрослого гиппокампа позво-
и физиологическим изменениям на различных
ляет генерировать библиотеку событий/нового
уровнях. Такой пластический механизм гаран-
опыта, каждое из которых регистрируется в
тирует, что поведенческая регуляция нервной
физиологических свойствах и коннективности
системы адаптируется к различным раздра-
зрелых гранулярных клеток зубчатой извили-
жителям окружающей среды. Принято счи-
ны [23]. По-видимому, нейрогенез обеспечи-
тать, что в гиппокампе млекопитающих про-
вает гибкость зубчатой извилины, позволяю-
цесс образования и развития функционально
щую быстро генерировать специфичное для
интегрированных нейронов происходит на
контекста распределенное представление важ-
протяжении всей жизни и вносит существен-
ных сенсорных стимулов, таких как простран-
ный вклад в высокопластичную природу зре-
ственные сигналы, что в конечном итоге при-
лой центральной нервной системы. Зубчатая
водит к их различению на поведенческом
извилина гиппокампа - одна из основных
уровне [24]. При этом бо льшая часть результа-
нейрогенных ниш во взрослом организме,
тов, положенных в основу концепций о роли
содержащая стволовые клетки, клетки-пред-
нейрогенеза взрослого гиппокампа в нейро-
шественники и новые нейроны, часть которых
пластичности, получена на млекопитающих
созревает и включается в нейронные сети [4].
животных, в основном грызунах, а ряд мето-
Нейрогенез во взрослом гиппокампе пред-
дических ограничений вызывает непрекраща-
ставляет собой динамический процесс, свя-
ющиеся дебаты об интенсивности (и вообще
занный с когнитивными функциями, такими
наличии) нейрогенеза в гиппокампе взрослого
как обучение и память. При этом ряд иссле-
человека [25]. Однако, несмотря на методи-
дователей считает, что нейрогенез не является
ческие трудности исследования нейрогенеза
механизмом замены клеток во взрослом мозге,
у человека, большинство специалистов при-
а вместо этого поддерживает пластическую
нимает, что зубчатая извилина гиппокампа
нейронную сеть гиппокампа за счет непрерыв-
эволюционно законсервирована как один из
ного добавления незрелых, новых нейронов с
немногих участков нейрогенеза у взрослых
уникальными свойствами и структурной плас-
млекопитающих, хотя и остается до конца не
тичностью, а также изменения пластичности
ясным, интегрируются ли новые нейроны в
зрелых нейронов, индуцированные новыми
существующие сети гиппокампа наравне с
нейронами [21].
нейронами, рожденными в процессе развития,
Принято считать, что у людей и других
или же они представляют собой дискретную
млекопитающих воспоминания о событиях
клеточную популяцию с уникальными функ-
кодируются ансамблями нейронов (энграм-
циями [26]. Возможно, в результате нейрогене-
мами) в гиппокампе. Мнемоническая инфор-
за во взрослом гиппокампе создается специа-
мация, хранящаяся в этих энграммах, может
лизированная субпопуляция нейронов, которая
затем использоваться для управления буду-
может играть ключевую роль в функциях гип-
щим поведением, включая прогнозирование и
покампа, таких как эпизодическая память.
принятие решений в динамичной среде. Неко-
Добавление новых нейронов во взрослом
торые энграммы гиппокампа могут храниться
возрасте происходит в рамках последователь-
БИОХИМИЯ том 88 вып. 5 2023
698
ГУЛЯЕВА
ного многоступенчатого процесса. Нейроген-
нейрогенеза во взрослом гиппокампе в опо-
ные стадии включают пролиферацию, диф-
средовании поведенческого ответа на хрони-
ференцировку, миграцию, созревание/выжи-
ческий стресс остается не до конца изученной,
вание и интеграцию новых нейронов в суще-
и вопрос о том, действуют ли новорождённые
ствующую нейронную сеть. Большинство ис-
нейроны как своеобразный буфер или, наобо-
следований, оценивающих влияние экзоген-
рот, повышают восприимчивость к вызванной
ных (например, ГК, стресса) или эндоген-
стрессом эмоциональной дезадаптации, оста-
ных (например, нейротрофинов и их рецеп-
ется спорным [31].
торов) факторов на нейрогенез у взрослых
В начале 2000-х гг. было подтверждено, что
на разных уровнях, были сосредоточены на
ГК/хронический стресс/нейровоспаление яв-
пролиферации, выживании и дифференци-
ляются одними из самых важных отрицатель-
ровке нейронов [27]. Взаимодействие между
ных регуляторов нейрогенеза у взрослых. Хотя
внешними и внутренними факторами играет
воздействие острого и умеренного стресса на
фундаментальную роль в регуляции нейро-
нейрогенез, как правило, кратковременно и
генеза. За последние десятилетия несколько
может быть быстро преодолено, хроническое
исследований
«внутренних» путей, включая
воздействие или более тяжелые формы стресса
факторы транскрипции, выявили их фунда-
могут вызывать более продолжительное угне-
ментальную роль в регуляции каждого этапа
тение нейрогенеза, которое лишь частично мо-
нейрогенеза. Однако вполне вероятно, что ре-
жет быть преодолено последующим воздей-
гуляция транскрипции является частью более
ствием физических упражнений, приемом
сложной регуляторной сети, которая включает
адаптогенных препаратов и некоторых анти-
эпигенетические модификации, некодирую-
депрессантов [32]. Не вызывает сомнения, что
щие РНК и метаболические пути [28]. Важно,
опосредованные ГК нарушения нейрогенеза у
что гормоны, в первую очередь стероидные,
взрослых способствуют возникновению болез-
осуществляют многогранное влияние на все
ней мозга, включая когнитивные и аффектив-
стадии нейрогенеза во взрослом гиппокампе:
ные нарушения, нейродегенеративные забо-
имеются доказательства гормональной сти-
левания. Кроме того, воздействие стресса,
муляции (через гормоны гонад - эстрогены
особенно в критические периоды раннего дет-
и андрогены, а также тиреоидные гормоны),
ства, нарушая процессы нейрогенеза на дли-
ингибирования (через ГК) и нейропротекции,
тельный период, может перепрограммировать
опосредованной нейротрофинами и нейромо-
пластичность гиппокампа, увеличивая риск
дуляторами [29].
развития в дальнейшем когнитивных наруше-
Нейрогенез во врослом гиппокампе в по-
ний или симптомов тревоги, общих для ряда
следние годы все чаще рассматривается через
церебральных патологий, таких как деменция
призму реакции мозга на стресс. Предполага-
и депрессия, ассоциированных с хронически-
ется, что нейрогенез играет ключевую роль
ми изменениями пластичности гиппокампа.
в формировании адаптации к изменениям
В обзоре Podgorny и Gulyaeva [33] подробно
окружающей среды, что и лежит в основе его
проанализировано влияние ГК на механизмы и
роли в реакции на стресс (избыток ГК). Гип-
физиологические особенности нейрогенеза во
покамп с его высокой конвергенцией на входе
взрослом гиппокампе и изменения нейрогене-
и дивергенцией на выходе представляет собой
за при церебральных патологиях. Нервно-пси-
своеобразный вычислительный центр, идеаль-
хические расстройства, как правило, ГК-зави-
но расположенный в мозге для обнаружения
симы, являясь результатом хронического стрес-
сигналов и контекстов, связанных с прошлым,
са или боли с последующим (нейро)воспале-
текущим и прогнозируемым опытом стресса,
нием; все эти состояния ассоциированы с нару-
а также для контроля реакции на стресс на
шением нейрогенеза и когнитивным дефици-
когнитивном, аффективном, поведенческом
том. Восприимчивость к стрессу и возможность
и физиологическом уровнях. Нейрогенез во
адаптироваться к новым условиям с помощью
врослом гиппокампе, по-видимому, способ-
механизмов устойчивости имеет прямое отно-
ствует контекстуальной дискриминации и
шение к особенностям нейрогенеза взрослого
когнитивной гибкости, снижая упреждение и
гиппокампа и регуляции его ГК [34].
обобщение переживаний стресса до безопас-
Скорость клеточного цикла и добавления
ного уровня. Таким образом, нижележащие
новых нейронов к существующим нейронным
области мозга получают более точную и кон-
цепям гиппокампа, несомненно, уменьшаются
текстуальную информацию, что позволяет бо-
с возрастом. Тем не менее нейральные стволо-
лее точно реагировать на стресс в конкретных
вые клетки/клетки-предшественники, кото-
контекстах [30]. Тем не менее конкретная роль
рые сохраняются в гиппокампе стареющего
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
699
мозга, могут активироваться и продуцировать
системы, включая различные типы клеток в
значительное количество новых функциональ-
нейрогенной нише [38].
ных нейронов, которые демонстрируют по-
вышенную выживаемость и интеграцию при
оптимальном наборе условий [35]. В зубчатой
ГЛУТАМАТЕРГИЧЕСКАЯ ТРАНСМИССИЯ
извилине новорождённые нейроны сосуще-
И ГИПЕРГЛУТАМАТЕРГИЧЕСКИЕ
ствуют с возникшими в процессе развития
СОСТОЯНИЯ ЗАВИСЯТ
зрелыми гранулярными нейронами, и связь
ОТ ГЛЮКОКОРТИКОИДОВ
между этими двумя типами клеток регулируют
как кооперативные, так и конкурентные про-
Хранение и обработка информации на си-
цессы. Можно предположить, что новые ней-
наптическом уровне обеспечивается способ-
роны в стареющем гиппокампе обладают за-
ностью синапсов постоянно изменять свою
метным потенциалом оптимизации процессов
эффективность. Считается, что это явление,
на уровне нейронных цепей и поведения, что
ключевое событие синаптической пластично-
делает нейрогенез потенциальной мишенью
сти, лежит в основе множественных форм дол-
для терапии. Как гиппокамп, так и основная
говременной памяти у млекопитающих. Имен-
область, иннервирующая эту структуру, энто-
но возбуждающие глутаматергические синапсы
ринальная кора, демонстрируют выраженную
играют решающую роль в синаптической пере-
атрофию у пациентов с БА, наиболее распро-
даче, синаптической пластичности и поведен-
страненной формой деменции у пожилых лю-
ческой адаптации. Почти три десятилетия на-
дей [25, 36]. Важно, что наряду с ГК, киназа
зад было сделано предположение о том, что ГК
гликогенсинтазы GSK-3β и гиперфосфорили-
и половые стероиды регулируют нейрохимиче-
рованный тау-белок, две основных молекулы,
скую и структурную пластичность гиппокампа
значимые для патогенеза БА, являются мощ-
посредством клеточных механизмов, опосре-
ными негативными регуляторами нейрогенеза
дованных N-метил-D-аспартатными глутамат-
взрослого гиппокампа [37].
ными рецепторами (NMDAR) [39], и с тех пор
При таких состояниях, как снижение па-
это было подтверждено многочисленными экс-
мяти c возрастом, нейродегенерация и психи-
периментальными результатами. Синаптиче-
ческие заболевания, зрелые нейроны погибают
ская пластичность гиппокампа, зависящая от
или становятся дефектными, поэтому стимуля-
глутаматных рецепторов, как считают многие
ция нейрогенеза у взрослых может обеспечить
ученые, является основой процессов обучения
терапевтическую стратегию для преодоления
и поведенческой адаптации. Глутамат известен
этих состояний. Обучающие задачи, зависи-
как основной возбуждающий нейромедиатор
мые от гиппокампа, обогащенная среда, физи-
в центральной нервной системе, а функцио-
ческие упражнения и зависимая от активности
нирование глутаматергической системы обес-
синаптическая пластичность мощно активи-
печивается многочисленными рецепторами,
руют пролиферацию предшественников нерв-
включающими ионотропные и метаботропные
ных клеток в гиппокампе [21]. Для объяснения
подтипы. Первый обеспечивает прохожде-
активации нейрогенеза такими воздействиями
ние катионов через постсинаптическую мем-
рассматривают механизмы усиления нейро-
брану, тогда как метаботропный подтип акти-
трофических и других влияний, которые в
вирует сигнальные каскады через вторичные
норме являются положительными регулято-
мессенджеры.
рами нейрогенеза (например, уровни BDNF).
Ионотропные рецепторы глутамата опо-
Интересно, что физические упражнения свя-
средуют синаптические и метаболические дей-
заны с повышением уровня ГК, однако отсут-
ствия глутамата. Наряду с NMDAR, к ионо-
ствие негативного эффекта этих гормонов
тропным глутаматным рецепторам относят-
на нейрогенез объясняется не чрезмерным и
ся семейства функциональных рецепторов
продолжительным, а «умеренным» и кратко-
α-амино-3-гидрокси-5-метил-4-изоксазол-
временным их выбросом, так что их концен-
пропионовой кислоты (AMPAR) и каинат-
трации остаются в стимулирующей нейрогенез
ные рецепторы. Функционирование ионо-
зоне. В одной из новых гипотез рассматрива-
тропных рецепторов в гиппокампе зависит от
ется влияние лактата, накопленного при фи-
их субъединичного состава, аминокислотной
зической нагрузке, на пластичность нейронов.
последовательности белковых доменов и кар-
Лактат, по-видимому, является одним из суще-
касных белков в синаптических мембранах.
ственных факторов, поскольку участвует в ме-
Эти рецепторы реактивно пластичны и пере-
таболизме и передаче сигналов в большинстве,
страиваются посредством регуляции субъеди-
если не во всех, клетках центральной нервной
ниц (количественно и качественно). Именно
БИОХИМИЯ том 88 вып. 5 2023
700
ГУЛЯЕВА
перестройки ионотропных рецепторов и изме-
в глутаматергическом пресинапсе и постси-
нение их субъединичного состава могут пре-
напсе. ГК быстро настраивают синаптические
вращать нейроны в «патологические» клетки,
NMDAR посредством мембранной динамики
определяя состояния пластичности или пато-
и передачи сигналов через MR и вызывают
логии гиппокампа [40]. Например, предпо-
долговременные изменения и сохранение «на-
лагается, что субъединица GluN2B может быть
строек» через механизмы, опосредованные GR.
особенно важна для пластичности и форми-
Тем самым ГК модулируют передачу глутамат-
рования памяти, и ее роль связана со взаимо-
ергических сигналов и зависимую от NMDAR
действием с кальций/кальмодулин-зависимой
синаптическую пластичность гиппокампа, спо-
протеинкиназой II [41]. Считают, что NMDAR
собствуя реализации адекватных поведенче-
обеспечивают ключевой триггер для индук-
ских реакций на факторы окружающей среды.
ции долговременной пластичности, приво-
При этом ГК специфически контролируют
дящей к изменениям экспрессии AMPAR.
динамику субъединицы GluN2B NMDAR и
AMPAR, одни из самых быстродействующих
состояния синапса, настраивая NMDAR-зави-
рецепторов нейротрансмиттеров, располо-
симую синаптическую адаптацию [47].
жены в возбуждающих синапсах, активиру-
Наряду с прямым действием на глутамат-
ются за сотни микросекунд, деактивируются
ергический синапс, регуляторное действие ГК
за миллисекунды из-за их низкого сродства к
осуществляется и на иные критические про-
глутамату, а также способны к глубокой десен-
цессы, обеспечивающие синаптическую плас-
сибилизации [42]. Третий тип ионотропных
тичность, например, нейрогенез. Известно,
рецепторов, каинатные, вносят вклад в кри-
что нейрогенез во взрослой и развивающей-
тические постсинаптические сигналы, а также
ся зубчатой извилине «ограничивается» ГК,
функционируют как пресинаптические ауто-
а также возбуждающими аминокислотами (в
рецепторы [43]. Каинатные рецепторы рассма-
первую очередь глутаматом), и в обоих случаях
триваются как гомеостатические модуляторы
механизмы задействуют NMDAR. Эти резуль-
высвобождения нейромедиаторов, способные
таты не только указывают на высокую степень
двунаправленно регулировать пластичность в
взаимозависимости между некоторыми нейро-
зависимости от «функциональной истории»
трансмиттерами и ГК, но также подчерки-
синапса [44]. Метаботропные глутаматные ре-
вают, насколько важным аспектом действия
цепторы (mGluR), группа рецепторов, связан-
стероидных гормонов является структурная
ных с G-белком, оказывают широкий спектр
пластичность [48]. Новые нейроны постоянно
модулирующих действий на возбуждающие
генерируются из резидентных пулов нервных
синапсы центральной нервной системы.
стволовых клеток и клеток-предшественников
В гиппокампе избирательная активация раз-
во взрослом гиппокампе, при этом NMDAR
личных mGluR модулирует внутреннюю воз-
участвуют в регуляции пролиферации клеток-
будимость, силу синаптической передачи и
предшественников. Агонисты и антагонисты
индуцирует множественные формы долго-
NMDAR модулируют пролиферацию как in vivo,
временной пластичности [45]. Эти рецепторы
так и in vitro, а в клетках-предшественниках ней-
критически необходимы как для устойчивых
ронов показано наличие NMDAR.
форм памяти, так и для устойчивой синапти-
Поглощение глутамата - это процесс, опо-
ческой пластичности. На основе связывания с
средованный натрий-зависимыми транспор-
G-белком и сродства к агонистам mGluR под-
терами глутамата, предотвращающий распро-
разделяются на несколько отдельных групп,
странение глутамата из синапса. Как правило,
которые выполняют разные функции в регу-
астроциты отвечают за бо льшую часть погло-
ляции гиппокамп-зависимых долговременной
щения глутамата, экспрессируя переносчики
пластичности и долговременной памяти [46].
глутамата, однако нейроны также могут экс-
Как было упомянуто выше, гиппокамп
прессировать эти переносчики, хотя и в мень-
является одной из наиболее важных мише-
ших количествах. Эти транспортеры активно
ней стероидных гормонов в мозге. Стероид-
вовлечены в реализацию наиболее изученных
ные гормоны и нейротрансмиттеры функцио-
феноменов долговременной синаптической
нируют согласованно, и эта согласованность
пластичности - длительной потенциации и
регулируется многочисленными механизма-
длительной депрессии
[49]. Недостаточный
ми. В обзоре Gulyaeva [11] приведена подроб-
обратный захват глутамата приводит к раз-
ная схема известных к настоящему времени
витию гиперактивации глутаматергической
геномных и негеномных механизмов прямой
системы, состояниям, которые в послед-
модуляции различных типов глутаматных ре-
нее время называют гиперглутаматергиче-
цепторов, осуществляемой ГК через MR и GR
скими [50], и к опосредованной глутаматной
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
701
эксайтотоксичностью гибели нейронов. Пока-
тичность. При БА β-амилоид и мутированный
зано, что кортикостерон ингибирует экспрес-
пресенилин-1 могут также ухудшать функцию
сию микроглиального транспортера глутамата
NMDAR, способствуя высвобождению Ca2+ из
GLT-1 [51], модулирует экспрессию астроци-
внутриклеточных запасов и усиливая окисли-
тарного транспортера глутамата GLT-1 [52, 53],
тельный стресс. Контроль mGluR5-зависимой
снижает активность транспортера глутамата
активации NMDAR и последующей дисфунк-
типа 3 (EAAC1 или EAAT3) [54].
ции Ca2+ при старении осуществляют адено-
Учитывая важность глутаматергической
зиновые рецепторы A2A [59]. При старении
передачи сигналов в синаптической пластично-
также наблюдаются изменения экспрессии и
сти, обучении и памяти, реализации движений,
функциональности других метаботропных глу-
считают, что именно особенности глутаматер-
таматных рецепторов, в т.ч. в синапсах мши-
гической нейротрансмиссии являются ключе-
стых волокон - СА3 гиппокампа [45].
выми для пластичности гиппокампа, а глутамат
Поскольку ГК регулируют состояние глу-
служит связующим звеном и основой баланса
таматергической системы мозга как непо-
между состояниями когнитивного здоровья и
средственно через рецепторы на глутамат-
болезни [55]. Глутаматергическая трансмиссия
ергических синапсах, так и опосредованными
в значительной степени определяет функцио-
путями [11], нарушение функционирования
нальные свойства гиппокампа в конкретных
ГГНО и ее неспособность оптимально регу-
ситуациях, обеспечивая ему соответствующее
лировать глутаматергическую синаптическую
положение в континууме «пластичность-пато-
пластичность приводят к развитию нейропси-
логия» [56]. Избыток внеклеточного глутамата
хических заболеваний, в патогенезе которых
вызывает чрезмерную стимуляцию ионотроп-
ключевую роль играют гиперглутаматергиче-
ных глутаматных рецепторов, вызывая гипер-
ские состояния. Нарушение контроля глута-
глутаматергические состояния с характерными
матергических процессов посредством ГК ле-
для них эксайтотоксичностью, окислительным
жит в основе когнитивных и эмоциональных
стрессом, структурно-функциональным повреж-
расстройств, эпилепсии и ряда других цереб-
дениям клеток мозга [50]. Эти процессы игра-
ральных патологий, являясь общим базовым
ют решающую роль при развитии различных
механизмом развития многих болезней мозга
патологий головного мозга, ассоциированных
и их коморбидностей [50]. В связи с этим ис-
с нарушениями нейропластичности, таких как
следование механизмов взаимодействия ГГНО
инсульты, эпилепсия и нейродегенеративные
и глутаматергической системы мозга имеет
заболевания [57].
приоритетное трансляционное значение.
Основной причиной возрастного сниже-
ния когнитивных функций долгое время счи-
талась потеря нейронов, но в настоящее время
ГЛЮКОКОРТИКОИДЫ И BDNF
эти изменения в большей степени связывают
СОГЛАСОВАННО РЕГУЛИРУЮТ
с постепенной синаптической дисфункцией,
ПЛАСТИЧНОСТЬ ГИППОКАМПА
вызванной кальциевым дисгомеостазом и из-
менениями в ионотропных/метаботропных ре-
Семейство небольших секретируемых бел-
цепторах. NMDAR играют центральную роль
ков, называемых нейротрофинами, включает
в механизмах, опосредующих старение синап-
мощные молекулярные медиаторы централь-
сов. Области мозга, уязвимые для старения,
ной синаптической пластичности. В част-
проявляют самые ранние патологические из-
ности, нейротрофический фактор головного
менения при БА. В гиппокампе, селективно
мозга (BDNF), а также нейротрофин 3 (NT3)
уязвимой к неблагоприятным факторам и ста-
играют ключевую роль в нейробиологических
рению области мозга, нарушение синаптиче-
механизмах, связанных с обучением и памя-
ской функции при старении ассоциировано
тью. Влияние BDNF и NT3 на синаптическую
со сдвигами Са2+-зависимой синаптической
пластичность может иметь пермиссивный ха-
пластичности, что, как полагают, способствует
рактер, устанавливая условия, при которых
раннему когнитивному дефициту, связанному
могут происходить пластические изменения,
с развитием деменции, в т.ч. альцгеймеров-
или может быть инструктивным, непосред-
ского типа [58]. Изменения внутриклеточного
ственно модифицирующим коммуникации
окислительно-восстановительного состояния
и морфологию синапсов. BDNF выделяется
сопровождаются нарушениями регуляции Ca2+,
среди всех нейротрофинов высоким уровнем
включая гипофункцию NMDAR и повышен-
экспрессии в головном мозге, в частности в
ное высвобождение Ca2+ из внутриклеточных
гиппокампе, и мощным воздействием на си-
запасов, что изменяет синаптическую плас-
напсы [60]. BDNF оказывает плейотропное
БИОХИМИЯ том 88 вып. 5 2023
702
ГУЛЯЕВА
действие на морфологию нейронов и синапти-
ские изменения дендритных шипиков, а также
ческую пластичность, которое лежит в основе
нейрогенеза взрослого гиппокампа можно на-
развития нервных цепей гиппокампа и ког-
блюдать в контексте нескольких форм обуче-
нитивной функции. BDNF способствует ста-
ния и памяти [64].
билизации и созреванию уже существующих
«Поведенческие решения», принимаемые
синапсов, а также генерации новых синапти-
мозгом во время стресса, зависят от сигналь-
ческих контактов. Поскольку BDNF модули-
ных путей ГК и BDNF, действующих синхрон-
рует как электрические свойства, так и струк-
но в мезолимбической (вознаграждение) и
турную организацию синапсов, он считается
кортиколимбической (эмоции) нейронных се-
важным биологическим маркером процессов
тях. Нарушение регуляции экспрессии BDNF
обучения и памяти [61].
и GR в осуществляющих оценку внешних фак-
Функция BDNF контролируется и дивер-
торов зонах мозга, включая гиппокамп, может
сифицируется с помощью молекулярных и кле-
поставить под угрозу интеграцию сигналов.
точных механизмов, включающих доставку и
Фосфорилирование GR при передаче сигналов
субклеточную компартментализацию раз-
BDNF в нейронах представляет собой один
личных видов мРНК BDNF, пре- и постси-
из механизмов, лежащих в основе интегра-
наптическое высвобождение BDNF, контроль
ции сигналов BDNF и ГК, который при дис-
передачи сигналов BDNF с помощью рецепто-
балансе может служить базисом для дезадап-
ров TrkB (киназы рецептора тропомиозина B)
тации к стрессу. Взаимодействие между ГК и
и превращение про-BDNF в зрелый BDNF
BDNF определяет реакцию на стресс: вызван-
и BDNF-пропептид. Разнообразные эффек-
ное стрессом ремоделирование гиппокампа,
ты BDNF на возбуждающие синапсы опреде-
префронтальной коры и миндалевидного тела
ляются активацией рецепторов TrkB и ниже-
совпадает с изменениями уровней BDNF [65].
лежащих сигнальных путей, а также противо-
Хронический стресс обычно связан со сниже-
положными в сравнении со зрелым BDNF
нием уровня BDNF, хотя эффект воздействия
функциями его незрелой формы (про-BDNF),
определяется характером и серьезностью сти-
активирующей рецепторы p75NTR. Наруше-
мула, различается в разных областях мозга и
ние этих регуляторных механизмов влияет на
изменяется со временем в период и после воз-
формирование дендритных шипиков и мор-
действия стрессора [66]. Эффекты ГК и BDNF
фологию пирамидных нейронов, а также на
на структурную и клеточную пластичность
синаптическую интеграцию [62]. Важнейшие
гиппокампа, как правило, имеют противопо-
аспекты биологии BDNF, такие как тран-
ложный характер [13, 66, 67]. Взаимодействие
скрипция, процессинг и секреция, регулиру-
между ГК и BDNF также может играть роль
ются синаптической активностью. Именно
в острых, быстрых и адаптивных реакциях на
эти наблюдения привели к мысли о том, что
стресс и является важной мишенью для пере-
BDNF может регулировать зависящие от ак-
дачи сигналов, опосредованных BDNF [68].
тивности нейронов формы синаптической
BDNF индуцирует фосфорилирование GR, что,
пластичности, такие как долговременная по-
обеспечивая скоординированные/парные дей-
тенциация (LTP), устойчивое усиление воз-
ствия BDNF и ГК, по-видимому, является не-
буждающей синаптической эффективности
обходимым звеном реакции нейропластично-
в гиппокампе, которая, как считается, лежит
сти на стресс. Таким образом, взаимодействие
в основе обучения и памяти [60]. BDNF вы-
между ГК и BDNF на фоне влияния других
свобождается из пресинаптических окончаний
молекул может способствовать пластичности
возбуждающих нейронов (вероятно, дополни-
в адаптивной реакции на стресс. Изменение
тельно также из постсинаптических оконча-
этого взаимодействия в экстремальных усло-
ний) и действует через рецептор TrkB на пре- и
виях также может быть вовлечено в неадап-
постсинаптических участках возбуждающих, в
тивные, патологические реакции на стресс,
первую очередь глутаматергических нейронов,
приводя к когнитивным нарушениям и болез-
и на тормозных нейронах [63]. BDNF счи-
ненным состояниям. Согласованность между
тают центральным регулятором пластичности
передачей сигналов TrkB и GR является опре-
нейронов во взрослом гиппокампе не только
деляющим фактором для адекватных клеточ-
потому, что он опосредует морфологические
ных ответов на стресс [60].
корреляты пластичности нейронов - изме-
Как было отмечено ранее, хроническое
нения на уровне дендритных шипиков, но по
воздействие ГК вызывает повреждение ней-
крайней мере в зубчатой извилине взрослого
ронов и атрофию дендритов, снижает нейро-
гиппокампа BDNF контролирует пластич-
генез в гиппокампе и ухудшает синаптическую
ность и на уровне нейрогенеза. Специфиче-
пластичность. Поскольку ГК также изменяют
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
703
экспрессию и передачу сигналов BDNF, ко-
тей на нескольких уровнях. ГК предотвраща-
торый способствует нейропластичности, по-
ют взаимодействие TrkB со специфическими
вышает выживаемость клеток, увеличивает
адаптерными белками, такими как Shp2, та-
нейрогенез гиппокампа и клеточную возбуди-
ким образом, нарушая активацию пути MAPK.
мость, было высказано предположение, что
Кроме того, ГК стимулируют транскрипцию
специфические побочные эффекты ГК могут
белка-ингибитора MAPK, фосфатазы MAPK-1
быть опосредованы ослаблением экспрессии
(MKP-1), который служит для прекращения
и передачи сигналов BDNF [13]. Глюкокор-
передачи сигналов MAPK. ГК также ухудшают
тикоидная регуляция BDNF осуществляется
взаимодействие TrkB и GR, тем самым ограни-
на нескольких уровнях, от глюкокортикоид-
чивая активацию фосфолипазного пути [69].
индуцированных изменений в мРНК BDNF
Роль BDNF, как трофического фактора и
до изменений в передаче сигналов, опосре-
центрального регулятора синаптической плас-
дованной TrkB. Транскрипция Bdnf может
тичности, осуществляется в рамках тесного
модулироваться ГК либо путем прямого свя-
взаимодействия BDNF с другими система-
зывания с предполагаемыми элементами глю-
ми. В первую очередь действие BDNF зави-
кокортикоидного ответа (GREs), присутству-
сит от коактивации ГК и других факторов
ющими в промоторных областях, либо путем
как детерминант окончательного клеточного
вмешательства в активность других факторов,
ответа [66]. Возбуждающий нейротрансмит-
способствующих транскрипции Bdnf, таких
тер глутамат и BDNF являются наиболее важ-
как комплекс активирующего белка-1 (AP-1)
ной «регуляторной парой» для синаптической
и транскрипционный фактор CREB (cAMP
пластичности во всей центральной нервной
response element-binding protein) [69]. В допол-
системе [70]. Cистема BDNF и глутаматерги-
нение к транскрипционной регуляции Bdnf ГК
ческая система тесно связаны и активно взаи-
также потенциально могут изменять трансля-
модействуют в формировании пластичности
цию гена Bdnf путем модуляции активности
гиппокампа. Связи между двумя системами
трансляционного механизма. Превращение
многочисленны и двунаправлены, и именно
секретированного pro-BDNF в зрелый BDNF
сложная и хорошо координируемая природа
опосредуется множеством внутриклеточных
этих связей обеспечивает оптимальную синап-
и внеклеточных протеаз, включая фуриновые
тическую и клеточную пластичность [71]. Обе
и прогормон-пропротеиновые конвертазы
системы находятся под контролем ГК, кото-
внутри клетки, а также систему плазмин-
рые и обеспечивают их координацию и согла-
тканевой активатор плазминогена (tPA) и
сованное функционирование. Обе системы
матриксные металлопротеиназы (MMP) вне
связаны с патогенезом депрессии, и наруше-
клеток. ГК могут модулировать уровни или
ние тесных и хорошо сбалансированных свя-
активность внутриклеточных и внеклеточ-
зей между ними приводит к неблагоприятным
ных протеаз и, таким образом, регулировать
изменениям нейронной пластичности, лежа-
уровни доступного зрелого BDNF. Зрелый
щим в основе депрессивных расстройств и
BDNF связывается с внутриклеточными ша-
других психических заболеваний.
перонами, которые позволяют сортировать
Все нейротрофины сначала синтезируются
BDNF по регулируемому секреторному пути
как пронейротрофины, а затем расщепляются
или конститутивному пути. Про-BDNF и зре-
внутриклеточно и внеклеточно. Все больше
лый BDNF упаковываются и доставляются
данных свидетельствует о том, что пронейро-
либо в дендриты, либо в аксоны. BDNF вы-
трофины и зрелые нейротрофины играют про-
свобождается в ответ на активность нейронов
тивоположную роль в центральной нервной
и постсинаптически взаимодействует со своим
системе. Это представление касается участия
рецептором TrkB или низкоаффинным рецеп-
фактора роста нервов (NGF), BDNF, нейро-
тором p75NTR для активации различных сиг-
трофинов 3 и 4 (NT3, NT4) и их соответствую-
нальных каскадов. Связываясь с TrkB, BDNF
щих форм в клеточных процессах, связанных с
активирует пути митоген-активируемой про-
обучением и памятью. Среди механизмов «со-
теинкиназы (MAPK), фосфолипазы C (PLC) и
зревания» BDNF раскрыт полностью конкрет-
фосфатидилинозитол-3-киназы (PI3-киназа).
ный посттрансляционный механизм, а именно
Активация этих сигнальных путей осущест-
превращение предшественника BDNF в зре-
вляет функциональную модуляцию нижележа-
лый BDNF путем протеолитического расщеп-
щих молекул-мишеней, участвующих в синап-
ления [72]. В дополнение к активно изучаемой
тической пластичности, выживании нейронов
роли BDNF оказалось, что специфические
и клеточной возбудимости. ГК потенциально
биологические роли в синаптической пластич-
модулируют активность этих сигнальных пу-
ности играют также эндогенно секретируемые
БИОХИМИЯ том 88 вып. 5 2023
704
ГУЛЯЕВА
нервными клетками белок-предшественник
так и мишени передачи сигналов ГК/стресса
BDNF и продомен BDNF, названный пропеп-
в мозге [77]. Одной из гипотез, объясняющих
тидом BDNF [73]. Первоначально считалось,
возникновение и тяжесть психических и нев-
что пронейротрофины являются простыми
рологических расстройств, является потеря
неактивными предшественниками, ответствен-
трофической поддержки [13]. Действительно,
ными только за обеспечение фолдинга зрелого
изменения уровней и активности BDNF про-
домена и за регуляцию секреторного пути ней-
исходят при многочисленных нейродегене-
ротрофинов. Однако оказалось, что пронейро-
ративных и психоневрологических заболе-
трофины являются биологически активными
ваниях. Дефицит способствует уязвимости,
благодаря передаче сигналов через специфи-
тогда как усиление функции системы BDNF
ческие рецепторы, в первую очередь р75NTR.
способствует восстановлению за счет повы-
Недавние исследования показывают, что про-
шения выживаемости, образования синапсов
нейротрофины могут секретироваться во вне-
и синаптической пластичности. Нормальный
клеточное пространство, связываться с высо-
уровень ГК поддерживает нормальную функ-
ким сродством со специфическими рецептор-
цию мозга, избыточная секреция ГК ускоряет
ными комплексами и индуцировать активацию
развитие аффективных расстройств, связан-
апоптотического механизма с последующей ги-
ных со стрессом. Другая логика, приводящая к
белью клеток различных популяций нейронов.
тем же выводам, основана на том, что синер-
В дополнение к очевидным патологическим
гические взаимодействия между активностью
ситуациям внеклеточные пронейротрофины
нейронов и синаптической пластичностью,
также играют ключевую роль во многих других
опосредованной BDNF, делают его идеальным
клеточных механизмах в нервной системе [74].
и важным регулятором клеточных процессов,
Показано, что пронейротрофины опосредуют
лежащих в основе познания и других сложных
синаптическую пластичность, а именно долго-
форм поведения, а дефицит передачи сигналов
временную депрессию в нейронах гиппокам-
BDNF способствует патогенезу ряда заболе-
па, и важны для развития аксонов. Превраще-
ваний мозга, таких как болезнь Гентингтона,
ние пронейротрофинов в соответствующую
БА и депрессия [78].
зрелую форму контролируется действием не-
Представление о том, что нарушение пе-
скольких ферментов (протеиназ) и регулято-
редачи сигналов BDNF может быть связано с
ров. Сбой в этой регуляции в настоящее время
аффективными расстройствами, возникло в
считается одним из возможных механизмов,
первую очередь из данных о противополож-
ответственных за патологическую гибель кле-
ных эффектах антидепрессантов и стресса на
ток, зависимую от пронейротрофинов. По со-
опосредованную BDNF сигнализацию. Анти-
временным представлениям, различают нейро-
депрессанты усиливают передачу сигналов
биологические действия трех различных под-
BDNF и синаптическую пластичность, а не-
типов BDNF, описанных выше, и сформули-
гативные факторы окружающей среды, та-
рована мультилигандная модель передачи сиг-
кие как тяжелый стресс, подавляют передачу
налов факторов роста [75]. Эффекты BDNF
сигналов BDNF, нарушают синаптическую
на синаптический протеом реализуются либо
активность и снижают устойчивость к аффек-
путем воздействия на механизм синтеза белка,
тивным расстройствам [79]. Исследования на
либо путем регуляции деградации белка каль-
людях с полиморфизмом одного нуклеотида
паинами и, возможно, убиквитин-протеасом-
в гене, кодирующем BDNF, BDNF Val66Met,
ной системой. Этот точно настроенный кон-
наличие которого влияет на регулируемое вы-
троль синаптического протеома, а не просто
свобождение BDNF, показали глубокий де-
активация синтеза белка, может играть ключе-
фицит пластичности гиппокампа и префрон-
вую роль в опосредованной BDNF синаптиче-
тальной коры, а также когнитивной функции
ской потенциации [76].
у носителей этой мутации. BDNF регулирует
Стресс, который, возможно, остается фак-
синаптические механизмы, ответственные за
тором риска «наименьшего общего знамена-
различные когнитивные процессы, включая
теля» для ряда психических и неврологиче-
ослабление аверсивных воспоминаний, что
ских заболеваний, влияет на систему BDNF в
является ключевым процессом в регуляции
областях и цепях мозга, селективно уязвимых
аффективного поведения. Поэтому уникаль-
к действию внешних факторов. Это представ-
ная роль BDNF в когнитивных функциях и
ление основано как на экспериментальных,
аффективном поведении предполагает, что
так и на клинических данных. Отмечается,
когнитивный дефицит из-за измененной пе-
что BDNF играет до сих пор недооценен-
редачи сигналов BDNF может лежать в осно-
ную многофакторную роль как регулятора,
ве аффективных расстройств. Хронический
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
705
стресс и депрессия связаны с атрофией ней-
пуляцию, но в настояшее время показано,
ронов и уменьшением синаптических свя-
что во взрослом гиппокампе астроциты очень
зей в областях мозга, таких как гиппокамп
гетерогенны и могут по-разному реагировать
и префронтальная кора, и это способствует
на изменения активности нейронов в зави-
депрессивному поведению, а лечение анти-
симости от субрегиона гиппокампа, активно
депрессантами может обратить этот дефицит.
модулируя синаптическую пластичность [83].
Воздействие стресса и депрессии снижает экс-
Изменения локальной активности нейронов
прессию BDNF в этих областях мозга, а лече-
регулируют взаимодействия между астроцита-
ние антидепрессантами может активировать
ми и синапсами либо путем модуляции секре-
BDNF в мозге взрослого человека и нивели-
ции глиотрансмиттеров и синаптогенных бел-
ровать последствия стресса. Новые данные
ков, либо через сигнальные пути, запускаемые
о механизмах действия быстродействующих
прямыми межклеточными контактами
[84].
антидепрессантов, в частности антагониста
Такие специфические реакции, индуцирован-
NMDAR кетамина, показали, что наблюдае-
ные в астроцитах, опосредуют взаимодействия
мые быстрые синаптические и антидепрес-
между астроцитами и нейронами, тем самым
сивные поведенческие эффекты кетамина
формируя синаптическую коммуникацию во
ассоциированы с зависимым от активности
взрослом гиппокампе. Нарушение регуляции
нейронов высвобождением BDNF [80].
этих взаимодействий и передачи сигналов мо-
BDNF действует как паракринный и ауто-
жет вызывать дисфункцию нейронных сетей
кринный фактор на участках-мишенях, как
гиппокампа при патологических состояниях,
пресинаптических, так и постсинаптических.
приводя к когнитивным нарушениям и нейро-
Это имеет решающее значение для преобразо-
дегенерации. Показано, что в мозге пациен-
вания синаптической активности в долговре-
тов с БА и у трансгенных мышей, моделей БА,
менные синаптические изменения, ассоции-
происходит индукция реактивных астроцитов,
рованные с воспоминаниями. BDNF влияет на
у которых нарушена регуляция передачи сиг-
дендритные шипики и, по крайней мере в гип-
налов, потенциально связанных с обучением
покампе, на нейрогенез, а именно изменения
и памятью [85].
скорости нейрогенеза и плотности шипиков
Наряду с нейронами, астроциты являют-
могут влиять на некоторые формы обучения и
ся стресс-реактивными клетками, а наличие
памяти, с одной стороны, или способствовать
астроцитарных GR обусловливает прямую
депрессивному поведению - с другой. С уче-
регуляцию посредством ГК этих глиальных
том этого не удивительно, что BDNF, одна из
клеток, в т.ч. в стрессорных ситуациях. «Дет-
ключевых молекул, модулирующих пластич-
ский стресс» (неблагоприятные переживания
ность мозга и влияющих на когнитивный де-
в детстве, один из наиболее значимых факто-
фицит, ассоциирован со старением и нейро-
ров риска развития расстройств настроения и
дегенеративными заболеваниями. Снижение
тревожных расстройств в более позднем воз-
когнитивных функций с возрастом является
расте) в настоящее время является одной из
основным фактором ряда заболеваний мозга,
наиболее часто используемых и трансляцион-
и изменения генерации и секреции BDNF, а
но валидных ГК-зависимых моделей стресса
также передачи сигналов BDNF/TrkB обна-
у грызунов. Особенно в лимбической системе
ружены при различных нейродегенеративных
стресс в раннем возрасте вызывает длитель-
заболеваниях, в том числе при БА и болезни
ные изменения в нейронных сетях, системах
Паркинсона, а также при расстройствах на-
нейротрансмиттеров, нейронной архитекто-
строения, таких как депрессия, расстройства
нике и пластичности, и эти изменения в даль-
пищевого поведения и шизофрения [81, 82].
нейшем существенно влияют на обработку
эмоциональной и когнитивной информации.
Показано, что функции астроцитов, наряду с
ГЛИАЛЬНЫЕ МЕХАНИЗМЫ
нейронами, также практичеcки пожизненно
ПЛАСТИЧНОСТИ ГИППОКАМПА:
изменяются после стресса в раннем возра-
АСТРОЦИТЫ, МИКРОГЛИЯ,
сте [86]. Являясь компонентом трехсторон-
НЕЙРОВОСПАЛЕНИЕ
него синапса, астроциты взаимодействуют с
нейронами несколькими способами, влияя на
Астроциты, наиболее распространенные
поглощение и метаболизм нейротрансмитте-
в головном мозге глиальные клетки, играют
ров, секретируя глиотрансмиттеры и обеспе-
ключевую роль в регуляции синаптической
чивая энергией нейроны в локальных сетях.
пластичности гиппокампа. Ранее астроциты
Таким образом, астроциты осуществляют мо-
описывали как гомогенную клеточную по-
дуляцию пластичности нейронов, опосредуя
2
БИОХИМИЯ том 88 вып. 5 2023
706
ГУЛЯЕВА
долгосрочные эффекты стресса в раннем воз-
окружающих условий микроглия по-разному
расте, запускаемые ГК.
модулирует состояние гиппокампа и влияет на
Как уже упоминалось, нейрогенез во взрос-
память [90]. Как было упомянуто выше, новые
лом гиппокампе является одной из самых
нейроны постоянно генерируются из ство-
ярких форм пластичности, и появляется все
ловых клеток и интегрируются во взрослый
больше доказательств того, что этот процесс
гиппокамп, внося свой вклад в высший уро-
ассоциирован как с механизмами памяти, так
вень нейропластичности, - функцию памяти.
и с развитием когнитивных и депрессивных
Получены данные, которые свидетельствуют о
расстройств. Астроциты являются частью ней-
модулирующем участии микроглии как в обра-
рогенной ниши, которая обеспечивает струк-
зовании новых нейронов, так и в механизмах,
турный и молекулярный каркас для пролифе-
управляющих их включением в цепи нейро-
рации стволовых клеток и дифференцировки,
нов, связанных с реализацией памяти [90].
и функциональной интеграции новых ней-
Микроглия гиппокампа взаимодействует с
ронов [87]. Астроциты вносят существенный
локальными факторами, например, BDNF, и
вклад в контроль нейрогенеза, а изменения
внешними стимулами, которые способствуют
в функции астроцитов могут нарушать регу-
нейрогенезу. Микроглия взаимодействует с се-
ляцию нейрогенеза у взрослых и способство-
ротонином, нейротрансмиттером, решающим
вать развитию когнитивных нарушений, в т.ч.
образом участвующим в нейрогенезе у взрос-
в контексте БА и расстройств эмоциональ-
лых и известным своей ролью в антидепрес-
ной сферы.
сивном действии [91].
Центральная нервная система ранее счи-
Стрессорные события вызывают, среди
талась иммунно-привилегированным участ-
прочего, быстрое повышение уровня адрена-
ком организма с отсутствием ответов иммун-
лина в мозге и более медленное повышение ГК.
ных клеток, но эта точка зрения к настоящему
Микроглия, ключевой регулятор функции ней-
времени полностью пересмотрена. Микроглия
ронов, содержит рецепторы адреналина и ГК,
представляет собой резидентные тканевые
и поэтому потенциально может быть вовлечена
макрофаги, врожденные иммунные клетки
в модуляцию воздействия стресса на функции
головного мозга, ответственные за поддержку
нейронов, обучение и память [92]. Поскольку в
функционирования нейронов и иммунную за-
зрелом мозге микроглия влияет на синаптиче-
щиту паренхимы головного мозга. Это первич-
скую передачу сигналов, обеспечивает трофи-
ные иммунные эффекторные клетки в ЦНС,
ческую поддержку и участвует в синаптической
которые регулируют широкое взаимодействие
пластичности, эти клетки являются, наряду
между нервной и иммунной системами в ответ
с нейронами, участниками реализации регу-
на различные иммунологические, физиологи-
ляторных эффектов ГК на различные формы
ческие и психологические стрессоры. Поэтому
пластичности мозга.
микроглия способствует нормальной функ-
Гиперактивность ГГНО при хроническом
ции мозга, но и вовлечена в различные цереб-
стрессе и ряде психоневрологических забо-
ральные патологии [88]. Микроглия обладает
леваний вызвана уменьшенным ингибирова-
высокой пластичностью и играет неотъемле-
нием ГК по обратной связи вследствие сни-
мую роль в формировании структуры мозга,
жения передачи сигнала ГГНО и повышенной
совершенствовании нейронных цепей и си-
секреции CRH из гипоталамического пара-
напсов, активно способствуя пластичности
вентрикулярного ядра и внегипоталамических
нейронов в здоровом мозге. Недавние иссле-
нейронов. Во время ингибирования систем-
дования выявили различные характеристики
ной обратной связи, вызванного хроническим
микроглии, специфичные для определенных
стрессом, происходит повышение уровня ци-
областей мозга, и показали, что созревание и
токинов, секретируемых как иммунными, так
функция отдельных нейронных цепей могут
и неиммунными клетками, при этом уровни
быть потенциально связаны с молекулярной
цитозольных GR в гиппокампе и префронталь-
идентичностью микроглии в разных структу-
ной коре изменяются. Продолжительные реак-
рах мозга [89]. Микроглия может играть роль
ции на стресс и избыток цитокинов нарушают
в физиологических и патологических состоя-
пластичность нейронов, а воспалительные ре-
ниях, регулируя рост аксонов и дендритов,
акции в мозге способствуют повреждению кле-
содействуя образованию, устранению и пере-
ток [93]. Стресс, особенно хронический, вызы-
мещению синапсов, модулируя функциони-
вает увеличение количества микроглии, а так-
рование возбуждающих синапсов, участвуя
же сдвиг в сторону провоспалительного фено-
в функциональной синаптической пластич-
типа. В результате значимых стрессорных воз-
ности. В конечном итоге в зависимости от
действий нарушается взаимодействие микро-
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
707
глии с нейронами и передача глутаматного
нов гиппокампа. Избыток ГК и связанные с
сигнала; иммунные реакции микроглии после
ним изменения экспрессии генов нейротро-
стресса изменяют метаболизм триптофана,
фических факторов, а также нейроактивных
активируя кинурениновый путь, в ходе кото-
веществ, секретируемых микробиотой кишеч-
рого образуются метаболиты, нарушающие
ника, влияют на морфологию и фенотип мик-
глутаматную передачу (кинуреновая кисло-
роглии [96]. Нейропсихические расстройства
та - эндогенный антагонист NMDAR). Все эти
(например, расстройства настроения и шизо-
эффекты могут лежать в основе нарушений па-
френия) и воспаление тесно переплетены и,
мяти и синаптической пластичности, вызван-
возможно, усиливают друг друга; например,
ных сильным или длительным стрессом разной
депрессия способствует воспалительным ре-
природы. Например, психологический стресс
акциям, а воспаление способствует депрес-
может нарушать функцию микроглии, что
сии и другим нервно-психическим расстрой-
вносит вклад в нарушение пластичности ней-
ствам. У пациентов с нервно-психическими
ронов и развитие изменений эмоционального
расстройствами обнаруживаются все основ-
поведения. Вызванная стрессом дисфункция
ные признаки воспаления, в том числе повы-
микроглии может лежать в основе дефицита
шенный уровень циркулирующих индукторов
нейропластичности, связанного со многими
воспаления, активированные мишени и ме-
психическими заболеваниями [88].
диаторы воспаления, воздействующие на все
Активация микроглии является отличи-
ткани. Воспаление может способствовать па-
тельной чертой практически всех известных
тофизиологии и клиническому прогрессиро-
патологий головного мозга. Хроническая ак-
ванию этих нарушений. Следует отметить, что
тивация микроглии может, в свою очередь,
избыток провоспалительных цитокинов нега-
вызывать повреждение нейронов за счет вы-
тивно модулирует эмоциональное поведение
свобождения потенциально цитотоксических
и познание, снижая уровень моноаминов в
молекул, таких как провоспалительные цито-
мозге, активируя нейроэндокринные реакции,
кины, кислородные радикалы, протеиназы
способствуя эксайтотоксичности и нарушая
и белки комплемента [94]. Острая воспали-
пластичность мозга. При этом изменения ре-
тельная реакция микроглии на травму, стресс
гуляции ГГНО выступают как важный триггер
или инфекцию включает высвобождение цито-
нейровоспаления [97].
кинов и фагоцитоз поврежденных клеток. На-
Считается, что воспаление в центральной
капливающиеся данные указывают на хрониче-
нервной системе играет ключевую роль и в про-
ское воспаление, опосредованное микроглией,
цессах, ведущих к гибели нейронов при ряде
практически при всех заболеваниях централь-
нейродегенеративных заболеваний, включая
ной нервной системы, ассоциированных с
болезнь Паркинсона, БА, прионные заболе-
эмоциональной и когнитивной сферами, и
вания, рассеянный склероз и ВИЧ-деменцию.
его связь с прогрессированием заболеваний.
Повторяющееся воздействие стресса, опосре-
Гиппокамп особенно уязвим для нейровос-
дованное избыточной секрецией ГК и наруше-
паления, хотя хемокины и цитокины активно
нием контроля ГГНО, повышает риск разви-
участвуют в нормальном нейрогенезе, клеточ-
тия нейродегенеративных заболеваний, вклю-
ной пластичности, обучении и памяти. Нейро-
чая спорадическую БА. Показано, что микро-
иммунные взаимодействия и иммунные сиг-
глия причинно связана с накоплением β-ами-
нальные молекулы, особенно хемокины, могут
лоида, гиперфосфорилированием тау-белка,
быть основным механизмом, объединяющим
нейродегенерацией и потерей синапсов при БА,
пластичность и уязвимость гиппокампа и пе-
хотя и играет позитивную роль, особенно в
реключающим эти состояния под действием
элиминации избытка β-амилоидных пептидов
внешних и внутренних факторов [95].
фагоцитами. Участие измененной в резуль-
Микроглия осуществляет регуляцию ней-
тате хронического стресса микроглии ассо-
роиммунных путей, влияющих на нейроплас-
циировано, в частности, с появлением новых
тичность и потенциально ведущих к депрес-
фенотипов микроглии, предположительно,
сивным расстройствам, патогенез которых
связанных нейропротекцией при БА
[98].
прямо связан с избыточной секрецией ГК и
БА рассматривается как вариант патологиче-
нарушенной регуляцией ГГНО. Было пред-
ского старения, но микроглия является клю-
ложено несколько гипотез о роли микроглии
чевым клеточным элементом и в механизмах
в возникновении депрессии, но все они так
нормального старения. Пожилые люди часто
или иначе включают ключевые молекулярные
испытывают снижение когнитивных функций
пути, опосредующие нейровоспаление, свя-
после стрессорных событий, которые вызыва-
занное с микроглией, и дегенерацию нейро-
ют активацию иммунной системы (например,
БИОХИМИЯ том 88 вып. 5 2023
2*
708
ГУЛЯЕВА
инфекции или травмы). Это происходит от-
ханизмов, участвующих в регуляции уровней
части потому, что старение повышает чув-
внутриклеточных и внеклеточных белков в
ствительность реакции микроглии к иммун-
разных клеточных и неклеточных компартмен-
ным сигналам. В стареющем мозге микроглия
тах [100]. Расщепление внеклеточных белков
реагирует на эти сигналы, производя больше
связано с изменениями постсинаптических
цитокинов и в течение более долгого перио-
внутриклеточных механизмов, а дополнитель-
да. Хотя присутствие микроглии необходимо
ные изменения в этом компартменте являются
для реализации памяти, сверхактивированная
результатом опосредованного протеазами рас-
иммунными сигналами микроглия избыточно
щепления внутриклеточных белков. Оба меха-
вырабатывает воспалительные цитокины, что
низма способствуют инициации сигнальных
неблагоприятно для функции памяти в связи с
каскадов, которые управляют нисходящими
мощным негативным воздействием цитокинов
путями, связанными с синаптической плас-
на синаптическую пластичность гиппокампа.
тичностью. В обзоре Salazar et al. [100] обоб-
BNDF помогает защитить нейроны от повреж-
щены данные о роли в синаптической плас-
дения, вызванного инфекцией или травмой,
тичности внеклеточных и внутриклеточных
и играет критическую роль в тех же процессах
протеаз с различной специфичностью, лока-
памяти и пластичности гиппокампа, которые
лизации и регуляции этих ферментов. Комби-
изменены нарушением регуляции продукции
нированные действия протеаз и механизмов
интерлейкинов микроглией [99]. Избыточная
трансляции обеспечивают жесткий контроль
воспалительная реакция мозга, возникающая
синаптического протеома, важного для долго-
при старении под действием вторичного им-
временной пластичности. Тем не менее можно
мунного вызова, может ослабить способность
признать, что роль протеаз в нейропластич-
обеспечивать BDNF, необходимый для про-
ности недооценена в связи с недостаточным
цессов пластичности, связанных с памятью, в
числом исследованиий.
синапсах гиппокампа. Нарушения ГГНО при
Регулируемый внеклеточный протеолиз иг-
старении, наиболее вероятно, являются клю-
рает ключевую роль в структурном и функцио-
чевой причиной многоступенчатого каскада,
нальном ремоделировании синапсов во время
который ассоциирован с изменением реак-
развития мозга, обучения и формирования
тивности микроглии на действие стрессорных
памяти. Синапсы мшистых волокон на пира-
факторов.
мидных клетках СА3 гиппокампа демонстри-
руют несколько уникальных функциональ-
ных особенностей, включая кратковременную
ГЛЮКОКОРТИКОИДЫ УЧАСТВУЮТ
фасилитацию, пресинаптические механизмы
В ЗАВИСИМОЙ ОТ ПРОТЕАЗ
долговременной потенциации, а также незави-
ПЛАСТИЧНОСТИ ГИППОКАМПА
симую от активации NMDAR и NMDA-зави-
симую метапластичность. Функциональная и
Поскольку все пластические перестройки
структурная пластичность синапсов мшистых
в мозге так или иначе связаны с модифика-
волокон опосредована внеклеточным протео-
цией структуры белковых молекул и проис-
лизом. Показано, что среди перисинаптиче-
ходящими вследствие этого изменениями их
ских протеаз решающую роль в формировании
функционирования, регуляция ферментов,
пластических изменений играют тканевый ак-
катализирующих посттрансляционные моди-
тиватор плазминогена (tPA)/система плазмина,
фикации белков, несомненно, важна для реа-
расщепляющий белок-предшественник ами-
лизации феноменов нейропластичности. Так,
лоида (APP), фермент β-секретаза 1 (BACE1)
обучение и память требуют изменения числа
и металлопротеиназы [101]. Хотя общепри-
и силы существующих синаптических свя-
знано, что именно синаптическая пластич-
зей, и внеклеточный протеолиз в синапсах
ность возбуждающих синапсов гиппокампа
играет ключевую роль в синаптической плас-
играет решающую роль в формировании
тичности, определяя структуру, функцию и
следов памяти, некоторые компоненты ней-
число синапсов. Ранняя фаза хорошо изучен-
ропластичности связаны с несинаптически-
ных феноменов синаптической пластичности,
ми изменениями. Активность внеклеточных
долговременной синаптической потенциации
протеаз может влиять на обработку инфор-
и депрессии, зависит от посттрансляционных
мации в нейронных сетях, воздействуя на
модификаций синаптических белков. Име-
мишени за пределами синапсов. Интересно,
ются многочисленные доказательства роли
что внеклеточный протеолиз может изменять
различных типов протеаз в синаптической
внутреннюю возбудимость нейронов и баланс
пластичности, что отражает разнообразие ме-
возбуждения/торможения как кратковременно
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
709
(от минут до часов), так и в долгосрочной
ческой пластичности и соответствующих типов
перспективе. Более того, оказалось, что пу-
обучения и памяти, в то время как активация
тем расщепления компонентов внеклеточ-
кальпаина-2 ограничивает степень пластич-
ного матрикса протеазы могут модулировать
ности и обучения. Кальпаин-1 оказывает ней-
функцию ионных каналов или изменять тор-
ропротекторное действие как во время пост-
можение и, следовательно, облегчать актив-
натального развития, так и у взрослых, тогда
ное участие дендритов и начальных сегментов
как кальпаин-2 стимулирует нейродегенера-
аксонов в регулировании функции нейронов.
цию [105]. К сожалению, прямых данных о
В целом, возникает картина, согласно которой
механизмах регуляции ГК «апоптотических»
как быстрый, так и длительный внеклеточный
протеаз, каспаз и кальпаинов при реализа-
протеолиз могут влиять на некоторые аспекты
ции нормальной пластичности до сих пор не-
обработки информации в нейронах, такие как
много. Показано, что в гиппокампе взрослых
инициация потенциала действия, адаптация
крыс Wistar 10-дневный иммобилизационный
частоты спайков, свойства потенциала дей-
стресс приводил к значительному снижению
ствия и обратное распространение нервного
числа нейрональных и астроглиальных кле-
импульса в дендритах [102].
ток в областях СА1 и СА3, увеличению чис-
Регуляторные эффекты ГК на активность
ла каспаза-3-позитивных клеток, повышению
важных для нейропластичности протеаз так-
уровня мРНК гена, кодирующего GR, и сни-
же недостаточно изучены, однако целый ряд
жению уровня мРНК гена, кодирующего MR
данных свидетельствует о том, что эта группа
(максимально в зубчатой извилине и обла-
ферментов находится под контролем ГК, хотя
сти СА3) [106]. В данном эксперименте появле-
конкретные механизмы не всегда детально опи-
ние активной каспазы-3 было связано, по-ви-
саны. Тем не менее ряд данных об изменениях
димому, с апоптотической гибелью клеток.
активности важных для нейропластичности
Исходя из плейотропной функции протеаз,
протеаз под действием стресса, ГК или лиган-
в основе которой лежит относительно низкая
дов рецепторов ГК указывают на роль протеаз
субстратная специфичность этих ферментов
как одного из основных факторов регуляции
и большое число потенциальных субстратов
нейропластичности под контролем ГК.
каждого из них, можно предположить, что
Прежде чем рассмотреть данные о регу-
имеется много потенциальных мишеней про-
ляции ГК протеолитической активности про-
теаз при реализации синаптической пластич-
теаз мозга при реализации феноменов нейро-
ности в гиппокампе и что эти процессы ас-
пластичности, напомним, что пагубное влия-
социированы с ГК. Например, ГК могут мо-
ние хронически повышенных уровней ГК на
дулировать уровни или активность внутри-
структуру и функцию нейронов вплоть до их
клеточных и внеклеточных протеаз и, таким
гибели многократно описано и может считать-
образом, регулировать уровни доступного
ся общим местом. Проапоптотические эффек-
зрелого BDNF [13]. Диффузный и структури-
ты ГК, приводящие к гибели нейронов, по
рованный внеклеточный матрикс составляет
определению, включают активацию апоптоти-
около 20% объема мозга и играет важную роль
ческих протеаз, в т.ч. каспаз и кальпаинов.
в развитии и пластичности взрослого мозга.
Тем не менее даже такие «разрушающие» фер-
Перинейронные сети, специализированные
менты экспрессируются в норме и расщеп-
структуры внеклеточного матрикса, окружают
ляют белки, важные для нейропластичности.
определенные типы нейронов в мозге. Стресс
Например, ранее мы показали, что в норме
влияет на диффузный матрикс, а также на
каспаза-3 необходима для поддержания плас-
перинейронные сети, причем эффекты стрес-
тичности гиппокампа, поскольку среди ее суб-
са зависят от возраста и области мозга [107].
стратов немало белков (в т.ч. цитоскелетных),
ММР являются компонентом внеклеточного
ограниченный протеолиз которых необходим
матрикса и мишенями ГК/стресса. Активность
для реализации нормальной синаптической
ММР9, желатиназы, участвующей в процес-
пластичности [103, 104]. Кальпаины представ-
сах синаптической пластичности, обучения
ляют собой семейство растворимых кальций-
и памяти, повышена как в моделях на живот-
зависимых протеаз, которые участвуют во
ных с хроническим стрессом, так и в образцах
многих регуляторных путях, а также играют
периферической крови пациентов с депрес-
существенную роль в нейропластичности.
сией. В мышиной модели депрессии/тревож-
Две изоформы кальпаина, кальпаин-1 и каль-
ности с хроническим введением кортикосте-
паин-2, выполняют противоположные функ-
рона активность MMP9 и уровни белка были
ции в головном мозге. Активация кальпаина-1
значительно повышены, а уровни субстрата
необходима для определенных форм синапти-
ММР9 нектина-3 - снижены в гиппокампе,
БИОХИМИЯ том 88 вып. 5 2023
710
ГУЛЯЕВА
в основном в областях СА1 и СА3 [108]. Ак-
зано со снижением активности нескольких
тивность MMP9 коррелировала с поведением
протеаз, деградирующих β-амилоидные пеп-
отчаяния в этой модели депрессии. Ремодели-
тиды, таких как инсулин-деградирующий фер-
рование гиппокампа при хроническом стрессе
мент и ММР9. Эти эффекты были опосредо-
сопровождается гиперэкспрессией GR, про-
ваны активацией рецепторов ГК. Таким обра-
теасом и каспазы-3. В культивируемых крыси-
зом, ГК могут усиливать накопление β-ами-
ных астроцитах добавление глюкокортикоида
лоида, уменьшать его деградацию в астроцитах
дексаметазона снижало базальные уровни
и так формировать молекулярный механизм,
MMP3 и мРНК MMP9, однако предваритель-
связывающий стрессорные факторы с развити-
ная обработка дексаметазоном уменьшала ин-
ем БА. В первичных культурах нейронов нео-
дуцированное эндотелином повышение мРНК
кортекса кортикостерон (1 мкМ) в зависимо-
ММР. Эффекты эндотелина-1 на высвобож-
сти от длительности применения ингибировал
дение белков MMP3 и MMP9 ослаблялись
продукцию BACE1 (при однократном примене-
предварительной обработкой дексаметазоном.
нии), что сопровождалось снижением уровней
Эти результаты показывают, что дексаметазон
β-амилоида 1-42, или активировал экспрессию
подавляет астроцитарные рецепторы эндоте-
BACE1 и β-амилоида 1-42 (при длительном
лина и снижает продукцию MMP, индуциро-
применении) [114]. По-видимому, таким обра-
ванную эндотелином [109]. В первичных куль-
зом ГК способны регулировать аккумуляцию
турах эндотелиальных клеток микрососудов
β-амилоидного фрагмента 1-42 при БА.
головного мозга крысы дексаметазон частично
ингибировал индуцированную цитокинами
активацию MMP9 [110], а в мышиной линии
УЧАСТИЕ ГЛЮКОКОРТИКОИДОВ
эндотелия сосудов головного мозга cEND дек-
В РЕГУЛЯЦИИ ПЛАСТИЧНОСТИ
саметазон индуцировал экспрессию ингиби-
ГИППОКАМПА МЕТАБОЛИЧЕСКИМИ
тора металлопротеиназ TIMP-1, который эф-
ГОРМОНАМИ
фективно подавляет активность ММР9 [111].
На рыбках Danio rerio также было показано,
ГК, «гормоны стресса», относятся к гор-
что экспрессия гена Mmp13 в мозге является
монам, координирующим метаболизм и энер-
мишенью для ГК [112].
гетический статус организма, они связаны с
В большинстве случаев молекулярный
метаболизмом пищевых веществ. Например,
механизм, лежащий в основе патогенеза спо-
циркадианный ритм секреции ГК регулиру-
радической БА, неизвестен. Повышенные ба-
ется временем приема пищи как у грызунов,
зальные уровни кортизола у пациентов с БА
так и у людей: уровни ГК повышаются перед
позволяют предположить, что ГК могут спо-
употреблением пищи, а манипуляции с режи-
собствовать развитию и/или поддержанию за-
мом приема пищи изменяют характер секре-
болевания. Амилоидные бляшки являются от-
ции ГК [115]. При этом низкие запасы энергии
личительной чертой БА, и считается, что они
быстро стимулируют секрецию ACTH и ГК в
играют роль на ранних стадиях БА. Однако
ситуациях отрицательного энергетического ба-
мало известно о том, как их образование ре-
ланса. Пациенты с избытком ГК либо эндо-
гулируется стрессом и ГК. В работе Wang
генного (синдром Кушинга), либо экзогенного
et al. [113] показано, что ГК стимулируют об-
(лечение кортикостероидами) происхождения
разование астроцитарного β-амилоидного
характеризуются повышением аппетита и на-
пептида за счет увеличения экспрессии APP
коплением жира, а пациенты с дефицитом ГК
и APP-расщепляющего фермента BACE1, а
(болезнь Аддисона) - снижением аппетита и
также снижение экспрессии β-амилоид-дегра-
потерей веса, при этом сходные закономер-
дирующих протеаз. Накопление астроцитов
ности получены и на животных [115]. Дей-
является одним из самых ранних изменений
ствительно, система, регулирующая реакции
при БА. Показано, что ГК повышают продук-
на стресс, ГГНО, также регулирует реакции
цию амилоида-β в первичных культурах астро-
на питание, поскольку нервные цепи, регу-
цитов за счет увеличения экспрессии гена App
лирующие потребление пищи, сходятся в па-
и β-сайта BACE1. Примечательно, что введе-
равентрикулярном ядре, которое содержит
ние ГК нормальным мышам среднего возраста
CRH- и урокортин-содержащие нейроны.
способствовало экспрессии АРР и BACE1 в
Учитывая одинаковую анатомию, системы,
астроцитах. ГК заметно снижали деградацию
которые контролируют потребление пищи и
и клиренс β-амилоида астроцитами in vitro,
реакцию на стресс, могут влиять друг на дру-
тем самым ограничивая нейропротекторные
га. Сложные механизмы такого взаимодей-
возможности астроцитов. Это могло быть свя-
ствия включают уровни ГК (в зависимости
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
711
от тяжести стрессора), взаимодействие между
лептину с возрастом функционально снижа-
ГК и связанными с питанием нейропепти-
ется, в частности, при старении уменьшается
дами, в частности нейропептидом Y, агути-
модуляторный эффект лептина в синапсах
подобным белком, меланокортинами и их
обоего типа [120].
рецепторами, CRH, урокортином и перифе-
Гиппокамп экспрессирует высокие уровни
рическими сигналами (лептином, инсулином,
как инсулиновых, так и лептиновых рецепто-
грелином) [116]. Гормоны, регулирующие пи-
ров, а также ключевых компонентов связан-
щевое поведение, регулируют и ГГНО, и кон-
ных с ними сигнальных каскадов, при этом
тролируются этой осью.
оба гормона модулируют гиппокамп-зависи-
На периферии инсулин играет критиче-
мые когнитивные функции [121]. Как лептин,
скую роль в регуляции метаболического го-
так и инсулин влияют на ключевые клеточ-
меостаза, стимулируя поглощение глюкозы
ные события в гиппокампе, лежащие в основе
периферическими органами. На протяжении
обучения и памяти, включая зависящую от
десятилетий мозг ошибочно считался нечув-
активности синаптическую пластичность и
ствительным к инсулину органом, однако в
транспорт глутаматных рецепторов в синапсы
последнее время начато исследование меха-
гиппокампа. Гиппокамп селективно чувстви-
низмов, с помощью которых инсулин способ-
телен к нейродегенеративным процессам, в
ствует критически важным функциям мозга,
частности при БА, при которой функции леп-
таким как метаболизм, познание и мотивиро-
тина и инсулина нарушены. Таким образом,
ванное поведение. Нет сомнений в существо-
способность метаболических гормонов, леп-
вании опосредованной инсулином синаптиче-
тина и инсулина, регулировать синаптическую
ской пластичности в мозге как в норме, так и
функцию гиппокампа имеет важное значение
при патологиях [117]. В центральной нервной
для нормальной функции мозга, а также для
системе инсулин играет решающую роль в
развития заболеваний мозга. Резистентность
формировании нейронных цепей и синапти-
мозга к инсулину может быть ключевым фак-
ческих связей и способствует нейропластич-
тором, вызывающим когнитивные нарушения,
ности взрослого мозга. Снижение активности
наблюдаемые при метаболических и нейроде-
рецепторов инсулина и передачи его сигналов
генеративных заболеваниях. Можно считать
в мозге (т.е. резистентность к инсулину), как
установленной критическую роль резистент-
показывают клинические и доклинические
ности мозга к инсулину в коморбидностях
исследования, вызывает дефицит нейроплас-
между метаболическими и нейродегенератив-
тичности, приводя к снижению когнитивной
ными заболеваниями. Сахарный диабет типа 2
функции и увеличению риска нервно-психи-
является фактором риска развития когнитив-
ческих расстройств (в частности, это наблю-
ного дефицита и БА (у людей с диабетом риск
дается при ожирении и сахарном диабете
развития деменции в 2,5 раза выше). При этом
типа 2) [118]. Резистентность мозга к инсули-
влияние на нейрогенез рассматривается как
ну непосредственно связана с пластичностью
одна из важных мишеней патогенного дей-
гиппокампа, поскольку трансдукция сигналов
ствия инсулинорезистентности [122].
инсулина влияет на молекулярные каскады
Общие нейробиологические пути, харак-
в гиппокампе, лежащие в основе пластично-
терные для диабета типа 2 и депрессивных
сти, обучения и памяти, а также модулирует
симптомов, в настоящее время широко об-
нейрогенез в субгранулярной нейрогенной
суждаются с учетом полученных в последнее
нише [119]. В настоящее время также стало
время морфологических и нейрокогнитивных
очевидным, что метаболический гормон леп-
данных. Клинические исследования показа-
тин выполняет в мозге множество функций,
ли частое сосуществование депрессии и диа-
выходящих за рамки его установленной роли
бета; оба заболевания связаны со сходными
в гипоталамическом контроле энергетиче-
изменениями в мозге и поведении. Некоторые
ского баланса. Гиппокамп содержит области с
морфологические и функциональные изме-
высокой плотностью лептиновых рецепторов,
нения, возникающие при этих заболеваниях,
которые, в частности, локализованы в синап-
по-видимому, являются результатом действия
сах поля CA1. Лептин оказывает прокогнитив-
избытка провоспалительных цитокинов или
ное действие, поскольку он быстро изменяет
глутамата. ГК, индуцированные стрессом, не
синаптическую эффективность в возбуждаю-
только влияют на синаптическую пластич-
щих коллатерали Шаффера-CA1 и височно-
ность, но и нарушают метаболизм глюкозы
аммонических-CA1 синапсах, повышая эф-
в мозге и снижают чувствительность к инсу-
фективность памяти в задачах, зависящих от
лину
[123]. Сходное снижение нейроплас-
гиппокампа. Чувствительность гиппокампа к
тичности в областях мозга, чувствительных
БИОХИМИЯ том 88 вып. 5 2023
712
ГУЛЯЕВА
к стрессу, в первую очередь в гиппокампе,
на самках, а сравнительные исследования, в
может быть связано как с диабетом типа 2,
дизайн которых включены животные обоего
так и с депрессивными симптомами, при этом
пола, проводятся чрезвычайно редко. Тем не
пациенты с диабетом демонстрируют сниже-
менее в последние годы получены данные, ко-
ние нейропластичности, включая морфологи-
торые позволяют приблизиться к пониманию
ческие аномалии и последующий нейроког-
стероид-зависимых механизмов половых осо-
нитивный дефицит, подобные тем, которые
бенностей нейропластичности.
характерны для пациентов с депрессивными
Половые различия в функции гиппокампа
симптомами [124]. Функциональные нейро-
наблюдают у многих видов млекопитающих.
визуализационные исследования продемон-
Однако величина, степень и специфичность
стрировали измененный метаболизм глюкозы
этих различий неясны, поскольку они могут за-
в головном мозге пациентов с депрессией.
висеть от таких факторов, как возраст, исполь-
Изменения уровней или активности ключевых
зованная методология и факторы окружающей
метаболических ферментов и более низкая
среды [127]. Пирамидные клетки поля CA3
чувствительность рецепторов инсулина были
гиппокампа самцов и самок крыс различа-
обнаружены в мозге животных моделей обоих
ются по структуре, функциям и пластичности,
этих заболеваний. Очевидно, что избыток ГК
причем эти половые различия не удается объ-
может приводить к нарушению действия инсу-
яснить просто действием циркулирующих го-
лина и метаболизма глюкозы, к ограничению
надных гормонов [128]. К настоящему времени
энергоснабжения, необходимого для правиль-
половые различия установлены для различных
ного функционирования нейронов и, как
механизмов пластичности гиппокампа, когни-
следствие, к нарушению синаптической плас-
тивных функций, а также для ряда патологиче-
тичности [123, 125].
ских состояний, затрагивающих пластичность
гиппокампа. Например, метаанализ показы-
вает, что самцы превосходят самок в задачах,
ПЛАСТИЧНОСТЬ ГИППОКАМПА
зависящих от гиппокампа, у грызунов и людей;
ЗАВИСИТ ОТ ПОЛА:
кроме того, у женщин чаще наблюдается более
РОЛЬ СТЕРОИДНЫХ ГОРМОНОВ
выраженное снижение когнитивных функций
при БА и депрессии, причем оба заболевания
Многочисленные исследования проде-
характеризуются дисфункцией гиппокампа.
монстрировали различия между мужчинами и
Гиппокамп
- очень пластичная структура,
женщинами в структуре, функции и пластич-
важная для обработки информации высокого
ности гиппокампа. Половые различия в меха-
порядка и чувствительная к факторам окру-
низмах нейропластичности являются одной
жающей среды, таким как стресс. Структура
из важнейших, но явно недостаточно иссле-
сохраняет способность производить новые
дованных областей. Важность этой области
нейроны, и этот процесс играет важную роль в
исследований определяется не только оче-
разделении паттернов, упреждающем поведе-
видными фундаментальными вопросами, но
нии и когнитивной гибкости. Интересно, что
и тем, что практически все заболевания, свя-
у грызунов обнаружены заметные половые раз-
занные с нарушениями нейропластичности
личия в уровне нейрогенеза и активации новых
(а это все церебральные патологии, затраги-
нейронов в ответ на когнитивные задачи, зави-
вающие как когнитивную, так и эмоциональ-
сящие от гиппокампа [126].
ную сферы), специфически зависят от пола.
Ранее считалось, что половые стероидные
Существует множество данных о разной пред-
гормоны синтезируются исключительно в го-
расположенности мужчин и женщин к забо-
надах (например, эстрогены - в яичниках) и
леваниям, в которых важную роль играет гип-
вызывают транскрипционные изменения в пе-
покамп, и, очевидно, что половые различия
риод от нескольких часов до нескольких дней.
в функции гиппокампа имеют существенное
Однако эстрогены также локально синтезиру-
значение для понимания механизмов когни-
ются в нейронных цепях (нейроэстрогены),
тивных и психических нарушений в зависимо-
где они быстро (в течение нескольких минут)
сти от пола [126]. Недостаточное число и каче-
модулируют ряд поведенческих реакций, вклю-
ство экспериментальных исследований в этой
чая пространственное обучение и контакты.
области также имеет объективную причину -
Все больше экспериментальных данных сви-
очевидные удобства и простота работы с сам-
детельствует о том, что половые нейроактив-
цами мелких экспериментальных животных.
ные стероиды (нейростероиды) необходимы
В результате преобладающее число исследо-
для формирования памяти. Нейростероиды
ваний выполнено на самцах, минимальное -
оказывают глубокое влияние на функцию
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
713
и структуру нервных цепей, и локальный син-
наряду с ГК [132]. Половые стероиды (дигид-
тез этих гормонов необходим для индукции как
ротестостерон, тестостерон, эстрадиол и про-
долговременной потенциации, так и долговре-
гестерон) и ГК модулируют синапсы гиппо-
менной депрессии синаптической передачи,
кампа за счет зависимых от киназ сигнальных
а также для формирования нервных отрост-
механизмов, обеспечивая быструю негеном-
ков в различных областях нервной системы.
ную модуляцию дендритного спиногенеза. Си-
С определенной степенью упрощения можно
наптические (классические) рецепторы поло-
заключить, что в гиппокампе 17β-эстрадиол
вых стероидов также участвуют в запуске этих
(E2) необходим для индукции длительной по-
быстрых синаптических модуляций.
тенциации, а 5α-дигидротестостерон (DHT)
Исследования полового диморфизма в си-
важен для индукции длительной депрессии.
наптических процессах кодирования, лежащих
Быстрое воздействие половых нейростероидов
в основе обучения, систематически начали
на долговременную синаптическую пластич-
проводиться недавно. Исследования на самцах
ность, в т.ч. формирование памяти, требует
грызунов проводили на модели долговремен-
поддержания тонического или фазического
ной потенциации зависимого от активности
локального синтеза стероидов, контролируе-
нейронов увеличения синаптической силы.
мого нейронной активностью, но также может
Эта модель используется для идентифика-
зависеть от циркулирующих гормонов, возра-
ции синаптических рецепторов и сигнальной
ста и пола животного [129].
активности, которые координируют ремоде-
Влияние половых гормонов (эстрогенов,
лирование субсинаптического актинового ци-
андрогенов и прогестерона) и ГК опосредовано
тоскелета, решающе важного для стойкой по-
различными типами задействованных стероид-
тенциации и памяти. У самок для длительной
ных рецепторов (мембранных или ядерных) и
потенциации и памяти задействованы те же
сопровождается локальными метаболически-
механизмы, что и у самцов, но только у самок
ми преобразованиями. Половые особенности
участие рецептора TrkB и синаптических сиг-
пластичности гиппокампа описаны для раз-
нальных посредников, включая Src и ERK1/2,
ных регионов этой структуры и касаются прак-
требуют эстрогена, синтезированного в нейро-
тически всех систем, реализующих механизмы
нах, и передачи сигналов через ассоциирован-
пластичности. Например, хорошо исследованы
ный с мембраной рецептор эстрогена α (ERα).
изменения структурной пластичности гиппо-
В связи с дополнительным участием ERα у
кампа в ответ на эстрогены у самок грызу-
самок наблюдается более высокий порог для
нов [130]. В частности, представление о том,
длительной потенциации гиппокампа и про-
что эстрадиол может действовать как локаль-
странственного обучения [133]. Данные о том,
ный нейромодулятор в головном мозге, бы-
что эстроген способствует пластичности, свя-
стро влияя на синаптическую функцию, было
занной с обучением, модифицируя синапти-
подтверждено исследованиями, проведенны-
ческий цитоскелет, и острые стимулирующие
ми за последние 30 лет. Был продемонстри-
эффекты эстрогена на глутаматергическую пе-
рован синтез эстрадиола de novo в головном
редачу и долговременную потенциацию позво-
мозге, а также сигнальные механизмы, опо-
ляют объяснить значительное влияние стерои-
средующие ответы на гормон, наряду с мор-
да на поведение. Недавняя работа определила
фологическими данными, указывающими на
механизмы, лежащие в основе этих синапти-
быстрые изменения синаптического входа по-
ческих эффектов [134]. 17β-Эстрадиол запу-
сле увеличения локальных уровней эстрадио-
скает полимеризацию актина в дендритных
ла [131]. Эстрогены опосредуют и модулируют
шипиках гиппокампа посредством сигналь-
образование шипиков и синапсов, клеточные
ного каскада, начинающегося с GTPазы RhoA
и молекулярные реакции гиппокампа, а также
и заканчивающегося инактивацией белка ко-
нейрогенез. Дендритные шипики, постсинап-
филина, разрезающего филамент. Наряду с
тические структуры синапсов, необходимы
прямым действием, гормон активирует синап-
для синаптической пластичности и обучения.
тические рецепторы TrkB BDNF секретируе-
Формирование и модуляция дендритных ши-
мого нейротрофина, который стимулирует путь
пиков изменяются как быстрым (вероятно,
от RhoA до кофилина. Поэтому, возможно, что
негеномным), так и классическим (геномным)
17β-эстрадиол действует через трансактива-
действием эстрогенов, и предполагается, что
цию соседних рецепторов, модифицируя со-
эти механизмы играют роль в эффектах эстро-
став и структуру возбуждающих контактов.
генов на обучение и память. Описана быстрая
Несколько десятилетий назад было выска-
негеномная модуляция дендритных шипиков в
зано предположение, что BDNF опосредует
гиппокампе нейростероидами и андрогенами,
некоторые эффекты эстрогена в гиппокампе
БИОХИМИЯ том 88 вып. 5 2023
714
ГУЛЯЕВА
и что эти взаимодействия играют роль как
гиппокамп [137]. Предполагается, что пластич-
в нормальном мозге, так и при некоторых
ность гиппокампа регулируется с помощью
заболеваниях. Например, в синапсах мши-
нейробластов, основной клеточной единицы
стых волокон гиппокампа грызунов показано
функционального нейрогенеза во взрослом
взаимодействие между BDNF и эстрогеном:
гиппокампе, а дефекты дифференцировки, ин-
17β-эстрадиол изменяет функцию гиппокам-
теграции и выживания нейробластов, по-види-
па, влияя на экспрессию BDNF в этих синап-
мому, являются основной причиной нейро-
сах. По-видимому, эстроген влияет на гиппо-
когнитивных расстройств. Было обнаружено,
камп посредством механизмов, связанных не
что рецепторы гонадотропина и стероидоген-
только со зрелой формой BDNF, действующей
ные ферменты экспрессируются в нейроблас-
на рецепторы TrkB, но также и путем регуля-
тах гиппокампа. На основании имеющихся
ции предшественника, про-BDNF, действую-
данных пересматриваются клеточная основа
щего на рецептор p75NTR. Предполагается,
синтеза нейроэстрадиола, потенциальная связь
что взаимодействия между BDNF и 17β-эст-
между синтезом нейроэстрадиола и нейроблас-
радиолом в мшистых волокнах потенциально
тозом в гиппокампе, возможное участие абер-
важны для нормальной функции гиппокампа
рантной продукции нейроэстрадиола в мито-
и имеют значение для половых различий в
хондриальных дисфункциях и дислипидемии
функциях, зависящих от мшистых волокон, а
в менопаузе и у взрослых, патогенез нейроде-
также при заболеваниях, при которых предпо-
генеративных расстройств; все эти феномены
лагается, что пластичность мшистых волокон
обсуждаются в рамках гипотезы о функциони-
играет важную роль (БА, эпилепсии и нарко-
ровании гипоталамо-гипофизарно-гиппокам-
мании) [135]. В целом, особый порог длитель-
пальной оси во взрослом мозге. В конечном
ной потенциации у самок ассоциирован с по-
счете понимание регуляции нейрогенеза гип-
ловыми различиями в обработке информации
покампа аномальными уровнями концентрации
и особенностями их обучения и памяти.
нейроэстрадиола по принципу обратной связи
В последнее десятилетие наблюдается зна-
может дать дополнительный базис для разработ-
чительный рост исследований, изучающих роль
ки нейрорегенеративного терапевтического ле-
фундаментальных нейроиммунных процессов
чения эмоциональных расстройств, депрессии
как ключевых механизмов, которые могут обра-
и снижения когнитивных функций в менопаузе,
зовать естественный мост между нормальной
а также нейрокогнитивных расстройств [137].
физиологией и патологическими ситуациями.
К настоящему времени получены данные о
том, что стрессорные воздействия вызывают
ЗАКЛЮЧЕНИЕ.
зависящие от времени и специфические для
ТРАНСЛЯЦИОННЫЕ АСПЕКТЫ
стрессора паттерны экспрессии цитокинов/
ГЛЮКОКОРТИКОИДНОЙ РЕГУЛЯЦИИ
хемокинов в мозге, а гены, связанные с воспа-
ПЛАСТИЧНОСТИ ГИППОКАМПА
лением, демонстрируют уникальные профили
экспрессии у самок и самцов в зависимости от
Просто сделать вещи сложными,
индивидуальных, кооперативных или антаго-
но сложно сделать вещи простыми
нистических взаимодействий между рецепто-
рами стероидных гормонов (в первую очередь
3-й закон Мейера
рецепторами эстрогена и ГК) [136]. Таким
образом, нейроиммунные механизмы стресса,
Исследования на животных показали, что
в значительной степени ассоциированные с
гиппокамп является особенно чувствительной
пластичностью гиппокампа, зависят от пола, и
и уязвимой областью мозга, которая реагиру-
это имеет значение для фармакотерапии забо-
ет на стресс и гормоны стресса. Гиппокамп -
леваний, связанных со стрессом.
важная область мозга для реализации рабо-
Как показано выше, нейроэстрадиол, син-
чей и пространственной памяти у животных
тезируемый в гиппокампе, играет важную роль
и человека, а также уязвимая и пластичная
в нейропластичности независимо от циркули-
структура в отношении ее чувствительности к
рующего эстрадиола, который секретируется
эпилепсии, ишемии, черепно-мозговой трав-
из половых желез. Реакция гипоталамо-гипо-
ме, стрессу и старению. Понимание губитель-
физарных областей на синтез нейроэстрадиола
ных последствий повышенных уровней ГК на
в гиппокампе открывает перспективы для но-
функционирование селективно чувствитель-
вой научной концепции в когнитивной нейро-
ных к этим гормонам структур мозга, в первую
биологии. Постулировано существование но-
очередь гиппокампа, стимулировало интерес
вой регуляторной оси гипоталамус-гипофиз-
к исследованиям влияния хронического ги-
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
715
перкортицизма на головной мозг. У пациен-
Избыток ГК нарушает функцию и ухудша-
тов с синдромом Кушинга отмечены наруше-
ет структуру гиппокампа, области мозга, клю-
ния памяти, связанной с гиппокампом, при
чевой для обучения, памяти и эмоций. Изби-
этом функциональные нарушения гиппокампа
рательная уязвимость гиппокампа к стрессу,
предшествуют структурным аномалиям, обна-
опосредованная ГК, секретируемыми во время
руженным нейровизуализационными метода-
стресса, является платой за высокую функ-
ми. При синдроме Кушинга также наблюда-
циональную пластичность и плейотропные
ются нарушения исполнительных функций
функции этой лимбической структуры. Общие
(включая принятие решений) и других функ-
для многих церебральных патологий моле-
ций, таких как зрительно-конструктивные на-
кулярные и клеточные механизмы включают
выки, речь, двигательные функции и скорость
дисфункцию GR, гиперглутаматергические со-
обработки информации. Ранняя диагностика
стояния, нарушение систем нейротрофических
и быстрая нормализация гиперкортицизма
факторов, развитие нейровоспаления, приво-
могут остановить и предотвратить прогресси-
дящего к нейродегенерации и потере нейро-
рование поражения гиппокампа и нарушений
нов гиппокампа, а также нарушения нейро-
памяти [138]. Среди пациентов с синдромом
генеза в субгранулярной нейрогенной нише
Кушинга наблюдается высокая распростра-
и формирование аберрантных нейронных се-
ненность психопатологии, в первую очередь
тей [17, 147]. Эти ГК-зависимые процессы ас-
депрессии и тревожности, также ассоцииро-
социированы с измененной реакцией на стресс
ванных с избыточной секрецией ГК и измене-
и развитием хронических сопутствующих па-
ниями гиппокампа.
тологий, вызванных стрессом.
Лечение критических заболеваний обычно
За последние 50 лет концепция стресса
фокусируется на кратковременном физиче-
значительно изменилась, и наше понимание
ском восстановлении пациента, однако люди,
лежащей в его основе нейробиологии резко
пережившие тяжелое заболевание, имеют зна-
расширилось [148]. Биология стресса актуаль-
чительно повышенный риск развития стойких
на не только в необычных и угрожающих усло-
когнитивных нарушений и психических рас-
виях, но современное представление опреде-
стройств. В работе Hill и Spencer-Segal [139]
ляет ее, как непрерывный адаптивный процесс
подробно рассматривается роль эндогенных
оценки окружающей среды, преодоления ее
и экзогенных ГК в развитии психоневрологи-
факторов и предоставления человеку возмож-
ческих патологий после критических заболе-
ности предвидеть будущие проблемы и справ-
ваний. Такие заболевания характеризуются
ляться с ними. Фундаментальная нейросхема,
резким повышением уровня свободного кор-
лежащая в основе этих процессов, в общих
тизола и подавлением уровня ACTH, которые
чертах понятна, определены ключевые моле-
обычно нормализуются после выздоровления,
кулярные процессы, установлено их влияние
однако иногда может наблюдаться длитель-
на нейропластичность. Однако все чаще пере-
ное нарушение регуляции ГГНО. Высокие
сматриваются концепции о механизмах пато-
уровни ГК могут вызывать длительные изме-
генеза заболеваний мозга, которые учитывали
нения пластичности и структурной целост-
роль какой-либо одной отдельной системы
ности гиппокампа и префронтальной коры;
как ключевой. Это хорошо видно на примере
этот механизм, вероятно, может способство-
эволюции понимания патогенеза депрессии.
вать развитию нарушений памяти и когнитив-
Существует несколько теорий депрессии, кото-
ных способностей у выживших в критических
рые предполагают альтернативно нарушения
состояниях, хотя строгие доказательства этого
регуляции ГГНО, модуляцию моноаминерги-
предположения до сих пор не получены. Тем
ческой нейротрансмиссии, изменения нейро-
не менее с повышенными уровнями ГК ассо-
трофических факторов и изменения нейро-
циированы самые различные церебральные
генеза в гиппокампе, однако ни одна из этих
патологии, затрагивающие когнитивную и
теорий не объясняет в достаточной мере этио-
эмоциональную сферы, от депрессивных рас-
патологию и подходы к лечению депрессии.
стройств до эпилепсии [140], инсульта [141, 142]
При этом концепции, основанные на нару-
и черепно-мозговой травмы [143, 144]. Общие
шениях системы BDNF или нейрогенеза, под-
механизмы различных патологий мозга под-
черкивают важную роль пластичности при
тверждают не только частые коморбидности, но
депрессии и тот факт, что гиппокамп является
и развитие одних патологий на базе других. На-
важной анатомической областью, связанной с
пример, депрессия является фактором риска и
депрессией. Исследования показали, что не-
компонентом БА, она также может быть триг-
которые антидепрессанты могут купировать
гером начальной стадии БА [145, 146].
симптомы депрессии, изменяя пластичность
БИОХИМИЯ том 88 вып. 5 2023
716
ГУЛЯЕВА
Рис. 2. Регуляция пластичности взрослого гиппокампа глюкокортикоидами. На сводной схеме представлены основные
пути регуляции глюкокортикоидными гормонами (ГК) различных механизмов пластичности. Слева показана гипо-
таламо-гипофизарно-надпочечниковая ось (ГГНО), названия составляющих ее структур отмечены красным; назва-
ния основных гормонов в рамках: кортикотропин-рилизинг-гормон (CRH), адренокортикотропный гормон (ACTH),
кортизол (у человека) или кортикостерон (у грызунов). Указаны также остальные компоненты лимбической системы
мозга, гиппокамп и миндалина. В левой колонке приведены ключевые системы гиппокампа, определяющие его плас-
тичность и одновременно являющиеся мишенями ГК (голубой фон). В средней колонке (зеленый фон) отмечены
основные патологические эффекты на эти системы избытка ГК, возникающего в результате нарушения регуляции
ГГНО и/или стресса (сильного, хронического у взрослых или стресса в раннем периоде онтогенеза). В последней
колонке (красный фон) представлены заболевания и состояния, для патогенеза которых ключевым является развитие
патологических последствий ГК-зависимых нарушений пластичности гиппокампа. Следует учесть, что действие ГК
на мишени, указанные в голубой колонке, не обязательно прямое. Кроме этого, одна красная стрелка может включать
множественные механизмы, по которым ГК действуют на специфическую мишень. Подробные объяснения в соответ-
ствующих разделах текста
гиппокампа, и последние варианты теории
основных патомеханизма БА: неправильный
постулируют, что именно синтез множествен-
процессинг АРР и образование β-амилоида,
ных механизмов пластичности мозга, вклю-
которые, наряду с гиперфосфорилированием
чая изменения серотонинергической системы,
и агрегацией тау-белка, связаны с изменения-
ГГНО, нейрогенеза и системы BDNF, а также
ми нейропластичности. Учитывая, что депрес-
нейровоспаление может объединить много-
сия прямо связана со стрессом, и доказатель-
численные «монотеории» [149]. Второй при-
ства того, что депрессия является фактором
мер - признание роли стресса в механизме
риска БА, общие для этих заболеваний ней-
патогенеза БА, многофакторного нейродеге-
робиологические механизмы и представляют
неративного заболевания [150]. Накапливаю-
собой описанные в данном обзоре изменения,
щиеся клинические и экспериментальные дан-
приводящие к нарушению пластичности гип-
ные свидетельствуют о ключевой роли стресса
покампа.
в развитии БА. Хронический стресс и сопро-
Основные данные, проанализированные в
вождающий его высокий уровень секреции ГК
этом обзоре, суммированы на достаточно про-
запускают, наряду со многими другими, два
стой схеме (рис. 2). Показано, как каскадная
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
717
сигнализация по ГГНО за счет связывания ее
ленных на схеме систем. Важность каждой из
конечных гормонов, ГК, с кортикостероид-
этих систем не подлежит сомнению, поэтому
ными рецепторами гиппокампа осуществляет
ключевые компоненты каждой системы рас-
контроль различных мишеней
- ключевых
сматриваются как мишени для терапии, и раз-
компонентов сложной и многоуровневой си-
рабатываются подходы (фармакологические и
стемы пластичности гиппокампа. С одной сто-
не фармакологические) к воздействию на эти
роны, эта схема показывает потенциальные
мишени. До сих пор такие подходы не привели
ключевые мишени регуляции нейропластич-
к выдающимся успехам лечения церебральных
ности посредством ГК в соответствии с дан-
патологий. Если ГК действительно выполняют
ными эксперимента и клиники, накопленны-
функции дирижера гиппокампальной нейро-
ми к настоящему моменту. С другой стороны,
пластичности, возможно, следует больше вни-
эта схема не содержит информации о десятках
мания уделить потенциальным возможностям
механистических связей между различными
коррекции ГГНО, уровня кортизола и состоя-
системами-мишенями ГК, влиянии каждой из
ния рецепторов ГК? Логика подсказывает,
этих систем на эффекты ГК, а также о регуля-
что, если научиться корректировать основную
торном влиянии ГК на взаимодействие между
регуляторную систему, благоприятный эффект
этими системами. Эти данные приведены в
будет оказан и на патологически измененные
тексте, но отображение их на этом рисунке
в результате ее нарушения нижележащие ком-
оказалось практически невозможным, в пол-
поненты. Очевидно, что направленно воздей-
ном сооветствии с известным высказыванием
ствовать на такую сложную нейрогуморальную
Поля Валери (Paul Valéry): «Все простое тео-
систему, как ГГНО, чрезвычайно сложно, од-
ретически ложно, а все сложное прагматиче-
нако, очень вероятно, что именно достижение
ски бесполезно» (“Everything that is simple is
управления этой системой позволит поддержи-
theoretically false, everything that is complicated is
вать оптимальный уровень нейропластичности
pragmatically useless”). Таким образом, анали-
и тем самым совершить давно ожидаемый про-
зируя схему, нужно иметь в виду, что практи-
рыв в терапии когнитивных и эмоциональных
чески все мишени, регулируемые ГК, связаны
расстройств, а также соответствующих комор-
между собой многочисленными процессами
бидных состояний. Синтез новых лигандов
на молекулярном, субклеточном и клеточном
рецепторов ГК, результаты их применения в
уровнях. С учетом вынесенного в качестве
экспериментах на моделях заболеваний мозга и
эпиграфа к заключению третьего закона Мей-
предварительные результаты их применения в
ера, гласящего, что просто усложнять вещи,
клинике [151-157] позволяют надеяться на то,
но сложно их упрощать, на этом этапе анализа
что этот подход принесет долгожданный успех.
мы оставляем простую схему, которая иллю-
стрирует роль ГК в качестве «дирижера» мно-
Финансирование. Работа выполнена в рам-
гокомпонентного оркестра, поддерживающего
ках государственного задания Министерства
нейропластичность гиппокампа, но подразу-
образования и науки Российской Федерации
меваем наличие контролируемых дирижером
на 2021-2023 гг.
сложных взаимоотношений между оркестран-
Конфликт интересов. Автор заявляет об от-
тами и их обратных связей с дирижером.
сутствии конфликта интересов.
При различных патологиях мозга, наря-
Соблюдение этических норм. Настоящая
ду с нарушениями регуляции ГГНО, секре-
статья не содержит описания каких-либо ис-
ции ГК, экспрессии и свойств их рецепторов,
следований с участием людей или животных в
происходят изменения в каждой из представ-
качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1. Gulyaeva, N. V.
(2017) Molecular mechanisms
3. Goto, A. (2022) Synaptic plasticity during systems
of
neuroplasticity:
an expanding universe,
memory consolidation, Neurosci. Res.,
183,
1-6,
Biochemistry (Moscow), 82, 237-242, doi: 10.1134/
doi: 10.1016/j.neures.2022.05.008.
S0006297917030014.
4. Toda, T., and Gage, F. H. (2018) Review: adult neuro-
2. Xiong, H., and Krugers, H. J.
(2015) Tuning
genesis contributes to hippocampal plasticity, Cell. Tis-
hippocampal synapses by stress-hormones: relevance
sue Res., 373, 693-709, doi: 10.1007/s00441-017-2735-4.
for emotional memory formation, Brain Res., 1621,
5. Deppermann, S., Storchak, H., Fallgatter, A. J., and
114-120, doi: 10.1016/j.brainres.2015.04.010.
Ehlis, A. C. (2014) Stress-induced neuroplasticity:
БИОХИМИЯ том 88 вып. 5 2023
718
ГУЛЯЕВА
(mal)adaptation to adverse life events in patients with
Biochemistry (Moscow), 86, 641-656, doi: 10.1134/
PTSD - a critical overview, Neuroscience, 283, 166-
S0006297921060031.
177, doi: 10.1016/j.neuroscience.2014.08.037.
18.
Madalena, K. M., and Lerch, J. K. (2017) The effect of
6.
Den Boon, F. S., and Sarabdjitsingh, R. A. (2017)
glucocorticoid and glucocorticoid receptor interactions
Circadian and ultradian patterns of HPA-axis activity
on brain, spinal cord, and glial cell plasticity,
in rodents: significance for brain functionality, Best
Neural Plast.,
2017,
8640970, doi:
10.1155/2017/
Pract. Res. Clin. Endocrinol. Metab., 31, 445-457,
8640970.
doi: 10.1016/j.beem.2017.09.001.
19.
Weerasinghe-Mudiyanselage, P. D. E., Ang, M. J.,
7.
Gray, J. D., Kogan, J. F., Marrocco, J., and McEwen,
Kang, S., Kim, J. S., and Moon, C. (2022) Structural
B. S. (2017) Genomic and epigenomic mechanisms of
plasticity of the hippocampus in neurodegenerative
glucocorticoids in the brain, Nat. Rev Endocrinol., 13,
diseases, Int. J. Mol. Sci., 23, 3349, doi: 10.3390/
661-673, doi: 10.1038/nrendo.2017.97.
ijms23063349.
8.
Meijer, O. C., Buurstede, J. C., and Schaaf, M. J. M.
20.
De Kloet, E. R., Sutanto, W., Rots, N., van Haarst, A.,
(2019) Corticosteroid receptors in the brain: tran-
van den Berg, D., Oitzl, M., van Eekelen, A., and
scriptional mechanisms for specificity and context-
Voorhuis, D. (1991) Plasticity and function of brain
dependent effects, Cell. Mol. Neurobiol., 39, 539-549,
corticosteroid receptors during aging, Acta Endocrinol.
doi: 10.1007/s10571-018-0625-2.
(Copenh), 125 Suppl 1, 65-72.
9.
Koning, A. C. A. M., Buurstede, J. C., van Weert, L.
21.
Fares, J., Bou Diab, Z., Nabha, S., and Fares, Y. (2019)
T. C. M., and Meijer, O. C. (2019) Glucocorticoid
Neurogenesis in the adult hippocampus: history,
and mineralocorticoid receptors in the brain: a
regulation, and prospective roles, Int. J. Neurosci.,
transcriptional perspective, J. Endocr. Soc., 3, 1917-
129, 598-611, doi: 10.1080/00207454.2018.1545771.
1930, doi: 10.1210/js.2019-00158.
22.
Ko, S. Y., and Frankland, P. W. (2021) Neurogenesis-
10.
Meijer, O. C., Buurstede, J. C., Viho, E. M. G., Amaya,
dependent transformation of hippocampal engrams,
J. M., Koning, A. C. A. M., van der Meulen, M.,
Neurosci. Lett., 762, 136176, doi: 10.1016/j.neulet.
van Weert, L. T. C. M., Paul, S. N., Kroon, J., and
2021.136176.
Koorneef, L. L. (2023) Transcriptional glucocorticoid
23.
Miller, S. M., and Sahay, A.
(2019) Functions
effects in the brain: Finding the relevant target genes,
of adult-born neurons in hippocampal memory
J. Neuroendocrinol., 35, e13213, doi: 10.1111/jne.13213.
interference and indexing, Nat. Neurosci., 22, 1565-
11.
Gulyaeva, N. V. (2021) Glucocorticoid regulation
1575, doi: 10.1038/s41593-019-0484-2.
of the glutamatergic synapse: mechanisms of stress-
24.
Tuncdemir, S. N., Lacefield, C. O., and Hen, R.
dependent neuroplasticity, J. Evol. Biochem. Phys., 57,
(2019) Contributions of adult neurogenesis to dentate
564-576, doi: 10.1134/S0022093021030091.
gyrus network activity and computations, Behav. Brain
12.
Fuxe, K., Diaz, R., Cintra, A., Bhatnagar, M.,
Res., 374, 112112, doi: 10.1016/j.bbr.2019.112112.
Tinner, B., Gustafsson, J. A., Ogren, S. O., and
25.
Moreno-Jiménez, E. P., Terreros-Roncal, J., Flor-
Agnati, L. F. (1996) On the role of glucocorticoid re-
García, M., Rábano, A., and Llorens-Martín, M.
ceptors in brain plasticity, Cell. Mol. Neurobiol., 16,
(2021) Evidences for adult hippocampal neurogenesis
239-258, doi: 10.1007/BF02088179.
in humans, J. Neurosci., 41, 2541-2553, doi: 10.1523/
13.
Suri, D., and Vaidya, V. A. (2015) The adaptive
JNEUROSCI.0675-20.2020.
and maladaptive continuum of stress responses - a
26.
Huckleberry, K. A., and Shansky, R. M.
(2021)
hippocampal perspective, Rev. Neurosci., 26, 415-442,
The unique plasticity of hippocampal adult-bornneu-
doi: 10.1515/revneuro-2014-0083.
rons: contributing to a heterogeneous dentate, Hippo-
14.
Uchoa, E. T., Aguilera, G., Herman, J. P., Fiedler,
campus, 31, 543-556, doi: 10.1002/hipo.23318.
J. L., Deak, T., and de Sousa, M. B. (2014) Novel
27.
Vilar, M., and Mira, H.
(2016) Regulation of
aspects of glucocorticoid actions, J. Neuroendocrinol.,
neurogenesis by neurotrophins during adulthood:
26, 557-572, doi: 10.1111/jne.12157.
expected and unexpected roles, Front. Neurosci., 10,
15.
Bolshakov, A. P., Tret’yakova, L. V., Kvichansky, A. A.,
26, doi: 10.3389/fnins.2016.00026.
and Gulyaeva, N. V. (2021) Glucocorticoids: Dr. Jekyll
28.
Niklison-Chirou, M. V., Agostini, M., Amelio, I., and
and Mr. Hyde of hippocampal neuroinflammation,
Melino, G. (2020) Regulation of adult neurogenesis
Biochemistry (Moscow), 86, 156-167, doi: 10.1134/
in mammalian brain, Int. J. Mol. Sci., 21, 4869,
S0006297921020048.
doi: 10.3390/ijms21144869.
16.
McEwen, B. S. (2002) Sex, stress and the hippo-
29.
Jorgensen, C., and Wang, Z. (2020) Hormonal regu-
campus: allostasis, allostatic load and the aging pro-
lation of mammalian adult neurogenesis: a multifac-
cess, Neurobiol. Aging, 23, 921-939, doi: 10.1016/
eted mechanism, Biomolecules, 10, 1151, doi: 10.3390/
s0197-4580(02)00027-1.
biom10081151.
17.
Gulyaeva, N. V. (2021) Stress-associated molecular
30.
Surget, A., and Belzung, C. (2022) Adult hippocampal
and cellular hippocampal mechanisms common
neurogenesis shapes adaptation and improves stress
for epilepsy and comorbid depressive disorders,
response: a mechanistic and integrative perspective,
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
719
Mol. Psychiatry, 27, 403-421, doi: 10.1038/s41380-
44.
Valbuena, S., and Lerma, J. (2021) Kainate recep-
021-01136-8.
tors, homeostatic gatekeepers of synaptic plasticity,
31.
Jones, K. L., Zhou, M., and Jhaveri, D. J. (2022)
Neuroscience, 456, 17-26, doi: 10.1016/j.neuroscience.
Dissecting the role of adult hippocampal neurogenesis
2019.11.050.
towards resilience versus susceptibility to stress-related
45.
Griego, E., and Galván, E. J. (2021) Metabotropic
mood disorders, NPJ Sci. Learn., 7, 16, doi: 10.1038/
glutamate receptors at the aged mossy fiber - CA3
s41539-022-00133-y.
synapse of the hippocampus, Neuroscience, 456, 95-
32.
Lucassen, P. J., Oomen, C. A., Naninck, E. F.,
105, doi: 10.1016/j.neuroscience.2019.12.016.
Fitzsimons, C. P., van Dam, A. M., Czeh, B., and
46.
Mukherjee, S., and Manahan-Vaughan, D.
(2013)
Korosi, A. (2015) Regulation of adult neurogenesis
Role of metabotropic glutamate receptors in
and plasticity by (early) stress, glucocorticoids, and
persistent forms of hippocampal plasticity and
inflammation, Cold Spring Harb. Perspect. Biol., 7,
learning, Neuropharmacology, 66, 65-81, doi: 10.1016/
a021303, doi: 10.1101/cshperspect.a021303.
j.neuropharm.2012.06.005.
33.
Podgorny, O. V., and Gulyaeva, N. V.
(2021)
47.
Mikasova, L., Xiong, H., Kerkhofs, A., Bouchet, D.,
Glucocorticoid-mediated mechanisms of hippocampal
Krugers, H. J., and Groc, L. (2017) Stress hormone
damage: contribution of subgranular neurogenesis,
rapidly tunes synaptic NMDA receptor through
J. Neurochem., 157, 370-392, doi: 10.1111/jnc.15265.
membrane dynamics and mineralocorticoid sig-
34.
Vasic, V., and Schmidt, M. H. H. (2017) Resilience
nalling, Sci. Rep.,
7,
8053, doi:
10.1038/s41598-
and vulnerability to pain and inflammation in the
017-08695-3.
hippocampus, Int. J. Mol. Sci., 18, 739, doi: 10.3390/
48.
Gonçalves-Ribeiro, J., Pina, C. C., Sebastião, A. M.,
ijms18040739.
and Vaz, S. H. (2019) Glutamate transporters in hip-
35.
Kirschen, G. W., and Ge, S. (2019) Young at heart:
pocampal LTD/LTP: not just prevention of excito-
insights into hippocampal neurogenesis inthe aged
toxicity, Front. Cell. Neurosci., 13, 357, doi: 10.3389/
brain, Behav. Brain. Res., 369, 111934, doi: 10.1016/
fncel.2019.00357.
j.bbr.2019.111934.
49.
Taylor, C. J., He, R., and Bartlett, P. F.
(2014)
36.
Chen, P., Guo, Z., and Zhou, B. (2023) Insight into
The role of the N-methyl-D-aspartate receptor in
the role of adult hippocampal neurogenesis in aging
the proliferation of adult hippocampal neural stem
and Alzheimer’s disease, Ageing Res. Rev., 84, 101828,
and precursor cells, Sci. China Life Sci., 57, 403-411,
doi: 10.1016/j.arr.2022.101828.
doi: 10.1007/s11427-014-4637-y.
37.
Teixeira, C. M., Pallas-Bazarra, N., Bolós, M.,
50.
Gulyaeva, N. V. (2022) Neuroendocrine control of
Terreros-Roncal, J., Ávila, J., and Llorens-Martín, M.
hyperglutamatergic states in brain pathologies: the
(2018) Untold new beginnings: adult hippocampal
effects of glucocorticoids, J. Evol. Biochem. Phys., 58,
neurogenesis and Alzheimer’s disease, J. Alzheimers
1425-1438, doi: 10.1134/S0022093022050131.
Dis., 64 (s1), S497-S505, doi: 10.3233/JAD-179918.
51.
Jacobsson, J., Persson, M., Hansson, E., and
38.
Nicola, R., and Oku, E. (2021) Adult hippocampal
Rönnbäck, L. (2006) Corticosterone inhibits expres-
neurogenesis: one lactate to rule them all, Neuromol.
sion of the microglial glutamate transporter GLT-1
Med., 23, 445-448, doi: 10.1007/s12017-021-08658-y.
in vitro, Neuroscience, 139, 475-483, doi: 10.1016/
39.
McEwen, B. S. (1996) Gonadal and adrenal steroids
j.neuroscience.2005.12.046.
regulate neurochemical and structural plasticity of
52.
Zschocke, J., Bayatti, N., Clement, A. M., Witan, H.,
the hippocampus via cellular mechanisms involving
Figiel, M., Engele, J., and Behl, C. (2005) Differential
NMDA receptors, Cell. Mol. Neurobiol., 16, 103-116,
promotion of glutamate transporter expression and
doi: 10.1007/BF02088170.
function by glucocorticoids in astrocytes from various
40.
Mihály, A.
(2019) The reactive plasticity of
brain regions, J. Biol. Chem., 280, 34924-34932,
hippocampal ionotropic glutamate receptors in animal
doi: 10.1074/jbc.M502581200.
epilepsies, Int. J. Mol. Sci., 20, 1030, doi: 10.3390/
53.
Chu, S. F., Zhang, Z., Zhou, X., He, W. B., Yang, B.,
ijms20051030.
Cui, L. Y., He, H. Y., Wang, Z. Z., and Chen, N. H.
41.
Shipton, O. A., and Paulsen, O. (2013) GluN2A and
(2021) Low corticosterone levels attenuate late life de-
GluN2B subunit-containing NMDA receptors in
pression and enhance glutamatergic neurotransmis-
hippocampal plasticity, Philos. Trans. R. Soc. Lond. B.
sion in female rats, Acta Pharmacol. Sin., 42, 848-860,
Biol. Sci., 369, 20130163, doi: 10.1098/rstb.2013.0163.
doi: 10.1038/s41401-020-00536-w.
42.
Pampaloni, N. P., and Plested, A. J. R. (2022) Slow
54.
Kang, M., Ryu, J., Kim, J. H., Na, H., Zuo, Z.,
excitatory synaptic currents generated by AMPA recep-
and Do, S. H. (2010) Corticosterone decreases the
tors, J. Physiol., 600, 217-232, doi: 10.1113/JP280877.
activity of rat glutamate transporter type 3 expressed in
43.
Nair, J. D., Wilkinson, K. A., Henley, J. M., and
Xenopus oocytes, Steroids, 75, 1113-1118, doi: 10.1016/
Mellor, J. R. (2021) Kainate receptors and syn-
j.steroids.2010.07.003.
apticplasticity, Neuropharmacology,
196,
108540,
55.
Cox, M. F., Hascup, E. R., Bartke, A., and Hascup,
doi: 10.1016/j.neuropharm.2021.108540.
K. N. (2022) Friend or foe? Defining the role of
БИОХИМИЯ том 88 вып. 5 2023
720
ГУЛЯЕВА
glutamate in aging and Alzheimer’s disease, Front.
ing, Adv. Exp. Med. Biol., 872, 33-57, doi: 10.1007/
Aging, 3, 929474, doi: 10.3389/fragi.2022.929474.
978-1-4939-2895-8_2.
56.
Gulyaeva, N. V. (2022) Multi-level plasticity-pathol-
69.
Jeanneteau, F., and Chao, M. V. (2013) Are BDNF
ogy continuum of the nervous system: functional
and glucocorticoid activities calibrated? Neuroscience,
aspects, Neurochem. J., 16, 424-428, doi: 10.1134/
239, 173-195, doi: 10.1016/j.neuroscience.2012.09.017.
S1819712422040092.
70.
Rothman, S. M., and Mattson, M. P. (2013) Activity-
57.
Bano, D., and Ankarcrona, M. (2018) Beyond the
dependent, stress-responsive BDNF signaling and
critical point: an overview of excitotoxicity, calci-
the quest for optimal brain health and resilience
um overload and the downstream consequences,
throughout the lifespan, Neuroscience, 239, 228-240,
Neurosci. Lett.,
663,
79-85, doi:
10.1016/j.neulet.
doi: 10.1016/j.neuroscience.2012.10.014.
2017.08.048.
71.
Gulyaeva, N. V. (2017) Interplay between brain BDNF
58.
Foster, T. C., Kyritsopoulos, C., and Kumar, A. (2017)
and glutamatergic systems: a brief state of the evidence
Central role for NMDA receptors in redox mediated
and association with the pathogenesis of depression,
impairment of synaptic function during aging and
Biochemistry (Moscow), 82, 301-307, doi: 10.1134/
Alzheimer’s disease, Behav. Brain Res., 322 (Pt B),
S0006297917030087.
223-232, doi: 10.1016/j.bbr.2016.05.012.
72.
Gibon, J., Barker, P. A. (2017) Neurotrophins and
59.
Temido-Ferreira, M., Coelho, J. E., Pousinha, P. A.,
proneurotrophins: focus on synaptic activity and
and Lopes, L. V. (2019) Novel players in the aging
plasticity in the brain, Neuroscientist, 23, 587-604,
synapse: impact on cognition, J. Caffeine Adenosine
doi: 10.1177/1073858417697037.
Res., 9, 104-127, doi: 10.1089/caff.2019.0013.
73.
Mizui, T., Ishikawa, Y., Kumanogoh, H., and
60.
Leal, G., Bramham, C. R., and Duarte, C. B. (2017)
Kojima, M. (2016) Neurobiological actions by three
BDNF and hippocampal synaptic plasticity, Vitam.
distinct subtypes of brain-derived neurotrophic fac-
Horm., 104, 153-195, doi: 10.1016/bs.vh.2016.10.004.
tor: multi-ligand model of growth factor signaling,
61.
Gómez-Palacio-Schjetnan, A., and Escobar, M. L.
Pharmacol. Res.,
105,
93-98, doi:
10.1016/j.phrs.
(2013) Neurotrophins and synaptic plasticity, Curr.
2015.12.019.
Top. Behav. Neurosci.,
15,
117-136, doi:
10.1007/
74.
Kojima, M., and Mizui, T. (2017) BDNF propeptide:
7854_2012_231.
a novel modulator of synaptic plasticity, Vitam. Horm.,
62.
De Vincenti, A. P., Ríos, A. S., Paratcha, G.,
104, 19-28, doi: 10.1016/bs.vh.2016.11.006.
and Ledda, F. (2019) Mechanisms that modulate
75.
Costa, R. O., Perestrelo, T., and Almeida, R. D.
and diversify BDNF functions: implications for
(2018) PROneurotrophins and CONSequences,
hippocampal synaptic plasticity, Front. Cell. Neurosci.,
Mol. Neurobiol., 55, 2934-2951, doi: 10.1007/s12035-
13, 135, doi: 10.3389/fncel.2019.00135.
017-0505-7.
63.
Zagrebelsky, M., and Korte, M.
(2014) Form
76.
Leal, G., Afonso, P. M., Salazar, I. L., and Duarte,
follows function: BDNF and its involvement in
C. B. (2015) Regulation of hippocampal synaptic
sculpting the function and structure of synapses,
plasticity by BDNF, Brain Res.,
1621,
82-101,
Neuropharmacology, 76 Pt C, 628-638, doi: 10.1016/
doi: 10.1016/j.brainres.2014.10.019.
j.neuropharm.2013.05.029.
77.
Notaras, M., and van den Buuse, M. (2020) Neu-
64.
Von Bohlen Und Halbach, O., and von Bohlen Und
robiology of BDNF in fear memory, sensitivity
Halbach, V. (2018) BDNF effects on dendritic spine
to stress, and stress-related disorders, Mol. Psy-
morphology and hippocampal function, Cell. Tissue
chiatry,
25,
2251-2274, doi:
10.1038/s41380-
Res., 373, 729-741, doi: 10.1007/s00441-017-2782-x.
019-0639-2.
65.
Jeanneteau, F., Borie, A., Chao, M. V., and
78.
Lu, B., Nagappan, G., and Lu, Y. (2014) BDNF
Garabedian, M. J. (2019) Bridging the Gap between
and synaptic plasticity, cognitive function, and
brain-derived neurotrophic factor and glucocorticoid
dysfunction, Handb. Exp. Pharmacol., 220, 223-250,
effects on brain networks, Neuroendocrinology, 109,
doi: 10.1007/978-3-642-45106-5_9.
277-284, doi: 10.1159/000496392.
79.
Ninan, I.
(2014) Synaptic regulation of affec-
66.
Gray, J. D., Milner, T. A., and McEwen, B. S. (2013)
tive behaviors; role of BDNF, Neuropharmacology,
Dynamic plasticity: the role of glucocorticoids,
76 Pt C, 684-695, doi: 10.1016/j.neuropharm.2013.
brain-derived neurotrophic factor and other trophic
04.011.
factors, Neuroscience, 239, 214-227, doi: 10.1016/
80.
Duman, R. S., Deyama, S., and Fogaça, M. V. (2021)
j.neuroscience.2012.08.034.
Role of BDNF in the pathophysiology and treatment
67.
Numakawa, T., and Odaka, H. (2022) The role of
of depression: activity-dependent effects distinguish
neurotrophin signaling in age-related cognitive decline
rapid-acting antidepressants, Eur. J. Neurosci., 53,
and cognitive diseases, Int. J. Mol. Sci., 23, 7726,
126-139, doi: 10.1111/ejn.14630.
doi: 10.3390/ijms23147726.
81.
Colucci-D’Amato, L., Speranza, L., and Volpicelli,
68.
Arango-Lievano, M., Lambert, W. M., and Jeanneteau, F.
F. (2020) Neurotrophic factor BDNF, physiological
(2015) Molecular biology of glucocorticoid signal-
functions and therapeutic potential in depression,
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
721
neurodegeneration and brain cancer, Int. J. Mol. Sci.,
brain diseases, Curr. Med. Chem., 14, 1189-1197,
21, 7777, doi: 10.3390/ijms21207777.
doi: 10.2174/092986707780597961.
82.
Numakawa, T., Adachi, N., Richards, M., Chiba, S.,
95. Williamson, L. L., and Bilbo, S. D. (2013) Chemokines
and Kunugi, H. (2013) Brain-derived neurotrophic
and the hippocampus: a new perspective on
factor and glucocorticoids: reciprocal influence on the
hippocampal plasticity and vulnerability, Brain. Behav.
central nervous system, Neuroscience, 239, 157-172,
Immun., 30, 186-194, doi: 10.1016/j.bbi.2013.01.077.
doi: 10.1016/j.neuroscience.2012.09.073.
96. Singhal, G., and Baune, B. T. (2017) Microglia:
83.
Jones, O. D. (2015) Astrocyte-mediated metaplasticity
an interface between the loss of neuroplasticity
in the hippocampus: help or hindrance? Neuroscience,
and depression, Front. Cell. Neurosci.,
11,
270,
309, 113-124, doi: 10.1016/j.neuroscience.2015.08.035.
doi: 10.3389/fncel.2017.00270.
84.
Fuchsberger, T., and Paulsen, O. (2022) Modulation
97. Bauer, M. E., and Teixeira, A. L. (2019) Inflammation
of hippocampal plasticity in learning and memory,
in psychiatric disorders: what comes first? Ann. N. Y.
Curr. Opin. Neurobiol., 75, 102558, doi: 10.1016/
Acad. Sci., 1437, 57-67, doi: 10.1111/nyas.13712.
j.conb.2022.102558.
98. Bisht, K., Sharma, K., and Tremblay, M. È. (2018)
85.
Wang, Y., Fu, A. K. Y., and Ip, N. Y. (2022) Instructive
Chronic stress as a risk factor for Alzheimer’s disease:
roles of astrocytes in hippocampal synaptic plasticity:
roles of microglia-mediated synaptic remodeling,
neuronal activity-dependent regulatory mechanisms,
inflammation, and oxidative stress, Neurobiol. Stress,
FEBS J., 289, 2202-2218, doi: 10.1111/febs.15878.
9, 9-21, doi: 10.1016/j.ynstr.2018.05.003.
86.
Çalışkan, G., Müller, A., and Albrecht, A. (2020)
99. Patterson, S. L. (2015) Immune dysregulation and
Long-term impact of early-life stress on hippocampal
cognitive vulnerability in the aging brain: Interactions
plasticity: spotlight on astrocytes, Int. J. Mol. Sci., 21,
of microglia, IL-1β, BDNF and synaptic plasticity,
4999, doi: 10.3390/ijms21144999.
Neuropharmacology, 96 (Pt A), 11-18, doi: 10.1016/
87.
Cassé, F., Richetin, K., and Toni, N. (2018) Astrocytes’
j.neuropharm.2014.12.020.
contribution to adult neurogenesis in physiology and
100. Salazar, I. L., Caldeira, M. V., Curcio, M., and
Alzheimer’s disease, Front. Cell. Neurosci., 12, 432,
Duarte, C. B. (2016) The role of proteases in hippo-
doi: 10.3389/fncel.2018.00432.
campal synaptic plasticity: putting together small piec-
88.
Delpech, J. C., Madore, C., Nadjar, A., Joffre, C.,
es of a complex puzzle, Neurochem. Res., 41, 156-182,
Wohleb, E. S., and Layé, S. (2015) Microglia in neu-
doi: 10.1007/s11064-015-1752-5.
ronal plasticity: Influence of stress, Neuropharma-
101. Wiera, G., and Mozrzymas, J. W. (2015) Extracel-
cology, 96 (Pt A), 19-28, doi: 10.1016/j.neuropharm.
lular proteolysis in structural and functional plas-
2014.12.034.
ticity of mossy fiber synapses in hippocampus,
89.
Guedes, J. R., Ferreira, P. A., Costa, J. M., Cardoso,
Front. Cell. Neurosci., 9, 427, doi: 10.3389/fncel.
A. L., and Peça, J. (2022) Microglia-dependent re-
2015.00427.
modeling of neuronal circuits, J. Neurochem., 163, 74-
102. Wójtowicz, T., Brzdąk, P., and Mozrzymas, J. W.
93, doi: 10.1111/jnc.15689.
(2015) Diverse impact of acute and long-term extra-
90.
Rodríguez-Iglesias, N., Sierra, A., and Valero, J.
cellular proteolytic activity on plasticity of neuronal
(2019) Rewiring of memory circuits: connecting adult
excitability, Front. Cell. Neurosci., 9, 313, doi: 10.3389/
newborn neurons with the help of microglia, Front.
fncel.2015.00313.
Cell. Dev. Biol., 7, 24, doi: 10.3389/fcell.2019.00024.
103. Gulyaeva, N. V. (2003) Non-apoptotic functions of
91.
Turkin, A., Tuchina, O., and Klempin, F.
(2021)
caspase-3 in nervous tissue, Biochemistry (Moscow), 68,
Microglia function on precursor cells in the adult hip-
1171-1180, doi: 10.1023/b:biry.0000009130.62944.35.
pocampus and their responsiveness to serotonin sig-
104. Yakovlev, A. A., and Gulyaeva, N. V. (2011) Pleio-
naling, Front. Cell. Dev. Biol., 9, 665739, doi: 10.3389/
tropic functions of brain proteinases: methodologi-
fcell.2021.665739.
cal considerations and search for caspase substrates,
92.
Sanguino-Gómez, J., Buurstede, J. C., Abiega, O.,
Biochemistry (Moscow), 76, 1079-1086, doi: 10.1134/
Fitzsimons, C. P., Lucassen, P. J., Eggen, B. J. L.,
S0006297911100014.
Lesuis, S. L., Meijer, O. C., and Krugers, H. J. (2022)
105. Wang, Y., Liu, Y., Bi, X., and Baudry, M. (2020)
An emerging role for microglia in stress-effects on
Calpain-1 and calpain-2 in the brain: new evidence for
memory, Eur. J. Neurosci., 55, 2491-2518, doi: 10.1111/
a critical role of calpain-2 in neuronal death, Cells, 9,
ejn.15188.
2698, doi: 10.3390/cells9122698.
93.
Gądek-Michalska, A., Tadeusz, J., Rachwalska, P.,
106. Orlowski, R. Z. (1999) The role of the ubiquitin-
and Bugajski, J. (2013) Cytokines, prostaglandins
proteasome pathway in apoptosis, Cell Death Differ., 6,
and nitric oxide in the regulation of stress-response
303-313, doi: 10.1038/sj.cdd.4400505.
systems, Pharmacol. Rep., 65, 1655-1662, doi: 10.1016/
107. Laham, B. J., and Gould, E. (2022) How stress
s1734-1140(13)71527-5.
influences the dynamic plasticity of the brain’s
94.
Dheen, S. T., Kaur, C., and Ling, E. A.
(2007)
extracellular matrix, Front. Cell. Neurosci., 15, 814287,
Microglial activation and its implications in the
doi: 10.3389/fncel.2021.814287.
3
БИОХИМИЯ том 88 вып. 5 2023
722
ГУЛЯЕВА
108. Breviario, S., Senserrich, J., Florensa-Zanuy, E.,
and brain causes from consequences, Exp. Neurol.,
Garro-Martínez, E., Díaz, Á., Castro, E., Pazos, Á.,
318, 71-77, doi: 10.1016/j.expneurol.2019.04.012.
and Pilar-Cuéllar, F. (2023) Brain matrix metallo-
119. Spinelli, M., Fusco, S., and Grassi, C. (2019) Brain
proteinase-9 activity is altered in the corticosterone
insulin resistance and hippocampal plasticity: mecha-
mouse model of depression, Prog. Neuropsychophar-
nisms and biomarkers of cognitive decline, Front. Neu-
macol. Biol. Psychiatry, 120, 110624, doi: 10.1016/
rosci., 13, 788, doi: 10.3389/fnins.2019.00788.
j.pnpbp.2022.110624.
120. Irving, A., and Harvey, J. (2021) Regulation of hippo-
109. Koyama, Y. (2021) Endothelin ETB receptor-mediated
campal synaptic function by the metabolic hormone
astrocytic activation: pathological roles in brain
leptin: implications for health and disease, Prog. Lipid
disorders, Int. J. Mol. Sci., 22, 4333, doi: 10.3390/
Res., 82, 101098, doi: 10.1016/j.plipres.2021.101098.
ijms22094333.
121. McGregor, G., Malekizadeh, Y., and Harvey, J. (2015)
110. Harkness, K. A., Adamson, P., Sussman, J. D.,
Minireview: food for thought: regulation of synaptic
Davies-Jones, G. A., Greenwood, J., and Woodroofe,
function by metabolic hormones, Mol. Endocrinol., 29,
M. N. (2000) Dexamethasone regulation of matrix
3-13, doi: 10.1210/me.2014-1328.
metalloproteinase expression in CNS vascular endo-
122. Lazarov, O., Minshall, R. D., and Bonini, M. G.
thelium, Brain, 123 (Pt
4), 698-709, doi: 10.1093/
(2020) Harnessing neurogenesis in the adult brain-A
brain/123.4.698.
role in type 2 diabetes mellitus and Alzheimer’s disease,
111. Förster, C., Kahles, T., Kietz, S., and Drenckhahn, D.
Int. Rev. Neurobiol.,
155,
235-269, doi:
10.1016/
(2007) Dexamethasone induces the expression of
bs.irn.2020.03.020.
metalloproteinase inhibitor TIMP-1 in the murine
123. Detka, J., Kurek, A., Basta-Kaim, A., Kubera, M.,
cerebral vascular endothelial cell line cEND,
Lasoń, W., and Budziszewska, B. (2013) Neuroen-
J. Physiol.,
580 (Pt.
3),
937-949, doi:
10.1113/
docrine link between stress, depression and diabe-
jphysiol.2007.129007.
tes, Pharmacol. Rep., 65, 1591-1600, doi: 10.1016/
112. Hillegass, J. M., Villano, C. M., Cooper, K. R., and
s1734-1140(13)71520-2.
White, L. A. (2007) Matrix metalloproteinase-13 is
124. Doyle, T., Halaris, A., and Rao, M. (2014) Shared
required for zebra fish (Danio rerio) development and
neurobiological pathways between type 2 diabetes and
is a target for glucocorticoids, Toxicol. Sci., 100, 168-
depressive symptoms: a review of morphological and
179, doi: 10.1093/toxsci/kfm192.
neurocognitive findings, Curr. Diab. Rep., 14, 560,
113. Wang, Y., Li, M., Tang, J., Song, M., Xu, X., Xiong, J.,
doi: 10.1007/s11892-014-0560-7.
Li, J., and Bai, Y. (2011) Glucocorticoids facilitate
125. Lyra E Silva, N. M., Gonçalves, R. A., Boehnke, S. E.,
astrocytic amyloid-β peptide deposition by increas-
Forny-Germano, L., Munoz, D. P., and De Felice,
ing the expression of APP and BACE1 and decreas-
F. G. (2019) Understanding the link between insulin
ing the expression of amyloid-β-degrading prote-
resistance and Alzheimer’s disease: Insights from
ases, Endocrinology, 152, 2704-2715, doi: 10.1210/
animal models, Exp. Neurol., 316, 1-11, doi: 10.1016/
en.2011-0145.
j.expneurol.2019.03.016.
114. Hou, Y., Luo, S., Zhang, Y., Jia, Y., Li, H., Xiao, C.,
126. Yagi, S., and Galea, L. A. M. (2019) Sex differences
Bao, H., and Du, J. (2019) Contrasting effects of
in hippocampal cognition and neurogenesis,
acute and long-term corticosterone treatment on
Neuropsychopharmacology, 44, 200-213, doi: 10.1038/
amyloid-β, beta-secretase
1 expression, and nu-
s41386-018-0208-4.
clear factor kappa B nuclear translocation, J. In-
127. Koss, W. A., and Frick, K. M. (2017) Sex differences in
tegr. Neurosci.,
18,
393-400, doi:
10.31083/j.jin.
hippocampal function, J. Neurosci. Res., 95, 539-562,
2019.04.1172.
doi: 10.1002/jnr.23864.
115. Proulx, K., and Seeley, R. J. (2005) The regulation
128. Scharfman, H. E., and MacLusky, N. J. (2017) Sex
of energy balance by the central nervous system,
differences in hippocampal area CA3 pyramidal cells,
Psychiatr. Clin. North Am., 28, 25-38, doi: 10.1016/
J. Neurosci. Res., 95, 563-575, doi: 10.1002/jnr.23927.
j.psc.2004.09.005.
129. Tozzi, A., Bellingacci, L., and Pettorossi, V. E. (2020)
116. Maniam, J., and Morris, M. J. (2012) The link between
Rapid estrogenic and androgenic neurosteroids effects
stress and feeding behaviour, Neuropharmacology, 63,
in the induction of long-term synaptic changes: impli-
97-110, doi: 10.1016/j.neuropharm.2012.04.017.
cation for early memory formation, Front. Neurosci.,
117. Ferrario, C. R., and Reagan, L. P. (2018) Insulin-
14, 572511, doi: 10.3389/fnins.2020.572511.
mediated synaptic plasticity in the CNS: Anatomical,
130. Sheppard, P. A. S., Choleris, E., and Galea, L. A. M.
functional and temporal contexts, Neuropharmacology,
(2019) Structural plasticity of the hippocampus in
136 (Pt B),
182-191, doi:
10.1016/j.neuropharm.
response to estrogens in female rodents, Mol. Brain,
2017.12.001.
12, 22, doi: 10.1186/s13041-019-0442-7.
118. Grillo, C. A., Woodruff, J. L., Macht, V. A.,
131. Nicholson, K., MacLusky, N. J., and Leranth, C.
and Reagan, L. P. (2019) Insulin resistance and
(2020) Synaptic effects of estrogen, Vitam. Horm., 114,
hippocampal dysfunction: disentangling peripheral
167-210, doi: 10.1016/bs.vh.2020.06.002.
БИОХИМИЯ том 88 вып. 5 2023
ГЛЮКОКОРТИКОИДЫ
723
132. Murakami, G., Hojo, Y., Kato, A., Komatsuzaki, Y.,
142. Gulyaeva, N. V., Onufriev, M. V., and Moiseeva,
Horie, S., Soma, M., Kim, J., and Kawato, S. (2018)
Y. V. (2021) Ischemic stroke, glucocorticoids, and
Rapid nongenomic modulation by neurosteroids
remote hippocampal damage: a translational outlook
of dendritic spines in the hippocampus: androgen,
and implications for modeling, Front. Neurosci., 15,
oestrogen and corticosteroid, J. Neuroendocrinol., 30,
781964, doi: 10.3389/fnins.2021.781964.
e12561, doi: 10.1111/jne.12561.
143. Komoltsev, I. G., and Gulyaeva, N. V. (2022) Brain
133. Gall, C. M., Le, A. A., and Lynch, G. (2021) Sex
trauma, glucocorticoids and neuroinflammation:
differences in synaptic plasticity underlying learn-
dangerous liaisons for the hippocampus, Biomedicines,
ing, J. Neurosci. Res., 101, 764-782, doi: 10.1002/
10, 1139, doi: 10.3390/biomedicines10051139.
jnr.24844.
144. Komoltsev, I. G., Frankevich, S. O., Shirobokova,
134. Kramár, E. A., Babayan, A. H., Gall, C. M., and
N. I., Volkova, A. A., Onufriev, M. V., Moiseeva, J. V.,
Lynch, G. (2013) Estrogen promotes learning-relat-
Novikova, M. R., and Gulyaeva, N. V. (2021) Neu-
ed plasticity by modifying the synaptic cytoskeleton,
roinflammation and neuronal loss in the hippocampus
Neuroscience, 239, 3-16, doi: 10.1016/j.neuroscience.
are associated with immediate posttraumatic seizures
2012.10.038.
and corticosterone elevation in rats, Int. J. Mol. Sci.,
135. Harte-Hargrove, L. C., Maclusky, N. J., and
22, 5883, doi: 10.3390/ijms22115883.
Scharfman, H. E. (2013) Brain-derived neurotrophic
145. Herbert, J., and Lucassen, P. J. (2016) Depression
factor-estrogen interactions in the hippocampal mossy
as a risk factor for Alzheimer’s disease: genes,
fiber pathway: implications for normal brain function
steroids, cytokines and neurogenesis - what do we
and disease, Neuroscience, 239, 46-66, doi: 10.1016/
need to know? Front. Neuroendocrinol., 41, 153-171,
j.neuroscience.2012.12.029.
doi: 10.1016/j.yfrne.2015.12.001.
136. Deakk, T., Quinnk, M., Cidlowskik, J. A., Victoriak,
146. Linnemann, C., and Lang, U. E. (2020) Pathways
N. C., Murphyk, A. Z., and Sheridank, J. F. (2015)
connecting late-life depression and dementia, Front.
Neuroimmune mechanisms of stress: sex differences,
Pharmacol., 11, 279, doi: 10.3389/fphar.2020.00279.
developmental plasticity, and implications for pharma-
147. Gulyaeva, N. V. (2019) Biochemical mechanisms and
cotherapy of stress-related disease, Stress, 18, 367-380,
translational relevance of hippocampal vulnerability to
doi: 10.3109/10253890.2015.1053451.
distant focal brain injury: the price of stress response,
137. Kandasamyk, M., Radhakrishnank, R. K., Poornimaik
Biochemistry (Moscow), 84, 1306-1328, doi: 10.1134/
Abirami, G. P., Roshank, S. A., Yesudhask, A., Bala-
S0006297919110087.
muthuk, K., Prahalathank, C., Shanmugaapriyak, S.,
148. McEwen, B. S., and Akil, H. (2020) Revisiting the
Moorthyk, A., Essakk, M. M., and Anusuyadevik, M.
stress concept: implications for affective disorders,
(2019) Possible existence of the hypothalamic-pitu-
J. Neurosci., 40, 12-21, doi: 10.1523/JNEUROSCI.
itary-hippocampal (HPH) axis: a reciprocal relation-
0733-19.2019.
ship between hippocampal specific neuroestradiol syn-
149. Xu, W., Yao, X., Zhao, F., Zhao, H., Cheng, Z.,
thesis and neuroblastosis in ageing brains with special
Yang, W., Cui, R., Xu, S., and Li, B. (2020) Changes in
reference to menopause and neurocognitive disorders,
hippocampal plasticity in depression and therapeutic
Neurochem. Res., 44, 1781-1795, doi: 10.1007/s11064-
approaches influencing these changes, Neural Plast.,
019-02833-1.
2020, 8861903, doi: 10.1155/2020/8861903.
138. Resmini, E., Santos, A., and Webb, S. M. (2016)
150. Sotiropoulos, I., Silva, J. M., Gomes, P., Sousa, N.,
Cortisol excess and the brain, Front. Horm. Res., 46,
and Almeida, O. F. X. (2019) Stress and the etio-
74-86, doi: 10.1159/000443868.
pathogenesis of Alzheimer’s disease and depression,
139. Hill, A. R., and Spencer-Segal, J. L. (2021) Glucocor-
Adv. Exp. Med. Biol., 1184, 241-257, doi: 10.1007/
ticoids and the brain after critical illness, Endocrinolo-
978-981-32-9358-8_20.
gy, 162, bqaa242, doi: 10.1210/endocr/bqaa242.
151. Meyer, M., Lara, A., Hunt, H., Belanoff, J., de Kloet,
140. Druzhkova, T. A., Yakovlev, A. A., Rider, F. K.,
E. R., Gonzalez Deniselle, M. C., and De Nicola,
Zinchuk, M. S., Guekht, A. B., and Gulyaeva, N. V.
A. F. (2018) The selective glucocorticoid receptor
(2022) Elevated serum cortisol levels in patients with
modulator cort
113176 reduces neurodegeneration
focal epilepsy, depression, and comorbid epilepsy and
and neuroinflammation in wobbler mice spinal
depression, Int. J. Mol. Sci., 23, 10414, doi: 10.3390/
cord, Neuroscience,
384,
384-396, doi:
10.1016/
ijms231810414.
j.neuroscience.2018.05.042.
141. Zhanina, M. Y., Druzhkova, T. A., Yakovlev, A. A.,
152. Dalm, S., Karssen, A. M., Meijer, O. C., Belanoff,
Vladimirova, E. E., Freiman, S. V., Eremina, N. N.,
J. K., and de Kloet, E. R. (2019) Resetting the
Guekht, A. B., and Gulyaeva, N. V. (2022) Devel-
stress system with a mifepristone challenge, Cell.
opment of post-stroke cognitive and depressive dis-
Mol. Neurobiol., 39, 503-522, doi: 10.1007/s10571-
turbances: associations with neurohumoral indices,
018-0614-5.
Curr. Issues Mol. Biol., 44, 6290-6305, doi: 10.3390/
153. De Kloet, E. R., de Kloet, S. F., de Kloet, C. S.,
cimb44120429.
and de Kloet, A. D. (2019) Top-down and bottom-
БИОХИМИЯ том 88 вып. 5 2023
3*
724
ГУЛЯЕВА
up control of stress-coping, J. Neuroendocrinol., 31,
CORT113176 in murine motoneuron degeneration,
e12675, doi: 10.1111/jne.12675.
Brain Res., 1727, 146551, doi: 10.1016/j.brainres.2019.
154. De Nicola, A. F., Meyer, M., Guennoun, R.,
146551.31726042.
Schumacher, M., Hunt, H., Belanoff, J., de Kloet,
156. De Kloet, E. R., and Joëls, M. (2023) The cortisol
E. R., and Gonzalez Deniselle, M. C. (2020) Insights
switch between vulnerability and resilience, Mol.
into the therapeutic potential of glucocorticoid
Psychiatry, doi: 10.1038/s41380-022-01934-8.
receptor modulators for neurodegenerative diseases,
157. Daskalakis, N. P., Meijer, O. C., and de Kloet, E. R.
Int. J. Mol. Sci., 21, 2137, doi: 10.3390/ijms21062137.
(2022) Mineralocorticoid receptor and glucocorticoid
155. Meyer, M., Kruse, M. S., Garay, L., Lima, A., Roig, P.,
receptor work alone and together in cell-type-specific
Hunt, H., Belanoff, J., de Kloet, E. R., Deniselle,
manner: implications for resilience prediction and
M. C. G., and De Nicola, A. F. (2020) Long-term
targeted therapy, Neurobiol. Stress,
18,
100455,
effects of the glucocorticoid receptor modulator
doi: 10.1016/j.ynstr.2022.100455.
GLUCOCORTICOIDS ORCHESTRATE
ADULT HIPPOCAMPAL PLASTICITY:
GROWING POINTS AND TRANSLATIONAL ASPECTS
Review
N. V. Gulyaeva1,2
1 Institute of Higher Nervous Activity and Neurophysiology, Russian Academy of Sciences,
117485 Moscow, Russia; e-mail: nata_gul@ihna.ru
2 Research and Clinical Center for Neuropsychiatry of Moscow Healthcare Department, 115419 Moscow, Russia
The review analyzes modern concepts regarding the control of various mechanisms of the hippocampal
neuroplasticity in adult mammals and humans by glucocorticoids. Glucocorticoid hormones ensure the
coordinated functioning of key components and mechanisms of hippocampal plasticity: neurogenesis,
glutamatergic neurotransmission, microglia and astrocytes, systems of neurotrophic factors, neuroinflam-
mation, protease activities, metabolic hormones, neurosteroids. Regulatory mechanisms are diverse; along
with the direct action of glucocorticoids through their receptors, there are indirect glucocorticoid-depend-
ent effects, as well as numerous interactions between various systems and components. Despite the fact that
many connections in this complex regulatory scheme have not yet been established, the study of the factors
and mechanisms considered in the review forms growth points in the field of glucocorticoid-regulated pro-
cesses in the brain and primarily in the hippocampus. These studies are fundamentally important for the
translation into the clinic and the potential treatment/prevention of common diseases of the emotional and
cognitive spheres and respective comorbid conditions.
Keywords: neuroplasticity, hippocampus, glucocorticoids, hypothalamic-pituitary-adrenal axis, synaptic plasticity,
stress, neurogenesis, neuroinflammation, glutamatergic transmission, proteases, BDNF, insulin resistance,
depression, Alzheimer’s disease, aging
БИОХИМИЯ том 88 вып. 5 2023