БИОХИМИЯ, 2023, том 88, вып. 8, с. 1366 - 1377
УДК 57.016
ГИБРИДНЫЕ ИМПЛАНТАТЫ НА ОСНОВЕ
КАЛЬЦИЙ-МАГНИЕВОЙ СИЛИКАТНОЙ
КЕРАМИКИ ДИОПСИДА В КАЧЕСТВЕ НОСИТЕЛЯ
РЕКОМБИНАНТНОГО BMP-2
И ДЕМИНЕРАЛИЗОВАННОГО КОСТНОГО МАТРИКСА
В КАЧЕСТВЕ КАРКАСА: ЭКТОПИЧЕСКИЙ ОСТЕОГЕНЕЗ
ПРИ ВНУТРИМЫШЕЧНОЙ ИМПЛАНТАЦИИ У МЫШЕЙ
© 2023 А.С. Карягина1,2,3*, П.А. Орлова1, А.В. Жулина1, М.С. Кривозубов1,
Т.М. Грунина1,3, Н.В. Струкова1, К.Е. Никитин1, В.Н. Манских1,2,
Ф.С. Сенатов1,4, А.В. Громов1*
1 Национальный исследовательский центр эпидемиологии
и микробиологии им. Н.Ф. Гамалеи Минздрава России, 123098 Москва, Россия;
электронная почта: akaryagina@gmail.com, alexander.v.gromov@gmail.com
2 НИИ физико-химической биологии имени А.Н. Белозерского,
Московский государственный университет имени М.В. Ломоносова, 119992 Москва, Россия
3 Всероссийский научно-исследовательский институт сельскохозяйственной биотехнологии,
127550 Москва, Россия
4 Национальный исследовательский технологический университет «МИСИС»,
119049 Москва, Россия
Поступила в редакцию 14.06.2023
После доработки 05.07.2023
Принята к публикации 06.07.2023
Высокая эффективность гибридных имплантатов на основе кальций-магниевой силикатной ке-
рамики диопсида в качестве носителя рекомбинантного костного морфогенетического белка-2
(BMP-2) и ксеногенного деминерализованного костного матрикса (ДКМ) в качестве каркасного
материала для регенерации костной ткани была продемонстрирована ранее на модели краниаль-
ных дефектов критического размера у мышей. С целью изучения возможности применения этих
имплантатов для выращивания аутологичной костной ткани с использованием принципа in vivo
биореактора в теле самого пациента проведено исследование эффективности вызываемого ими
эктопического остеогенеза при внутримышечной имплантации мышам. При дозе BMP-2 в 7 мкг
на имплантат через 1 неделю вокруг имплантатов наблюдалось плотное скопление клеток, веро-
ятно, сателлитных клеток-предшественников скелетной мускулатуры, с участками интенсивного
хондрогенеза, начальной стадии непрямого остеогенеза. Через 12 недель формировалась плотная
костная капсула трабекулярного строения, покрытая надкостницей, со зрелым костным мозгом,
расположенным в промежутках между трабекулами. Объём капсулы приблизительно в 8-10 раз
превышал объём исходного имплантата. Признаки воспалительной и клеточной реакции на вве-
дение инородного тела в группе с BMP-2 практически отсутствовали. Данные микрокомпьютер-
ной томографии показали значительно бóльшие относительный объём костной ткани, количе-
ство трабекул и плотность костной ткани в группе c BMP-2 по сравнению с группой без BMP-2.
С учётом того, что ДКМ может быть получен практически в неограниченных количествах, требуе-
мого размера и формы, а используемый BMP-2, получаемый синтезом в клетках E. coli, относи-
тельно недорог, дальнейшая разработка модели in vivo биореактора на основе гибридных имплан-
татов из BMP-2, диопсида и ксеногенного ДКМ представляется перспективной.
КЛЮЧЕВЫЕ СЛОВА: диопсид, кальций-магниевая силикатная керамика, имплантат, BMP-2, деминера-
лизованный костный матрикс, эктопический остеогенез.
DOI: 10.31857/S0320972523080067, EDN: IJYNDL
Принятые сокращения: ГК - гиалуроновая кислота; ДКМ - деминерализованный костный матрикс; микроКТ -
микрокомпьютерная томография; BMP-2 - bone morphogenetic protein-2, костный морфогенетический белок-2.
* Адресат для корреспонденции.
1366
ИМПЛАНТАТЫ ИЗ ДКМ, ДИОПСИДА И BMP-2
1367
ВВЕДЕНИЕ
двумя другими, в частности, она практически
так же удобна в плане хирургической техни-
Восстановление крупных костных дефек-
ки, как подкожная имплантация, значительно
тов, вызванных травмой, остеопорозом, уда-
более проста по сравнению с имплантацией в
лением опухоли или остеомиелитом, является
почечную капсулу и при этом полностью пере-
одной из сложнейших задач реконструктивной
носима на крупных лабораторных животных и
хирургии [1, 2]. Золотым стандартом лечения
человека. По сравнению с подкожной внутри-
при этом является аутотрансплантация соб-
мышечная имплантация, как правило, обеспе-
ственной костной ткани, забираемой обычно
чивает более выраженное и более раннее обра-
из подвздошной кости пациента, которая,
зование костной ткани [15], что может быть
однако, имеет много проблем, таких как боли
связано с лучшим кровоснабжением мышеч-
в месте забора материала, а также ограничен-
ной ткани, а также наличием в скелетных мыш-
ность объёма аутотрансплантата [3, 4]. Возмож-
цах сателлитных клеток-предшественников,
ной альтернативой при этом является выра-
способных к остеогенной дифференцировке
щивание аутологичных костных имплантатов
под действием соответствующих индукторов,
с использованием так называемого принципа
например, костных морфогенетических бел-
in vivo биореактора, заключающегося в том,
ков (bone morphogenetic proteins, BMPs) [14].
что биореактором служит тело самого паци-
Так, в исследовании, проведённом на собаках
ента [5]. При этом можно вырастить кость
и свиньях, при внутримышечной имплантации
нужной формы и размера, например, в мыш-
образование костной ткани наблюдалось уже
це спины или живота, используя подходящий
через 45 дней, в то время как при подкожной
каркас и остеоиндуктивные факторы, а затем
имплантации - только через 60 дней [16]. С по-
трансплантировать её в нужное место. В на-
мощью внутримышечной имплантации была
стоящее время имеется более сотни публика-
успешно выращена костная ткань для замеще-
ций с описанием эктопического наращива-
ния крупных челюстных дефектов у человека.
ния кости в мелких (мыши, крысы, кролики)
Например, в 2004 г. опубликована работа,
и крупных (бараны, свиньи, обезьяны, козы,
описывающая выращивание костной ткани в
собаки) лабораторных животных. Также опуб-
мышце пациента с использованием аутологич-
ликованы статьи, описывающие клинические
ного костного мозга и BMP-7 [7]. Собственно,
случаи, в основном касающиеся восполнения
именно на модели внутримышечной имплан-
крупных челюстных дефектов у людей, на ос-
тации была показана способность BMPs инду-
нове этого подхода [6-13].
цировать эктопический остеогенез [17].
Для достижения успеха при разработке но-
Существенным моментом при разработ-
вой модели in vivo биореактора требуется под-
ке модели in vivo биореактора является выбор
бор комбинации целого ряда факторов, спо-
каркасного материала, который должен слу-
собствующих формированию зрелой костной
жить матрицей для наращивания собственной
ткани в эктопическом сайте: существенным яв-
кости. Желательно, чтобы такой материал был
ляется выбор лабораторного животного, модели
достаточно жёстким, но эластичным, прибли-
имплантации, каркасного материала, обеспе-
женным по свойствам к костной ткани. Так-
чивающего требуемую форму кости, носителя
же материал должен быть биосовместимым и
индуктора остеогенеза и собственно индукто-
биорезорбируемым, обеспечивая постепенное
ра остеогенеза.
замещение его новой костной тканью. Одним
Наиболее экономичными среди лаборатор-
из материалов, удовлетворяющих требуемым
ных животных с точки зрения закупочной цены
параметрам, является высокоочищенный ксе-
и стоимости содержания являются мыши. По-
ногенный деминерализованный костный ма-
этому их использование представляется целе-
трикс (ДКМ), получаемый из костей крупного
сообразным для первоначальной отработки мо-
рогатого скота [18]. ДКМ обладает высокой
дели с целью последующего переноса на более
остеокондуктивностью, его можно получить в
крупных лабораторных животных и человека.
большом количестве, из него могут быть полу-
Чрезвычайно важным является выбор мо-
чены объёмные имплантаты требуемой формы,
дели имплантации. В настоящее время наи-
по механическим свойствам и пористости,
более часто используемыми являются модель
включая микропористость, он максимально
подкожной имплантации, имплантации в мы-
приближен к костной ткани человека. Кроме
шечный карман (внутримышечная импланта-
того, возможно получение низкоиммуногенно-
ция) и имплантации в почечную капсулу [14].
го ДКМ, обладающего повышенной биосовме-
При этом модель внутримышечной имплан-
стимостью и пониженной аллергенностью за
тации имеет ряд преимуществ по сравнению с
счёт сниженного содержания неколлагеновых
БИОХИМИЯ том 88 вып. 8 2023
1
368
КАРЯГИНА и др.
белков [19, 20]. Ограниченная остеоиндуктив-
соответствовал стандартной карточке ICDD
ность ДКМ может быть преодолена за счёт
№ 01-075-1092 с небольшой примесью вторич-
его совместного применения с экзогенными
ной фазы - акерманита [23].
индукторами остеогенеза, например, реком-
Получение пористых каркасов для имплан-
бинантным костным морфогенетическим бел-
татов из ДКМ. Высокоочищенный ксеноген-
ком-2 (BMP-2) [19, 21]. При введении в орга-
ный ДКМ получали по ранее описанной мето-
низм BMP-2 обеспечивает привлечение из
дике из эпифизов бедренных костей крупного
окружающих тканей и остеогенную дифферен-
рогатого скота [25]. Имплантаты, представ-
цировку мезенхимальных стволовых клеток, а
ляющие собой диски диаметром 4 мм и тол-
также обладает ангиогенными свойствами, что
щиной 1 мм, изготавливали из костных плас-
важно для образования полноценной костной
тин с помощью металлического пробойника.
ткани с хорошим кровоснабжением [22]. ДКМ
Для стерилизации диски ДКМ выдерживали в
сам по себе может выступать в качестве носи-
96%-ном спирте в течение 1 ч, отмывали сте-
теля BMP-2, однако его сорбционная ёмкость
рильным PBS и высушивали в ламинарном
ограничена [23]. Для возможности введения
шкафу с ультрафиолетом в течение ночи.
больших и регулируемых доз BMP-2, а также
Насыщение порошка диопсида BMP-2. Ре-
обеспечения более постепенного выхода белка
комбинантный BMP-2, полученный синтезом
на основе ДКМ в качестве каркасного мате-
в клетках Escherichia coli и очищенный, как
риала разработаны гибридные имплантаты, в
описано ранее [26], с удельной активностью
которых функцию носителя BMP-2 выполняют
0,1 Ед./мкг иммобилизовывали на порошке
взвешенные в гиалуроновой кислоте (ГК) ча-
диопсида, как описано ранее [23]. Кратко,
стицы кальций-магниевой силикатной керами-
50 мг порошка диопсида выдерживали 30 мин
ки диопсида, обладающей очень высокой сорб-
в 10 мM натрий-фосфатном буфере (рН 5,5) с
ционной ёмкостью по отношению к BMP-2,
50 мM NaCl, центрифугировали, раствор уда-
во много раз превышающую ёмкость гидр-
ляли, осадок суспендировали в том же рас-
оксилапатита. Такие имплантаты продемон-
творе, содержащем 500 или 1000 мкг BMP-2,
стрировали высокую остеогенность на модели
и инкубировали в течение 2 ч. Несвязавший-
краниальных дефектов критического размера у
ся белок удаляли после центрифугирования,
мышей [23].
осадок трижды промывали тем же буфером
Целью данного исследования является раз-
без белка.
работка модели эктопического наращивания
Подготовка образцов для имплантации. Для
трабекулярной костной ткани на основе прин-
приготовления 5%-ной (w/v) суспензии диоп-
ципа in vivo биореактора при внутримышечной
сида в ГК 50 мг порошка диопсида (с 10 или
имплантации мыши гибридных имплантатов
20 мкг/мг BMP-2 или без него) в 250 мкл сте-
с ксеногенным ДКМ в качестве каркасного
рильного физраствора добавляли к
750 мл
материала и кальций-магниевой силикатной
2%-ной ГК (~100 кДа, «Shanghai Macklin Bio-
керамикой диопсидом в качестве носителя ре-
chemical Industry Co., Ltd.», Китай) в физрас-
комбинантного BMP-2.
творе и тщательно перемешивали. Непосред-
ственно перед имплантацией простерилизо-
ванные диски ДКМ погружали в предвари-
МАТЕРИАЛЫ И МЕТОДЫ
тельно ещё раз перемешанную суспензию.
Один диск впитывал примерно 7 мкл суспен-
Получение порошка диопсида. В работе ис-
зии и содержал около 0,35 мг диопсида и 3,5
пользовали порошок диопсида (CaMgSi2O6),
или 7 мкг BMP-2.
синтезированный твердофазным методом по
Имплантация. Провели 2 эксперимента на
ранее опубликованной методике [24] с моди-
самцах аутбредных мышей линии ICR (CD-1)
фикациями [23]. Кратко, в качестве источника
возраста 38-47 дней. Первый - пилотный -
кальция использовали яичную скорлупу, ис-
проводился на 24 мышах, которых случайным
точника кремния - рисовую шелуху, получая
образом разделили на две группы по 12 мы-
на её основе с помощью прогревания диоксид
шей. Первой группе имплантировали диски
кремния. Измельчённую яичную скорлупу,
из ДКМ с суспензией частиц диопсида, не
диоксид кремния и синтетический оксид маг-
содержащих BMP-2, второй группе - диски с
ния («Русхим», Россия) смешивали в соот-
суспензией частиц, содержащих около 3,5 мкг
ношении 1 : 2 : 1 в планетарной шаровой мель-
BMP-2 на диск. Каждому животному вводили
нице Fritsch Pulverisette
5
(«Fritsch GmbH»,
по 2 идентичных имплантата - в левое и правое
Германия) и выдерживали при температуре
бедро. Второй эксперимент проводили анало-
1100 °C в течение 6 ч. Полученный диопсид
гично первому, но использовали 16 мышей,
БИОХИМИЯ том 88 вып. 8 2023
ИМПЛАНТАТЫ ИЗ ДКМ, ДИОПСИДА И BMP-2
1369
разделённых на две группы по 8 мышей. В пер-
и быстрым зелёным FCF [27] и азаном по Гей-
вой группе вводили имплантаты без белка, во
денгайну [28].
второй количество BMP-2 составляло 7 мкг на
Микрокомпьютерная томография. МикроКТ
диск. В обоих случаях операцию проводили
образцов проводили ex vivo на томографе
на термостатируемом хирургическом столике
SkyScan 1172 («Bruker», США) с помощью про-
(«Medax», Германия) при температуре 37 °С.
грамм NRecon и CTAn с подбором парамет-
Подготовив хирургическое поле, в каудальной
ров, позволяющих отличить минерализованную
части бедра производили кожный разрез, далее
костную ткань от других тканей.
формировали карманы в ягодичных мышцах
Статистическая обработка данных микро-
тупым методом, после чего в них закладывали
КТ проводилась с использованием пакета про-
имплантаты, ткани послойно ушивали атрав-
грамм Statistica 12.0 («Statsoft», США). Проверку
матическим шовным материалом Mepfil № 4/0
на нормальность проводили с помощью теста
и обрабатывали антибиотиком «Террамицин»
Колмогорова-Смирнова. Для оценки досто-
(«Pfizer Animal Health», США). В первом экс-
верности отличий проводили анализ с при-
перименте эвтаназию углекислым газом про-
менением критерия Манна-Уитни. Различия
водили на 7, 24, 63 и 84 сутки трём мышам из
считались значимыми при р < 0,05.
каждой группы. Во втором - на 7 сутки двум
мышам, на 84 - шести мышам из каждой груп-
пы. Гистологический анализ образцов, извле-
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
чённых из мышей после эвтаназии, проводили
на сроке 1 и 12 недель с начала эксперимента;
Дизайн эксперимента. В пилотном экспе-
микрокомпьютерную томографию (микроКТ) -
рименте по внутримышечной имплантации
на сроке 12 недель.
мышам дисков из ДКМ, содержащих суспен-
Гистологический анализ. Образцы, вклю-
зию порошка диопсида в ГК, в опытной груп-
чающие область имплантации и окружающие
пе использовали BMP-2 в количестве около
ткани, извлекали из бедренных мышц, фик-
3,5 мкг на имплантат, как в ранее описанном
сировали забуференным нейтральным фор-
исследовании по имплантации в краниальные
малином в течение 24 ч, декальцинировали
дефекты мышей [23], в которых за 9 недель
в 14%-ном растворе ЭДТА, отмывали и про-
происходило практически полное заполнение
водили через батарею спиртов возрастающей
пор имплантата новообразованной костной
концентрации и заливали в парафин. Срезы
тканью с костным мозгом и ремоделирование
толщиной 3 мкм окрашивали гематоксилином
матрикса ДКМ. На 1, 4, 9 и 12 неделях гисто-
и эозином, Сафранином О, гематоксилином
логический анализ выявил картину непрямого
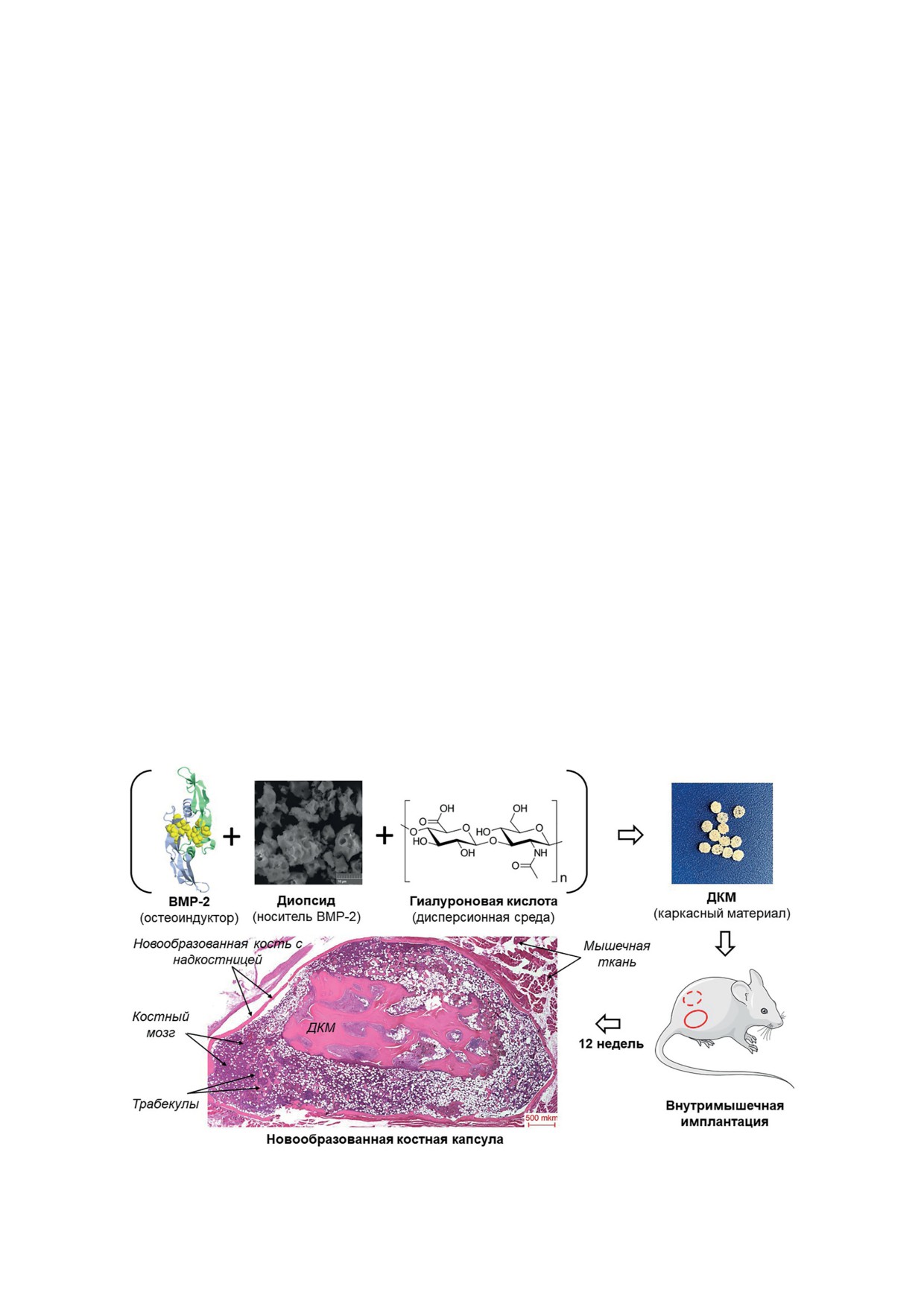
Рис. 1. Дизайн эксперимента по внутримышечной имплантации мышам гибридных имплантатов из ДКМ и взвеси
частиц диопсида с адсорбированным BMP-2 в ГК
БИОХИМИЯ том 88 вып. 8 2023
1370
КАРЯГИНА и др.
эктопического остеогенеза с формированием
это не сопровождалось появлением ново-
через 1 неделю хрящевой ткани, а на более
образованной костной ткани (рис. 3, а, 4-6,
поздних сроках - костной структуры, похожей
рис. 4, а, 4-6).
по строению на трабекулярную кость, которая
В присутствии BMP-2 через 12 недель по
к 12 неделе у некоторых животных оказалась
данным микроКТ во всех образцах наблю-
покрыта слоем костной ткани с надкостницей
далась крупная, сильно минерализованная
(данные не приводятся). По результатам этого
костная капсула (рис. 2, а), значительно пре-
эксперимента было решено общий дизайн ос-
вышающая по объёму (в 8-10 раз) первона-
новного эксперимента оставить неизменным
чальный имплантат, с выраженной трабе-
(рис. 1), но увеличить в два раза количество
кулярной структурой (рис. 2, в). Параметры
BMP-2, гистологический анализ проводить
BV/TV (относительный объём костной ткани),
на 1 и 12 неделе, микроКТ - на 12 неделе.
Tb.Th (толщина трабекул), Tb.N (количество
Оценка результатов внутримышечной им-
трабекул) и BMD (плотность костной ткани)
плантации гибридных имплантатов с помощью
в группе с BMP-2 достоверно различаются
микроКТ и гистологического анализа. Данные
(в бóльшую сторону) с группой без BMP-2
по микроКТ образцов, полученных через 12 не-
(p < 0,05) (рис. 2, б).
дель после проведения внутримышечной им-
Согласно гистологическому исследова-
плантации гибридных имплантатов из ДКМ,
нию, в группе без BMP-2 через одну неделю
ГК и диопсида, содержащих и не содержащих
после имплантации диск был окружён молодой
BMP-2, представлены на рис. 2. Присутствие
грануляционной тканью (рис. 3, а, 1-3). Во-
частиц диопсида без BMP-2 в ряде образ-
круг частиц диопсида обнаруживались скоп-
цов индуцировало формирование объёмной
ления эпителиоидных клеток (рис. 4, а, 1-3).
сетки минерализации, соответствующей по
Через 12 недель диск был окружён и запол-
форме макропорам диска из ДКМ (рис. 2, а).
нен хорошо организованной фиброзной тка-
Однако по данным гистологического анализа
нью (рис. 3, а, 4-6). Вокруг частиц диопсида
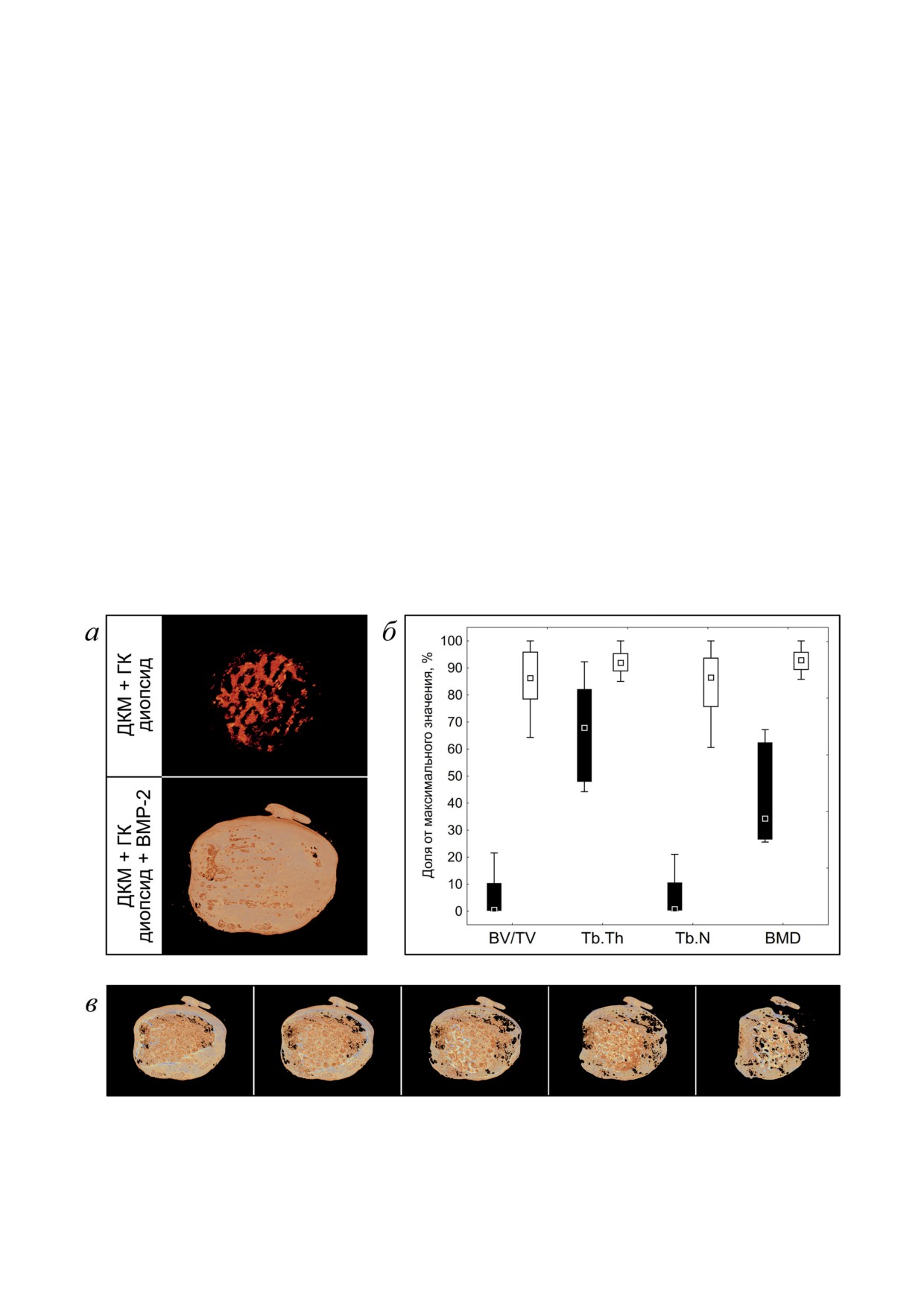
Рис. 2. Результаты микроКТ образцов, извлечённых через 12 недель после внутримышечной имплантации. a - Ви-
зуализация участков минерализации. б - Выраженность относительного объёма костной ткани (BV/TV), количества
трабекул (Tb.N), толщины трабекул (Tb.Th) и плотности костной ткани (BMD) в группах без (чёрные прямоуголь-
ники) и с (незакрашенные прямоугольники) BMP-2. в - Последовательные поперечные срезы при 3D-визуализации
результатов микроКТ костной капсулы из группы с BMP-2
БИОХИМИЯ том 88 вып. 8 2023
ИМПЛАНТАТЫ ИЗ ДКМ, ДИОПСИДА И BMP-2
1371
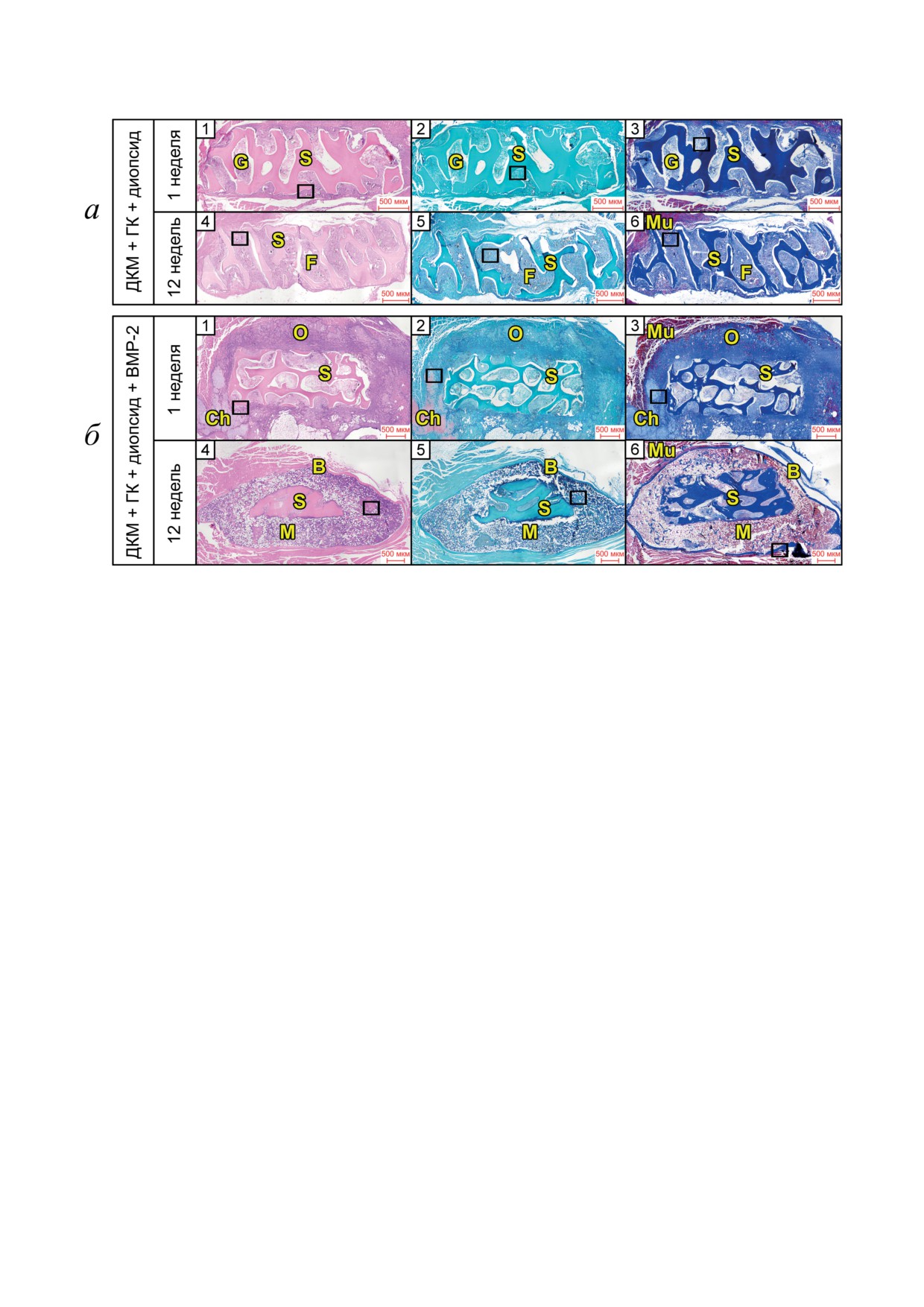
Рис. 3. Гистологический анализ образцов, полученных в результате имплантации в бедренную мышцу мышей гибрид-
ных имплантатов из ДКМ, диопсида и ГК, не содержащих (а) и содержащих (б) BMP-2. а, б: Слева - окраска ге-
матоксилином и эозином, по центру - Сафранином О, гематоксилином и быстрым зелёным FCF, справа - азаном
по Гейденгайну. Увеличение 10×. Обозначения: B - новообразованная костная ткань, трабекулы, Ch - хондроциты,
F - фиброз, G - грануляционная ткань, M - костный мозг, Mu - мышечная ткань, O - остеопрогениторные клет-
ки, S - скаффолд ДКМ. Чёрными прямоугольниками обозначены области, соответствующие областям, показанным
при большем увеличении на рис. 4
наблюдалось присутствие гигантских много-
хорошо видно при окраске по Гейденгайну,
ядерных клеток инородных тел, а также кол-
где синим цветом окрашиваются коллагенсо-
лагенизация и фиброзирование гранулематоз-
держащие структуры (рис. 3, б, 6; рис. 4, б, 6).
ных узелков/очагов воспаления без признаков
На большом увеличении можно наблюдать вклю-
неоостеогенеза (рис. 4, а, 4-6).
чение частиц диопсида в новообразованную
В группе с BMP-2 начальные признаки
костную ткань (рис. 4, б, 4, 5), которую можно
остеогенеза появлялись уже через неделю по-
отличить от деминерализованной кости кар-
сле имплантации: вокруг имплантата наблю-
касного материала по присутствию остеоцитов.
дались обширные зоны хондрогенеза (окра-
шиваемые Сафранином О в красный цвет) в
окружении многочисленных остеопрогенитор-
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
ных клеток, вероятно, образовавшихся из пула
нативных скелетных прогениторных клеток
По результатам микроКТ области имплан-
(рис. 3, б, 1-3). При большем увеличении на-
тации выраженная минерализация тканей
блюдаются резидуальные хондроидные клетки,
наблюдается как в случае образцов с BMP-2,
замещающиеся на клетки с признаками остео-
так и без него (рис. 2). В отсутствие BMP-2
цитов, которые погружены в матрикс, не даю-
через 12 недель после имплантации минерали-
щий положительной реакции на Сафранин О
зованные участки располагаются в открытых
(рис. 4, б, 1-3). Через 12 недель имплантат
порах скаффолда ДКМ, образуя характерную
окружён костной капсулой, значительно пре-
сетку (рис. 2, а), однако это не сопровожда-
вышающей размеры имплантата, весь объём
ется появлением новообразованной костной
которой заполнен преимущественно костным
ткани
- на гистологических срезах видно
мозгом с адипоцитами и тонкими костными
присутствие в порах имплантатов фиброзной
трабекулами (рис. 3, б, 4-6). Наружный слой
ткани (рис. 4, а, 4-6). Наблюдаемые рентге-
капсулы представлен плотной новообразо-
ноконтрастные участки, по-видимому, соот-
ванной костью, покрытой надкостницей, что
ветствуют кальциевым депозитам на частицах
БИОХИМИЯ том 88 вып. 8 2023
1372
КАРЯГИНА и др.
Рис. 4. Гистологический анализ образцов, полученных в результате имплантации в бедренную мышцу мышей ги-
бридных имплантатов из ДКМ, диопсида и ГК, не содержащих (а) и содержащих (б) BMP-2. а, б: Слева - окраска
гематоксилином и эозином, по центру - Сафранином О, гематоксилином и быстрым зелёным FCF, справа - азаном
по Гейденгайну. Увеличение 40×. Обозначения: A - адипоциты, B - новообразованная костная ткань, трабекулы,
Ch - хондроциты, Os - клетки с признаками остеоцитов, Ob - остеобласты, D - диопсид, F - фиброз, G - грану-
ляционная ткань, M - костный мозг, Mu - мышечная ткань, P - надкостница, S - скаффолд ДКМ. Чёрной стрелкой
обозначены остеоциты в новообразованной костной ткани, зелёными стрелками - эпителиоидные клетки, жёлтыми
стрелками - гигантские клетки инородных тел
диопсида, появляющимся в результате харак-
что свидетельствует об оптимальном подборе
терной для диопсида биоминерализации
-
компонентов имплантата, в частности, носи-
образования поверхностного слоя апатита при
теля BMP-2. Выбор носителя для BMP-2 очень
инкубации в организме или в SBF (simulated
существенен для успешного формирования
body fluid, раствор, имитирующий внеклеточ-
эктопической костной ткани. Так, в случае
ную жидкость организма) [29]. Таким образом,
использования в качестве носителя BMP-2
диопсид, обладая способностью к биоминера-
β-трикальцийфосфата наблюдалось образова-
лизации, тем не менее не способен сам по себе
ние эктопической кости при внутримышечной
индуцировать остеогенез.
имплантации крысам [30], в то же время при
В присутствии BMP-2 наблюдается фор-
использовании гидроксилапатита лишь допол-
мирование замкнутой костной капсулы, по-
нительное введение в имплантат коллагена
крытой надкостницей, с развитой системой
привело к образованию костной ткани [17].
трабекул, построенных из новообразованной
Выраженная способность диопсида к био-
костной ткани, промежутки между которыми
минерализации может приводить к усилению
заполнены зрелым костным мозгом. Таким
остеогенеза в окрестности частиц диопсида в
образом, разработанный нами имплантат при
присутствии остеоиндуктора вследствие созда-
введении в мышцу приводит к образованию
ния высокой локальной концентрации ионов
полностью сформированной аутогенной кост-
кальция в месте имплантации. Это может быть
ной структуры, готовой к аутотрансплантации,
дополнительным фактором, обеспечивающим
БИОХИМИЯ том 88 вып. 8 2023
ИМПЛАНТАТЫ ИЗ ДКМ, ДИОПСИДА И BMP-2
1373
выраженность эктопического остеогенеза в
происходит. При этом в случае введения ана-
данном эксперименте, а также ортотопиче-
логичного имплантата в краниальные дефек-
ского остеогенеза в ранее проведённом экспе-
ты критического размера у мышей уже через
рименте по имплантации ДКМ и диопсида с
9 недель с начала эксперимента и при вдвое
BMP-2 в краниальные дефекты критического
меньшем количестве BMP-2 наблюдалось
размера у мышей [23]. В пользу перспектив-
практически полное ремоделирование ДКМ с
ности применения диопсида в качестве носи-
формированием новообразованной костной
теля BMP-2 свидетельствует также то обстоя-
ткани с включёнными в неё остеоцитами [23].
тельство, что в отсутствие BMP-2 в области
Разная скорость ремоделирования может быть
имплантации наблюдается умеренно выражен-
обусловлена различными причинами, в част-
ная воспалительная и клеточная реакция на
ности, вариациями в интенсивности и путях
введение имплантата, не превышающая обыч-
остеогенеза из-за разного происхождения остео-
ную реакцию на введение остеопластических
прогениторных клеток: в случае ортотопиче-
материалов, содержащих ДКМ и частицы ке-
ского остеогенеза это мезенхимальные стро-
рамики. При этом такая реакция значительно
мальные стволовые клетки костного мозга
снижена на фоне присутствия BMP-2.
материнской кости и периоста (надкостницы),
Нас интересовала не только возможность
в случае же эктопического остеогенеза в мы-
получения эктопической кости, но и характе-
шечном кармане - сателлитные клетки-пред-
ристика ранних и поздних стадий остеогене-
шественники скелетной мускулатуры
[14].
за, включая структуру и качество получаемой
Представляет интерес исследование судьбы
костной ткани. В связи с этим были проведены
такого имплантата на более поздних сроках.
микроКТ и детальный гистологический анализ
В перспективе можно предположить полную
с тремя окрасками на разном увеличении, по-
перестройку с замещением ксеногенного кост-
зволивший оценить на двух сроках как общую
ного матрикса аутогенной костью за счёт под-
картину, наблюдающуюся при имплантации,
ключения в качестве источника остеопрогени-
так и явления, происходящие на клеточном
торных клеток периоста костной капсулы.
уровне. Картина, наблюдаемая в присутствии
Рекомбинантный BMP-2, используемый
BMP-2, соответствует непрямому остеогенезу,
в эксперименте, был синтезирован в клетках
проходящему с образованием на раннем сроке
E. coli [26]. Высокая остеогенная активность
хрящевой ткани. Структуры, подобные обра-
данного белка показана при совместном при-
зующейся на позднем сроке костной капсуле
менении с различными природными и синтети-
с трабекулярной структурой (подобие корти-
ческими материалами [21, 31-36]. Этот вариант
кальной и губчатой кости), достаточно редко
BMP-2 способен самопроизвольно сорбиро-
наблюдаются в исследованиях по эктопическо-
ваться на частицах диопсида в количестве бо-
му остеогенезу. Возможно, это связано с мень-
лее 150 мкг/мг, демонстрируя постоянный вы-
шей остеогенностью используемых материа-
ход на протяжении нескольких дней [23], что
лов, использованием более жёстких моделей
делает данную комбинацию «остеоиндуктор -
эктопического остеогенеза, а также тем, что во
носитель» очень привлекательной для исполь-
многих случаях исследователей интересует сам
зования в экспериментах по регенерации
факт возможности эктопического остеогенеза
костных дефектов. В данном исследовании мы
с использованием тех или иных материалов,
подобрали дозу BMP-2 в 7 мкг на имплантат,
и сроки эксперимента, как правило, относи-
обеспечивающую эффективный эктопический
тельно небольшие.
остеогенез с образованием трабекулярной ко-
Интересно проследить судьбу ксеноген-
сти. Следует отметить, что обычно доза BMP-2,
ного костного матрикса, выступающего в ка-
используемая в экспериментах по эктопиче-
честве скаффолда в используемых импланта-
скому остеогенезу, в особенности на крупных
тах. Через 12 недель исходный скаффолд ДКМ
животных, существенно выше [17, 35], кроме
всё ещё присутствует внутри капсулы, однако
того, как правило, используется коммерческий
наблюдается ремоделирование его верхних
BMP-2, синтезируемый в клетках китайского
слоёв с образованием новой костной ткани с
хомячка, что заведомо будет определять очень
лакунами, включающими остеоциты. Отно-
высокую стоимость получения аутологичной
сительная толщина трабекул скаффолда ДКМ
кости на основе принципа in vivo биореактора
к 12 неделям существенно увеличивается, что
и ограничит применимость такого подхода.
хорошо заметно на рис. 3, б с общим видом об-
Использование более дешёвого, но не менее
разовавшихся костных капсул. Однако полной
активного BMP-2, полученного синтезом в
перестройки костного матрикса ДКМ в случае
клетках E. сoli, должно способствовать более
нашего эксперимента на сроке 12 недель не
широкому распространению данного метода.
БИОХИМИЯ том 88 вып. 8 2023
1374
КАРЯГИНА и др.
ЗАКЛЮЧЕНИЕ
татов на основе диопсида в качестве носителя
BMP-2 - например, включающих различные
В настоящей работе на модели внутри-
гидрогели и/или пористые скаффолды поли-
мышечной имплантации у мышей проведён
мерной природы.
эксперимент по эктопическому остеогенезу,
индуцируемому гибридными имплантатами,
Вклад авторов. А.С. Карягина - концеп-
состоящими из губчатого ДКМ, заполненного
ция и руководство работой, написание статьи;
суспензией частиц диопсида с BMP-2 в ГК.
П.А. Орлова, А.В. Жулина, М.С. Кривозубов,
Через 12 недель на месте имплантации обра-
Т.М. Грунина, Н.В. Струкова - проведение экс-
зовывались округлые костные капсулы тра-
периментов; П.А. Орлова, М.С. Кривозубов,
бекулярной структуры, заполненные зрелым
А.В. Громов - написание фрагментов статьи, под-
костным мозгом и покрытые костью с над-
готовка иллюстраций; А.С. Карягина, В.Н. Ман-
костницей, в несколько раз превышающие
ских, Ф.С. Сенатов, А.В. Громов - обсуждение
по объёму исходный имплантат. Гистологиче-
результатов, редактирование текста статьи.
ское исследование на раннем сроке - 1 неделя
Финансирование. Исследование выполне-
после имплантации - подтвердило механизм
но при поддержке Российского научного фон-
непрямого остеогенеза с промежуточным об-
да (проект № 22-15-00216).
разованием хрящевой ткани. Предлагаемый
Благодарности. Авторы выражают благо-
подход для эктопического наращивания кости
дарность Раджану Чоулдхари и Инне Булы-
с использованием в качестве носителя BMP-2
гиной за предоставление порошка диопсида,
частиц кальций-магниевой силикатной кера-
Марии Генераловой и Анне Рязановой за по-
мики диопсида является новым, преимуще-
мощь в проведении имплантации. Синтез ди-
ством данного подхода является возможность
опсида проводился на базе НИТУ МИСИС,
очень высокой и регулируемой загрузки BMP-2
ряд стадий выделения BMP-2 - в НИИ ФХБ
в имплантат. Имплантаты на основе ДКМ и
имени А.Н. Белозерского МГУ имени М.В. Ло-
диопсида, насыщенного BMP-2, могут быть
моносова и во ВНИИСБ.
использованы для разработки подходов по по-
Конфликт интересов. Авторы заявляют об
лучению аутологичной костной ткани с исполь-
отсутствии конфликта интересов.
зованием принципа in vivo биореактора для
Соблюдение этических норм. Все примени-
замещения крупных дефектов трабекулярных
мые международные, национальные и/или ин-
костей. Перспективной представляется также
ституциональные принципы ухода и использо-
разработка других видов гибридных имплан-
вания животных были соблюдены.
СПИСОК ЛИТЕРАТУРЫ
1. Tan, W., Gao, C., Feng, P., Liu, Q., Liu, C.,
ent anatomical sites as a basis for functionally strati-
Wang, Z., Deng, Y., and Shuai, C. (2021) Dual-func-
fied repair material for bone defects, J. Mech. Be-
tional scaffolds of poly(L-lactic acid)/nanohydroxy-
hav. Biomed. Mater.,
125,
104965, doi:
10.1016/
apatite encapsulated with metformin: Simultaneous
j.jmbbm.2021.104965.
enhancement of bone repair and bone tumor inhibi-
5. Huang, R. L., Kobayashi, E., Liu, K., and Li, Q.
tion, Mater. Sci. Eng. C Mater. Biol. Appl., 120, 111592,
(2016) Bone graft prefabrication following the in vivo
doi: 10.1016/j.msec.2020.111592.
bioreactor principle, EBioMedicine,
12,
43-54,
2. Xu, B., Zheng, P., Gao, F., Wang, W., Zhang, H.,
doi: 10.1016/j.ebiom.2016.09.016.
Zhang, X., Feng, X., and Liu, W. A. (2017) Mineralized
6. Orringer, J. S., Shaw, W. W., Borud, L. J., Freymiller,
high strength and tough hydrogel for skull bone
E. G., Wang, S. A., and Markowitz, B. L. (1999)
regeneration, Adv. Funct. Mater.,
27,
1604327,
Total mandibular and lower lip reconstruction
doi:10.1002/adfm.201604327.
with a prefabricated osteocutaneous free flap,
3. Farokhi, M., Mottaghitalab, F., Shokrgozar, M. A.,
Plast. Reconstr. Surg., 104, 793-797, doi: 10.1097/
Ou, K. L., Mao, C., and Hosseinkhani, H. (2016)
00006534-199909030-00028.
Importance of dual delivery systems for bone tissue
7. Warnke, P. H., Springer, I. N., Wiltfang, J., Acil, Y.,
engineering, J. Control. Release, 225, 152-169, doi:
Eufinger, H., Wehmöller, M., Russo, P. A., Bolte, H.,
10.1016/j.jconrel.2016.01.0334.
Sherry, E., Behrens, E., and Terheyden, H. (2004)
4. Norbertczak, H. T., Fermor, H. L., Edwards, J. H.,
Growth and transplantation of a custom vascularised
Rooney, P., Ingham, E., and Herbert, A.
(2022)
bone graft in a man, Lancet,
364,
766-770,
Decellularised human bone allograft from differ-
doi: 10.1016/S0140-6736(04)16935-3.
БИОХИМИЯ том 88 вып. 8 2023
ИМПЛАНТАТЫ ИЗ ДКМ, ДИОПСИДА И BMP-2
1375
8.
Warnke, P., Wiltfang, J., Springer, I., Acil, Y.,
applications: an overview, Orthopaedic Surg.,
11,
Bolte, H., Kosmahl, M., Russo, P., Sherry, E.,
725-737, doi: 10.1111/os.12509.
Lutzen, U., and Wolfart, S. (2006) Man as living
19.
Bartov, M. S., Gromov, A. V., Poponova, M. S.,
bioreactor: fate of an exogenously prepared customized
Savina, D. M., Nikitin, K. E., Grunina, T. M.,
tissue-engineered mandible, Biomaterials, 27, 3163-
Manskikh, V. N., Gra, O. A., Lunin, V. G., Karyagina,
3167, doi: 10.1016/j.biomaterials.2006.01.050.
A. S., and Gintsburg, A. L. (2016) Modern approaches
9.
Heliotis, M., Lavery, K. M., Ripamonti, U., Tsiridis, E.,
to research of new osteogenic biomaterials on the
and di Silvio, L. (2006) Transformation of a prefab-
model of regeneration of cranial critical-sized
ricated hydroxyapatite/osteogenic protein-1 implant
defects in rats, Bull. Exp. Biol. Med., 162, 273-276,
into a vascularised pedicled bone flap in the human
doi: 10.1007/s10517-017-3693-2.
chest, Int. J. Oral Maxillofac, Surg., 35, 265-269,
20.
Громов А. В., Никитин К. Е., Карпова Т. А., Зай-
doi: 10.1016/j.ijom.2005.07.013.
цев В. В., Сидорова Е. И., Андреева Е. В., Бартов
10.
Cheng, M., Brey, E. M., Ulusal, B. G., and Wei, F.
М. С., Мишина Д. М., Субботина М. Е., Шев-
(2006) Mandible augmentation for osseointegrated
лягина Н. В., Сергиенков М. А., Соболева Л. А.,
implants using tissue engineering strategies,
Котнова А. П., Шарапова Н. Е., Семихин А. С.,
Plast. Reconstr. Surg.,
118,
1e-4e, doi:
10.1097/
Диденко Л. В., Карягина А. С., Лунин В. Г. (2012)
01.prs.0000221120.11128.1a.
Разработка методики получения остеопластиче-
11.
Mesimäki, K., Lindroos, B., Törnwall, J., Mauno, J.,
ского материала на основе деминерализованного
Lindqvist, C., Kontio, R., Miettinen, S., and
костного матрикса с максимальным содержанием
Suuronen, R. (2009) Novel maxillary reconstruction
нативных факторов роста костной ткани, Биотех-
with ectopic bone formation by GMP adipose stem
нология, 5, 66-75.
cells, Int. J. Oral Maxillofac. Surg., 38, 201-209,
21.
Gromov, A. V., Bartov, M. S., Orlova, P. A.,
doi: 10.1016/j.ijom.2009.01.001.
Manskikh, V. N., Krivozubov, M. S., Grunina, T. M.,
12.
Kokemueller, H., Spalthoff, S., Nolff, M., Tavassol, F.,
Manukhina, M. S., Strukova, N. V., Nikitin, K. E.,
Essig, H., Stuehmer, C., Bormann, K. H., Rücker, M.,
Lunin, V. G., Karyagina, A. S., and Gintsburg, A. L.
and Gellrich, N. C. (2010) Prefabrication of vascu-
(2019) Combined effect of bone morphogenetic
larized bioartificial bone grafts in vivo for segmental
protein-2 and erythropoietin on regeneration of cranial
mandibular reconstruction: experimental pilot study in
bone defects in mice, Bull. Exp. Biol. Med., 167,
sheep and first clinical application, Int. J. Oral Maxillo-
408-412, doi: 10.1007/s10517-019-04538-5.
fac Surg., 39, 379-387, doi: 10.1016/j.ijom.2010.01.010.
22.
Gromov, A. V., Poponova, M. S., and Karyagina, A. S.
13.
Horch, R. E., Beier, J. P., Kneser, U., and Arkudas, A.
(2020) Recombinant human bone growth factor
(2014) Successful human long-term application of in
BMP-2 produced in Escherichia coli, Part 1: from
situ bone tissue engineering, J. Cell. Mol. Med., 18,
protein purification to experimental models for efficacy
1478-1485, doi: 10.1111/jcmm.12296.
research, Mol. Genet. Microbiol. Virol., 35, 22-31,
14.
Scott, M. A., Levi, B., Askarinam, A., Nguyen, A.,
doi: 10.3103/S0891416820010036.
Rackohn, T., Ting, K., Soo, C., and James, A. W.
23.
Karyagina, A. S., Orlova, P. A., Poponova, M. S.,
(2012) Brief review of models of ectopic bone
Bulygina, I. N., Choudhary, R., Zhulina, A. V.,
formation, Stem Cells Dev., 21, 655-667, doi: 10.1089/
Grunina, T. M., Nikitin, K. E., Strukova, N. V.,
scd.2011.0517.
Generalova, M. S., Ryazanova, A. V., Kovalyova, P. A.,
15.
Habibovic, P., and de Groot, K. (2007) Osteoinductive
Zimina, A. I., Lukinova, E. M., Plakhotniuk, E. D.,
biomaterials
- properties and relevance in bone
Kirsanova, M. A., Kolesnikov, E. A., Zakharova, E. V.,
repair, J. Tissue Engin. Regenerat. Med., 1, 25-32,
Manskikh, V. N., Senatov, F. S., and Gromov, A. V.
doi: 10.1002/term.5.
(2022) Hybrid implants based on calcium-magnesium
16.
Yang, Z., Yuan, H., Tong, W., Zou, P., Chen, W.,
silicate ceramics diopside as a carrier of recombinant
and Zhang, X. (1996) Osteogenesis in extraskeletally
BMP-2 and demineralized bone matrix as a scaffold:
implanted porous calcium phosphate ceramics:
dynamics of reparative osteogenesis in a mouse crani-
variability among different kinds of animals,
otomy model, Biochemistry (Moscow), 87, 1277-1291,
Biomaterials, 17, 2131-2137, doi: 10.1016/0142-9612
doi: 10.1134/S0006297922110074.
(96)00044-0.
24.
Choudhary, R., Venkatraman, S. K., Bulygina, I.,
17.
Takaoka, K., Nakahara, H., Yoshikawa, H., Masu-
Senatov, F., Kaloshkin, S., Anisimova, N., Kiselev-
hara, K., Tsuda, T., and Ono, K. (1988) Ectopic bone
skiy, M., Knyazeva, M., Kukui, D., Walther, F., and
induction on and in porous hydroxyapatite combined
Swamiappan, S. (2021) Biomineralization, dissolution
with collagen and bone morphogenetic protein, Clin.
and cellular studies of silicate bioceramics prepared
Orthopaed. Rel. Res., 234, 250-254.
from eggshell and rice husk, Mater. Sci. Engin. C, 118,
18.
Zhang, H., Yang, L., Yang, X. G., Wang, F., Feng,
111456, doi: 10.1016/j.msec.2020.111456.
J. T., Hua, K. C., Li, Q., and Hu, Y. C. (2019)
25.
Plantz, M. A., Minardi, S., Lyons, J. G., Greene, A. C.,
Demineralized bone matrix carriers and their clinical
Ellenbogen, D. J., Hallman, M., Yamaguchi, J. T.,
БИОХИМИЯ том 88 вып. 8 2023
1376
КАРЯГИНА и др.
Jeong, S., Yun, C., Jakus, A. E., Blank, K. R., Havey,
Kiselevskiy, M., Scholz, R., Knyazeva, M., Walther, F.,
R. M., Muriuki, M., Patwardhan, A. G., Shah, R. N.,
Lunin, V., Gromov, A., and Karyagina, A. (2020)
Hsu, W. K., Stock, S. R., and Hsu, E. L. (2021)
Biomimetic UHMWPE/HA scaffolds with rhBMP-2
Osteoinductivity and biomechanical assessment of
and erythropoietin for reconstructive surgery, Mater.
a 3D printed demineralized bone matrix-ceramic
Sci. Eng. C. Mater. Biol. Appl, 111, 110750, doi:
composite in a rat spine fusion model, Acta Biomater.,
10.1016/j.msec.2020.110750.
127, 146-158, doi: 10.1016/j.actbio.2021.03.060.
33.
Senatov, F., Maksimkin, A., Chubrik, A., Kolesnikov, E.,
26.
Karyagina, A. S., Boksha, I. S., Grunina, T. M.,
Orlova, P., Krivozubov, M., Nikitin, K., Gromov, A.,
Demidenko, A. V., Poponova, M. S., Sergien-
and Karyagina, A. (2021) Osseointegration evaluation
ko, O. V., Lyashchuk, A. M., Galushkina, Z. M.,
of UHMWPE and PEEK-based scaffolds with BMP-2
Soboleva, L. A., Osidak, E. O., Bartov, M. S., Gro-
using model of critical-size cranial defect in mice and
mov, A. V., and Lunin, V. G. (2017) Two variants of
push-out test, J. Mech. Behav. Biomed. Mater., 119,
recombinant human bone morphogenetic protein 2
104477, doi: 10.1016/j.jmbbm.2021.104477.
(rhBMP-2) with additional protein domains: synthe-
34.
Senatov, F., Zimina, A., Chubrik, A., Kolesnikov, E.,
sis in an Escherichia coli heterologous expression sys-
Permyakova, E., Voronin, A., Poponova, M., Orlova, P.,
tem, Biochemistry (Moscow), 82, 613-624, doi: 10.1134/
Grunina, T., Nikitin, K., Krivozubov, M., Stru-
S0006297917050091.
kova, N., Generalova, M., Ryazanova, A., Manskikh, V.,
27.
Bryan, J. H. D. (1954) Differential staining with a
Lunin, V., Gromov, A., and Karyagina, A. (2022) Ef-
mixture of safranin and fast green FCF, Stain Technol.,
fect of recombinant BMP-2 and erythropoietin on os-
30, 153-157.
teogenic properties of biomimetic PLA/PCL/HA and
28.
Heidenhain, M. (1905) Zeitschrift für wissenschaftliche
PHB/HA scaffolds in critical-size cranial defects mod-
Mikroskopie und für mikroskopische Technik, S. Hirzel,
el, Mater. Sci. Eng. C. Mater. Biol. Appl, 135, 112680,
Leipzig, 22, pp. 339.
doi: 10.1016/j.msec.2022.112680.
29.
Wu, C., and Chang, J. (2013) A review of bioactive
35.
Karpov, T. E., Peltek, O. O., Muslimov, A. R.,
silicate ceramics, Biomed. Mater., 8, 032001, doi:
Tarakanchikova, Y. V., Grunina, T. M., Poponova,
10.1088/1748-6041/8/3/032001.
M. S., Karyagina, A. S., Chernozem, R. V., Pariy,
30.
Oda, S., Kinoshita, A., Higuchi, T., Shizuya, T., and
I. O., Mukhortova, Y. R., Zhukov, M. V., Surmeneva,
Ishikawa, I. (1997) Ectopic bone formation by biphasic
M. A., Zyuzin, M. V., Timin, A. S., and Surmenev,
calcium phosphate (BCP) combined with recombinant
R. A. (2020) Development of optimized strategies
human bone morphogenetic protein-2 (rhBMP-2),
for growth factor incorporation onto electrospun
J. Med. Dent. Sci., 44, 53-62.
fibrous scaffolds to promote prolonged release, ACS
31.
Zimina, A., Senatov, F., Choudhary, R., Kolesnikov, E.,
Appl. Mater. Interfaces, 12, 5578-5592, doi: 10.1021/
Anisimova, N., Kiselevskiy, M., Orlova, P., Strukova, N.,
acsami.9b20697.
Generalova, M., Manskikh, V., Gromov, A., and
36.
Chubrik, A., Senatov, F., Kolesnikov, E., Orlova, P.,
Karyagina, A. (2020) Biocompatibility and physi-
Poponova, M., Grunina, T., Bartov, M., Nikitin, K.,
co-chemical properties of highly porous PLA/HA
Krivozubov, M., Generalova, M., Manskikh, V.,
scaffolds for bone reconstruction, Polymers, 12, 2938,
Lunin, V., Gromov, A., and Karyagina, A. (2020)
doi: 10.3390/polym12122938.
Highly porous PEEK and PEEK/HA scaffolds
32.
Senatov, F., Gulbanu, A., Orlova, P., Bartov, M.,
with Escherichia coli-derived recombinant BMP-2
Grunina, T., Kolesnikov, E., Maksimkin, A.,
and erythropoietin for enhanced osteogenesis and
Kaloshkin, S., Poponova, M., Nikitin, K., Krivo-
angiogenesis, Polym. Test., 87, 106518, doi: 10.1016/
zubov, M., Strukova, N., Manskikh, V., Anisimova, N.,
j.polymertesting.2020.
HYBRID IMPLANTS BASED ON CALCIUM-MAGNESIUM SILICATE
CERAMIC DIOPSIDE AS A CARRIER OF RECOMBINANT BMP-2
AND DEMINERALIZED BONE MATRIX AS A SCAFFOLD: ECTOPIC
OSTEOGENESIS IN INTRAMUSCULAR IMPLANTATION IN MICE
A. S. Karyagina1,2,3*, P. A. Orlova1, A. V. Zhulina1, M. S. Krivozubov1, T. M. Grunina1,3,
N. V. Strukova1, K. E. Nikitin1, V. N. Manskikh1,2, F. S. Senatov1,4, and A. V. Gromov1*
1 Gamaleya National Research Center of Epidemiology and Microbiology,
Ministry of Healthcare of the Russian Federation, 123098 Moscow, Russia;
e-mail: akaryagina@gmail.com, alexander.v.gromov@gmail.com
БИОХИМИЯ том 88 вып. 8 2023
ИМПЛАНТАТЫ ИЗ ДКМ, ДИОПСИДА И BMP-2
1377
2 Belozersky Institute of Physico-Chemical Biology, Lomonosov Moscow State University,
119992 Moscow, Russia
3 All-Russia Research Institute of Agricultural Biotechnology, 127550 Moscow, Russia
4 National University of Science and Technology “MISIS”, 119049 Moscow, Russia
High efficiency of hybrid implants based on calcium-magnesium silicate ceramic diopside as a carrier of
recombinant BMP-2 and xenogenic demineralized bone matrix (DBM) as a scaffold for bone tissue re-
generation was demonstrated previously on the model of critical size cranial defects in mice. In order to
investigate the possibility of using these implants for growing autologous bone tissue using the in vivo bio-
reactor principle in the patient’s own body, the effectiveness of the ectopic osteogenesis induced by them in
intramuscular implantation in mice was studied. At 7 μg dose of BMP-2 per implant, after 1 week we ob-
served a dense agglomeration of cells, probably skeletal muscle satellite precursor cells, with areas of intense
chondrogenesis, the initial stage of indirect osteogenesis, around the implants. After 12 weeks, a dense bone
capsule of trabecular structure was formed, covered with periosteum, with mature bone marrow located
in the spaces between the trabeculae. The capsule volume was about 8-10 times the volume of the original
implant. There were practically no signs of inflammation and foreign body reaction. Microcomputer tomog-
raphy data showed a significant increase of the relative bone volume, number of trabeculae and bone tissue
density in the group with BMP-2 in comparison with the group without BMP-2. Considering that DBM
can be obtained in practically unlimited quantities, of the required size and shape, and the BMP-2 used,
which is obtained by synthesis in E. coli cells, is relatively inexpensive, further development of the in vivo
bioreactor model based on hybrid implants from BMP-2, diopside and xenogenic DBM seems promising.
Keywords: diopside, calcium-magnesium silicate ceramics, implant, BMP-2, demineralized bone matrix, ectopic
osteogenesis
7
БИОХИМИЯ том 88 вып. 8 2023