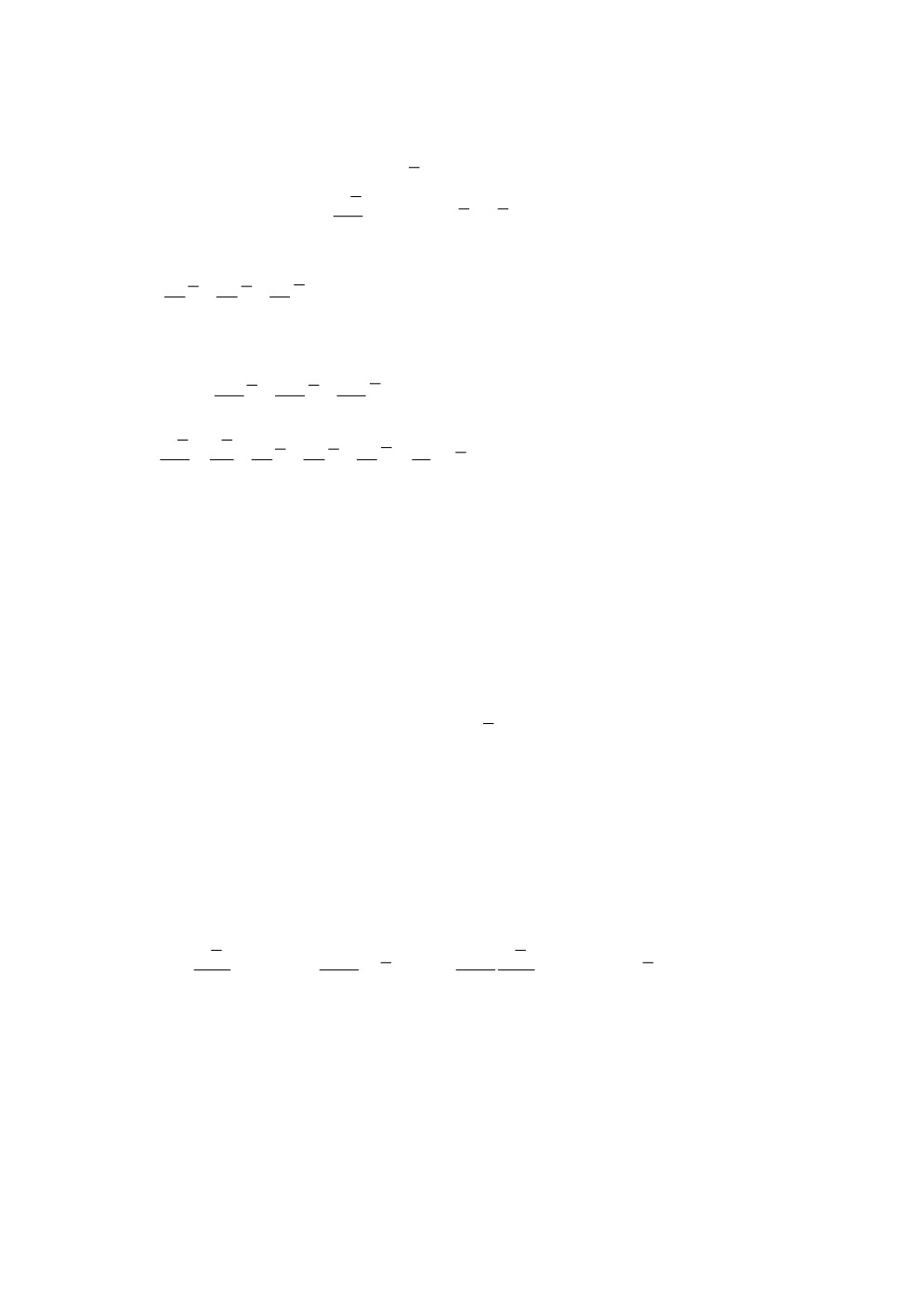ЭНТОМОЛОГИЧЕСКОЕ ОБОЗРЕНИЕ, 100, 4, 2021
УДК 595.7, 591.47, 575.8, 577.353, 533.6.04, 533.69.04
ВЛИЯНИЕ МИНИАТЮРИЗАЦИИ НА СТРОЕНИЕ КРЫЛЬЕВ
И МЕХАНИКУ ПОЛЕТА НАСЕКОМЫХ
© 2021 г. Н. А. Лапина,* С. Э. Фарисенков,** П. Н. Петров,***
А. А. Полилов****
Кафедра энтомологии, биологический факультет, Московский государственный университет
имени М. В. Ломоносова
Ленинские горы, д. 1, стр. 12, Москва, 119234 Россия
*e-mail: nnadlappa@gmail.com
**e-mail: farisenkov@entomology.bio.msu.ru
***e-mail: tinmonument@gmail.com
****e-mail: polilov@gmail.com
Поступила в редакцию 10.07.2021 г.
После доработки 16.07.2021 г.
Принята к публикации 16.07.2021 г.
Миниатюризация - одна из основных тенденций в эволюции крылатых насекомых (Pterygota),
во многих группах которых независимо возникали миниатюрные формы, по размерам тела срав-
нимые с одноклеточными протистами. Микронасекомые обладают способностью к активному
полету, механика которого существенно отличается от таковой у более крупных представителей
родственных групп. Многие миниатюрные насекомые конвергентно приобрели перистое строе-
ние крыльев: узкая крыловая пластинка несет по периметру веер длинных щетинок. Благодаря
низкой проницаемости для воздуха перистое крыло практически не уступает в аэродинамиче-
ской эффективности мембранозному, имея при этом намного меньшие массу и момент инерции.
Нестационарные аэродинамические механизмы машущего полета крупных насекомых, птиц и
рукокрылых не могут обеспечить достаточную подъемную силу при доминировании сил вяз-
кого трения. В связи с этим миниатюрные насекомые используют гребной тип полета: крылья
движутся с высокими углами атаки и существенная часть аэродинамической силы генерируется
за счет их лобового сопротивления. Изучение локомоции миниатюрных насекомых не только
важно для понимания биологии этих животных, но и ставит новые задачи в области механики
движения при низких числах Рейнольдса. В последние годы происходит интенсивное накопле-
ние данных об особенностях строения и функциональной морфологии крыльев миниатюрных
насекомых и механике их полета. Авторами представлен обзор публикаций, посвященных этой
проблеме.
Ключевые слова: полет, насекомые, миниатюризация, кинематика, аэродинамика, птилоптери-
гия, функциональная морфология.
DOI: 10.31857/S0367144521040079
814
Насекомые (Insecta) - самый богатый видами класс животных: их описано уже более
миллиона (Zhang, 2013). Подавляющее большинство представителей этого класса от-
носится к группе крылатых насекомых (Pterygota), важнейшая синапоморфия кото-
рых - крыловой аппарат - во многом и определила их исключительный эволюционный
успех (Mayhew, 2018). Другой ключевой фактор эволюционного успеха насекомых -
небольшие размеры тела, позволяющие занимать многие экологические ниши, недо-
ступные более крупным животным. В результате миниатюризации в нескольких
отрядах независимо возникли виды, взрослые особи которых сопоставимы по разме-
рам с одноклеточными эукариотами. Условно микронасекомыми считаются виды,
у которых длина тела имаго в норме составляет менее 2 мм. Этот показатель соответ-
ствует нижней границе размеров живых организмов, после перехода через которую
обычно происходит сильное упрощение строения, связанное с крайне малыми разме-
рами, - так называемая пумилистическая дегенерация (Городков, 1984). Насекомые с
длиной тела менее 2 мм известны среди по меньшей мере 245 семейств, большинство
из которых относится к отрядам Hymenoptera и Coleoptera. Как минимум 106 из этих
семейств включают виды с длиной тела имаго меньше 1 мм, и только в трех семей-
ствах она бывает меньше 0.5 мм: Mymaridae, Trichogrammatidae (Hymenoptera) и
Ptiliidae (Coleoptera). Самые миниатюрные из известных насекомых - это бескрылые
самцы наездников Dicopomorpha echmepterygis (Mymaridae) (139 μm) (Mockford,
1997), а самые миниатюрные летающие насекомые принадлежат к родам Kikiki Huber
et Beardsley, 2000 (Mymaridae; 158 μm) и Megaphragma Timberlake, 1924 (Tricho-
grammatidae; 170 μm) (Huber, Noyes, 2013; Polilov, 2016). Мельчайшие летающие
непаразитоидные насекомые - жесткокрылые из рода Scydosella Hall, 1999 (Ptiliidae)
(300 μm) (Polilov, 2016).
Изначально было распространено мнение, что микронасекомые летают во многом
пассивно, как аэропланктон, передвигаясь с потоками воздуха, но уже первые полу-
ченные видеозаписи демонстрируют, что миниатюрные насекомые сохраняют способ-
ность к машущему полету (Weiss-Fogh, 1973). В последнее время стало возможным
изучение летных характеристик микронасекомых и было показано, что как минимум
миниатюрные Coleoptera и Hymenoptera способны к быстрому и маневренному полету
(Farisenkov et al., 2020; Sarig, Ribak, 2021).
Полет насекомых давно приковывает внимание не только биологов, но также меха-
ников и инженеров, однако до середины ХХ в. возможности его исследования были
ограничены как технически, так и в связи с недостатками аэродинамической теории
того времени, поскольку стационарная аэродинамика непригодна для описания взаи-
модействия машущего крыла с потоками воздуха. С появлением скоростной видео-
съемки стало возможным точное изучение кинематики работы крыльев насекомых,
благодаря чему начала формироваться теория машущего полета (Weiss-Fogh, 1973;
Ellington, 1984a, 1984b, 1984c), изначально использовавшая квазистационарный под-
ход и теорию вихрей. В последние три десятилетия развитие методов тензометрии,
анемометрии, масштабного моделирования и вычислительной аэродинамики с ис-
пользованием компьютерных мощностей позволило сформулировать современную те-
орию нестационарной аэродинамики машущего полета и изучить такие важные
нестационарные эффекты, как отложенный срыв вихря передней кромки (Dickinson
et al., 1999), ротационная циркуляция (Sane, 2003), добавленная масса (Sane, 2003),
механизм «хлопкá и броска» (clap and fling) (Miller, Peshkin, 2005) и взаимодействие
крыла с вихрями спутной струи (Sun, Tang, 2002).
815
Кинематика полета микронасекомых принципиально отличается от таковой круп-
ных насекомых (Lyu et al., 2019). Для полета всех изученных к настоящему времени
микронасекомых характерны высокие углы атаки при трансляционных движениях,
механизм хлопкá и броска и явная асимметрия крылового цикла. Данные особенности
связаны с условиями полета при низких (порядка 10) числах Рейнольдса (Re), при ко-
торых преобладают силы вязкого трения, в то время как крупные насекомые летают
при Re до 104, на их полет большее влияние оказывают силы инерции (Бродский, 1988;
Walker, 2002; Sane, 2003).
В большинстве предельных случаев миниатюризации у крылатых насекомых раз-
ных отрядов неоднократно конвергентно возникала птилоптеригия (перокрылость):
очень узкая крыловая пластинка окаймлена по периферии бахромой из длинных щети-
нок (Родендорф, 1949, 1951). При явном сходстве строения крыльев представителей
разных групп микронасекомых между ними наблюдаются и различия, которые требу-
ют подробного анализа в связи с особенностями экологии этих групп и свойственных
им механизмов полета.
Большой объем публикаций, в том числе новейших, посвященных полету насеко-
мых разных размеров и функциональной морфологии их крыльев (Полилов, 2015;
Polilov, 2015; Sane, 2016; Polilov et al., 2019a; Sun et al., 2019; Yavorskaya et al., 2019;
Farisenkov et al., 2020; Kolomenskiy et al., 2020; Song et al., 2021), требует обобщающе-
го обзора, позволяющего систематизировать накопленные данные и наметить пути
дальнейших исследований. Миниатюризация беспилотных летательных аппаратов с
машущим крылом делает изучение полета микронасекомых задачей потенциально
большого практического значения (Ma et al., 2013; Vu, Cheol, 2020; Song et al., 2021).
Цель нашего обзора - восполнить этот пробел, осветив историю изучения и совре-
менные данные об эволюции крыльев насекомых при миниатюризации, функциональ-
ной морфологии крыльев и особенностях полета миниатюрных насекомых.
СТРОЕНИЕ КРЫЛЬЕВ МИНИАТЮРНЫХ НАСЕКОМЫХ
Coleoptera
Среди жесткокрылых перокрылость в разной степени выражена у представителей
семейств Ptiliidae (длина тела 0.3-3 мм) (Hall, 2000; Polilov et al., 2019a), Corylophidae
(0.5-2.3 мм) (Polilov, 2016), Jacobsoniidae (0.7-2.1 мм) (Philips et al., 2002; Cai et al.,
2016; Yamamoto et al., 2017), Sphaeriusidae (0.5-1.2 мм) и Torridincolidae (1.0-2.7 мм)
(Lawrence et al., 2011; Beutel, Vanin, 2016). Среди представителей сем. Staphylinidae
известны виды с длиной тела от 1 мм, но ни один из них не имеет перистых крыльев
(Newton et al., 2000).
У жесткокрылых из семейств Corylophidae, Jacobsoniidae, Sphaeriusidae и Torridincol-
idae перокрылость выражена слабо (Bowestead, 1999; Hall, 2000; Lawrence et al., 2011;
Cai et al., 2016; Yamamoto et al., 2017; Hall, 2019). Крыловая пластинка относительно
широкая, окаймление из щетинок составляет не очень большую часть общей площади
крыла (включая площадь, занимаемую щетинками, и промежутки между ними). Про
строение и аллометрию крыльев представителей этих семейств известно немного.
У мельчайших Corylophidae в крыле развиты три жилки: предположительно это ScP,
RA и RP (Bowestead, 1999). У многих представителей сем. Torridincolidae наблюдается
диморфизм по длине крыльев: в популяциях некоторых видов встречаются как длин-
816
нокрылая, так и короткокрылая формы (Reichardt, 1973; Hájek et al., 2011). Коротко-
крылая форма неспособна к полету, а длиннокрылая имеет более крупные размеры и
достаточно развитый для полета крыловой аппарат (Reichardt, 1973). Крылья длинно-
крылой формы окаймлены щетинками, но степень перокрылости невысока, жилкова-
ние крыльев упрощено (Hájek, Fikáček, 2008). К сем. Ptiliidae относятся самые
маленькие известные жесткокрылые (Полилов, 2008), строение их крылового аппара-
та изучено подробнее, чем у других мельчайших насекомых.
Крылья Ptiliidae состоят из двух основных частей: округлого в сечении черешка и
уплощенной пластинки. Черешок сильно склеротизован и немного уплощен дорсо-
вентрально. Обычно черешок лишен щетинок, исключение составляет род Sindosium
Johnson, 2007, у которого щетинки имеются, в том числе на заднем крае черешка.
Крыловая пластинка чаще всего саблеобразно выгнута вперед и несет по периметру
длинные щетинки (рис. 1а). В черешке и в основании крыловой пластинки есть не-
большая заполненная гемолимфой полость, объем которой составляет несколько про-
центов от общего объема крыла. Жилкование редуцировано и олигомеризовано.
У всех Ptiliidae жилка ScP + RA сильно склеротизована и занимает значительную часть
черешка крыла (Polilov et al., 2019a).
По строению крыльев Ptiliidae разделяются на два подсемейства: Nossidiinae, харак-
теризующееся невысокой степенью перокрылости, и Ptiliinae с высокой степенью
перокрылости. Разделение сем. Ptiliidae на эти два подсемейства подтверждается и
молекулярными данными (Polilov et al., 2019b).
Черешок крыла представителей подсем. Nossidiinae содержит две жилки: ScP + RA
на переднем крае крыла и CuA на заднем крае крыла. На дистальной части черешка
между этими жилками начинается складка, которая продолжается на крыловой пла-
стинке. Пластинка содержит по меньшей мере три жилки: RA4, RP2 и MP1 + 2 (+ RP3 + 4).
Две склеротизованные части пластинки, расположенные по обе стороны от складки,
могут быть истолкованы как отдельные жилки или как дистальная часть CuA. Щетин-
ки крепятся к краю крыла с вентральной стороны и покрыты чешуевидными кутику-
лярными выростами (рис. 1б).
У Ptiliinae наблюдается очень сильная редукция жилкования крыльев. Число жилок
убывает по мере уменьшения размеров тела и ширины крыла, при этом жилки не вет-
вятся. На крыльях у видов трибы Nanosellini развиты всего две жилки: RA2 и RP2.
У трибы Acrotrichini жилкование крыла похожее, но MP1 + 2 (+ RP3 + 4) слита с RP2. Ще-
тинки крепятся к крылу с вентральной стороны, вся их поверхность, за исключением
базальной части, покрыта удлиненными пирамидальными или крючковидными кути-
кулярными выростами. Длина и плотность расположения выростов увеличиваются
к вершине щетинки (Polilov et al., 2019a).
У видов подсем. Nossidiinae щетинки распределены по периметру крыла равномер-
но, а у Ptiliinae веер периферических щетинок четко разделен на три зоны: прокси-
мальную часть переднего края крыловой пластинки, дистальную часть крыловой
пластинки и проксимальную часть заднего края крыла. Такое расположение щетинок
важно для складывания крыльев (Polilov et al., 2019a; Petrov et al., 2020).
Основания щетинок неподвижно сочленены с крыловой пластинкой, но они гибкие
благодаря внутренним полостям и высокой концентрации резилина, что позволяет жу-
кам компактно складывать крылья под надкрыльями, сгибая щетинки при основании
817
Рис. 1. Крыло Acrotrichis sericans Heer (Ptiliidae).
а - общий вид, б - кутикулярные выросты одной из периферических щетинок.
(Polilov et al., 2019a; Petrov et al., 2020). Представители сем. Ptiliidae складывают кры-
лья, сгибая их по четырем косым линиям на участках крыловой пластинки, богатых
резилином, который придает мембране крыла эластичность и поэтому ожидаемо рас-
пределен в тех ее участках, которые должны сгибаться при складывании и быстро вы-
прямляться при расправлении крыла (Haas et al., 2000). Сначала жуки отводят крылья
назад и немного поворачивают вокруг своей оси, при этом соединяя надкрылья. После
этого насекомое сгибает крыло при помощи движений брюшка. Для лучшего сцепле-
ния с крыльями поверхности, участвующие в складывании, покрыты микроскульпту-
рой. На поверхности тергитов брюшка есть складки и щетинки, на внутренней
поверхности надкрылий развиты складки. На крыловой пластинке имеются кутику-
лярные шипики (Polilov et al., 2019a; Petrov et al., 2020). Крылья у Ptiliinae (к которым
относятся мельчайшие жесткокрылые) складываются симметрично (Polilov et al.,
2019a; Petrov et al., 2020) в отличие от крыльев Nossidiinae и Staphylinidae (Hammond,
1985; Sun, Bhushan, 2012). Расправление крыльев у Ptiliidae не может происходить за
счет нагнетания в крыло гемолимфы, как у многих более крупных насекомых, по-
скольку полость внутри крыла замкнутая. Крыло расправляется пассивно благодаря
упругости кутикулы крыла с высоким содержанием резилина и упругости пластинки
с продольными складками, придающими крылу дополнительную жесткость (Petrov
et al., 2020).
Hymenoptera
Мельчайшие перепончатокрылые, относящиеся к семействам Mymaridae (длина те-
ла 0.14-4.0 мм) и Trichogrammatidae (0.17-2.0 мм), весьма разнообразны по строению
крыльев, на которых веер щетинок развит в разной степени (Polilov, 2016, 2017). Ще-
тинки миниатюрных перепончатокрылых гладкие, без кутикулярных выростов. Они
расположены по периметру дистальной части крыла, как и у миниатюрных жестко-
крылых, в отличие от которых их крыло, как правило, не имеет обособленного череш-
ка. Поскольку крылья не складываются, щетинки расположены по краю крыла
намного равномернее, чем у Ptiliidae (Polilov, 2016, 2017).
818
Рис. 2. Крылья миниатюрных перепончатокрылых (Hymenoptera).
а - Anaphes flavipes Förster (Mymaridae), б - Megaphragma amalphitanum Timberlake (Trichogrammatidae).
В переднем крыле миниатюрных Mymaridae три жилки: субмаргинальная, марги-
нальная и стигмальная, которые происходят от Sc и R; жилки часто сливаются в одну
на переднем крае крыла (рис. 2а). В заднем крыле только одна субмаргинальная жил-
ка. У представителей рода Mymar Curtis, 1828 крылья имеют длинный черешок с не-
большой округлой пластинкой на конце, которая несет радиально расходящиеся
щетинки. Самцы Dicopomorpha echmepterygis Mockford, 1997 лишены крыльев (Burks,
1938; Bradley, 1955; Polilov, 2016). В переднем крыле миниатюрных Trichogrammatidae
три жилки: субмаргинальная (субкостальная и премаргинальная), маргинальная и
стигмальная (радиальная). Обычно все они сливаются в одну жилку у переднего края
крыла. Эти жилки происходят от Sc и R. В заднем крыле всего одна жилка неясной го-
мологии (рис. 2б) (Burks, 1938; Bradley, 1955; Polilov, 2016).
В обоих семействах при миниатюризации наблюдаются укорочение и сужение кры-
ловой пластинки, смещение центра площади крыла к вершине, увеличение относи-
тельной площади крыла, которую занимают щетинки, и уменьшение их количества
(Polilov, 2016, 2017).
Для перепончатокрылых, включая по меньшей мере часть миниатюрных видов,
характерна функциональная двукрылость. У крупных представителей отряда перед-
нее и заднее крылья соединены и действуют как единая аэродинамическая поверх-
ность (Wootton, 2002). У миниатюрных перепончатокрылых крылья соединены только
в проксимальной трети, дистальные части переднего и заднего крыла каждой стороны
довольно далеко разделены.
Thysanoptera
Самые миниатюрные из трипсов принадлежат к сем. Thripidae, длина представите-
лей которого составляет от 0.5 до 2 мм (Polilov, 2016). Крыловые пластинки трипсов
узкие (рис. 3). Переднее крыло имеет одну или две жилки, в заднем крыле остается
819
Рис. 3. Переднее (вверху) и заднее (внизу) крылья Heliothrips haemorrhoidalis Bouché
(Thysanoptera).
одна жилка; гомология этих жилок неизвестна (Polilov, 2016). На поверхности щети-
нок имеются продольные ребра (Ellington, 1980). Основание каждой щетинки нахо-
дится в имеющем форму цифры 8 углублении, которое позволяет зафиксировать
щетинку в одном из двух положений (Sane, 2016). В полете щетинки расположены под
большим углом относительно крыловой пластинки, а в покое - под углом в 15-20°.
Чтобы сложить или расправить щетинки, насекомое поглаживает по ним ногами и
брюшком (Ellington, 1980; Grimaldi, Engel, 2004). Щетинки расположены рядами, на-
клоненными под разным углом к крылу, образуя в расправленном виде сложную трех-
мерную структуру (Ellington, 1980; Polilov, 2016). На заднем крае крыла щетинки
длиннее, чем на переднем, и расположены заметно плотнее (Polilov, 2016). Считается,
что малые размеры тела - это базальный признак трипсов, сравнительно крупные
формы которых возникли вторично. Перокрылость выражена у всех трипсов, даже
крупных (достигающих 8-15 мм в длину). Почему даже самые крупные трипсы не
утратили перокрылость, неизвестно (Grimaldi, Engel, 2004). Аллометрия крыльев
трипсов пока не изучена.
Diptera
Крылатые двукрылые c длиной тела меньше 1 мм встречаются в семействах
Cecidomyiidae (0.5-8 мм), Ephydridae (0.5-10 мм), Phoridae (0.5-8 мм), Scatopsidae
(0.5-4 мм), Sciaridae (0.6-10 мм) и Sphaeroceridae (0.5-4 мм) (Нарчук, 2003). Особен-
ности морфологии, связанные с миниатюризацией, и аллометрия крыльев Diptera изу-
чены очень слабо.
Известно, что выраженная перокрылость не наблюдается даже у самых миниатюр-
ных двукрылых (за исключением представителей сем. Nymphomyiidae, к которому от-
носятся далеко не мельчайшие из двукрылых), хотя у многих миниатюрных форм
чешуйки на заднем крае крыла, которые гомологичны щетинкам на крае крыла других
820
отрядов насекомых, заметно увеличены. Жилкование миниатюрных двукрылых силь-
но редуцировано, иногда жилки сливаются и смещаются к переднему краю крыла
(Нарчук, 2003; Перковский, Федотова, 2004; Макарченко и др., 2014).
Nymphomyiidae - это монотипическое реликтовое семейство. Длина тела имаго
Nymphomyiidae 1.5-2.5 мм, крылья лишены жилок, крыловая пластинка сужена и име-
ет форму бумеранга; передний и задний края крыла окаймлены коническими щетин-
ками (Нарчук, 2003; Макарченко и др., 2014).
Hemiptera
Мельчайшие летающие представители отряда Hemiptera принадлежат к надсемей-
ству тлей Aphidoidea, длина представителей которого составляет от 0.5 до 7 мм (Eastop,
1966; Stroyan, 1979; Polilov, 2016). Морфологические особенности, связанные с малы-
ми размерами, и аллометрия крыльев тлей почти не изучены. Перокрылость у тлей не
наблюдается. Жилкование сильно редуцировано (Eastop, 1966; Stroyan, 1979). У мель-
чайших Aphidoidea, принадлежащих к вымершим семействам Parvaverrucosidae и
Burmitaphidae, функциональными были только передние крылья, а задние были почти
полностью редуцированы (Poinar, Brown, 2005; Poinar, 2017). Для жилкования кры-
льев характерны олигомеризация и костализация (Stroyan, 1979; Poinar, Brown, 2005;
Poinar, 2017).
КИНЕМАТИКА И АЭРОДИНАМИКА ПОЛЕТА НАСЕКОМЫХ
ПРИ НИЗКИХ ЧИСЛАХ РЕЙНОЛЬДСА
Фазы крылового цикла
Крыловой цикл большинства насекомых состоит из четырех фаз (Sane, 2003; Chin,
Lentink, 2016). Две из них трансляционные (взмах вверх и взмах вниз), т. е. крыло про-
ходит значительное расстояние с относительно большой скоростью и малым измене-
нием угла атаки. Они разделены двумя ротационными фазами (пронация и супинация):
крыло почти не смещается относительно тела, но разворачивается и меняет направле-
ние движения. В цикле взмаха крыло во всех фазах движется костальным краем впе-
ред.
При активном полете скорость крыла имеет не только линейную составляющую, но
и угловую, так как крыло вращается относительно своего основания. Поэтому потоки
воздуха, которые возникают при работе крыльев насекомого, имеют более сложную
структуру, чем при обтекании стационарного крыла (Sane, 2003; Shyy et al., 2008;
Lentink, Dickinson, 2009; Nabawy, Crowther, 2017).
Влияние размеров тела на аэродинамику полета
Необычное строение крыльев микронасекомых связано с особенностями аэродина-
мики полета в условиях, когда силы вязкого трения сопоставимы с силами инерции
или преобладают над ними. Соотношение этих сил описывается числом Рейнольдса
(Re) (1):
(1)
где ρ - плотность среды; R - характерная длина; V - скорость движения среды; μ -
динамическая вязкость среды.
821
Для описания потоков несжимаемых жидкостей и газов используют систему уравне-
ний Навье-Стокса (2). Это система из двух дифференциальных уравнений в частных
производных (Sane, 2003; Anderson et al., 2009; Lentink, Dickinson, 2009).
u
0
(2)
Du
p
u g,
Dt
где
i
j
k
- оператор набла; ū - вектор скорости; ρ - плотность; t -
x
y
z
время; p - давление; μ = vρ - динамическая вязкость; v - кинематическая вязкость;
2
2
2
2
i
j
k
– оператор Лапласа; ḡ - ускорение свободного
2
2
2
x
y
z
Du u
падения;
i
j
k
(u
)
- производная Лагранжа.
Dt
t
x
y
z
t
Первое уравнение системы, уравнение неразрывности, напрямую следует из закона
сохранения массы (Sane, 2003; Anderson et al., 2009). Второе уравнение, или уравнение
движения, представляет собой второй закон Ньютона (Sane, 2003; Shyy et al., 2008;
Anderson et al., 2009). В левой части уравнения движения находится произведение
плотности и производной Лагранжа от скорости по времени. Производная Лагранжа -
это производная, взятая в системе координат, движущейся вместе с частицами среды.
Другими словами, она описывает изменение со временем некой характеристики части
среды. В правой части уравнения - сумма внутренних и внешних сил, которые дей-
ствуют на среду: p - барический градиент, u - вязкое трение (внутренние силы)
и ρḡ - гравитация (внешняя сила) (Sane, 2003; Anderson et al., 2009).
Число Рейнольдса - это коэффициент безразмерной формы уравнения движения.
Переход к безразмерной форме позволяет корректно сравнивать поведение среды в
различных системах, так как учитываются только соотношения их параметров. Чтобы
получить безразмерную форму уравнения движения (3), нужно разделить его размер-
ные компоненты на характеристические величины. Например, время нужно разделить
на частоту взмахов.
*
*
Du
RV Du
*
*
*
*
*
*
*
*
*
*
p
u
g
p
u
g
,
(3)
*
*
Dt
RV
Dt
где u* - безразмерная скорость; V - средняя скорость за характерный период; p* -
безразмерное давление; ḡ* - безразмерное ускорение свободного падения; R - харак-
терная длина.
При вычислении Re машущего крыла в качестве характерной длины обычно исполь-
зуют радиус инерции плоской фигуры, описанной контуром крыла относительно оси,
проходящей через основание и перпендикулярной продольной оси крыла (Cheng, Sun,
2016).
822
При полете крупных животных (Re = 104-107) инерционные силы, действующие на
тело, преобладают над силами вязкого трения воздуха. При уменьшении размеров жи-
вотного масса, которой пропорциональна сила инерции, уменьшается пропорциональ-
но кубу линейных размеров, а площадь поверхности, которой пропорциональна сила
трения, уменьшается пропорционально квадрату линейных размеров, и отношение
силы трения к силе инерции увеличивается, поэтому для миниатюрных насекомых
преодоление сил вязкого трения имеет большее значение, чем для крупных.
Полет при малых Re накладывает отпечаток на кинематику крыльев, поскольку сила
лобового сопротивления, действующая на крыло, становится значительно больше
подъемной силы, т. е. уменьшается его аэродинамическое качество. В таких условиях
гораздо эффективнее становится движение крыла с большими углами атаки, когда ос-
новной вклад в аэродинамическую силу вносит лобовое сопротивление крыла
(Horridge, 1956; Ford et al., 2019).
Нестационарные механизмы генерации аэродинамических сил
Большинство крупных насекомых генерируют аэродинамические силы за счет пяти
основных механизмов: прикрепленный вихрь на передней кромке крыла, добавленная
масса, хлопок и бросок, ротационная циркуляция и взаимодействие крыла с ранее
сброшенными вихрями (Sane, 2003; Chin, Lentink, 2016). Все эти механизмы нестаци-
онарные, т. е. потоки воздуха зависят от скорости и расположения крыла в предыду-
щие моменты, однако при малых Re, когда инерция воздушных потоков относительно
мала, роль нестационарных эффектов может быть не так важна. Вклад некоторых не-
стационарных механизмов в генерацию аэродинамических сил заметно изменяется по
мере уменьшения Re и увеличения выраженности перокрылости.
Прикрепленный вихрь на передней кромке крыла
Основной механизм генерации подъемной силы у большинства крупных насеко-
мых - это прикрепленный вихрь на передней кромке крыла (leading edge vortex, далее
LEV). Например, у Drosophila melanogaster (Drosophilidae) (Re = 150) он может
обеспечивать до 45 % подъемной силы при зависающем полете (Vogel, 1966; Dickinson
et al., 1999). Существует две теории, которые объясняют, каким образом LEV позволя-
ет создавать аэродинамические силы (Nabawy, Crowther, 2017). Согласно одной тео-
рии, разная скорость движения над и под крылом и пониженное давление внутри
вихря приводят к возникновению дополнительной подъемной силы (Sane, 2003; Chin,
Lentink, 2016, Nabawy, Crowther, 2017). Согласно другой теории, LEV позволяет избе-
жать полного срыва потока даже при движении с большими углами атаки: присоеди-
няясь к крылу позади вихря, воздух сходит с крыла на задней кромке, создавая
дополнительный импульс, направленный вниз даже при таких углах атаки, при кото-
рых в отсутствие вихря возникает заваливание (Nabawy, Crowther, 2017). Скорее всего,
обе эти теории верны, но какой вклад вносит каждый из механизмов, пока неизвестно.
При малых Re вихри, которые возникают на передней кромке крыла, гораздо более
диффузные и не могут обеспечить достаточной подъемной силы (Jones et al., 2016; Lee
et al., 2018), поэтому для микронасекомых характерны большие углы атаки во время
трансляций, а аэродинамические силы создаются преимущественно за счет лобового
сопротивления, а не подъемной силы. Во время остальных фаз крыло движется с ми-
823
нимальными углами атаки, чтобы уменьшить его лобовое сопротивление. В связи с
этим для миниатюрных насекомых LEV не имеет такого большого значения, как для
крупных насекомых.
Присоединенный слой и добавленная масса воздуха
Когда тело движется в вязкой среде, за счет адгезии к поверхности тела и когезии
между молекулами среды около его поверхности возникает зона, в которой среда дви-
жется вместе с телом. Так, непосредственно у поверхности тела скорость среды равна
скорости тела, а при удалении от тела постепенно уменьшается вплоть до скорости
свободной среды (Schlichting, Gersten, 1968; Chin, Lentink, 2016; Jones et al., 2016).
Слой среды вокруг тела, который движется со скоростью, близкой к скорости тела,
называется присоединенным слоем. В данном случае стандартный термин «пригра-
ничный слой» не используется, чтобы подчеркнуть, что толщина такого слоя, возника-
ющего на крыле миниатюрного насекомого, сравнима с размерами крыла (Sane, 2003;
Chin, Lentink, 2016; Kolomenskiy et al., 2020).
Толщину ламинарного присоединенного слоя δ на плоском крыле можно вычислить
следующим образом (Schlichting, Gersten, 1968) (4):
vx
xx
x
4.91
4.91
4.91
,
(4)
u
0
xu
0
Re
где u0 - скорость свободной среды; x - расстояние, пройденное средой вдоль твердо-
го тела; ρ - плотность; v = μ/ρ - кинематическая вязкость; μ - динамическая вязкость;
Re - число Рейнольдса.
Толщина присоединенного слоя тем больше, чем меньше Re. Поэтому она значи-
тельно влияет на аэродинамику полета микронасекомых (Cheer, Koehl, 1987; Jones
et al., 2016; Lee, Kim, 2017; Lee et al., 2018).
При движении крыло увлекает за собой массу воздуха, которая ускоряется и затор-
маживается вместе с крылом и имеет собственную инерцию. Эффект добавленной
массы увеличивает нагрузку на крыловой аппарат, при этом создавая дополнительную
аэродинамическую силу (Chin, Lentink, 2016).
Аэродинамика перистого крыла
Относительная толщина присоединенного слоя, возникающего на щетинках, на-
столько велика, что становится сравнимой с расстоянием между щетинками, в резуль-
тате промежутки между ними в значительной степени перекрыты присоединенным
слоем (Jones et al., 2016; Lee, Kim, 2017; Lee et al., 2018). Это позволяет перистому
крылу действовать практически так же, как мембранозное.
Силу трения, действующую на машущее крыло, можно разделить на две составляю-
щие: нормальное напряжение и напряжение сдвига. Они направлены соответственно
перпендикулярно и параллельно поверхности крыла. За счет сложной формы крыла и
увеличения толщины присоединенного слоя по мере уменьшения Re вклад напряже-
ния сдвига в общую силу трения, действующую на крыло, увеличивается, а вклад нор-
824
мального напряжения уменьшается. Это приводит к уменьшению проницаемости
перистого крыла при уменьшении Re (Kolomenskiy et al., 2020).
Значительное число работ посвящено изучению формирования и динамики присо-
единенного слоя с использованием двумерных математических моделей, что позволя-
ет сделать только очень общие выводы относительно поведения приграничного слоя
на настоящем перистом крыле, так как в моделях не учитывается нестационарность
потоков среды (Loudon et al., 1994; Santhanakrishnan et al., 2014; Jones et al., 2016; Lee
et al., 2018).
В диапазоне Re и углов атаки, характерных для полета миниатюрных насекомых,
перистое крыло может действовать почти так же, как мембранозное. Благодаря малым
Re и сложной форме перистого крыла особое значение приобретают силы вязкого тре-
ния воздуха.
Для описания проницаемости крыла для воздуха используется коэффициент проте-
кания (5). Коэффициент протекания между щетинками - это отношение объема среды,
которая протекла между щетинками за единицу времени, к объему среды, который
протек через мнимую рамку той же ширины (Hansen, Tiselius, 1992; Jones et al., 2016).
V
leak
K
(5)
l
sweep
V
где Kl - коэффициент протекания, Vleak - объем среды, протекающей между щетинка-
ми, а Vsweep - объем среды, протекающей через мнимую рамку.
Если требуется более точное описание, используют закон Дарси (6).
kSp
Q
,
(6)
a
где Q - скорость среды, проходящей через крыло; k - коэффициент проницаемости;
S - площадь крыла; ∆p - разница давлений на поверхностях крыла; μ - динамическая
вязкость среды; а - толщина крыла.
Для мембранозного крыла k и Kl равны нулю, а для перистого - больше нуля (вплоть
до единицы). Проницаемость крыла зависит от расстояния между щетинками, их диа-
метра, угла атаки крыла и Re (Cheer, Koehl, 1987; Pal et al., 2006; Stockie, 2009;
Santhanakrishnan et al., 2014).
В диапазоне Re и углов атаки, характерных для полета миниатюрных насекомых, за
счет проницаемости перистое крыло имеет несколько меньшее лобовое сопротивле-
ние, чем мембранозное. При Re = 35 разница составляет 40 %, однако при Re = 2 -
всего 10 %, вследствие чего при малых Re перистое крыло создает практически такую
же аэродинамическую силу, как мембранозное (Kolomenskiy et al., 2020).
Стадия хлопка и броска
Для многих насекомых характерно наличие особого паттерна хлопка и броска (clap
and fling) в крыловом цикле: после взмаха вверх крылья схлопываются над телом, на-
чиная с костальных краев, а затем снова расходятся, тоже начиная с костальных краев
825
(Sane, 2003; Lehmann, Pick, 2007; Chin, Lentink, 2016; Jones et al., 2016). Схлопывая
крылья, насекомое сбрасывает с них вихри передних кромок и выбрасывает назад
струю воздуха (Chin, Lentink, 2016). По иной версии хлопок и бросок используются,
чтобы максимально увеличить амплитуду взмаха, хотя одно не противоречит другому.
Когда крылья начинают расходиться перед взмахом вниз, воздух устремляется в обра-
зовавшееся пространство, что ускоряет развитие прикрепленных вихрей на передних
кромках.
Жуки сем. Ptiliidae схлопывают крылья не только после взмаха вверх, но и после
взмаха вниз. Паттерны хлопка и броска преобразованы в возвратные движения: соеди-
ненные крылья продолжительное время движутся над и под телом с малой скоростью
и околонулевыми углами атаки. Это позволяет снизить их лобовое сопротивление и
значительно увеличить амплитуду взмаха по сравнению с насекомыми с одним хлоп-
ком в крыловом цикле. В результате трансляции почти перпендикулярны друг другу
(Yavorskaya et al., 2019).
Вклад силы лобового сопротивления и подъемной силы
в полную аэродинамическую силу крыла
При Re порядка 10, характерных для полета микронасекомых, вязкое трение оказы-
вает значительное воздействие на движущиеся объекты. Полет в таких условиях име-
ет большие отличия от полета при больших Re (Бродский, 1988; Walker, 2002).
Траектория движения вершины крыла в боковой проекции у крупных насекомых
имеет вид сильно вытянутой восьмерки. Крылья движутся с малыми углами атаки,
а трансляции практически параллельны траектории движения. Аэродинамические си-
лы генерируются на обеих трансляционных фазах, причем преобладает компонент,
перпендикулярный направлению движения крыла, т. е. подъемная сила. Такой тип по-
лета называется машущим.
По мере уменьшения размеров насекомого и, как следствие, уменьшения Re траек-
тория вершины крыла на трансляционных фазах приобретает U-образную форму,
а крылья движутся с большими углами атаки. Основная часть аэродинамической силы
генерируется во время трансляционных фаз, при этом преобладает компонент аэроди-
намической силы, параллельный направлению движения крыла, т. е. лобовое сопро-
тивление. Для полета миниатюрных насекомых характерно также наличие стадии
хлопка и броска в кинематическом цикле (Walker, 2002; Lyu et al., 2019). Такой тип
полета называется гребным.
ЭВОЛЮЦИЯ КРЫЛЬЕВ НАСЕКОМЫХ ПРИ МИНИАТЮРИЗАЦИИ
И ИХ ФУНКЦИОНАЛЬНАЯ МОРФОЛОГИЯ
Крылья большинства мельчайших насекомых имеют бедное жилкование вследствие
редукции и олигомеризации жилок, которые зачастую слабо склеротизованы, у неко-
торых видов на крыле имеется всего одна жилка (Polilov, 2015). Данная эволюционная
тенденция, по-видимому, связана с аллометрией скелетных структур, которая присуща
всем наземным животным и растениям: механическая прочность является функцией
квадрата линейных размеров (площадь поперечного сечения), в то время как нагрузка
при уменьшении размеров снижается в общем виде пропорционально массе тела, т. е.
кубу линейных размеров (Schmidt-Nielsen, 1984).
826
Геометрия контура крыла также претерпевает аллометрические изменения, которые
возможно анализировать при помощи морфометрии на уровне семейств и, реже, под-
отрядов, но трудно выявить на уровне высших таксонов из-за большого числа физио-
логических и морфологических факторов, влияющих на геометрию крыла.
Было показано, что уменьшение удлинения крыла (отношение квадрата длины
к площади) сопутствует миниатюризации у представителей Hymenoptera, Coleoptera
Adephaga и Diptera Nematocera; у представителей Diptera Brachycera и, в меньшей сте-
пени, у Hymenoptera наблюдается тенденция к смещению центра площади крыла в
сторону вершины, т. е. происходит относительное расширение его дистальной части
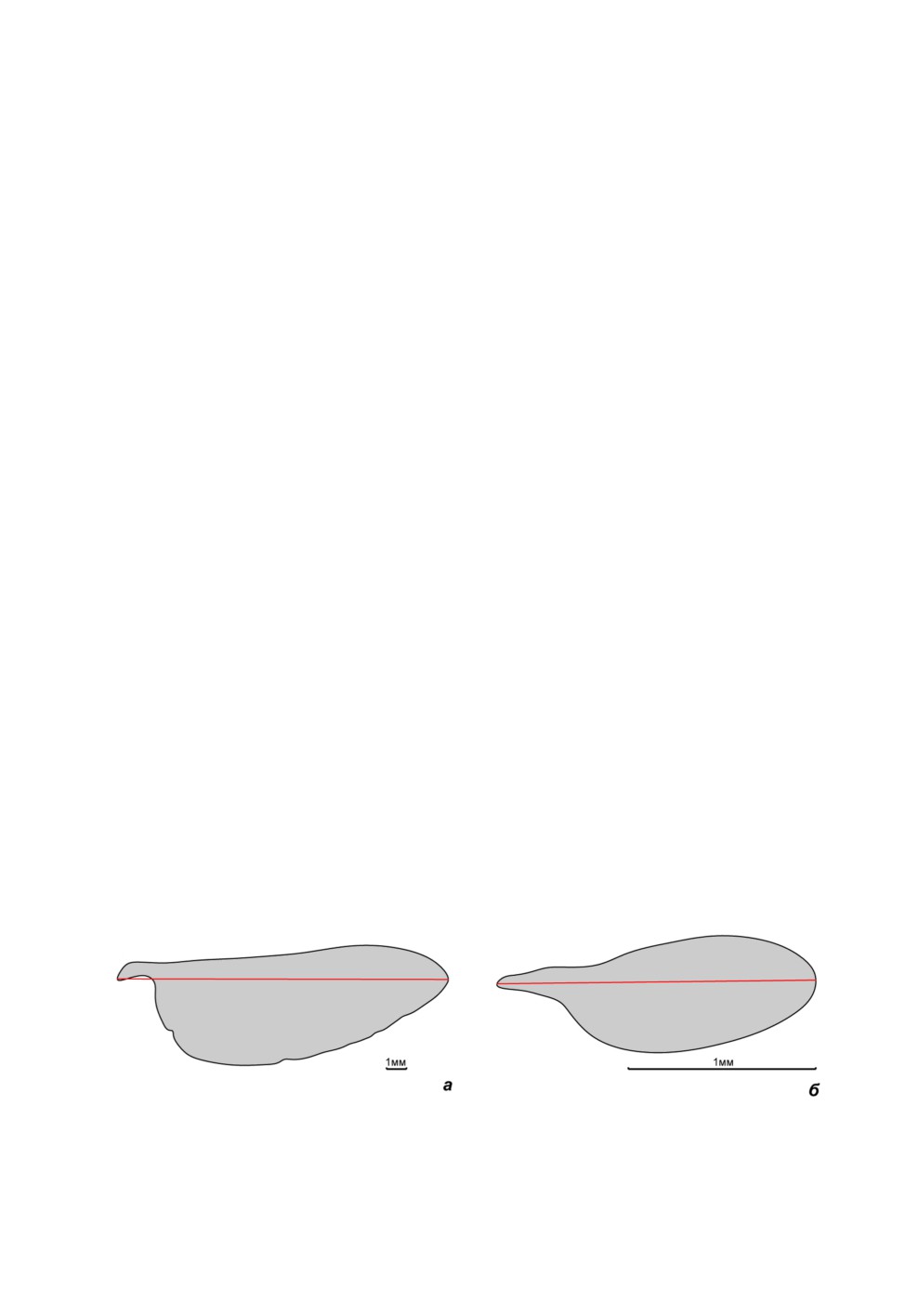
(рис. 4) (Danforth, 1989; Oertli, 1991; Беляев, Фарисенков, 2018, 2019). Такая алломет-
рия геометрии крыла отвечает особенностям развития LEV при различных Re: чем
ниже Re, тем дальше от костального края происходит срыв LEV, особенно в дисталь-
ной части (Harbig et al., 2013). При Re порядка 10 в условиях гребного полета расши-
рение дистальной части крыла также оказывается адаптивным, так как приводит
к смещению центра аэродинамического давления к вершине крыла, которая имеет
большую линейную скорость и, следовательно, большее лобовое сопротивление. Кро-
ме того, А. К. Бродский отмечает, что у миниатюрных насекомых зачастую вершина
крыла имеет округлую и симметричную относительно продольной оси форму в связи
с тем, что при больших углах атаки центр аэродинамического давления смещен ближе
к середине хорды (Бродский, 1988). У крупных насекомых центр давления находится
ближе к костальному краю, где находится зона LEV, поэтому их крылья имеют несим-
метричную треугольную форму (риc. 4a).
В результате миниатюризации представители отрядов Hymenoptera, Thysanoptera и
Coleoptera конвергентно приобрели перистое строение крыльев. Среди мельчайших
Diptera (Нарчук, 2003) (за исключением Nymphomyiidae) и Hemiptera (Eastop, 1966;
Stroyan, 1979) птилоптеригия не встречается. Поскольку аэродинамика полета мель-
чайших насекомых в целом базируется на общих принципах, причины сохранения
мембранозных крыльев у миниатюрных Diptera и Hemiptera остаются важным нере-
шенным вопросом их эволюции.
Становление перокрылости у трипсов можно проследить благодаря данным об ис-
копаемых видах. У раннемезозойских трипсов (триас) с изначально небольшими раз-
мерами тела
(1-2 мм) крыловая пластинка широкая с тонкой мембраной и
выраженными элементами жилкования, которые несут относительно короткие щетин-
ки. Уже у позднемезозойских трипсов (мел) крыловая пластинка узкая, элементы жил-
Рис. 4. Различия в геометрии контура крыла у крупных и миниатюрных насекомых.
а - Tabanus bovinus L., б - Hydrellia albilabris (Meigen).
Красной линией обозначена продольная ось крыла.
827
кования выражены слабо на фоне склеротизованной мембраны и есть длинные
щетинки на периферии крыла (Grimaldi et al., 2004).
Наиболее полный предполагаемый эволюционный ряд, отражающий изменения
крыльев при уменьшении размеров насекомых, реконструирован на примере надсем.
Staphylinoidea (Polilov et al., 2019a). У жуков сем. Hydraenidae с длиной тела 2 мм жил-
кование редуцированное (рис. 5б) по сравнению с крупными стафилиноидами (напри-
мер Silphidae) (рис. 5а), Sc сливается с радиальным стволом; кроме того, в крыле есть
лишь медиальная и кубитоанальная жилки. Периферийные щетинки относительно ко-
роткие и отсутствуют на костальном крае, индекс перокрылости (отношение площади,
занимаемой щетинками, к совокупной площади крыла) всего около 10 %. У видов под-
сем. Nossidiinae (Ptiliidae), длина тела которых не достигает минимальных в этом се-
мействе значений, набор жилок сходный с Hydraenidae, но крыловая пластинка уже и
несет многочисленные (более 250) длинные щетинки, индекс перокрылости составля-
ет 60-80 % (рис. 5в). У Ptiliinae крылья с еще более узкой пластинкой, черешок полно-
стью склеротизован и удлинен, составляя до 1/3 общей длины крыла. Индекс
перокрылости у них 90-95 %, а число щетинок у самых мелких видов уменьшено до
30 (рис. 5г). Жилкование претерпевает дальнейшую редукцию: у миниатюрных видов
трибы Nanosellini остаются только две жилки.
Индекс перокрылости аллометрически зависит от размеров тела, что было показано
не только для Ptiliidae (Coleoptera) (Polilov et al., 2019a), но и для Mymaridae
(Hymenoptera) (Jones et al., 2016): кроме того, увеличивается отношение расстояния
между щетинками к их диаметру (Jones et al., 2016; Polilov et al., 2019a). Данные зако-
номерности согласуются с аэродинамической теорией перистого крыла. При умень-
шении размеров тела и Re для обеспечения достаточно низкой проницаемости крыла
для воздуха достаточно меньшего числа тонких щетинок. С другой стороны, перокры-
Рис. 5. Гипотетический ряд, отображающий эволюционные изменения крыла Staphylinoidea
в процессе миниатюризации.
а - Nicrophorus vespillo L. (Silphidae), б - Hydraena riparia Kugelann (Hydraenidae), в - Motschulskium
sinuatocolle Matthews (Ptiliidae: Nossidiinae), г - Primorskiella anodonta Polilov (Ptiliidae: Ptiliinae).
828
лость, вероятно, ограничивает максимальные размеры тела насекомого при сохране-
нии способности к полету, так как количество щетинок на одном крыле ограничено
длиной периметра крыловой пластинки, к которому они прикреплены, а их минималь-
ный диаметр - необходимой жесткостью. Щетинки расположены, как правило, вееро-
образно, поэтому их основания находятся ближе друг к другу, чем вершины. В связи с
этим длина щетинок также имеет некоторое оптимальное значение, при котором коэф-
фициент проницаемости не слишком велик. По всей вероятности, самой важной пере-
менной, характеризующей проницаемость перистого крыла и способность к полету,
является число Рейнольдса, рассчитанное по зазору между щетинками. Для изучен-
ных Ptiliinae оно находится в достаточно узком диапазоне 0.4-0.6, и есть основания
предполагать, что оно принимает сходные значения у других летающих перокрылых
насекомых.
В условиях гребного полета с использованием механизма хлопка и броска перистое
крыло имеет преимущества перед мембранозным. Проницаемость, незначительно
уменьшающая лобовое сопротивление, компенсируется снижением массы и момента
инерции (Farisenkov et al., 2021). Было показано, что крыло Paratuposa placentis
(Ptiliidae) в 5-7 раз легче мембранозного крыла такой же формы. C учетом добавлен-
ной массы воздуха разница составляет 3-4 раза. Вторичные выросты щетинок вносят
существенный вклад в облегчение крыла: гипотетическое перистое крыло с голыми
цилиндрическими щетинками, имеющими аналогичное лобовое сопротивление,
в 1.75 раза тяжелее, но все еще в 3-4 раза легче мембранозного. Таким образом, пери-
стые крылья Hymenoptera и Thysanoptera, лишенные вторичных выростов, также
должны быть в несколько раз легче своих гипотетических мембранозных аналогов.
Поскольку перистое крыло обладает значительной проницаемостью для воздуха при
больших углах атаки, насекомому требуется приложить значительно меньшие силы,
чтобы разделить их перед взмахом вниз, чем насекомому с мембранозными крыльями
(Jones et al., 2016).
Уменьшение инерции и усилия для разведения схлопнутых крыльев снижает необ-
ходимую для полета мощность, развиваемую летательной мускулатурой, как среднюю
по кинематическому циклу, так и пиковую, что увеличивает энергоэффективность. Со-
ответственно снижается масса летательной мускулатуры, что дополнительно облегча-
ет тело насекомого и должно уменьшать энергозатраты на полет. Масса летательных
мышц Paratuposa placentis прямого и непрямого действия составляет 6.9 % массы те-
ла (Farisenkov et al., 2021), в то время как у крупных насекомых доля ее составляет
десятки процентов и у стрекоз достигает 60 % (Ellington, 1985; Marden, 1989). Вероят-
но, эти различия связаны не только с эффективностью перистых крыльев, но и с алло-
метрией мощности мышц. Масса и объем мышцы пропорциональны кубу линейных
размеров, а мощность - площади сечения и частоте сокращений (Hettinger, 1961;
Ellington, 1985), поэтому удельная мощность летательных мышц насекомых предполо-
жительно растет при миниатюризации, однако подтверждений этого пока нет. На эф-
фективность перистых крыльев безотносительно к влиянию размеров тела на
удельную мощность мускулатуры указывает тот факт, что объем летательной мускула-
туры Paratuposa placentis в 5 раз меньше, чем у миниатюрных двукрылых Corynoneura
scutellata (Winnertz, 1846) из сем. Chironomidae (Веко, Полилов, 2020).
Миниатюризация почти не влияет на число мышц, которое соответствует минималь-
ному числу мышц у крупных представителей родственных групп; у большинства ми-
829
ниатюрных насекомых уменьшается число склеритов и упрощается строение
эндоскелета, к которому крепятся мышцы (Polilov, 2016).
ЗАКЛЮЧЕНИЕ
Мельчайшие крылатые насекомые способны к активному машущему полету. Мини-
атюризация сопровождается изменением геометрии крыльев, отвечающим особенно-
стям аэродинамики полета при низких значениях числа Re (когда силы вязкого трения
сравнимы с инерционными силами, что неизбежно при очень малых размерах тела):
уменьшается удлинение, происходит дистальное смещение центра площади и окру-
гление вершины крыла.
Представители отрядов Thysanoptera, Coleoptera и Hymenoptera конвергентно при-
обрели перистые крылья, которые имеют малую проницаемость для воздуха и при
этом в несколько раз легче мембранозных и требуют меньших усилий для разведения
после хлопка.
При полете в условиях малых Re велико значение сил вязкого трения воздуха, поэто-
му кинематика полета миниатюрных насекомых значительно отличается от таковой у
более крупных насекомых. Для микронасекомых характерны хлопок и бросок и греб-
ной тип полета, при котором аэродинамические силы генерируются преимущественно
за счет лобового сопротивления крыла на трансляционных фазах, во время которых
крылья движутся с большими углами атаки. Траектория вершины крыла мельчайших
Diptera, Hymenoptera и Thysanoptera имеет U-образную форму. Мельчайшие жестко-
крылые сем. Ptiliidae демонстрируют уникальную кинематику крыльев: трансляции
практически перпендикулярные, между трансляционными фазами крылья схлопыва-
ются над и под телом и совершают возвратные движения с околонулевыми углами
атаки.
Исследования полета микронасекомых это междисциплинарное направление, кото-
рое в последние несколько лет интенсивно расширяется с развитием новых методов,
таких как трехмерная морфология, скоростная видеосъемка и вычислительная аэроди-
намика. Тем не менее, многие аспекты полета и морфологии крылового аппарата ми-
кронасекомых изучены лишь поверхностно и на небольшом круге объектов из-за
многочисленных технических сложностей, сопровождающих сбор микронасекомых,
трехмерную реконструкцию их строения, скоростную видеосъемку полета и ресурсо-
емкие вычисления аэродинамики. До сих пор остаются неизученными полет самых
миниатюрных Diptera и Hymenoptera, аллометрия геометрии крыльев большинства
микронасекомых, физиология мускулатуры и механические свойства крыльев.
Дальнейшее изучение функциональной морфологии крылового аппарата и механи-
ки полета микронасекомых имеет фундаментальное значение для понимания общей
биологии и локомоции миниатюрных животных, а также для развития нестационар-
ной аэродинамической теории при низких числах Рейнольдса, которая в перспективе
может иметь практическое применение.
ФИНАНСИРОВАНИЕ
Работа выполнена при финансовой поддержке Российского фонда фундаменталь-
ных исследований (грант № 20-14-50397).
830
СПИСОК ЛИТЕРАТУРЫ
Беляев О. А., Фарисенков С. Э. 2018. Исследование аллометрии формы и жилкования крыльев насекомых.
Часть 1. Hymenoptera. Вестник Московского университета. Серия 16: Биология 73 (4): 277-284.
Беляев О. А., Фарисенков С. Э. 2019. Исследование аллометрии формы и жилкования крыльев насекомых.
Часть 2. Diptera. Вестник Московского университета. Серия 16: Биология 74 (1): 10-18.
Бродский А. К. 1988. Механика полета насекомых. Л.: Издательство Ленинградского университета, 207 с.
Веко Е. Н., Полилов А. А. 2020. Влияние миниатюризации на анатомию Corynoneura scutellata Winnertz,
1846 (Diptera: Chironomidae) - одного из мельчайших двукрылых. Зоологический журнал 99 (12):
1398-1410. doi: 10.31857/S0044513420090184
Городков К. Б. 1984. Олигомеризация и эволюция систем морфологических структур: 2. Олигомеризация и
уменьшение размеров тела. Зоологический журнал 63 (12): 1765-1778.
Макарченко Е. А., Гундерина Е. И., Сато С. 2014. Морфологическое и молекулярно-генетическое описание
Nymphomyia kannasatoi sp. n. (Diptera, Nymphomyiidae) из Японии и Южного Сахалина, с данными по
биологии вида. Евразиатский энтомологический журнал 13 (6): 535-544.
Нарчук Э. П. 2003. Определитель семейств двукрылых насекомых (Insecta: Diptera) фауны России и сопре-
дельных стран (с кратким обзором семейств мировой фауны). СПб.: Зоологический институт РАН,
250 с. (Труды Зоологического института РАН, т. 294).
Перковский Е. Э., Федотова З. А. 2004. Новые виды галлиц (Diptera, Cecidomyiidae) из ровенского янтаря.
Подсемейство Lestremiinae, трибы Micromyiini и Peromyiini. Палеонтологический журнал 38 (4): 44-
54.
Полилов А. А. 2008. Анатомия мельчайших жесткокрылых жуков-перистокрылок трибы Nanosellini
(Coleoptera, Ptiliidae) и пределы миниатюризации насекомых. Зоологический журнал 87 (2): 181-188.
Полилов А. А. 2015. Морфологические особенности насекомых, связанные с миниатюризацией. Вестник
Московского университета. Серия 16: Биология 3: 37-43.
Родендорф Б. Б. 1949. Эволюция и классификация летательного аппарата насекомых. М.; Л.: Палеонтологи-
ческий институт АН СССР, 176 с. (Труды Палеонтологического института АН СССР, т. 16).
Родендорф Б. Б. 1951. Органы движения двукрылых насекомых и их происхождение. М.; Л.: Палеонтологи-
ческий институт АН СССР, 179 с. (Труды Палеонтологического института АН СССР, т. 35).
Anderson J. D., Degrez G., Degroote J., Dick E., Grundmann R., Vierendeels J. 2009. Computational Fluid
Dynamics: An Introduction. 3rd edn. Berlin, Germany: Springer, 332 p.
Beutel R. G., Vanin S. A. 2016. Torridincolidae Steffan, 1964. In: Handbook of Zoology. Vol. 1. Morphology and
Systematics. 2nd ed. Berlin; Boston: De Gruyter, p. 67-70. doi: 10.1515/9783110373929-009
Bowestead S. 1999. A Revision of the Corylophidae (Coleoptera) of the West Palaearctic Region. Geneve: Museum
d’Histoire Naturelle, 203 p.
Bradley J. C. 1955. The wing-venation of Chalcidoidea and of some allied Hymenoptera. Mémoires de la Société
Entomologique de Belgique 27: 127-137.
Burks B. D. 1938. A study of chalcidoid wings (Hymenoptera). Annals of the Entomological Society of America 31
(2): 157-161. doi: 10.1093/aesa/31.2.157
Cai C., Leschen R. A. B., Liu Y., Huang D. 2016. First fossil jacobsoniid beetle (Coleoptera): Derolathrus groehni
n. sp. from Eocene Baltic amber. Journal of Paleontology 89 (5): 762-767. doi: 10.1017/jpa.2015.65
Cheer A. Y. L., Koehl M. A. R. 1987. Paddles and rakes: fluid flow through bristled appendages of small organisms.
Journal of Theoretical Biology 129 (1): 17-39. doi: 10.1016/S0022-5193(87)80201-1
Cheng X., Sun M. 2016. Wing-kinematics measurement and aerodynamics in a small insect in hovering flight.
Scientific Reports 6 (25706): 1-12. doi: 10.1038/srep25706
Chin D. D., Lentink D. 2016. Flapping wing aerodynamics: from insects to vertebrates. Journal of Experimental
Biology 219 (7): 920-932. doi: 10.1242/jeb.042317
Danforth N. 1989. The evolution of hymenopteran wings: the importance of size. Journal of Zoology 218: 247-276.
doi: 10.1111/j.1469-7998.1989.tb02536.x
Dickinson M. H., Lehmann F.-O., Sane S. P. 1999. Wing rotation and the aerodynamic basis of insect flight. Science
284 (5422): 1954-1960. doi: 10.1126/science.284.5422.1954
Eastop V. F. 1966. A taxonomic study of Australian Aphidoidea (Homoptera). Australian Journal of Zoology 14 (3):
399-592. doi: 10.1071/ZO9660399
Ellington С. P. 1980. Wing mechanics and take-off preparation of thrips (Thysanoptera). Journal of Experimental
Biology 85: 129-136. doi: 10.1242/jeb.85.1.129
Ellington C. P. 1984a. The aerodynamics of hovering insect flight. III. Kinematics. Philosophical Transactions of the
Royal Society of London, B 305: 41-78. doi: 10.1098/rstb.1984.0051
Ellington C. P. 1984b. The aerodynamics of hovering insect flight. IV. Aerodynamic mechanisms. Philosophical
Transactions of the Royal Society of London, B 305: 79-113. doi: 10.1098/rstb.1984.0052
831
Ellington C. P. 1984c. The aerodynamics of hovering insect flight. V. A vortex theory. Philosophical Transactions of
the Royal Society of London, B 305: 115-144. doi: 10.1098/rstb.1984.00523
Ellington C. P. 1985. Power and efficiency of insect flight muscle. Journal of Experimental Biology 115 (1):
293-304. doi: 10.1242/jeb.115.1.293
Farisenkov S., Lapina N., Petrov P., Polilov A. 2020. Extraordinary flight performance of the smallest beetles.
Proceedings of the National Academy of Sciences of the United States of America 117 (40): 24643-24645.
doi: 10.1073/pnas.2012404117
Farisenkov S. E., Kolomenskiy D., Petrov P. N., Lapina N. A., Engels T., Lehmann F.-O., Onishi R., Liu Н., Polilov
А. А. [Интернет документ] 2021. A novel flight style allowing the smallest featherwing beetles to excel.
Ford M. P., Kasoju V. T., Gaddam M. G., Santhanakrishnan A. 2019. Aerodynamic effects of varying solid surface
area of bristled wings performing clap and fling. Bioinspiration & Biomimetics 14 (4): 046003. doi:
10.1088/1748-3190/ab1a00
Grimaldi D., Engel M. S. 2004. Evolution of the Insects. Cambridge; New York; Melbourne; Madrid; Cape Town;
Singapore; São Paulo: Cambridge University Press, 755 p.
Grimaldi D., Shmakov A., Fraser N. 2004. Mesozoic thrips and early evolution of the order Thysanoptera (Insecta).
Journal of Paleontology 78 (5): 941-952. doi: 10.1666/0022-3360(2004)078<0941:mtaeeo>2.0.co;2
Haas F., Gorb S., Blickhan R. 2000. The function of resilin in beetle wings. Proceedings of the Royal Society.
B: Biological Sciences 267: 1375-1381. doi: 10.1098/rspb.2000.1153
Hájek J., Fikáček M. 2008. A review of the genus Satonius (Coleoptera: Myxophaga: Torridincolidae): taxonomic
revision, larval morphology, notes on wing polymorphism, and phylogenetic implications. Acta Entomologica
Musei Nationalis Pragae 42 (2): 655-676.
Hájek J., Yoshitomi H., Fikáček M., Hayashi M., Jia F.-L. 2011. Two new species of Satonius Endrödy-Younga from
China and notes on the wing polymorphism of S. kurosawai Satô (Coleoptera: Myxophaga: Torridincolidae).
Zootaxa 3016 (1): 51-62. doi: 10.11646/zootaxa.3016.1.4
Hall W. E. 2000. Ptiliidae Erichson, 1845. In: R. H. Arnett Jr., M. C. Thomas (eds). American Beetles. Vol. 1.
Archostemata, Myxophaga, Adephaga, Polyphaga: Staphyliniformia. Boca Raton; London; New York;
Washington, D. C.: CRC Press, p. 233-246.
Hall W. E. 2019. Sphaerusidae Erichson, 1845. In: A. Slipinski, J. Lawrence (eds). Australian Beetles. Vol. 2.
Archostemata, Myxophaga, Adephaga, Polyphaga (part). Clayton South: CSIRO Publishing, p. 15-17.
Hammond P. M. 1985. Dimorphism of wings, wing-folding and wing-toiletry devices in the ladybird, Rhyzobius
litura (F.) (Coleoptera: Coccinellidae), with a discussion of inter-population variation in this and other
wing-dimorphic beetle species. Biological Journal of the Linnean Society
24
(1):
15-33.
doi: 10.1111/j.1095-8312.1985.tb00157.x
Hansen B., Tiselius P. 1992. Flow through the feeding structures of suspension feeding zooplankton: a physical
model approach. Journal of Plankton Research 14 (6): 821-834. doi: 10.1093/plankt/14.6.821
Harbig R. R., Sheridan J., Thompson M. C. 2013. Reynolds number and aspect ratio effects on the leading-edge
vortex for rotating insect wing planforms. Journal of Fluid Mechanics 717: 166-192. doi: 10.1017/
jfm.2012.565
Hettinger T. 1961. Physiology of Strength. Springfield: Bannerstone House, 83 p.
Horridge G. A. 1956. The flight of very small insects. Nature 178: 1334-1335. doi: 10.1038/1781334a0
Huber J. T., Noyes J. S. 2013. A new genus and species of fairyfly, Tinkerbella nana (Hymenoptera, Mymaridae),
with comments on its sister genus Kikiki, and discussion on small size limits in arthropods. Journal of
Hymenoptera Research 32: 17-44. doi: 10.3897/jhr.32.4663
Jones S. K., Yun Y. J. J., Hedrick T. L., Griffith L. A., Miller B. E. 2016. Bristles reduce the force required to ‘fling’
wings apart in the smallest insects. Journal of Experimental Biology 219 (23): 3759-3772. doi: 10.1242/
jeb.143362
Kolomenskiy D., Farisenkov S., Engels T., Lapina N., Petrov P., Lehmann F.-O., Onishi R., Liu H., Polilov A. 2020.
Aerodynamic performance of a bristled wing of a very small insect. Experiments in Fluids 61: 194.
doi: 10.1007/s00348-020-03027-0
Lawrence J. F., Ślipiński A., Seago A. E., Thayer M. K., Newton A. F., Marvaldi A. E. 2011. Phylogeny of the
Coleoptera based on morphological characters of adults and larvae. Annales Zoologici 61 (1): 1-217.
doi: 10.3161/000345411X576725
Lee S. H., Kim D. 2017. Aerodynamics of a translating comb-like plate inspired by a fairyfly wing. Physics of Fluids
29 (8): 081902. doi: 10.1063/1.4998434
Lee S. H., Lahooti M., Kim D. 2018. Aerodynamic characteristics of unsteady gap flow in a bristled wing. Physics
of Fluids 30 (7): 071901. doi: 10.1063/1.5030693
Lehmann F.-O., Pick S. 2007. The aerodynamic benefit of wing-wing interaction depends on stroke trajectory in
flapping insect wings. Journal of Experimental Biology 210 (8): 1362-1377. doi: 10.1242/jeb.02746
832
Lentink D., Dickinson M. H. 2009. Rotational accelerations stabilize leading edge vortices on revolving fly wings.
Journal of Experimental Biology 212 (16): 2705-2719. doi: 10.1242/jeb.022269
Loudon С., Best B. A., Koehl M. A. R. 1994. When does motion relative to neighboring surfaces alter the flow
through arrays of hairs? Journal of Experimental Biology 193: 233-254. doi: 10.1242/jeb.193.1.233
Lyu Y. Z., Zhu H. J., Sun M. 2019. Flapping-mode changes and aerodynamic mechanisms in miniature insects.
Physical Review 99 (1): 012419. doi: 10.1103/PhysRevE.99.012419
Ma K. Y., Chirarattananon P., Fuller S. B., Wood R. J. 2013. Controlled flight of a biologically inspired, insect-scale
robot. Science 340 (6132): 603-607. doi: 10.1126/science.1231806
Marden J. H. 1989. Bodybuilding dragonflies: Costs and benefits of maximizing flight muscle. Physiological and
Biochemical Zoology 62 (2): 505-521. doi: 10.1086/physzool.62.2.30156182
Mayhew P. J. 2018. Explaining global insect species richness: lessons from a decade of macroevolutionary
entomology. Entomologia Experimentalis et Applicata 166 (4): 225-250. doi: 10.1111/eea.12673
Miller L. A., Peshkin C. S. 2005. A computational fluid dynamics of ‘clap and fling’ in the smallest insects. Journal
of Experimental Biology 208 (2): 195-212. doi: 10.1242/jeb.01376
Mockford E. L. 1997. A new species of Dicopomorpha (Hymenoptera: Mymaridae) with diminutive, apterous
males. Annals of the Entomological Society of America 90 (2): 115-120. doi: 10.1093/aesa/90.2.115
Nabawy M. R. A., Crowther W. J. 2017. The role of the leading edge vortex in lift augmentation of steadily revolving
wings: a change in perspective. Journal of the Royal Society 14 (132): 20170159. doi: 10.1098/rsif.2017.0159
Newton A. F., Thayer M. K., Ashe J. S., Chandler D. S. 2000. Staphylinidae Latreille, 1802. In: R. H. Arnett Jr.,
M. C. Thomas (eds). American Beetles. Vol. 1. Archostemata, Myxophaga, Adephaga, Polyphaga:
Staphyliniformia. Boca Raton; London; New York; Washington, D. C.: CRC Press, p. 272-290.
Oertli J. 1991. Interspecific scaling (relative size change) of wing beat frequency and morphometrics in flying
seals-402439
Pal L., Joyce M. C., Fleming P. D. 2006. A simple method for calculation of the permeability coefficient of porous
media. TAPPI Journal 5 (9): 10-16.
Petrov P. N., Farisenkov S. E., Polilov A. A. 2020. Miniaturization re-establishes symmetry in the wing folding
patterns of featherwing beetles. Scientific Reports 10: 16458. doi: 10.1038/s41598-020-73481-7
Philips T. K., Ive M. A., Giersch J. J. 2002. Jacobsoniidae Heller 1926. In: R. Arnett, M. C. Thomas, P. Skelley,
J. H. Frank (eds). American Beetles. Vol. 2. Polyphaga: Scarabaeoidea through Curculionoidea. Boca Raton;
London; New York; Washington, D. C.: CRC Press, p. 219-220. doi: 10.1201/9781420041231
Poinar G. Jr.2017. A new family of aphids (Hemiptera: Aphidoidea) in mid-Cretaceous Myanmar amber. Cretaceous
Research 75: 7-10. doi: 10.1016/j.cretres.2017.03.013
Poinar G. Jr., Brown A. E. 2005. New Aphidoidea (Hemiptera: Sternorrhyncha) in Burmese amber. Proceedings of
the Entomological Society of Washington 107 (4): 835-845.
Polilov A. A. 2015. Small is beautiful: Features of the smallest insects and limits to miniaturization. Annual Review
of Entomology 60: 103-121. doi: 10.1146/annurev-ento-010814-020924
Polilov A. A. 2016. At the Size Limit - Effects of Miniaturization in Insects. Berlin; Heidelberg: Springer, 325 p. doi:
10.1007/978-3-319-39499-2
Polilov A. A. 2017. Anatomy of adult Megaphragma (Hymenoptera: Trichogrammatidae), one of the smallest
insects, and new insight into insect miniaturization. PLoS ONE 12 (12): 0175566. doi: 10.1371/journal.
pone.0175566
Polilov A. A., Reshetnikova N. I., Petrov P. N., Farisenkov S. E. 2019a. Wing morphology in featherwing beetles
(Coleoptera: Ptiliidae): Features associated with miniaturization and functional scaling analysis. Arthropod
Structure & Development 48: 56-70. doi: 10.1016/j.asd.2019.01.003
Polilov A. A., Ribera I., Yavorskaya M. I., Cardoso A., Grebennikov V. V., Beutel R. G. 2019b. The phylogeny of
Ptiliidae (Coleoptera: Staphylinoidea) - the smallest beetles and their evolutionary transformations.
Arthropod Systematics & Phylogeny 77 (3): 433-455. doi: 10.26049/ASP77-3-2019-4
Reichardt H. 1973. A critical study of the suborder Myxophaga, with a taxonomic revision of the Brazilian
Torridincolidae and Hydroscaphidae (Coleoptera). Arquivos de Zoologia 24 (2): 73-162.
Sane S. P. 2003. The aerodynamics of insect flight. Journal of Experimental Biology 206 (23): 4191-4208. doi:
10.1242/jeb.00663
Sane S. P. 2016. Neurobiology and biomechanics of flight in miniature insects. Current Opinion in Neurobiology 41:
158-166. doi: 10.1016/j.conb.2016.09.008
Santhanakrishnan A., Robinson A. K., Jones S., Low A. A., Gadi S., Hedrick T. L., Miller L. A. 2014. Clap and fling
mechanism with interacting porous wings in tiny insect flight. Journal of Experimental Biology 217 (21):
3898-3909. doi: 10.1242/jeb.084897
Sarig A., Ribak G. 2021. To what extent can the tiny parasitoid wasps, Eretmocerus mundus, fly upwind? Journal of
Applied Entomology 145 (7): 660-674. doi: 10.1111/jen.12890
833
Schlichting H., Gersten K. 1968. Boundary-Layer Theory. Berlin; Heidelberg: Springer, 817 p. doi: 10.1007/978-3-
662-52919-5
Schmidt-Nielsen K. 1984. Scaling: Why Is Animal Size So Important? Cambridge; New York: Cambridge University
Press, Xi + 241 p.
Shyy W., Lian Y., Tang J., Viieru D., Liu H. 2008. Aerodynamics of Low Reynolds Number Flyers. Cambridge:
Cambridge University Press, 193 p. doi: 10.1017/S0001924000005376
Song Z., Tong J., Pfleging W., Sun J. 2021. A review: Learning from the flight of beetles. Computers in Biology and
Medicine 133: 104397. doi: 10.1016/j.compbiomed.2021.104397
Stroyan H. L. G. 1979. Additions to the British aphid fauna (Homoptera: Aphidoidea). Zoological Journal of the
Linnean Society 65 (1): 1-54. doi: 10.1111/j.1096-3642.1979.tb01079.x
Stockie J. M. 2009. Modelling and simulation of porous immersed boundaries. Computers and Structures 87:
701-709. doi: 10.1016/j.compstruc.2008.11.001
Sun J., Bhushan B. 2012. Structure and mechanical properties of beetle wings: A review. RSC Advances 2 (33):
12606-12623. doi: 10.1039/C2RA21276E
Sun J., Liu C., Bhushan B. 2019. A review of beetle hindwings: Structure, mechanical properties, mechanism and
bioinspiration. Journal of the Mechanical Behavior of Biomedical Materials 94: 63-73. doi: 10.1016/j.
jmbbm.2019.02.031
Sun M., Tang J. 2002. Unsteady aerodynamic force generation by a model fruit fly wing in flapping motion. Journal
of Experimental Biology 205 (1): 55-70. doi: 10.1242/jeb.205.1.55
Vogel S. 1966. Flight in Drosophila I. Flight performance of tethered flies. Journal of Experimental Biology 44:
567-578. doi: 10.1242/jeb.44.3.567
Vu H. P., Cheol H. P. 2020 Mimicking nature’s flyers: a review of insect-inspired flying robots. Current Opinion in
Insect Science 42: 70-75. doi: 10.1016/j.cois.2020.09.008
Walker J. A. 2002. Functional morphology and virtual models: physical constraints on the design of oscillating
wings, fins, legs, and feet at intermediate Reynolds numbers. Integrative and Comparative Biology 42 (2):
232-242. doi: 10.1093/icb/42.2.232
Weis-Fogh T. 1973. Quick estimates of flight fitness in hovering animals, including novel mechanisms for lift
production. Journal of Experimental Biology 59 (1): 169-230. doi: 10.1242/jeb.59.1.169
Wootton R. J. 2002. Design, function and evolution in the wings of holometabolous insects. Zoologica Scripta 31
(1): 31-40. doi: 10.1046/j.0300-3256.2001.00076.x
Yamamoto S., Takahashi Y., Parker J. 2017. Evolutionary stasis in enigmatic jacobsoniid beetles. Gondwana
Research 45: 275-281. doi: 10.1016/j.gr.2016.12.008
Yavorskaya M. I., Beutel R. G., Farisenkov S. E., Polilov A. A. 2019. The locomotor apparatus of one of the smallest
beetles - The thoracic skeletomuscular system of Nephanes titan (Coleoptera, Ptiliidae). Arthropod Structure
& Development 48: 71-82. doi: 10.1016/j.asd.2019.01.002
Zhang Z.-Q. 2013. Phylum Arthropoda. In: Z.-Q. Zhang (ed.). Animal Biodiversity: An Outline of Higher-Level
Classification and Survey of Taxonomic Richness (Addenda 2013). Zootaxa 3703 (1): 17-26. doi: 10.11646/
zootaxa.3703.1.6
THE EFFECTS OF MINIATURIZATION ON WING STRUCTURE AND FLIGHT
MECHANICS IN INSECTS
N. A. Lapina, S. E. Farisenkov, P. N. Petrov, A. A. Polilov
Key words: flight, insects, miniaturization, kinematics, aerodynamics, ptiloptery, functional
morphology.
SUMMARY
Miniaturization is one of the principal trends in the evolution of winged insects (Pterygota), in many
groups of which miniature forms with body sizes comparable to those of unicellular protists evolved
independently. It has been shown that microinsects are capable of active flight, the mechanics of
which differ considerably from those of larger representatives of related groups. It has been found that
many miniature insects convergently acquired peculiar features of the structure of the wing apparatus,
called ptiloptery. Miniature insects display a rowing type of flight, since non-stationary mechanisms
834
that provide lift during flapping flight typical of large insects, birds, and bats are inefficient or poorly
efficient when the forces of friction are comparable to inertial forces. During rowing flight, the wing
cycle is asymmetric: during the power stroke, in some phases of the cycle, the wings move with high
angles of attack and velocities, providing the generation of aerodynamic forces, and during the recovery
stroke, in other phases, with small angles of attack and speeds, which allows the insects to minimize the
drag of the wing. The study of the locomotion of miniature insects is not only an important aspect of the
research on the biology of these animals, but also poses new problems in the field of motion mechanics
at ultralow Reynolds numbers. In recent years, there has been an active accumulation of data on the
structural features and functional morphology of the wings of miniature insects and the mechanics of
their flight. This article provides an overview of the publications available on this issue. This study was
supported by the Russian Foundation for Basic Research (project no. 20-14-50397).
835