НЕФТЕХИМИЯ, 2021, том 61, № 1, с. 103-112
УДК 66.081.6
ПАРОВАЯ КОНВЕРСИЯ ПРОПАНА В МЕМБРАННОМ РЕАКТОРЕ
С ПРОМЫШЛЕННЫМ НИКЕЛЕВЫМ КАТАЛИЗАТОРОМ
© 2021 г. Л. П. Диденко1,*, В. Н. Бабак1, Л. А. Семенцова1, П. Е. Чижов1, Т. В. Дорофеева1
1 Институт проблем химической физики РАН, Черноголовка, 142432 Россия
*E-mail: ludi@icp.ac.ru
Поступила в редакцию 13 июля 2020 г.
После доработки 12 августа 2020 г.
Принята к публикации 18 сентября 2020 г.
При исследовании конверсии пропана в мембранном реакторе с промышленным Ni-катализатором
марки НИАП-03-01 при температурах 673, 723, 773 и 823 K, объемных скоростях сырья 1800 и
3600 ч-1, соотношениях пар/пропан = 5 и 7 показано, что отвод Н2 через мембрану приводит к увели-
чению конверсии сырья в Н2 и СО2, образующихся по реакции водяного газа. Глубина превращения по
указанной реакции возрастает с увеличением скорости отвода Н2 через мембрану путем вакуумирования
пермеата. В температурном интервале 773-823 K конверсия сырья составляет 100%, а из реакционной
смеси отводится около 90% Н2 высокой чистоты. Уменьшение времени контакта сырья с катализато-
ром приводит к снижению конверсии сырья в целевые продукты и увеличению скорости образования
углеродных отложений. Закономерности паровой конверсии пропана в мембранном реакторе сходны с
установленными ранее на том же катализаторе и в тех же условиях для н-бутана.
Ключевые слова: паровая конверсия, пропан, мембранный реактор, Pd-Ru-фольга, водород высокой
чистоты
DOI: 10.31857/S0028242121010111
Водород - наиболее перспективный, доступный
сырья паровой конверсии могут быть использо-
и экологически чистый энергоноситель, получае-
ваны метанол, этанол, а также сжиженные нефтя-
мый из природного сырья. Он обеспечивает в 2-3
ные газы (СНГ), содержащие в основном пропан
раза больше энергии на единицу массы, чем бензин
и н-бутан. Хотя по содержанию водорода метан
и другие виды топлива (биодизельное, метанол,
превосходит пропан и н-бутан, в последних, явля-
этанол, природный и сжиженный нефтяной газ)
ющихся жидкостями при комнатной температуре
[1], однако его широкое применение в качестве то-
и умеренном давлении (менее 1.5 МПа), содержа-
плива сдерживает высокая стоимость получения в
ние водорода выше, что следует из соответствую-
больших количествах, сложность хранения на бор-
щих показателей (кг Н2/м3 углеводорода) для СН4
ту транспортного средства и т.д. Важная область
(1.19 МПа, 152.65 K), С3Н8 (0.86 МПа, 293.15 K) и
применения водорода - топливные элементы, в
С4Н10 (0.21 МПа, 293.15 K) составляющих 88.66,
которых химическая энергия водорода преобразу-
91.53 и 100.4 [2]. В то же время по сравнению с бо-
ется в электрическую при окислении кислородом
лее тяжелым углеводородным сырьем, таким, как
воздуха. В настоящее время топливные элемен-
нафта или дизельное топливо, СНГ являются более
ты применяются в различных областях, поэтому
чистым сырьем и содержат более высокий весовой
потребность в водороде возрастает. Особенно ве-
процент водорода, а в сжиженном виде легко хра-
лика потребность в водороде высокой чистоты
нятся и транспортируются. В целом, СНГ является
(99.999 об.%), который необходим, например, для
перспективным сырьем для получения Н2 и иссле-
низкотемпературных топливных элементов с поли-
дование паровой конверсии этого сырья имеет важ-
мерными протоно-обменными мембранами.
ное значение.
В настоящее время основным методом полу-
Для более глубокого понимания этого процес-
чения Н2 является паровая конверсия природного
са необходимо изучить паровую конверсию от-
газа, содержащего преимущественно метан. Этот
дельных компонентов СНГ - пропана и н-бутана.
метод наиболее экономичен вследствие доступно-
Результаты выполненного нами исследования па-
сти и низкой цены сырья. Кроме метана в качестве
ровой конверсии н-бутана представлены в [3]. В
103
104
ДИДЕНКО и др.
данной работе в тех же условиях исследована паро-
Ni/Al2O3 при введении в качестве допирующей до-
вая конверсия пропана.
бавки CeO2 установлено в [16].
В основе процесса лежит реакция паровой кон-
Помимо использования подходящего катализа-
версии пропана [реакция (1)], сопровождающаяся
тора для снижения выхода УО предложен и другой
реакциями водяного газа и метанирования, выход
подход, заключающийся в проведении паровой
продуктов которых ограничен термодинамическим
конверсии СНГ в две стадии: на первой стадии,
равновесием [реакции (2)-(4) соответственно]:
называемой предриформингом, при температурах
673-773 K и соотношениях пар/алкан < 1 компо-
С3Н8 + 3Н2О → 3СО + 7Н2, ΔН0298 = 497,7 кДж/моль, (1)
ненты СНГ превращаются в смесь метана, водо-
СО + Н2О ↔ СО2+ Н2, ΔН0298 = -41 кДж/моль,
(2)
рода и оксидов углерода на второй стадии полу-
СО + 3Н2 ↔ СН4+ Н2О, ΔН0298 = -205.9 кДж/моль,
(3)
ченная смесь конвертируется в оксиды углерода
СО2 + 4Н2 ↔ СН4 +2 Н2О, ΔН0298 = -164.7 кДж/моль. (4)
и водород по реакции паровой конверсии при Т =
973 K и соотношениях пар/алкан = 2-4 [17, 18].
Суммирование уравнений (1) и (2) приводит
Следует отметить, что аналогичный подход пред-
к общему уравнению (5), согласно которому из
ложен для конверсии пропан-метановых [19, 20] и
1 моля С3Н8 максимально можно получить 10 мо-
модельных факельных газовых смесей, содержа-
лей Н2, что значительно выше соответствующего
щих С2Н6-С5Н12 в избытке метана [21].
значения для СН4, составляющего 4 моля Н2:
Снижения температуры реакции и уменьшения,
С3Н8 + 6Н2О ↔ 3СО2 + 10Н2, ΔН0298 = 374.7 кДж/моль. (5)
вследствие этого, выхода УО можно достичь, ис-
Основная проблема получения Н2 паровой кон-
пользуя мембранную технологию, объединяющую
версией пропана - образование углеродных отло-
реакционный процесс и отвод Н2. Отвод Н2 при-
жений (УО), дезактивирующих катализатор. Для
водит к смещению равновесия термодинамически
снижения выхода УО используют двух-трех-крат-
ограниченных реакций и достижению высокой
ный избыток пара, способствующий переходу УО в
конверсии сырья при более низких температурах.
газовую фазу по реакции:
При этом не требуется стадия доокисления СО по
С + Н2О → СО + Н2.
(6)
реакции водяного газа [реакция (2)], а использова-
ние водородселективной мембраны позволяет ис-
В настоящее время в реакции используют пре-
ключить стадию очистки получаемого Н2. В целом,
имущественно катализаторы на основе Ni, что об-
мембранная технология позволяет снизить капита-
условлено их доступностью и низкой ценой. Од-
ло- и энергоемкость паровой конверсии. Впервые
нако, они недостаточно устойчивы к дезактивации
концепция каталитического мембранного процесса
УО даже при большом избытке пара относительно
сформулирована и реализована в работах академи-
алкана [4, 5]. В литературе представлены результа-
ка В.М. Грязнова и сотрудников [22-24], что поло-
ты большого числа исследований, направленных
жило начало большому числу исследований в этой
на создание устойчивых катализаторов. Показано,
области [25-31].
что высокую активность и устойчивость имеют
Pt-, Rh- и Ru-катализаторы, нанесенные на оксид-
Результаты нашего более раннего исследования
ные носители [6, 7]. Однако они дороги, поэтому
паровой конверсии н-бутана в мембранном реак-
более экономично использовать их в качестве до-
торе при температурах 673-823 K, объемных ско-
пирующих добавок к никелевым катализаторам
ростях сырья 1800 и 3600 ч-1 и соотношениях пар/
[8, 9]. Промотирование катализатора оксидами K
бутан = 3, 5 и 7 показали, что отвод Н2 из реакцион-
[10] или Mg [11] приводит к снижению выхода УО
ной смеси приводит к значительному увеличению
вследствие их частичного перехода в газовую фазу,
конверсии бутана в целевые продукты и снижению
однако при этом снижается и активность катализа-
выхода УО [3]. В оптимальных условиях (823 K,
тора. При промотировании лантанидами (La, Ce и
1800 ч-1, соотношение пар/бутан 5, вакуумирова-
ние пермеата) наблюдается полная конверсия сы-
Yb) каталитическая активность и стабильность ка-
рья, а из реакционной смеси отводится 95% водо-
тализатора увеличиваются вследствие сохранения
высокой дисперсности Ni-центров [12]. В работах
рода высокой чистоты.
[13, 14] предложено в качестве носителя для Ni-ка-
В данной работе в тех же условиях исследована
тализатора использовать оксид циркония, стаби-
паровая конверсия пропана. Цель работы - изуче-
лизированный иттрием (YSZ). В кристаллической
ние влияния условий реакции на конверсию сырья,
решетке указанного носителя кислород более под-
состав продуктов и скорость образования углерод-
вижен, чем в традиционном носителе Al2O3, что
ных отложений в мембранном реакторе.
препятствует накоплению на поверхности УО. Вве-
дение в Ni/YSZ в качестве промотора Rh приводит
к дополнительному увеличению подвижности кис-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
лорода решетки носителя, что повышает стабиль-
Описание мембранного реактора. В каче-
ность катализатора [15]. Повышение устойчивости
стве водородселективной мембраны использова-
НЕФТЕХИМИЯ том 61 № 1 2021
ПАРОВАЯ КОНВЕРСИЯ ПРОПАНА В МЕМБР
АННОМ РЕАКТОРЕ
105
ли фольгу толщиной 30 мкм из сплава Pd-6% Ru,
холодильник для конденсирования непрореагиро-
предоставленную сотрудниками Института ме-
вавшей воды. Объемную скорость «сухих» газов,
таллургии и материаловедения РАН (ИМЕТ РАН,
содержащих непрореагировавший С3Н8, Н2, СО,
Москва) [32]. Заготовки под фольгу получали плав-
СО2, и СН4 на выходе из реактора измеряли, ис-
кой в электродуговой печи в инертной атмосфере.
пользуя пенный расходомер, и подавали в хрома-
Фольгу заданной толщины получали холодным
тограф.
прокатом с промежуточными вакуумными отжига-
Состав продуктов анализировали в режиме ре-
ми. Мембрана из фольги имела форму диска диа-
ального времени с использованием хроматографа
метром 56 мм (эффективная площадь поверхности
«Кристалл-5000» с ПИД и детектором по тепло-
15.2 см2). Для поддержания механической проч-
проводности. Содержание Н2 в продуктах реакции
ности ее помещали между сетками тонкого плете-
определяли на колонке с молекулярными сита-
ния из нержавеющей стали. Мембранный реактор
ми 13Х (2 мм × 2 м, 50°С, газ-носитель - аргон).
включал отделения подвода сырья (ретентат) и от-
Углеводородный состав продуктов определяли на
вода Н2 (пермеат), между которыми помещали мем-
колонке НР-Al/KCl (0.5 мм × 30 м, 80°С, газ-носи-
брану. Конструкция реактора подробно описана в
тель - гелий), содержание СО и СО2 - на колонке с
[3]. В отделении ретентата поддерживали атмос-
активированным углем (2 мм × 2 м, 100°С, газ-но-
ферное давление. Движущую силу для отвода Н2
ситель - гелий). Для расчета содержания продук-
из реакционной смеси через мембрану создавали,
тов использовали метод абсолютной калибровки.
снижая парциальное давление Н2 в отделении пер-
меата. С этой целью в отделение пермеата противо-
Расходы газовых потоков контролировали ре-
током сырью с заданной скоростью (150 см3/мин)
гуляторами расхода газа РРГ-12 («Элточприбор»,
подавали отводящий газ - азот. Кроме того, для от-
г. Зеленоград). Нагрев реактора осуществляли
вода Н2 применяли еще один способ - вакуумиро-
электрической печью. Для контроля за температу-
вание отделения пермеата. Для этого использовали
рой в реакторе и печи использовали хромель-алю-
безмасляный диафрагменный (мембранный) ва-
мелевые термопары.
куумный насос MZ 2CNT (Германия). При вакуу-
Влияние отвода Н2 через мембрану на конвер-
мировании давление Н2 в пермеате снижается до
сию пропана и состав продуктов устанавливали на
3 мм рт. ст., что приводит к увеличению скорости
основании сравнения с экспериментами без отво-
отвода Н2 через мембрану.
да Н2 («немембранный» процесс), в которых вме-
Паровая конверсия пропана сопровождается об-
сто мембраны использовали газонепроницаемую
разованием УО, которые могут оказывать негатив-
перегородку из нержавеющей стали. Конверсию
ное влияние на поток Н2 через мембрану. Поэтому
пропана (α, %), и отвод Н2 через мембрану (φ, %)
скорость потока Н2 периодически контролировали.
рассчитывали по формулам:
С этой целью в отделении ретентата мембранного
реактора создавали избыточное давление (127, 145
(7)
и 177 кПа), а в отделении пермеата поддерживали
атмосферное давление и измеряли скорость пото-
ка Н2 на выходе из отделения пермеата, используя
(8)
пенный расходомер. Измерения выполняли при
Т = 823 K и результаты сравнивали с полученными
в тех же условиях до начала экспериментальных
где Vвх - объемная скорость газового потока на
вх
исследований.
входе в реактор, см3/мин; XС
- объемная концен-
3H8
трация С3Н8 в газовом потоке на входе в реактор,
Изучение паровой конверсии пропана. Ре-
вых
%; XС
- объемная концентрация пропана в про-
акцию изучали при температурах 673, 723, 773 и
3
H8
дуктах
реакции на выходе из реактора, %; Vвых -
823 K при объемных скоростях смесей пропана с
паром 1800 и 3600 ч-1 и соотношениях пар/про-
объемная скорость продуктов на выходе из реак-
пан = 5 и 7. В отделение ретентата помещали 2 см3
тора, см3/мин; Vперм - объемная скорость газового
(3.35 г) промышленного никелевого катализатора
потока на выходе из отделения пермеата, см3/мин;
п
XHерм - объемная концентрация Н2 в пермеате, %;
паровой конверсии природного газа марки НИАП-
2
Vрет - объемная скорость газового потока на выходе
03-01 (производитель ООО «НИАП-КАТАЛИЗА-
р
из отделения ретентата, см3/мин; XHет - объемная
ТОР», г. Новомосковск), содержащего 11.2 масс.%
2
концентрация Н2 в ретентате, %.
Ni в пересчете на NiO. Пропан (о.ч.) смешивали с
водяным паром в требуемом соотношении и пода-
Катализатор, используемый в виде зерен фрак-
вали с заданной скоростью на катализатор через
ции
0.2-0.4 мм, предварительно обрабатывали
отверстия, расположенные по периферии отделе-
непосредственно в реакторе смесью
60% Н2-
ния ретентата, а образующиеся продукты отводили
40% Ar-пар в течение 60 мин при температуре экс-
через центральное отверстие и пропускали через
перимента (предварительные эксперименты пока-
НЕФТЕХИМИЯ том 61 № 1 2021
106
ДИДЕНКО и др.
Таблица 1. Зависимость основных показателей конверсии пропана от соотношения пар/пропан. Для отвода Н2 через
мембрану использовали отводящий газ. Время реакции 60 мин
Содержание продукта, об. %
Конверсия,
Отвод Н2,
УО, ммоль/мин/г
Пар/С3Н8
Т, K
СН
4
СО
СО2
Н2
%
%
кат-ра
1800 ч-1
3
723/823
44.5/10.6
1.1/5.9
26.6/31.2
27.5/52.5
98.4/100
77.4/79.4
0.07/0.14
5
21.2/6.0
0.8/4.8
32.0/38.5
45.9/50.8
99.8/100
77.8/89.5
0.07/0.07
7
26.1/2.7
0.7/4.2
34.5/38.2
38.5/55.0
97.6/100
64.3/77.9
0.02/0.04
3600 ч-1
5
723/823
31.7/15.2
0.7/5.4
23.8/29.0
34.5/50.0
83.6/99.5
73.0/78.0
0.13/0.19
7
34.2/10.6
1.4/4.5
27.0/29.3
37.5/56.8
99.8/100
73.3/63.6
0.09/ 0.10
зали, что изменение температуры предварительной
личение избытка пара также приводит к снижению
обработки катализатора в интервале 773-973 K не
образования УО, хотя оно выше, чем при 1800 ч-1.
влияет на его активность).
Например, при соотношении пар/пропан = 7 ско-
рость образования УО при Т = 723 K в 4.5 раза, а
при Т = 823 K в 2.5 раза выше, чем при том же соот-
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
ношении и объемной скорости сырья 1800 ч-1.
В результате паровой конверсии пропана обра-
На отвод Н2 увеличение избытка пара не ока-
зуются Н2, СО2, СО и СН4. Расчет материального
зывает сильного влияния, небольшое снижение
баланса по углероду показывает, что помимо ука-
наблюдается при соотношении 7. При объемной
занных газообразных продуктов, реакция сопрово-
скорости 1800 ч-1 снижение отвода Н2 до 64% про-
ждается образованием УО.
исходит при Т = 723 K, а при 3600 ч-1 - при Т = 823 K.
Влияние соотношения пар/пропан на пока-
В составе реакционной смеси соотношение пар/
затели реакции. В реакции паровой конверсии
пропан влияет, в основном, на содержание СН4.
углеводородного сырья обычно используют более
Наиболее высокое содержание СН4 наблюдается
высокое соотношение пар/алкан, чем требуется по
при соотношении 3 - при Т = 723 K в реакционной
стехиометрии. Это необходимо как для увеличения
смеси содержится 44.5%, а при 823 K - 10.6% СН4.
конверсии сырья, так и для снижения образования
С увеличением избытка пара содержание СН4 сни-
УО. Однако, с практической точки зрения боль-
жается.
шой избыток водяного пара нежелателен, так как
В целом, данные табл. 1 показывают, что для
увеличивает капитало- и энергоемкость процесса.
снижения скорости образования УО и сохранения
Кроме того, в мембранном процессе водяной пар
при этом высокого отвода Н2 оптимальное соотно-
может негативно влиять на скорость отвода Н2 из
шение пар/пропан при объемной скорости сырья
реакционной смеси, поскольку его адсорбция на
1800 ч-1 равно 5. При увеличении объемной ско-
поверхности палладиевой мембраны приводит к
рости сырья до 3600 ч-1 для снижения скорости
уменьшению количества доступных для диссоци-
образования УО требуется более высокий избыток
ации Н2 поверхностных центров. Поэтому должен
пара.
существовать оптимум по соотношению пар/алкан.
В данной работе влияние соотношения пар/пропан
Влияние температуры и объемной скорости
исследовано при температурах 723 и 823 K, объем-
сырья на конверсию пропана, состав реакцион-
ных скоростях сырья 1800 и 3600 ч-1; полученные
ной смеси и скорость образования углеродных
результаты представлены в табл.1.
отложений. При соотношении пар/пропан = 5 из-
менение конверсии пропана в температурном ин-
Результаты в табл. 1, показывают, что соотно-
тервале 673-823 K при объемных скоростях сырья
шение пар/пропан влияет, прежде всего, на ско-
1800 и 3600 ч-1 показано на рис. 1. Для отвода Н2
рость образования УО. При соотношении пар/
из реакционной смеси использовали отводящий газ
пропан = 3 и объемной скорости сырья 1800 ч-1
(N2) и вакуумирование пермеата (кривые 1, 2 соот-
наиболее высокая скорость образования УО,
равная
0.14 ммоль/мин∙г∙кат, наблюдается при
ветственно). Для сравнения на рис. 1 представлены
Т = 823 K, а при снижении температуры до 723 K
кривые 3, соответствующие экспериментам без от-
она снижается до 0.07 ммоль/мин∙г∙кат. При увели-
вода Н2 («немембранный» процесс). Кроме того, на
чении избытка пара до 7 скорость образования УО
том же рисунке показан отвод Н2 из реакционной
снижается и составляет 0.04 и 0.02 ммоль/мин∙г∙кат
смеси (кривые 4, 5).
при температурах 823 и 723 K, соответствен-
Можно видеть, что при объемной скорости
но. При более высокой объемной скорости сырья
1800 ч-1 в температурном интервале 700-823 K
3600 ч-1, скорость образования УО возрастает; уве-
конверсия сырья в мембранном реакторе близка к
НЕФТЕХИМИЯ том 61 № 1 2021
ПАРОВАЯ КОНВЕРСИЯ ПРОПАНА В МЕМБР
АННОМ РЕАКТОРЕ
107
100% (рис. 1а). С увеличением объемной скорости
до 3600 ч-1 конверсия возрастает с температурой и
достигает близкого к 100% значения при темпера-
турах 773-823 K (рис. 1б).
Увеличение скорости отвода Н2 через мембрану
путем вакуумирования пермеата практически не
влияет на конверсию, как при объемной скорости
1800 ч-1, так и при 3600 ч-1. Некоторое снижение
конверсии при вакуумировании наблюдается при
Т = 673 K. Отвод Н2 при использовании отводяще-
го газа составляет 75-80%, а при вакуумировании
возрастает и в конце температурного интервала
приближается к 90% (кривые 4, 5). В «немембран-
ном» процессе более низкий показатель конверсии
наблюдается только при Т = 673 K, а при остальных
условиях он практически не отличается от полу-
ченного в мембранном реакторе (рис. 1а, б, кривые 3).
В отличие от конверсии, содержание продуктов,
прежде всего СО2 и СН4, зависит от способа отвода
Н2. На рис. 2а, б показано изменение содержания
СО2 с температурой в экспериментах с использова-
нием отводящего газа, при вакуумировании перме-
ата и в «немембранном» процессе (кривые 1, 2 и 3
соответственно). Можно видеть, что в мембранном
реакторе содержание СО2 выше, чем в «немем-
бранном» процессе, и при увеличении скорости
отвода Н2 путем вакуумирования пермеата возрас-
тает до ~60% при Т = 823 K и объемной скорости
1800 ч-1. При увеличении объемной скорости до
3600 ч-1содержание СО2 уменьшается, что может
быть обусловлено снижением времени контакта
сырья с катализатором. В тех же условиях содержа-
ние СО значительно ниже, чем СО2, увеличивается
с температурой и в конце температурного интер-
вала составляет около 5% при объемной скорости
1800 ч-1 и около 8% при 3600 ч-1 (рис. 2а, б, кри-
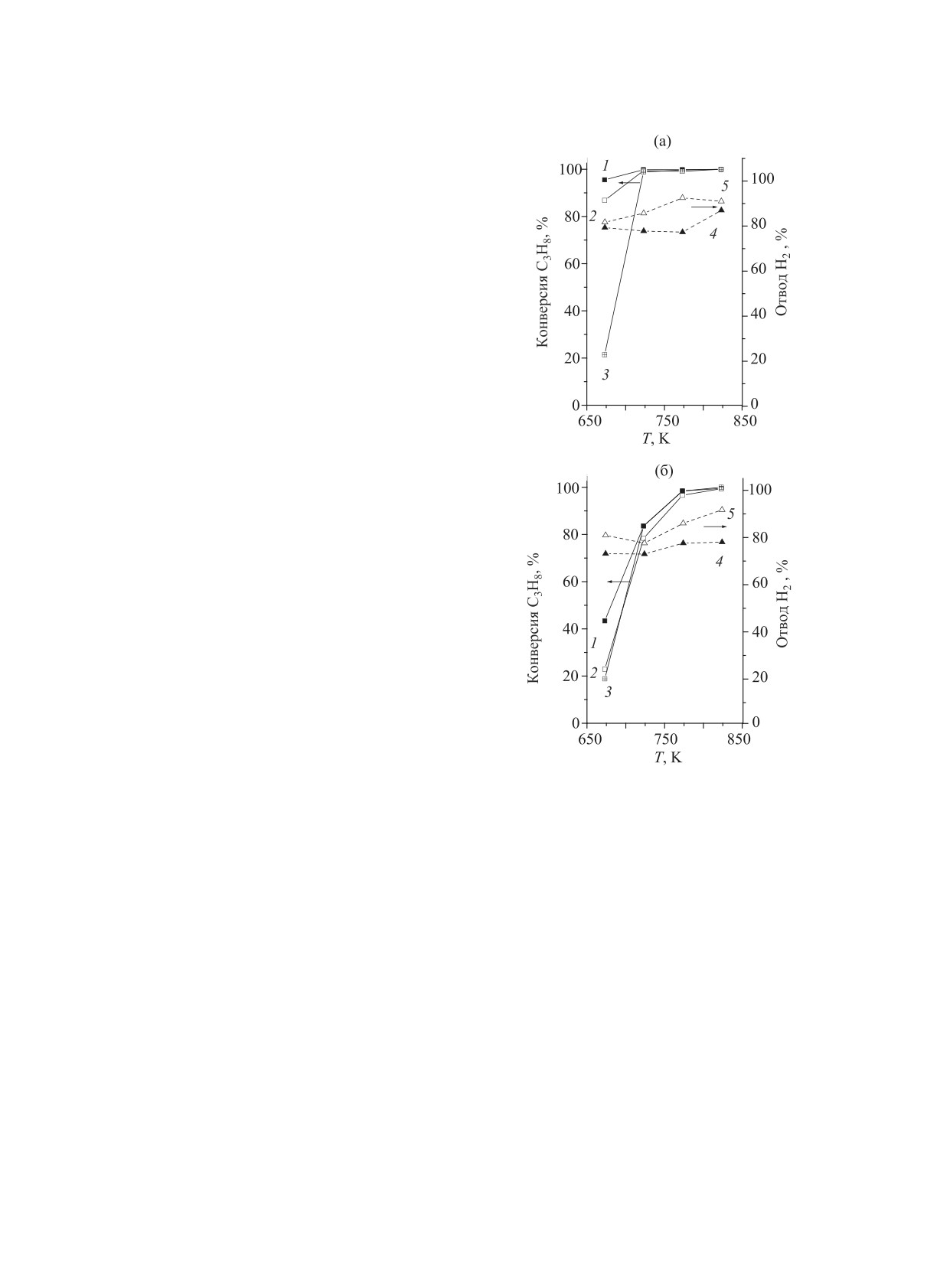
Рис. 1. Зависимость конверсии пропана (кривые 1, 2,
вые 4). Вакуумирование пермеата приводит к не-
3) и отвода Н2 из реакционной смеси (кривые 4, 5) от
большомуснижению содержания СО (кривые 5). В
температуры при объемных скоростях сырья 1800 (а) и
«немембранном» процессе содержание СО практи-
3600 ч-1 (б). Кривые 1,4 соответствуют экспериментам с
чески не отличается от полученного в мембранном
использованием отводящего газа; 2,5 - вакуумирование
реакторе (кривые 6).
пермеата; 3 - без отвода Н2.
Изменение содержания СН4 представлено на
рис. 3, a и б. В мембранном реакторе при объемной
ванием УО, которое значительно возрастает при
увеличении объемной скорости сырья от 1800 до
скорости 1800 ч-1 содержание СН4 плавно снижа-
3600 ч-1 (рис. 4). Влияние отвода Н2 из реакцион-
ется с температурой, а при 3600 ч-1 температур-
ной смеси незначительно в начале исследуемого
ные зависимости проходят через максимум (кри-
температурного интервала, но с увеличением тем-
вые 1). При вакуумировании пермеата содержание
пературы скорость образования УО в мембранном
СН4 уменьшается (кривые 2). В «немембранном»
реакторе ниже, причем, вакуумирование пермеата
процессе содержание СН4 возрастает в интервале
приводит к ее дальнейшему снижению (кривые 1,
723-773 K, а при дальнейшем увеличении темпера-
2). Погрешность расчетной величины скорости об-
туры снижается (кривые 3), причем при объемной-
разования УО не выходила за пределы ±5 отн.%.
скорости 3600 ч-1 содержание СН4 выше, чем при
Следует отметить, что аналогичное возраста-
1800 ч-1, что, вероятно, обусловлено уменьшением
ние скорости образования УО при увеличении
времени контакта пропана с катализатором.
объемной скорости сырья установлено нами и
Расчет материального баланса по углероду по-
при исследовании паровой конверсии н-бутана
казывает, что реакция сопровождается образо-
в мембранном реакторе при тех же условиях [3].
НЕФТЕХИМИЯ том 61 № 1 2021
108
ДИДЕНКО и др.
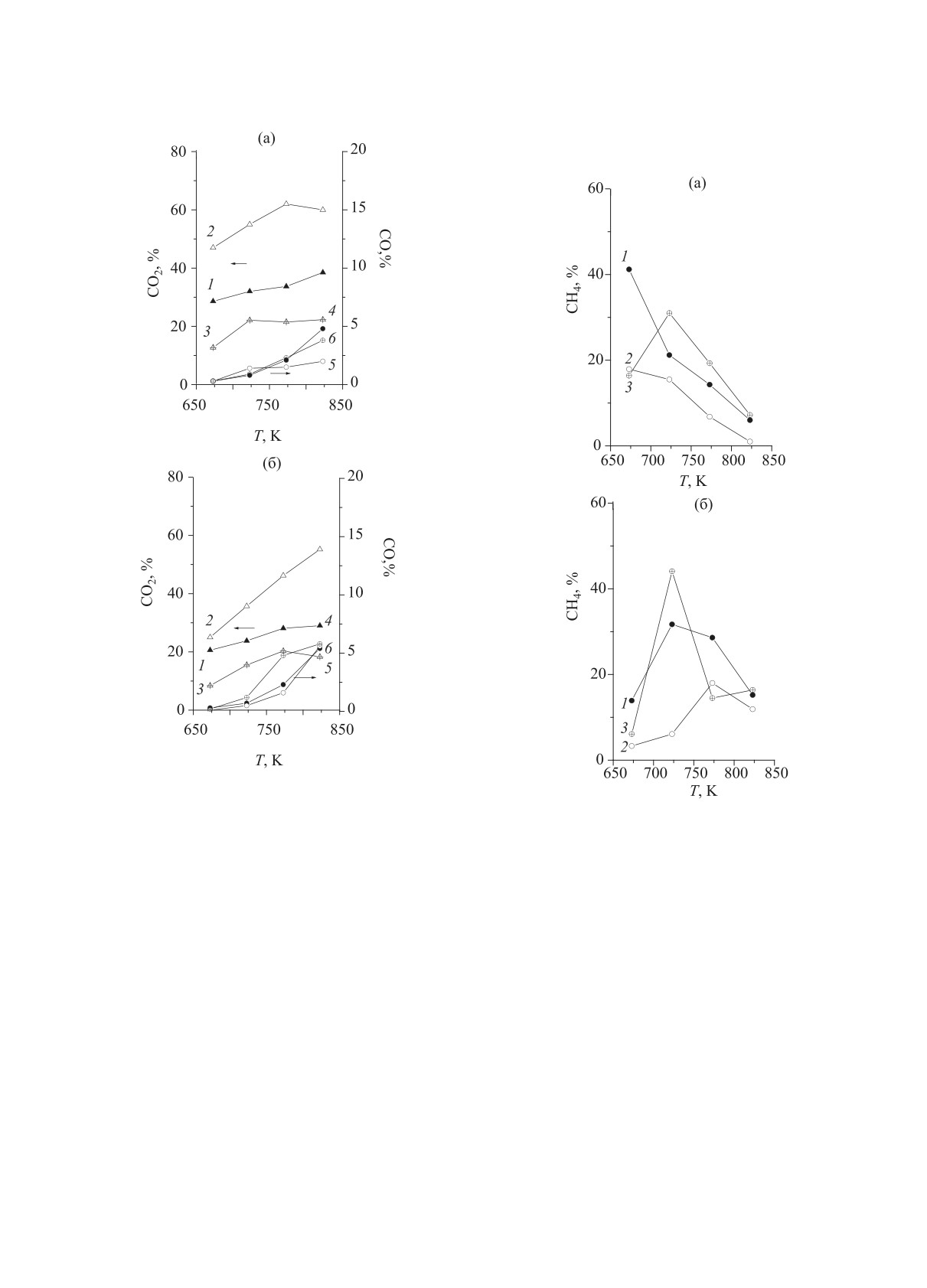
Рис. 2. Зависимость содержания СО2 (кривые 1, 2, 3) и
СО (кривые 4, 5, 6) в продуктах реакции от температу-
Рис. 3. Зависимость содержания СН4 в продуктах ре-
ры при объемных скоростях подачи сырья 1800 ч-1 (а)
и 3600 ч-1 (б) с применением: отводящего газа (кривые
акции от температуры при объемных скоростях сырья
1, 4), вакуумирования (кривые 2, 5) и без отвода Н2
1800 (а) и 3600 ч-1 (б): 1 - с отводящим газом, 2 - при
вакуумировании пермеата; 3 - без отвода Н2.
(кривые 3, 6).
Для объяснения этого экспериментального факта
таном) и водяным паром на размер области проте-
необходимо дополнительное детальное исследова-
кания реакции [3].
ние. На основании имеющихся в настоящее время
Надо также сказать, что углеродные отложения
данных можно предположить, что при увеличении
накапливаются не только в катализаторе, но и на
объемной скорости до 3600 ч-1этот факт обуслов-
поверхности опорной сетки, обращенной в отде-
лен переходом реакции из диффузионной области
ление ретентата. В зависимости от условий реак-
протекания реакции в кинетическую. В пользу дан-
ции за 2 ч на сетке накапливается 2-5 мг УО. По-
ного предположения свидетельствует слабое влия-
скольку сетка имеет крупные ячейки, накопление
ние температуры на скорость образования УО при
УО не препятствует потоку Н2. После каждого экс-
1800 ч-1, что характерно для диффузионного кон-
перимента сетку отжигали в муфельной печи при
троля реакции. Кроме того, справедливость пред-
873 K в течение 4-х ч. В тех же условиях на по-
положения подтверждает математическое описание
верхности Pd-Ru-фольги углеродные отложения
влияния объемной скорости сырья и кинетической
не накапливаются, поэтому образец использовали
константы прямой реакции между метаном (н-бу-
многократно. Периодический контроль показал,
НЕФТЕХИМИЯ том 61 № 1 2021
ПАРОВАЯ КОНВЕРСИЯ ПРОПАНА В МЕМБР
АННОМ РЕАКТОРЕ
109
что снижения скорости потока Н2 через мембрану
при многократном использовании не происходит.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты исследования показывают, что при
отводе Н2 из реакционной смеси в продуктах ре-
акции возрастает содержание СО2. Образование
СО2, наряду с целевым продуктом Н2, происходит
по реакции водяного газа [реакция (2)]. Реакция
водяного газа слабо экзотермична, а выход продук-
тов ограничен термодинамическим равновесием.
С увеличением температуры константа равнове-
сия снижается в соответствии с выражением: K =
exp [(4577.8/T) - 4/33] [33]. Однако отвод Н2 через
мембрану приводит к смещению равновесия в сто-
рону образования продуктов, и в исследуемом тем-
пературном интервале содержание СО2 увеличива-
ется. Выход продуктов в значительной мере зависит
от скорости отвода Н2 через мембрану, что отража-
ет особенность мембранного процесса, описанную
в работах [34, 35]. На примере реакций дегидриро-
вания легких алканов показано, что максимальное
увеличение конверсии алкана в результате отвода
Н2 через мембрану («мембранный эффект») проис-
ходит при близких скоростях образования Н2 и его
отвода через в мембрану. В противном случае либо
скорость образования Н2, либо его отвод являются
лимитирующими стадиями мембранного процес-
са в целом. В исследуемой системе значительное
возрастание содержания СО2 при вакуумировании
пермеата может указывать на высокую скорость
образования Н2 по реакции водяного газа, в резуль-
тате чего достигается необходимый для «мембран-
ного эффекта» баланс скоростей образования и от-
вода Н2. С увеличением объемной скорости сырья
от 1800 до 3600 ч-1 и снижением, вследствие этого,
времени контакта сырья с катализатором, превра-
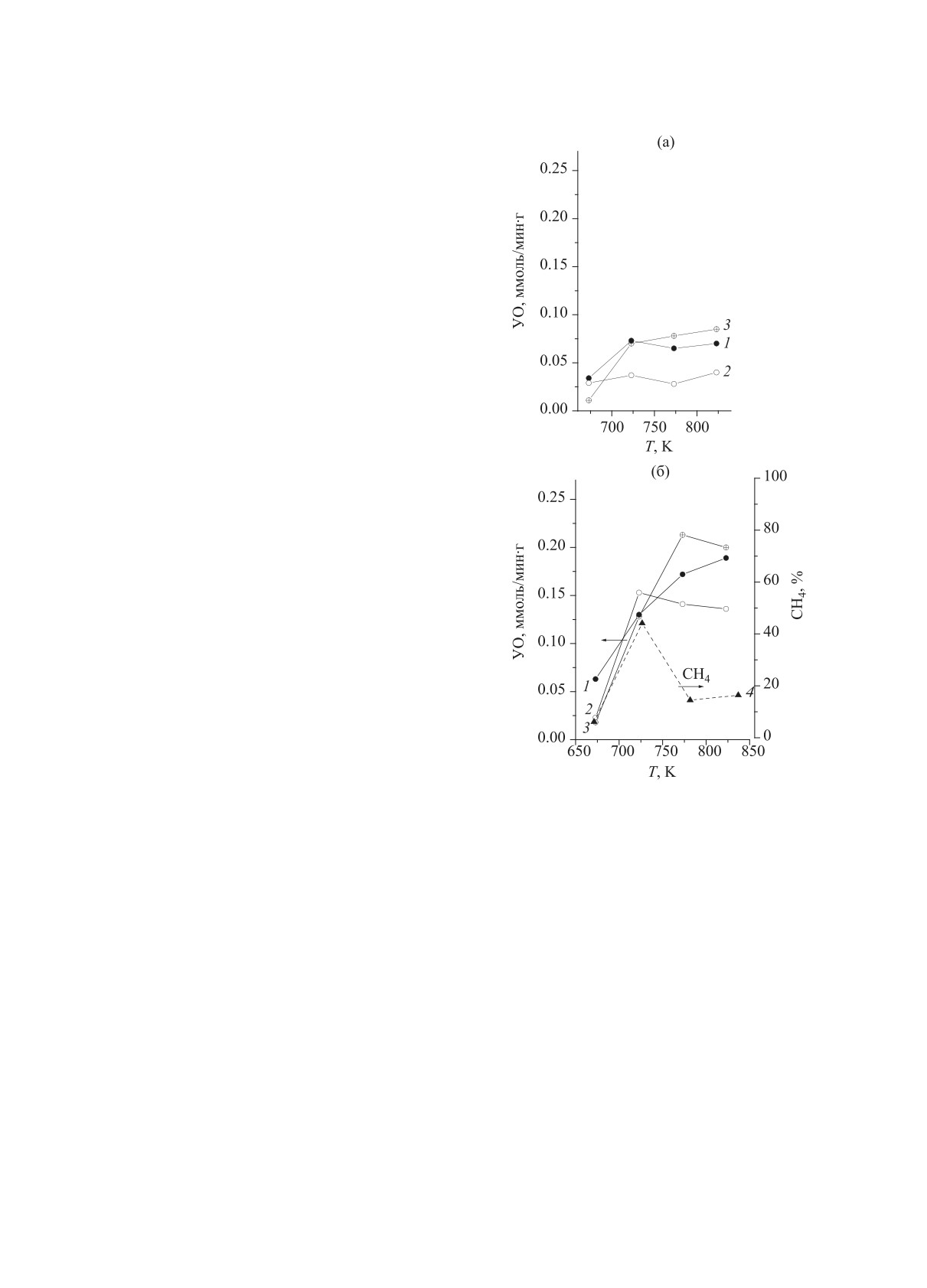
Рис. 4. Зависимость скорости образования УО от тем-
щение СО по реакции 2 снижается и возрастает
пературы в мембранном реакторе (кривые 1, 2) и “не-
его расходование по реакции метанирования [реак-
мембранном” процессе (кривая 3) от объемной скорости
ция (3)].
подачи сырья: 1800 ч-1 (а); 3600 ч-1 (б). Для наглядности
приведена кривая 4 - содержание СН4 в “немембран-
Результаты работы показывают, что существу-
ном” процессе. Способ отвода Н2: 1 - с применением
ет обратная взаимозависимость между содержа-
отводящего газа; 2 - вакуумирование пермеата.
нием СО2 и СН4. Условия, способствующие обра-
зованию СО2 по реакции водяного газа (отвод Н2
С + 2Н2 ↔ СН4.
(10)
из реакционной смеси, вакуумирование пермеата,
увеличение температуры), приводят к снижению
Можно видеть, что по реакции (9) возможно
превращения СО по реакции метанирования, что
образование УО, и этому благоприятствует умень-
наиболее выражено при объемной скорости сырья
шение времени контакта сырья с катализатором.
1800 ч-1. С увеличением объемной скорости вдвое
Помимо реакции (9), к образованию УО может при-
снижается конверсия сырья в целевые продукты и
водить каталитический крекинг С3Н8 по реакции:
возрастает скорость образования УО. При этом из-
С3Н8 → 3С + 4Н2.
(11)
меняется характер влияния температуры на содер-
В начале температурного интервала крекинг
жание СН4 в мембранном реакторе. Образование
С3Н8 может быть представлен в виде:
СН4 по реакции метанирования [реакция (3)] мож-
но представить в виде стадий:
С3Н8 → CН4 + 2С + 2Н2.
(12)
СО + Н2 ↔ С + Н2О,
(9)
Образование УО также может происходить в ре-
НЕФТЕХИМИЯ том 61 № 1 2021
110
ДИДЕНКО и др.
зультате диспропорционирования СО по реакции
конверсия сырья в целевые продукты снижается, и
Будуара:
возрастает выход УО, главным образом в результа-
те каталитического крекинга С3Н8.
2СО → С + СО2.
(13)
Закономерности паровой конверсии пропана в
Однако реакция (13) происходит при более низ-
мембранном реакторе сходны с установленными
ких температурах (573-673 K) и поэтому некото-
ранее на том же катализаторе и в тех же условиях
рый вклад в общий процесс может вносить только
при 673 K.
для н-бутана [3]. Это позволяет предположить, что
конверсия СНГ в исследуемой мембранной систе-
В «немембранном» процессе образование УО,
ме будет происходить по тем же закономерностям,
по-видимому, происходит главным образом по ре-
и что основное внимание должно быть уделено оп-
акции (12). На это указывает сходный характер из-
тимизации объемной скорости сырья. Также, в ре-
менения скорости образования УО и содержания
акции необходимо использовать более устойчивый
СН4 в «немембранном» процессе в температурном
к дезактивации УО катализатор. Промышленный
интервале 673 - 723 K (рис. 4б, кривые 3 и 4 со-
Ni-катализатор не является достаточно устойчи-
ответственно). При дальнейшем увеличении тем-
вым, хотя представленные в литературе результаты
пературы содержание СН4 в продуктах крекинга
исследования паровой конверсии С3-С4-алканов
снижается, по-видимому, в результате его разложе-
указывают на возможность повышения стабиль-
ния по обратной реакции (10), и этим обусловлено
ности каталитической системы в условиях высо-
снижение содержания СН4 с температурой.
кой скорости образования углеродных отложений
[12-16, 20].
ЗАКЛЮЧЕНИЕ
В целом, представленные результаты показыва-
Результаты исследования паровой конверсии
ют, что исследуемая мембранная система является
пропана на промышленном Ni-катализаторе при
перспективной для конверсии СНГ.
выбранных условиях (температурный интер-
вал 673-823 K, объемные скорости сырья 1800 и
ФИНАНСИРОВАНИЕ РАБОТЫ
3600 ч-1) показывают, что при отводе Н2 из реакци-
онной смеси конверсия сырья возрастает. С увели-
Работа выполнена по теме Государственно-
чением скорости отвода Н2 путем вакуумирования
го задания, Государственнаяй регистрация№
пермеата происходит дополнительное увеличение
AAAA-A19-119022690098-3
конверсии, и в температурном интервале 773-823 K
она составляет 100%, а из реакционной смеси отво-
КОНФЛИКТ ИНТЕРЕСОВ
дится около 90% Н2 высокой чистоты. Следует от-
метить, что в большинстве представленных в лите-
Авторы заявляют об отсутствии конфликта ин-
ратуре исследований для отвода Н2 через мембрану
тересов, требующего раскрытия в данной статье.
используют повышенное давление в отделении ре-
тентата. В отличие от них, в данной работе реакцию
ИНФОРМАЦИЯ ОБ АВТОРАХ
проводили при атмосферном давлении, что важно,
поскольку повышение давления, согласно принци-
Диденко Людмила Павловна, к.х.н., ORCID -
пу Ле-Шателье, приводит к снижению выхода Н2 в
0000-0001-8870-1829
реакции паровой конверсии пропана [реакция (5)].
Бабак Владислав Николаевич, д.ф.-м.н.,
Кроме того, атмосферное давление более предпоч-
ORCID - 0000-0003-4126-4574
тительно, если рассматривать применение паровой
Семенцова Лариса Анатольевна, ORCID - 0000-
конверсии углеводородного сырья в небольших
0002-5477-5149.
установках с топливными элементами для получе-
Чижов Петр Евгеньевич, ORCID - 0000-0003-
ния электроэнергии, где проблематично примене-
1967-0787
ние компрессорных установок высокого давления
[36]. Как и при конверсии другого углеводородного
Дорофеева Татьяна Викторовна, ORCID - 0000-
сырья, основной проблемой исследуемой реакции
0003-4554-0919
является образование УО, дезактивирующих ката-
лизатор. Результаты данного исследования показы-
СПИСОК ЛИТЕРАТУРЫ
вают, что скорость этой нежелательной реакции в
значительной мере зависит от объемной скорости
1. Momirlan M.,Vezirogly T.N. The properties of hydrogen
сырья. Реакцию изучали при объемных скоростях
as fuel tomorrow in sustainable energy system for a
сырья 1800 и 3600 ч-1, которые, как показано ра-
cleaner planet // Int. J. of Hydrogen Energy. 2005. V. 30.
нее [37, 38], являются оптимальными для данного
P. 795.
мембранного процесса. В работе установлено, что
2. Rakib M.A., Grace J.R., Lim C.J., Elnashaie S.S.E.H.,
при увеличении объемной скорости до 3600 ч-1
Ghiasi B. Steam reforming of propane in a fluidized bed
НЕФТЕХИМИЯ том 61 № 1 2021
ПАРОВАЯ КОНВЕРСИЯ ПРОПАНА В МЕМБР
АННОМ РЕАКТОРЕ
111
membrane reactor for hhydrogen production // Int J. of
16.
Laosiripojana N., Sangtongkitcharoen W., Assabumrun-
Hydrogen Energy. 2010. V. 35. P. 6276.
grat S. Catalytic steam reforming of ethane and propane
3.
Диденко Л.П., Семенцова Л.А., Бабак В.Н., Чижов
over CeO2-doped Ni/Al2O3 at SOFC temperature: im-
П.Е., Дорофеева Т.В., Квурт Ю.П. // Паровая кон-
provement of resistance toward carbon formation by the
версия н-бутана в мембранном реакторе с промыш-
property of CeO2 // Fuel. 2006. V. 85. P. 323.
ленным никелевым катализатором и фольгой из Pd-
17.
Suzuki T., Iwanami H.I., Iwamoto O., Kitahara T. Pre-re-
Ru-сплава // Мембраны и мембранные технологии.
forming of liquefied petroleum gas on supported ruthe-
2020. 10. № 2. С. 85.
nium catalyst // Int. J. Hydrogen Energy. 2001. V. 26.
4.
Matsuka M., Shigedomi K., Ishihara T. Comparative
P. 935.
study of propane steam reforming in vanadium based
18.
Zheng J., Strohm J.J., Song C.S. Steam reforming of liq-
catalytic membrane reactor with nickel-based catalysts //
uid hydrocarbon fuels for micro-fuel cells. Pre-reforming
Int. J. Hydrogen Energy. 2014. V. 39. P. 14792.
of model jet huels over supported metal catalysts // Fuel
5.
Malaibari Z.O., Croset E., Amin A., Epling W. Effect of
Process Tech. 2008. V. 89. P. 440.
19.
Zyryanova M.M., Snytnikov P.V., Shigarov A.B., Belya-
Interactions between ni and mo on catalytic properties of
ev V.D., Kirillov V.A., Sobyanin V.A. Low Temperature
a bimetallic Ni-Mo/Al2O3 propane reforming catalyst //
catalytic steam reforming of propane-methane mix-
Appl. Catal. A Gen. 2015. V. 490. P. 80.
ture into methane-rich gas: experiment and macroki-
6.
Suzuki T., Iwanami H.-I., Iwamoto O., Kitahara T.
Pre-reforming of liquefied petroleum gas on supported
org/10.1016/j.fuel.2014.06.032
ruthenium catalyst // Int. J. Hydrogen Energy. 2001. V. 26.
20.
Uskov S.I., Enikeeva L.V., Potemkin D.I., Belyaev V.D.,
№ 9. P. 935.
Snytnikov P.V., Gubaidullin I.M., Kirillov V.A., Sobya-
7.
Avci A.K., Trimm D.L., Aksoylu A.E., Onsan Z.I. Ignition
nin V.A. Kinetics of low-temperature steam reforming
characteristics of Pt-, N-i and Pt-Ni catalysts used for
of propane in a methane excess on a Ni-based catalyst //
autothermal fuel processing // Catal. Lett. 2003. V. 88.
Catal. Ind. 2017. V. 9. P. 104.
P. 17.
21.
Uskov S.I., Potemkin D.I., Shigarov A.B., Snytnikov P.V.,
8.
Kaftan A., Kusche M., Laurin M., Wasserscheid P.,
Kirillov V.A., Sobyanin V.A. Low-temperature steam con-
Libuda J. KOH-Promoted Pt/Al2O3 catalysts for water
version of fare gases for various applications // Chem.
gas shift and methanol steam reforming: an operando
Eng. J. 2019. V. 368. P. 533.
DRIFTS-MS study // Appl. Catal. B: Env. 2017. V. 201.
22.
Грязнов В.М. Катализ на мембранах с избирательной
P. 169.
проницаемостью // Докл. АН СССР. 1969. Т. 189.
9.
Li Y., Wang X., Song C. Spectroscopic characterization
С. 794.
and catalytic activity of Rh supported on CeO2-modified
23.
Gryaznov V.M. Hydrogen permeable palladium mem-
Al2O3 for low-temperature steam reforming of propane //
brane catalysts. An aid to the efficient production of ultra
Catal. Today. 2016. V. 263. P. 22.
pure chemicals and pharmaceuticals // Platinum Met.
10.
Carrero A., Calles J.A., Vizcaíno A.J. Effect of Mg and
Rev. 1986. V. 30. P. 68.
Ca addition on coke deposition over Cu-Ni/SiO2 cata-
24.
Gryaznov V.M. Metal Containing membranes for the
lysts for ethanol steam reforming // Chem. Eng. J. 2010.
production of ultrapure hydrogen and the recovery of
V. 163. P. 395.
hydrogen isotopes // Sep. Purif. Rev. 2000.V. 29. P. 171.
11.
Vizcaino A.J., Carrero A., Calles J.A. Ethanol steam
25.
Лыткина А.А., Орехова Н.В., Ярославцев А.Б. Паро-
reforming on Mg- and Ca-modified Cu-Ni/SBA-15 cat-
вой риформинг метанола в мембранных реакторах //
alysts // Catal. Today. 2009. V. 146. P. 63.
Мембраны и мембранные технологии. 2018. Т. 8.
12.
Natesakhawat S., Watson R.B., Wang X., Ozkan U.S.
№ 5. С. 301 [Petrol. Chemistry. 2018. V. 58. № 11.
Deactivation characteristics of lanthanide-promoted sol-
P. 911.]
gel Ni/Al2O3 catalysts in propane steam reforming //
26.
Mironova E.Yu., Ermilova M.M., Orekhova N.V., Mura-
J. Catal. 2005. V. 234. P. 496.
viev D.N., Yaroslavtsev A.B. Production of high purity
13.
Takeguchi T., Kani Y., Yano T., Kikuchi R., Eguchi K., Tsu-
hydrogen by ethanol steam reforming in membrane re-
jimoto K., Uchida Y., Ueno A., Omoshiki K., Aizawa M.
actor // Catal. Today. 2014. V. 236. P. 64.
Study on steam reforming of CH4 and C2 hydrocarbons
27.
Диденко Л.П., Савченко В.И., Семенцова Л.А., Чи-
and carbon deposition on Ni-YSZ cermets // J. Power
жов П.Е., Быков Л.А. Дегидрирование пропана в
Sources. 2002. V. 112. P. 588.
комбинированном мембранном реакторе с водород-
14.
Laosiripojana N., Assabumrungrat S. Catalytic steam
проницаемым палладиевым модулем // Нефтехимия.
reforming of methane, methanol, and ethanol over Ni/
2013. Т. 6. № 1. С. 30 [Petrol. Chemistry. 2013. V. 53.
YSZ: the possible use of these fuels in internal reforming
№ 1. P. 27.]
SOFC // J. Power Sources. 2007. V. 163. P. 943.
28.
Ermilova M., Kucherov A., Orekhova N., Finashina E.,
15.
Im Y., Lee J.H., Kwak B.S., Do J.Y., Kang M. Effective
Kustov L., Yaroslavtsev A. Ethane oxidative dehydroge-
hydrogen production from propane steam reforming
nation to ethylene in a membrane reactor with asymmet-
using M/NiO/YSZ catalysts (M = Ru, Rh, Pd, and Ag) //
ric ceramic membranes // Chem. Eng. Process: Process
Catal. Today. 2018. V. 303. P. 168.
Intensification. 2018. V. 126. P. 150.
НЕФТЕХИМИЯ том 61 № 1 2021
112
ДИДЕНКО и др.
29. Tsodikov M.V., Fedotov A.S., Antonov D.O., Uvarov V.I.,
membrane reactor: influence of the operating conditions
Luck F.C. Hydrogen and syngas production by dry re-
on the performance // Catal. Today. 2001. V. 67. P. 177.
forming of fermentation products on porous ceramic
35. Miachon S., Dalmon J.-A. Catalysis in membrane reac-
membrane-catalytic converters // Int. J. Hydrogen Ener-
tors: what about catalyst? // Topics in Catalysis. 2004.
gy. 2016. V. 41. № 4. P. 2424.
V. 29. P. 59.
30. Цодиков М.В., Федотов А.С., Антонов Д.О., Ува-
36. Tsuru T., Morita T., Shintani H., Yoshioka T., Asaeda M.
ров В.И., Хаджиев С.Н. // Патент РФ №2638 350.
Membrane reactor performance of steam reforming of
2017. Бюл. № 35.
methane using hydrogen-permeselective catalytic SiO2
31. Шигаров А.Б., Мещеряков В.Д., Кириллов В.А. При-
membranes // J. Membr. Sci. 2008.V. 316. P. 53.
менение Pd-мембран в каталитических реакторах
парового риформинга метана для производства чи-
37. Диденко Л.П., СеменцоваЛ.А., Чижов П.Е., Дорофее-
стого водорода // Теоретические основы химической
ва Т.В. Паровая конверсия метана и его смесей с про-
технологии. 2011. Т. 45. № 5. С. 504 [Theoret. Found.
паном в мембранном реакторе с промышленным ни-
of Chem. Engineering. 2011. V. 45. № 5. P. 595.]
келевым катализатором и фольгой из Pd-Ru-сплава //
32. Burkhanov G.S., Gorina N.B., Kolchugina N.B., Ro-
Нефтехимия. 2019. Т. 59. № 3. С. 271 [Petrol. Chem-
shan N.R., Slovetsky D.I., Chistov E.M. Palladium-based
istry. 2019. V. 59. № 4. P. 394.]
alloy membranes for separation of high purity hydrogen
38. Didenko L.P., Sementsova L.A., Chizhov P.E., Dorofee-
from hydrogen-containing gas mixtures // Platinum Met.
va T.V. Influence of the propane content in methane on
Rev. 2011. V.55. P. 3.
the parameters of steam reforming of a mixture in a
33. Moe J.M. Design of water-gas shift reactors // Chemical
membrane reactor with the industrial nickel catalyst and
Engineering Progress. 1962. V. 58. № 3.Р. 33.
34. Ciavarella P., Casanave D., Moueddeb H., Miachon S.,
Pd-Ru alloy foil // Int. J. Hydrogen Energy. 2019. V. 44.
Fiaty K., Dalmon J.-A. Isobutane dehydrogenation in a
P. 26396.
НЕФТЕХИМИЯ том 61 № 1 2021