ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2019, том 89, № 12, с. 1909-1914
УДК 546.661:535.37
ЛЮМИНЕСЦЕНТНЫЕ СВОЙСТВА СОЕДИНЕНИЙ
ЕВРОПИЯ(III) С ХИНАЛЬДИНОВОЙ КИСЛОТОЙ
И СЕРОСОДЕРЖАЩИМИ НЕЙТРАЛЬНЫМИ
ЛИГАНДАМИ
© 2019 г. И. В. Калиновская*
Институт химии Дальневосточного отделения Российской академии наук,
пр. 100-летия Владивостока 159, Владивосток, 690022 Россия
*e-mail: kalinovskaya@ich.dvo.ru
Поступило в Редакцию 26 апреля 2019 г.
После доработки 8 мая 2019 г.
Принято к печати 14 мая 2019 г.
Получены люминесцирующие комплексные разнолигандные соединения европия(III) c хинальдиновой
кислотой и серосодержащими нейтральными лигандами состава Eu(Quin)3∙D∙3H2O, гдe Quin - хиналь-
диновая кислота, D - диметилсульфоксид (DMSO), дигексилсульфоксид (DHSO), гидрат европия(III)
Eu(Quin)3·3H2O. Определен их состав и строение. Изучены термические и спектрально-люминесцентные
свойства комплексных разнолигандных соединений европия(III). Установлено, что хинальдинат-ион
координируется к иону европия(III) бидентатно. Проведен анализ штарковской структуры 5D0-7Fj (j = 0,
1, 2) переходов в низкотемпературных спектрах люминесценции комплексных соединений европия(III).
Ключевые слова: люминесценция, ион европия, комплексы европия, хинальдиновая кислота
DOI: 10.1134/S0044460X19120151
Комплексные соединения редкоземельных эле-
Присутствие двух функциональных групп в
ментов с карбоновыми кислотами являются од-
хинальдиновой кислоте и возможные различные
ним из перспективных классов люминесцентных
способы координации карбоксильных групп могут
соединений [1-6]. Структурное и композицион-
привести к образованию нескольких рядов хиналь-
ное разнообразие карбоновых кислот делают их
динатов редкоземельных элементов с нейтральны-
удобными модельными объектами для изучения
ми лигандами с интересными люминесцентными
взаимосвязи между физико-химическими свой-
свойствами. Например, нами были синтезиро-
ствами и молекулярными структурами компонен-
ваны комплексные хинальдинаты европия(III) с
тов. Карбоновые кислоты широко используются
островной и полимерной структурами [11-13].
в качестве мостиковых лигандов в многоядерных
Разнолигандные комплексные соединения евро-
комплексах f-элементов и, как и другие мостико-
пия(III) с хинальдиновой кислотой и другими ли-
вые лиганды, определяют свойства соединений в
гандами трудно получить: обычно кристаллизу-
целом, а также их склонность к образованию су-
ется осадок, содержащий несколько соединений
прамолекулярных систем [7-9]. Интенсивная лю-
[13]. Синтез и люминесцентные свойства хиналь-
минесценция, фотостабильность и высокая терми-
динатов европия(III) с азот- и фосфорсодержащи-
ческая устойчивость соединений редкоземельных
ми нейтральными лигандами описаны в работе
элементов позволяет использовать их в качестве
[14].
допантов в функциональные оптические матери-
В настоящей работе представлены результаты
алы для оптоэлектроники, лазерной техники, для
изучения термических и спектрально-люминес-
создания светотрансформирующих полимерных
центных свойств разнолигандных комплексных
материалов [10, 11].
соединений европия(III) с хинальдиновой кисло-
1909
1910
КАЛИНОВСКАЯ
Данные элементного анализа разнолигандных соединений европия(III) c хинальдиновой кислотой
Найдено, %
Вычислено, %
Соединение
Формула
C
H
N
Н
О
Eu
S
C
H
N
Н2О
Eu
S
2
Eu(Quin)3·3H2O
50.4
3.3
6.0
7.7
21.4
0.0
EuC30H24O9N3
50.1
3.3
5.8
7.5
21.1
0.0
Eu(Quin)3·DMSO·3H2O
48.3
4.1
5.1
6.7
18.8
4.3
EuC32H30O10N3S
48.0
3.8
5.3
6.8
19.0
4.0
Eu(Quin)3·DHSO·3H2O
41.1
3.3
4.6
6.0
16.1
3.7
EuC42H54O10N3S
40.9
3.2
4.5
5.7
16.2
3.4
той и серосодержащими нейтральными лиганда-
Область температур 90-135°С соответствует про-
ми состава Eu(Quin)3∙D∙3H2O, где Quin - анион
цессу дегидратации комплексных хинальдина-
хинальдиновой кислоты, D - диметилсульфоксид
тов европия(III), протекающему в одну стадию с
(DMSO), дигексилсульфоксид (DHSO), а также ги-
эндотермическим эффектом. Содержание воды,
драта европия(III) Eu(Quin)3·3H2O.
вычисленное по убыли массы образца, соответ-
ствует расчетному. На основании расчета потери
По данным элементного химического анализа
массы можно сделать вывод, что отщепление ней-
состав синтезированных комплексных соединений
тральных лигандов (DMSO, DHSO) протекает в
европия(III) отвечает формуле Eu(Quin)3·D·3H2O,
одну стадию c эндотермическим эффектом в ин-
где D - серосодержащий нейтральный лиганд
тервале 130-155°С. Для Eu(Quin)3·DMSO·3H2O
(см. таблицу). Полученные разнолигандные ком-
потеря массы на второй стадии составляет 10.5%.
плексные соединения европия(III) желтого цвета
Для Eu(Quin)3·DHSO·3H2O потеря массы состав-
растворимы только в полярных растворителях, не
ляет 24.6%. У данных комплексных соединений
разлагаются при длительном хранении. Для опре-
европия(III) на конец отщепления нейтрально-
деления гидратного состава, получения данных
го лиганда накладывается процесс разложения
о дегидратации, составе и разложении разноли-
комплексных соединений европия(III), поэтому
гандных комплексных хинальдинатов европия(III)
невозможно получить безводное комплексное со-
проведен их термогравиметрический анализ в
единение Eu(Quin)3. Интенсивная деструкция хи-
интервале температур 25-700°С. Характер раз-
нальдинатов, приводящая к образованию оксида
ложения комплексных соединений европия(III)
европия(III), наблюдается в интервале температур
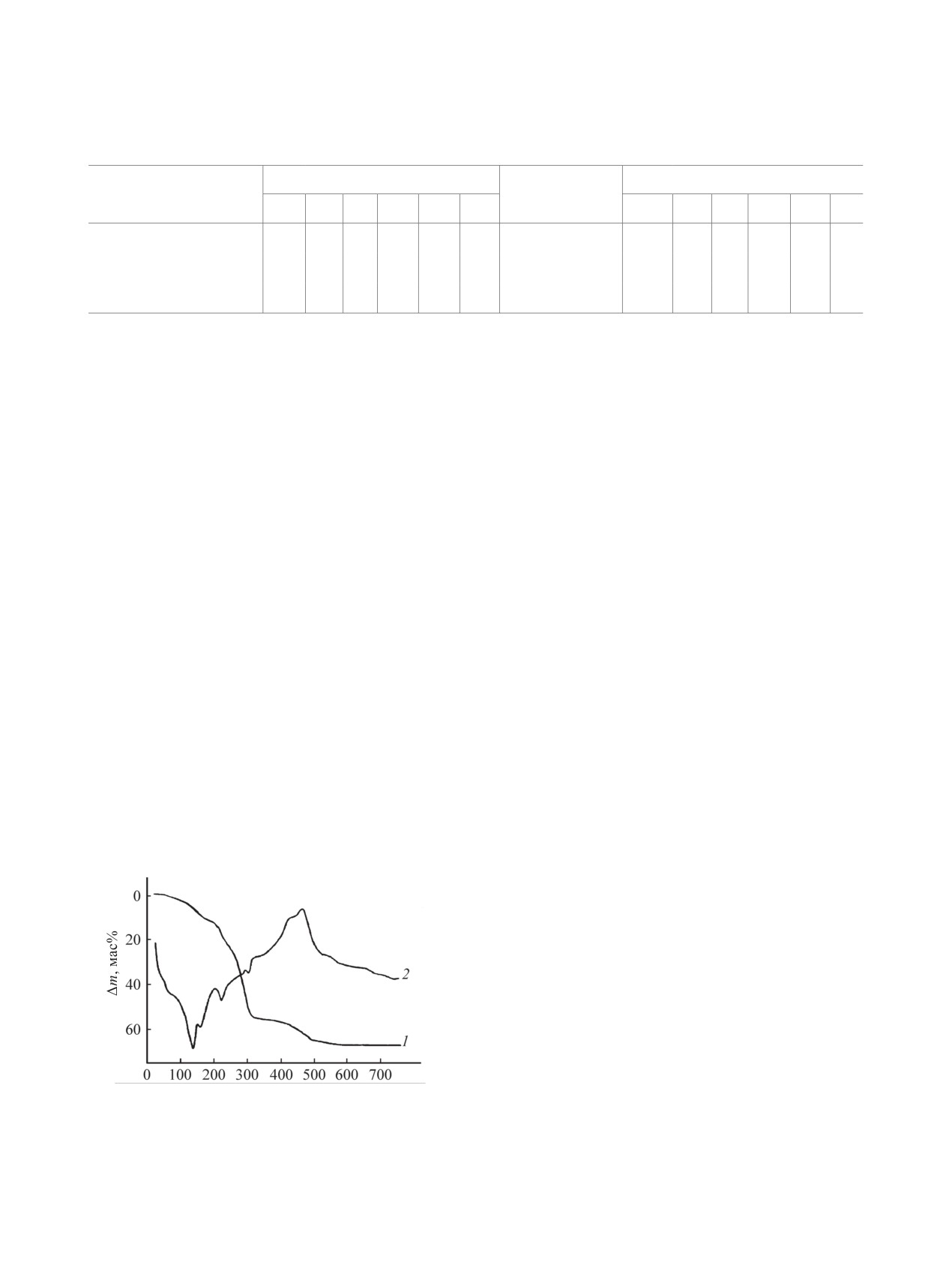
однотипен (рис. 1). Разложение происходит в че-
380-500°С.
тыре стадии. Термогравиметрический анализ ком-
Термическая устойчивость исследуемых ком-
плексных хинальдинатов европия(III) c серосо-
плексных соединений европия(III) ниже терми-
держащими нейтральными лигандами выявил на
ческой устойчивости хинальдинатов европия(III)
кривых ТГ и ДТА один эндотермический эффект,
полимерного строения [13] и сравнима с термиче-
который сопровождается потерей массы (рис. 1).
ской устойчивостью хинальдинатов европия(III)
с азотсодержащими нейтральными лигандами
островного строения [12]. По-видимому, наличие
связи иона европия(III) с двумя функциональными
группами в случае комплексных соединений поли-
мерного строения [12, 13] существенно повышает
термическую стабильность комплексных соедине-
ний европия(III).
ИК спектры полученных хинальдинатов евро-
пия(III) изучали в интервале частот 400-3600 см-1.
T, °C
На наличие депротонированной карбоксильной
Рис. 1. Данные термогравиметрического анализа ком-
группы в комплексных соединениях указывает
плекса Eu(Quin)3·DMSO·3H2O. 1 - ТГ, 2 - ДТА.
исчезновение полосы деформационного колеба-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 12 2019
ЛЮМИНЕСЦЕНТНЫЕ СВОЙСТВА СОЕДИНЕНИЙ ЕВРОПИЯ(III)
1911
1
2
3
250
275
325
375
Ȝ ɧɦ
Ȝ ɧɦ
Рис. 2. Электронные спектры поглощения Eu(Quin)3·
Рис.
3.
Спектры возбуждения люминесценции
DMSO·3H2O (1), Eu(Quin)3·DHSO·3H2O (2), Нquin
Eu(Quin)3·DMSO·3H2O
(1), Eu(Quin)3·DHSO·3H2O
(3), Eu(Quin)3·3H2O (4) в этаноле (с = 10-4 моль/л).
(2), Eu(Quin)3·3H2O (3) при 300 K (λlum = 615 нм).
ния ОН-группы при 990 см-1 [15, 16]. Поглощение
ет о бидентатной координации СОО--группы ио-
карбонильной группы свободной хинальдиновой
ном европия(III). Частоты ν(Eu-N) и ν(Eu-O) ле-
кислоты при 1705 см-1 в спектрах хинальдинатов
жат в спектрах синтезированных комплексов ниже
европия(III) отсутствует [17]. Интенсивные поло-
400 см-1 [16]. В спектре исследуемых комплекс-
ных соединений наблюдаются полосы поглощения
сы при 800-807, 1620-1630 и 1372-1385 см-1 от-
при 3300-3500 см-1 в области валентных коле-
носятся, соответственно, к полосам поглощения
баний воды [17, 18]. В ИК спектрах полученных
δ(ОСО-), γas(СОО-) и γs(СОО-) бидентатно связан-
комплексов полоса поглощения в области 1018-
ных карбоксильных групп, а поглощение меньшей
1020 см-1 соответствует частоте валентных коле-
интенсивности при 1469-1474 и 1594-1597 см-1
баний связи S=O. Кроме того, это значение ниже,
может быть обусловлено валентными колебания-
чем соответствующие значения, найденные для
ми связей С-С и С-N [17, 18]. Подобные полосы
свободных дигексил- и диметилсульфоксида
поглощения найдены в ИК спектрах хинальдина-
(1050-1100 см-1 [16]).
тов европия(III) островного строения. В работе
Электронные спектры поглощения разноли-
[13] на основании данных ИК и рентгеноэлектрон-
гандных хинальдинатов европия с серосодержа-
ной спектроскопии установлено, что хинальдино-
щими нейтральными лигандами представлены на
вая кислота в комплексных хинальдинатах европи-
рис. 2. Максимум широкой полосы λmax = 300 нм в
я(III) островного строения координируется биден-
УФ спектрах хинальдинатов европия(III) несколь-
татно. В ИК спектре синтезированных комплекс-
ко сдвинут в более длинноволновую область по
ных соединений европия особенно сильно про-
отношению к максимуму данной полосы в спектре
являются симметричные колебания карбоксиль-
свободной хинальдиновой кислоты. В спектрах
ной группы кислоты в области 1372-1385 см-1.
поглощения растворов разнолигандных хиналь-
Проявление этих колебаний также свидетельству-
динатов европия с серосодержащими нейтральны-
ет о существовании бидентатной координации
ми лигандами проявляются полосы поглощения
карбоксильной группы [16]. Разность частот Δν =
нейтральных cеросодержащих лигандов с λmax =
νas(СОО-) - νs(СОО-) больше 200 см-1, что указы-
290-294 и 308-312 нм, отсутствующие в спектре
гидрата хинальдината европия (рис. 2).
вает на ионный характер связи Eu-O карбоксиль-
ной группы хинальдиновой кислоты [17]. Согласно
Анализ электронных спектров поглощения по-
работе [18], величина Δν > 100 см-1 свидетельству-
зволил определить положение синглетных уров-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 12 2019
1912
КАЛИНОВСКАЯ
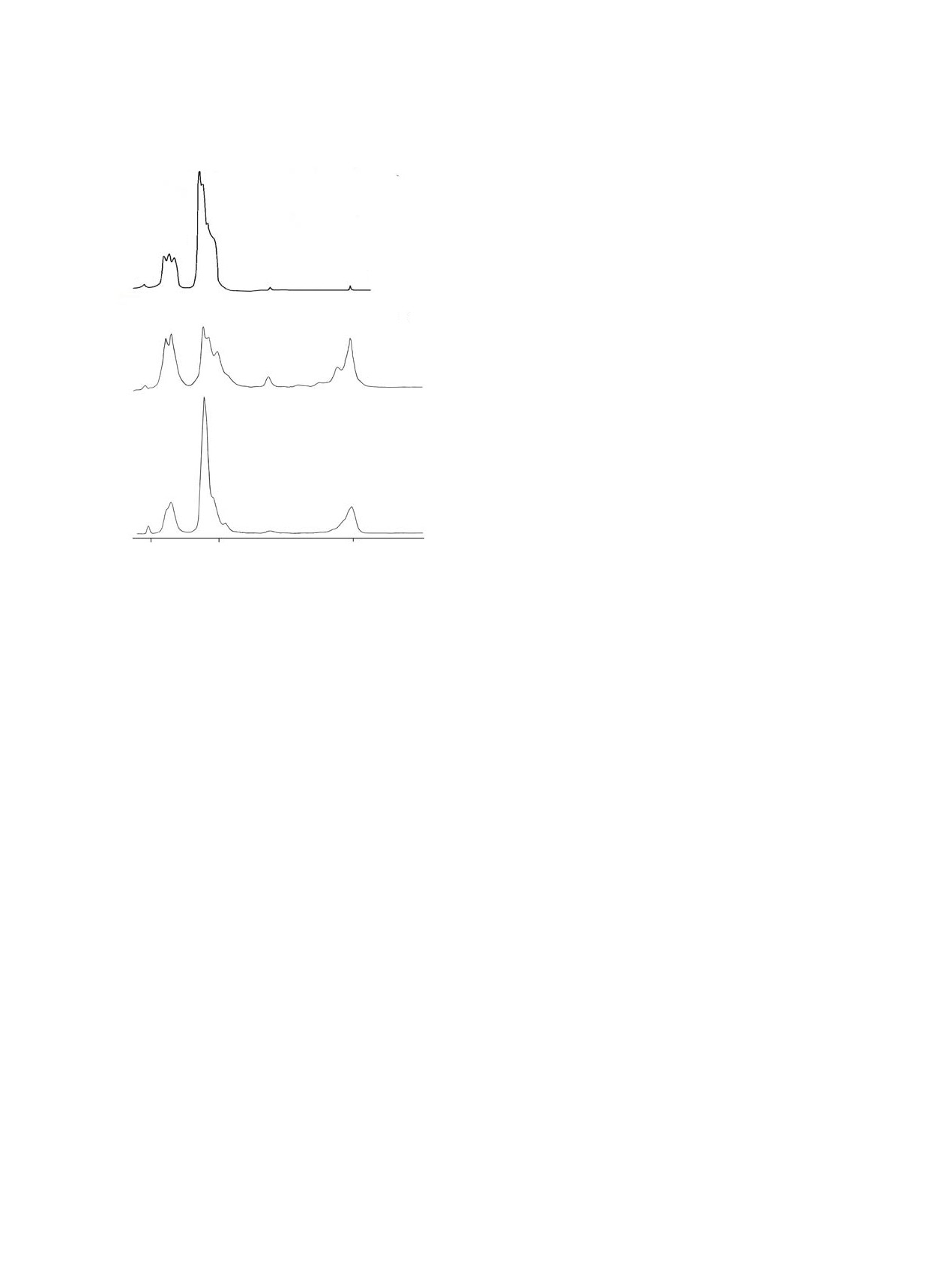
люминесценции при 612 нм (рис. 4). В спектрах
2
5D0-7F
люминесценции хинальдинатов европия(III) с се-
росодержащими нейтральными лигандами наи-
более интенсивны полосы, относящиеся к элект-
родипольному 5D0-7F2 переходу. Интенсивность
1
5D0-7F
полос, соответствующих триплетному магнитно-
1
5D0-7
F0
дипольному 5D0-7F1 переходую, ниже интенсив-
5D0-7F4
ности полос электродипольного 5D0-7F2 перехода.
Спектр люминесценции Eu(Quin)3·DMSO·3H2O
представляет значительный интерес, интенсивно-
2
сти переходов 5D0-7F1 и 5D0-7F4 практически та-
кие же как интенсивность 5D0-7F2 перехода.
Как и для большинства комплексных соедине-
ний европия(III) интенсивность линии запрещен-
ного 5D0-7F0 перехода невысока. Причем относи-
тельная интенсивность линии электродипольного
5D0-7F0 перехода увеличивается при переходе
3
от Eu(Quin)3·3H2O к Eu(Quin)3·DMSO·3H2O и
Eu(Quin)3·DHSO·3H2O. Одной из причин этого
580
615
700
Ȝ ɧɦ
может быть увеличение искажения координаци-
Рис. 4. Спектры люминесценции Eu(Quin)3·3H2O (1),
онного полиэдра комплексного соединения евро-
Eu(Quin)3·DMSO·3H2O (2), Eu(Quin)3·DHSO·3H2O (3)
пия при образовании аддуктов. Общий характер
при 300 K.
спектров люминесценции по исследуемому ряду
соединений европия с хинальдиновой кислотой
ней S: Quin (34960-35240 см-1), DMSO (47778-
сохраняется. Однако при замене серосодержащего
47790 см-1) и DHSO
(46882-46890 см-1).
нейтрального лиганда происходит существенное
Положение триплетного уровня хинальдиновой
перераспределение интенсивностей отдельных
кислоты определяли по спектру флуоресценции
линий 5D0-7F1,2 переходов. Замещение нейтраль-
хинальдината гадолиния (18602-17485 см-1 [13]).
ного лиганда при переходе от Eu(Quin)3·3H2O к
Спектры возбуждения люминесценции иссле-
Eu(Quin)3·DMSO·3H2O и Eu(Quin)3·DHSO·3H2O
дуемых комплексных соединений европия(III) по-
оказывает влияние на величину энергетического
казаны на рис. 3. В спектрах возбуждения люми-
зазора резонансного 5D0-7F0 перехода (смещение
несценции исследуемых соединений, в отличие от
О-О полосы в красную область), а также приводит
гидрата хинальдината европия(III), проявляются
к уменьшению величины расщепления штарков-
полосы в области (250-320 нм), относящиеся к пе-
ских компонент терма 7F1 (ΔF1).
реходам серосодержащих нейтральных лигандов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Это указывает на то, что происходит эффективная
передача энергии с уровней хинальдиновой кисло-
Для синтеза разнолигандных исследуемых
ты и серосодержащих нейтральных лигандов на
комплексных соединений европия(III) использо-
ион европия(III).
вали следующие реактивы марки Ч: шестиводный
Полученные разнолигандные комплексные сое-
нитрат европия(III), хинальдиновую кислоту, се-
динения европия(III) аналогично разнолигандным
росодержащие лиганды (диметилсульфоксид,
комплексным соединениям европия(III) с хиналь-
дигексилсульфоксид). Хинальдиновую кислоту
диновой кислотой и азотсодержащим нейтральны-
перекристаллизовывали из
96%-ного этанола.
ми лигандами островного строения [13] уже при
Разнолигандные комплексные соединения с хи-
комнатной температуре обладают интенсивной
нальдиновой кислотой и серосодержащими ней-
люминесценцией красного цвета с максимумом
тральными лигандами получали по методике [13].
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 12 2019
ЛЮМИНЕСЦЕНТНЫЕ СВОЙСТВА СОЕДИНЕНИЙ ЕВРОПИЯ(III)
1913
Полученные комплексные соединения евро-
2. Jin J., Li Y., Wang X., Chi Y., Niu S. // Struct. Chem.
пия(III) представляют собой мелкокристалличе-
2012. Vol. 23. N 5. P. 1523. doi 10.1007/s11224-012-
9957-6
ские порошки желтого цвета, растворимые в боль-
шинстве неполярных и полярных растворителей.
3. Калиновская И.В., Задорожная А.Н., Курявый В.Г.,
Термограммы соединений получены на деривато-
Карасев В.Е. // ЖФХ. 2207. Т. 81. № 7. С. 1147;
графе системы Паулик-Паулик-Эрдей. Скорость
Kalinovskaya I.V., Zadorozhnaya A.N., Kuryavji V.G.,
Kаrasev V.E. // Russ. J. Phys. Chem. 2007. Vol. 81.
нагрева 5 град/мин (в качестве эталона использо-
N 7. P. 1147. doi 10.1134/s0036024407070242
вали α-Al2O3).
4. Svakumar S., Reddy M.L.P., Cowley A.H., Vasude-
Низкотемпературные спектры люминесцен-
van K.V. // Dalton Trans. 2010. Vol. 39. N 3. 776. doi
ции регистрировали на спектрометре СДЛ-1 при
10.1039/B917256D
77 K, λexc = 365 нм. Возбуждение осуществляли
5. Bukvetskii B.V., Mirochnik A.G., Zhikhareva P.A. // Lu-
ртутной лампой ДРШ-250. Электронные спек-
minescence. 2017. Vol. 32. N 3. P. 341. doi 10.1002/
тры поглощения регистрировали на спектрометре
bio.3184
RF-2550 Shimadzu. Концентрация комплексных
6. Marques L.F., Cantariti A.B., Correa C.C., Lahoud M.G.,
соединений в 96%-ном этаноле составляла 10-4
Silva R.R., Riberto S.J.L., Machado F.C. // J. Photochem.
моль/л. Спектры возбуждения люминесценции
Photobiol. (A). 2013. Vol. 252. N 1 P. 69. doi 10.1016/j.
регистрировали на приборе RF-5301 рс Shimadzu.
jphotochem.2012.11.012
Рентгенограммы образцов снимали на дифракто-
7. Калиновская И.В., Карасев В.Е., Зайцева Н.Н. //
метре ДРОН-1.5 при СuKα-излучении. Содержание
ЖНХ. 1989. Т. 34. № 3. С. 618; Kаrаsev V.E.,
азота определяли методом Дюма, содержание
Kalinovskaya I.V. // Russ. J. Inorg. Chem. 1996. Vol. 41.
воды - титрованием по Фишеру. Для определения
N 5. P. 766.
содержания серы использовали энергодисперси-
8. Seminara A., Musumeci A.J. // Inorg. Nucl. Chem. 1977.
онный рентгенофлуоресцентный спектрометр
Vol. 39. N 4. P. 599. doi 10.1016/0022-1902(77)80572-1
Shimadzu EDX-800 HS. Образцы прессовали с
9. Bukvetskii B.V., Kalinovskaya I.V. // J. Fluorescence.
борной кислотой в качестве субстрата. Время из-
2017. Vol. 27. N 3. P.773. doi 10.1007/s10895-016-
мерения в каждой области Ti-U, C-Sc составило
2009-7
100 с. Для регистрации ИК спектров использо-
10. Sage I., Bourhil G. // J. Mater. Chem. 2001. Vol. 11.
вали спектрометр Tensor-27 Bruker (область 350-
N 2. P. 231. doi 10.1039/B007029J
4000 см-1). Спектры регистрировали для образцов
11. Калиновская И.В., Мирочник А.Г., Карасев В.Е. //
в таблетках с KBr.
ЖПХ. 2008. Т. 81. № 12. С. 2073; Kalinovskaya I.V.,
ФОНДОВАЯ ПОДДЕРЖКА
Mirochnik A.G., Kаrasev V.E. // Russ. J. Appl.
Chem. 2008. Vol. 81. N 12. P. 2183. doi 10.1134/
Работа выполнена при финансовой поддержке
S1070427208120306
Министерства образования и науки в рамках госу-
12. Калиновская И.В., Мирочник А.Г., Карасев В.Е. //
дарственного задания (№ 0265-2014-0001).
ЖНХ. 1991. Т. 36. № 3. С. 618; Kalinovskaya I.V.,
Mirochnik A.G., Kаrasev V.E. // Russ. J. Inorg. Chem.
КОНФЛИКТ ИНТЕРЕСОВ
1991. Vol. 36. N 7. P. 1778.
Авторы заявляют об отсутствии конфликта
13. Kalinovskaya I.V., Kаrasev V.E., Zaitseva N.N. // Russ.
интересов.
J. Inorg. Chem. 1989. Vol. 34. N 3. P. 618.
14. Калиновская И.В. // Оптика и спектр. 2016. Т. 120.
СПИСОК ЛИТЕРАТУРЫ
№ 6. С. 988; Kalinovskaya I.V. // Оpt. Spectr. 2016.
1. Duarte M.G., Prata M.I.M., Gil M.H.M., Geral-
Vol. 120. N 6 . P. 948. doi 10.1134/S0030400X16060102
des C.F.G.C. // J. Alloys Compd. 2002. Vol. 344. N 1.
15. Hollerman W.A., Fontenot R.S., Bha K.N., Aggar-
P. 4. doi 10.1016/S0925-8388(02)00295-5
wal M.D., Guidry C.J., Nguyen K.M. // Opt. Mater.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 12 2019
1914
КАЛИНОВСКАЯ
2012. Vol. 34. N 3. P. 1517. doi 10.1016/j.opt-
17. Zolin V., Puntus L., Kudryashova V.V., Tsaryuk V.,
Legendziewicz J., Gawryszewska P., Szostak R. // J.
mat.2012.03.011
Alloys Compd. 2002. Vol. 341. P. 376. doi 10.1016/j.
16. Nakamoto K. Infrared and Raman Spectra of Inorganic
jallcom.2004.03.055
and Coordination Compounds. Hoboken: Wiley, 2009.
18. Йохансен А.В., Куркчи А, Дементьева Л.А. // ЖСХ.
416 p.
1977. Т. 18. № 2. С. 743.
Luminescent Properties of Europium(III) Complexes
with Quinaldic Acid and Sulfur-Containing Neutral Ligands
I. V. Kalinovskaya*
Institute of Chemistry, Far Eastern Branch of the Russian Academy of Sciences,
pr. 100-Letiya Vladivostoka 159, Vladivostok, 690022 Russia
*e-mail: kalinovskaya@ich.dvo.ru
Received April 26, 2019; revised May 8, 2019; accepted May 14, 2019
The luminescent complex multi-ligand compounds of europium(III) with quinaldic acid and sulfur-containing
neutral ligands Eu(Quin)3∙D∙3H2O (Quin - quinaldic acid, D - dimethyl sulfoxide, dihexyl sulfoxide) and
Eu(Quin)3·3H2O were obtained. Their composition and structure were determined. The thermal and spectral-
luminescent properties of multi-ligand europium(III) complex compounds were studied. The quinaldinate ion
was found to coordinate to the europium(III) ion in a bidentate manner. An analysis was made of the Stark
structure of 5D0-7Fj (j = 0, 1, 2) transitions in the low-temperature luminescence spectra of europium(III)
complex compounds.
Keywords: luminescence, europium ion, europium complexes, quinaldic acid
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 12 2019