ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2019, том 89, № 3, с. 464-467
ПИСЬМА В
РЕДАКЦИЮ
УДК 547.332;547.391.1;547.323;547.26
АЛКИЛ-3-БРОМ-3-НИТРОАКРИЛАТЫ В РЕАКЦИЯХ
С АЛИФАТИЧЕСКИМИ СПИРТАМИ
© 2019 г. С. В. Макаренко*, В. В. Пелипко, М. М. Павченко, Р. И. Байчурин
Российский государственный педагогический университет имени А. И. Герцена,
наб. р. Мойки 48, Санкт-Петербург, 191186 Россия
Поступило в Редакцию 11 октября 2018 г.
После доработки 26 октября 2018 г.
Принято к печати 27 октября 2018 г.
Взаимодействие алкил-3-бром-3-нитроакрилатов с алифатическими спиртами протекает при кипячении и
приводит к образованию О-аддуктов - алкил-2-алкокси-3-бром-3-нитропропаноатов, выделяемых в виде
смесей диастереомеров; их строение охарактеризовано с использованием методов ЯМР 1Н, 13С-{1H} и
ИК спектроскопии.
Ключевые слова: нитроакрилаты, спирты, нуклеофильное присоединение, диастереомеры, диастереотопия
DOI: 10.1134/S0044460X1903020X
Геминальные бромнитроэтены, благодаря высокой
Изученное нами взаимодействие препаративно
реакционной способности и широкому диапазону
доступных представителей β-функционализиро-
химических свойств, активно используются в
ванных гем-бромнитроэтенов
- алкил-3-бром-3-
реакциях с нуклеофилами при целенаправленном
нитроакрилатов 1 и 2 [14] - с алифатическими
синтезе разнообразно построенных органических
спиртами (метанол, этанол, изопропанол) показало,
молекул [1-8]. Вместе с тем их взаимодействие со
что процесс также требует кипячения в растворе
спиртами представлено довольно немногочислен-
соответствующего спирта, протекает в отсутствие
ными примерами
[9-13]. Так, реакции гем-
реагентов основного характера и завершается
бромнитроалкенов и -стиролов, протекающие при
образованием О-аддуктов
- алкил-2-алкокси-3-
кипячении в спирте [11], в присутствии гидроксида
бром-3-нитропропаноатов
3-8,
выделяемых
калия [9, 10] или при использовании алкоксидов
методом колоночной хроматографии на силикагеле
натрия [9, 11], приводят к получению О-аддуктов.
(элюент - CCl4) в виде слабоокрашенных под-
Следует отметить, что
1-бром-1-нитро-3,3,3-
трихлор-1-пропен, содержащий в молекуле гем-
вижных масел с выходами
64-74% (схема
1).
бромнитровинильный фрагмент, образует О-
Отметим, что не содержащий атома брома этил-3-
аддукты в реакциях со спиртами также при
нитроакрилат реагирует со спиртами в сопоста-
кипячении, но в отсутствие основания [13].
вимых условиях [15].
Схема 1.
RO2C
Br
RO2C
Br
, 46 ч
*
*
+ AlkOH
HB
HA
H
NO2
AlkO
NO2
1, 2
3а, б8а, б
R = Me (1), Et (2); R = Me, Alk = Me (3), Et (4), i-Pr (5); R = Et, Alk = Me (6), Et (7), i-Pr (8).
464
АЛКИЛ-3-БРОМ-3-НИТРОАКРИЛАТЫ
465
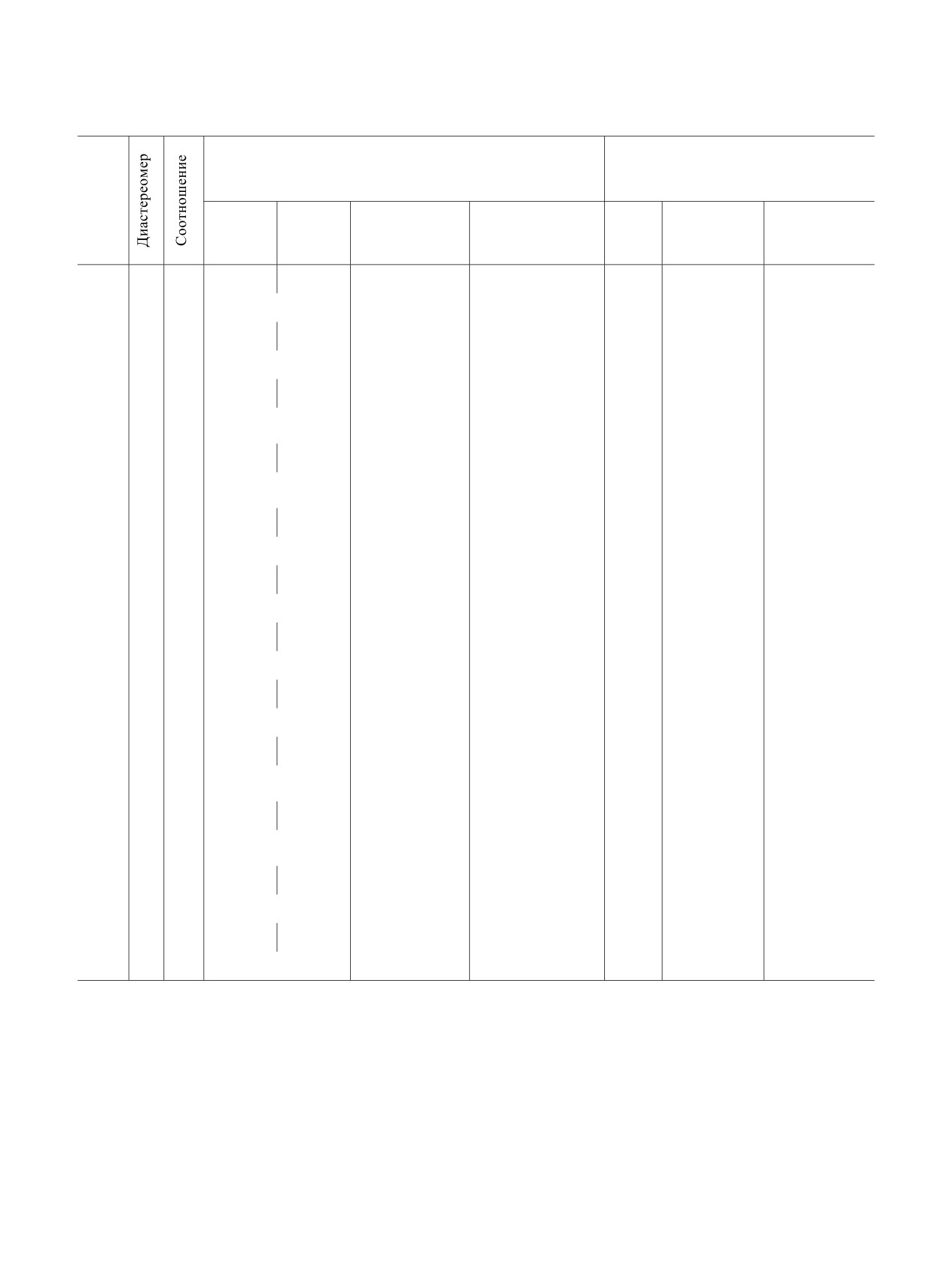
Данные спектроскопии ЯМР 1Н и 13С-{1H} для алкил-2-алкокси-3-бром-3-нитропропаноатов 3-8
δH, м. д. (J, Гц)
δС, м. д.
№
CH3O,
CH3O,
CO2Me
C3
CO2Me
HA
HB
(СН3CH2O)
(СН3CH2O)
(CO2Et)
(C2)
(CO2Et)
[(CH3)2CHO]
[(CH3)2CHO]
3
а
1.5
6.07 д
4.42 д
3.86 c
3.51 c
75.60
53.25, 166.96
60.44
(82.38)
3J
AB = 7.9
б
1
6.37 д
4.74 д
3.85 c
3.58 c
80.23
53.33, 167.29
60.43
(80.85)
3J
AB = 3.9
4
а
1.9
6.06 д
4.50 д
3.84 c
(1.18 т, 3.76 д. к,
75.64
53.15, 167.34
(14.82, 68.89)
3.60 д. к, 3J = 7.0,
(80.89)
3JAB = 8.2
2J = 9.2)
б
1
6.36 д
4.80 д
3.83 c
(1.23 т, 3.91 д. к,
80.32
53.23, 167.69
(14.82, 68.76)
3.59 д. к, 3J = 7.0,
(79.33)
3JAB = 4.1
2J = 9.2)
5
а
2.4
6.02 д
4.57 д
3.83 с
[1.13 д, 1.16 д, 3.78
75.92
53.13, 167.89
[21.47, 22.37,
септет, 3J = 6.4]
(79.41)
75.59]
3J
AB = 8.2
б
1
6.35 д
4.86 д
3.82 с
[1.14 д, 1.24 д, 3.81
80.87
53.20, 168.11
[21.20, 22.45,
септет, 3J = 6.1]
(77.63)
74.98]
3J
AB = 4.3
6
а
1
6.06 д
4.37 д
(1.32 т, 4.20-
3.49 c
75.73
(14.12, 62.61,
60.27
4.35 м)
(82.39)
166.38)
3J
AB = 7.9
б
1
6.36 д
4.69 д
(1.31 т, 4.20-
3.56 c
80.28
(14.14, 62.70,
60.29
4.35 м)
(80.81)
166.70)
3J
AB = 3.8
7
а
1.8
6.05 д
4.48 д
(1.33 т, 4.20-
(1.18 т, 3.61 д. к,
75.70
(14.13,
(14.89, 68.78)
4.40 м)
3.76 д. к, 3J = 7.0,
(80.94)
62.52, 166.81)
3JAB = 8.3
2J = 9.2)
б
1
6.36 д
4.77 д
(1.31 т, 4.20-
(1.23 т, 3.60 д. к,
80.40
(14.15,
(14.89, 68.69)
4.40 м)
3.91 д. к, 3J = 7.0,
(79.31)
62.64, 167.13)
3JAB = 4.2
2J = 9.2)
8
а
2.4
5.97 д
4.51 д
(1.33 т, 4.19-
[1.13 д, 1.17 д, 3.78
75.73
(14.14, 62.25,
[21.54, 22.49,
4.36 м)
септет, 3J = 6.1]
(79.48)
167.11)
75.43]
3J
AB = 8.6
б
1
6.31 д
4.78 д
(1.32 т, 4.19-
[1.14 д, 1.25 д, 3.83
80.70
(14.16,
[21.23, 22.56,
4.36 м)
септет, 3J = 6.1]
(77.60)
62.40, 167.38)
74.80]
3J
AB = 4.5
Полученные аддукты 3-8, судя по данным ЯМР
спинового взаимодействия (КССВ)
между ними
1H (см. таблицу), существуют в виде смеси двух
(3JAB = 7.9-8.6 Гц), в то время как изомеры б -
диастереомеров а и б с преимущественным содер-
слабопольное расположение этих дублетов и
жанием диастереомера а. При этом изомеры а
меньшие значения КССВ (3JAB = 3.8-4.5 Гц).
демонстрируют в спектрах ЯМР 1Н расположение
дублетов метиновых протонов HA и HB в сильном
Наличие в молекуле соединений 3-8 хиральных
поле, а также большие значения констант спин-
центров создает условия для проявления в спектрах
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 3 2019
466
МАКАРЕНКО и др.
ЯМР
1Н эффекта диастереотопии протонами
Метил-3-бром-2-изопропокси-3-нитропропаноат
соседних с ними СН2-групп. Действительно, в
(5) получали аналогично из бромнитроакрилата 1
спектрах ЯМР 1Н соединений 4 и 7 метиленовые
(0.416 г, 2.0 ммоль) и 5 мл изопропанола; время
протоны этоксигруппы при С2-атоме образуют два
реакции - 5 ч. Выход 0.395 г (74%), Rf = 0.44. ИК
дублета квартетов в областях 3.59-3.61 и 3.76-
спектр, ν, см-1: 1750 ш (C=O), 1573, 1354 (NO2).
3.91 м. д. (3J = 7.0, 2J = 9.2 Гц), что согласуется с
Найдено, %: С 31.01; H 4.38; N 5.12. C7H12BrNO5.
результатами dqf-COSY экспериментов, получен-
Вычислено, %: C 31.11; H 4.44; N 5.19.
ных для этих веществ.
Этил-3-бром-2-метокси-3-нитропропаноат (6)
В спектрах ЯМР 13С-{1H} алкоксибромнитро-
получали аналогично из бромнитроакрилата
2
пропаноатов
3-8 сигналы атомов С2 и С3
(0.522 г, 2.3 ммоль) и 5 мл метанола; время реакции -
диастереомеров a проявляются удаленно друг от
6 ч. Выход 0.417 г (69%), Rf = 0.48. ИК спектр, ν, см-1:
друга, а для диастереомеров б
- сближено.
1761 пл, 1746 (C=O), 1574, 1345 (NO2). Найдено, %:
Принятое отнесение сигналов в спектрах 1H и 13C-
С 28.38; H 3.97; N 5.53. C6H10BrNO5. Вычислено,
{1H} продуктов 3-8 подтверждают результаты 1Н-
%: C 28.13; H 3.91; N 5.47.
13С HMQC и 1H-13C HMBC экспериментов.
Этил-3-бром-3-нитро-2-этоксипропаноат
(7)
ИК спектры соединений 3-8 содержат полосы
получали аналогично из бромнитроакрилата
2
поглощения асимметричных (νas 1573-1574 см-1) и
(0.522 г, 2.3 ммоль) и 5 мл этанола; время реакции -
симметричных (νs
1345-1355 см-1) колебаний
6 ч. Выход 0.396 г (64%), Rf = 0.45. ИК спектр, ν, см-1:
несопряженной нитрогруппы, а также валентных
1760, 1744 (C=O), 1573, 1355 (NO2). Найдено, %: С
колебаний карбонильной группы сложноэфирной
31.33; H 4.46; N 5.30. C7H12BrNO5. Вычислено, %:
функции (νC=O
1745-1765 см-1). Наблюдаемое
C 31.11; H 4.44; N 5.19.
удвоение полосы поглощения карбонильной
Этил-3-бром-2-изопропокси-3-нитропропаноат
группы в ИК спектрах соединений 3, 4, 6, 7 может
(8) получали аналогично из бромнитроакрилата 2
быть связано с проявлением резонанса Ферми [16].
(0.302 г, 1.3 ммоль) и 5 мл изопропанола; время
Таким образом, на основе реакций алкил-3-бром-
реакции - 4 ч. Выход 0.262 г (68%), Rf = 0.51. ИК
3-нитроакрилатов с алифатическими спиртами
спектр, ν, см-1: 1745 ш (C=O), 1573, 1354 (NO2).
осуществлен синтез алкил-2-алкокси-3-бром-3-
Найдено, %: С 33.90; H 4.92; N 4.78. C8H14BrNO5.
нитропропаноатов, существующих в виде смесей
Вычислено, %: C 33.80; H 4.94; N 4.93.
диастереомеров.
Физико-химические исследования выполнены с
Алкил-3-бром-3-нитроакрилаты 1, 2 получали
использованием оборудования Центра коллектив-
по модифицированной методике [14].
ного пользования факультета химии Российского
государственного педагогического университета
Метил-3-бром-2-метокси-3-нитропропаноат (3).
им. А. И. Герцена.
Раствор 0.511 г (2.4 ммоль) бромнитроакрилата 1 в
5 мл метанола кипятили 4 ч. После удаления
Спектры ЯМР 1H, 13C-{1H}, 1Н-1Н dqf-COSY,
растворителя получали
0.540 г светло-желтого
1Н-13С HMQC, 1Н-13С HMBC зарегистрированы на
масла, которое хроматографировали на силикагеле
спектрометре Jeol ECX400A с рабочими частотами
[Chemapol
100/250]. Из фракций, вымываемых
399.78 МГц (1H) и 100.53 (13С); растворитель -
четыреххлористым углеродом, выделяли 0.369 г
хлороформ-d. В качестве стандарта использованы
(63%) соединения 3, Rf = 0.40. ИК спектр, ν, см-1:
остаточные сигналы недейтерированного раство-
1765 пл, 1751 (C=O), 1574, 1353 (NO2). Найдено, %:
рителя. ИК спектры получены на Фурье-
С 24.90; H 3.40; N 6.03. C5H8BrNO5. Вычислено, %:
спектрометре Shimadzu IR-Prestige-21 в хлоро-
C 24.79; H 3.31; N 5.79.
форме (с
=
40 мг/мл). Элементный анализ
выполнен на анализаторе EuroVector EA
3000
Метил-3-бром-3-нитро-2-этоксипропаноат (4)
(CHN Dual). Ход реакций и индивидуальность
получали аналогично из бромнитроакрилата
1
продуктов контролировали методом тонкослойной
(0.514 г, 2.4 ммоль) и 5 мл этанола; время реакции -
хроматографии на пластинках Silufol UV-254 с
6 ч. Выход 0.438 г (70%), Rf = 0.45. ИК спектр, ν, см-1:
использованием смеси растворителей гексан-
1765 пл, 1750 (C=O), 1573, 1354 (NO2). Найдено, %:
ацетон
(3:1), проявление парами иода и на
С 28.17; H 3.91; N 5.35. C6H10BrNO5. Вычислено,
хроматоскопе (l = 254 нм).
%: C 28.13; H 3.91; N 5.47.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 3 2019
АЛКИЛ-3-БРОМ-3-НИТРОАКРИЛАТЫ
467
КОНФЛИКТ ИНТЕРЕСОВ
8. Zhang J.-W., Yu L.-S.-H., Dong J.-L., Sun Q.-C., Xie J.-W. //
Synlett. 2018. Vol. 29. N 5. P. 603. doi 10.1055/s-0036-
Авторы заявляют об отсутствии конфликта
1591838
интересов.
9. Loevenich J., Koch J., Pucknat U. // Ber. 1930. Bd 63.
H 3. S. 636. doi 10.1002/cber.19300630316
СПИСОК ЛИТЕРАТУРЫ
10. Reichert B., Koch W. // Ber. 1935. Bd 68. H 3. S. 445.
doi 10.1002/cber.19350680315.
1. Perekalin V.V., Lipina E.S., Berestovitskaya V.M.,
11. Yamamura K., Watarai S., Kinugasa T. // Bull. Chem.
Efremov D.A. Nitroalkenes. Conjgated Nitrocompounds.
Chichester: John Wiley and Sons, 1994. 256 p.
Soc. Japan. 1971. Vol. 44. N 9. P. 2440. doi 10.1246/
bcsj.44.2440
2. Soengas R.G., Acúrcio R.C., Silva A.M.S. // Eur. J. Org.
Chem.
2014. N
29. P.
6339. doi
10.1002/
12. Shiga M., Tsunashima M., Kono H., Motoyama I., Hata K. //
ejoc.201402043
Bull. Chem. Soc. Japan. 1970. Vol. 43. N 3. P. 841. doi
3. Soengas R.G., Rodríguez-Solla H., Silva A.M.S. Llavona R.,
10.1246/bcsj.43.841
Paz F.A.A. // J. Org. Chem. 2013. Vol. 78. N 24.
13. Стукань Е.В., Макаренко С.В., Беркова Г.А.,
P. 12831. doi 10.1021/jo4021634
Берестовицкая В.М. // ЖОХ. 2010. Т. 80. Вып. 12.
4. Berestovitskaya V.M., Ozerova O.Yu., Efimova T.P.,
С. 1998; Stukan’ E.V., Makarenko S.V., Berkova G. A.,
Gurzhiy V.V., Novikova T.A. // Mendeleev Commun.
Berestovitskaya V.M. // Russ. J. Gen. Chem.
2010.
2016. Vol.
26. N
4.
P.
323. doi
10.1016/
Vol. 80. N 12. P. 2460. doi 10.1134/S1070363210120108
j.mencom.2016.07.019
14. Саркисян З.М., Садиков К.Д., Смирнов A.C., Кужае-
5. Макаренко С.В., Садиков К.Д., Байчурин Р.И. //
ва A.A., Макаренко С.В., Анисимова H.A., Дейко Л.И.,
ХГС. 2018. Т. 54. № 5. С. 502; Makarenko S.V.,
Берестовицкая В.М. // ЖОрХ. 2004. Т. 40. Вып. 6.
Sadykov K.D., Baichurin R.I. // Chem. Heterocycl.
С. 944; Sarkisyan Z.M., Sadikov K.D., Smirnov A.S.,
Compd. 2018. Vol. 54. N 5. P. 502. doi 10.1007/s10593-
Kuzhaeva A.A., Makarenko S.V., Anisimova N.A.,
018-2296-9
Deiko L.I., Berestovitskaya V.M. // Russ. J. Org. Chem.
6. Макаренко С.В., Байчурин Р.И., Гуржий В.В.,
2004. Vol.
40. N
6.
P.
908. doi
10.1023/
Байчурина Л.В. // Изв. АН. Сер. хим. 2018. № 5.
B:RUJO.0000044559.83690.b4
С. 815; Makarenko S.V., Baichurin R.I., Gurzhiy V.V.,
15. Anderson J.C., Kalogirou A.S., Tizzard G.J.
//
Baichurina L.V. // Russ. Chem. Bull. 2018. Vol. 67.
Tetrahedron. 2014. Vol. 70. N 49. P. 9337. doi 10.1016/
N 5. P. 815. doi 10.1007/s11172-013-0196-9
j.tet.2014.10.042
7. Baiju T.V., Almeida R.G., Sivanandan S.T., de Simone C.A.,
Brito L.M., Cavalcanti B.C., Pessoa C., Namboothiri I.N.N.,
16. Сильверстейн Р., Вебстер Ф., Кимл Д. Спектро-
da Silva Júnior E.N. // Med. Chem. 2018. Vol. 151.
скопическая идентификация органических соеди-
P. 686. doi 10.1016/j.ejmech.2018.03.079
нений. М.: БИНОМ. Лаборатория знаний, 2011. C. 93.
Alkyl 3-Bromo-3-nitroacrylates in Reactions
with Aliphatic Alcohols
S. V. Makarenko*, V. V. Pelipko, M. M. Pavchenko, and R. I. Baichurin
Herzen State Pedagogical University of Russia, nab. r. Moiki 48, St. Petersburg, 191186 Russia
*e-mail: kohrgpu@yandex.ru
Received October 11, 2018; revised October 26, 2018; accepted October 27, 2018
The reactions of alkyl 3-bromo-3-nitroacrylates with aliphatic alcohols at reflux led to the formation of O-adducts -
alkyl 2-alkoxy-3-bromo-3-nitropropanoates, released as mixtures of diastereomers; their structure was proved
using 1H, 13C-{1H} NMR and IR spectroscopy methods.
Keywords: nitroacrylates, alcohols, nucleophilic addition, diastereomers, diastereotopy
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 3 2019