ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2019, том 89, № 4, с. 607-612
УДК 547.979.733
СИНТЕЗ И КИНЕТИКА ДИССОЦИАЦИИ КОМПЛЕКСОВ
ЦИНКА, МЕДИ, КОБАЛЬТА, МАРГАНЦА
С 2,3,7,8,12,18-ГЕКСАМЕТИЛ-5-ФЕНИЛ-13,17-
ДИЭТИЛПОРФИНОМ И ЕГО НИТРОЗАМЕЩЕННЫМИ
АНАЛОГАМИ В ПРОТОНОДОНОРНЫХ СРЕДАХ
© 2019 г. Е. М. Кувшиноваa, *, М. А. Быковаa, И. А. Вершининаb,
О. В. Горнухинаa,c, А. С. Семейкинa,c
a Ивановский государственный химико-технологический университет,
пр. Шереметевский 7, Иваново, 153000 Россия
*е-mail: kuvshinovae@isuct.ru
b Институт химии растворов имени Г. А. Крестова Российской академии наук, Иваново, Россия
c Научно-исследовательский институт химии макрогетероциклических соединений
Ивановского государственного химико-технологического университета, Иваново, Россия
Поступило в Редакцию 15 ноября 2018 г.
После доработки 15 ноября 2018 г.
Принято к печати 24 ноября 2018 г.
Синтезированы нитрозамещенные
2,3,7,8,12,18-гексаметил-5-фенил-13,17-диэтилпорфины с нитро-
группами в положениях 10, 20 ядра порфирина и в пара-положении бензольного кольца. Структура
полученных соединений доказана данными ЯМР Н1, ИК спектроскопии, масс-спектрометрии и ЭСП.
Исследована кинетика диссоциации цинковых, медных, кобальтовых, марганцевых комплексов
полученных порфиринов в протонодонорных средах. Устойчивость порфириновых металлокомплексов
связана с электронными эффектами заместителей тетрапиррольного цикла и его пространственным
искажением.
Ключевые слова: порфирины, координационные свойства, кинетика диссоциации, металлокомплексы
DOI: 10.1134/S0044460X19040164
Порфирины катализируют многочисленные
фенил)-13,17-диэтилпорфин
3 были получены
химические, электрохимические и фотохимические
кислотной конденсацией
3,4-диметилпиррол-2-
реакции [1, 2], в связи с этим актуальна задача
карбальдегида 4 с 3,3'-диэтил-4,4'-диметилдипирро-
синтеза новых порфириновых соединений и
лилметаном
5 с последующей циклизацией
изучения их физико-химических свойств. Введение
Схема 1.
нитрогруппы в молекулу порфина
- один из
способов его модификации, которая приводит к
Me R1 Me
деформации макроцикла и к изменению его физико-
Me
химических свойств
[3-5]. В продолжение
Et
изучения влияния деформации тетрапиррольного
N
NH
макроцикла на его координационные свойства
R2
исследована устойчивость комплексов цинка, меди,
кобальта, марганца с
2,3,7,8,12,18-гексаметил-5-
N HN
Me
фенил-13,17-диэтилпорфином и его нитрозамещен-
Et
ными производными в протонодонорных средах
Me
R1 Me
(схема 1).
1-3
2,3,7,8,12,18-Гексаметил-5-фенил-13,17-диэтил-
R1 = R2 = H (1); R1 = NO2, R2 = H (2); R1 = H, R2 = NO2 (3).
порфин
1 и
2,3,7,8,12,18-гексаметил-5-(4-нитро-
607
608
КУВШИНОВА и др.
Схема 2.
Me
Me
Me
Me
Et
Et
Me
Me
HN+
NH
NH
HBr
2Br-
+ 2
CHOBuOH
N
NH HN
NH
H
Me
Et
Et
Me
Me
Me
5
4
6
CHO
Me
Me
Me
Et
NH
N
R2
R2
[O]
N HN
Me
Et
Me
Me
1-3
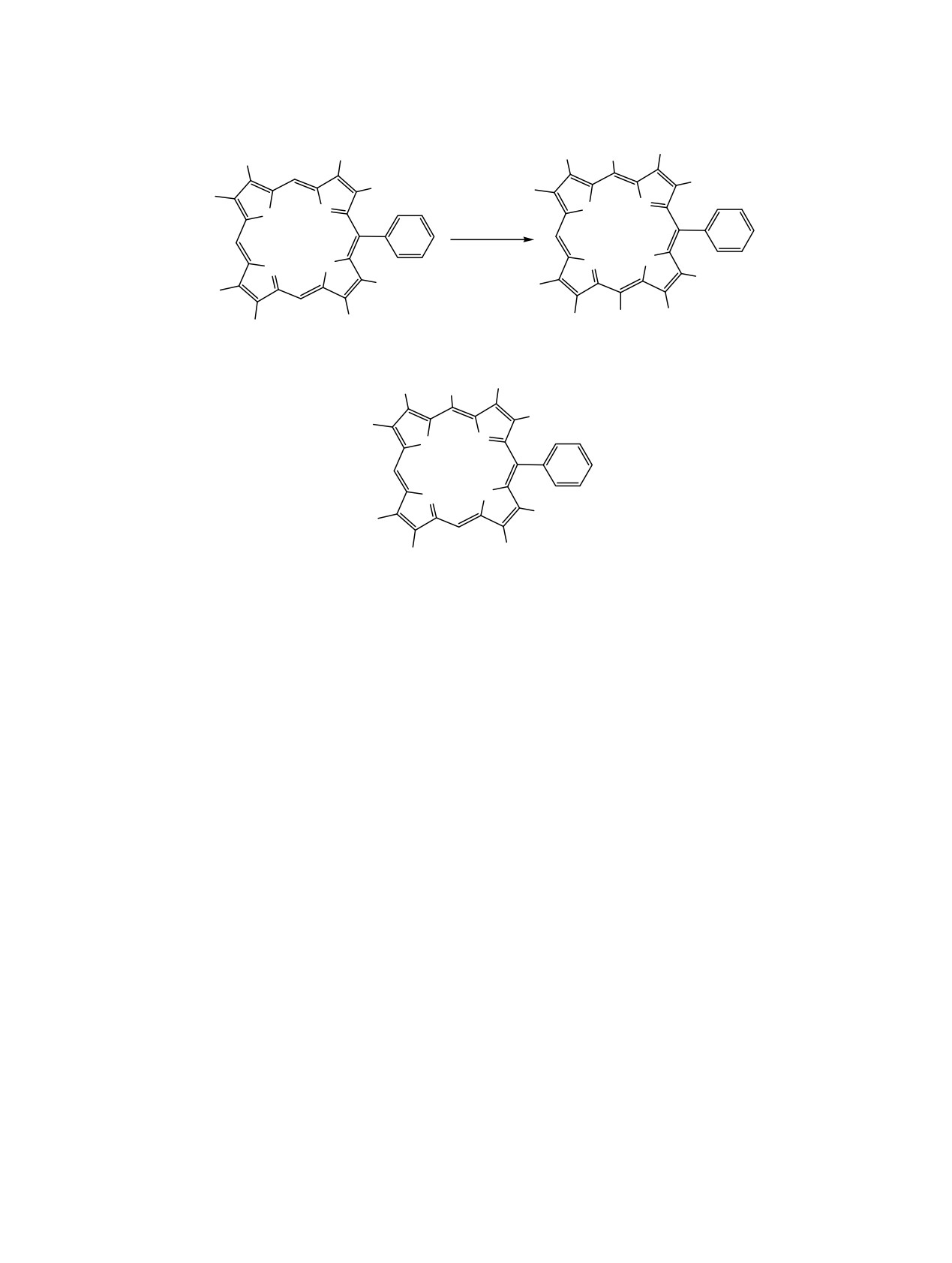
промежуточного биладиена 6 с бензальдегидом
образующегося
10,15-изомера
7 с помощью
(R2 = H) или 4-нитробензальдегидом (R2 = NO2) c
препаративной тонкослойной хроматографии на
дальнейшим окислением (схема 2) [6, 7].
силуфоле в бензоле.
2,3,7,8,12,18-Гексаметил-10,20-динитро-5-фенил-
Состав и cтроение полученных соединений
13,17-диэтилпорфин 2 был получен окислительным
доказана методами масс-спектрометрии MALDI-
электрофильным нитрованием порфирина
1
TOF, ЭСП, ЯМР Н1, ИК спектроскопии.
нитритом натрия в трифторуксусной кислоте [7]
Кинетику диссоциации цинковых (ZnP), медных
(схема 3) с последующим отделением от попутно
(CuP),
кобальтовых
(CoP),
марганцевых
[(АсО)MnP] комплексов порфиринов
1-3
исследовали в уксуснокислых растворах с 1.5%-
ной добавкой смеси H2SO4-CF3COOH, 1:1. Все
металлокомплексы (МР) диссоциируют
(1) с
образованием
дипротонированной
формы
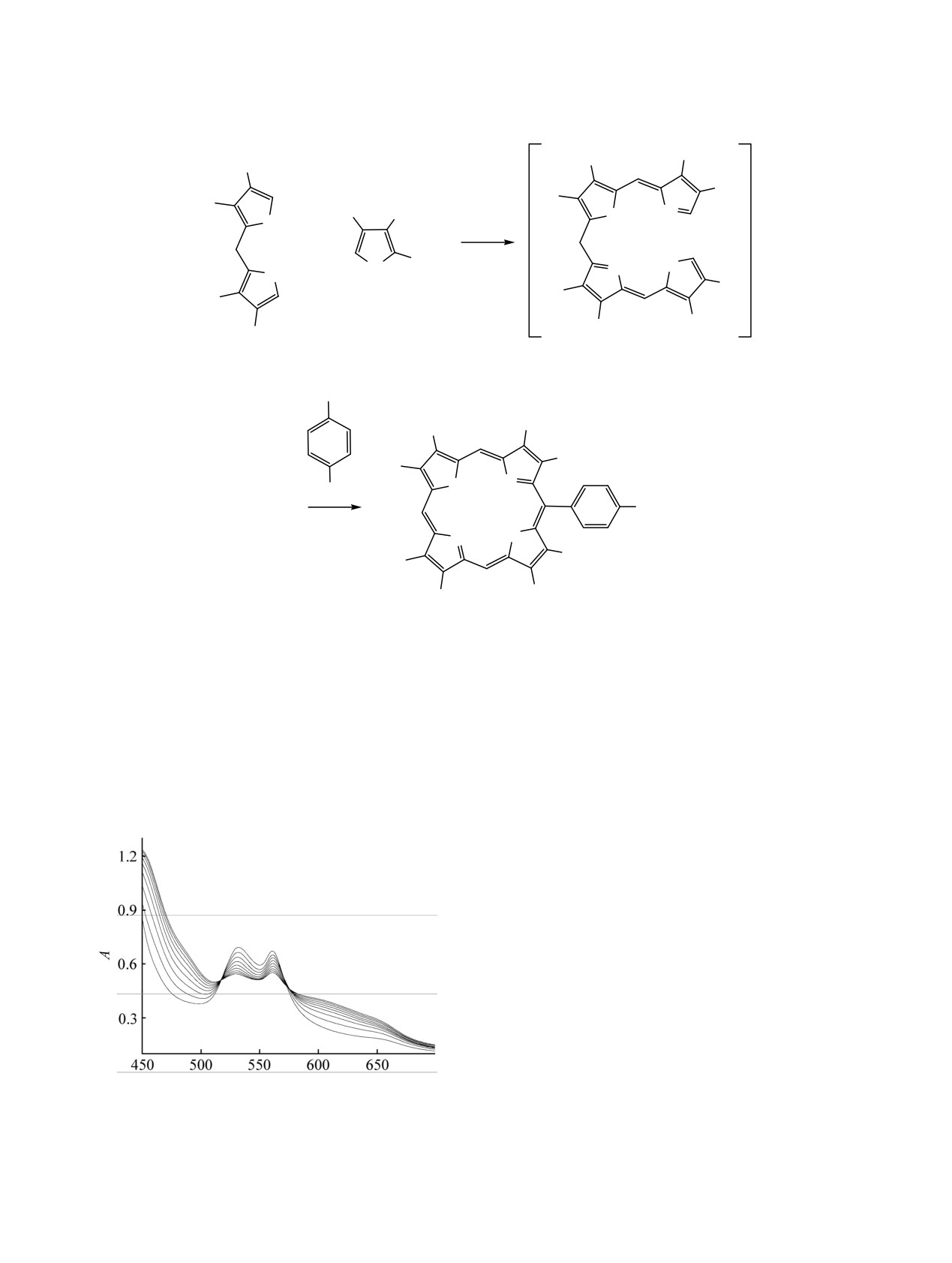
порфиринов (Н4Р2+). В спектрах всех реагирующих
систем наблюдались четкие изобестические точки
(см. рисунок).
МР + 4Н+ = М2+ + Н4Р2+.
(1)
Кинетические опыты проводили при
~100-
кратном избытке смеси H2SO4-CF3COOH, 1:1, по
отношению к МР, что позволяет рассчитать
λ, nm
эффективные константы скорости (kэф) по
Изменение ЭСП в ходе диссоциации CoР(1) в уксусной
уравнению (2).
кислоте с добавкой 1.5 мас% смеси H2SO4-CF3COOH,
1:1.
kэф = (1/t)ln[(А0 - А∞)/(А - А∞)].
(2)
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 4 2019
СИНТЕЗ И КИНЕТИКА ДИССОЦИАЦИИ КОМПЛЕКСОВ ЦИНКА, МЕДИ, КОБАЛЬТА
609
Схема 3.
Me
Me
Me O2N
Me
Me
Me
Et
Et
NH
N
NH
N
NaNO2
CF3CO2H
N HN
N HN
Me
Me
Et
Et
NO2
Me
Me
Me
Me
1
2
Me
Me O2N
Me
Et
NH
N
+
N HN
Me
Et
Me
Me
7
Здесь А0, А, А∞ - оптические плотности раствора в
Деформация тетрапиррольного макроцикла в
начальный момент, в момент времени t и по
порфириновой молекуле приводит к снижению его
окончании реакции соответственно.
ароматичности и увеличению электронной
плотности на центральных атомах азота [8, 11]. В
Энергию активации (Е) рассчитывали по
связи с этим возрастают основные свойства
уравнению (3).
порфиринов
[12,
13]. По мере увеличения
Е = 8.3Т1Т2/(Т2 - Т1)ln(k2/k1).
(3)
искажения плоского строения металлопорфирина
связи М-N становятся более доступными для атаки
Кинетические параметры диссоциации ком-
сольватированным протоном, что приводит к
плексов ZnP, CuP, CoP, (АсО)MnP приведены в
уменьшению его устойчивости.
таблице.
Увеличение деформации молекулы порфирина
При сопоставлении результатов таблицы видно,
при переходе от соединения
1 к нитро-
что по мере увеличения количества нитрогрупп в
производному 3 вызывает уменьшение скорости
молекуле порфирина наблюдается уменьшение
диссоциации и увеличение энергии активации для
константы скорости диссоциации Mn3+, Co2+ и Сu2+
всех исследованных металлокомплексов. По-
комплексов и увеличение энергии активации.
видимому, это связано с тем, что в металло-
Расчеты геометрических параметров структуры
комплексах порфиринов происходит частичное
методом РМ3 (силовое поле ММ+) показали, что
сглаживание
деформационных
искажений
ароматическое тетрапиррольное ядро порфирина 1
порфиринов, и структура макроцикла становится
плоское. Ведение нитрогрупп в мезо-положения 10
более плоской. Стерические искажения плоского
и
20 приводит к существенной деформации
строения порфиринов относительно мало влияют
макроцикла из-за пространственного взаимо-
на кинетические параметры сольвопротоли-
действия нитрогрупп с соседними метильными
тической
диссоциации
металлокомплексов.
заместителями.
Характер искажения ядра
Эффект деформации и
-I-эффект нитрогрупп
молекулы, приобретающего рифленую структуру,
оказывают противоположное влияние на скорость
типичен для непланарных порфиринов [8-10].
реакции диссоциации [5]. Очевидно, в этом случае
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 4 2019
610
КУВШИНОВА и др.
Кинетические параметры диссоциации цинковых, медных, кобальтовых и марганцевых комплексов порфиринов 1-3
в уксусной кислоте с добавкой 1.5 мас% смеси H2SO4-CF3COOH, 1:1
Е,
Kэф×103, с-1
Порфирин
λ, нм
кДж/моль
298 K
308 K
318 K
328 K
ZnP
Реакция протекает при сливании растворов
СuР
1
56±1
564
13±0.6
27.00±1.350
55.00±2.70
-
2
58±2
563
3.2±17
6.90±0.290
14.00±0.72
0.54±0.000
3
65±2
650
-
0.11±0.008
0.24±0.01
24
СоР
1
59±1
532
2.30±0.1100
5.000±0.2500
10.5±0.5
-
2
63±2
553
0.60±0.0300
1.400±0.0600
3±0.14
-
3
72±2
643
0.03±0.0013
0.079±0.0039
0.187±0.009
-
МnP
1
78±1
600
-
0.1100±0.0050
0.3±0.012
0.700±0.030
2
82±2
578
-
0.0720±0.0030
0.2±0.01
0.520±0.025
3
129±2
568
-
0.0048±0.0001
0.023±0.0011
0.103±0.006
определяющий вклад в энергетику переходного
ангидрида в течение 20 ч и перегоняли, используя
состояния вносит растяжение связей M-N из-за
дефлегматор. Содержание воды в растворителе
наличия в мезо-положениях 10, 20 порфирина и в
определяли титрованием по методу Фишера, оно
пара-положении бензольного кольца электроно-
составило 0.02 мас%. Моногидрат Н2SO4 получали
акцепторных нитрогрупп.
насыщением 95%-ной серной кислоты олеумом с
потенциометрическим контролем содержания
В ходе исследования установлено, что в зави-
воды. Трифторуксусную кислоту марки Ч
симости от природы катиона соли устойчивость
смешивали с концентрированной серной кислотой
металлокомплексов
уменьшается
в
ряду:
в соотношении
10:1. Обезвоженную кислоту
[(АсО)MnP](1-3) > CoР(1-3) > CuР(1-3) > ZnP(1-3).
отгоняли из смеси при атмосферном давлении,
Как и следовало ожидать, наиболее стабильными в
используя дефлегматор. Собирали фракцию с т.
протонодонорных средах оказались комплексы
кип. 72-73°С, затем повторно перегоняли.
трехзарядного катиона Mn3+вследствие высокой
прочности ковалентных связей Mn-N. Более
Электронные спектры поглощения (ЭСП)
высокая устойчивость CoР(1-3) по сравнению с
снимали на сканирующем спектрометре СПЕК
CuР(1-3) обусловлена склонностью
3d9-катиона
ССП-715 в хлороформе. ИК спектры регис-
Сu2+ к образованию квадратно-пирамидальных
трировали на спектрометре Avatar 360 FT-IR в
комплексов с ослабленными связями М-Solv
таблетках с KBr. Спектры ЯМР 1Н получены на
вследствие проявления Эффекта Яна-Теллера.
спектрометре Bruker
500 в дейтерохлороформе
Цинковые комплексы порфиринов 1-3 диссоци-
(внутренний стандарт
- сигнал остаточного
ируют при сливании растворов. Увеличение
хлороформа). Масс-спектры снимали на время-
скорости диссоциации при переходе от кобаль-
пролетном масс-спектрометре Shimadzu Axima
товых к цинковым комплексам также связано со
Confidence (MALDI-TOF).
структурой металлкомплексов этих металлов [14].
2,3,7,8,12,18-Гексаметил-5-фенил-13,17-ди-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
этилпорфин (1). ИК спектр, ν, см-1: 2961, 2923,
2863, 1446, 1264, 1226, 1117, 1062, 1030, 951, 834,
Уксусную кислоту марки ХЧ обезвоживали
751, 701. ЭСП, λmax, нм (lgε): 623 (3.51), 571 (3.83),
кипячением с расчетным количеством уксусного
536 (3.86), 502 (4.15), 403 (5.22). Спектр ЯМР 1H, δ,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 4 2019
СИНТЕЗ И КИНЕТИКА ДИССОЦИАЦИИ КОМПЛЕКСОВ ЦИНКА, МЕДИ, КОБАЛЬТА
611
м. д.: -3.18 уш. с и -3.27 уш. с (2H, NH), 10.19 с
(проект
№ 4.7305.2017/8.9) с использованием
(2H, H10,20), 9.98 с (1H, H15), 8.07 д (2H, H2,6-Ph, J =
оборудования Центра коллективного пользования
7.4 Гц), 7.82 т (1H, H4-Ph, J = 7.4 Гц), 7.75 т (2H,
Ивановского государственного химико-технологи-
H3,5-Ph, J = 7.4 Гц), 4.09 к (4H, CH2,13, 17-Et, J =
ческого университета и Верхневолжского регио-
7.7 Гц), 3.67 с (6H, 12,18-CH3), 3.55 с (6H, 2,8-CH3),
нального центра физико-химических исследований.
2.47 с (6H, 3,7-CH3), 1.90 т (6H, CH3, 13,17-Et, J =
7.7 Гц). Масс-спектр (MALDI-TOF), m/z: 526.184
КОНФЛИКТ ИНТЕРЕСОВ
[M]+. Мвыч 526.728.
Авторы заявляют об отсутствии конфликта
2,3,7,8,12,18-Гексаметил-10,20-динитро-5-фенил-
интересов.
13,17-диэтилпорфин (2). ИК спектр, ν, см-1: 2971,
2930, 2876, 1533, 1447, 1361, 1158, 1137, 1058, 947,
СПИСОК ЛИТЕРАТУРЫ
855, 798, 705, 664. ЭСП, λmax, нм (lgε): 648 (3.57),
591 (3.87), 518 (4.15), 413 (5.08). Спектр ЯМР 1Н, δ,
1. Березин Д.Б., Ениколопян Н.С. Металлопорфирины.
м. д.: -3.22 уш. с (2H, NH), 9.86 с (1H, H15), 8.04 д
М.: Наука, 1988. 160 с.
(2H, H2,6-Ph, J = 7.0 Гц), 7.85 т (2H, H4-Ph, J =
2. Vashurin A., Maizlish V., Kuzmin I., Petrov O.,
7.0 Гц), 7.80 т (4H, H3,5-Ph, J = 7.0 Гц), 3.61 к (4H,
Razumov M., Pukhovskaya S., Golubchikov O., Koi-
CH2, Et, J = 7.6 Гц), 3.20 с (6H, 12,18-CH3), 3.02 с
fman O. // J. Incl. Phenom. Mac. Chem. 2016. Vol. 1-2.
(6H, 2,8-CH3), 2.12 с (6H, 3,7-CH3), 1.56 т (6H, CH3,
P. 37. doi 10.1007/s10847-016-0674-4
Et, J = 7.6 Гц). Масс-спектр (MALDI-TOF), m/z:
3. Семейкин А.С., Колодина Е.А., Кувшинова Е.М.,
617.169 [M + H]+. Мвыч 617.793.
Сырбу С.А., Голубчиков О.А. // ЖОХ. 2012. Т. 82.
Вып.
3. С.
495; Semeikin A.S., Kolodina E.A.,
2,3,7,8,12,18-Гексаметил-5-(4-нитрофенил)-13,17-
Kuvshinova E.M., Syrbu S.A., Golubchikov O.A. // Russ.
диэтилпорфин (3). ЭСП, λmax, нм (lgε): 624 (3.50),
J. Gen. Chem. 2012. Vol. 82. N 3. P. 488. doi 10.1134/
573 (3.82), 537 (3.87), 505 (4.15), 403 (5.18). Спектр
S1070363212030218
ЯМР 1Н, δ, м. д.: -3.25 уш. с (2H, NH), 10.16 с (2H,
4. Кувшинова Е.М., Вершинина И.А., Сырбу С.А.,
H10,20), 9.97 с (1H, H15), 8.56 д (2H, H2,6-Ph, J =
Голубчиков О.А.
// Рос. хим. ж. 2015. Т. 59. № 4.
7.2 Гц), 8.20 д (2H, H3,5-Ph, J = 7.2 Гц), 4.05 к (4H,
С. 51; Kuvshinova E.M., Vershinina I.A., Syrbu S.A.,
CH2, Et, J = 7.4 Гц), 3.62 с (6H, 12,18-CH3), 3.62 с
Golubchikov O.A. // Russ. J. Gen. Chem. 2017. Vol. 87.
(6H, 2,8-CH3), 2.38 с (6H, 3,7-CH3). Масс-спектр
N 9. P. 2181. doi 10.1134/S1070363217090444
(MALDI-TOF), m/z: 571,363 [M]+. Мвыч 571.725.
5. Кувшинова Е.М., Вершинина И.А., Исляйкин М.К.,
Комплексы ZnP, CuP, CoP, (АсО)MnP
Сырбу С.А., Голубчиков О.А. // Рос. хим. ж. 2016.
получали кипячением порфиринов 1-3 с избытком
Т. 60. № 5. С. 35.
соответствующих ацетатов (цинка, меди, кобальта,
6. Kolodina E.A., Lubimova T.V., Syrbu S.A., Semeikin A.S. //
марганца) в смеси растворителей уксусная кислота-
Macroheterocycles. 2009. Vol. 2. N 1. P. 33.
хлороформ,
1:1,
и очищали двукратным
7. Колодина Е.А., Сырбу С.А., Семейкин А.С., Койф-
хроматографированием на оксиде алюминия III
ман О.И. // ЖОрХ. 2010. Т. 46. Вып. 1. С. 136;
степени активности по Брокману, элюент
-
Kolodina E.A., Syrbu S.A., Semeikin A.S. Koifman O.I. //
хлороформ. Чистоту комплексов контролировали
Russ. J. Org. Chem. 2010. Vol. 46. N. 1. P. 138. doi
по электронным спектрам поглощения.
10.1134/S107042801001015X
8. Barkigia K.M., Berber M.D., Fajer J., Medforth C.J.,
Кинетику диссоциации металлопорфиринов в
Renner M.W., Smith K.M. // J. Am. Chem. Soc. 1990.
уксусной кислоте, содержащей 1.5 мас% смеси
Vol. 112. N 24. P. 8851. doi 10.1021/ja00180a029
H2SO4-CF3COOH, 1:1, исследовали спектрофото-
9. Barkigia K.M., Fajer J., Berber M.D., Smith K.M. //
метрическим методом на приборе Shimadzu UV-
Acta Crystallogr. Sect. (C). 1995. Vol. 51. P. 511. doi
1800 в термостатируемых кюветах в интервале
10.1107/S0108270194008978
температур 298-338 K. Колебание температуры не
превышало ±0.1 K.
10. Medforth C.J., Hobbs J.D., Rodriguez M.R., Abraham R.J.,
Smith K.M., Shelnutt J.A. // Inorg. Chem. 1995. Vol. 34.
ФОНДОВАЯ ПОДДЕРЖКА
N. 6. P. 1333. doi 10.1021/ic00110a008
11. Кувшинова Е.М., Семейкин А.С., Сырбу С.А.,
Работа выполнена в рамках государственного
Голубчиков О.А // ЖФХ. 2010. Т. 84. № 9. С. 1666;
задания Министерства образования и науки РФ
Kuvshinova E.M., Semeikin A.S., Syrbu S.A.,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 4 2019
612
КУВШИНОВА и др.
Golubchikov O.A. // Russ. J. Phys. Chem. (A). 2010.
13. Березин Д.Б., Иванова Ю.Б., Шейнин В.Б. // ЖФХ.
Vol. 84. N 9. С. 1516. doi 10.1134/S0036024410090128
2007. Т. 81. № 12. С. 2205; Berezin D.B., Ivanova Yu.B.,
12. Advanced Biologically Active Polyfunctional Com-
Sheinin V.B. // Russ. J. Phys. Chem. (A). 2007. Vol. 81.
pounds and Composites: Health, Cultural Heritage and
N 12. P. 1986. doi 10.1134/S003602440712014X
Environmental Protection
/ Eds. N. Lekishvili, G.
14. Березин Б.Д., Голубчиков О.А. Координационная
Zaikov, B. Howell. New York: Nova Biomedical, 2010.
химия сольватокомплексов солей переходных
P. 169.
металлов. М.: Наука, 1992. 234 с.
Synthesis and Dissociation Kinetics of Zinc, Copper, Cobalt,
and Manganese Complexes with 2,3,7,8,12,18-Hexamethyl-
5-phenyl-13,17-diethylporphin and Its Nitro-Substituted Analogs
in Proton-Donor Media
E. M. Kuvshinovaa, *, M. A. Bykovaa, I. A. Vershininab,
O. V. Gornukhinaa,c, and A. S. Semeikina,c
a Ivanovo State University of Chemistry and Technology, Sheremetevskii pr. 7, Ivanovo, 153000 Russia
*e-mail: kuvshinovae@isuct.ru
b G.A. Krestov Institute of Solutions Chemistry of the Russian Academy of Sciences, Ivanovo, Russia
c Research Institute of Macroheterocyclic Chemistry, Ivanovo State University of Chemistry and Technology, Ivanovo, Russia
Received November 15, 2018; revised November 15, 2018; accepted November 24, 2018
Nitrosubstituted 2,3,7,7,8,12,18-hexamethyl-5-phenyl-13,17-diethylporphins with nitro groups in positions 10,
20 of the porphyrin core and in the para-position of the benzene ring were synthesized. The structure of the
compounds obtained was proved by H1 NMR, IR spectroscopy, mass spectrometry and UV spectroscopy. The
kinetics of dissociation of zinc, copper, cobalt, and manganese complexes of the obtained porphyrins in proton-
donor media was studied. The stability of porphyrin metal complexes is associated with the electronic effects of
substituents of the tetrapyrrole cycle and its spatial distortion.
Keywords: porphyrins, coordination properties, dissociation kinetics, metal complexes
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 4 2019