ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2019, том 89, № 8, с. 1151-1156
УДК 547.551.1;547.552;54-44
КОЛЛОИДНЫЕ И НАНОРАЗМЕРНЫЕ КАТАЛИЗАТОРЫ
В ОРГАНИЧЕСКОМ СИНТЕЗЕ:
XXI1. ВОССТАНОВЛЕНИЕ НИТРОАРЕНОВ
ПРИ КАТАЛИЗЕ ИММОБИЛИЗОВАННЫМИ
НАНОЧАСТИЦАМИ НИКЕЛЯ
© 2019 г. В. М. Мохов, Ю. В. Попов*, Д. Н. Небыков, Е. В. Нищик,
К. В. Щербакова, Ю. Л. Зотов
Волгоградский государственный технический университет, пр. Ленина 28, Волгоград, 400131 Россия
*e-mail: tons@vstu.ru
Поступило в Редакцию 12 марта 2019 г.
После доработки 12 марта 2019 г.
Принято к печати 14 марта 2019 г.
Установлено, что наночастицы никеля, нанесенные на цеолит NaX, γ-оксид алюминия, активированный
уголь или оксид магния катализируют процесс восстановления нитробензола и его гомологов с высо-
кими выходами анилина и его производных. Исследовано влияние подложки на проведение данных
процессов в непрерывном реакторе при атмосферном давлении водорода. Использование в качестве
носителя активированного угля или оксида магния позволяет проводить реакцию при 80-100°С.
Ключевые слова: катализ, наночастицы, никель, восстановление, нитроарены, анилин
DOI: 10.1134/S0044460X19080018
Основным способом получения анилина и его
дом восстановления адсорбированных солей ги-
С-замещенных гомологов, широко применяемых
дразингидратом. Содержание никеля в составе
в производстве красителей, полиуретанов и фар-
катализатора составляло около 5%, размер частиц
макологических препаратов [2-6], является гидри-
никеля - 2-8 нм. Катализатор Ni/TiO2 показал вы-
рование нитробензола в газовой или жидкой фазе.
сокую активность (конверсия до 99% при высокой
Большинство промышленных способов получения
селективности) [15], в то время как Ni/ZrO2 дезак-
предполагает применение жестких условий - вы-
тивировался при 250°С и длительной работе. Для
соких давлений или температур.
газофазного гидрирования нитробензола приме-
нялись также Ru/SBA15 (275°С, конверсия 94%,
Селективное восстановление нитроаренов в
производные анилина достигалось при катализе
селективность 100%) [16], Pd на гидротальките
(225°С, конверсия 99%, селективность 100%) [17],
рядом металлических катализаторов, таких как
Ni/SBA-15 (250°С, конверсия 97%, селективность
Au/TiO2 [7] палладий или платина на угле [8-10],
100%) [18], Cu/MgO (280°С, конверсия 94%, се-
двуокись платины [11], никель Ренея [12] или Ni/
лективность 100%) [19].
TiO2 [13]. В качестве катализаторов гидрирования
используются и сульфид никеля при 250-350°С [14].
Известно о применении наночастиц никеля в
В качестве катализаторов гидрирования ни-
виде коллоидных растворов в качестве катализа-
тробензола применялись наночастицы никеля,
тора восстановления нитрогруппы нитроаренов.
нанесенные на поверхность ZrO2 или TiO2 мето-
Так, нитробензол и его замещенные производные
восстанавливаются в соответствующие замещен-
1 Сообщение XX см. [1].
1151
1152
МОХОВ и др.
ные анилины при катализе наночастицами никеля,
Схема 1.
полученными восстановлением солей Ni(II) ги-
NO2
NH2
дразингидратом [20]. Гидрирование 4-нитрофено-
1 атм, 80-240°С
ла водородом также осуществлялось коллоидны-
R
+ 3H2
R
+ 2H2O
ми наночастицами никеля в автоклаве водородом
Ni0
при 100°С и 8 атм [21]. Обнаружена зависимость
1a-e
2a-e
активности катализатора от размеров наночастиц
R= H (а), 2-CH3 (б), 3-CH3 (в), 4-CH3 (г), 2-OCH3 (д),
никеля, в свою очередь, определяемых применяе-
4-OCH3 (е).
мым растворителем. Так, при уменьшении разме-
Нитроарены 1а-е восстанавливали в интервале
ров частиц с 300 до 60 нм конверсия нитробензо-
температур 160-240°С на наночастицах никеля,
ла за время реакции 2 ч повышается с 14 до 80%.
нанесенных на цеолит NaX при удельном рас-
Показано, что наночастицы никеля по сравнению
ходе исходного вещества 0.6 или 0.9 л/(кгкат∙ч) в
с никелем Ренея дают конверсию нитробензола в
зависимости от взятого количества катализатора
8 раз больше при идентичных условиях процесса.
и удельном расходе водорода 300-1700 л/(кгкат∙ч)
Наночастицы никеля размерами около 4 нм, нане-
(схема 1). Выходы продуктов составляли 91-100%,
сенные на силикагель катализируют восстанов-
основными примесями являлись исходные нитро-
ление нитробензола при 90°С и 10 атм водорода
арены.
с конверсией 100% и селективностью по анилину
99% [22].
На примере 2-нитротолуола 1б было рассмотре-
но влияние температуры на конверсию исходного
Широкие исследования проведены в области
нитроарена и выход 2-метиланилина 2б. В интер-
катализа восстановления нитроаренов ферромаг-
вале 160-240°С выход соединения 2б уменьшается
нитными нанокатализаторами [23]. В частности,
с 99.9 до 97.2% вследствие появления продуктов
приводятся сведения об использовании наноча-
побочной реакции при повышенных температу-
стиц палладия (3 нм), нанесенных на Fe3O4 (11 нм)
рах выше 180°С. При понижении температуры от
для гидрирования нитробензола водородом при 1
140 до 100°С конверсия исходного нитроарена 1б
атм и комнатной температуре [24]. Катализатор ис-
и выход 2-метиланилина 2б снижаются с 82.2 до
пользовался многократно без потери активности.
29.5% при селективности синтеза 100%. Для 3-ни-
Предыдущими исследованиями показано, что
тротолуола 1в выход соединения 2в снижается с
нанесенные на подложку наночастицы никеля
99.3 до 98.4% при понижении температуры от 240
показали высокую каталитическую активность
до 200°С.
в ряде реакций гидрирования при атмосферном
Влияние носителя на выход продукта было
давлении водорода [25, 26]. Целью настоящей ра-
рассмотрено на примере восстановления нитро-
боты являлось изучение процесса восстановления
бензола. Установлено, что все катализаторы про-
нитроаренов при атмосферном давлении водорода
являют высокую каталитическую активность при
в реакторе проточного типа на субмикро- и нано-
удельном расходе нитробензола 0.6 л/(кгкат∙ч) и
частицах никеля, иммобилизованных на разных
удельном расходе водорода 1330 л/(кгкат∙ч) при
носителях: цеолите NaХ, γ-оксиде алюминия, ак-
мольном соотношении водород:нитробензол
=
тивированном угле, оксиде магния.
(10-15):1 в температурном интервале 140-200°С,
Катализаторы получали пропиткой носителей
при этом конверсия нитробензола 1а составляет
(фракция 1-1.5 мм) водным раствором гексаги-
100%. Однако при использовании в качестве но-
драта хлорида никеля(II) в течение суток, филь-
сителя цеолита NaX при температурах ниже 180°С
тровании и последующей обработкой раствором
активность частиц никеля сильно снижается, при
тетрагидробората натрия в воде при комнатной
этом наблюдается быстрая дезактивация катализа-
температуре. Катализатор загружали во влажном
тора. При прекращении подачи сырья и продувке
виде в реактор и сушили от воды в токе водорода
реактора водородом при 240°С в течение 30 мин
непосредственно перед реакцией. Размеры частиц
катализатор полностью восстанавливает свои
никеля на поверхности составляли 40-120 нм [27].
свойства.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
КОЛЛОИДНЫЕ И НАНОР
АЗМЕРНЫЕ КАТАЛИЗАТОРЫ В ОРГАНИЧЕСКОМ СИНТЕЗЕ: XXI.
1153
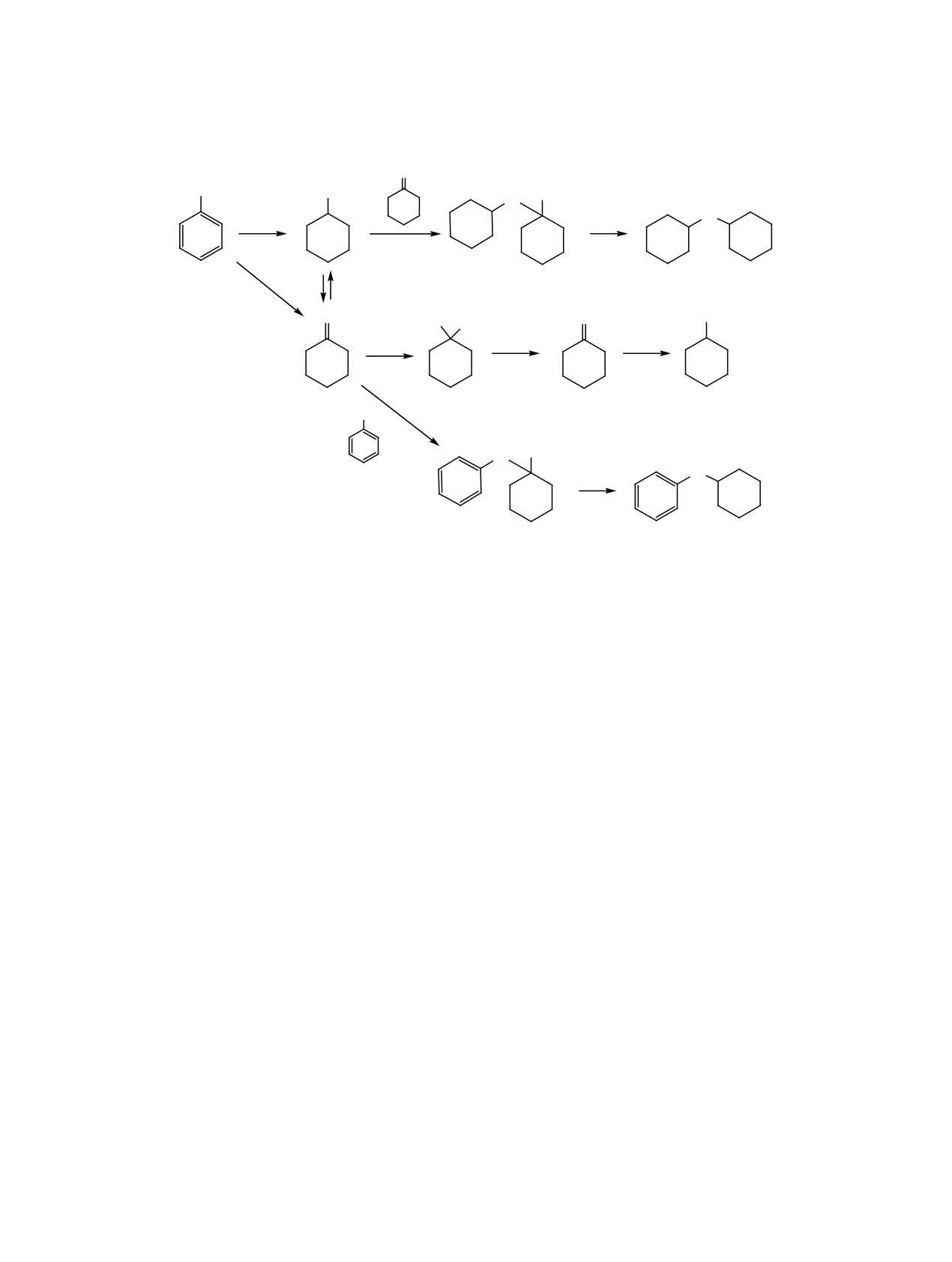
Схема 2.
NH
NH2
NH2
H
NH2
N
H
+
N
+3H2
+H2
-NH3
-H2
+H2
+2H2
NH
O
OH
HO
NH2
+H2
H2O
-NH3
NH2
+
H
NH2
N
H
N
+H2
-NH3
При использовании слабокислых или основных
ственным выходом при 120-180°С, при этом ак-
носителей активность катализатора при пониже-
тивность катализатора не снижается в течение 10 ч
нии температуры сохранялась. Так, наночастицы
непрерывной работы. В интервале 80-100°С дан-
никеля, нанесенные на прессованный порошок
ный катализатор также активен и позволяет вос-
оксида магния восстанавливают нитроарен 1a при
станавливать нитробензол с конверсией 94-96%.
температурах 100-120°С. Однако их активность
Частицы никеля, нанесенные на активирован-
в данном температурном интервале в течение 1 ч
ный уголь Norit RX 3 EXTRA, также как при нане-
непрерывной работы также снижается, что, по-ви-
сении на оксид магния, проявляют высокую актив-
димому, связано с сильными адсорбционными
ность в широком интервале температур (80-240°С),
свойствами нитробензола, тормозящими процесс
при этом наблюдается полная конверсия нитробен-
его восстановления водородом при данных темпе-
зола. В отличие от оксида магния в интервале 80-
ратурах. Активность катализатора восстанавлива-
140°С не наблюдается диффузионных или адсорб-
ется при повышении температуры до 180-200°С
ционных затруднений работы катализатора, и раз-
и продувке водородом (деблокируются активные
бавления нитробензола не требуется. Однако дан-
центры катализатора), при этом десорбируется до
ный катализатор проявляет невысокую селектив-
2.5 г смеси соединений 1а и 2а с 3 г катализатора.
ность по целевому анилину. Так, при 200°С в реак-
С целью увеличения срока активности катали-
ционной смеси, согласно данным газожидкостной
затора при 100-120°С нитроарен 1а был разбавлен
хроматографии (ГЖХ) и хромато-масс спектро-
инертным разбавителем (толуолом), что позволи-
метрии, присутствует анилин (91.3 мас%), цикло-
ло равномерно распределить молекулы нитроаре-
гексиламин (1 мас%), циклогексанон (1.6 мас%),
на и толуола по поверхности катализатора. При
циклогексанол (0.4 мас%), фенилциклогексила-
этом толуол, как более летучий компонент, легче
мин (2 мас%) и дициклогексиламин (3.7 мас%).
десорбируется с поверхности катализатора, осво-
При повышении температуры до 300°С доля вы-
бождая активные центры для адсорбции молекул
сококипящих побочных продуктов увеличивается
водорода, что способствует протеканию процесса
до 20 мас%. Установлено, что неполной селек-
восстановления нитроарена 1а. Установлено, что
тивности не удается избежать и при 80-100°С,
разбавление в соотношении нитробензол-толуол,
когда содержание анилина достигает 93 мас%,
равном 1:5, позволяет получать анилин с количе-
но присутствуют и производные циклогексана.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
1154
МОХОВ и др.
Образование побочных продуктов (суммар-
вторичных электронов - ETD, детектор обратно
но 1-9 мас%) обнаружено и при использовании
рассеянных электронов - CBS, метод элементного
в качестве носителей цеолита NaX, и γ-Al2O3. С
анализа - EDS.
другой стороны, применение в качестве носителя
Приготовление катализатора. Катализатор по-
оксида магния позволяет получать анилин с селек-
лучалипутемпропиткиносителя(фракция1-1.5мм)
тивностью до 100%.
водным раствором гексагидрата хлорида никеля(II)
Таким образом, в указанных условиях проходит
в течение суток в соотношении 0.7 г хлорида ни-
частичное гидрирование ароматического кольца.
келя на 2 г цеолита NaХ, 1 г хлорида никеля на 3 г
Образование циклогексанона можно объяснить
γ-Al2O3 цеолита NaX или Сакт, 3 г хлорида никеля
гидролизом промежуточного имина (схема 2), а
на 3 г MgO. Пропитанный носитель фильтровали
наличие дициклогексиламина - реакцией диспро-
и промывали дистиллированной водой с последу-
порционирования циклогексиламина и кросс-со-
ющей обработкой раствором тетрагидробората на-
четания с анилином, что на нанесенных наноча-
трия в воде (3×0.1 г) при комнатной температуре.
стицах никеля было изучено ранее [28].
Восстановление каждой порцией проводили в те-
Следует отметить, что промышленные катали-
чение 2 мин. Восстановленный катализатор загру-
заторы, такие как НТК-4 и ЛОК, обладают удель-
жали в реактор во влажном виде, осушали от воды
ной производительностью 0.24 кгнб/(кгкат·ч) (нб -
в токе водорода при 300°С непосредственно перед
нитробензол), что ниже, чем использованные в
реакцией.
настоящей работе [1.08 кгнб/(кгкат·ч) при исполь-
Общая методика проведения реакции. Реак-
зовании неразбавленного нитробензола], что сви-
цию проводили в реакторе вытеснения при атмос-
детельствует о перспективности исследований по
ферном давлении и температуре 80-240°С. В этом
улучшению характеристик исследуемого типа ка-
температурном интервале реакция может осу-
тализаторов.
ществляться как в газовой фазе, так и в системе
Таким образом, установлено, что иммобилизо-
газ-жидкость-твердый катализатор в зависимости
ванные на оксиде магния, активированном угле,
от температуры кипения исходных нитроаренов.
γ-оксиде алюминия или цеолите NaX наночасти-
Лабораторный реактор представлял собой трубку
цы никеля проявляют высокую каталитическую
из стали 12Х18Н10Т с внутренним диаметром 9 мм
активность в процессах восстановления нитроаре-
и высотой зоны нагрева 50 мм, помещенный в
нов. На основании полученных эксперименталь-
электрическую печь. Удельная скорость подачи
ных данных установлено, что применение в каче-
жидкой смеси - 0.6 или 0.9 л/(кгкат·ч) в зависимо-
стве носителя оксида магния позволяет получать
сти от количества катализатора. Расход водорода -
анилин с селективностью до 100%, в то время как
300-1700 л/(кгкат·ч)
(10-15-кратный мольный
на носителях цеолит NaX, γ-Al2O3, активирован-
избыток).
ный уголь образуется до 20 мас% побочных про-
Анилин (2а). а. На катализатор Ni/NaX (3 г)
дуктов гидрирования ароматического кольца.
подавали водород с расходом 1330 л/(кгкат·ч).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Одновременно с водородом прямоточно с ним с
·ч) при 200°С подавали ни-
расходом 0.6 л/(кгкат
Хромато-масс-спектральный анализ выпол-
тробензол 1а. Конверсия 100%, селективность и
нен на приборе Saturn 2100 T/GC3900 (ЭУ, 70 эВ).
выход 90.7%. Масс-спектр, m/e (Iотн, %): 93.9 (13)
Количественный ГЖХ-анализ реакционной массы
[M + 1]+, 93.0 (100) [M]+, 92.0 (9), 66.0 (35), 65.0
проводили на хроматографе Кристаллюкс-4000М
(20), 63.0 (5).
(tн = 100-210°С, tисп = 250°С, полярная колонка
HP-5, l = 50 м, d = 0.32 мм, газ-носитель - азот,
б. На катализатор Ni/Сакт (3 г) подавали водо-
детектор - ПИД, tПИД = 250°C, растворитель - аце-
род с расходом 1330 л/(кгкат·ч). Одновременно по-
тонитрил). Сканирующая электронная микроско-
давали нитробензол 1а с расходом 0.6 л/(кгкат·ч)
пия выполнена при помощи прибора FEI Versa 3D
при 200°С. Конверсия 100%, селективность и вы-
DualBeam. Рабочее расстояние - 10 мм, детектор
ход 91.3%.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
КОЛЛОИДНЫЕ И НАНОР
АЗМЕРНЫЕ КАТАЛИЗАТОРЫ В ОРГАНИЧЕСКОМ СИНТЕЗЕ: XXI.
1155
в. Проводили аналогично на катализаторе
селективность 97.4%, выход 97.2%. Масс-спектр,
Ni/γ-Al2O3 (3 г). Конверсия 100%, селективность и
m/e (Iотн, %): 123.9 (51) [M + 1]+, 123.0 (100) [M]+,
выход 80.0%.
108.0 (63), 80.1 (66), 53.0 (14).
г. Проводили аналогично на катализаторе
КОНФЛИКТ ИНТЕРЕСОВ
Ni/MgO (3 г) при 140°С. Конверсия 100%, селек-
тивность и выход 99.4%.
Авторы заявляют об отсутствии конфликта
2-Метиланилин (2б). На катализатор Ni/NaX
интересов.
(2 г) подавали водород с расходом 1700 л/(кгкат·ч).
Одновременно с водородом прямоточно с ним с
СПИСОК ЛИТЕРАТУРЫ
расходом 0.9 л/(кгкат·ч) подавали 2-нитротолуол
1б при 200°С. Конверсия 99.9%, селективность
1.
Попов Ю.В., Мохов В.М., Латышова С.Е., Небы-
99.5%, выход 99.4%. Масс-спектр, m/e (Iотн, %):
ков Д.Н., Панов А.О., Давыдова Т.М. // ЖОХ. 2018.
108.0 (6) [M + 2]+, 107.0 (78) [M + 1]+, 106.0 (100)
Т. 88. Вып. 10. С. 1585; Popov Y.V., Mokhov V.M.,
[M]+, 89.0 (7), 79.0 (12), 78.0 (6), 77.1 (16), 52.0 (7),
Latysho-va S.E., Nebykov D.N., Panov A.O., Davydo-
51.0
(7).
va T.M. // Russ. J. Gen. Chem. 2018. Vol. 88. N 10. P.
3-Метиланилин (2в). На катализатор Ni/NaX
2035. doi 10.1134/S1070363218100018
(3 г) подавали водород с расходом 1130 л/(кгкат·ч).
2.
Dao S., Qian W., Luo G., Wei F., Wang Y. // Appl. Catal.
Одновременно с водородом прямоточно с ним с
(A). 2005. Vol. 286. N 1. Р. 30. doi 10.1016/j.apca-
расходом 0.6 л/(кгкат·ч) подавали 3-нитротолуол
ta.2005.02.026
1в при 240°С. Конверсия 100%, селективность и
3.
Chary K.V.R., Srikanth C.S. // Catal. Lett. 2009. Vol. 128.
выход 99.3%. Масс-спектр, m/e (Iотн, %): 107.9 (7)
N 1-2. Р. 164. doi 10.1007/s10562-008-9720-1
[M + 2]+, 107.0 (69) [M + 1]+, 106.0 (100) [M]+, 79.0
4.
Nieto-Márquez A., Gil S., Romero A., Valverde J.L.,
(17), 77.0 (17), 51.0 (8).
Gómez-Quero S., Keane M.A. // Appl. Catal. (A).
4-Метиланилин (2г). На катализатор Ni/NaX
2009. Vol. 363. N 1-2. Р. 188. doi 10.1016/j.apca-
(3 г) подавали водород с расходом 300 л/(кгкат·ч).
ta.2009.05.016
Одновременно с водородом прямоточно с ним
5.
Wang J., Yuan Z., Nie R., Hou Z., Zheng X. // Ind. Eng.
с расходом 0.6 л/(кгкат·ч) подавали смесь 4-ни-
Chem. Res. 2010. Vol. 49. N 10. Р. 4664. doi 10.1021/
тротолуола
1г
[0.15 моль/(кгкат·ч)] и толуола
ie1002069
[0.45 моль/(кгкат·ч)] при 200°С. Конверсия 96.9%,
селективность 97.5%, выход 94.5%. Масс-спектр,
6.
SangeethaP., ShanthiK.,RamaRaoK.S.,ViswanathanB.,
Selvam P. // Appl. Catal. (A). 2009. Vol. 353. N 2.
m/e (Iотн, %): 108.0 (6) [M + 2]+, 107.0 (83) [M + 1]+,
Р. 160. doi 10.1016/j.apcata.2008.10.044
106.0 (100) [M]+, 79.0 (11), 78.1 (7), 77.0 (13).
7.
Torres C., Campos C., Fierro J.G., Oportus M., Reyes P. //
2-Метоксианилин (2д). На катализатор Ni/NaX
Catal. Lett. 2013. Vol. 143. N 8. Р. 763. doi 10.1007/
(3 г) подавали водород с расходом 1100 л/(кгкат·ч).
s10562-013-1034-2
Одновременно с водородом прямоточно с ним с
расходом 0.6 л/(кгкат·ч) подавали 2-нитроанизол
8.
Takasaki M., Motoyama Y., Higashi K., Yoon S.-H., Mo-
2д при 200°С. Конверсия 100%, селективность и
chida I., Nagashima H. // Org. Lett. 2008. Vol. 10. N 8.
выход 99.3%. Масс-спектр, m/e (Iотн, %): 123.9 (15)
Р. 1601. doi 10.1021/ol800277a
[M + 1]+, 123.0 (76) [M]+, 108.0 (88), 80.1 (100), 53.0
9.
Fine Chemicals through Heterogeneous Catalysis /
(26), 52.1 (13), 51.1 (8).
Eds R.A. Sheldon, H. van Bekkum, Weinheim: Wi-
ley-VCH, 2001. P. 389.
4-Метоксианилин (2е). На катализатор Ni/NaX
(3 г) подавали водород с расходом 1100 л/(кгкат·ч).
10.
Cаrdenas-Lizana F., Gomez-Quero S., Keane M.A. //
Одновременно с водородом прямоточно с ним
ChemSusChem. 2008. Vol. 1. Р. 215. doi 10.1002/
с расходом 0.6 л/(кгкат·ч) подавали смесь 4-ни-
cssc.200700105
тротолуола
1е
[0.15 моль/(кгкат·ч)] и толуола
11.
Kuhn L.P. // J. Am. Chem. Soc. 1951. Vol. 73. N 4.
[0.45 моль/(кгкат·ч)] при 200°С. Конверсия 99.8%,
Р. 1510. doi 10.1021/ja01148a029
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
1156
МОХОВ и др.
12.
Allen C.F.H., Van Allan J. // Org. Synth. Coll. 1955.
23. Shokouhimehr M. // Catalysts. 2015. Vol. 5. N 2. P. 534.
Vol. 3. Р. 63.
doi 10.3390/catal5020534
13.
Xiong J., Chen J., Zhang J. // Catal. Commun. 2007.
24. Pelisson C.-H., Denicourt-Nowicki A., Meriadec C.,
Vol. 8. N 3. Р. 345. doi 10.1016/j.catcom.2006.06.028
Greneche J.-M., Roucoux A. // ChemCatChem. 2015.
14.
Winstrom L.O. Pat. US 2822397A (1955).
Vol. 7. N 2. P. 309. doi 10.1002/cctc.201402761
15.
Varkolu M., Velpula V., Pochamoni R., Muppala A.R.,
25. Попов Ю.В., Мохов В.М., Латышова С.Е., Небы-
Burri D.R., Kamaraju S.R.R. // Appl. Petrochem. Res.
ков Д.Н., Панов А.О., Плетнева М.Ю. // ЖОХ. 2017.
2016. Vol. 6. N 1. Р. 15. doi 10.1007/s13203-015-0115-0
Т. 87. Вып. 10. C. 1616; Popov Y.V., Mokhov V.M.,
16.
Chary K.V.R., Srikanth C.S. // Catal. Lett. 2009. Vol. 128
Latyshova S.E., Nebykov D.N., Panov A.O., Pletne-
N 1-2. Р. 164. doi 10.1007/s10562-008-9720-1
va M.Y. // Russ. J. Gen. Chem. 2017. Vol. 87. N. 10.
17.
Sangeetha P., Seetharamulu P., Shanthi K., Narayanan S.,
P. 2276. doi 10.1134/S107036321710005X
Rama Rao K.S. // J. Mol. Catal. (A). 2007. Vol. 273.
26. Мохов В.М., Попов Ю.В., Небыков Д.Н. // ЖОХ.
N 1-2. Р. 244. doi 10.1016/j.molcata.2007.03.020
2016. Т. 52. Вып. 3. C. 339; Mokhov V.M., Popov Yu.V.,
18.
Mohan V., Pramod C.V., Suresh M., Reddy K.H.P.,
Nebykov D.N. // Russ. J. Gen. Chem. 2016. Vol. 53. N 3.
Raju B.D., Rao K.S.R. // Catal. Commun. 2012. Vol. 18.
P. 319. doi 10.1134/S1070428016030040
Р. 89. doi 10.1016/j.catcom.2011.11.030
27. Попов Ю.В., Мохов В.М., Небыков Д.Н., Латышо-
19.
Hari Prasad Reddy K., Rahul R., Sree Vardhan Reddy S.,
ва С.Е., Панов А.О., Донцова А.А., Ширханян П.М.,
David Raju B., Rama Rao K.S. // Catal. Commun. 2009.
Щербакова К.В. // ЖОХ. 2016. Т. 86. Вып. 12. С. 1951;
Vol. 10. N 6. Р. 879. doi 10.1016/j.catcom.2008.12.014
Popov Yu.V., Mokhov V.M., Nebykov D.N., Latysho-
20.
Мохов В.М., Попов Ю.В., Небыков Д.Н. // ЖОХ. 2014.
va S.E., Panov A.O., Dontsova A.A., Shirkhanyan P.M.,
Т. 84. Вып. 8. С. 1289; Mokhov V.M., Popov Yu.V.,
Shcherbakova K.V. // Russ. J. Gen. Chem. 2016. Vol. 86.
Nebykov D.N. // Russ. J. Gen. Chem. 2014. Vol. 84. N 8.
N 12. P. 2589. doi 10.1134/S1070363216120033
Р. 1515. doi 10.1134/S107036321408012X
21.
Wang A., Yin H., Ren M., Lu H., Xue J., Jiang T. // New
28. Попов Ю.В., Мохов В.М., Латышова С.Е., Небы-
J. Chem. 2010. Vol. 34. N 4. Р. 708. doi 10.1039/b9n-
ков Д.Н., Панов А.О., Давыдова Т.М. // ЖОХ. 2017.
j00657e
Т. 87. Вып. 12. С. 1937; Popov Yu.V., Mokhov V.M.,
22.
Wang J., Yuan Z., Nie R., Hou Z., Zheng X. // Ind. Eng.
Latyshova S.E., Nebykov D.N., Panov A.O., Davydo-
Chem. Res. 2010. Vol. 49. N 10. Р. 4664. doi 10.1021/
va T.M. // Russ. J. Gen. Chem. 2017. Vol. 87. N 12.
ie1002069
P. 2757. doi 10.1134/S1070363217120015
Colloid and Nanosized Catalysts in Organic Synthesis:
XXI. Reduction of Nitroarenes Catalyzed
by Immobilized Nickel Nanoparticles
V. M. Mokhov, Yu. V. Popov*, D. N. Nebykov, E. V. Nishchik,
K. V. Shcherbakova, and Yu. L. Zotov
Volgograd State Technical University, pr. Lenina 28, Volgograd, 400131 Russia
*e-mail: tons@vstu.ru
Received March 12, 2019; revised March 12, 2019; accepted March 14, 2019
It was found that nickel nanoparticles supported on NaX zeolite, γ-alumina, activated carbon or magnesium
oxide catalyze the reduction process of nitrobenzene and its homologs with high yields of aniline and its deriv-
atives. The effect of the substrate on carrying out these processes in a continuous reactor at atmospheric hydro-
gen pressure was investigated. The use of activated carbon or magnesium oxide as a carrier makes it possible
to conduct the reaction at 80-100°С.
Keywords: catalysis, nanoparticles, nickel, reduction, nitroarenes, aniline
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019