ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2019, том 89, № 8, с. 1269-1273
УДК 541.49;546.562
КОМПЛЕКСЫ МАРГАНЦА И ЖЕЛЕЗА
С БИС[2-(2-ГИДРОКСИ-3,5-ДИ-трет-БУТИЛБЕНЗИЛ)-
ГИДРАЗИДОМ] МАЛОНОВОЙ КИСЛОТЫ
© 2019 г. П. А. Фатуллаева*
Институт катализа и неорганической химии имени академика M. Нагиева
Национальной академии наук Азербайджана, пр. Г. Джавида 113, Баку, AZ1143 Азербайджан
*e-mail: iradam@rambler.ru
Поступило в Редакцию 21 января 2019 г.
После доработки 3 апреля 2019 г.
Принято к печати 4 апреля 2019 г.
Синтезированы новые комплексы Mn(II) и Fe(III) с гидразоном на основе дигидразида малоновой кис-
лоты и 3,5-ди-трет-бутилсалицилового альдегида. Методами ИК, электронной спектроскопии и рент-
геноструктурного анализа изучено строение полученных комплексов. Бис[(2-гидрокси-3,5-ди-трет-
бутилбензилиден)гидразид] малоновой кислоты образует биядерные комплексы с ионами марганца и
железа, в которых наблюдается ферромагнитное взаимодействие между ионами металлов.
Ключевые слова: основания Шиффа, гидразид малоновой кислоты, комплексы Mn(II), комплексы Fe(III)
DOI: 10.1134/S0044460X1908016X
Aцилгидразоны и их комплексы с ионами пере-
ми кислорода и азота, и образуют комплексы раз-
ходных металлов находят применение как лекар-
личного типа [6-16].
ственные препараты против туберкулеза [1]. Они
Дигидразоны на основе дигидразида малоно-
обладают противоопухолевой [2, 3] и антимикроб-
вой кислоты обладают более высокой гибкостью
ной активностью [4].
по сравнению с дигидразонами других двухоснов-
Дигидразоны на основе гидразидов двухос-
ных кислот (например, щавелевой, фталевой и др.)
из-за возможности вращения вокруг метиленовой
новных кислот являются полидентатными лиган-
группы [15]. Еще большая гибкость может быть
дами и образуют с ионами переходных металлов
достигнута за счет восстановления азометиновых
комплексы различного типа [5]. Дигидразоны на
основе гидразида малоновой кислоты являются
связей в таких лигандах.
полидентатными лигандами, обладающими по
В данной работе нами проведен синтез комплексов
меньшей мере шестью координирующими атома-
Mn(II) и Fe(II) с бис[(2-гидрокси-3,5-ди-трет-бу-
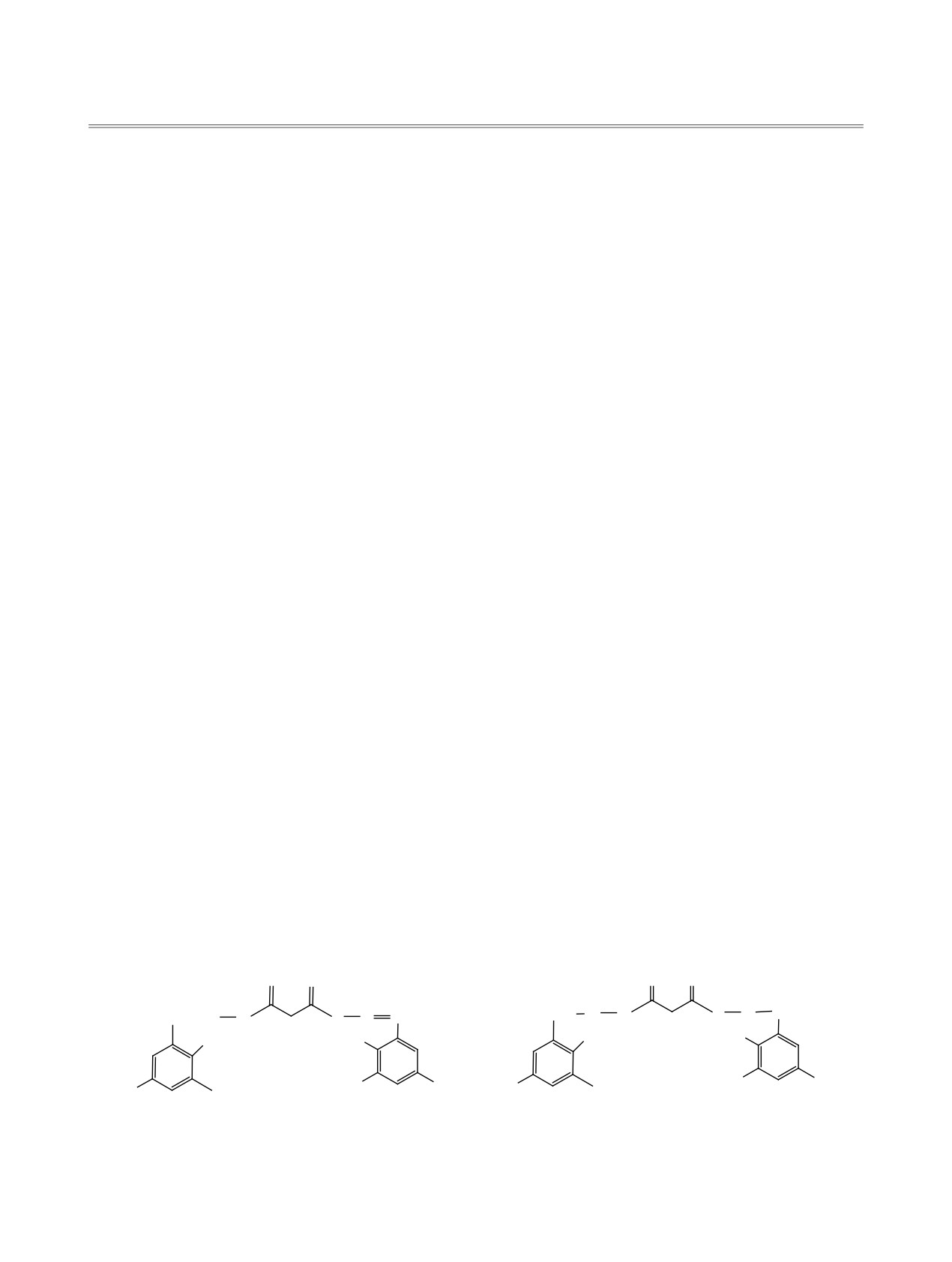
Схема 1.
O O
O O
H
H
H
H
H
H
CH2
N
N
N
CH2
CH N
N
N
N
CH
N
OH
HO
OH
HO
t-Bu
t-Bu
t-Bu
t-Bu
t-Bu
t-Bu
t-Bu
t-Bu
L1H4
L2H4
1269
1270
ФАТУЛЛАЕВА
тилбензил)гидразидом} малоновой кислоты L2H4, по-
щиеся к полосе переноса заряда лиганд-металл и
лучен-ным путем восстановления азометиновых
двум d-d-переходам соответственно. В комплексе
групп в бис[(2-гидрокси-3,5-ди-трет-бутилбензи-
марганца с лигандом L2H4 синглетная полоса при
лиден)гидразиде} малоновой кислоты L1H4 (схема 1).
285 нм, наблюдаемая в спектре свободного гидра-
В лигандах L1H4 и L2H4 карбонильная группа,
зида, заметно уширяется и сдвигается в длинно-
связанная с гидразиновым фрагментом, способна
волновую область (λmax = 305 нм). В видимой обла-
переходить из кето-формы в енольную, атом водо-
сти спектра наблюдается поглощение при ~400 нм
рода которой может депротонироваться при коор-
(перегиб) и слабая широкая полоса с λmax= 550 нм.
динировании, поэтому эти соединения потенци-
В спектре комплекса железа с малоноилдиги-
ально способны выступать как моно-, би-, три- и
дразоном
2-гидрокси-3,5-ди-трет-бутилбензаль-
тетраанионные лиганды.
дегида L1H4 присутствуют практически те же по-
Ионы переходных металлов, как правило, об-
лосы поглощения, что и в спектре комплекс мар-
разуют с бис[(2-гидроксибензилиден)гидразидом]
ганца. Такое же подобие в электронных спектрах
малоновой кислоты комплексы, нерастворимые в
поглощения проявляют между собой комплексы
воде и органических растворителях, что ограничи-
Mn(II) и Fe(III) с лигандом L2H4.
вает возможность изучения их строения и свойств.
В ИК спектре основания Шиффа L1H4 наблю-
Нами были получены малоноилдигидразоны 2-ги-
даются полосы поглощения, относящиеся к азо-
дрокси-3,5-ди-трет-бутилбензальдегида. Комп-
метиновой группе CH=N при 1630 см-1 и полоса
лексы на его основе с ионами Mn(II) и Fe(II) хо-
амидной группы при 1694 см-1, которую можно
рошо растворимы в полярных (метанол, этанол) и
отнести к колебаниям карбонильной группы С=О.
малополярных (бензол, хлороформ) растворителях.
Две интенсивные полосы при 3200 и 3080 см-1 мо-
Малоноилдигидразон
2-гидрокси-3,5-ди-трет-
гут быть отнесены к валентным колебаниям вза-
бутилбензальдегида был восстановлен боргидри-
имодействующих групп NH и OH [15]. В восста-
дом натрия по азометиновой группе с образованием
новленном по азометиновой группе лиганде L2H4
бис[(2-гидрокси-3,5-ди-трет-бутилбензил)гидра-
полосы азометиновой и карбонильной групп при
зидом} малоновой кислоты L2H4. Комплексы на
1630 и 1695 см-1 исчезают, и появляется уширен-
его основе с ионами Mn(II) и Fe(III) также облада-
ная полоса с максимумом при 1620 см-1.
ли хорошей растворимостью в органических рас-
В ИК спектре комплекса марганца с шиффовым
творителях.
основанием L1H4 полоса при 1690 см-1, присут-
Строение полученных соединений было изуче-
ствующая в спектре свободного лиганда, исчезает,
но методами ИК и УФ спектроскопии. Так, в элек-
а полоса при 1630 см-1 несколько сдвигается в сто-
тронных спектрах раствора лиганда L1H4 в эта-
рону низких энергий (1609 см-1). Кроме того, по-
ноле наблюдаются полосы поглощения при 285 и
является новая полоса поглощения при 1654 см-1,
296 нм (дублет) и 340 нм. Эти полосы могут быть
которую можно отнести к координированной кар-
отнесены к π-π*- и n-π-переходам соответствен-
бонильной группе.
но [15]. Полосу при 340 нм обычно относят к по-
В ИК спектре комплекса марганца с восста-
глощению азометиновой группы, сопряженной с
нов-ленным лигандом L2H4 полосы в области
бензольным кольцом. В восстановленном лиганде
1600-1700 см-1 исчезают, а в области валентных
L2H4 полоса при 340 нм исчезает, что подтвержда-
колебаний наблюдаются слабое поглощение при
ет ее принадлежность к сопряженной азометино-
3200 см-1 и сильное поглощение при 3400 см-1, ко-
вой группе. Вместо дублетной полосы при 285 и
торые можно отнести к колебаниям связей N-H и
296 нм появляется синглетная полоса при 285 нм.
O-H в амино- и фенольной группах. Эти данные
При образовании комплекса марганца с лиган-
указывают на то, что карбонильная группа еноли-
дом L1H4 в ультрафиолетовой области появляются
зована и выступает как анион при координации.
пики при 267, 290 нм и перегибы при 320 и 340 нм.
Попытки получения монокристаллов для
В видимой области спектра наблюдаются три по-
рентгеноструктурных измерений не увенчались
лосы поглощения при 445, 610 и 720 нм, относя-
успехом. Получаемые монокристаллы имели де-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
КОМПЛЕКСЫ МАРГАНЦА И ЖЕЛЕЗА
1271
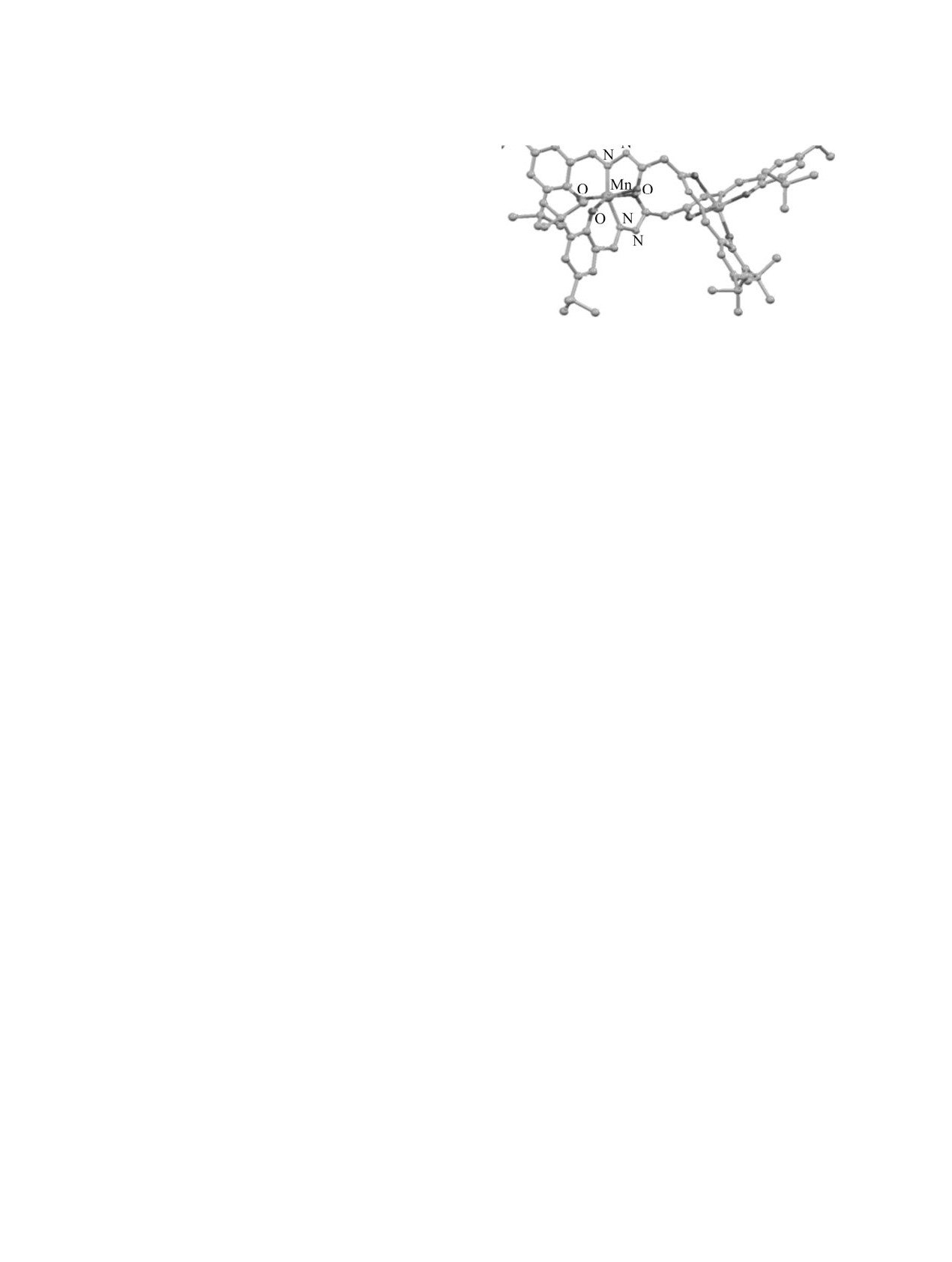
фектную структуру, однако с большой долей ве-
роятности была установлена молекулярная струк-
тура для комплекса марганца с бис[(2-гидрок-
си-3,5-ди-трет-бутилбензил)гидразидом} мало-
новой кислоты (см. рисунок). По данным РСА,
комплекс является биядерным с отношением ме-
талл:лиганд = 1:1. Координация каждого иона мар-
ганца осуществляется двумя фенольными атомами
кислорода, двумя атомами азота аминогруппы и
двумя атомами кислорода амидного фрагмента,
так что вокруг иона металла осуществляется ок-
Общий вид молекулы комплекса Mn2(L2H2)2 в кристалле.
таэдрическое окружение. Аналогичное строение,
по-видимому, имеет комплекс железа, у которого
лучали на спектрофотометре UV-VIS Evolution
наблюдаются подобные комплексу марганца спек-
60S. Элементный анализ проводили в аналити-
тральные и магнитные свойства.
ческой лаборатории Тубитак (Анкара) на анали-
заторе LECOCHNS 932. Магнитные измерения
Величины магнитных моментов, измерен-
проводили на собранной нами установке типа
ные при комнатной температуре, указывают на
Фарадея с использованием в качестве эталона
высокоспиновое состояние ионов железа и мар-
[HgCo(SCN)4]. В качестве баланса использовали
ганца в полученных комплексах: μэфф= 7.2 М. Б.
аналитические весы с точностью измерений 10-5 г.
[Mn2(L2H2)2] и μэфф = 6.8 М. Б. [Fe2(L2H)2]. В со-
Рентгеноструктурный анализ выполнен на диф-
ответствии с данными магнитных измерений ион
рактометре D8-QUEST с графитовым монохрома-
марганца имеет степень окисления +2 (электрон-
тором с использованием MoKα-излучения.
ная конфигурация d5), поэтому лиганд в этом слу-
чае ведет себя как дианионный, и общую форму-
Дигидразид малоновой кислоты получали по
лу этого соединения можно представить в виде
известной методике [17], т. пл. 153°С (т. пл. 152-
[Mn2(L2H2)2].
154°С [17]).
Комплекс железа с лигандом L2H4 обладает
Получение основания Шиффа из дигидра-
также высоким магнитным моментом, соответ-
зида малоновой кислоты и 3,5-ди-(трет-бу-
ствующим трехвалентному иону с электронной
тил)салицилового альдегида (L1H4). Смесь 1.32 г
конфигурацией d5. В этом случае состав комплекс
(10-2 моль) дигидразида малоновоой кислоты в
должен иметь состав [Fe2(L2H)2].
20 мл метанола и 4.68 г (2×10-2 моль) 2-гидрок-
си-3,5-ди-трет-бутилбензальдегида в 30 мл ме-
Зависимость магнитной восприимчивости обо-
танола перемешивали при температуре 30-40°С
их комплексов от напряженности магнитного поля
в течение 20 мин. Выпавшие светло-желтые кри-
отклоняется от линейности, что может свидетель-
сталлы отделяли и сушили на воздухе. Выход 70%,
ствовать о ферромагнитном внутримолекулярном
т. пл. 238°С. Найдено,%: С 70.11; Н 8.40; N 9.72; O
взаимодействии между ионами Mn(II).
11.25. С33H48N4O4. Вычислено, %: C 70.21; H 8.51;
Таким образом, азометиновая группа в дигидра-
N 9.93; O 11.35.
зоне
3,5-ди-трет-бутилсалицилового альдегида
и дигидразида малоновой кислоты может быть
Восстановление бис[(2-гидрокси-3,5-ди-трет-бу-
тилбензилиден)гидразида] малоновой кислоты.
восстановлена до аминной с образованием гидри-
рованного аналога исходного гидразона. Получен-
К суспензии 5.64 г (10-2 моль) основания Шиффа
L1H4 в 40 мл метанола при интенсивном переме-
ный восстановленный лиганд образует биядерные
комплексы с ионами марганца(II) и железа(III).
шивании прибавляли малыми порциями 1 г NaBH4.
После прибавления всего количества боргидрида
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
и обесцвечивания реакционной массы перемеши-
ИК спектры снимали на спектрометре Nicolet
вание продолжали еще 0.5 ч. На следующий день
IS10. Электронные абсорбционные спектры по-
бесцветный раствор разбавляли
3-кратным ко-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
1272
ФАТУЛЛАЕВА
личеством воды и подкисляли 10%-ным водным
3. Easmon J., Puerstinger G., Roth T., Fiebig H.-H.,
раствором HCl до pH~7. Осадок отфильтровыва-
Jenny M., Jaeger W., Heinisch G., Hofmann J. // Int.
ли, промывали водой, сушили и перекристаллизо-
Cancer. 2001. Vol. 94. P. 89. doi 10.1002/ijc.1427
вывали из смеси этанол-вода (1:1). Выход 68%, т.
4. Vicini P., Zani F., Cozzini P., Doytchinova I. // Eur.
пл. 210°С. Найдено, %: С 69.59; Н 9.05; N 9.60; O
Med. Chem. 2002. Vol. 37. P. 553. doi 10.1016/S0223-
11.17. С33H52N4O4. Вычислено, %: C 69.72; H 9.15;
5234(02)01378-8
N 9.86; O11.27.
5. Gatto C.C., Schulz Lang E., Kupfer A., Hagenbach A.,
Abram U. // Z. anorg. allg. Chem. 2004. Vol. 630.
Получение комплекса Mn(II) с лигандом
P. 1286. doi 10.1002/zaac.200400103
L2Н4. Смешивали растворы лиганда (0.57 г,
0.01 моль) в этаноле и ацетата марганца (0.24 г,
6. Saini R.P., Kumar V., Gupta A.K., Gupta G.K. // Med.
Chem. Res. 2014. Vol. 23. P. 690. doi 10.1007/s00044-
0.01 моль) в метаноле. Цвет раствора изменялся на
014-09494-0
коричневый. Через 10-15 мин наблюдалось обра-
7. Halli M.B., Vijayalaxmi B., Patil Sumathi R.B.,
зование мелкокристаллического темно-коричнево-
Mallikarjun Kinni // Pharma Chem. 2012. Vol. 4. N 6.
го осадка, который отфильтровывали, промывали
P. 2360.
водой и сушили на воздухе. Выход 75%, т. пл.
8. Amin R.R., Yamany Y.B., Abo-Aly M., Hassan A.M. //
205°C. Найдено, %: С 63.59; Н 8.08; Mn 8.56; N
Nat. Sci. 2011. Vol. 3. N 9. P. 783. doi 10.4236/
9.22; O 10.20. С66H100N8O8Mn2. Вычислено, %: C
ns.2011.39103
63.77; H 8.05; Mn 8.85; N 9.02; O 10.31.
9. Boroujeni Kaveh P., Tamami B., Abdulmaleki A.,
Получение комплекса Fe(III) с лигандом
Osfouri S., Fadavi A. // Polymer Bull. 2012. Vol. 68.
L2Н4. К раствору 0.57 г (0.01 моль) лиганда
N 4. P. 909. doi 10.1007/s00289-011-0581-1
L2Н4 в 20 мл этанола прибавляли раствор 0.39 г
10. Shobha R.S., Agaiah B., Srinivas K., Sarangapani M. // Int.
(0.01 моль) соли Мора в 3 мл воды. Через 30 мин
J. Chem. Sci. 2010. Vol. 8. N 3. P. 1621.
раствор фильтровали. Из фильтрата при длитель-
11. Shobha R.S., Agaiah B., Sarangapani M. // Int. J. Pharm.
ном стоянии выпадали темные кристаллы, кото-
Technol. 2010. Vol. 2. P. 356.
рые отфильтровывали и сушили. Выход 65%, т. пл.
12. Lal R.A., Chakraborty J., Kumar A., Bhaumik S., Nath R.K.,
>250°C. С66H100N8O8Fe2. Вычислено, %: C 63.68;
Ghosh D. // Indian J. Chem. (A). 2004. Vol. 43. P. 516.
H 8.04; Fe 8.98; N 9.01; O 10.29. Найдено, %: С
doi 10.1007/s11243-007-0189-3
63.49; Н 8.00; Fe 8.81; N 9.15; O 10.12.
13. Backes G.L., Neumann D.M., Jursic B.S. // Bioorg.
Med. Chem. 2014. Vol. 22. P. 4629. doi 10.1016/j.
КОНФЛИКТ ИНТЕРЕСОВ
bmc.2014.07.022
14. Pal R., Kumar V., Beniwal V., Gupta G.K., Gupta A.K. //
Авторы заявляют об отсутствии конфликта
Pharma Chem. 2014. Vol. 6. P. 31.
интересов.
15. Kundan T., Amanpreet K., Sandesh T., Krisha-
na Ch.G., Kuwar S.N. // Analyt. Chim. Acta. 2014.
СПИСОК ЛИТЕРАТУРЫ
Vol. 852. P. 196. doi 10.1016/j.aca.2014.09.016
1. Patole J., Sandbhor U., Padhye S., Deobagkar D.N.,
16. Koch A., Kumar A., De A.K., Phukan A., Lal R.A. //
Anson C.E., Powell A. // Bioorg. Med. Chem. Lett. 2003.
Spectrochim. Acta (A). 2014. Vol. 129. P. 103. doi
Vol. 13. P. 51. doi 10.1016/S0960-894X(02)00855-7
10.1016/j.saa.2014.02.202
2. Terzioglu N., Gürsoy A. // Eur. J. Med. Chem. 2003.
17. Ali A.A., Allazov M.R., Ilyasli T.M. // Caspian J. Appl.
Vol. 38. P. 781. doi 10.1016/S0223-5234(03)00138-7
Sci. Res. 2013. Vol. 2. P. 85.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019
КОМПЛЕКСЫ МАРГАНЦА И ЖЕЛЕЗА
1273
Complexes of Manganese and Iron with Malonic Acid
Bis[2-(2-hydroxy-3,5-di-tert-butylbenzyl)hydrazide]
P. A. Fatullaeva*
Academician M. Nagiev Institute of Catalysis and Inorganic Chemistry of National Academy of Sciences of Azerbaijan,
pr. G. Dzhavida 113, Baku, AZ1143 Azerbaijan
*e-mail: iradam@rambler.ru
Received January 21, 2019; revised April 3, 2019; accepted April 4, 2019
New Mn(II) and Fe(III) complexes were synthesized with hydrazone based on malonic acid dihydrazide and
3,5-di-tert-butylsalicylic aldehyde. Structure of the obtained complexes was studied by IR, electron spectroscopy
and X-ray diffraction analysis methods. Malonic acid bis[(2-hydroxy-3,5-di-tert-butylbenzylidene)hydrazide]
forms binuclear complexes with manganese and iron ions, in which ferromagnetic interaction between metal
ions is observed.
Keywords: Schiff bases, malonic acid hydrazide, Mn(II) complexes, Fe(III) complexes
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 89 № 8 2019