ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 11, с. 1643-1646
УДК 661.8.244:544.42:544.4.032.7
ТЕРМИЧЕСКАЯ СТАБИЛЬНОСТЬ
ЦИКЛОДОДЕЦИЛИДЕН-1,1-БИСГИДРОПЕРОКСИДА
В ПРИСУТСТВИИ ФЕРРОЦЕНА
© 2020 г. Н. М. Андрияшина, С. А. Грабовский*, Н. Н. Кабальнова
Уфимский институт химии Российской академии наук, пр. Октября 71, Уфа, 450054 Россия
*e-mail: stas_g@anrb.ru
Поступило в Редакцию 26 июня 2020 г.
После доработки 26 июня 2020 г.
Принято к печати 9 июля 2020 г.
Изучена термическая стабильность циклододецилиден-1,1-бисгидропероксида в ксилоле и определены
активационные параметры реакции. Показано, что в присутствии ферроцена одновременно с термоли-
зом протекает реакция с ферроценом и индуцированный радикально-цепной распад циклододецили-
ден-1,1-бисгидропероксида.
Ключевые слова: циклододецилиден-1,1-бисгидропероксид, ферроцен, термическая стабильность
DOI: 10.31857/S0044460X20110013
Известно, что система ферроцен-пероксиды
дорода, органическими пероксидами и некото-
инициирует процессы полимеризации олефинов
рыми гидропероксидами в присутствии кислот.
[1-6]. Наиболее изучено взаимодействие перок-
Показано, что алканы легко окисляются H2O2 или
сида бензоила с ферроценом [7-10]. Недавно по-
t-BuOOH в мягких гомогенных условиях до со-
казано, что в присутствии ферроцена пероксид
ответствующих алкилгидропероксидов в присут-
бензоила одновременно расходуется в нескольких
ствии каталитических количеств ферроцена и пи-
реакциях - термический распад, распад, катализи-
разин-2-карбоновой кислоты [16].
руемый ионами железа(III), и реакция с ферроце-
О термической стабильности
1,1-бисгидро-
ном с образованием катион радикала ферроцения
пероксидов, которые являются эффективными
[11]. Данные о взаимодействии гидропероксидов с
инициаторами полимеризации олефинов [17-19]
ферроценом немногочисленны и противоречивы.
известно немного. Сообщается, что циклические
Так, гидропероксиды бутила, трет-бутила, куми-
1,1-бисгидропероксиды достаточно стабильны
ла неактивны в реакции с ферроценом [8]. Мето-
при комнатной температуре и их стабильность
дом ЭПР показано, что производные ферроцена
увеличивается с увеличением молекулярной мас-
после индукционного периода медленно разлага-
сы. Так, циклододецилиден-1,1-бисгидропероксид
ют t-BuOOH с образованием алкокси радикалов
и
2-н-нонилциклододецилиден-1,1-бисгидропе-
[12]. Реакции между FcBF4 и t-BuOOH протека-
роксид можно хранить без видимого разложения
ют быстро (1, 2). Характерный сине-зеленый цвет
при комнатной температуре 6 месяцев [20, 21].
раствора соли ферроцения мгновенно исчезает,
давая желтый цвет восстановленного ферроцена
В данной работе изучена термическая стабиль-
после добавления t-BuOOH.
ность циклододецилиден-1,1-бисгидропероксида
Fc + t-BuOOH → Fc+· + OH- + t-BuO· (медленно), (1)
1 в ксилоле в отсутствие и присутствии ферроцена.
FcBF4 + t-BuOOH
Кинетические кривые расходования соединения 1
→ Fc + HBF4 + t-BuOO• (очень быстро).
(2)
описываются уравнением первого порядка с вы-
Серия работ [13-15] посвящена взаимодей-
соким коэффициентом корреляции (r = 0.994 при
ствию производных ферроцена с пероксидом во-
120°С). Активационные параметры распада соеди-
1643
1644
АНДРИЯШИНА и др.
пероксида бензоила (k1/k0) увеличивается с повы-
шением температуры. В случае соединения 1 мы
наблюдаем обратный эффект - вклад термическо-
го распада уменьшается с повышением температу-
ры (см. таблицу). Отличие от распада пероксида
бензоила в присутствии ферроцена, по-видимому,
связано с образованием в системе более актив-
ного оксильного радикала. В случае пероксида
бензоила образуется малоактивный фенильный
радикал, в то время как при распаде циклододеци-
лиден-1,1-бисгидропероксида 1 образуется актив-
ный оксильный радикал, способный претерпевать
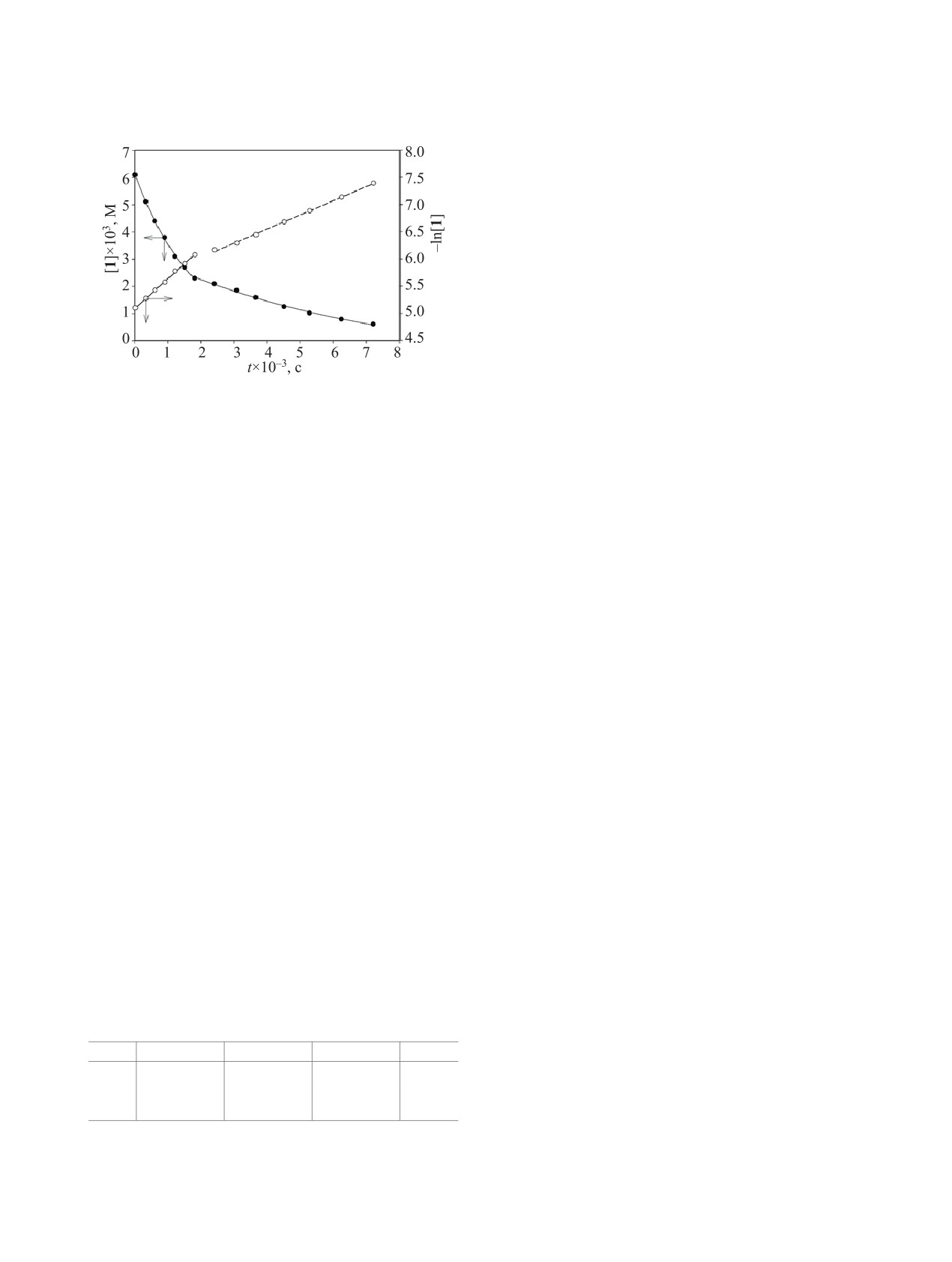
Кинетика распада циклододецилиден-1,1-бисги-
β-распад с образованием алкильного радикала.
дропероксида в ксилоле в присутствии ферроцена
Известно, что в инертной атмосфере эти радикалы
(20 ммоль/л) при 100°
могут индуцировать радикально-цепное разложе-
нения 1 определены в ксилоле в интервале темпе-
ние перекисных соединений [22].
ратуры 90-130°С (lgA = 7.4, Ea = 20.6 ккал/ моль).
Таким образом, изучена термическая стабиль-
Распад соединения 1 в присутствии ферроцена
ность циклододецилиден-1,1-бисгидропероксида
(Fc) изучен в интервале температур 80-120°С. По-
в ксилоле. Показано, что в присутствии ферроцена
сле завершения реакции, по данным спектрофото-
одновременно с термолизом протекает реакция с
метрического анализа, ферроцен в реакционной
ферроценом и индуцированный радикально-цеп-
массе отсутствует. На кинетических кривых тер-
ной распад циклододецилиден-1,1-бисгидропе-
мического распада наблюдается два участка. Оба
роксида.
участка кинетической кривой с высоким коэффи-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
циентом корреляции линеаризуются по уравне-
нию первого порядка (см. рисунок).
Циклододецилиден-1,1-бисгидропероксид син-
тезирован по методике [23]. Чистоту реагентов
Рассчитанные брутто-константы скорости рас-
контролировали методом спектроскопии ЯМР 1Н
пада на первом (k1) и втором (k2) участке, а также
и 13С{1H}. Спектры ЯМР записывали в CDCl3 на
константа скорости термического распада (k0) в
приборе Bruker Avance 500, внутренний стандарт -
отсутствие ферроцена приведены в таблице.
тетраметилсилан.
Характер влияния Fc на термическую стабиль-
Термический распад пероксидов изучали в ре-
ность соединения 1 и пероксида бензоила значи-
акторе объемом 20 мл, снабженном обратным холо-
тельно отличается. Конверсия соединения 1 на
дильником и капилляром для продувки инертным
быстром участке увеличивается при повышении
газом. В реактор помещали 5-10 мл растворителя,
температуры - 16, 46, 74% при 80, 100, 120°C со-
ответственно. В случае пероксида бензоила на
выдерживали в течение 5 мин при заданной тем-
первом участке кинетической кривой в изученном
пературе. В отдельных опытах добавляли навеску
β-нафтола, постоянно продувая инертным газом,
интервале температуры расходуется ~30%. Вклад
термического распада в процесс расходования
затем добавляли раствор пероксида и через опре-
деленные промежутки времени отбирали пробы
Зависимость константы скорости распада циклододе-
и анализировали на содержание гидроперокси-
цилиден-1,1-бисгидропероксида 1 в ксилоле в присут-
да. Количественный анализ гидропероксидов ос-
ствии ферроцена от температурыa
нован на спектрофотометрическом определении
T, °C
k0, c-1×10-4
k1, c-1×10-4
k2, c-1×10-4
k1/k0
ионов I–, образующихся при взаимодействии пе-
80
0.044±0.003
0.95±0.06
0.36±0.02
21.6
роксидных групп с иодид-ионами. В кювету (l =
100
0.21±0.02
5.5±0.3
2.6±0.2
26.2
1 см) вносили 3 мл уксусной кислоты, закрывали
120
0.86±0.04
42.6±3.1
10.0±0.7
49.5
мембраной и продували в течение 15 мин азотом
= 0.5 ммоль/л.
а [1]0 = 5 ммоль/л, [InH]0 = 20 ммоль/л, [Fc]0
для удаления растворенного О2. Затем в кювету
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 11 2020
ТЕРМИЧЕСКАЯ СТАБИЛЬНОСТЬ ЦИКЛОДОДЕЦИЛИДЕН-1,1-БИСГИДРОПЕРОКСИДА
1645
вводили ~10 мкл насыщенного раствора KI и из-
7. Puzin Yu.I., Yumagulova R.Kh., Kraikin V.A. // Eur.
меряли оптическую плотность (А0) при 360 нм.
Polym. J. 2001. Vol. 37. P. 1801. doi 10.1016/S0014-
3057(01)00038-6
Анализируемый раствор пероксидного соедине-
8. Kalenda P. // Eur. Polym. J. 1995. Vol. 31. N 11.
ния, (2-4 мкл; с = 1×10-3-1×10-2 М.) вводили че-
P. 1099. doi 10.1016/0014-3057(95)00067-4
рез мембрану и определяли оптическую плотность
9. Агарева Н.А., Иванов В.Ф., Александров А.П., Битю-
после достижения постоянного значения (A∞) [24].
рин Н.М., Смирнова Л.А. // Высокомол. соед. (А).
Спектрофотометрическое изучение реак-
2004. T. 46. № 2. C. 217; Agareva N.A., Ivanov V.F.,
ции
циклододецилиден-1,1-бисгидроперокси-
Aleksandrov A.P., Bityurin N.M., Smirnova L.A. //
да с ферроценом проводили в закрытой термо-
Polym. Sci. (A). 2004. Vol. 46. P. 105.
10. Murinov Yu.I., Grabovskii S.A., Islamova R.M.,
статированной кювете (l = 1 см) в изооктане,
Kuramshina A.R. Kabal’nova N.N. // Mendeleev
начальные концентрации [1]0 = 1.0×10-2, [Fc]0 =
Commun. 2013. Vol. 23. P. 53. doi 10.1016/j.
1.0×10-3 М. Через определенные промежутки
mencom.2013.01.020
времени на спектрофотометре Specord M40 UV-
11. Андрияшина Н.М., Грабовский С.А., Кабально-
Vis записывали спектр ферроцена {442 нм, ε =
ва Н.Н. // ЖОХ. 2019. Т. 89. № 8. С. 1164;
96 л/(моль ·см) [25]}.
Andriyashina N.M., Grabovskii S.A., Kabal’nova N.N. //
Russ. J. Gen. Chem. 2019. Vol. 89. P. 1560. doi 10.1134/
ФОНДОВАЯ ПОДДЕРЖКА
S10703632190800
Работа выполнена в рамках научно-исследова-
12. Erben M., Vesely D., Vinklarek, J. Honzicek J. // J. Mol.
тельских работ Уфимского института химии РАН
Catal. (A). 2012. Vol. 353-354. P. 13. doi 10.1016/j.
(№ госрегистрации AAAA-A20-120012090025-2) с
molcata.2011.10.024
13. Фомин В.М., Терехина А.А., Зайцева К.С. // ЖОХ.
использованием оборудования Центра коллектив-
2013. Т. 83. № 12. С. 2041; Fomin V.M., Terekhina A.A.,
ного пользования «Химия» Уфимского института
Zaitseva K.S. // Russ. J. Gen. Chem. 2013. Vol. 83.
химии Уфимского федерального исследователь-
N 12. P. 2324. doi 10.1134/S1070363213120177
ского центра РАН.
14. Фомин В.М., Кочеткова К.С., Галкина М.С. // ЖФХ.
КОНФЛИКТ ИНТЕРЕСОВ
2017. Т. 91. № 7. С. 1186; Fomin V.M., Kochetkova K.S.,
Galkina M.S. // Russ. J. Phys. Chem. (A). 2017. Vol. 91.
Авторы заявляют об отсутствии конфликта
N 7. P. 1285. doi 10.1134/S0036024417070111
интересов.
15. Фомин В.М., Орлова Е.А., Зайцева К.С. // ЖОХ. 2014.
Т. 84. № 4. С. 645; Fomin V.M., Orlova E.A., Zaitse-
СПИСОК ЛИТЕРАТУРЫ
va K.S. // Russ. J. Gen. Chem. 2014. Vol. 84. N 4.
1. Beckwith A.L.J., Leydon R.J. // Tetrahedron. 1964.
P. 722. doi 10.1134/S1070363214040215
Vol. 20. P. 791. doi 10.1016/S0040-4020(01)98412-1
16. Shul’pin G.B., Kirillova M.V., Shul’pina L.S., Pom-
2. Chen E.Y.-X., Marks T.J. // Chem. Rev. 2000. Vol. 100.
beiro A.J.L., Karslyan E.E., Kozlov Yu.N. // Catal.
N 4. P. 1391. doi 10.1021/cr980462j
Commun. 2013. Vol. 31. P. 32. doi 10.1016/j.
3. Ayres N. // Polym. Rev. 2011. Vol. 51. N 2. 138. doi
catcom.2012.11.003
10.1080/15583724.2011.566402
17. Терентьев А.О., Платонов М.М., Никишин Г.И.,
4. Исламова Р.М. // ЖОХ. 2016. Т. 86. № 1. С. 133;
Корольков М.М., Куткин А.В., Уткин А.Ю. Пат.
Islamova R.M. // Russ. J. Gen. Chem. 2016. Vol. 86.
2006146697 (2006). РФ.
N 1. P. 125. doi 10.1134/S1070363216010217
18. Сахарова А.А., Выгодский Я.С., Терентьев А.О., Пла-
5. Monakov Yu.B., Islamova R.M., Frizen A.K.,
тонов М.М., Сапожников Д.А., Волкова Т.В., Ники-
Golovochesova O.I., Nazarova S.V. // Mendeleev
шин Г.И. Пат. 2007147786 (2007). РФ.
Commun. 2011. Vol. 21. P. 206. doi 10.1016/j.
19. Терентьев А.О., Сахарова А.А., Выгодский Я.С.,
mencom.2011.07.012
Платонов М.М., Сапожников Д.А., Волкова Т.В.,
6. Исламова Р.М., Ишкинина О.И., Назарова С.В.
Никишин Г.И. Пат. 2008112023 (2008). РФ.
Чупахин О.Н. Утепова И.А., Андрияшина Н.М.,
20. Terent’ev A.O., Kutkin A.V., Platonov M.M., Ogibin Yu.N.,
Терентьев А.О. // Изв. АН. Сер. хим. 2013. № 5.
Nikishin G.I. // Tetrahedron Lett. 2003. Vol. 44. P. 7359.
С. 1282; Islamova R.M., Ishkinina O.I., Nazarova S.V.,
doi 10.1016/S0040-4039(03)01844-6
Chupakhin O.N., Utepova I.A., Andriyashina N.M.,
21. Терентьев А.О., Куткин А.В., Платонов В.В., Во-
Terent’ev A.O. // Russ. Chem. Bull. 2013. Vol. 62. N 5.
ронцов И.И., Антипин М.Ю., Огибин Ю.Н., Ники-
P. 1282. doi 10.1007/s11172-013-0177-z
шин Г.И. // Изв. АН Сер. xим. 2004. № 3. C. 650;
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 11 2020
1646
АНДРИЯШИНА и др.
Terentґev A.O., Kutkin A.V., Platonov M.M., Voron-
23. Terent’ev A.O., Platonov M.M., Ogibin Y.N., Niki-
shin G.I. // Synth. Commun. 2007. Vol. 37. N 8. P. 1281.
tsov I.I., Antipin M.Yu., Ogibin Yu.N., Nikishin G.I. //
doi 10.1080/00397910701226384
Russ. Chem. Bull. 2004. Vol. 53. N 3. P. 681. doi
24. Сафиуллин Р.Л., Еникеева Л.Р., Серенко С.Ю.,
10.1023/B:RUCB.0000035657.58776.cc
Комиссаров В.Д., Толстиков А.Г. // Изв. АН Сер.
22. Хурсан С.Л., Грабовский С.А., Кабальнова Н.Н.,
xим. 1991. № 2. С. 333; Safiullin R.L., Enikeeva L.R.,
Галкин Е.Г., Шерешовец В.В. // Изв. АН Сер. xим.
Serenko S.Yu., Komissarov V.D., Tolstikov G.A. // Bull.
Acad. Sci. USSR. Div. Chem. Sci. 1991. Vol. 40. No2.
2000. № 8. С. 1344; Khursan S.L., Grabovskii S.A.,
P. 280.
Kabal’nova N.N., Galkin E.G., Shereshovets V.V. //
25. Vorotyntsev M.A., Zinovyeva V.A., Konev D.V.,
Russ. Chem. Bull. 2000. Vol. 49. P. 1338. doi 10.1007/
Picquet M. // J. Phys. Chem. (B). 2009. Vol. 113. N 4.
BF02495074
P. 1085. doi 10.1021/jp809095q
Thermal Stability of Cyclododecylidene-1,1-bishydroperoxide
in the Presence of Ferrocene
N. M. Andriyashina, S. A. Grabovsky*, and N. N. Kabalnova
Ufa Institute of Chemistry, Russian Academy of Sciences, Ufa, 450054 Russia
*e-mail: stas_g@anrb.ru
Received June 26, 2020; revised June 26, 2020; accepted July 9, 2020
The thermal stability of cyclododecylidene-1,1-bishydroperoxide in xylene was studied and the activation
parameters of the reaction were determined. The reaction with ferrocene and the induced radical chain
decomposition of cyclododecylidene-1,1-bishydroperoxide occur simultaneously with thermolysis.
Keywords: cyclododecylidene-1,1-bishydroperoxide, ferrocene, thermal stability
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 11 2020