ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 12, с. 1910-1920
УДК 544.18;544.163
ЭЛЕКТРОННОЕ СТРОЕНИЕ И МАГНИТНЫЕ
СВОЙСТВА СМЕШАННО-ЛИГАНДНЫХ
КОМПЛЕКСОВ КОБАЛЬТА, СОДЕРЖАЩИХ
ГЕРМАНИЙОРГАНИЧЕСКИЕ ТРИАНГУЛЕНЫ
© 2020 г. М. Г. Чегерев, А. А. Старикова*, А. Г. Стариков, В. И. Минкин
Научно-исследовательский институт физической и органической химии Южного федерального университета,
пр. Стачки 194/2, Ростов-на-Дону, 344090 Россия
*e-mail: aastarikova@sfedu.ru
Поступило в Редакцию 27 июля 2020 г.
После доработки 27 июля 2020 г.
Принято к печати 8 августа 2020 г.
С применением метода теории функционала плотности выполнено компьютерное моделирование
аддуктов дикетонатов кобальта(II) с о-бензохиноном, модифицированным германийорганическими
триангуленами различного размера. Энергетические характеристики изомеров комплексов зависят от
терминальных заместителей в дикетонатах. Предсказан парамагнетизм всех состояний изученных моле-
кул. Найдены системы, магнитные свойства которых переключаются в результате внутримолекулярного
переноса электрона между ионом кобальта и лигандом.
Ключевые слова: комплексы кобальта, о-бензохинон, германийорганические полициклические соеди-
нения, валентная таутомерия, магнитные свойства
DOI: 10.31857/S0044460X20120148
Металлокомплексы с о-бензохиноновыми (ди-
докс-изомерии (валентной таутомерии) наиболее
оксоленовыми) лигандами, обладающими богатым
часто встречается в соединениях кобальта с про-
окислительно-восстановительным потенциалом
изводными о-бензохинона [7, 10-15]. Изомеры,
[1, 2], привлекают внимание специалистов в об-
участвующие в редокс-превращении, различаются
ласти химии и материаловедения [3-7]. Электро-
распределением зарядов и, следовательно, имеют
ноактивность металлических центров и органиче-
различные оптические, электронные и магнитные
ских фрагментов, приводящая к возникновению
свойства, что указывает на потенциальное приме-
различных электронных изомеров (электромеров
нение валентно-таутомерных соединений в моле-
[8]), - отличительная особенность координаци-
кулярных переключающих материалах и устрой-
онных соединений переходных металлов с ре-
ствах [4, 9, 16-18].
докс-лигандами. Такие молекулы обладают замет-
Особое внимание привлекают молекулы, име-
ной чувствительностью к окружающей среде, и
ющие в своем составе, кроме иона металла и
внешнее воздействие, например, свет, температу-
редокс-лиганда, заместитель, придающий пара-
ра или давление, способно вызывать взаимопре-
магнетизм всем электромерам вне зависимости от
вращение изомеров [9]. К электронно-лабильным
степени окисления и спинового состояния метал-
системам относятся валентно-таутомерные ком-
лоцентра и окислительно-восстановительной фор-
плексы с двумя, по меньшей мере, редокс-актив-
мы лиганда. Исследованы соединения d-металлов
ными центрами (ион металла и лиганд), между
с о-хинонами, замещенными нитронилнитрок-
которыми происходит обратимый внутримолеку-
сильным радикалом [19-21], изучены гетероспи-
лярный перенос электрона [1, 10-12]. Феномен ре-
новые металлокомплексы с двумя редокс-актив-
1910
ЭЛЕКТРОННОЕ СТРОЕНИЕ И МАГНИТНЫЕ СВОЙСТВА
1911
Схема 1.
ными лигандами, в которых парамагнитная группа
сических углеводородных аналогов феналенила
непосредственно связана с комплексообразовате-
[35-40], которые характеризуются ферромагнит-
лем [22, 23] или присоединена к азотистому осно-
ными обменными взаимодействиями внутри по-
ванию [24-26].
лициклического фрагмента [31, 41-43].
Недавно нами были выполнены квантово-хими-
С целью поиска соединений, потенциально
ческие расчеты аддуктов дикетонатов кобальта(II)
способных к переключению магнитных свойств
и о-бензохинонов с триангуленовыми углеводо-
родными группами [27]. Проведенное исследова-
ние позволило выявить перспективные гетероспи-
новые магнитно-активные соединения, склонные
к протеканию термически управляемых валент-
но-таутомерных перегруппировок. Преимущество
таких систем над предложенными ранее сериями
1 LSCoIII-SQ-X
комплексов кобальта с разными лигандами [28-30]
заключается в уникальном свойстве триангулено-
вых заместителей, а именно, в увеличении коли-
чества неспаренных электронов с возрастанием
числа шестичленных циклов в основании треу-
гольника [31, 32]. Благодаря этому возможно по-
вышение общего спина системы посредством рас-
ширения полициклической части лиганда.
2 HSCoII-Q-X
Частичное замещение атомов углерода на ато-
Рис. 1. Распределение спиновой плотности в изомерах
мы других элементов 14 группы в α-положениях
1 и 2 комплекса А (R1 = R2 = Me), рассчитанное мето-
триангуленовых колец [33, 34] приводит к фор-
дом DFT UB3LYP*/6-311++G(d,p). Здесь и далее атомы
водорода опущены.
мированию систем, сохраняющих свойства клас-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
1912
ЧЕГЕРЕВ и др.
Таблица 1. Спин (S), полная энергия (E), энергия стабилизации (Естаб), относительная энергия (ΔE), значения опера-
тора квадрата спина (S2) и величина параметра обменных взаимодействий (J) в изомерах комплексов А (R1, R2 = Me,
CF3), рассчитанные методом DFT UB3LYP*/6-311++G(d,p)
Естаба
ΔE
№
Изомер
S
E, ат. ед.
S2
J, см-1
ккал/моль
R1 = R2 = Me
1
LS
CoIII-SQ-X
1
-15153.033174
22.0
0.0
2.050
215
LS
CoIII-SQ-X BSб
0
-15153.032186
1.040
2
HS
CoII-Q-X
2
-15153.007556
5.9
16.1
6.602
-54
HS
CoII-Q-X BS
1
-15153.008291
3.623
R1 = Me, R2 = CF3
3
LS
CoIII-SQ-X
1
-15745.751538
21.4
0.0
2.052
266
LS
CoIII-SQ-X BS
0
-15745.750309
1.039
4
HS
CoII-Q-X
2
-15745.732857
9.7
11.7
6.301
-41
HS
CoII-Q-X BS
1
-15745.733409
3.329
R1 = R2 = CF3
5
LS
CoIII-SQ-X
1
-16338.460865
21.9
0.0
2.055
351
LS
CoIII-SQ-X BS
0
-16338.459233
1.033
6
HS
CoII-Q-X
2
-16338.450862
15.7
6.3
6.152
-31
HS
CoII-Q-X BS
1
-16338.451283
3.185
а Здесь и далее энергии стабилизации вычислены относительно суммы энергий молекул дикетоната Co(II) и редокс-лиганда.
б Здесь и далее состояние с нарушенной симметрией (broken symmetry - BS).
по механизму валентной таутомерии, методом те-
в изомер 1 LSCoIII-SQ-X (X - полициклический
ории функционала плотности (DFT) нами выпол-
фрагмент) трехвалентного низкоспинового иона
нено компьютерное моделирование электронного
кобальта и редокс-активного лиганда в анион-ра-
строения, энергетических параметров и магнит-
дикальной семихиноновой (SQ) форме. Спиновые
ных свойств электромерных форм аддуктов А-В
плотности на смежных атомах органических ра-
бис(ацетилацетонатов), бис(трифторацетилацето-
дикалов имеют противоположные знаки (0.19 на
натов) и бис(гексафторацетилацетонатов) кобаль-
атоме С бензохинонового кольца и -0.14 на атоме
та(II) с о-бензохиноном, замещенным германийор-
Ge производного феналенила), что, согласно сфор-
ганической триангуленовой группой. Исследована
мулированному ранее правилу [44], позволяет
возможность внутримолекулярного переноса элек-
ожидать реализацию ферромагнитного обмена. И
трона в комплексах А-В (схема 1), оценены об-
действительно, поиск состояния с «нарушенной
менные взаимодействия между парамагнитными
симметрией» (broken symmetry - BS) 1 LSCoIII-
центрами, сделаны выводы о влиянии включения
SQ-X BS и последующая оценка обменного свя-
атомов германия в триангуленовые кольца.
зывания свидетельствуют о сильных ферромаг-
нитных взаимодействиях между органическими
Как следует из результатов квантово-химиче-
фрагментами (табл. 1). Следовательно, электромер
ских расчетов, основному состоянию комплекса
1 LSCoIII-SQ-X проявляет парамагнетизм во всем
бис(ацетилацетоната) кобальта A (R1 = R2 = Me)
диапазоне температур.
соответствует минимум на триплетной поверхно-
сти потенциальной энергии. Отсутствие в обсуж-
Согласно распределению спиновой плотности,
даемой структуре спиновой плотности на ионе
в изомере 2 соединения A (R1 = R2 = Me) (рис. 1)
металла и наличие по одному делокализованному
на ионе кобальта сосредоточено три неспаренных
электрону в о-бензохиноновом и полицикличе-
электрона, что позволяет приписать минимуму на
ском фрагментах (рис. 1) указывают на вхождение
квинтетной поверхности потенциальной энергии
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
ЭЛЕКТРОННОЕ СТРОЕНИЕ И МАГНИТНЫЕ СВОЙСТВА
1913
1 LSCoIII-SQ-X
2 HSCoII-Q-X
3 LSCoIII-SQ-X
4 HSCoII-Q-X
5 LSCoIII-SQ-X
6 HSCoII-Q-X
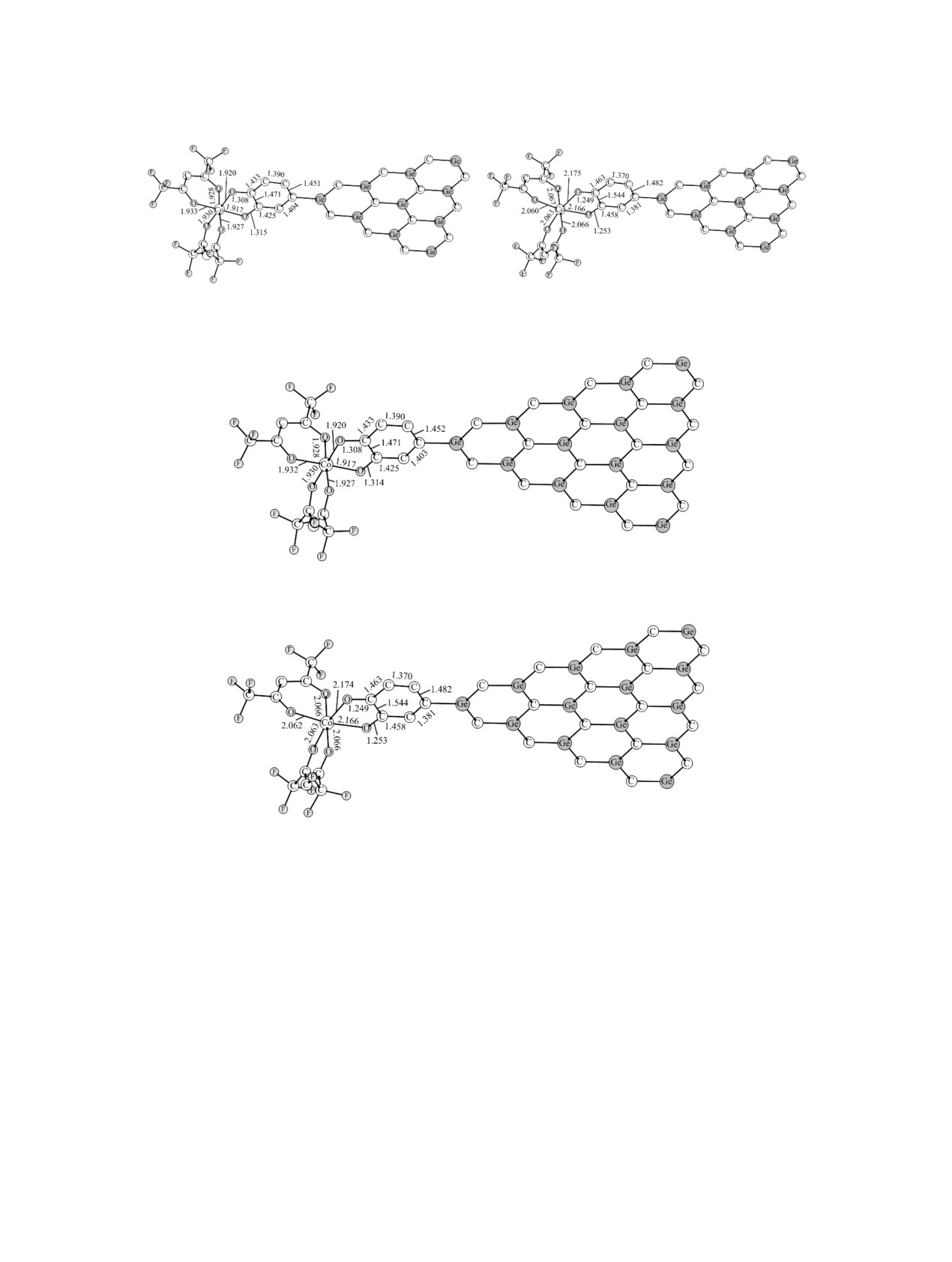
Рис. 2. Геометрические параметры изомеров комплексов А (R1, R2 = Me, CF3), рассчитанные методом DFT UB3LY-
P*/6-311++G(d,p). Здесь и далее длины связей приведены в Å.
электронное состояние HSCoII-Q-X, включающее
R2 = CF3) аналогично строению структур 1 и 2
высокоспиновый двухвалентный ион металла и
(табл. 1). Замена одной из метильных групп в дике-
хинон (Q) в нейтральной форме. В структуре 2
тоновом лиганде на группу CF3 ожидаемо [30, 45,
CoII-Q-X предсказаны умеренные антиферро-
HS
46] приводит к сокращению энергетической щели
магнитные обменные взаимодействия между па-
между низко- (LSCoIII-SQ-X, 3) и высокоспиновым
рамагнитными центрами HSCoII и X (табл. 1). Вы-
(HSCoII-Q-X, 4) электромерами (рис. 1, табл. 1).
численные параметры J соединения A (R1 = R2 =
Однако расчетное значение ΔE = 11.7 ккал/моль
Me) в 2 раза превышают значения, найденные для
свидетельствует о низкой вероятности термически
аналогичного бис(ацетилацетонатного) комплек-
инициированного внутримолекулярного переноса
са, включающего углеводородный полицикли-
электрона.
ческий фрагмент [27]. Дестабилизация электро-
мера 2 относительно основного состояния на
Оттягивание спиновой плотности сильными
16.1 ккал/моль указывает на его термическую
электроноакцепторными заместителями CF3 в ди-
недостижимость. Таким образом, соединение A
кетоновых фрагментах высокоспинового изомера
(R1 = R2 = Me) находится в триплетном состоянии
6 HSCoII-Q-X бис(гексафторацетилацетоната) ко-
1 LSCoIII-SQ-X.
бальта A (R1 = R2 = CF3) способствует усилению
Электронное строение изомеров 3 и 4 бис(триф-
альтернирования связей в о-бензохиноновом коль-
торацетилацетонатного комплекса) A (R1 = Me,
це и формированию межатомных расстояний, ха-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
1914
ЧЕГЕРЕВ и др.
Таблица 2. Спин (S), полная энергия (E), энергия стабилизации (Естаб), относительная энергия (ΔE), значения опера-
тора квадрата спина (S2) и величина параметра обменных взаимодействий (J) в изомерах комплексов Б (R1, R2 = Me,
CF3), рассчитанные методом DFT UB3LYP*/6-311++G(d,p)
Естаб
ΔE
№
Изомер
S
E, ат. ед.
S2
J, см-1
ккал/моль
R1 = R2 = Me
7
CoIII-SQ-X
3/2
-23636.544781
22.1
0.0
3.840
123
LS
CoIII-SQ-X BSб
1/2
-23636.543654
1.829
LS
8
CoII-Q-X
5/2
-23636.518926
5.9
16.2
9.397
-31
HS
CoII-Q-X BS
1/2
-23636.519772
3.421
HS
R1 = Me, R2 = CF3
9
CoIII-SQ-X
3/2
-24229.263103
21.5
0.0
3.842
156
LS
CoIII-SQ-X BS
1/2
-24229.261667
1.829
LS
10
CoII-Q-X
5/2
-24229.244178
9.6
11.9
9.093
-24
HS
CoII-Q-X BS
1/2
-24229.244828
3.123
HS
R1 = R2 = CF3
11
CoIII-SQ-X
3/2
-24821.972502
22.1
0.0
3.845
210
LS
CoIII-SQ-X BS
1/2
-24821.970566
1.823
LS
12
CoII-Q-X
5/2
-24821.962448
15.8
6.3
8.963
-22
HS
CoII-Q-X BS
1/2
-24821.963035
3.021
HS
рактерных для нейтральной Q-формы редокс-ли-
ся в основном низкоспиновом состоянии LSCoIII-
ганда (рис. 2). Такие геометрические изменения
SQ-X (табл. 2). Судя по предсказанным величинам
стабилизируют высокоспиновое состояние, что
относительной энергии и энергии стабилизации
находит отражение в уменьшении разности энер-
электромеров 11 LSCoIII-SQ-X и 12 HSCoII-Q-X,
гий между структурами 5 и 6 до величины 6.3
в комплексe Б (R1, R2 = CF3) возможна валентная
ккал/моль, при которой возможен валентно-тауто-
таутомерия. Длины связей (рис. 3) в координаци-
мерный переход (1) [9, 11].
онном узле и бензохиноновом кольце комплекса Б
(R1 = R2 = CF3) близки к найденным величинам в
5 LSCoIII-SQ-X ← 6 HSCoII-Q-X.
(1)
соединении A (R1 = R2 = CF3) (рис. 2), что указы-
Термодинамическая устойчивость молекуляр-
вает на несущественное влияние размера полици-
ного комплекса 6 HSCoII-Q-X к диссоциации на
клического фрагмента на расстояния между атома-
исходные молекулы дикетоната кобальта(II) и за-
ми в редокс-активной части аддукта.
мещенного о-бензохинона (табл. 1) позволяет ожи-
Германийорганический заместитель в изомерах
дать завершенность редокс-процесса. Сильный
11 и 12 с двумя локализованными неспаренными
ферромагнитный обмен в низкоспиновом изомере
электронами представляет собой единый пара-
и слабое антиферромагнитное связывание в высо-
магнитный центр благодаря сильному ферромаг-
коспиновом электромере (табл. 1) не препятствуют
нитному обмену внутри треугольного фрагмента
изменению спина системы от S = 1 до S = 2. Таким
[31, 41-43]. Как показали расчеты параметров
образом, соединение A (R1 = R2 = CF3) перспек-
обменного связывания в электромерах 11 и 12
тивно для дизайна молекулярных переключателей.
(табл. 2), расширение триангуленового заместите-
При теоретическом изучении комплексов Б (R1,
ля не приводит к изменению характера обмена, но
R2 = Me, CF3) зависимость энергетических харак-
сопровождается некоторым ослаблением величин
теристик изомеров от количества аннелированных
J, обусловленным увеличением расстояния между
колец в полициклическом заместителе не обнару-
парамагнитными центрами ввиду делокализации
жена: соединения на основе бис(ацетилацетоната)
неспаренных электронов полицикла. Полученные
и бис(трифторацетилацетоната) кобальта находят-
теоретические данные позволяют заключить, что
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
ЭЛЕКТРОННОЕ СТРОЕНИЕ И МАГНИТНЫЕ СВОЙСТВА
1915
11 LSCoIII-SQ-X
12 HSCoII-Q-X
17 LSCoIII-SQ-X
18 LSCoIII-SQ-X
Рис. 3. Геометрические параметры валентно-таутомерных изомеров комплексов Б и В (R1 = R2 = CF3), рассчитанные ме-
тодом DFT UB3LYP*/6-311++G(d,p).
комплекс Б (R1 = R2 = CF3) потенциально способен
сделанные ранее выводы о независимости энер-
к термически инициированной валентной тауто-
гетических параметров и геометрических харак-
мерии с ожидаемым переходом системы из квар-
теристик координационного узла от размера по-
тетного в секстетное спиновое состояние.
лициклического фрагмента. Увеличение размера
триангуленового заместителя приводит к повыше-
В заключение рассмотрим комплексы В, в ко-
нию количества электронов в системе: ожидаемый
торых германийорганический заместитель имеет
редокс-изомерный переход (2) сопровождается пе-
в основании треугольника 4 шестичленных цикла.
реключением спинового состояния с S = 2 до S = 3.
Согласно результатам расчетов соединений В (R1,
R2 = Me, CF3), только в комплексе бис(гексафто-
17 LSCoIII-SQ-X ← 18 HSCoII-Q-X.
(2)
рацетилацетоната) кобальта проявляется валент-
Несмотря на ослабление обменного связыва-
ная таутомерия (рис. 3, табл. 3), что подтверждает
ния в структурах 17 и 18 (табл. 3), по сравнению
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
1916
ЧЕГЕРЕВ и др.
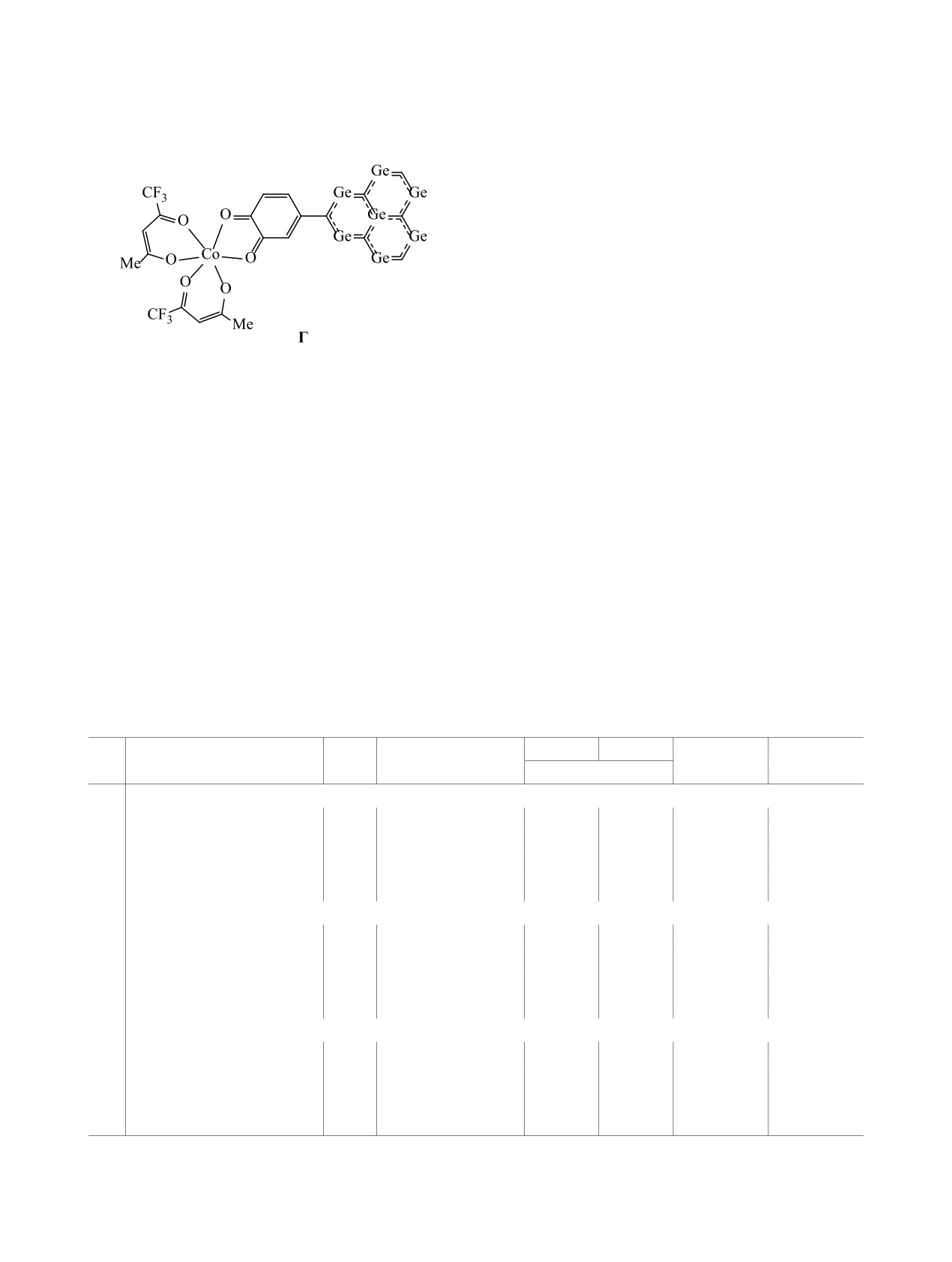
Схема 2.
нийорганическими триангуленами. Можно пред-
положить, что энергетические характеристики
соединений А-В зависят от положения (α или β)
атомов германия в триангулене. С целью проверки
данной гипотезы исследован комплекс Г (схема 2).
Размещение атомов германия в β-положениях
полициклического заместителя приводит к зна-
чительному изменению электронного и геоме-
трического строения триангуленового фрагмента
комплекса Г (рис. 4). Согласно расчетам, в низ-
коспиновом изомере 1а LSCoIII-SQ-X один из двух
с предсказанными в электромерах 5, 6 (табл. 1) и
β-атомов Ge выходит из плоскости полицикла и
11, 12 (табл. 2), оба изомера 17, 18 комплекса В
его пространственное окружение становится пи-
(R1 = R2 = CF3) характеризуются ненулевыми об-
рамидальным. Такое искажение цикла приводит к
менными взаимодействиями, и это делает ком-
разрушению единой сопряженной sp2-гибридизо-
плекс В подходящим кандидатом для дизайна
ванной системы и сопровождается локализацией
молекулярной памяти или спиновых квантовых
спиновой плотности (0.60) на p-орбитали вышед-
битов.
шего из плоскости атома Ge. Подобное поведение,
Среди изученных ранее комплексов с триангу-
вероятнее всего, обусловлено слабовыраженной
леновыми углеводородными заместителями [27]
склонностью к образованию кратных связей ато-
производные бис(трифторацетилацетоната) ко-
ма углерода с элементом, находящимся ниже в
бальта(II) также обладали валентной таутомерией:
подгруппе углерода [47]. Величины межатомных
вычисленная разность энергий в комплексах [27]
расстояний (~1.95 Å) Ge-C (Ge - вышедший из
на 3-4 ккал/моль меньше, чем аналогичные ве-
плоскости полицикла атом германия) близки к зна-
личины для рассмотренных соединений с герма-
чениям, характерным для ординарных связей Ge-
Таблица 3. Спин (S), полная энергия (E), энергия стабилизации (Естаб), относительная энергия (ΔE), значения опера-
тора квадрата спина (S2) и величина параметра обменных взаимодействий (J) в изомерах комплексов В (R1, R2 = Me,
CF3), рассчитанные методом DFT UB3LYP*/6-311++G(d,p)
Естаб
ΔE
№
Изомер
S
E, ат. ед.
S2
J, см-1
ккал/моль
R1 = R2 = Me
13
CoIII-SQ-X
2
-34231.049123
22.1
0.0
6.122
75
LS
CoIII-SQ-X BSб
1
-34231.048096
3.112
LS
14
CoII-Q-X
3
-34231.023290
5.9
16.2
12.684
-19
HS
CoII-Q-X BS
0
-34231.024065
3.706
HS
R1 = Me, R2 = CF3
15
CoIII-SQ-X
2
-34823.767358
21.5
0.0
6.124
95
LS
CoIII-SQ-X BS
1
-34823.766051
3.111
LS
16
CoII-Q-X
3
-34823.748487
9.6
11.8
12.373
-15
HS
CoII-Q-X BS
0
-34823.749080
3.401
HS
R1 = R2 = CF3
17
CoIII-SQ-X
2
-35416.476701
22.0
0.0
6.127
130
LS
CoIII-SQ-X BS
1
-35416.474914
3.106
LS
18
CoII-Q-X
3
-35416.466836
15.8
6.2
12.241
-14
HS
CoII-Q-X BS
0
-35416.467386
3.298
HS
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
ЭЛЕКТРОННОЕ СТРОЕНИЕ И МАГНИТНЫЕ СВОЙСТВА
1917
1a LSCoIII-SQ-X
2a HSCoII-SQ-X
2a
1a
Рис. 4. Распределение спиновой плотности, геометрические, энергетические и магнитные характеристики изомеров
комплекса Г, рассчитанные методом DFT UB3LYP*/6-311++G(d,p). Вверху приведены значения спиновой плотности на
отдельных атомах, внизу - избранные длины связей.
C, а гибридизацию атомных орбиталей можно опи-
налениле (табл. 1). Следовательно, энергетически-
сать как sp3 (рис. 4). Геометрические изменения в
ми и электронными характеристиками аддуктов
полициклическом заместителе находят отражение
А-В можно управлять не только варьированием
в магнитных свойствах изомера: из-за близости
заместителей в дикетонатных лигандах, но и вы-
неспаренных электронов ожидаются сильные ан-
бором положения гетероатомов в триангуленовом
тиферромагнитные обменные взаимодействия (J =
фрагменте. Предсказанный переход (3) не явля-
-726 cм-1), и основное состояние 1а LSCoIII-SQ-X
ется классическим валентно-таутомерным, он об-
становится диамагнитным.
условлен переносом заряда с полициклического
Поиск высокоспинового изомера 2а на квинтет-
заместителя X на металл через редокс-активный
ной поверхности потенциальной энергии привел
лиганд.
к структуре, в которой длины связей о-бензохино-
1а LSCoIII-SQ-X ← 2а HSCoII-SQ-X.
(3)
нового фрагмента имеют промежуточное значение
Таким образом, выполненное методом DFT
между предсказанными в изомерах 4 HSCoII-Q-X
UB3LYP*/6-311++G(d,p) компьютерное моделиро-
(рис. 2) и 1а LSCoIII-SQ-X, а спиновая плотность
вание комплексов на основе дикетонатов кобаль-
триангулена практически полностью перенесе-
та(II) и о-бензохиноновых лигандов с германий-
на на редокс-активный лиганд, что позволяет
органическими триангуленовыми заместителями
приписать обсуждаемому электромеру 2а форму
позволило выявить магнитно-активные гетеро-
CoII-SQ-X (рис. 4). Расчет состояния с нару-
HS
спиновые системы. Комплексы бис(гексафтора-
шенной симметрией (BS) и последующая оценка
цетилацетоната) кобальта склонны к проявлению
параметра обмена предсказывают сильное фер-
термически-инициированных валентно-таутомер-
ромагнитное обменное связывание между высо-
ных переходов не зависимо от размера полицикли-
коспиновым двухвалентным ионом кобальта и се-
ческого заместителя. Сравнение полученных ре-
михиноновым (SQ) анион-радикалом (J = 138 cм-1).
зультатов с данными для аналогичных комплексов
Разность энергий между электромерами 1а
с фрагментом углеводородного феналенила в ре-
и 2а комплекса Г (6.1 ккал/моль) почти в 2 раза
докс-лиганде [27] показывает усиление обменного
меньше, чем в аналогичном комплексе А (R1 = Me,
связывания при частичной замене атомов углерода
R2 = CF3) c α-положением атомов германия в фе-
на атомы германия. Благодаря взаимодействую-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
1918
ЧЕГЕРЕВ и др.
щим парамагнитным центрам во всех перегруппи-
СПИСОК ЛИТЕРАТУРЫ
ровывающихся электромерах, изученные комплек-
1.
Rajput A., Sharma A.K., Barman S.K., Saha A., Mukher-
сы можно рассматривать в качестве молекулярных
jee R. // Coord. Chem. Rev. 2020. Vol. 414. P. 213240.
переключателей и спиновых квантовых битов.
doi 10.1016/j.ccr.2020.213240
Размещение атомов германия в β-положениях три-
2.
Poddel’sky A.I., Cherkasov V.K., Abakumov G.A. // Co-
ангулена приводит к реализации необычного ре-
ord. Chem. Rev. 2009. Vol. 253. N 3-4. P. 291. doi
докс-процесса, заключающегося в переносе заряда
10.1016/j.ccr.2008.02.004
с полициклического заместителя на металл через
3.
Чегерев М.Г., Пискунов А.В. // Коорд. хим. 2018.
редокс-активный лиганд. Ряды магнитно-актив-
Т. 44. № 2. С. 109; Chegerev M.G., Piskunov A.V. //
Russ. J. Coord. Chem. 2018. Vol. 44. N 4. P. 258. doi
ных соединений с замещенным о-бензохиноном
10.1134/S1070328418040036
могут быть расширены за счет использования в ка-
4.
Drath O., Boskovic C. // Coord. Chem. Rev. 2018. Vol.
честве вспомогательных лигандов тетрадентатных
375. P. 256. doi 10.1016/j.ccr.2017.11.025
макроциклических азотсодержащих оснований [7,
5.
Witt A., Heinemann F.W., Sproules S., Khusniya-
11, 12, 15], что открывает перспективы для даль-
rov M.M. // Chem. Eur. J. 2014. Vol. 20. N 35. P. 11149.
нейших исследований.
doi 10.1002/chem.201402129
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
6.
Pierpont C.G. // Inorg. Chem. 2011. Vol. 50. N 20.
P. 9766. doi 10.1021/ic201237d
Квантово-химические расчеты проведены с ис-
7.
Dei A., Sorace L. //Appl. Magn. Res. 2010. Vol. 38.
пользованием программы Gaussian 16 [48] методом
P. 139. doi 10.1007/s00723-010-0121-4
теории функционала плотности в приближении
8.
Bally T. // Nature Chem. 2010. Vol. 2. N 3. P. 165. doi
UB3LYP*/6-311++G(d,p), корректно воспроизво-
10.1038/nchem.564
дящем энергетические и магнитные характеристи-
9.
Spin-Crossover Materials: Properties and Applications /
ки комплексов кобальта с редокс-активными ли-
Ed. M.A. Halcrow Chichester: John Wiley & Sons,
2013. 564 p.
гандами [23, 49-53]. Локализацию стационарных
10.
Buchanan R.M., Pierpont C.G. // J. Am. Chem. Soc.
точек на поверхности потенциальной энергии осу-
1980. Vol. 102. N 15. P. 4951. doi 10.1021/ja00535a021
ществляли путем полной оптимизации геометрии
11.
Tezgerevska T., Alley K.G., Boskovic C. // Coord.
молекулярных структур без наложения ограниче-
Chem. Rev. 2014. Vol. 268. P. 23. doi 10.1016/j.
ний по симметрии с проверкой стабильности DFT
ccr.2014.01.014
волновой функции. Параметры обменного взаимо-
12.
Gransbury G.K., Boulon M.-E., Petrie S., Gable R.W.,
действия (J, см-1) находили посредством расчета
Mulder R.J., Sorace L., Stranger R., Boskovic C. //
всех возможных спиновых состояний изомеров
Inorg. Chem. 2019. Vol. 58. N 7. P. 4230. doi 10.1021/
в рамках формализма “нарушенной симметрии”
acs.inorgchem.8b03291
(broken symmetry) [54] с применением формулы
13.
Poneti G., Mannini M., Cortigiani B., Poggini L., Sor-
Ямагучи [55]. Графические изображения молеку-
ace L., Otero E., Sainctavit P., Sessoli R., Dei A. // In-
лярных структур, представленные на рис. 1-4, по-
org. Chem. 2013. Vol. 52. N 20. P. 11798. doi 10.1021/
ic4011949
лучены при помощи программы ChemCraft [56], в
14.
Wu S.-Q., Liu M., Gao K., Kanegawa S., Horie Y., Aoya-
качестве входных параметров для которой исполь-
ma G., Okajima H., Sakamoto A., Baker M.L., Huzan M.S.,
зованы декартовы координаты атомов, получен-
Bencok P., Abe T., Shiota Y., Yoshizawa K., Xu W.,
ные в квантово-химических расчетах.
Kou H.-Z., Sato O. // Nat. Commun. 2020. Vol. 11.
ФОНДОВАЯ ПОДДЕРЖКА
P. 1992. doi 10.1038/s41467-020-15988-1
15.
Gransbury G.K., Livesay B.N., Janetzki J.T., Hay M.A.,
Работа выполнена при поддержке Министер-
Gable R.W., Shores M.P., Starikova A., Boskovic C. //
ства науки и высшего образования Российской
J. Am. Chem. Soc. 2020. Vol. 142. N 24. P. 10692. doi
Федерации (государственное задание в сфере на-
10.1021/jacs.0c01073
учной деятельности, проект № 0852-2020-0031).
16.
Molecular Switches / Eds. Feringa B.L., Browne W.R.
Wiley-VCH: Weinheim, 2011. 824 p.
КОНФЛИКТ ИНТЕРЕСОВ
17.
Demir S., Jeon I.-R., Long J.R., Harris T.D. // Coord.
Авторы заявляют об отсутствии конфликта
Chem. Rev. 2015. Vol. 289-290. P. 149. doi 10.1016/j.
интересов.
ccr.2014.10.012
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
ЭЛЕКТРОННОЕ СТРОЕНИЕ И МАГНИТНЫЕ СВОЙСТВА
1919
18.
Sato O. // Nature Chem. 2016. Vol. 8. N 7. P. 644. doi
33.
Гапуренко О.А., Миняев Р.М., Стариков А.Г., Мин-
10.1038/nchem.2547
кин В.И. // Доклады АН. 2013. Т. 448. № 3. P. 301;
19.
Shultz D.A., Vostrikova K.E., Bodnar S.H., Koo H.-J.,
Gapurenko O.A., Minyaev R.M., Starikov A.G., Min-
Whangbo M.-H., Kirk M.L., Depperman E.C.,
kin V.I. // Dokl. Chem. 2013. Vol. 448. N 1. P. 23. doi
Kampf J.W. // J. Am. Chem. Soc. 2003. Vol. 125. N 6.
10.1134/S0012500813010072
P. 1607. doi 10.1021/ja020715x
34.
Gapurenko O.A., Starikov A.G., Minyaev R.M., Min-
20.
Kirk M.L., Shultz D.A. // Coord. Chem. Rev. 2013.
kin V.I. // J. Comput. Chem. 2015. Vol. 36. N 29.
Vol. 257. N 1. P. 218. doi 10.1016/j.ccr.2012.07.007
P. 2193. doi 10.1002/jcc.24199
21.
Tichnell C.R., Shultz D.A., Popescu C.V., Sokirniy I.,
35.
Itkis M.E., Chi X., Cordes A.W., Haddon R.C. //
Boyle P.D. // Inorg. Chem. 2015. Vol. 54. N 9. P. 4466.
Science. 2002. Vol. 296. N 5572. P. 1443. doi 10.1126/
doi 10.1021/acs.inorgchem.5b00298
science.1071372
22.
Protasenko N.A., Poddel’sky A.I., Bogomyakov A.S.,
36.
Pal S.K., Itkis M.E., Tham F.S., Reed R.W., Oakley R.T.,
Fukin G.K., Cherkasov V.K. // Inorg. Chem. 2015.
Haddon R.C. // Science. 2005. Vol. 309. N 5732. P. 281.
Vol. 54. N 13. P. 6078. doi 10.1021/acs.inorgc-
doi 10.1126/science.1112446
hem.5b00912
37.
Train C., Norel L., Baumgarten M. // Coord. Chem.
23.
Protasenko N.A., Poddel’sky A.I., Bogomyakov A.S.
Rev. 2009. Vol. 253. N 19-20. P. 2342. doi 10.1016/j.
Starikov A.G., Smolyaninov I.V., Berberova N.T.,
ccr.2008.10.004
Fukin G.K., Cherkasov V.K. // Inorg. Chim. Acta. 2019.
38.
Morita Y., Nishida S., Murata T., Moriguchi M.,
Vol. 489. P. 1. doi 10.1016/j.ica.2019.02.002
Ueda A., Satoh M., Arifuku K., Sato K., Takui T. // Nat.
24.
Bubnov M., Cherkasova A., Teplova I., Kopylova E.,
Mater. 2011. Vol. 10. P. 947. doi 10.1038/nmat3142
Fukin G., Samsonov M., Bogomyakov A., Fokin S.,
39.
Nishida S., Kawai J., Moriguchi M., Ohba T., Haneda N.,
Romanenko G., Cherkasov V., Ovcharenko V. // Poly-
Fukui K., Fuyuhiro A., Shiomi D., Sato K., Takui T.,
hedron. 2016. Vol. 119. P. 317. doi 10.1016/j.po-
Nakasuji K., Morita Y. // Chem. Eur. J. 2013. Vol. 19.
ly.2016.09.020
N 36. P. 11904. doi 10.1002/chem.201301783
25.
Zolotukhin A.A., Bubnov M.P., Arapova A.V.,
40.
Baumgarten M. // Phys. Status Solidi (B). 2019.
Fukin G.K., Rumyantcev R.V., Bogomyakov A.S.,
Vol. 256. N 9. P. 1800642. doi 10.1002/pssb.201800642
Knyazev A.V., Cherkasov V.K. // Inorg. Chem. 2017.
41.
Melle-Franco M. // Chem. Commun. 2015. Vol. 51.
Vol. 56. N 24. P. 14751. doi 10.1021/acs.inorgc-
N 25. P. 5387. doi 10.1039/C5CC01276G
hem.7b02597
42.
Sharma V., Som N., Dabhi S.D., Jha P.K. // Chem.
26.
Bubnov M., Teplova I., Kozhanov K., Rumyantcev R.,
Select. 2018. Vol. 3. N 8. P. 2390. doi 10.1002/
Fukin G., Bogomyakov A., Cherkasov V. // Inorg.
slct.201703054
Chim. Acta. 2019. Vol. 486. P. 113. doi 10.1016/j.
43.
Minkin V.I., Starikov A.G., Starikova A.A., Gapuren-
ica.2018.10.024
ko O.A., Minyaev R.M., Boldyrev A.I. // Phys. Chem.
27.
Starikov A.G., Starikova A.A., Minyaev R.M., Minkin V.I.,
Chem. Phys. 2020. Vol. 22. N 3. P. 1288. doi 10.1039/
Boldyrev A.I. // Chem. Phys. Lett. 2020. Vol. 740.
C9CP05922A
P. 137073. doi 10.1016/j.cplett.2019.137073
44.
Baumgarten M., Karabunarliev S. // Chem. Phys. 1999.
28.
Стариков А.Г., Старикова А.А., Минкин В.И. //
Vol. 244. N 1. P. 35. doi 10.1016/S0301-0104(99)00090-
ЖОХ. 2016. Т. 86. № 4. С. 672; Starikov A.G., Stariko-
7
va A.A., Minkin V.I. // Russ. J. Gen. Chem. 2016.
45.
Старикова А.А., Миняев Р.М., Минкин В.И. // Изв.
Vol. 86. N 4. P. 859. doi 10.1134/S1070363216040174
АН. Сер. хим. 2014. № 4. С. 812; Starikova A.A.,
29.
Стариков А.Г., Старикова А.А., Минкин В.И. //
Minyaev R.M., Minkin V.I. // Russ. Chem. Bull. 2014.
ЖОХ. 2017. Т. 87. № 1. C. 104; Starikov A.G., Stariko-
Vol. 63. N 4. P. 812. doi 10.1007/s11172-014-0514-x
va A.A., V.I. Minkin, // Russ. J. Gen. Chem. 2017.
46.
Starikova A.A., Starikov A.G., Minkin V. I. // Comput.
Vol. 87. N 1. P. 98. doi 10.1134/S1070363217010169
Theor. Chem. 2016. Vol. 1076. P. 74. doi 10.1016/j.
30.
Старикова А.А., Минкин В.И. // Усп. хим. 2018.
comptc.2015.12.012
Т. 87. №. 11. С. 1049; Starikova A.A., Minkin V.I. //
47.
Sasamori T., Tokitoh N. In: Encyclopedia of Inorganic
Russ. Chem. Rev. 2018. Vol. 87. N 11. Р. 1049. doi
Chemistry / Ed. R.A. Scott. New York: John Wiley &
10.1070/RCR4837
Sons, Ltd, 2006. P. 1. doi 10.1002/0470862106.ia301
31.
Ovchinnikov A.A. // Theor. Chem. Acc. 1978. Vol. 47.
48.
Frisch M.J., Trucks G.W., Schlegel H.B., Scuseria G.E.,
P. 297. doi 10.1007/BF00549259
Robb M.A., Cheeseman J.R., Scalmani G., Barone V.,
32.
Stable Radicals: Fundamental and Applied Aspects of
Petersson G.A., Nakatsuji H., Li X., Caricato M.,
Odd-electron Compounds / Ed. R. Hicks. Wiley: Chich-
Marenich A.V., Bloino J., Janesko B.G., Gomperts R.,
ester, 2011, 588 p.
Mennucci B., Hratchian H.P., Ortiz J.V., Izmaylov A.F.,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
1920
ЧЕГЕРЕВ и др.
Sonnenberg J.L., Williams-Young D., Ding F., Lippa-
51. Minkin V.I., Starikov A.G., Starikova A.A. // Pure Appl.
rini F., Egidi F., Goings J., Peng B., Petrone A., Hender-
Chem. 2018. Vol. 90. N 5. P. 811. doi 10.1515/pac-
son T., Ranasinghe D., Zakrzewski V.G., Gao J., Rega N.,
2017-0803
Zheng G., Liang W., Hada M., Ehara M., Toyota K.,
52. Piskunov A.V., Pashanova K.I., Bogomyakov A.S.,
Fukuda R., Hasegawa J., Ishida M., Nakajima T., Hon-
Smolyaninov I.V., Starikov A.G., Fukin G.K. // Dalton
da Y., Kitao O., Nakai H., Vreven T., Throssell K., Mont-
Trans. 2018. Vol. 47. N 42. P. 15049. doi 10.1039/C8D-
gomery J.A., Jr., Peralta J.E., Ogliaro F., Bearpark M.J.,
T02733A
Heyd J.J., Brothers E.N., Kudin K.N., Staroverov V.N.,
53. Ershova I.V., Smolyaninov I.V., Bogomyakov A.S., Fe-
Keith T.A., Kobayashi R., Normand J., Raghavachari
din M.V., Starikov A.G., Cherkasov A.V., Fukin G.K.,
K., Rendell A.P., Burant J.C., Iyengar S.S., Tomasi J.,
Piskunov A.V. // Dalton Trans. 2019. Vol. 48. N 28.
Cossi M., Millam J.M., Klene M., Adamo C., Cammi R.,
P. 10723. doi 10.1039/C9DT01424A
Ochterski J.W., Martin R.L., Morokuma K., Farkas O.,
54. Noodleman L. // J. Chem. Phys. 1981. Vol. 74. P. 5737.
Foresman J.B., Fox D.J. Gaussian 16, Revision A.03,
doi 10.1063/1.440939.
Gaussian, Inc., Wallingford CT, 2016.
55. Shoji M., Koizumi K., Kitagawa Y., Kawakami T.,
49. Sato D., Shiota Y., Juhasz G., Yoshizawa K. // J. Phys.
Yamanaka S., Okumura M., Yamaguchi K. // Chem.
Chem. (A). 2010. Vol. 114. N 49. P. 12928. doi 10.1021/
jp107391x
Phys. Lett. 2006. Vol. 432. N 1. P. 343. doi 10.1016/j.
50. Biswas M.K., Patra S.C., Maity A.N., Ke S.-C., Weyher-
cplett.2006.10.023.
müller T., Ghosh P. // Dalton Trans. 2013. Vol. 42. N 18.
P. 6538. doi 10.1039/C3DT00038A
prog.com.
Electronic Structure and Magnetic Properties of Mixed-Ligand
Cobalt Complexes Containing Organogermanium Triangulenes
M. G. Chegerev, A. A. Starikova*, A. G. Starikov, and V. I. Minkin
Institute of Physical and Organic Chemistry, Southern Federal University, Rostov-on-Don, 344090 Russia
*e-mail: aastarikova@sfedu.ru
Received July 27, 2020; revised July 27, 2020; accepted August 8, 2020
Computational modeling of cobalt(II) diketonate adducts with o-benzoquinones modified with organogermanium
cycles of various sizes was performed with the use of densify functional theory method. Energy characteristics
of the isomers of the investigated compounds were ascertained to be controlled by substituents in terminal dike-
tone ligands. Paramagnetism of all the states of studied molecules has been predicted. The systems, magnetic
properties of which can be switched as a result of intramolecular electron transfer between the cobalt ion and
organic radical, were revealed.
Keywords: cobalt complexes, о-benzoquinone, organogermanium polycyclic compounds, valence tautomerism,
magnetic properties
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020