ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 12, с. 1953-1957
КРАТКИЕ
СООБЩЕНИЯ
УДК 546.492;547.31;547.37;547.442.3
ОСОБЕННОСТИ ВЗАИМОДЕЙСТВИЯ ДИМЕДОНА С
АМИНАМИ В ПРИСУТСТВИИ АЦЕТАТА РТУТИ(II)
© 2020 г. Н. Г. Обосяна,*, К. В. Баляна, Р. С. Нерсисяна, Л. М. Галечяна,
A. Б. Саргсяна, Р. А. Тамазянb, А. Г. Айвазянb
a Институт органической химии Научно-технологического центра органической и фармацевтической химии
Национальной академии наук Армении, пр. Азатутян 26, Ереван, 0014 Армения
b Центр исследования строения молекул Национальной академии наук Армении, Ереван, 0014 Армения
*е-mail: ninahobosyan@mail.ru
Поступило в Редакцию 11 августа 2020 г.
После доработки 11 августа 2020 г.
Принято к печати 24 августа 2020 г.
Исследована региохимия взаимодействия N-замещенных пропаргиламинов с димедоном в присутствии
ацетата ртути(II). Получены ксантеновое и диеновое производные, а также симметричные аминопропи-
ниды ртути, для одного из которых приведены кристаллографические параметры.
Ключевые слова: димедон, ксантендион, аминоацетиленид ртути, ацетат ртути(II)
DOI: 10.31857/S0044460X20120197
Сопряженное присоединение димедона к ал-
ляют антивирусную [3], противовосполительную
кил- и фенилацетиленам и к пропаргилацетату в
[4, 5] и противобактерицидную активность [6]. Из
присутствии ацетата ртути(II) сопровождается
описанных в литературе способов получения ксан-
внутримолекулярной циклизацией образующихся
теновых аналогов отметим метод, основанный на
на промежуточной стадии ненасыщенных дикар-
взаимодействии 1,3-оксазинанов и оксазолидинов
бонильных соединений в производные фурана
с расплавленными пиранами [7], а также односта-
и тетрагидробензофурана [1]. Нами расширены
дийный синтез на основе димедона и карбониль-
пределы применимости вышеуказанной реакции
ных соединений, инициируемый наночастицами
меркурирования-демеркурирования путем ис-
гетерогенного катализатора [8]. Предложенный
пользования в качестве реагентов азотсодержащих
нами способ отличается от упомянутых путей
соединений с терминальной ацетиленовой группи-
синтеза
3,3,6,6,9-пентаметил-3,4,5,6,7,9-гексаги-
ровкой.
дро-1Н-ксантен-1,8(2Н)-диона простотой экспери-
При использовании в качестве пропаргилпроиз-
мента. В условиях демеркурирования образуется
также бис[3-(диэтиламино)проп-1-ин-1-ил]ртуть 4.
водных N,N-диэтилпроп-2-ин-1-амина 1 и 4-(проп-
2-ин-1-ил)морфолина 5 региохимия их реакций с
В пользу образования симметричной структу-
димедоном отличается от приведенной в литерату-
ры 4 и отсутствия взаимодействия между атома-
ре [2]. Взаимодействие натриевой соли димедона
ми азота и ртути в молекуле соединения 4 свиде-
2 с N,N-диэтилпроп-2-ин-1-амином 1 в метано-
тельствуют снятые в хлороформе электронные
ле или в ДМСО в присутствии ацетата ртути(II)
спектры, в которых не наблюдается характерных
с последующей обработкой реакционной смеси
максимумов поглощения. Структура соединения 4
соляной кислотой приводит к
3,3,6,6,9-пента-
подтверждена данными ЯМР 1H, 13C и ИК спек-
метил-3,4,5,6,7,9-гексагидро-1Н-ксантен-1,8-(2Н)-
троскопии. Кристаллографические параметры со-
диону 3 (схема 1). Производные ксантена прояв-
единения 4 депонированы в Кембриджском центре
1953
1954
ОБОСЯН и др.
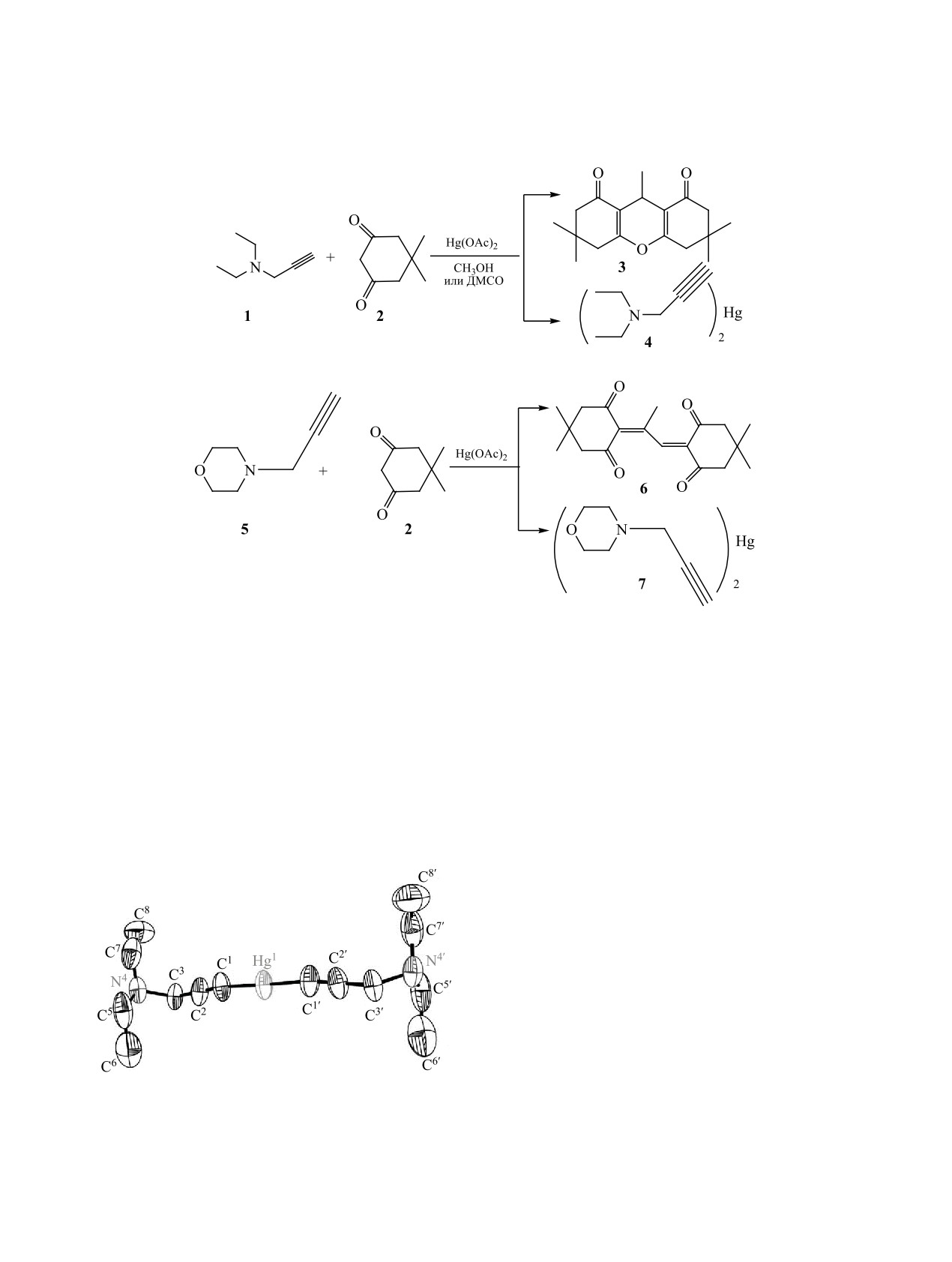
Схема 1.
Схема 2.
кристаллографических данных (номер депозита
гексан-1,3-дион) 6 и бис[3-(морфолин-4-ил)проп-
CCDC 996070). Основные кристаллографические
1-ин-1-ил]ртуть 7 (схема 2). Присутствие диеново-
и экспериментальные данные рентгеноструктур-
го фрагмента подтверждается данными ЯМР 1Н: в
ного анализа приведены в таблице. Структура
спектрах присутствует сигнал винильного протона
молекулы бис[3-(диэтиламино)проп-1-ин-1-ил]-
при 4.29 м. д.
ртути 4 представлена на рисунке. Эллипсоиды
Соединение 7 образуется, как и соединение 4,
анизотропных тепловых колебаний изображены с
в реакции с пропаргилдиэтиламином 1 в условиях
50%-ной вероятностью.
восстановления соляной кислотой (схема 2).
При использовании в качестве реаген-
В спектрах ЯМР 13C соединения 7 химиче-
та
4-(проп-2-ин-1-ил)морфолина
5 получены
ский сдвиг связанных с ртутью атомов Сsp равен
2,2′-(пропан-1,2-диилиден)бис(5,5-диметилцикло-
115.982 м. д. По обе стороны от вышеуказанного
сигнала присутствуют расщепленные сигналы с
δС 99 и 133 м. д. (JCHg = 2540.0 Гц), обусловлен-
ные спин-спиновым взаимодействием ядер ртути
и атомов Сsp. Наличие фрагмента ≡C-Hg в полу-
ченном симметричном алкининиде ртути 7 под-
тверждается характерным поглощением в ИК об-
ласти при 440, 520 см-1.
Таким образом, при взаимодействии произво-
дных пропаргиламина с димедоном в присутствии
ацетата ртути(II) с последующим восстановлени-
ем соляной кислотой получены ксантеновые и ди-
Общий вид молекулы бис[3-(диэтиламино)проп-1-ин-
1-ил]ртути 4 в кристалле с произвольной нумерацией
еновые производные димедона, а также аминоал-
атомов.
киниды ртути.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
ОСОБЕННОСТИ ВЗАИМОДЕЙСТВИЯ ДИМЕДОНА
1955
Основные кристаллографические характеристики и параметры уточнения структуры бис[3-(диэтиламино)проп-1-
ин-1-ил]ртути 4
Параметр
Значение
Формула
C14H24HgN2
М
420.94
Сингония
Oрторомбическая
Пространственная группа
Pbcn
a, Å
13.298(3)
b, Å
12.380(3)
c, Å
9.756(2)
V, Å3
1606.1(6)
Z
4
dвыч, г/см3
1.741
μ(MoKα), мм-1
9.567
F(000)
808
Размер кристалла, мм
0.25×0.32×0.40
Т, K
293
λ, Å
0.71073
θmin, θmax, град
2.2, 27.0
Область сканирования
-16 ≤ h ≤0, 0 ≤ k ≤ -15, -12 ≤ l ≤ 12
Число измеренных отражений
3312
Число наблюдаемых отражений [I > 2.0σ(I)]
976
Взаимодействие
N,N-диэтилпроп-2-ин-1-
СH2), 50.1 (2С, CH2), 115.7 (2С), 161.5 (2С), 194.8
амина 1 с димедоном. К 16 г (0.05 моль) ацетата
(2C, CO).
ртути(II) прибавляли 15 мл ДМСО (или метанола) и
Водный слой после экстракции эфиром подще-
5.6 г (0.05 моль) соединения 1. Отдельно получали
лачивали раствором карбоната натрия, органиче-
натриевую соль 5,5-диметилциклогексан-1,3-дио-
ские вещества экстрагировали эфиром (3 × 30 мл).
на 2 в метаноле из 1.2 г (0.05 моль) натрия и 7 г
Эфирные вытяжки сушили сульфатом магния. По-
(0.05 моль) димедона. К полученной соли прибав-
сле удаления растворителя остаток кристаллизо-
ляли приготовленный комплекс ацетата ртути(II)
вали из CCl4. Выход бис[3-(диэтиламино)проп-1-
и соединения 1, полученную смесь перемешивали
ин-1-ил]ртути (4) 4.23 г (20%). ИК спектр, см-1:
3 ч при 25°С. К реакционной смеси прибавляли
2140, 2170, 440, 520. Спектр ЯМР 1Н, δ, м. д. (J,
30 мл 15%-ной соляной кислоты, перемешивали
Гц): 1.02 т (12Н, СН3, J = 6.7), 2.48 к (8Н, СН2),
5 ч при 25°С, затем фильтровали, и отгоняли мета-
3.28 с (4Н, СН2). Спектр ЯМР 13С, δС, м. д.: 12.2
нол. Нейтральные органические вещества экстра-
(CH3), 49.4 (CH2N), 45.3 (NCH2C≡C), 95.5 (Hg-
гировали диэтиловым эфиром (3 × 30 мл). Эфир-
C≡C),115.7 (Hg-C≡C).
ные вытяжки сушили сульфатом магния. После
Взаимодействие
4-(проп-2-ин-1-ил)мор-
удаления растворителя остаток кристаллизовали
фолина 5 с натриевой солью димедона. К 16 г
из CCl4. Выход пентаметил-3,4,5,6,7,9-гексаги-
дро-1H-ксантен-1,8(2H)-диона (3) 5.148 г (36%).
(0.05 моль) ацетата ртути(II) прибавляли 15 мл ме-
Спектральные данные идентичны приведенным
танола и 6.25 г (0.05 моль) 4-(проп-2-ин-1-ил)мор-
ранее [9]. Спектр ЯМР 1Н, δ, м. д. (J, Гц): 1.00
фолина 5. Отдельно получали раствор натриевой
д (3Н, СН3, J = 6.5), 1.09 с (6Н, СН3), 1.11 с (6Н,
соли димедона в метаноле из 1.2 г (0.05 моль) на-
СН3), 2.19 д (2Н, СН2, J = 16.1), 2.22 д (2Н, СН2,
трия и 7 г (0.05 моль) димедона, к которому прибав-
J = 16.1), 2.33 д (2Н, СН2, J =17.5), 2.39 д. д (2Н,
ляли приготовленный комплекс ацетата ртути(II) и
СН2, J1 = 17.5, J2 = 1.2), 3.41уш. к (1Н, СН, J = 6.5).
соединения 5. Полученную смесь перемешивали
Спектр ЯМР 13С, δС, м. д.: 20.1 (СН), 21.1 (СН3),
3 ч при 25°С, затем прибавляли 20 мл 15%-ной со-
26.6 (2C, СН3), 28.7 (2C, СН3), 31.4 (2С), 40.0(2C,
ляной кислоты и перемешивали еще 5 ч при 25°С.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
1956
ОБОСЯН и др.
После фильтрования отгоняли метанол, остаток
0.20260) [11]. Структуры расшифрованы прямым
обрабатывали эфиром (3 × 30 мл). Эфирные вы-
методом. Координаты атомов водорода определе-
тяжки сушили сульфатом магния. После удаления
ны по геометрическим расчетам и уточнены по
растворителя остаток кристаллизовали из CCl4.
модели наездника. Структура уточнена полнома-
Получили 6.6 г (41.8%) 2,2′-(пропан-1,2-диили-
тричным МНК в анизотропном приближении для
ден)бис(5,5-диметилциклогексан-1,3-диона) (6).
неводородных атомов и в изотропном - для атомов
Спектр ЯМР 1Н, δ, м. д. (J, Гц): 1.06 с (6Н, СН3),
водорода.
1.12 с (6Н, СН3 ), 2.20 д (4Н, СН2, J = 16.0), 2.42 с
КОНФЛИКТ ИНТЕРЕСОВ
(3Н, СН3), 2.46 д (4Н, СН2, J = 16.0) 4.29 с (1Н, =СН).
Авторы заявляют об отсутствии конфликта
Водный слой после экстракции эфиром подще-
интересов.
лачивали раствором карбоната натрия, органиче-
ские вещества экстрагировали эфиром (3 × 30 мл).
СПИСОК ЛИТЕРАТУРЫ
Эфирные вытяжки сушили сульфатом магния. По-
1.
Баданян Ш.О., Чобанян Ж.А., Тиракян М.Р., Да-
сле удаления растворителя остаток кристаллизо-
ниелян А.О. // ХГС. 1998. Т. 34. № 7. С. 904; Bada-
вали из CCl4. Получили 5.2 г (23.2%) бис[3-(мор-
nyan Sh.O., Chobanyan Zh.A., Tirakyan M.R., Danie-
фолин-4-ил)проп-1-ин-1-ил]ртути
(7). Спектр
lyan A.O. // Chem. Heterocycl. Compd. 1998. Vol. 34.
ЯМР 1Н, δ, м. д. (J, Гц): 2.50 м (8Н, СН2N), 3.22 с
N 7. P. 781. doi 10.1007/BF02251682
(4Н, СН2), 3.60 т (8Н, СН2О, J = 6.7). Спектр ЯМР
2.
El Ashry E.S.H., Awad L.F., El Kilany Y., Ibrahim E.I. //
13С, δС, м. д. (J, Гц): 47.848 (CH2N), 51.29 (α-CH2),
Adv. Heterocycl. Chem. 2009. Vol. 98. P. 1. doi 10.1016/
65.66 (OCH2), 99.901 (C≡), 115.982 (≡C), 133 (≡C-
S0065-2725(09)09801-8
Hg, JCHg = 2540.0).
3.
Knight D.W., Little P.B. // J. Chem. Soc. Perkin Trans. 1.
Спектры ЯМР 1Н и 13С регистрировали на
2001. N 14. P. 1771. doi 10.1039/B103834F
спектрометре Varian Mercury-300 VX с частотами
4.
Vazquez R., de la Fuente M.C., Castedo L., Domnguez D. //
300.077 и 75.462 МГц соответственно. Химиче-
Synlett. 1994. N 6. P. 433. doi 10.1055/s-1994-22878
ские сдвиги приведены для раствора ДМСО-d6-
5.
Ishibashi H., Takagaki K., Imada N., Ikeda M. // Synlett.
CCl4 (1:3) относительно внутреннего стандарта
1994. N 1. P. 49. doi 10.1055/s-1994-22734
(ТМС) при 303 K. Отнесение сигналов сделано на
6.
Jha A., Beal J. // Tetrahedron Lett. 2004. Vol. 45.
основании данных 2D спектров DEPT и HMQC.
P. 8999. doi 10.1016/j.tetlet.2004.10.046
ИК спектры записаны на приборе и IR-75 в тонком
7.
Singh K., Singh J., Singh H. // Tetrahedron. 1996. Vol.
слое. За ходом реакции следили с помощью ТСХ
52. P. 14273. doi 10.1016/0040-4020(96)00879-4
на пластинах Silufol UV-254, проявители - KMnO4
8.
Khalafi-Nezhad A., Panahi F., Mohammadi S., Foroug-
и пары иода.
hi H.O. // J. Iran. Chem. Soc. 2012. Vol. 10. P. 189. doi
Дифракционные измерения кристаллов про-
10.1007/s13738-012-0140-1
ведены при комнатной температуре на автодиф-
9.
Castillo A.M., Patiny L., Wist J. // J. Magn. Reson. 2011.
рактометре Enraf-Nonius CAD-4
[графитовый
Vol. 209. P. 123. doi 10.1016/j.jmr.2010.12.008
монохроматор, λ(МоKα) = 0.71073 Å, θ/2θ-сканиро-
10.
Sheldrick G.M. // Acta Crysttallogr. (A). 2007. Vol. 64.
вание]. Все расчеты проводили с использованием
P. 112. doi 10.1107/S0108767307043930
комплекса программ SHELX TL [10]. Учет погло-
11.
North A.C.T., Phillips D.C., Mathews F.S. // Acta
щения сделан по экспериментальным кривым ази-
Crystallogr. (A). 1968. Vol. 24. P. 351. doi 10.1107/
мутального сканирования (Tmin = 0.03495, Tmax =
S0567739468000707
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020
ОСОБЕННОСТИ ВЗАИМОДЕЙСТВИЯ ДИМЕДОНА
1957
Features of the Reaction of Dimedone with Some Amines
in the Presence of Mercury(II) Acetate
N. G. Hobosyana,*, K. V. Balyana, H. S. Nersisyana, L. M. Galechyana, A. B. Sargsyana,
R. A. Tamazyanb, and A. G. Ayvazyanb
a Institute of Organic Chemistry, Scientific-Technological Center of Organic and Pharmaceutical Chemistry,
National Academy of Sciences of Armenia, Yerevan, 0014 Armenia
b Center for Molecular Structure Research, National Academy of Sciences of Armenia, Yerevan, 0014 Armenia
*e-mail: ninahobosyan@mail.ru
Received August 11, 2020; revised August 11, 2020; accepted August 24, 2020
Regiochemistry of the reaction of N-substituted propargylamines with dimedone in the presence of mercury(II)
acetate was studied. Xanthene and diene derivatives, as well as symmetric mercury aminopropinides, were
obtained, for one of which the crystallographic parameters are given.
Keywords: dimedone, xanthenedione, mercury aminoacetylenide, mercury(II) acetate
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 12 2020