ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 2, с. 315-319
УДК 546.05;546.06
СИНТЕЗ НАНОЧАСТИЦ MnO2,
СТАБИЛИЗИРОВАННЫХ МЕТИОНИНОМ
© 2020 г. А. В. Блинов, А. А. Кравцов, С. О. Крандиевский, В. П. Тимченко,
А. А. Гвозденко, А. А. Блинова*
Северо-Кавказский федеральный университет, ул. Пушкина 1, Ставрополь, 355009 Россия
*e-mail: blinov.a@mail.ru
Поступило в Редакцию 19 июля 2019 г.
После доработки 19 июля 2019 г.
Принято к печати 30 июля 2019 г.
Предложен способ синтеза золь-гель методом наночастиц диоксида марганца, стабилизированных
метионином. Проведены исследования оптических свойств золей MnO2, морфологии, элементного и
фазового состава. Выполнен квантово-химический расчет и построены модели образования химиче-
ской связи между молекулой метионина и фрагментом элементарной ячейки диоксида марганца. По
результатам компьютерного моделирования установлен наиболее вероятный механизм стабилизации
наночастиц MnO2.
Ключевые слова: наночастицы, диоксид марганца, метионин
DOI: 10.31857/S0044460X20020195
Наночастицы диоксида марганца вызывают зна-
щий фазовую и морфологическую однородность
чительный интерес исследователей как с фунда-
продукта [9].
ментальной, так и с прикладной точек зрения бла-
Другим способом получения наноразмерных
годаря уникальным каталитическим [1] и адсорб-
частиц оксида марганца является электрохимиче-
ционным [2] свойствам. Наноразмерный MnO2 яв-
ский способ [10], преимущество которого состоит
ляется устойчивым соединением марганца и имеет
в возможности управления скоростью процесса
перспективы широкого применения в различных
путем изменения величины тока или приложен-
областях науки и техники, в частности в произ-
ного напряжения, что дает возможность задавать
водстве биосенсоров [3] и синтезе нитевидных
размеры получаемых наночастиц и их количество
кристаллов [4].
[11].
Анализ литературных данных выявил различ-
Синтез наночастиц MnO2, стабилизированных
ные способы получения наноразмерного диоксида
метионином проведен с использованием золь-гель
марганца. Один из методов основан на гидротер-
метода
[12-13]. Несомненным преимуществом
мально-микроволновой обработке раствора пер-
золь-гель метода является его простота и высокая
манганата калия и нитрита натрия в присутствии
воспроизводимость в лабораторных условиях для
серной кислоты [8]. Недостатками гидротермаль-
получения наночастиц различных веществ [5, 6].
но-микроволновой обработки являются необходи-
Выбор метионина при синтезе наночастиц диок-
мость использования дополнительного оборудова-
сида марганца в данной работе обусловлен воз-
ния - автоклава, что усложняет процесс. К досто-
инствам гидротермально-микроволновой обработ-
можностью использования данного вещества од-
ки относят высокую скорость протекания реакции,
новременно в качестве восстановителя в реакции
возможность направленного изменения фазового
химического восстановления MnO2 из MnO4- и в
состава продуктов синтеза, равномерный нагрев
качестве стабилизатора полученных наноразмер-
всего объема реакционной среды, обеспечиваю-
ных частиц MnO2 (схема 1).
315
316
БЛИНОВ и др.
Схема 1.
O
O
CH3 S CH2 CH2 CH C
+ KMnO4
MnO2 + H2O + CH3 S CH2 CH2 CH C
OH
OK
NH2
O
NH
2
В рамках данной работы стояли задачи син-
молекуле метионина, и кислородом в подрешетке
теза наночастиц MnO2, стабилизированных ме-
неметалла элементарной ячейки диоксида марган-
тионином, а также исследования их оптических
ца, (в) взаимодействием кислорода карбоксильной
свойств, морфологии, элементного и фазового со-
группы метионина с атомом марганца во фрагмен-
става. Оптические свойства золей диоксида мар-
те элементарной ячейки диоксида марганца. Нами
ганца исследовали методом спектрофотометрии
были построены модели для каждого из возмож-
(рис. 1). Анализ спектров поглощения золей по-
ных механизмов взаимодействия молекул метио-
казал, что максимум интенсивности поглощения,
нина при стабилизации наночастиц MnO2 (рис. 2)
при соотношении KMnO4:метионин = 1:1 лежит в
и проведен квантово-химический расчет значений
области 350 нм. С увеличением концентрации ме-
полной энергии моделей (см. таблицу). В резуль-
тионина интенсивность поглощения смещается в
тате моделирования и анализа полученных данных
область 340-320 нм. Также присутствуют полосы
установлено, что механизм стабилизации наноча-
поглощения в области 500-580 нм, соответствую-
стиц диоксида марганца путем взаимодействия
щие электронным переходам в перманганат-ионе
атома серы, входящего в структуру метионина с
MnO4- [7]. При изменении мольного соотношения
атомами кислорода в подрешетке неметалла эле-
метионина от 1:5 до 1:1 интенсивность поглоще-
ментарной ячейки диоксида марганца, является
ния в этой области уменьшается и при соотноше-
наиболее вероятным, так как обеспечивает мини-
нии KMnO4:метионин = 1:1 полосы отсутствуют,
мальное значение полной энергии модели.
что соответствует восстановлению MnO2 из MnO4-.
Размеры частиц в образцах золей MnO2 опреде-
Предположим, что стабилизация наночастиц
ляли методом фотонно-корреляционной спектро-
диоксида марганца может происходить по трем
скопии. Было установлено присутствие в образцах
механизмам: (а) взаимодействием атома серы, вхо-
наночастиц MnO2 со средним гидродинамическим
дящего в состав метионина, с атомами кислорода
радиусом 25-30 нм.
в подрешетке неметалла элементарной ячейки ди-
Порошки исследовали методами растровой
оксида марганца, (б) взаимодействием между азо-
электронной микроскопии, энергодисперсионного
том аминогруппы, находящимся в α-положении в
анализа, рентгенофазового анализа, синхронного
термического анализа. Для изучения морфологии
образцов MnO2 использовали растровую элек-
тронную микроскопию. Анализ микрофотографий
показал, что в синтезированных образцах присут-
ствуют крупные агрегаты наночастиц диоксида
марганца различной формы и размеров. При уве-
личении разрешения видно, что агрегаты состо-
ят из наночастиц сферической формы диаметром
41-72 нм.
При помощи рентгенофазового анализа иден-
тифицировали различные фазы в образцах MnO2.
Ȝ ɧɦ
Анализ дифрактограммы показал присутствие
Рис. 1. Cпектры поглощения золей диоксида марганца
слабоинтенсивных уширенных пиков, свиде-
с мольным соотношением KMnO4:метионин = 1:1 (1),
тельствующих о присутствии аморфизирован-
1:2 (2), 1:3 (3), 1:4 (4), 1:5 (5).
ной фазы MnO2, с тетрагональной кристалли-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 2 2020
СИНТЕЗ НАНОЧАСТИЦ MnO
2
, СТАБИЛИЗИРОВАННЫХ МЕТИОНИНОМ
317
D
ɛ
ɜ
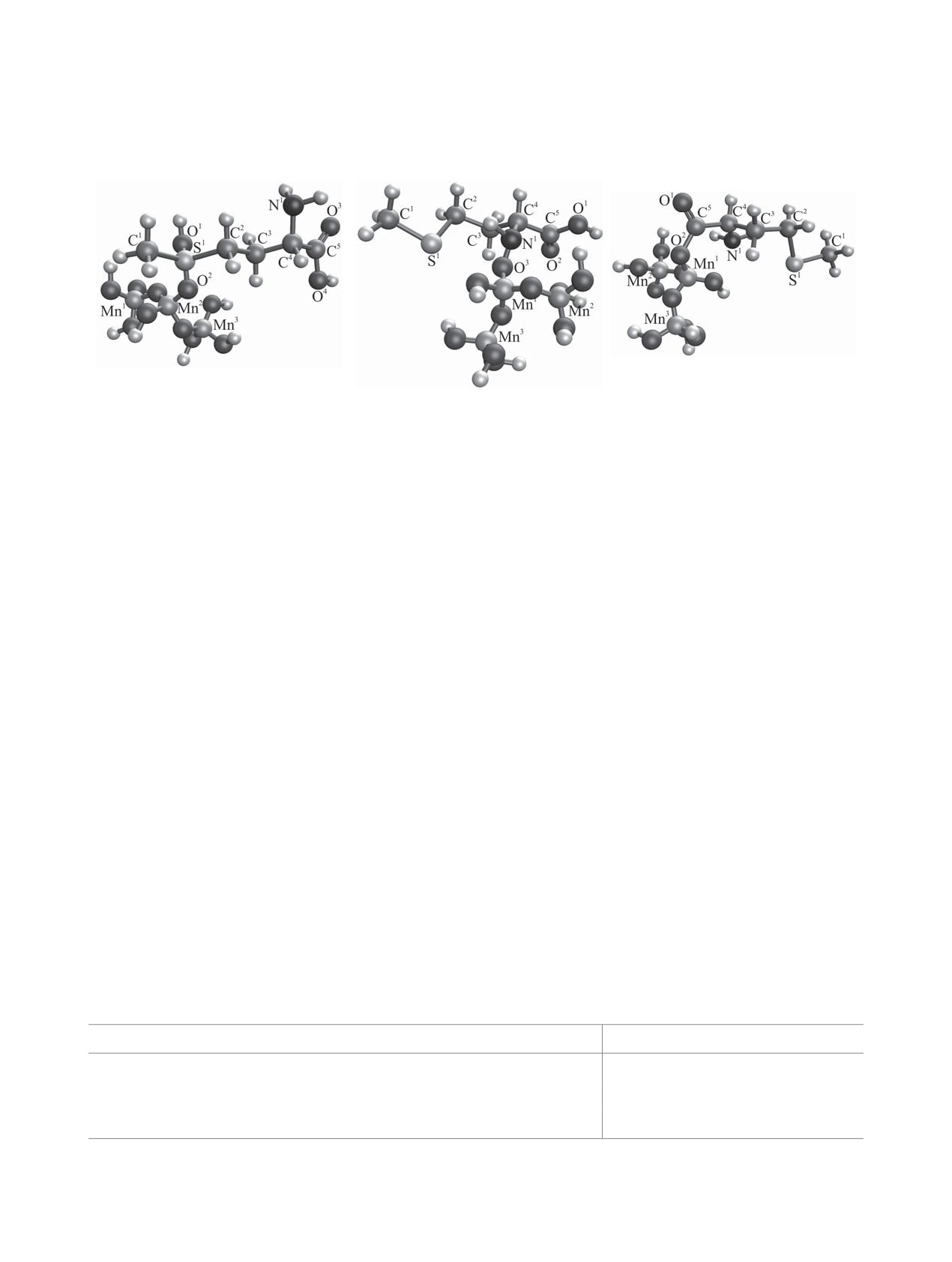
Рис. 2. Модели образования химической связи между метионином и MnO2: (а) стабилизация наночастиц диоксида марганца
путем взаимодействия серы с кислородом; (б) стабилизация наночастиц диоксида марганца путем взаимодействия между
азотом аминогруппы и кислородом; (в) стабилизация наночастиц диоксида марганца путем взаимодействия кислорода
карбоксильной группы с марганцем.
ческой решеткой, имеющей пространственную
с дальнейшим окислением и разложением мети-
группу I4/m (параметры элементарной ячейки:
онина, сопровождающимся выраженным экзотер-
a = 9.8150 Å, b = 9.8150 Å, c = 2.8470 Å). Также
мическим пиком. При достижении температуры
установлено присутствие второй фазы Mn3O4,
800-900°С происходит переход Mn2О3 в Mn3О4 с
с тетрагональной кристаллической решеткой,
выделением О2, сопровождающийся поглощением
имеющей пространственную группу I41/amd
энергии и потерей массы около 4%.
(параметры элементарной ячейки: a = 5.7574 Å,
По данным масс-спектрометрии не наблюдает-
b = 5.7574 Å, c = 9.4239 Å).
ся выделения оксида серы, поскольку температура
Синхронный термический анализ осуществля-
разложения сульфатов выше 1100°С.
ли методами дифференциальной сканирующей ка-
Таким образом, синтезированы наночастицы
лориметрии и термогравиметрии совмещенными с
MnO2 золь-гель методом путем смешивания во-
масс-спектрометрией. В температурном диапазоне
дных растворов перманганата калия и метионина.
110-300°С наблюдается выделение углекислого
Установлено образование агрегатов наночастиц
газа (по данным масс-спектрометрии), связанное
сферической формы со средним гидродинамиче-
с деструкцией метионина, сопровождающейся
ским радиусом 25-30 нм и диаметром 41-72 нм.
выделением теплоты и потерей массы образца
Предположены три возможных механизма стаби-
(около 23%). В этом же температурном диапазоне
лизации наночастиц диоксида марганца и проведе-
происходит значительная потеря связанной воды.
При дальнейшем нагревании образца в присут-
но молекулярное моделирование, по результатам
ствии кислорода выше 300°С Mn2О3 окисляется
которого установлено, что механизм стабилизации
до MnО2. При температуре 500-600°С происхо-
наночастиц диоксида марганца путем взаимодей-
дит разложение MnО2 до Mn2О3 с выделением
ствия атома серы, входящего в структуру метиони-
кислорода. Также наблюдается выделение азота
на, с атомами кислорода в подрешетке неметалла
(NO, по данным масс-спектрометрии), связанное
элементарной ячейки диоксида марганца является
Значения полных энергий моделей образования химической связи между метионином и MnO2
Способ стабилизации наночастиц диоксида марганца метионином
Полная энергия модели, ккал/моль
Взаимодействие между серой с кислородом
-5064
Взаимодействие между азотом аминогруппы и кислородом
-4987
Взаимодействие между кислородом карбоксильной группы и марганцем
-4913
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 2 2020
318
БЛИНОВ и др.
наиболее вероятным, так как обеспечивает мини-
ФОНДОВАЯ ПОДДЕРЖКА
мальное значение полной энергии модели.
Исследование выполнено при финансовой
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
поддержке Совета по грантам при Президенте
Российской Федерации (проект СП-1191.2019.4).
Наночастицы MnO2 синтезировали золь-гель
методом, путем химического восстановления
КОНФЛИКТ ИНТЕРЕСОВ
MnO2 из MnO4-. Была подготовлена серия из
Авторы заявляют об отсутствии конфликта
5 образцов с исходным составом: [KMnO4] =
интересов.
0.158 ммоль/л, [Met] = 0.167, 0.334, 0.501, 0.668,
0.835 ммоль/л. К водному раствору перманганата
СПИСОК ЛИТЕРАТУРЫ
калия при температуре 20-25°С при постоянном
1. Иванова Н.Д., Иванов С.В., Болдырев Е.И., Со-
перемешивании добавляли водный раствор метио-
кольский Г.В., Макеева И.С. // ЖПХ. 2002. Т. 75.
нина. После завершения реакции золи подвергали
Вып. 9. С. 1452; Ivanova N.D., Ivanov S.V.,
старению, отделяли надосадочную жидкость, про-
Boldyrev E.I., Sokol’skii G.V., Makeeva I.S. // Russ.
мывали путем многократного центрифугирования
J. Appl. Chem. 2002. Vol. 75. N 9. P 1420. doi
и сушили при 100°С.
10.1023/A:1022216626347
Фазовый состав образцов исследованы методом
2. Гришина А.В., Беляев А.П., Гришин В.В. // Молодой
рентгенофазового анализа на приборе ARL Xtra,
ученый. 2014. № 18. С. 121.
TermoScientific с помощью программного обеспе-
3. Окислы марганца / Под ред. Н.В. Лазарева, Э.Н.
чения Crystallographica Search-Match. Медный ка-
Левиной. М: Изд. медицинской литературы, 1962.
тод (λ = 1.54 Å), диапазон измерения 2θ = 10-90°,
176 с.
частота дискретизации 2θ = 0.01°. Оптические
4. Белова А.И., Иткис Д.М., Семененко Д.А., Гуди-
свойства золей исследованы методом спектро-
лин Е.А., Третьяков Ю.Д. // Альтернативная энерге-
фотометрии с использованием прибора СФ-56 в
тика и экология. 2010. С. 70.
диапазоне 190-1100 нм. Распределение гидроди-
5. Spanhel L., Anderson M.A. // J. Am. Chem. Soc. 1991.
намических радиусов наночастиц по размерам
Vol. 113. P. 2826. doi 10.1021/ja00008a004
исследовано методом фотонно-корреляционной
6. Znaidi L., Soler Illia G.J.A.A., Benyahia S., Sanchez C.,
спектроскопии на приборе Photocor Complex (дли-
Kanaev A.V. // Thin Solid Films. 2003. Vol. 428. P. 257.
на волны лазера 632.8 нм). Микрофотографии
doi 10.1016/S0040-6090(02)01219-1
образцов получены на растровом электронном
7. Воронцов Д.А., Егорова А.Е., Ким Е.Л., Марычев М.О.,
микроскопе TESCAN MIRA-3. Синхронный тер-
Петрова А.А., Портнов В.Н., Сомов Н.В. // Вестн.
мический анализ, проведенный методами диф-
Нижегородск. унив. им. Н.И. Лобачевского. 2010.
ференциальной сканирующей калориметрии и
С. 210.
термогравиметрии, совмещенными с масс-спек-
8. Бойцова О.В., Шекунова Т.О., Баранчиков А.Е. //
трометрией, осуществлен на приборе NETZSCH
ЖНХ. 2015. Т. 60. № 5. С. 612; Boytsova O.V.,
Shekunova T.O., Baranchikov A.E // Russ. J. Inorg.
STA 449 F5 Jupiter. В качестве программного обе-
Chem. 2015. Vol. 60. N 5. P. 612. doi 10.1134/
спечения использован пакет программ NETZSCH
S0036023615050022
Proteous-Thermal Analysis v. 6.1.0. Диапазон темпе-
9. Егорышева А.В., Гайтко О.М., Руднев П.О., Кув-
ратур - 25-1050°С, скорость нагревания образца -
шинова Т.Б., Япрынцев А.Д. // ЖНХ. 2015. Т 60.
30 град/мин. Измерения проводили в потоке возду-
№ 11. С. 1425; Egorysheva A.V., Gaitko O.M., Rud-
ха с расходом 40 мл/мин.
nev P.O., Kuvshinova T.B., Yapryntsev A.D. // Russ. J.
Построение моделей молекулярных структур
Inorg. Chem. 2015. Vol. 60. N 11. P. 1425. doi 10.1134/
диоксид марганца-метионин выполнено в моле-
S0036023615110042
кулярном редакторе IQmol. Квантово-химический
10. Петрова Е.В., Дресвянников А.Ф., Винокуров А.В. //
расчет моделей проведен с использованием про-
ЖФХ. 2013. Т. 87. № 3. С. 494; Petrova E.V., Dres-
граммного обеспечения QChem.
vyannikov A.F., Vinokurov A.V. // Russ. J. Phys.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 2 2020
СИНТЕЗ НАНОЧАСТИЦ MnO
2
, СТАБИЛИЗИРОВАННЫХ МЕТИОНИНОМ
319
Chem. (A). 2013. Vol. 87. N 3. P 494. doi 10.1134/
12. Lazareva S.V., Shikina N.V., Tatarova L.E., Ismagi-
S0036024413030217
lov Z.R. // Eurasian Chem. Tech. J. 2017. N 19. P. 295.
11. Михайлов М.Д. Химические методы получения на-
13. Shaikh R.S., Rakh R.R., Ravangave L.S. // Int. Res. J.
ночастиц и наноматериалов. СПб: Изд. Политехн.
унив., 2012. 259 с.
Sci. Eng. 2016. Vol. 4. N 1. P. 31.
Synthesis of MnO2 Nanoparticles Stabilized by Methionine
A. V. Blinov, A. A. Kravtsov, S. O. Krandievskii, V. P. Timchenko,
A. A. Gvozdenko, and A. A. Blinova*
North Caucasus Federal University, Stavropol, 355009 Russia
*e-mail: blinov.a@mail.ru
Received July 19, 2019; revised July 19, 2019; accepted July 30, 2019
A sol-gel method for the synthesis of manganese dioxide nanoparticles stabilized with methionine is proposed.
The optical properties of MnO2 sols, as well as morphology, elemental and phase composition were studied. A
quantum-chemical calculation was performed and models for the formation of a chemical bond between a me-
thionine molecule and a fragment of a unit cell of manganese dioxide were constructed. According to the results
of computer simulation, the most probable mechanism of stabilization of MnO2 nanoparticles was revealed.
Keywords: nanoparticles, manganese dioxide, methionine
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 2 2020