ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 4, с. 581-590
УДК 541.8.002;544.174.3
ВЛИЯНИЕ ОСОБЕННОСТЕЙ МЕХАНИЗМА
НАЧАЛЬНЫХ СТАДИЙ РАСПАДА ЛИГАНДОВ
НА ИНИЦИИРУЮЩУЮ СПОСОБНОСТЬ
АММИНТЕТРАЗОЛАТОВ КОБАЛЬТА(III)
© 2020 г. М. А. Илюшинa,*, И. В. Шугалейa, А. С. Тверьяновичb, А. В. Смирновa
a Санкт-Петербургский государственный технологический институт (технический университет),
Московский пр. 26, Санкт-Петербург, 190013 Россия
b Санкт-Петербургский государственный университет, Санкт-Петербург, 198504 Россия
*e-mail: explaser1945@yandex.ru
Поступило в Редакцию 1 октября 2019 г.
После доработки 1 октября 2019 г.
Принято к печати 3 октября 2019 г.
Представлены результаты квантово-химических расчетов изолированных молекул перхлоратов пен-
тааммин-(5-циано-2H-тетразолато-N2)кобальта(III), пентааммин-(5-нитротетразолато-N2)кобальта(III),
тетрааммин-цис-бис(5-нитро-2H-тетразолато-N2)кобальта(III), тетрааммин-цис-бис-(1-метил-5-аминоте-
тразоло-N3,N4)кобальта(III) и продуктов их возможной первичной стадии разложения. Определены энер-
гетика и пути протекания таких реакций. Впервые с помощью квантово-химических расчетов показано,
что распад амминатов кобальта может начаться с деструкции тетразольного лиганда и элиминирования
молекулы азота, а не с диссоциации молекулы координированного аммиака из внутренней сферы ком-
плекса кобальта(III). Определены энергии активации и диссоциации этих процессов.
Ключевые слова: квантово-химический расчет, разложение, комплексные амминтетразолаты, иници-
ирующая способность
DOI: 10.31857/S0044460X20040137
Известно, что на первой стадии термического
комплекса и последующее элиминирование мо-
разложения, являющейся общей для всех энерге-
лекулярного аммиака [3, 4]. Например, термиче-
тических материалов, происходит разрыв слабых
ское разложение энергонасыщенного комплекса
связей в молекуле, протекающий с поглощением
[Co(NH3)6](NO3)3 является окислительно-восста-
тепла (стадия фрагментации). Последующие экзо-
новительным процессом и сопровождается элими-
термические процессы, включающие окислитель-
нированием на начальных стадиях распада 1.5 мо-
но-восстановительные реакции, рекомбинацию
лей аммиака на 1 моль исходного комплекса {см.
свободных радикалов и т. д., приводят к образо-
уравнение (1) [3]}.
ванию стабильных конечных продуктов [1]. При
12[Co(NH3)6](NO3)3 → 4Со2O3·СоO + 18NH3
этом легкость возбуждения быстрого разложения
+ 7N2O + 73H2O + 4NH4NO3 + 34N2.
(1)
энергетических материалов, в том числе детона-
Можно предположить, что разложение амми-
ции, в значительной степени зависит от энергии
акатов кобальта(III), содержащих теразолатные
активации и энтальпии начальных стадий разло-
лиганды, начинается с диссоциации молекул ам-
жения [1, 2].
миака из внутренней сферы октаэдра, находящих-
На первой стадии термораспада изученных
ся в транс-положении по отношению к азольным
к настоящему времени амминатов кобальта(III)
лигандам. Далее, вероятно, протекают параллель-
происходит диссоциация из внутренней сферы
но-последовательные процессы изомеризации
581
582
ИЛЮШИН и др.
Минимальный заряд комплексов кобальта 1-4 по цикло-
го материала проводили лучом огня отрезка огне-
триметилентринитроамину
проводного шнура или электровоспламенителем.
Комплекс
Минимальный заряд, г
Ссылка
Например, минимальный заряд перхлора-
1
0.30
[6]
тов
пентааммин-(5-циано-2H-тетразолато-N2)-
2
0.15
[6]
кобальта(III)
1, пентааммин-(5-нитротетразола-
3
0.05
[4]
то-N2)кобальта(III)
2, тетрааммин-цис-бис(5-ни-
4
0.10
[4]
тро-2H-тетразолато-N2)кобальта(III) 3 и тетраам-
мин-цис-бис(1-метил-5-аминотетразоло-N3,N4)ко-
во внутренних сферах комплексов. Эти реакции
бальта(III) 4 по вторичному энергетическому мате-
сопровождаются изменением дентатности тетра-
риалу - циклотриметилентринитроамину умень-
золатных лигандов, окислением лигандов и ча-
шается в ряду 1 < 2 < 4 < 3 (см. таблицу). Чем мень-
стичным восстановлением центрального иона.
ше минимальный заряд, тем выше инициирующая
Исследования показали, что оксид кобальта Co3O4
способность и эффективность комплекса кобальта.
является основным твердым продуктом разложе-
Энергонасыщенные комплексы 1-4 представля-
ния перхлоратных аммиакатов кобальта(III) с тет-
ют собой кристаллические вещества оранжевого
разольными лигандами. В твердых продуктах тер-
цвета плотностью от 1.90 до 2.05 г/см3. Уровень
мораспада этих соединений также найдены следы
чувствительности рассматриваемых комплексов к
CoCl2. Восстановление Co(III) до Со(II) в процес-
механическому воздействию соответствовал уров-
се термолиза амминных комплексов кобальта(III),
ню современных мощных бризантных энергетиче-
очевидно, осуществляется внутрисферным амми-
ских материалов, т. е. они значительно безопаснее
аком.
в обращении по сравнению с классическими ини-
Амминаты кобальта(III) с тетразольными ли-
циирующими энергетическими материалами [1].
гандами являются энергетическими материалами
Поскольку комплексы 1-4 не содержат в составе
и некоторые из них обладают инициирующей спо-
суперэкотоксикантов - атомов свинца и ртути, то
собностью. Если задаться постоянством импуль-
они более экологичны, чем штатные инициирую-
са инициирующей ударной волны, выбрав неко-
щие энергетические материалы (например, азид
торый вторичный (бризантный) энергетических
свинца или гремучая ртуть) [5].
материалов с известными и постоянными пара-
Сокращение минимального заряда в ряду
метрами чувствительности к ударной волне при
комплексов
1-3 не противоречит приведенно-
неизменных условиях нагружения, то критерием
му единому механизму термораспада амминатов
инициирующей способности может стать масса
кобальта(III). Так, введение вместо нитрильной
инициирующего заряда, так как она определяет
группы эксплозофорной NO2-группы в тетразо-
временные характеристики ударной волны и ее
льный лиганд должно было увеличить эффектив-
суммарный импульс фазы сжатия. Минимальную
ность комплекса 2 по сравнению с комплексом
массу инициирующего (первичного) энергети-
1. Действительно, минимальный заряд комплек-
ческого материала, обеспечивающую детонацию
са 2 в два раза меньше, чем у комплекса 1 (см.
в испытываемом бризантном энергетическом
таблицу). Замена молекулы аммиака на 5-нитроте-
материале, называют минимальным иницииру-
разолатный лиганд в комплексе 3 также привела
ющим импульсом или предельным инициирую-
к ожидаемому сокращению участка перехода го-
щим зарядом (минимальным зарядом). Сравнивая
рения в детонацию и уменьшению минимальный
величины предельного (минимального) заряда
заряд по сравнению с комплексом 2 (см. таблицу).
инициирующего энергетического материала по
Повышение инициирующей способности в при-
отношению к какому-нибудь одному вторичному
веденном ряду амминатов кобальта 1-3 сопрово-
энергетическому материалу, можно судить об их
ждалось сокращением времени перехода горения в
относительной инициирующей способности, если
детонацию (75, 12 и 6-8 мкс соответственно), что
испытания проводили в одних и тех же условиях,
также можно связать с накоплением числа экспло-
например в гильзе от капсюля-детонатора КД №8.
зофорных групп у тетразолатных лигандов в ком-
Инициирование заряда первичного энергетическо-
плексах кобальта 1-3 [7].
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
ВЛИЯНИЕ ОСОБЕННОСТЕЙ МЕХАНИЗМА НА
ЧАЛЬНЫХ СТАДИЙ РАСПАДА ЛИГАНДОВ
583
1
2
3
4
Рис. 1. Оптимизированные в базисе 6-31+G(d) структуры молекул 1-4.
В стройную картину влияния NO2-группы на
дией которого является элиминирование молекулы
инициирующую способность комплексов кобальта
аммиака, поскольку в комплексе 4 тетразольные
не вписывается необычно высокая инициирующая
лиганды не имели эксплозофорных заместителей,
способность комплекса 4, который по эффективно-
а введение метильной группы в азольный лиганд
сти оказался на втором месте, лишь незначитель-
практически всегда ранее приводило к снижению
но уступая комплексу 3. Так, минимальный заряд
эффективности металлокомплекса как первичного
комплекса 4 по циклотриметилентринитроамину
энергетического материала, по сравнению с ком-
больше, чем у комплекса 3, но меньше, чем у ком-
плексом, в состав которого входил лиганд - неза-
плекса 2 (см. таблицу). Полученный результат не
мещенный тетразол, не говоря уже о комплексе
может быть объяснен в рамках единого механизма
с лигандом, содержащем эксплозофорную гуппу
разложения амминатов кобальта(III), первой ста-
(5-нитротетразол) [2, 4, 8].
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
584
ИЛЮШИН и др.
ɚ
ɛ
x Å
x Å
Рис. 2. Элиминирование молекулы аммиака (a) и раскрытие тетразольного цикла (б) в молекуле комплекса 1. (а) Растяжение
связи центрального иона с аммиаком Co1-N9; (б) растяжение связи в тетразольном цикле N8-N13.
Мы предположили, что для амминатов кобаль-
молекул и фрагментов, в том числе, полные элек-
та с тетразольными лигандами, имеющими заме-
тронные энергии молекул Ee, поправки на нулевые
стители, могут реализовываться и иные механиз-
энергии E0, энергии атомизации, энергии высшей
мы начальных стадий разложения, отличные от
занятой молекулярной орбитали (ВЗМО) и низ-
процессов элиминирования молекулярного амми-
шей свободной молекулярной орбитали (НСМО)
ака из внутренней сферы комплекса. Квантово-
и энергетические зазоры между ними Eg, распре-
химические расчеты позволили выявить основные
деления электронной плотности на атомах (мaл-
первичные механизмы и энергетику разложения
ликеновских зарядов). Инфракрасные спектры
комплексов 1-4. Квантово-химические расчеты
для основных состояний молекул 1-4, их ионов и
были выполнены с привлечением пакета программ
фрагментов молекул, образующихся при разложе-
Gaussian 09 в приближении теории функционала
нии, также были рассчитаны и сравнены с экспе-
плотности [9] с использованием гибридного функ-
риментальными ИК спектрами кристаллических
ционала B3LYP и спин-поляризационного базис-
образцов. Оптимизированные в базисе 6-31+G(d)
ного набора электронных функций
6-31+G(d).
структуры молекул 1-4 показаны на рис. 1 [10].
Простейший валентно-расщепленный базисный
Вычисления механизмов начальных стадий
набор 3-21G использовали для большого числа
разложения были выполнены для оптимизиро-
предварительных и вспомогательных расчетов.
ванных молекулярных структур 1-4 в основном
Так, набор 3-21G был применен для большого
состоянии, а также в возбужденном триплетном
объема вычислений различных возможных пу-
и заряженном (положительно и отрицательно)
тей первичных стадий разложения: определения
состояниях. Были рассмотрены иные механизмы
энергетических барьеров этих реакций, переход-
начальных стадий распада комплексов 1-4, в том
ных состояний и кривых потенциальной энергии
числе раскрытие тетразольного цикла. Некоторые
для процессов отрыва фрагментов или раскрытия
из полученных результатов рассмотрены ниже. На
цикла. Свойства рассмотренных веществ опреде-
рис. 2-5 показаны кривые изменения потенциаль-
ляли для состояния изолированных молекулярных
ной энергии при последовательном растяжении
комплексов. Проводили расчеты геометрии и элек-
одной из межатомных связей. Результаты для мо-
тронных состояний молекул и образующихся при
лекулярных единиц 1 и 2 показаны на рис. 2, 3. Из
их разложении отдельных фрагментов. Поправки
рис. 2 следует, что для комплекса 1 раскрытие те-
на энергию нулевых колебаний E0 принимали во
тразольного цикла на начальных стадиях разложе-
внимание в расчетах всех стационарных и пере-
ния энергетически невыгодно (рис. 2б). Для этого
ходных состояний. Были определены практиче-
соединения реализуется только классический ме-
ски все молекулярные свойства рассмотренных
ханизм первой стадии распада - элиминирование
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
ВЛИЯНИЕ ОСОБЕННОСТЕЙ МЕХАНИЗМА НА
ЧАЛЬНЫХ СТАДИЙ РАСПАДА ЛИГАНДОВ
585
ɚ
ɛ
x Å
x Å
Рис. 3. Элиминирование молекулы аммиака (a) и раскрытие тетразольного цикла с последующим элиминированием моле-
кулы азота (б) в молекуле комплекса 2. (а) Растяжение связи центрального атома с аммиаком Co1-N20; (б) растяжение связи
в тетразольном цикле N15-N16.
молекулы аммиака из внутренней сферы комплек-
состояний (рис. 4ж), находящегося в транс-поло-
са (рис. 2a).
жении по отношению к 5-нитротетразолатному
Для комплекса 2 реализуется как классический
заместителю. Причем в молекуле комплекса 3 в
основном состоянии диссоциация NH3 сопрово-
механизм первой стадии распада - элиминирова-
ние молекулы аммиака из внутренней сферы ком-
ждается одновременной перестройкой оставше-
плекса (рис. 3a), так и разрыв связи в тетразольном
гося молекулярного фрагмента, в то время как
кольце с элиминированием молекулы N2 (рис. 3б).
диссоциация молекулы аммиака в цис-положении
Причем в молекуле комплекса 2 диссоциация NH3
к аниону 5-нитротетразола энергетически невы-
сопровождается одновременной перестройкой
годна для данного соединения (рис. 4б). Также
оставшегося молекулярного фрагмента [11, 12].
энергетически невыгодным оказалось отщепле-
Следует отметить, что в комплексе 2 более энер-
ние хлорной кислоты (рис. 4г) и отщепление ни-
гетически выгодно элиминирование молекулы
трогруппы от
5-нитротетразолатного лиганда
аммиака из внутренней сферы координационного
(рис. 4д). Полученные результаты совпали с ре-
соединения. Энергетически невыгодным оказа-
зультатами предварительных квантово-химиче-
лось отщепление от комплекса 2 хлорной кислоты,
ских исследований для комплекса 3 [11, 12]. Для
5-нитротеразолатного лиганда, и нитрогруппы от
комплекса 3 вероятно также раскрытие тетразоль-
5-нитротетразолатного лиганда [11, 12].
ного цикла лиганда (рис. 4в).
Результаты исследования термораспада ком-
Несколько менее вероятен процесс элимини-
плекса
2 полностью подтвердили результаты
рования молекулы аммиака из транс- положе-
квантово-химических расчетов. Так, методом
ния к 5-нитротетразолатному лиганду от катиона
масс-спектрометрии было показано, что термолиз
(рис. 4з), образовавшегося после потери комплек-
соли 2 начинается с диссоциации молекулы амми-
сом 3 перхлорат-аниона (рис. 5a) [10].
ака в диапазоне 150-250°C. Однако выше 200°С
Для комплекса 4 возможно элиминирование
в продуктах термораспада обнаружен HCN, что
молекулы NH3, находящейся в транс-положении
является прямым доказательством предсказанной
к тетразольному лиганду (рис. 6a). Энергетически
деструкции тетразольного кольца в комплексе 2
значительно менее выгодна диссоциация молеку-
[13, 14].
лы NH3, расположенной в цис-положении по от-
Для комплекса 3 возможны несколько путей на-
ношению к тетразольному лиганду (рис. 6б) Еще
чала разложения: элиминирование молекулы ам-
менее энергетически выгодно элиминирование
миака из основного (рис. 4a), возбужденного (три-
молекулы NH3 от катиона комплекса 4 (рис. 6в)
плетного) (рис. 4е), и положительно заряженного
после потери им внешнесферных перхлорат-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
586
ИЛЮШИН и др.
ɚ
ɛ
x Å
x Å
ɜ
ɝ
x Å
x Å
ɞ
ɟ
x Å
x Å
ɠ
ɡ
x Å
x Å
Рис. 4. Возможные пути начальных стадий разложения в молекуле комплекса 3. (a, б) Элиминирование молекулы аммиака
(растяжение связи Co1–N13 и Co1–N14 соответственно); (в) раскрытие тетразольного цикла (растяжение связи N12-N19);
(г) отщепление нитрогруппы (растяжение связи N3-C22); (д) отщепление молекулы хлорной кислоты (растяжение связи
Co1-Cl4); (е, ж) отщепление молекулы аммиака от возбужденного состояния и положительно заряженной молекулы (растя-
жение связи Co1-N13); (з) элиминирование молекулы аммиака от катиона (растяжение связи Co1-N10).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
ВЛИЯНИЕ ОСОБЕННОСТЕЙ МЕХАНИЗМА НА
ЧАЛЬНЫХ СТАДИЙ РАСПАДА ЛИГАНДОВ
587
ɚ
ɛ
Рис. 5. Оптимизированные структуры катионов комплексов 3 (a) и 4 (б) после потери ими перхлорат-анионов.
ионов (рис. 6б). Наличие заместителя у атома азо-
щений на начальной стадии разложения комплекса
та N1 приводит к тому, что раскрытие тетразольно-
4 является маловероятным.
го цикла становится более выгодным у атома азота
Можно отметить, что в первом приближении
N4, не имеющего заместителя (ср. рис. 6г и 6е).
реализуются два основных наблюдаемых механиз-
Процесс начинается с раскрытия тетразольного
ма разложения перхлоратов амминтетразолатовко-
цикла у атома азота N4, затем осуществляется эли-
бальта(III): элиминирование молекулы аммиака и
минирование молекулы N2, что является наиболее
раскрытие тетразольного кольца с последующим
энергетически выгодным для комплекса (рис. 6е).
удалением молекулы азота, которые имеют доста-
Изменение начальной стадии распада ком-
точно близкие энергетические барьеры. Уточнение
плекса 4 и ее повышенная энтальпия за счет об-
этой проблемы требует более сложных методов
разования молекулы азота привели к сокращению
исследования.
участка перехода горения в детонацию соедине-
Таким образом, расчетно-экспериментальными
ния 4 и повышения эффективности как иницииру-
исследованиями было подтверждено предположе-
ющего энергетического материала (см. таблицу).
ние, что на механизм начальных стадий терморас-
Раскрытие тетразольного цикла по атомам азота
пада амминатов кобальта с тетразольными лиган-
N2 или N3 (рис. 6ж, з) оказалось энергетически
дами влияет природа заместителей в тетразольном
значительно менее выгодным, чем по атому азота
лиганде. Впервые расчетами показано, что распад
N4 с последующим элиминированием молекулы
амминатов кобальта может начаться с деструкции
N2 (рис. 6е). Поэтому протекание данных превра-
тетразольного лиганда и элиминирования молеку-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
588
ИЛЮШИН и др.
ɚ
ɛ
x Å
x Å
ɜ
ɝ
x Å
x Å
ɞ
ɟ
ɠ
ɡ
x Å
x Å
x Å
x Å
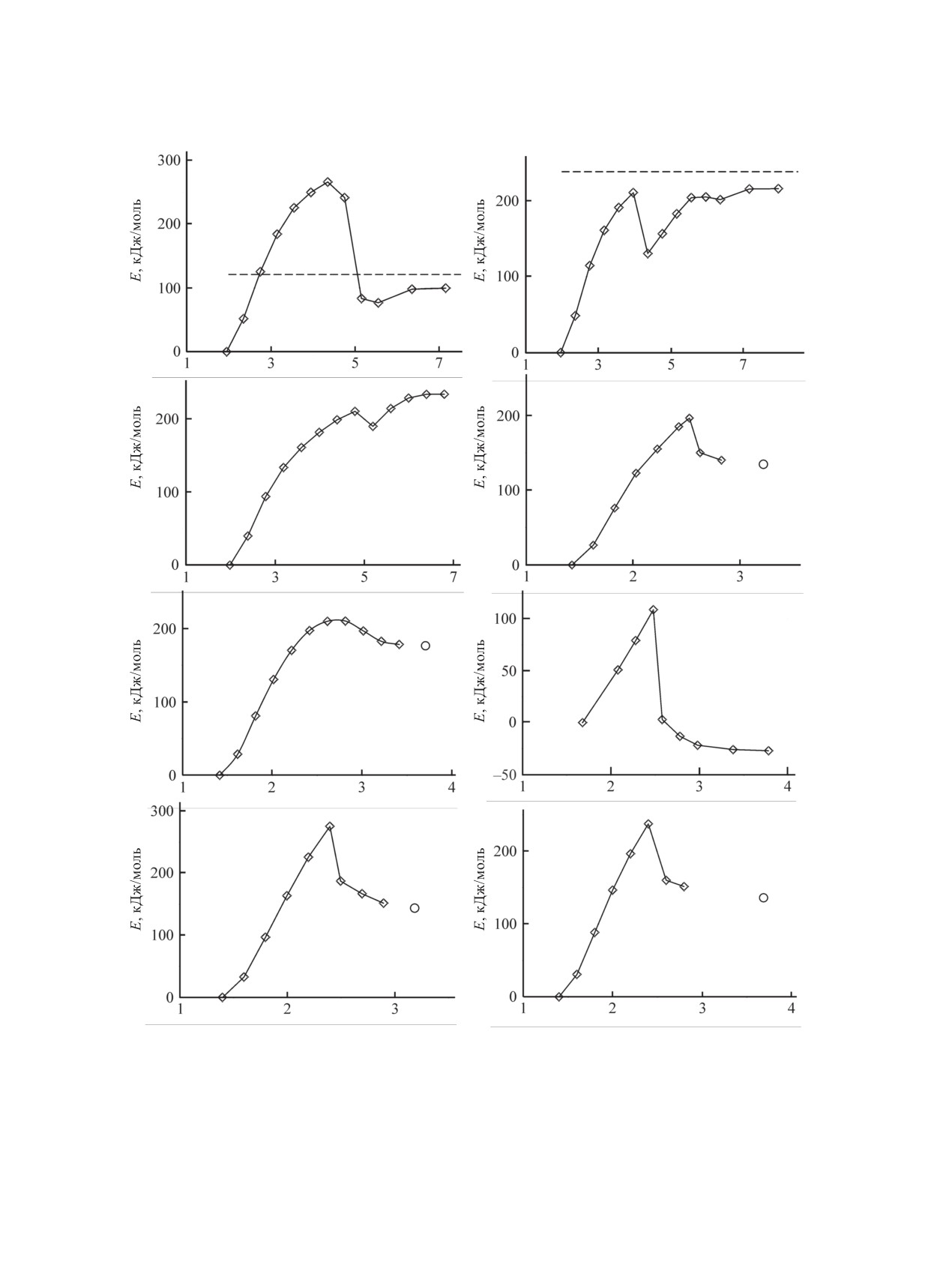
Рис. 6. Возможные пути начальных стадий разложения в молекуле комплекса 4. (a, б) Элиминирование молекулы аммиака
(растяжение связи N34-Co36 и N35-Co36); (в) элиминирование молекулы аммиака от катиона (растяжение связи Co1-N8);
(г) раскрытие тетразольного цикла по атому азота N4 (растяжение связи N38-N50); (д) раскрытие тетразольного цикла по
атому азота N1, имеющего метильную группу (растяжение связи N51- N52); (е) элиминирование молекулы азота после рас-
крытия тетразольного цикла по атому азота N4 (растяжение связи N38-N50); (ж) раскрытие тетразольного цикла по атому
азота N2 (растяжение связи N42-N53); (з) раскрытие тетразольного цикла по атому азота N3 (растяжение связи N33-N41).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
ВЛИЯНИЕ ОСОБЕННОСТЕЙ МЕХАНИЗМА НА
ЧАЛЬНЫХ СТАДИЙ РАСПАДА ЛИГАНДОВ
589
лы азота, а не с диссоциации молекулы координи-
8. Ostrovskii V.A., Popova E.A., Trifonov R.E. //Adv.
рованного аммиака из внутренней сферы комплек-
Heterocycl. Chem. 2017. Vol. 123. P. 1. doi 10.1016/
са кобальта(III). Возможность изменения началь-
bs.aihch.2016.12.003
ных стадий разложения амминатов кобальта(III) с
9. Frisch M.J., Trucks G.W., Schlegel H.B., Scuseria G.E.,
тетразольными лигандами в зависимости от при-
Robb M.A., Cheeseman J.R., Scalmani G., Barone V.,
роды заместителей в тетразольном кольце следует
Mennucci B., Petersson G.A., Nakatsuji H., Caricato M.,
учитывать при прогнозировании эффективности
Li X., Hratchian H.P., Izmaylov A.F., Bloino J., Zheng G.,
этих комплексов как инициирующих энергетиче-
Sonnenberg J.L., Hada M., Ehara M., Toyota K., Fuku-
ских материалов.
da R., Hasegawa J., Ishida M., Nakajima T., Honda Y.,
ФОНДОВАЯ ПОДДЕРЖКА
Kitao O., Nakai H.,Vreven T., Montgomery J.A., Pe-
ralta J.E., Jr., Ogliaro F., Bearpark M., Heyd J.J.,
Работа выполнена при финансовой поддержке
Brothers E., Kudin K.N., Staroverov V.N., Kobayashi R.,
Российского фонда фундаментальных исследо-
Normand J., Raghavachari K., RendellA., Burant J.C.,
ваний (гранты №№ 16-29-01056-офи_м, 17-03-
Iyengar S.S., Tomasi J., Cossi M., Rega N., Millam J.M.,
00566).
Klene M., Knox J.E., Cross J.B., Bakken V., Adamo C.,
КОНФЛИКТ ИНТЕРЕСОВ
Jaramillo J., Gomperts R., Stratmann R.E., Yazyev O.,
Авторы заявляют об отсутствии конфликта ин-
Austin A.J., Cammi R., Pomelli C., Ochterski J.W.,
тересов.
Martin R.L., Morokuma K., Zakrzewski V.G., Voth G.A.,
Salvador P., Dannenberg J.J., Dapprich S., Da-
СПИСОК ЛИТЕРАТУРЫ
niels A.D., Farkas O., Foresman J.B., Ortiz J.V.,
1. Matyáš R., Pachman J. Primary explosives. Heidelberg:
Cioslowski J. Gaussian 09, Revision A1, Gaussian Inc.,
Springer, 2013. doi 10.1007/431 978-8-642-28436-6
Wallingford CT, 2009.
2. Klapoetke T.M. Chemistry of High-Energy Materials.
10. Golubev V.K., Ilyushin M.A. // Proc. 20 Seminar «New
Berlin; Boston: Walter de Gruyter Gmbh, 2017.
trends in research of energetic materials», Pardubice,
3. Браун М., Доллимор Д., Галвей А. Реакции твер-
Czech Republic, 2017. Pt 1. P. 580.
дых тел. М.: Мир, 1983. 359 с.; Comprehensive
11. Голубев В.К., Илюшин М.А. // ЖОХ. 2017. Т. 87.
Chemical Kinetics / Eds C.H. Bamford, C.F.H. Tipper.
Вып. 2. С. 312; Golubev V.K., Ilyushin M.A. // Russ.
Amsterdam; Oxford; New York: Elsevier, 1980.
J. Gen. Chem. 2017. Vol. 87. N 2. P. 286. doi 10.1134/
Vol. 22.
S1070363217020220
4. Илюшин М.А., Шугалей И.В., Судариков А.М. Высо-
12. Golubev V.K., Ilyushin M.A. // Proc. 19 Seminar «New
коэнергетические металлокомплексы. Синтез, свой-
trends in research of energetic materials», Pardubice,
ства, применение. Saarbrucken: Lambert Academic
Czech Republic, 2016. Pt 2. P. 535.
Publishing RU, 2017. 268 с.
13. Ilyushin M.A., Smirnov A.V., Shugalei I.V., Golubev V.K. //
5. Ilyushin M.A., Shugalei I.V. In: Handbook of
Ecomaterials / Eds L.M.T. Martínez, O.V. Kharisso-
Proc. 20 Seminar «New trends in research of energetic
va, B.I. Kharisov. Cham: Springer Nature Switzerland
materials», Pardubice, Czech Republic, 2017. Pt 2.
AG, 2019. P. 3433. doi 10.1007/978-3-319-68255-6_46
P. 701.
6. Смирнов А.В., Федотов С.А., Агеев М.В., Ведерни-
14. Илюшин М.А., Тверьянович Ю.С., Тверьянович А.С.,
ков Ю.Н., Илюшин М.А. // Боеприпасы и высоко-
Аверьянов А.О., Смирнов А.В., Шугалей И.В. //
энергетические конденсированные системы. 2018.
ЖОХ. 2017. Т. 87. Вып. 11. С. 1860; Ilyushin M.A.,
№ 1. С. 31.
Tverjanovich Yu.S., Tverjanovich A.S., Aver’yanov A.O.,
7. Bates L.R. // Proc. 13 Symposium on Explosives and
Smirnov A.V., Shugalei I.V. // Russ. J. Gen. Chem. 2017.
Pyrotechnics, Hilton Head Island, USA, 1986. P. III/1.
Vol. 87. N 11. P. 2600. doi 10.1134/S1070363217110147
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020
590
ИЛЮШИН и др.
Influence of Peculiarities of the Mechanism of the Initial Stages
of Ligand Decomposition on the Initiating Ability of Cobalt(III)
Amminetetrazolates
M. A. Ilyushina,*, I. V. Shugaleya, A. S. Tver’yanovichb, and A. V. Smirnova
a St. Petersburg State Institute of Technology (Technical University), St. Petersburg, 190013 Russia
b St. Petersburg State University, St. Petersburg, 198504 Russia
*e-mail: explaser1945@yandex.ru
Received October 1, 2019; revised October 1, 2019; accepted October 3, 2019
The results of quantum chemical calculations of isolated molecules of pentaammine-(5-cyano-2H-tetrazo-
lato-N2)-, pentaammine-(5-nitrotetrazolato-N2)-, tetraammine-cis-bis(5-nitro-2H-tetrazolato-N2)-, tetraam-
mine-cis-bis(1-methyl-5-aminotetrazolo-N3,N4)cobalt(III) perchlorates and the products of their possible primary
decomposition stage are presented. The energetics and pathways of such reactions are determined. For the first
time, using quantum chemical calculations, it was shown that the decomposition of cobalt amminates can begin
with the destruction of the tetrazole ligand and elimination of the nitrogen molecule, and not with the dissocia-
tion of the coordinated ammonia molecule from the inner sphere of the cobalt(III) complex. The activation and
dissociation energies of these processes are determined.
Keywords: quantum-chemical calculation, decomposition, complex amminetetrazolates, initiating ability
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 4 2020