ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2020, том 90, № 8, с. 1283-1289
УДК 546.185;547.551.2;547.53.024;548.312.3
СИНТЕЗ И СТРОЕНИЕ ГЕКСАБРОМОПЛАТИНАТОВ
ОРГАНИЛТРИФЕНИЛФОСФОНИЯ И -СТИБОНИЯ
© 2020 г. А. Р. Зыкова*, В. В. Шарутин, О. К. Шарутина, В. С. Сенчурин
Южно-Уральский государственный университет (национальный исследовательский университет),
пр. Ленина 76, Челябинск, 454080 Россия
*e-mail: aesya@mail.ru
Поступило в Редакцию 26 февраля 2020 г.
После доработки 4 марта 2020 г.
Принято к печати 4 марта 2020 г.
Гексабромоплатинаты органилтрифенилфосфония и -стибония синтезированы при взаимодействии
гексабромoплатината калия с бромидами органилтрифенилфосфония в ацетонитриле или воде. Комплек-
сы [Ph3PC2H5]2[PtBr6] и [Ph3PCH2Ph]2[PtBr6] получены перекристаллизацией из диметилсульфоксида;
комплексы [Ph3PCH2Ph][PtBr5(Et2SO-S)], [Ph4Sb·Et2SO-O]2[PtBr6] - перекристаллизацией гексабро-
моплатинатов бензилтрифенилфосфония и тетрафенилстибония из диэтилсульфоксида. По данным
рентгеноструктурных исследований, атомы фосфора в катионах имеют искаженную тетраэдрическую
координацию, атомы сурьмы - искаженную тригонально-бипирамидальную координацию за счет вза-
имодействия Sb···O=SEt2.
Ключевые слова: бромид этилтрифенилфосфония, бромид бензилтрифенилфосфония, бромид тетра-
фенилстибония, гексабромоплатинат калия
DOI: 10.31857/S0044460X20080168
Реакции галогенидов тетраорганилфосфония
гексабромоплатинатными анионами, полученны-
или тетраорганилстибония с солями платины
ми при взаимодействии бромида тетраорганил-
K2[PtHal6] (Hal = Cl, Br) в диметилсульфоксиде ча-
фосфония или -аммония с гексабромоплатино-
сто сопровождаются лигандным обменом в анионе
вой кислотой или гексабромоплатинатом калия
с замещением атома галогена на молекулу Me2SO
[14-19]. Кроме того, диалкилсульфоксид не всегда
с образованием анионов
[PtBr5(Me2SO-S)]2- и
замещает атом галогена в анионах. В связи с этим
[PtCl5(Me2SO-S)]2- [1-5]. В анионе возможно так-
нами синтезированы гексабромоплатинатные ком-
же замещение галогена на молекулу диэтилсуль-
плексы и исследованы их реакции с диалкилсуль-
фоксида [PtCl5(Et2SO-S)]- [6].
фоксидами.
Помимо замещения в анионе для ионных
При взаимодействии гексабромоплатината ка-
комплексов сурьмы возможно вхождение мо-
лия с бромидами трифенил(этил)- и бензил(три-
лекулы Me2SO в координационную сферу ато-
фенил)фосфония в ацетонитриле (мольное со-
ма сурьмы в катионе, например [Ph4Sb(Me2SO-
отношение исходных реагентов 1:2) образуются
kO)][PtCl5(Me2SO-S)]
и
[Ph4Sb(Me2SO-S)]·
комплексы 1 и 2 (схема 1).
[PdCl3(Me2SO-O)] [7]. Реакции диметилсульфок-
сида с комплексами платины могут сопровождать-
Перекристаллизация комплексов 1, 2 из диме-
ся понижением степени окисления центрального
тилсульфоксида не сопровождается замещением
атома за счет восстановительных свойств Me2SO
атома брома. Однако при перекристаллизации из
[8-13].
диэтилсульфоксида молекула растворителя встра-
Химия бромоплатинатных комплексов изучена
ивается в координационную сферу платины, за-
не так хорошо, как химия гексахлороплатинатных.
мещая атом брома c образованием комплекса 3
Описано небольшое число ионных комплексов с
(схема 2).
1283
1284
ЗЫКОВА и др.
Схема 1.
Схема 2.
Схема 3.
Взаимодействие гексабромоплатината калия с
погрешности эксперимента: 1.79(3)-1.82(3) (1),
бромидом тетрафенилстибония в воде (мольное
1.79(2)-1.80(2) (2), 1.80(6)-1.82(6) (3) (табл. 2).
соотношение исходных реагентов 1:2) приводит
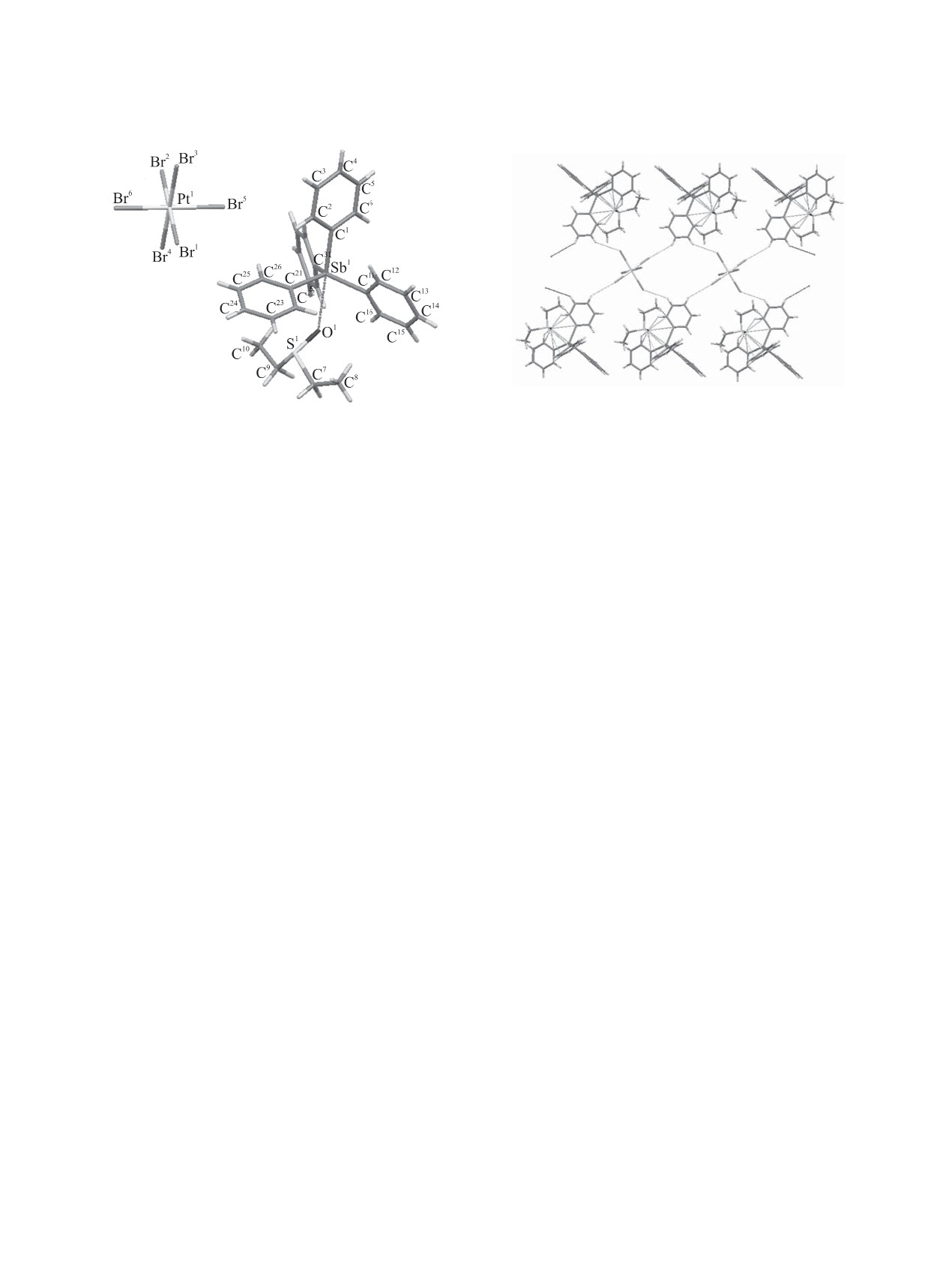
Атомы сурьмы в катионах [Ph4Sb·Et2SO]+ име-
к образованию гексабромоплатината тетрафенил-
ют искаженную тригонально-бипирамидальную
стибония, при перекристаллизации которого из
координацию. Молекула диэтилсульфоксида коор-
диэтилсульфоксида лигандного обмена в анионе
динируется к атому сурьмы через атом кислорода
не происходит, но молекула растворителя коорди-
(рис. 3). Псевдоаксиальный угол СSbО составляет
нируется к атому сурьмы с образованием комплек-
178.4(2)°, а псевдоэкваториальные углы C21Sb1C11,
са 4 (схема 3). Комплексы 1-4 представляют собой
C21Sb1C31, C11Sb1C31 - 113.7(2), 114.7(2), 120.3(2)°
красно-коричневые кристаллы, выход которых со-
соответственно; их сумма [348.7(2)°] меньше те-
ставил 87, 61, 70 и 84% соответственно.
оретического значения 360°. Аксиальная связь
Методом рентгеноструктурного
анализа
Sb-С1 2.129(6) Å несколько длиннее экватори-
(табл. 1) установлено строение комплексов 1-4. Ка-
альных связей Sb-С11, Sb-С21, Sb-С31 [2.088(5)-
тионы органилтрифенилфосфония 1-3 обладают
2.121(5) Å], что характерно для тригонально-
мало искаженной тетраэдрической конфигурацией
бипирамидальных структур. Расстояние Sb···О
(рис. 1, 2). Величины валентных углов СРС не-
[2.708(7) Å] при сумме ван-дер-ваальсовых ради-
значительно различаются между собой [угол CPC
усов 3.58 Å [20] больше аналогичного расстояния
108.3(11)-109.9(13)
(1),
107.2(11)-111.3(11)
(2),
в комплексе
[Ph4Sb(Me2SO-S)][PdCl3(Me2SO-S)]
108.1(3)-110.3(3)° (3)]. Расстояния P-C в пределах
2.567(2) Å [7].
Рис. 1. Общий вид молекулы комплекса 1 в кристалле.
Рис. 2. Общий вид молекулы комплекса 3 в кристалле.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 8 2020
СИНТЕЗ И СТРОЕНИЕ ГЕКСАБРОМОПЛАТИНАТОВ
1285
Таблица 1. Кристаллографические данные, параметры эксперимента и уточнения структуры комплексов 1-4
Параметр
1
2
3
4
М
1257.21
1381.34
1054.22
1747.21
Сингония
Триклинная
Триклинная
Моноклинная
Триклинная
-
-
-
Пространственная группа
P1
P1
P21/n
P1
a, Å
10.173(5)
10.000(5)
12.968(10)
10.781(12)
b, Å
10.573(7)
10.696(6)
9.906(7)
11.406(12)
c, Å
11.109(6)
13.504(6)
26.28(3)
12.921(11)
α, град
79.61(2)
94.17(2)
90.00
74.66(4)
β, град
67.631(16)
108.89(2)
98.56(5)
83.79(5)
γ, град
72.16(3)
116.26(3)
90.00
77.19(6)
V, Å3
1049.0(10)
1185.1(10)
3338(5)
1492(3)
Z
1
1
4
1
dвыч, г/см3
1.990
1.935
2.098
1.945
μ, мм-1
9.162
8.119
10.321
7.363
F(000)
598.0
662.0
1992.0
834.0
Размер кристалла, мм
0.22 × 0.14 × 0.12
0.34 × 0.14 × 0.08
0.2 × 0.1 × 0.05
0.58 × 0.28 × 0.23
Область сбора данных по θ, град
6.8-72.92
6.12-67.6
5.82-53.48
5.94-65.56
Интервалы индексов отражений
-17 ≤ h ≤ 16,
–15 ≤ h ≤ 15,
-16 ≤ h ≤ 16,
-16 ≤ h ≤ 16,
-17 ≤ k ≤ 17,
-16 ≤ k ≤ 16,
-12 ≤ k ≤ 12,
-17 ≤ k ≤ 17,
-18 ≤ l ≤ 18
-21 ≤ l ≤ 21
-33 ≤ l ≤ 33
-19 ≤ l ≤ 19
Измерено отражений
69143
69371
39836
62178
Rint
0.0428
0.0402
0.0560
0.0682
Независимых отражений
10188
9453
7047
10930
Переменных уточнения
224
268
345
315
GOOF
1.063
1.058
1.054
1.019
R-Факторы по F2 > 2σ(F2)
R1 = 0.0317
R1 = 0.0286
R1 = 0.0360
R1 = 0.0516
wR2 = 0.0642
wR2 = 0.0562
wR2 = 0.0674
wR2 = 0.1160
R-Факторы по всем отражениям
R1 = 0.0481
R1 = 0.0434
R1 = 0.0551
R1 = 0.0884
wR2 = 0.0692
wR2 = 0.0601
wR2 = 0.0732
wR2 = 0.1309
Остаточная электронная
0.70/-1.88
1.25/-1.85
1.08/-1.19
4.22/-2.16
плотность (min/max), e/A3
Геометрия координированных диэтилсульфок-
мом серы. транс-Углы BrPtBr в комплексах 1, 2, 4
сидных лигандов в анионе комплекса 3 и в кати-
равны 180°, в комплексе 3 - 176.25(3), 179.11(3)°,
оне комплекса 4 отличается от геометрии свобод-
транс-угол SPtBr - 177.96(5)°. цис-Углы BrPtBr
ной молекулы диэтилсульфоксида. Углы СSC в
в комплексах 1, 2 и 4 близки к идеальному зна-
комплексах 3 и 4 [95.9(4) и 99.6(7)°] отличаются
чению 89.69(4)-90.07(4)° (1), 89.69(4)-90.69(4)°
от аналогичного угла в несвязанной молекуле ди-
(2), 89.16(8)-90.91(6) (4); цис-углы BrPtBr и SPtBr
этилсульфоксида [97.3(3)°] [21]. Наиболее замет-
в комплексе 3 изменяются в пределах 88.70(3)-
ные различия наблюдаются для длин связи S-O:
91.81(7)°, 89.14(5)-93.77(5)°. Длины связей Pt-Br:
связь в анионе комплекса 3 короче [1.432(6) Å (3)],
2.467(14)-2.480(14) Å (1), 2.466(9)-2.480(14) Å (2),
чем в катионе комплекса 4 [1.519(5) Å], и отлича-
2.459(18)-2.502(2) Å (3), 2.451(2)-2.467(2) Å (4),
ется от длины связи в свободной молекуле диэтил-
что меньше суммы ковалентных радиусов атомов
сульфоксида [1.496(14) Å] [21].
платины и брома (2.56 Å [22]).
В центросимметричных октаэдрических анио-
нах [PtBr6]2- комплексов 1, 2, 4 атомы Pt(IV) ко-
Cвязь Pt-S в анионе комплекса 3 укорочена
ординированы с шестью атомами брома, в анионе
[2.364(2) Å] по сравнению с суммой ковалентных
[PtBr5(Et2SO-S)]- комплекса 3 молекула диэтил-
радиусов (2.41 Å [22]) и близка к наблюдаемым
сульфоксида координируется к атому платины ато-
значениям в аналогичных анионах [2, 6].
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 8 2020
1286
ЗЫКОВА и др.
Таблица 2. Основные длины связей и валентные углы в молекулах комплексов 1-4
Связь
d, Å
Связь
d, Å
Угол
ω, град
Угол
ω, град
1
Pt1-Br1
2.480(14)
P1-C1
1.798(2)
Br2Pt1Br1
180.0
Br5Pt1Br1
90.06(4)
Pt1- Br2
2.480(14)
P1-C11
1.793(2)
Br3Pt1Br4
179.998(2)
Br6Pt1Br3
89.96(3)
Pt1- Br3
2.469(12)
P1-C21
1.792(2)
Br5Pt1Br6
180.0
C21P1C7
109.86(13)
Pt1- Br4
2.469(12)
P1-C7
1.797(2)
Br3Pt1 Br1
90.31(4)
C11P1C1
108.29(11)
Pt1- Br5
2.467(14)
C7-C8
1.521(4)
Br3Pt1Br2
89.69(4)
C1P1C7
109.60(12)
Pt1- Br6
2.467(14)
Br6Pt1Br1
89.94(4)
C21P1C1
108.76(11)
2
Pt1-Br1
2.477(11)
P1-C21
1.802(2)
Br2Pt1Br1
180.0
Br5Pt1Br1
90.07(4)
Pt1- Br2
2.477(11)
P1-C11
1.797(2)
Br3Pt1Br4
179.999(16)
Br6Pt1Br3
89.86(4)
Pt1- Br3
2.480(14)
P1-C37
1.822(3)
Br5Pt1Br6
179.999(17)
C21P1C37
107.18(11)
Pt1- Br4
2.480(14)
P1-C1
1.795(3)
Br3Pt1 Br1
90.06(4)
C11P1C1
112.63(11)
Pt1- Br5
2.467(14)
C37-C31
1.516(3)
Br3Pt1Br2
89.94(4)
C1P1C37
110.16(12)
Pt1- Br6
2.466(9)
Br6Pt1Br1
89.93(4)
C21P1C1
111.31(11)
3
Pt1-Br1
2.479(18)
P1-C11
1.809(6)
Br2Pt1Br1
90.70(3)
Br5Pt1Br4
90.54(7)
Pt1-Br2
2.459(18)
P1-C37
1.825(6)
Br3Pt1Br4
91.81(7)
C21P1C37
109.4(3)
Pt1-Br3
2.502(2)
P1-C1
1.807(6)
Br5Pt1Br2
88.80(7)
C11P1C1
109.8(3)
Pt1-Br4
2.485(18)
S1-Ο1
1.432(6)
Br4Pt1 Br1
88.70(3)
C1 P1C37
108.9(3)
Pt1-Br5
2.480(2)
S1-C7
1.782(7)
Br3Pt1Br2
88.82(7)
C11P1C37
110.3(3)
Pt1-S1
2.364(2)
S1-C9
2.035(15)
Br4Pt1Br2
179.11(3)
C7S1C9
95.9(4)
P1-C21
1.801(6)
Br5Pt1Br3
176.25(3)
4
Pt1-Br1
2.467(2)
Sb1-C11
2.098(5)
Br2Pt1Br1
180.0
C21Sb1C31
114.7(2)
Pt1- Br2
2.467(2)
Sb1-C31
2.121(5)
Br3Pt1Br4
180.00(5)
C11Sb1C1
101.5(2)
Pt1- Br3
2.451(2)
Sb1-C1
2.129(6)
Br5Pt1Br6
180.0
C1 Sb1C31
99.8(2)
Pt1- Br4
2.451(2)
S1-Ο1
1.519(5)
Br3Pt1 Br1
89.70(9)
C21Sb1C1
102.7(2)
Pt1- Br5
2.464(19)
S1-C7
1.764(11)
Br3Pt1Br2
90.30(9)
O1Sb1C1
178.4(2)
Pt1- Br6
2.464(19)
S1-C9
1.735(11)
Br6Pt1Br1
89.08(6)
C21Sb1C11
113.7(2)
Sb1-C21
2.088(5)
Sb1∙∙∙Ο1
2.708(7)
Br5Pt1Br1
90.91(6)
C9S1C7
99.6(7)
Br4Pt1Br6
89.16(8)
В кристаллах комплексов 1-4 катионы и ани-
Таким образом,
взаимодействие гексабромо-
оны связаны слабыми водородными связями
платината калия с бромидами органилтрифенил-
C-H···Br [2.87-3.03 Å] (рис. 4). В кристалле ком-
фосфония приводит к образованию комплексов,
перекристаллизация которых из диэтилсульфокси-
плекса 1 каждый анион окружен шестью катиона-
да, в отличие от перекристаллизации из диметил-
ми, в комплексе 2 в окружении аниона находятся 8
сульфоксида, сопровождается лигандным обменом
катионов, каждый анион в комплексах 3 и 4 связа-
в анионе. В случае гексабромоплатината тетрафе-
ны с четырьмя катионами. В образовании слабых
нилстибония молекула диэтилсульфоксида входит
водородных связей между анионами комплекса 3
в координационную сферу атома сурьмы катиона.
принимают участие атомы водорода диэтилсуль-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
фоксидного лиганда (C7-H7···Br5 3.04 Å). Помимо
координационной связи с атомом сурьмы в кри-
ИК спектры записывали на спектрометре
сталле комплекса 4 молекулы диэтилсульфоксида
Shimadzu IRAffinity-1S в таблетках KBr в обла-
образуют с фенильными лигандами водородные
сти 4000-400 см-1. Рентгеноструктурный анализ
связи O···H-C [2.33-2.52 Å].
кристаллов комплексов 1-4 проводили на авто-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 8 2020
СИНТЕЗ И СТРОЕНИЕ ГЕКСАБРОМОПЛАТИНАТОВ
1287
Рис. 4. Водородные связи Br∙∙∙H-C и O∙∙∙H-C в кри-
Рис. 3. Общий вид молекулы комплекса 4 в кристалле.
сталле комплекса 4.
матическом четырехкружном дифрактометре D8
Гексабромоплатинат бис[бензил(трифенил)-
QUEST Bruker (MoKα-излучение, λ = 0.71073 Å,
фосфония] (2). Выход 61%, красно-коричневые
графитовый монохроматор) при 296(2) K. Струк-
кристаллы, т. пл. 227°С (разл.). ИК спектр, ν, см-
1: 3056, 2890, 1584, 1493, 1481, 1436, 1187, 1164,
туры расшифрованы прямым методом, позиции и
1143, 1110, 1072, 1027, 995, 923, 837, 784, 743,
температурные параметры неводородных атомов
716, 686, 583,514. Найдено, % С 43.48; Н 3.23.
уточнены в изотропном, а затем в анизотропном
C50H44Br6P2Pt. Вычислено, %: С 43.51; Н 3.19.
приближении полноматричным МНК. Атомы во-
Пентабромо(диэтилсульфоксидо)платинат
дорода помещены в геометрически рассчитанные
бензил(трифенил)фосфония
(3).
62
мг
положения и включены в уточнение в модели
(0.045 ммоль) комплекса 2 растворяли в 2 мл ди-
наездника. Сбор, редактирование данных и уточ-
этилсульфоксида. После испарения растворителя
нение параметров элементарной ячейки, а так-
наблюдали образование кристаллов. Выход 33 мг
же учет поглощения проведены по программам
(70%), красно-коричневые кристаллы, т. пл. 199°С
SMART и SAINT-Plus [23]. Все расчеты по опреде-
(разл.). ИК спектр, ν, см-1: 3057, 2937, 2852, 2363,
лению и уточнению структур выполнены по про-
1585, 1494, 1438, 1406, 1188, 1151, 1111, 995, 836,
граммам SHELXL/PC [24] и OLEX2 [25]. Полные
782, 759, 745, 719, 691, 583, 509, 495. Найдено, %:
таблицы координат атомов, длин связей и валент-
С 33.01; Н 3.05. C29H32Br5OPPtS. Вычислено, %: С
ных углов депонированы в Кембриджском банке
33.02; Н 3.03.
структурных данных: CCDC 1968768 (1), 1970908
Гексабромоплатинат бис[тетрафенил(диэтил-
(2), 1983823 (3), 1973723 (4).
сульфоксид)стибония] (4). 100 мг (0.065 ммоль)
Гексабромоплатинат бис[трифенил(этил)-
гексабромоплатината тетрафенилстибония, полу-
фосфония]
(1). Раствор
37 мг
(0.1 ммоль)
ченного при взаимодействии гексабромоплатината
бромида
трифенил(этил)фосфония
в
калия с бромидом тетрафенилстибония (1:2 мол.) в
7 мл ацетонитрила приливали к раствору 50 мг
воде, растворяли в 2 мл диэтилсульфоксида. После
испарения растворителя происходило образование
(0.05 ммоль) гексабромоплатината калия в 5 мл
кристаллов. Выход 96 мг (84%), красно-коричне-
ацетонитрила. Удаляли растворитель, остаток пе-
вые кристаллы, т. пл. 163°С (разл.). ИК спектр,
рекристаллизовывали из диметилсульфоксида.
ν, см-1: 3048, 2974, 2932, 2897, 1477, 1435, 1070,
Выход 110 мг (87%), красно-коричневые кристал-
1059, 995, 962, 737, 689, 457, 447. Найдено, %: С
лы, т. пл. 214°С (разл.). ИК спектр, ν, см-1: 3056,
38.41; Н 3.49. C56H60Br6O2PtS2Sb2. Вычислено, %:
3015, 2896, 1584, 1484, 1451, 1436, 1398, 1383,
С 38.49 Н 3.44.
1187, 1161, 1113, 1027, 995, 846, 754, 737, 722,
689, 529, 503, 491. Найдено, %: С 38.20; Н 3.21.
КОНФЛИКТ ИНТЕРЕСОВ
C40H40Br6P2Pt. Вычислено, %: С 38.25; Н 3.19.
Авторы заявляют об отсутствии конфликта
Комплекс 2 получен аналогично.
интересов.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 8 2020
1288
ЗЫКОВА и др.
СПИСОК ЛИТЕРАТУРЫ
Vol. 361. P. 2591. doi 10.1016/j.ica.2007.10.041
14. Юсенко К.В., Громилов С.А., Байдина И.А., Шу-
1. Bokach N.A., Haukka M., Pombeiro A.J.L., Morozki-
бин Ю.В., Корольков И.В., Дребущак Т.Н., Басо-
na S.N., Kukushkin V.Yu. // Inorg. Chim. Acta. 2002.
ва Т.В., Коренев С.В. // ЖСХ. 2002. Т. 43. № 4. С. 699;
Vol. 336. N 95. P. 100. doi 10.1016/s0020-
Yusenko K.V., Gromilov S.A., Baidina I.A., Shubin Yu.V.,
1693(02)00867-8
Korol’kov I.V., Drebushchak T.N., Basova T.V., Kore-
2. Шарутин В.В., Сенчурин В.С., Шарутина О.К., Со-
nev S.V. // J. Struct. Chem. 2002. Vol. 43. N.4. P. 649.
мов Н.В., Гущин А.В. // Коорд. хим. 2011. Т. 37. № 11.
doi 10.1023/A:1022004721745
С. 857; Sharutin V.V., Senchurin V.S., Sharutina O.K., So-
15. Hu J.J., Hor F.Li. A. // J. Organomet. Chem. 2009.
mov N.V., Gushchin A.V. // Russ. J. Coord. Chem. 2011.
Vol. 28. N 4. P. 1212. doi 10.1021/om800978j
Vol. 37. N.11. P. 854. doi 10.1134/S1070328411100113
16. Kim N.H., Ha K. // Z. Kristallogr. NCS. 2010. Vol. 225.
3. Cotton F.A., Francis R. // J. Am. Chem. Soc. 1960.
P. 37. doi 10.1524/ncrs.2010.0014.
Vol. 82. P. 2986. doi 10.1021/ja01497a003.9
17. Rosokha S.V., Kumar A. // J. Mol. Struct. 2017.
4. Kukushkin V.Yu., Pombeiro A.J.L., Ferreira C.M.P.,
Vol. 1138. P. 129. doi 10.1016/j.molstruc.2017.03.009
Elding L.I. // Inorg. Synth. 2002. Vol. 33. P. 189.
0022-2860
5. Панина Н.С., Кукушкин Ю.Н. // ЖНХ. 1999. Т. 44.
18. Ha K. // Z. Kristallogr. 2013. Vol. 228. N 2. P. 255. doi
№ 5. С. 798; Panina N.S., Kukushkin Yu.N. // J. Inorg.
10.1524/ncrs.2013.0130
Chem. 1999. Vol. 44. N. 5. P. 798.
19. Ha K. // Acta Crystallogr. (E). 2010. Vol. 66. N. 2.
6. Tкачёва A.Р., Шарутин В.В., Шарутина O.K. // ЖОХ.
P. 105. doi 10.1107/S1600536809055196
2019. Т. 89. Вып. 2. С. 283; Tkacheva A.R., Sharu-
20. Mantina M., Chamberlin A.C., Valero R., Cramer C.J.
tin V.V., Sharutina O.K. // Russ. J. Gen. Chem. 2019.
Truhlar D.G. // J. Phys. Chem. (A). 2009. Vol. 113.
Vol. 89. N 2. P. 277. doi 10.1134/S107036321902018X
N 19. P. 5806. doi 10.1021/jp8111556.
7. Шарутина В.В., Сенчурин В.С., Шарутина О.К. //
21. Карапетян А.А., Маркарян Ш.А., Антипин М.Ю.,
Коорд. хим. 2013. Т. 58. № 5. С. 616; Sharutin V.V.,
Стручков Ю.Т. // Арм. хим. ж. 1989. Т. 42. № 8.
Senchurin V.S., Sharutina O.K. // Russ. J. Coord.
Chem. 2013. Vol. 58. N 5. P. 543. doi 10.1134/
С. 483.
S0036023613050203
22. Cordero B., Gómez V., Platero-Prats A.E., Revés M.,
8. Кукушкин В.Ю., Паньков Е.Ю. // ЖOХ. 1987. Т. 57.
Echeverría J., Cremades E., Barragána F., Alvarez S. //
Вып. 10. С. 2691; Kukushkin V.Yu., Pan’kov V.Yu. //
Dalton Trans. 2008. Vol. 21. P. 2832. doi 10.1039/
USSR J. Gen. Chem. 1987. Vol. 58. P. 2297.
B801115J
9. Ткачёва А.Р., Шарутин В.В. // Вестн. ЮУрГУ. 2018.
23. SMART and SAINT-Plus. Versions 5.0. Data Collection
Т. 10. № 3. С. 63. doi 10.14529/chem180307
and Processing Software for the SMART System.
10. Сотман С.С., Фундаменский В.С., Кукушкин В.Ю.,
Bruker AXS Inc. 1998. Madison, Wisconsin, USA.
Панькова Е.Ю. // ЖОХ. 1988. Т. 58. Вып. 10. С. 2297.
24. SHELXTL/PC. Versions 5.10. An Integrated System
11. Кукушкин Ю.Н., Хроменкова З.А., Эсаулова В.А. //
for Solving, Refining and Displaying Crystal Structures
ЖОХ. 1994. Т. 64. Вып. 9. С. 1554.
From Diffraction Data. Bruker AXS Inc. 1998. Madison,
12. Belsky V.K., Konovalov V.E., Kukushkin V.Y. // Acta
Wisconsin, USA.
Crystallogr. 1993. Vol. 49. P. 751. doi 10.1107/
25. Dolomanov O.V., Bourhis L.J., Gildea R.J., Ho-
S0108270192008308
ward J.A.K., Puschmann H. // J. Appl. Cryst. 2009.
13. Rochon F.D., Tessier C. // Inorg. Chim. Acta. 2008.
Vol. 42. P. 339. doi 10.1107/S0021889808042726
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 8 2020
СИНТЕЗ И СТРОЕНИЕ ГЕКСАБРОМОПЛАТИНАТОВ
1289
Synthesis and Structure of Organyltriphenylphosphonium
and -Stibonium Hexabromoplatinates
A. R. Zykova*, V. V. Sharutin, O. K. Sharutina, and V. S. Senchurin
South Ural State University (National Research University), Chelyabinsk, 454080 Russia
*e-mail: aesya@mail.ru
Received February 26, 2020; revised March 4, 2020; accepted March 4, 2020
Organyltriphenylphosphonium and -stibonium hexabromoplatinates were synthesized by reacting potassium
hexabromoplatinate with organyltriphenylphosphonium and -stibonium bromides in acetonitrile or water.
Complexes [Ph3PC2H5]2[PtBr6] and [Ph3PCH2Ph]2[PtBr6] were obtained by recrystallization from dimethyl
sulfoxide; complexes [Ph3PCH2Ph][PtBr5(Et2SO-S)] and [Ph4Sb·Et2SO-O]2[PtBr6] were obtained by the
recrystallization of benzyltriphenylphosphonium and tetraphenylstibonium hexabromoplatinates from diethyl
sylfoxide. According to X-ray data, phosphorus atoms in the cations have a distorted tetrahedral coordination,
the antimony atom has a distorted trigonal-bipyramidal coordination due to the Sb···O=SEt2 interaction.
Keywords: ethyltriphenylphosphonium bromide, benthyltriphenylphosphonium bromide, tetraphenylstibonium
bromide, potassium hexabromoplatinate
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 90 № 8 2020