ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 1, с. 157-164
УДК 543.062
РОЛЬ КИСЛОРОДА В ФОРМИРОВАНИИ
ПЕРОВСКИТОПОДОБНЫХ ОКСИДОВ
ГОМОЛОГИЧЕСКОГО РЯДА BamBim+nOy
(m = 1-9; n = 0-3, 5, 7, 9)
© 2021 г. Н. В. Барковский*
Институт физики твердого тела Российской академии наук, ул. Академика Осипьяна 2, Черноголовка, 142432 Россия
*e-mail: barkov@issp.ac.ru
Поступило в Редакцию 18 сентября 2020 г.
После доработки 12 октября 2020 г.
Принято к печати 17 октября 2020 г.
Методами рентгенофазового и химического анализа исследовано влияние условий синтеза на фазовый
состав и валентное состояние висмута в перовскитоподобных оксидах гомологического ряда BamBim+nOy
(m = 1-9; n = 0-3, 5, 7, 9). Оксиды, полученные при p(O2) = 1 кПа, практически не содержат Bi(V), ха-
—
рактеризуются средней степенью окисления висмута Bi
= 3.00-3.01 и термодинамически устойчивы от
области кристаллизации до 20°C. При охлажднии ниже линии солидуса происходит окисление оксидов
—
BamBim+nOy и возрастание степени окисления (Bi
> 3.06). Конечные продукты окисления при ~700-20°С -
оксиды ВаВiO3 и Ba4Bi+3.00O23.5. Перовскитоподобные оксиды BamBim+nOy со средней степенью окисле-
—
ния висмута Bi
> 3.06 не обнаружены. Индивидуальные оксиды этого ряда со значительным количеством
Bi(V) или только Bi(V) не могут быть получены при p(O2) = 21-100 кПа.
Ключевые слова: гомологические ряды, перовскитоподобные оксиды Ba-Bi-O, валентное состояние,
картины рентгеновской дифракции, химический анализ
DOI: 10.31857/S0044460X21010170
Исследования системы Ba-Bi-O имеют более
цвет на черный, и доля ионов Bi5+ доходила до 34%
чем полувековую историю. Первый оксид этой
от общего количества висмута. Таким образом, в ис-
системы Ba(BiO3)2·4H2O синтезирован при кипя-
следованных твердых растворах висмут находится
чении NaBiO3 с 15%-ным раствором BaCl2 [1]. В
в «смешанно-валентном» состоянии Bi(III) и Bi(V).
полученном оксиде, по данным иодометрического
Для количественной характеристики валентного
титрования, весь висмут имеет степень окисления
состояния висмута в таких образцах используют
+5. Однако индивидуальность полученного соеди-
среднюю степень окисления висмута (Bi— ). В полу-
нения не подтверждена рентгенографически.
ченных образцах [2] максимальное значение Bi— =
3.68.
Методом порошковой рентгеновской дифрак-
ции обнаружен твердый раствор Ba2xBi2(1-x)O3-x
При отжиге смеси оксидов бария и висмута в
с перовскитоподобной структурой (x = 0.22-0.50,
соотношении [Ba]:[Bi] = 1:2 в атмосфере кисло-
катионное соотношение Ba-Bi 0.28-1.0) [2]. В об-
рода при 1000°С c последующим медленным ох-
разцах, полученных на воздухе или в атмосфере
лаждением получен оксид, в котором, по данным
сухого азота при 850-1000°С, по данным иодоме-
волюмометрического определения активного
трического титрования, практически нет висмута
кислорода, средняя степень окисления висмута
со степенью окисления +5. При последующем низ-
Bi— = 3.46 [3]. Рентгенографические данные окси-
котемпературном отжиге при 550°С в кислородсо-
да не приведены. Для впервые синтезированного
держащей атмосфере образцы изменяли красный
оксида BaBiO3 на основании данных химическо-
157
158
БАРКОВСКИЙ
Параметры и объемы элементарных ячеек перовскитоподобных оксидов гомологического ряда BamBim+nOy
Состав фазы BamBim+nOy
Параметры (±0.002) ячейки, Å
V, Å3
m
n
[Ba]:[Bi]
а
b
с
6
1
6:7
4.374
4.402
4.514
86.91
4
1
4:5
4.365
4.385
4.520
86.52
3
1
3:4
4.362
4.382
4.511
86.22
2
1
2:3
4.361
4.375
4.502
85.90
3
2
3:5
4.353
4.367
4.503
85.60
6
5
6:11
4.362
4.364
4.486
85.39
1
1
1:2
4.353
4.358
4.495
85.27
1
5
4:9
4.367
4.390
4.405
84.45
2
3
2:5
4.352
4.359
4.401
83.49
4
7
4:11
4.352
4.359
4.400
83.49
1
2
1:3
4.374
83.68
4
9
4:13
4.370
83.45
го анализа рассчитано значение Bi— = 4.04, позже
стей их термической устойчивсти на схемах фазо-
уточненное (4.00) [4-6]. Методами рентгеновской
вых равновесий системы Ba-Bi-O, построенных
дифракции и нейтронной дифракции показано [7],
ранее [8]. Для исследования фазообразования ок-
что перовскитовая ячейка этого оксида удвоена
сидов образцы отжигали при различных парциаль-
(Ba2Bi3+Bi5+O6) и в ней ионы висмута Bi3+ и Bi5+ в
ных давлениях кислорода (1-101 кПа) в широких
эквимолярном соотношении занимают два набора
интервалах температуры и времени. Фазовый со-
неэквивалентных позиций.
став закаленных в жидком азоте образцов контро-
лировали по картинам рентгеновской дифракции.
С использованиемметодов визуального политер-
Полученные образцы тестировали разработанны-
мического, рентгенофазового, дифференцально-
ми методами [11, 12] на наличие или отсутствие
термического, термогравиметрического, локаль-
ного рентгеноспектрального, химического, эле-
Bi(V). При положительных результатах методом
иодометрического титрования определяли количе-
ментного анализа и электронной дифракции в
ство Bi(V) и рассчитывали среднюю степень окис-
просвечивающем электронном микроскопе в
ления висмута Bi— .
обогащенной висмутом системе Ba-Bi-O дока-
зано отсутствие твердых растворов замещения
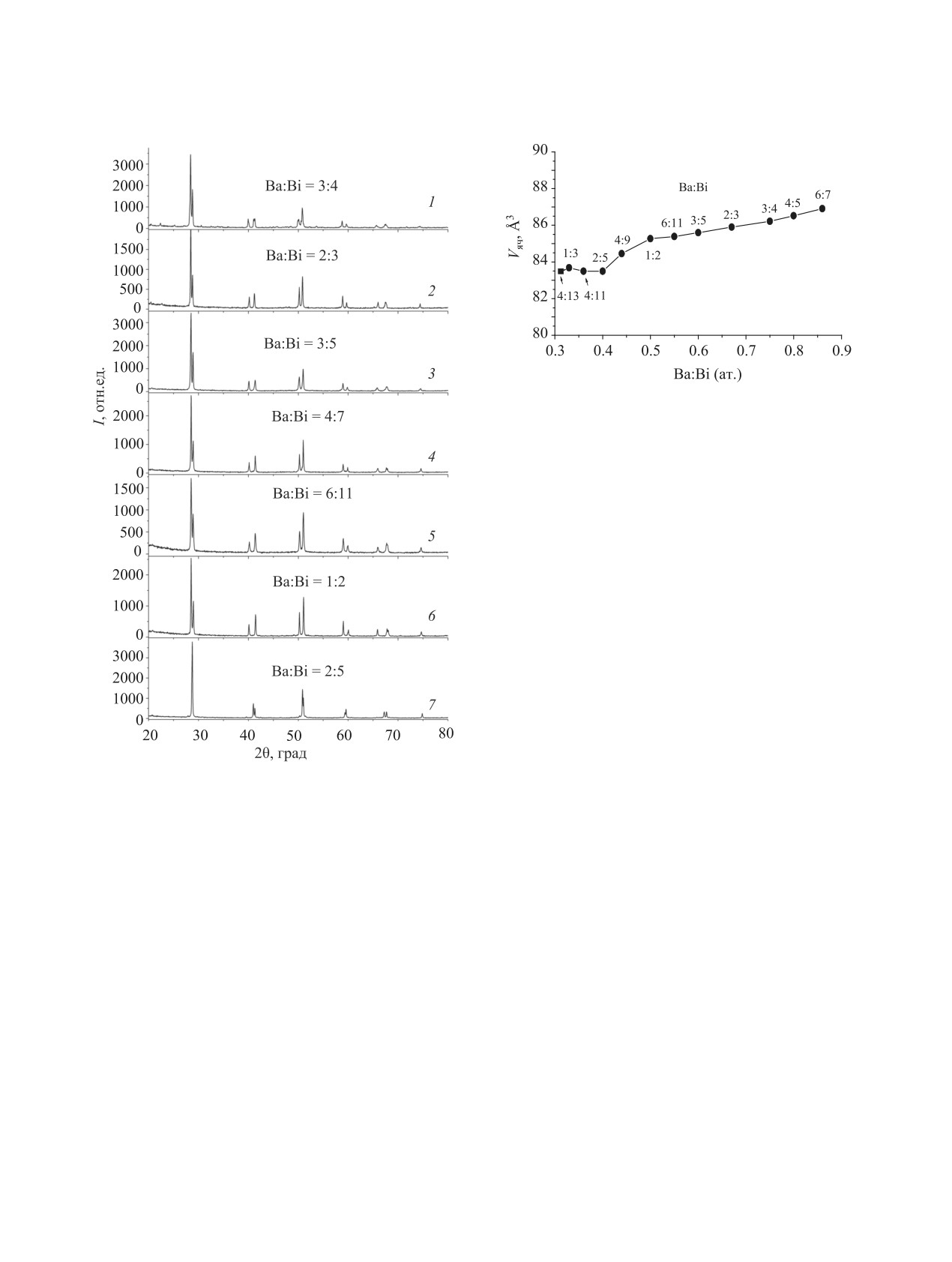
Все оксиды BamBim+nOy кристаллизуются в
Ba2xBi2(1-x)O3-x [8, 9]. В этой области существуют
ячейке перовскита. На рис. 1 представлены карти-
два гомологических ряда оксидов - BamBim+nOy
ны рентгеновской дифракции, демонстрирующие
(m = 1-9; n = 0-3, 5, 7, 9) с перовскитоподобной и
главную особенность оксидов гомологического
Ba2Bi8+nOy (n = 0, 1, 2, 4, 6, 8 и 10) с ромбоэдриче-
ряда BamBim+nOy - их изоструктурность. Близкие
ской структурой [10]. Все обнаруженные оксиды
параметры ячеек (см. таблицу) и наложение реф-
бария-висмута характеризуются упорядоченной
лексов затрудняют их идентификацию по картинам
по барию и висмуту перовскитоподобной или
рентгеновской дифракции, но индивидуальные
ромбоэдрической структурой, что подтверждается
картины электронной дифракции [8, 9] позволяют
наличием индивидуальной сверхструктуры (метод
справиться с этой проблемой. Элементарная ячей-
электронной дифракции) и картинами высокого
ка оксидов BamBim+nOy - ромбическая (рис. 1) за
разрешения в просвечивающем электронном ми-
исключением фаз с соотношением [Ba]:[Bi] = 1:3 и
кроскопе [8-10].
4:13 с кубической ячейкой.
В настоящей работе представлены результаты
Параметры a и b мало зависят от катионного
исследования влияния условий синтеза на фазо-
состава фаз BamBim+nOy. Объемы ячеек [8] с уве-
вый состав и валентное состояние висмута в пе-
личением доли висмута в оксиде BamBim+nOy име-
ровскитоподобных оксидах гомологического ряда
ют тенденцию к уменьшению (рис. 2) по причине
BamBim+nOy. Поиск оптимальных условий синтеза
уменьшения параметра с, что особенно заметно на
оксидов бария-висмута проведен исходя из обла-
обогащенных висмутом оксидах ([Ba]:[Bi] = 4:11-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021
РОЛЬ КИСЛОРОДА В ФОРМИРОВАНИИ ПЕРОВСКИТОПОДОБНЫХ ОКСИДОВ
159
Рис. 2. Зависимость объема элементарной ячейки окси-
дов гомологического ряда BamBim+nOy от соотношения
[Ba]:[Bi], по данным настоящей работы и работы [8].
Все оксиды, за исключением оксида с соотношением
[Ba]:[Bi] = 4:13 (■), получены при p(O2) = 1 кПа.
2:3 (2), 5:8, 3:5 (3), 4:7 (4), 6:11 (5), 1:2 (6), 4:9, 2:5
(7), 3:8, 4:11 и 1:3 [8]. Согласно данным иодоме-
трического титрования, за исключением оксидов
с соотношениями [Ba]:[Bi] = 6:7 и 4:5 (Bi— = 3.01),
во всех остальных оксидах BamBim+nOy, синтези-
рованных при p(O2) = 1 кПа, отсутствует Bi(V)
(Bi
— = 3.00-3.01). Это подтверждается химическими
тест-методами [11, 12]: образцы оксидов BamBim+nOy
с Bi— = 3.00 не окисляют Mn(II) в Mn(VII), Ce(III) в
Ce(IV), а из органических реагентов - метиловый
красный, дифениламин, основание Арнольда. Сле-
довательно, фазы BamBim+nOy представляют собой
оксиды бария-висмута(III) со стехиометрическим
количеством кислорода.
Рис. 1. Картины рентгеновской дифракции изострук-
турных перовскитоподобных оксидов гомологического
Если при p(O2) = 1 кПа наиболее обогащенные
: m = 3, n = 1 (1); m = 2, n = 1 (2); m =
ряда BamBim+nOy
висмутом фазы оксидов BamBim+nOy с соотноше-
3, n = 2 (3); m = 4, n = 3 (4); m = 6, n = 5 (5); m = 1, n =
ниями [Ba]:[Bi] = 3:8, 4:11 и 1:3 формируются в
1 (6); m = 2, n = 3 (7). Oксиды получены при p(O2) = 1
области ликвидус-солидус, то на воздухе [p(O2) =
кПа методом твердофазного синтеза последовательным
отжигом стехиометрических смесей Ba(NO3)2 и Bi2O3,
21 кПа] эти оксиды и близкая по соотношению
начиная от 600°C и окончательно при 880 (1-4), 780 (5,
к [Ba]:[Bi] = 1:3 фаза [Ba]:[Bi] = 4:13 обнаруже-
6) и 750°C (7).
на в субсолидусной области [8]. Эта фаза имеет
4:9). Минимальный объем ромбической ячейки
широкую по температуре область термической
найден для фазы оксидов BamBim+nOy с соотноше-
устойчивсти (20-710°C). Завершает ряд оксидов
нием [Ba]:[Bi] = 2:5 (V = 83.49 Å3) (рис. 1, 7). В этой
BamBim+nOy, формирующихся на воздухе в области
фазе степень ромбического искажения уменьшена
ливидус-солидус, фаза с соотношением [Ba]:[Bi] =
по сравнению с остальными членами ряда, для ко-
2:5.
торых значения объемов находятся в интервале
Таким образом, перовскитоподобные оксиды го-
V = 84.45 ([Ba]:[Bi] = 4:9) - 86.91 Å3 ([Ba]:[Bi] = 6:7).
мологического ряда BamBim+nOy (m = 1-9; n = 0-3,
В области ликвидус-солидус при p(O2) = 1 кПа
5, 7, 9) формируются преимущественно в области
формируются 16 фаз оксида BamBim+nOy с соотно-
ливидус-солидус [8]. Независимо от парциального
шениями [Ba]:[Bi] = 6:7, 4:5, 7:9, 3:4 (рис. 1, 1), 5:7,
давления кислорода [p(O2) = 1 и 21 кПа] образцы,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021
160
БАРКОВСКИЙ
сти при охлаждении образцов до 20°C происходят
окислительно-восстановительные реакции (1)-(5).
(1)
(2)
(3)
(4)
(5)
В интервале температур 20-710°C образуют-
ся продукты окисления ВаВiO3 и Ba4Bi13+3.00O23.5
Рис. 3. Зависимость средней степени окисления висму-
—
Поскольку оксиды BamBim+nOy легко окисляются
та Bi
от температуры закалки Т образцов оксидов бария-
на воздухе, достоверную информацию о фазовом
висмута с соотношениями [Ba]:[Bi] = 1:1 (1), 4:5 (2),
3:4 (3), 2:3 (4), 1:2 (5), 1:3 (6), 4:13 (7), 1:4 (8). Образцы,
составе исследуемых образцов можно получить
за исключением 6-8, расплавлены на воздухе, медлен-
только закалкой в жидком азоте. Закаленные на
но охлаждены до температуры Т и закалены в жидком
воздухе образцы всегда окислены и включают
азоте. Прямые линии - области термической устойчи-
примесные продукты окисления.
вости фаз оксидов BamBim+nOy аналогичного состава.
—
Звездочкой отмечены значения Bi, рассчитанные для
На рис. 3 показан характер изменения Bi— = f(T)
двухфазных смесей ([Ba]:[Bi] = 1:1-4:13).
для образцов оксидов с соотношениями [Ba]:[Bi] =
1:1 (1), 4:5 (2), 3:4 (3), 2:3 (4), 1:2 (5), 1:3 (6), 4:13 (7)
и 1:4 (8) при их охлаждении на воздухе. Для каждой
закаленные от линии ликвидуса, обеднены кисло-
фазы такого же номинального состава показаны
родом и не содержат Bi(V). Можно утверждать,
области их термической устойчивости. Образцы
что в оксидах BamBim+nOy находится незначитель-
оксидов с соотношениями [Ba]:[Bi] = 4:5-1:3 (2-6)
ное количество Bi(V) или он отсутствует.
при температуре ниже области их термической
Область термической устойчивсти оксидов
устойчивости являются двухфазными [8]. Образцы
BamBim+nOy зависит от парциального давления кис-
интенсивно поглощают кислород при 750-900°C
лорода [8]. Фазы оксидов BamBim+nOy, полученные
(4:5), 500-800°C (3:4), 700-800°C (2:3), о чем сви-
при p(O2) = 1 кПа, термодинамически устойчивы в
детельствует возрастание значений Bi— . В отличие
интервале температур от области кристаллизации
от обогащенных барием образцов оксидов с соот-
до 20°C. Охлаждение расплава Ba-Bi-O в преде-
ношениями [Ba]:[Bi] = 1:1-2:3 (1-4), образец с со-
лах области кристаллизации на воздухе сопрово-
отношением [Ba]:[Bi] = 1:2 (рис. 3, 5) поглощает
ждается незначительным поглощением кислорода
незначительное количество кислорода: в охлаж-
при изменении значений Bi— = 3.00-3.06 без разло-
денном до 20°C образце Bi— = 3.19. С увеличением
жения сформировавшихся в расплаве фаз оксидов
доли висмута в образцах способность к поглощению
BamBim+nOy. Область термической устойчивсти по-
кислорода значительно снижается. Оксид с соотно-
следних, как правило, составляет 10-20°C [8]. Как
шением [Ba]:[Bi] = 1:3 практически не поглощает
отмечалось выше, фазы с более широкими диапа-
кислорода (Bi— = 3.06 при 20°C), а оксиды с соотно-
зонами термической устойчивсти формируются на
шениями [Ba]:[Bi] = 4:13 и 1:4 не поглощают кис-
воздухе в субсолидусной области.
лород вообще (рис. 3, 7, 8). Фаза оксида ([Ba]:[Bi] =
Фазы оксидов BamBim+nOy, сформировавшиеся
1:3) при p(O2) = 21 кПа - продукт твердофазных
в расплаве, при охлаждении на воздухе ниже линии
превращений - существует в узком температурном
солидуса окисляются, о чем свидетельствует воз-
интервале температур (710-720°C). Обнаруженный
растание значений Bi— . Продукты окисления - кис-
в образце шихтового оксида ([Ba]:[Bi] = 1:3) при
лорододефицитные фазы оксидов гомологическо-
температуре ниже 700°C сверхстехиометричный
го ряда Ba2nBi3n++1Bi5n+-1O6n-1 (n = 1, 2, ...): ВаВiO2.55,
кислород обусловлен присутствием оксида ВаВiO3,
ВаВiO2.83, ВаВiO2.88, полностью окисленный ВаВiO3
образовавшегося при разложении фазы оксида с со-
[13, 14] и фаза того же ряда оксидов BamBim+nOy,
отношениями [Ba]:[Bi] = 1:3 в соответствии с урав-
обогащенная висмутом. В субсолидусной обла-
нением (5).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021
РОЛЬ КИСЛОРОДА В ФОРМИРОВАНИИ ПЕРОВСКИТОПОДОБНЫХ ОКСИДОВ
161
Поглощение кислорода обогащенными висму-
том образцами оксидов Ba-Bi-O обусловлено окис-
лением кислорододефицитных фаз ВаВiO2.55 →
ВаВiO2.83 → ВаВiO2.88 → ВаВiO3 - продуктов раз-
ложения оксидов BamBim+nOy. В двухфазных об-
разец шихтового состава оксидов с соотношени-
ями [Ba]:[Bi] = 4:5, 3:4, 2:3, 1:2 и 1:3 количество
кислорододефицитных фаз Ba2nBi3n++1Bi5n+-1O6n-1
уменьшается с обогащением фаз висмутом. Доля
поглощенного кислорода уменьшается в этом же
направлении, о чем свидетельствует снижение
значений Bi— (рис. 3). В образцах, полученных из
расплава, как правило, средняя степень окисления
висмута Bi— занижена по сравнению с керамически-
ми образцами (точки с пометкой «А» на рис. 3), что
объясняется более высокой плотностью первых и
образованием корки расплава на поверхности, пре-
пятствующей диффузии кислорода вглубь образца.
Разложение и окисление оксидов BamBim+nOy
с участием кислорододефицитных фаз ВаВiO2.55,
ВаВiO2.83, ВаВiO2.88 и образованием конечного
продукта окисления ВаВiO3 описываются суммар-
Рис. 4. Рентгеновская дифракция граничных оксидов -
ными реакциями (1-5). Например, фаза оксида
моноклинного BaBiO3 (1) и кубического Ba4Bi+3.00O23.5
с соотношением [Ba]:[Bi] = 2:3 формируется из
(3), образующих протяженную по составу (50-
расплава путем протекания последовательных
76.5 мол% BiO1.5) и по температуре (20-710°С) двух-
жидкофазных превращений с участием ВаВiO2.55
фазную область при p(O2) = 21 кПа [8], а также двух-
фазного образца шихтового состава (2) с соотношени-
(1000-1015°С) и оксидов с соотношениями
ем [Ba]:[Bi] = 4:5, полученного на воздухе медленным
[Ba]:[Bi] = 7:8 (990-1000°С), 6:7 (980-990°С), 9:11
охлаждением расплава от 1030 до 20°С.
(965-980°С), 4:5 (945-965°С), 7:9 (925-945°С), 3:4
Рентгенографически идентифицировать гра-
(910-925°С), 5:7 (890-910°С) [8]. Фаза оксида с
ничные фазы в двухфазных областях достаточно
соотношением [Ba]:[Bi] = 2:3 существует в интер-
сложно [15], поскольку рефлексы ВаВiO3 (или кис-
вале температур 875-890°С. Ниже 875°С фазовые
лорододефицитной фазы) и оксида Ba4Bi+3.00O23.5
превращения протекают без участия жидкой фазы.
накладываются, но благодаря разным картинам
Оксид с соотношением [Ba]:[Bi] = 2:3 окисляется
электронной дифракции могут быть обнаружены
до ВаВiO3-x и обогащенных висмутом фаз окси-
[8, 9]. Картины рентгеновской дифракции, пред-
дов BamBim+nOy с соотношениями [Ba]:[Bi] = 5:8
ставленные на рис. 4, - яркое тому подтверждение.
(860-875°С), 7:5 (835-860°С), 4:7 (825-835°С), 6:11
Медленное (2 град/ч) охлаждение расплавленного
(820-835°С), 1:2 (810-920°С), 4:9 (795-810°С), 2:5
шихтового образца оксида BamBim+nOy ([Ba]:[Bi] =
(780-795°С), 3:8 (755-780°С), 4:11 (720-755°С), 1:3
4:5) до 20°С приводит к образованию двухфазной
(710-720°С) и 4:13 (20-710°С). Состав соседствую-
мелкодоменной смеси. По данным рентгеновской
щей с оксидом BamBim+nOy кислорододефицитной
дифракции, этот образец оксида является псевдо-
фазы Ba2nBi3n++1Bi5n+-1O6n-1 в интервале температур
кубическим (рис. 4, 2).
650-875°С требует уточнения. Поскольку оксид
ВаВiO3 начинает терять кислород при ~650-700°С
Результаты настоящей работы позволяют объ-
[14], в образцах, закаленных при 650-875°С, долж-
яснить имеющиеся в литературе немногочислен-
ны присутствовать кислорододефицитные фазы
ные данные о валентном состоянии висмута в ок-
ВаВiO2.97 (n = 15), ВаВiO2.95 (n = 10), ВаВiO2.93 (n = 7),
сидах BamBim+nOy, синтезированных в атмосфере
ВаВiO2.92 (n = 6), ВаВiO2.90 (n = 5) [13].
кислорода. Рассчитанные из экспериментальных
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021
162
БАРКОВСКИЙ
данных [2] значения Bi— , равные 3.42, 3.62 и 3.68
p(O2) >> 101 кПа. Как показано ниже, высокое дав-
соответственно для образцов оксидов с соотно-
ление кислорода не гарантирует значительного по-
шениями [Ba]:[Bi] = 2:3, 3:4 и 4:5, отожженных
вышения доли Bi(V).
при 550°С, не являются характеристикой инди-
Предпринята попытка получения сверхпро-
видуальных фаз. В условиях синтеза при p(O2) =
водящего
«электрондопированного»
оксида
101 кПа и Т = 550°С эти значения Bi— характерны
(Ba0.6Bi0.4)BiO2.92 при высоком давлении кислоро-
для двухфазной смеси, состоящей из BaBiO3 и ок-
да [17] с катионными соотношениями [Ba]:[Bi] =
сида с соотношением [Ba]:[Bi] = 4:11 (Bi— = 3.00)
0.59:1.41, 0.43, 3:7. Доля кислорода (y), по данным
[8]. Расчет средней степени окисления висмута
иодометрического титрования, составила 2.92, Bi— =
для трех шихтовых образцов с соотношениями
3.30 [15% Bi(V)], несмотря на достаточно высокое
[Ba]:[Bi] = 2:3, 3:4 и 4:5 дает значения Bi— = 3.47,
давление кислорода при окончательном отжиге
3.61 и 3.69 соответственно, хорошо согласующи-
[6×107 Па (600 атм), 400°C]. Полученный оксид не
еся (кроме первого) с экспериментально получен-
проявляет сверхпроводящих свойств, кристаллизу-
ными [2]. Доли кислорода и Bi(V) только в одном
ется в кубической структуре перовскита (параметр
из образцов Ba2xBi2(1-x)O3-x (x = 0.262, [Ba]:[Bi] =
не приведен). По всей вероятности, как и в работе
4:11) аномально завышены (Bi— = 3.16). Такая сред-
[2], получена мелкодоменная смесь псевдокубиче-
няя степень окисления висмута характеризует
ских оксидов BamBim+nOy, по данным рентгенов-
двухфазные смеси, обогащенные барием, близкие
ской дифракции.
по катионному составу к оксидам с соотношения-
Таким образом, в индивидуальных перовскито-
ми [Ba]:[Bi] = 4:9 и 1:2.
подобных оксидах BamBim+nOy отсутствует висмут
Данные настоящей работы подтверждают, что
со средней степенью окисления Bi— >3.06. Доля
в области ликвидуса образцы оксидов системы
кислорода в оксидах BamBim+nOy, обусловленная
Ba-Bi-O обеднены кислородом, что хорошо со-
величиной Bi— = 3.00-3.06, может считаться крити-
гласуется с полученными ранее результатами [2].
ческой. В отличие от оксидов BamBim+nOy [8] низ-
Для четырех образцов Ba2xBi2(1-x)O3-x [x = 0.262,
котемпературных фаз, обогащенных кислородом
[Ba]:[Bi] = 4:11; 0.363 (4:7), 0.389 (~5:8), 0.406
и Bi(V), не обнаружено. Большинство оксидов
(2:3)] степени окисления Bi— = 3.01-3.02. В образцах
BamBim+nOy стехиометричны по кислороду и пред-
оксидов, синтезированных на воздухе или в атмос-
ставляют собой оксиды бария-висмута(III). Опи-
фере сухого азота при 850-1000°С [2], находятся
санные в литературе образцы номинальных со-
упорядоченные по катионам оксиды BamBim+nOy
ставов, соответствующих оксидам BamBim+nOy, со
[8]. Низкотемпературный (550°С) окислительный
средней степенью окисления Bi— > 3.06 представля-
отжиг таких образцов приводит к спинодальному
ют собой двухфазные смеси, состоящие из ВаВiO3
распаду оксидов BamBim+nOy с образованием мел-
и кислорододефицитных фаз гомологического
кодоменной смеси псевдокубических фаз (по дан-
ряда Ba2nBi3n++1Bi5n+-1O6n-1 (n = 1, 2, ...): ВаВiO2.55,
ным рентгеновской дифракции [8, 16]).
ВаВiO2.83, ВаВiO2.88 [13, 14] - и соседней фазы
Как показано выше, фаза с соотношением
того же ряда оксидов BamBim+nOy, обогащенной
[Ba]:[Bi] = 1:2 существует в субсолидусной обла-
висмутом. При p(O2) = 21-100 кПа индивидуаль-
сти только при p(O2) = 1 кПа (рис. 1, 6) и не со-
ные оксиды BamBim+nOy, содержащие в значитель-
держит Bi(V) (Bi— = 3.00) в отличие от двухфазной
ном количестве Bi(V) или только Bi(V), не могут
смеси с соотношениями [Ba]:[Bi] = 1:1 и 4:11 та-
быть получены. Вероятно, оксиды BamBim+nOy
кого же валового состава, полученной при p(O2) =
имеют незначительную область гомогенности по
101 кПа, для которой значение Bi— = 3.46 [23%
кислороду, обусловленную смешанно-валентным
Bi(V)] [3]. Oксид Ba(Bi5+O3)2·4H2O [1] не может
состоянием висмута в пределах средней степени
присутствовать на схемах фазовых соотношений
окисления Bi— = 3.00-3.06. Кислород незначитель-
при p(O2) = 1-101 кПа, поскольку независимо от
но растворяется в расплаве Ba-Bi-O, полученном
парциального давления кислорода в обогащенной
в кислородсодержащей атмосфере, поскольку при
висмутом области системы Ba-Bi-O формируются
кристаллизации закалкой можно получить оксиды
фазы, практически не содержащие Bi(V). По всей
с низкой долей Bi(V) (Bi—
= 3.02-3.06). Фазы ок-
вероятности, эта фаза может быть обнаружена при
сидов BamBim+nOy со средней степенью окисления
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021
РОЛЬ КИСЛОРОДА В ФОРМИРОВАНИИ ПЕРОВСКИТОПОДОБНЫХ ОКСИДОВ
163
Bi— = 3.00-3.01 формируются в атмосфере аргона,
СПИСОК ЛИТЕРАТУРЫ
p(O2) =1 кПа, и существуют в интервале темпера-
1.
Von Sholder R., H.Stobbe // Z. anorg. allg. Chem. 1941.
тур от области кристаллизации до комнатной.
Bd 247. H. 4. S. 392. doi 10.1002/zaac.19412470404
2.
Aurivillius B. // Ark. Kemi. Mineral. Geol. (A). 1943.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Bd 16. N 17. P. 1.
3.
Von Sholder R., Ganter K.-W. // Z. anorg. allg.
Однофазные образцы оксидов BamBim+nOy син-
Chem. 1963. Bd 19. H. 5-6. S. 375. doi 10.1002/
тезированы в атмосфере аргона, p(O2) = 1 кПа, при
zaac.19633190518
последовательных отжигах шихты, состоящей из
4.
Nakamura T., Kose S., Sata T. // J. Phys. Soc. Jap. 1971.
Ba(NO3)2 (ХЧ) и оксида Bi2O3 (ОСЧ. 13-3), начиная
Vol. 31. P. 1284. doi 10.1143/JPSJ.31.1284
от 600°C. Образец оксида с соотношением [Ba]:[Bi] =
5.
Takahashi Т., Esaka Т., Iwahara H. // J. Solid State
4:13 получен при p(O2) = 21 кПа. Закаленные об-
Chem. 1976. Vol. 16. P. 317. doi 10.1016/0022-
4596(76)90047-5
разцы оксидов гомогенизировали измельчением
6.
Скориков В.М., Шевчук А.В., Неляпина Н.И. // ЖНХ.
и прессованием после каждого отжига с шагом
1988. Т. 33. № 10. С. 2467.
100 град по 24 ч. Температура окончательного от-
7.
Cox D.E., Sleight A.W. // Acta Crystallogr. (B). 1979.
жига при твердофазном синтезе была ниже темпе-
Vol. 35. N 1. P. 1. doi 10.1107/S0567740879002417
ратуры плавления образца, определенной визуаль-
8.
Клинкова Л.А., Николайчик В.И., Барковский Н.В.,
Федотов В.К. // ЖНХ. 1999. Т. 44. № 12. С. 2081;
но, на ≈100-150°C. В ряде экспериментов образцы
Klinkova L.A., Nikolaichik V.I., Barkovskii N.V., Fedo-
расплавляли при p(O2) = 1 и 21 кПа и медленно
tov V.K. // Russ. J. Inorg. Chem. 1999. Vol. 44. N 12.
(2-20 град/ч) охлаждали до заданной температу-
P. 1974.
ры. Полная характеристика синтезированных ок-
9.
Nikolaichik V.I., Amelinckx S., Klinkova L.A., Barkov-
сидов BamBim+nOy, включая картины электронной
skii N.V., Lebedev O.I., Van Tendeloo G. // J. Solid
State Chem. 2002. Vol. 163. N 1. P. 44. doi 10.1006/
дифракции в просвечивающем электронном ми-
jssc.2001.9362
кроскопе, представлены в работах [8, 9].
10.
Клинкова Л.А., Николайчик В.И., Барковский Н.В.,
В синтезированных образцах методом иодоме-
Федотов В.К. // ЖHХ. 2006. Т. 51. № 7. C. 1201;
трического титрования [15] определяли среднюю
Klinkova L.A., Nikolaichik V.I., Barkovskii N.V., Fedo-
tov V.K. // Russ. J. Inorg. Chem. 2006. Vol. 51. N 7. P.
степень окисления висмута Bi— .
1122. doi 10.1134/ S0036023606070175
Картины рентгеновской дифракции снимали
11.
Барковский Н.В. // Зав. лаб. Диагностика материалов.
при комнатной температуре на установке Siemens
2019. Т. 85. № 8. С. 16. doi 10.26896/1028-6861-2019-
D-500 с излучением CuKα1 и монохроматором. Па-
85-8-16-28
12.
Барковский Н.В. // ЖАХ. 2015. Т. 70. № 11. С. 1171;
раметры ячеек с погрешностью ±0.002 Å рассчи-
Barkovskii N.V. // J. Anal. Chem. 2015. Vol. 70. N 11.
тывали методом профильного анализа.
P. 1346. doi 10.1134/ S1061934815090048
13.
Клинкова Л.А., Николайчик В.И., Барковский Н.В.,
БЛАГОДАРНОСТЬ
Федотов В.К. // ЖНХ. 1997. Т. 42. № 6. С. 905;
Автор выражает глубокую признательность
Klinkova L.A., Nikolaichik V.I., Barkovskii N.V., Fedotov
О.Ф. Шахлевич (Институт физики твердого тела
V.K. // Russ. J. Inorg. Chem. 1997. Vol. 42. N 6. P. 810.
14.
Klinkova L.A., Nikolaichik V.I., Barkovskii N.V., Fedo-
РАН), принявшей участие в выполнении рентгено-
tov V.K. // J. Solid State Chem. 1999. Vol. 146. P. 439.
фазового анализа.
doi 10.1006/ jssc.1999.8390
15.
Барковский Н.В. // ЖOX. 2019. Т. 89. Вып. 2. С. 167.
ФОНДОВАЯ ПОДДЕРЖКА
doi 10.1134/S0044460X1902001X; Barkovskii N.V. //
Работа выполнена в рамках госзадания Инсти-
Russ. J. Gen. Chem. 2019. Vol. 89. N 2. P. 173. doi
тута физики твердого тела РАН (№ 0032-2018-
10.1134/S1070363219020014
16.
Клинкова Л.А., Барковский Н.В., Филатова М.В.,
0005).
Шевченко С.А. // Сверхпроводимость. Физика,
КОНФЛИКТ ИНТЕРЕСОВ
химия, техника. 1992. Т. 5. № 9. С. 1691.
17.
Imai Y., Kato M., Koike Y., Sleight A.W. // Physica
Автор заявляет об отсутствии конфликта
(C). 2003. Vol. 388-389. P. 449. doi 10.1016/S0921-
интересов.
4534(02)02572-8
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021
164
БАРКОВСКИЙ
Role of Oxygen in the Formation of Perovskite-Like Oxides
of Homologous Series BamBim+nOy (m = 1-9; n = 0-3, 5, 7, 9)
N. V. Barkovskii*
State Physics of the Russian Academy of Sciences, Chernogolovka, 142432 Russia
*e-mail: barkov@issp.ac.ru
Received September 18, 2020; revised October 12, 2020; accepted October 17, 2020
The effect of synthesis conditions on the phase composition and valence state of bismuth in perovskite-like ox-
ides of BamBim+nOy (m = 1-9; n = 0-3, 5, 7, 9) homologous series was studied by X-ray diffraction and chemical
analyses. The oxides synthesized at p(O2) = 1 kPa almost do not contain Bi(V), are characterized by an average
—
oxidation number of bismuth Bi
= 3.00-3.01, and, consequently, are stoichiometric in oxygen content. These
phases are thermodynamically stable from the crystallization region to 20°C. Under cooling below the solidus
—
line, BamBim+nOy oxides are oxidized, as shown by an increase of Bi
> 3.06. The final oxidation products at
≈700-20°С are ВаВiO3 and Ba4Bi+3.00O23.5 oxides. Perovskite-like BamBim+nOy oxides with an average oxi-
—
dation number Bi
> 3.06 were not been found. At p(O2) = 21-100 kPa, one cannot obtain individual oxides of
this series which contain a significant amount of Bi(V) or Bi(V) only.
Keywords: homologous series, Ba-Bi-O perovskite-like oxides, valence state, X-ray diffraction patterns,
chemical analysis
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 1 2021