ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 2, с. 283-289
УДК 547.1;546.02;546.62
КВАНТОВО-ХИМИЧЕСКИЙ РАСЧЕТ ГЕОМЕТРИИ
АЛКОКСИ(ГИДРОКСИ)(ЭТИЛАЦЕТОАЦЕТАТ)-
АЛЮМОКСАНА
© 2021 г. Г. И. Щербаковаa, М. К. Шаухинb, А. Д. Кирилинb,
П. А. Стороженкоa, А. С. Похоренкоa,*
a Государственный научно-исследовательский институт химии и технологии элементоорганических соединений,
ш. Энтузиастов 38, Москва, 105118 Россия
b МИРЭА - Российский технологический университет, Институт тонких химических технологий
имени М.В. Ломоносова, Москва, 119454 Россия
*e-mail: anastasiyapohorenko@yandex.ru
Поступило в Редакцию 8 декабря 2020 г.
После доработки 25 декабря 2020 г.
Принято к печати 30 декабря 2020 г.
С использованием методов самосогласованного поля (метод Хартри-Фока) и полуэмпирического PM3 в
программном комплексе HyperChem 6.01 рассчитаны геометрические параметры двух вероятных моле-
кулярных структур аморфного олигомера алкокси(гидрокси)(этилацетоацетат)алюмоксана, приведены
длины связей, валентные углы и результаты квантово-химического расчета полной энергии.
Ключевые слова: олигомерный алкокси(гидрокси)(этилацетоацетат)алюмоксан, молекулярная струк-
тура, квантово-химический расчет
DOI: 10.31857/S0044460X21020128
Синтезированные в Государственном науч-
ских трет-бутилалюмоксанов: [(t-Bu)Al(μ3-O)]8,
но-исследовательском институте химии и техно-
[(t-Bu)2Al{μ-O)Al(t-Bu)2}]2,
[(t-Bu)Al(μ3-О)]6,
логии элементоорганических соединений хела-
[(t-Bu)Al(μ3-O)]7 и др. [7-9]. Их молекулы постро-
тированные алкокси(гидрокси)алюмоксановые
ены из четырехчленных (А12О2) и шестичленных
олигомеры [1-3], в частности алкокси(гидрокси)
(А13О3) циклов со степенью координации атома
(этилацетоацетат)алюмоксаны, могут служить
А1 4, т. е. внутренняя структура трет-бутилалю-
предшественниками высокочистых компонентов
моксанов подобна фрагменту структуры минерала
(связующих, покрытий, порошков и т. п.) для по-
бемита [Al(O)(OH)]n [10]. Отмечалась особая роль
лучения алюмооксидных керамокомпозитов [1-6].
алюмоксанов в качестве универсальных предше-
Развитие представлений о их структуре и молеку-
ственников для создания алюмооксидной керами-
лярной организации может обеспечить проведение
ки [11-16].
синтеза олигомеров с оптимальной структурой.
Проведены рентгенографические исследования
Органоалюмоксановые олигомеры
- слож-
кристаллических карбоксилатов трет-бутилалю-
ные объекты для исследования, в зависимости от
моксанов - продуктов взаимодействия трет-бу-
тилалюмоксанов с бензойной и др. кислотами
способов их получения и природы лигандов они
[17-22].
могут находиться в различных легко циклизую-
щихся и сшивающихся структурных формах [1-3].
В отличие от кристаллических трет-бутила-
Группой американских ученых выполнены рент-
люмоксанов, синтезированные нами алкокси(ги-
генографические исследования ряда кристалличе-
дрокси)(этилацетоацетат)алюмоксановые (RO
=
283
284
ЩЕРБАКОВА и др.
OEt
O
OR
OR
Me
Al
Al
O
OR
Al
HO
O
OH
Al
RO
OH
O
O
O
RO
OR
Al
Al
Al
HO
O
OR
O
O
Al
Al
O
O
OR
RO
O
EtO
Me
OEt
O
Me
Me
OEt
А
Б
Рис. 1. Вероятная структура расчетных фрагментов олигомера гидрокси(этилацетоацетат)(этокси)алюмоксана.
EtO, i-PrO, i-BuO) олигомеры рентгеноаморфны
ждают присутствие структурных фрагментов в
и состоят из молекул, различающихся по составу
полученном аморфном олигомерном гидрокси-
и строению [1-3]. На основании детальных физи-
(этилацетоацетат)(этокси)алюмоксане. В спектрах
ко-химических исследований (1Н, 13С, 27Al ЯМР,
ЯМР 1Н олигомера
[Al(OEt)x[OC(Me)=CHC(O)
ИК спектроскопия, масс-спектрометрия, ГПХ,
OEt]y(OH)zOq]m наблюдаются сигналы метильных
криоскопия, ТГА, элементный анализ) была пред-
протонов этоксигрупп при 0.5-1.5 м. д., метиль-
ложена вероятная схема образования таких оли-
ных групп при 1.7-2.0 м. д., метиленовых групп
гомеров [1], рассчитаны более 100 эмпирических
при 3.2-4.5 м. д., протонов в группах СН= при
формул для возможных олигомерных молекул и
4.8-5.1 м. д. В спектрах ЯМР 13C присутствуют
представлено их вероятное строение [2].
сигналы атомов углерода при 14-20 (СН3СН2),
Современные компьютерные методы расчета
24-26 (СН3С=), 55-60 (ОСН2), 172-175 (СОО) и
неэмпирической и полуэмпирической квантовой
184-189 (С=О) м. д. В спектрах ЯМР 27Al концен-
химии позволяют с высокой вероятностью пред-
трированных и разбавленных растворов олигоме-
сказать строение соединений и определить термо-
ра обнаружены сигналы при 55.0-80.0, 30.0-45.0
динамически стабильные молекулярные структу-
и 0.0-10 м. д., принадлежащие атомам алюминия с
ры [23-25].
координацией 4, 5, 6 соответственно.
Моделирование геометрии и квантово-химиче-
В ИК спектрах олигомера наблюдаются поло-
ский расчет полной энергии подобных олигомер-
сы (см-1): 615, 660 ν(Al-О6), 861 ν(Al-О-Al), 981
ных молекул ранее не проводились, поэтому были
ν(Al-О4), 1021, 1066 ν(Al-О-С), 785, 1118, 1177,
выбраны наиболее простые олигомерные фраг-
1308, 1372, 1390, 1422 δ{СН, C(CH3)} и ν(С-О),
менты (рис. 1) [2, 3], из которых состоит олиго-
1533 ν(С=С), 1635 ν(С=О, координационно связан-
мер, полученный в результате последовательного
ная с атомом Al), 2925, 2976 ν(С-Н), 3374 ν(-ОH).
гидролиза и алкоголиза диэтил(этокси)алюминия
Данные элементного и термогравиметрическо-
в присутствии енольной формы ацетоуксусного
го анализов олигомера [Al(OEt)x[OC(Me)=CHC(O)
эфира (ROH) (схема 1).
OEt]y(OH)zOq]m хорошо совпадают с усредненным
Результаты спектроскопических исследований
значением по элементному составу для выбран-
(1Н, 13С, 27Al ЯМР и ИК спектроскопия) подтвер-
ных нами олигомерных фрагментов А, Б (рис. 1,
Схема 1.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 2 2021
КВАНТОВО-ХИМИЧЕСКИЙ Р
АСЧЕТ
285
А
Б
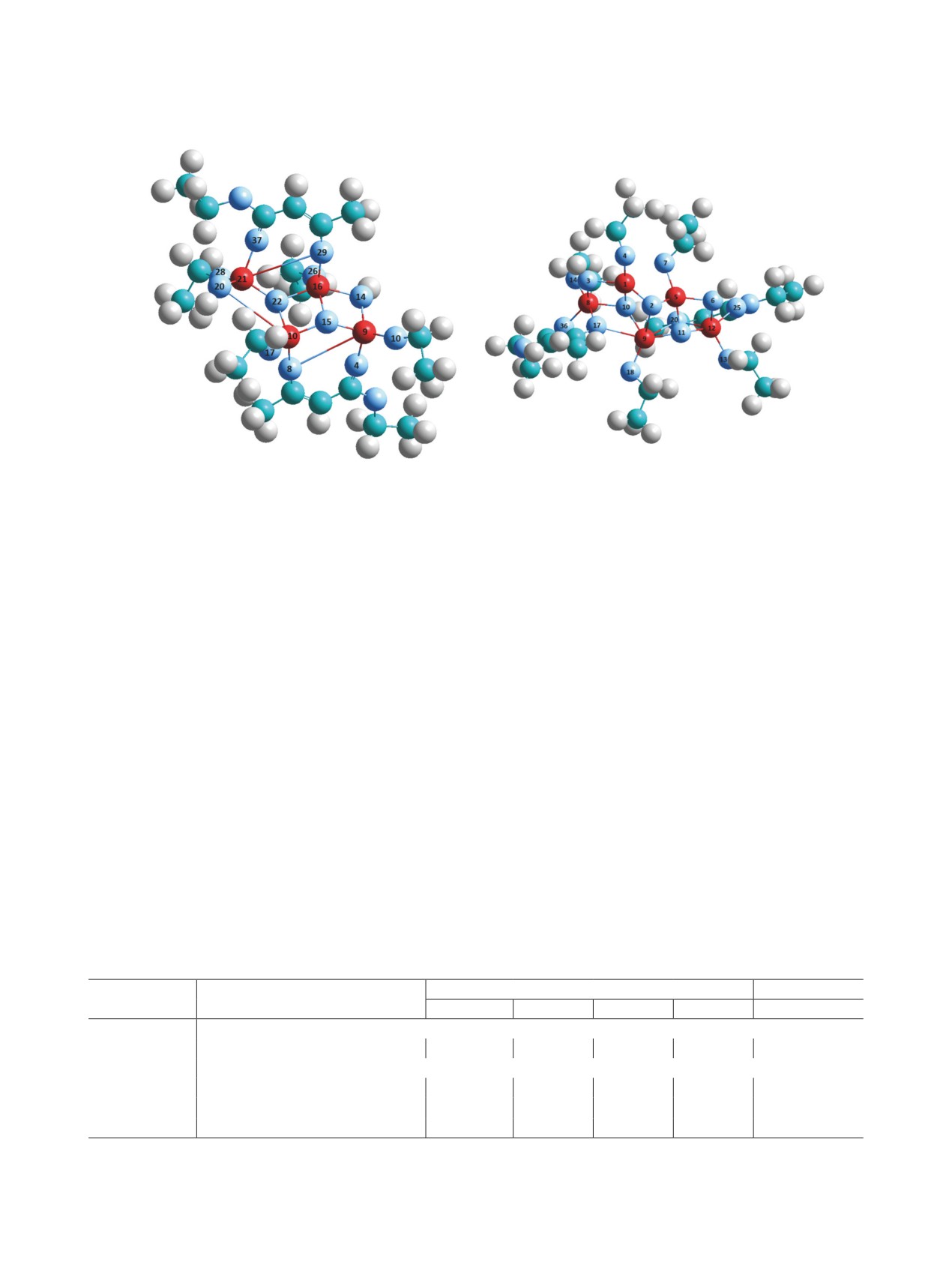
Рис. 2. Молекулярная структура основных олигомерных фрагментов гидрокси(этилацетоацетат)(этокси)алюмоксана: А -
C20H40Al4O14 (Al - №№ 9, 10, 16, 21; O - атомы, обозначенные остальными номерами), Б - C22H45Al5O16 (Al - №№ 1, 5, 8,
9, 12; O - остальные номера).
табл. 1). Рассчитанная молекулярная структура
(STO-3G, 3-21G, 6-31G* и 6-31G**). Выбор базиса
двух фрагментов аморфного олигомера представ-
3-21G обусловлен тем, что базис STO-3G не смог
лена на рис. 2.
бы адекватно описать структуру с множествен-
Моделирование геометрии двух молекулярных
ными координационными связями в молекуле
(рис. 1), а базисы 6-31G* и 6-31G** потребовали
структур аморфного олигомерного гидрокси(эти-
бы значительных вычислительных ресурсов.
лацетоацетат)(этокси)алюмоксана проводили с ис-
пользованием методов самосогласованного поля
В ранее опубликованных работах [10, 27] было
(метод Хартри-Фока) и полуэмпирического PM3 в
показано, что базис 3-21G дает хорошее описание
программном комплексе HyperChem 6.01 [26].
геометрии (длин связей Al-O и углов AlOС, AlOAl)
алкоксидов алюминия, карбоксилатов алюмокса-
Поиск оптимальных структур - расчеты основ-
нов и др., а использование более крупного базис-
ных структурных параметров молекул (длины свя-
ного набора 6-31G* не приводит к значительному
зи и валентные углы) (табл. 2, 3), расчет полной
изменению предсказанной геометрии [27].
энергии (табл. 4) двух вероятных молекул олиго-
мера проводили в первом приближении с примене-
Таким образом, нами осуществлена визуа-
нием валентно расщепленного базиса 3-21G, вхо-
лизация двух ранее предложенных [2, 3] олиго-
дящего в стандартный набор базисов HyperChem
мерных фрагментов гидрокси(этилацетоацетат)-
Таблица 1. Результаты элементного и термогравиметрического анализов олигомера гидрокси(этилацетоацетат)
(этокси)алюмоксана и эмпирические формулы основных олигомерных фрагментов А, < (1:1)
Химический состав, мас%
с, мас% (ТГА)
Фрагмент
Формула
С
Н
Al
OH
Al2О3
Найдено
[Al(OEt)x(OR)y(OH)zOq]m
38.08
6.78
18.52
6.20
35.09
Вычислено
A
C20H40O14Al4
39.22
6.54
17.65
5.56
33.33
Б
C22H45O16Al5
37.71
6.43
19.29
4.86
36.43
Усредненное значение
38.47
6.49
18.47
5.21
34.89
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 2 2021
286
ЩЕРБАКОВА и др.
Таблица 2. Основные рассчитанные длины связей Al-O и валентные углы в молекуле C20H40Al4O14 (А)
Длина связи, Å
Валентный угол, град
Связь
3-21G
PM3
Угол
3-21G
PM3
Al9-O4а
1.765
1.833
O8Al9O15
49.2
50.9
Al9-O8
3.523
2.558
O8Al9O11
136.9
139.2
Al9-O11
1.661
1.772
Al9O15Al10
140.6
141.5
Al9-O14а
1.772
1.809
Al16O14Al9
98.0
96.1
Al9-O15
1.730
1.777
O15Al10O17
124.5
121.4
Al10-O8а
1.764
1.874
C6O8Al9
111.1
122.9
Al10-O15
1.739
1.823
O15Al10O20
122.2
111.4
Al10-O17
1.682
1.771
O17Al10O20
70.3
123.5
Al10-O20
3.640
1.802
O11Al9O15
125.6
117.2
Al10-O22а
1.764
2.470
O17Al10O22
120.3
133.1
Al16-O14
1.930
1.884
O29Al21O22
52.3
74.8
Al16-O15а
1.885
1.837
O26Al16O15
139.9
134.9
Al16-O22
1.874
1.765
O29Al21O23
130.0
123.9
Al16-O26
1.737
1.786
O26Al16O14
86.2
86.9
Al16-O29а
1.762
2.592
CO29Al21
109.9
112.1
Al21-O20а
1.729
2.502
Al10O20Al21
62.3
121.3
Al21-O22
1.742
1.746
O23Al21O22
115.6
139.7
Al21-O23
1.688
1.771
Al21O22Al16
126.6
123.8
Al21-O29
3.600
1.832
O22Al16O26
99.9
134.0
Al21-O37а
1.787
1.851
O22Al16O14
147.4
131.8
Таблица 3. Основные рассчитанные длины связей Al-O и валентные углы в молекуле C22H45Al5O16 (Б)
Длина связи, Å
Валентный угол, град
Связь
3-21G
PM3
Угол
3-21G
PM3
Al1-O4
1.673
1.783
O4Al1O3
113.2
94.3
Al1-O2
1.700
1.781
O3Al1O10
81.9
85.4
Al1-O3
1.822
1.853
O10Al1O2
104.5
80.4
Al1-O10а
1.790
1.888
O2Al1O4
121.3
105.8
Al5-O2
1.700
1.781
O7Al5O6
113.2
111.4
Al5-O6
1.823
1.846
O6Al5O11
82.0
74.9
Al5-O7
1.673
1.790
O11Al5O2
105.1
91.2
Al5-O11а
1.793
1.803
O11Al5O7
118.6
153.2
Al8-O3а
1.822
1.822
O10Al8O3
80.6
86.9
Al8-O10
1.838
1.867
O17Al8O10
78.4
67.3
Al8-O14
1.704
1.792
O36Al8O17
85.3
96.6
Al8-O17
1.905
1.873
O36Al8O14
97.2
83.5
Al8-O36а
1.878
1.863
O36Al8O3
90.1
137.3
Al9-O2а
3.313
2.363
O17Al9O10
77.7
53.3
Al9-O10а
1.759
1.830
O17Al9O18
95.8
83.6
Al9-O11
1.764
1.796
O18Al9O20
93.5
117.6
Al9-O17
2.001
2.564
O20Al9O2
85.4
102.1
Al9-O18
1.732
1.766
O20Al9O11
78.0
49.9
Al9-O20а
1.969
2.612
O11Al9O10
113.2
111.1
Al12-O6а
1.820
1.836
O20Al12O11
78.1
65.5
Al12-O11
1.841
1.839
O11Al12O6
80.8
74.2
Al12-O13
1.708
1.787
O6Al12O25
91.0
89.1
Al12-O20
1.897
1.862
O25Al12O13
96.0
92.7
Al12-O25а
1.876
1.888
O25Al12O20
85.2
104.3
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 2 2021
КВАНТОВО-ХИМИЧЕСКИЙ Р
АСЧЕТ
287
Таблица 4. Полные энергии молекул А и Б (ат. ед.), рассчитанные методом Хартри-Фока в стандартных базисах
Базис
C20H40Al4O14 (А)
C22H45Al5O16 (Б)
STO-3G
-2624.279
-2683.271
3-21G
-2782.189
-3250.114
6-31G*
-2797.227
-2808.810
6-31G**
-2797.305
-3267.730
(этокси)алюмоксана. Рассчитаны длины связей и
Varfolomeev M.S., Kuznetsova M.G., Polyakova M.V.,
валентные углы для двух вероятных молекуляр-
Trokhachenkova O. P. // Inorg. Mater. 2007. Vol. 43.
N 3. P. 320. doi 10.1134/s002016850703020x
ных структур аморфного олигомера и проведен
2.
Щербакова Г.И. Автореф. дис
докт. хим. наук.
квантово-химический расчет полной энергии из-
Москва, 2009. 50 с.
бранных молекулярных структур.
3.
Щербакова Г.И., Стороженко П.А., Жигалов Д.В.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Варфоломеев М.С., Блохина М.Х., Кутинова Н.Б. //
Изв. АН. Сер. хим. 2020. Т. 69. № 5. С. 875;
ИК спектры олигомера
[Al(OEt)x[OC(Me)=
Shcherbakova G.I., Storozhenko P.A., Zhigalov D.V.,
CHC(O)OEt]y(OH)zOq]m регистрировали на при-
Varfolomeev M.S., Blokhina M.Kh., Kutinova N.B. //
боре Nicolet iS50R в интервале 400-4000 см-1 с
Russ. Chem. Bull. 2020. Vol. 69. N 5. P. 875. doi
помощью универсальной приставки однократно-
10.1007/s11172-020-2844-1
го НПВО Smart iTR (кристалл - алмаз). Спектры
4.
Абакумов Г.А., Пискунов А.В., Черкасов В.К.,
ЯМР на ядрах 1Н, 13С, 27Al измеряли для растворов
Федюшкин И.Л., Анаников В.П., Еремин Д.Б.,
в дейтерохлороформе (CDCl3) на спектрометре
Гордеев Е.Г., Белецкая И.П., Аверин А.Д., Бочка-
рев М.Н., Трифонов А.А., Джемилев У. М., Дьяко-
ЯМР AVANCE-600 Bruker (600.13 МГц, внешний
нов В.А., Егоров М.П., Верещагин А.Н., Сыроеш-
эталон - [Al(H2O)6]+). Алюминий определяли три-
кин М.А, Жуйков В.В., Музафаров А.М., Аниси-
лонометрическим методом, углерод и водород -
мов А.А., Арзуманян А.В., Кононевич Ю.Н., Тем-
гравиметрическим методом, сжигая навески в токе
ников М.Н., Синяшин О.Г., Будникова Ю.Г., Бури-
кислорода на газоанализаторе Eurovector EA3000.
лов А.Р., Карасик А.А., Миронов В.Ф, Сторожен-
Количество гидроксильных групп определяли
ко П.А., Щербакова Г.И., Трофимов Б.А., Амосо-
газометрическим методом. Термогравиметриче-
ва С.В., Гусарова Н.К., Потапов В.А., Шур В.Б.,
ский анализ (ТГА) олигомера [Al(OEt)x[OC(Me)=
Бурлаков В.В., Богданов В.С., Андреев М.В. // Усп.
CHC(O)OEt]y(OH)zOq]m проводили на приборе
хим. 2018. Т. 87. С. 393; Abakumov G.A., Pisku-
TGA/SDTA 851 Mettler Toledo со скоростью нагре-
nov A.V., Cherkasov V.K., Fedushkin I.L., Anani-
kov V.P., Eremin D.B., Gordeev E.G., Beletskaya I.P.,
ва 10 град/мин до 1100°C в атмосфере воздуха.
Averin A.D., Bochkarev M.N., Trifonov A.A., Dzhemi-
ФОНДОВАЯ ПОДДЕРЖКА
lev U.M., Dyakonov V.A., Egorov M.P., Vereshcha-
gin A.N., Syroeshkin M.A., Zhuikov V.V., Muzafa-
Работа выполнена при финансовой поддержке
rov A.M., Anisimov A.A., Arzumanyan A.V., Konone-
Государственного научно-исследовательского ин-
vich Yu.N., Temnikov M.N., Sinyashin O.G., Budniko-
ститута химии и технологии элементоорганиче-
va Yu.H, Burilov A.R., Karasik A.A., Mironov V.F.,
ских соединений.
Storozhenko P.A., Shcherbakova G.I., Trofimov B.A.,
Amosova S.V., Gusarova N.K., Potapov V.A., Shur V.B.,
КОНФЛИКТ ИНТЕРЕСОВ
Burlakov V.V., Bogdanov V.S., Andreev M.V. // Russ.
Авторы заявляют об отсутствии конфликта
Chem. Rev. 2018. Vol. 87. N 5. P. 393. doi 10.1070/
интересов.
RCR4795
5.
Варфоломеев М.С., Моисеев В.С., Щербакова Г.И.,
СПИСОК ЛИТЕРАТУРЫ
Стороженко П.А., Шатунов В.В. // Неорг. матер.
1. Стороженко П.А., Щербакова Г.И., Цирлин
2015. Т.
51.
№ 1. С. 86. doi
10.7868/
А.М. Муркина А. С., Варфоломеев М. С., Кузне-
S0002337X15010200; Varfolomeev M.S., Moiseev V.S.,
цова М. Г., Полякова М. В., Трохаченкова О. П. //
Shcherbakova G.I., Storozhenko P.A., Shatunov V.V. //
Неорг. матер. 2007. Т. 43. № 3. С. 373; Storozhen-
Inorg. Mater. 2015. Vol. 51. N 1. P. 76. doi 10.1134/
ko P.A., Shcherbakova G.I., Tsirlin A.M., Murkina A.S.,
S0020168515010203
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 2 2021
288
ЩЕРБАКОВА и др.
6.
Баранова Т.Ф., Валиахметов С.А., Гоголев Г.В.,
16.
DeFriend K.A., Wiesner M.R., Barron A.R. // J. Membr.
Шункина Н.И., Варфоломеев М.С., Щербакова Г.И.,
Sci. 2003. Vol. 224. N 1-2. P. 11. doi 10.1016/s0376-
Вартанян Г.А. // Новые огнеупоры. 2016. № 8. С. 3;
7388(03)00344-2
Baranova T.F., Valiakhmetov S.A., Gogolev G.V.,
17.
McMahon C.N., Francis J.A., Bott S.G., Barron A.R. //
Shunkina N.I., Varfolomeev M.S., Shcherbakova G.I.,
J. Chem. Soc. Dalton Trans. 1999. P. 67. doi 10.1039/
Vartanyan G.A. // Refractories Industrial Ceramics.
A806350H
2016. Vol. 57. N 4. P. 3. doi 10.1007/s11148-016-9981-y
18.
Aitken C.L., Barron A.R. // J. Chem. Cryst. 1996.
7.
Mason M.R., Smith J.M., Bott S.G., Barron A.R. // J.
Am. Chem. Soc. 1993. Vol. 115. P. 4971. doi 10.1021/
Vol. 26. P. 293. doi 10.1007/BF01677784
ja00065a005
19.
Barron A.R. // Polyhedron. 1995. Vol. 14. P. 3197. doi
8.
Harlan C.J., Mason M.R., Barron A.R.
/ /
0.1016/0277-5387(95)85006-6
Organometallics. 1994. Vol. 13. P. 2957. doi 10.1021/
20.
Van Poppel L.G., Bott S.G., Barron A.R. // J. Chem. Cryst.
om00020a011
2001. Vol. 31. P. 417. doi 10.1023/A:1015627502327
9.
Landry C.C., Harlan C.J., Bott S.G., Barron A.R. //
21.
Harlan C.J., Bott S.G., Wu B., Lenz R.W., Barron A.R. //
Angew. Chem. Int. Ed. Engl. 1995. Vol. 34. P. 1202. doi
Chem. Commun. 1997. P. 2183. doi 10.1039/A705437H
10.1002/anie.199512011
10.
Bethley C.E., Aitken C.L., Koide Y., Harlan C.J.,
22.
Koide Y., Barron A.R. // Organometallics. 1995. Vol. 14.
Bott S.G., Barron A.R. // Organometallics. 1997. Vol. 16.
P. 4026. doi 10.1021/om00008a060
P. 329. doi 10.1021/om960576q
23.
Цирельсон В.Г. Квантовая химия. Молекулы, моле-
11.
Apblett A.W., Landry C.C., Mason M.R., Barron A.R. //
кулярные системы и твердые тела: учебное пособие
Mat. Res. Soc. Symp. Proc. 1992. Vol. 249. P. 75. doi
для вузов. М.: БИНОМ. Лаборатория знаний, 2014.
10.1557/PROC-249-75
495 с.
12.
Callender R.L., Harlan C.J., Shapiro N.M., Jones C.D.,
24.
Atkins P.W., Friedman R.S. Molecular quantum
Callahan D.L., Wiesner M.R., Cook R., Barron A.R. //
Chem. Mater. 1997. Vol. 9. N 11. P. 2421. doi 10.1021/
mechanics. New York: Oxford University Press Inc.,
cm9703684
2005. 565 p.
13.
Shafi K.V.P.M., Ulman A., Lai J., Yang N.-L., Cui M.-H. //
25.
Соловьев М.Е., Соловьев М.М. Компьютерная химия.
J. Am. Chem. Soc. 2003 Vol. 125. N 14. P. 4010. doi
М.: СОЛОН-Пресс, 2005. С. 303.
10.1021/ja0213625
26.
HyperChem release 6.01 for Windows, Molecular
14.
Vogelson C.T., Koide Y., Cook R., Bott S.G., Ale-
Modeling System, 2000, Hypercube, Inc.
many L.B., Barron A.R. // Chem. Mater. 2000. Vol. 12.
27. Barron A.R., Dobbs K.D., Francl M.M. // J.
P. 795. doi 10.1021/cm990648e
15.
Ji L., Lin J., Tan K.L., Zeng H.C. // Chem. Mater. 2000.
Am. Chem. Soc. 1991. Vol. 113. P.39. doi10.1021/
Vol. 12. N 4. P. 931. doi10.1021/cm990404u
ja00001a007
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 2 2021
КВАНТОВО-ХИМИЧЕСКИЙ Р
АСЧЕТ
289
Quantum-Chemical Calculation
of Alkoxy(hydroxy)(ethyl acetoacetate)alumoxane Geometry
G. I. Shcherbakovaa, M. K. Shaukhinb, A. D. Kirilinb,
P. A. Storozhenkoa, and A. S. Pokhorenkoa,*
a State Research Institute for Chemistry and Technology of Organoelement Compounds, Moscow, 105118 Russia
b MIREA - Russian Technological University, M.V. Lomonosov Institute of Fine Chemical Technology,
Moscow 119454, Russia
*e-mail: anastasiyapohorenko@yandex.ru
Received December 8, 2020; revised December 25, 2020; accepted December 30, 2020
Using self-consistent field methods (Hartree-Fock method) and semiempirical PM3 in the HyperChem 6.01
software package, the geometric parameters of two probable molecular structures of amorphous alkoxy(hy-
droxy)(ethyl acetoacetate)alumoxane were calculated. Bond lengths, valance angles, and the results of quan-
tum-chemical calculations of the total energy for two molecular structures of amorphous alkoxy(hydroxy)(ethyl
acetoacetate)alumoxane were presented.
Keywords: alkoxy(hydroxy)(ethyl acetoacetate)alumoxane oligomer, molecular structure, quantum-chemical
calculation
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 2 2021