ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 3, с. 417-424
УДК 542.61:546.65/66
ЭКСТРАКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ(III)
СМЕСЯМИ НОВЫХ ТРИДЕНТАТНЫХ
КАРБАМОИЛМЕТИЛФОСФИНОКСИДОВ И
1-ФЕНИЛ-3-МЕТИЛ-4-БЕНЗОИЛ-5-ПИРАЗОЛОНА ИЗ
СОЛЯНОКИСЛЫХ РАСТВОРОВ
© 2021 г. А. Н. Турановa, В. К. Карандашевb, В. А. Хвостиковb,
О. И. Артюшинc, Н. А. Бондаренкоd,e,*
a Институт физики твердого тела Российской академии наук, Черноголовка, 142432 Россия
b Институт проблем технологии микроэлектроники и особо чистых материалов Российской академии наук,
Черноголовка, 142432 Россия
c Институт элементоорганических соединений имени А. Н. Несмеянова Российской академии наук,
Москва, 119991 Россия
d Институт химических реактивов и особо чистых химических веществ, Национальный исследовательский центр
«Курчатовский институт», ул. Богородский вал 3, Москва, 107076 Россия
e Национальный исследовательский центр «Курчатовский институт», Москва, 123182 Россия
*e-mail: bond039@mail.ru
Поступило в Редакцию 25 ноября 2020 г.
После доработки 21 декабря 2020 г.
Принято к печати 30 декабря 2020 г.
Изучена экстракция ионов редкоземельных элементов(III) из солянокислых растворов смесями новых
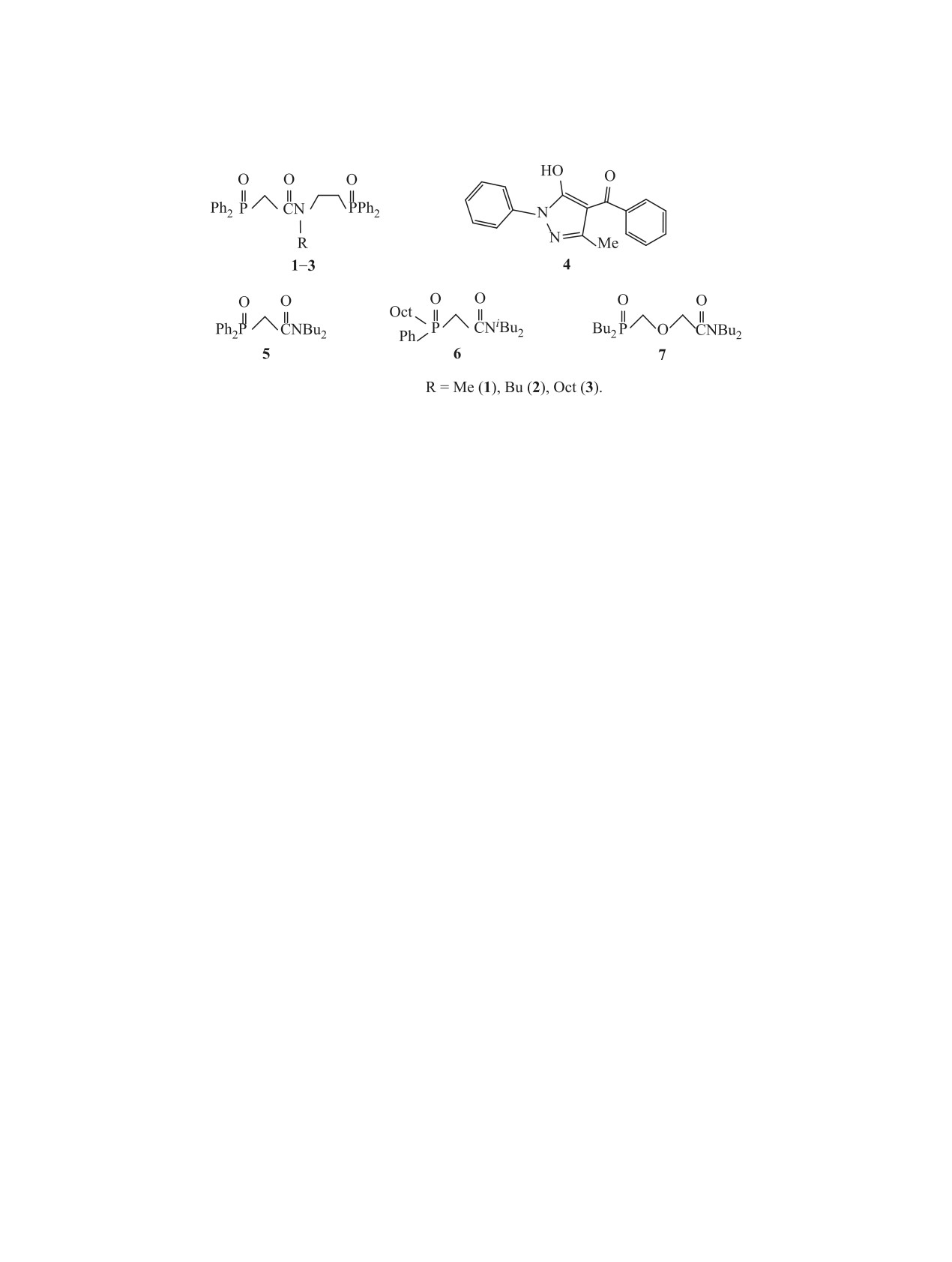
тридентатных карбамоилметилфосфиноксидов общей формулы Ph2P(O)CH2CON(R)CH2CH2P(O)Ph2,
где R = Me, Bu, Oct, содержащих фосфорильную группу в амидной части молекулы, и 1-фенил-3-ме-
тил-4-бензоил-5-пиразолона в органических растворителях. Наблюдаемый значительный синергетиче-
ский эффект связан с образованием в органической фазе гидрофобных смешанно-лигандных комплексов
редкоземельных элементов(III). Определена стехиометрия экстрагируемых комплексов, рассчитаны
константы экстракции. Рассмотрено влияние природы органического растворителя и состава водной
фазы на эффективность извлечения ионов редкоземельных элементов(III) в органическую фазу.
Ключевые слова: карбамоилметилфосфиноксиды, редкоземельные элементы(III), экстракция, синер-
гизм, 1-фенил-3-метил-4-бензоил-5-пиразолон
DOI: 10.31857/S0044460X21030070
В настоящее время при выделении и разделе-
С целью увеличения эффективности экстрак-
нии редкоземельных элементов, а также при их
ции редкоземельных элементов(III) из водных
отделении от актинидов при глубокой переработке
растворов с середины прошлого века широко ис-
отработанного ядерного топлива, экстракционные
следуется и используется эффект синергизма -
технологии являются основными [1, 2]. Высокой
неаддитивное увеличение коэффициентов распре-
экстракционной способностью по отношению к
деления ионов металлов при экстракции ионов
редкоземельным элементам(III) обладают поли-
металлов смесями кислотного и нейтрального экс-
дентатные нейтральные фосфорорганические со-
трагентов в малополярном растворителе [9-11].
единения, среди которых особенно выделяются
Синергетический эффект был обнаружен при экс-
карбамоилметилфосфиноксиды [3-8].
тракции редкоземельных элементов(III) смесями
417
418
ТУРАНОВ и др.
Схема 1.
хелатообразующих кислотных реагентов, таких
что увеличение числа координирующих групп
как β-дикетоны, 4-ацил-5-пиразолоны, 4-ацил-5-и-
Р=О в молекуле приводит к существенному уси-
зоксазолоны, пикролоновая кислота с нейтраль-
лению способности модифицированных карба-
ными донорноактивными экстрагентами (краун-
моилметилфосфиноксидов
1-3 извлекать ионы
эфиры [9], каликсарены [10, 12, 13] монодентат-
редкоземельных элементов(III) из азотнокислых
ные фосфорилсодержащие соединения [14-16],
растворов в сравнении с таковой аналогичных по
а также би- и полидентатные карбамоилметил-
строению бидентатных карбамоилметилфосфи-
фосфиноксиды [15, 17-21]). По данным много-
ноксидов [23].
численных исследований, проявление наблюда-
В настоящей работе представлены результаты
емого синергетического эффекта обусловлено
исследования экстракции ионов редкоземельных
образованием экстрагируемого из органической
элементов(III) из хлоридсодержащих растворов
фазы смешанно-лигандного комплекса редкозе-
смесями тридентатных фосфиноксидов 1-3 [22] и
мельных элементов(III), более гидрофобного, чем
1-фенил-3-метил-4-бензоил-5-пиразолона 4, ранее
комплексы с участием одного из использованных
успешно использованного в смеси с аналогичны-
лигандов [10, 16]. Образованию таких комплексов
ми по строению бидентатными карбамоилметил-
способствует увеличение кислотных свойств хела-
фосфиноксидами 5-7 (схема 1) [21].
тообразующих кислотных реагентов и повышение
Влияние структуры амидов 1-3 на эффектив-
комплексообразующей способности нейтральных
экстрагентов [10]. К усилению синергетическо-
ность синергетической экстракции редкоземель-
го эффекта обычно приводит и увеличение числа
ных элементов(III) смесями этих соединений и
донорноактивных групп в молекуле нейтрального
пиразолона 4 в толуоле рассмотрено путем со-
экстрагента [13, 20].
поставления величины коэффициентов распре-
деления ионов редкоземельных элементов (DLn),
С целью изучения влияния строения карбамо-
найденных в одинаковых экспериментальных
илметилфосфиноксидов на эффективность экс-
условиях. Прежде всего было установлено, что
тракции редкоземельных элементов(III) нами были
редкоземельные элементы(III) практически не
синтезированы тридентатные карбамоилметил-
фосфиноксиды нового типа - дифенил{[N-(2-ди-
экстрагируются 0.03 М. растворами пиразолона 4
фенилфосфинилэтил)-N-алкил]карбамоилметил}-
в толуоле при pH 2 (значения DLn не превышают
фосфиноксиды, амиды дифенилфосфинилуксус-
10-2). Соединения 1-3 также практически не экс-
ной кислоты 1-3, содержащие в амидной части
трагируют редкоземельные элементы(III) в этих
молекулы дополнительную фосфорильную груп-
условиях. Однако при использовании смесей сое-
пу (схема 1) [22]. Изучение экстракции микроко-
динений 1-3 и пиразолона 4 извлечение ионов ред-
личеств U(VI), Th(IV) и редкоземельных элемен-
коземельных элементов(III) в органическую фазу
тов(III) растворами этих экстрагентов показало,
значительно возрастает.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
ЭКСТР
АКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ(III)
419
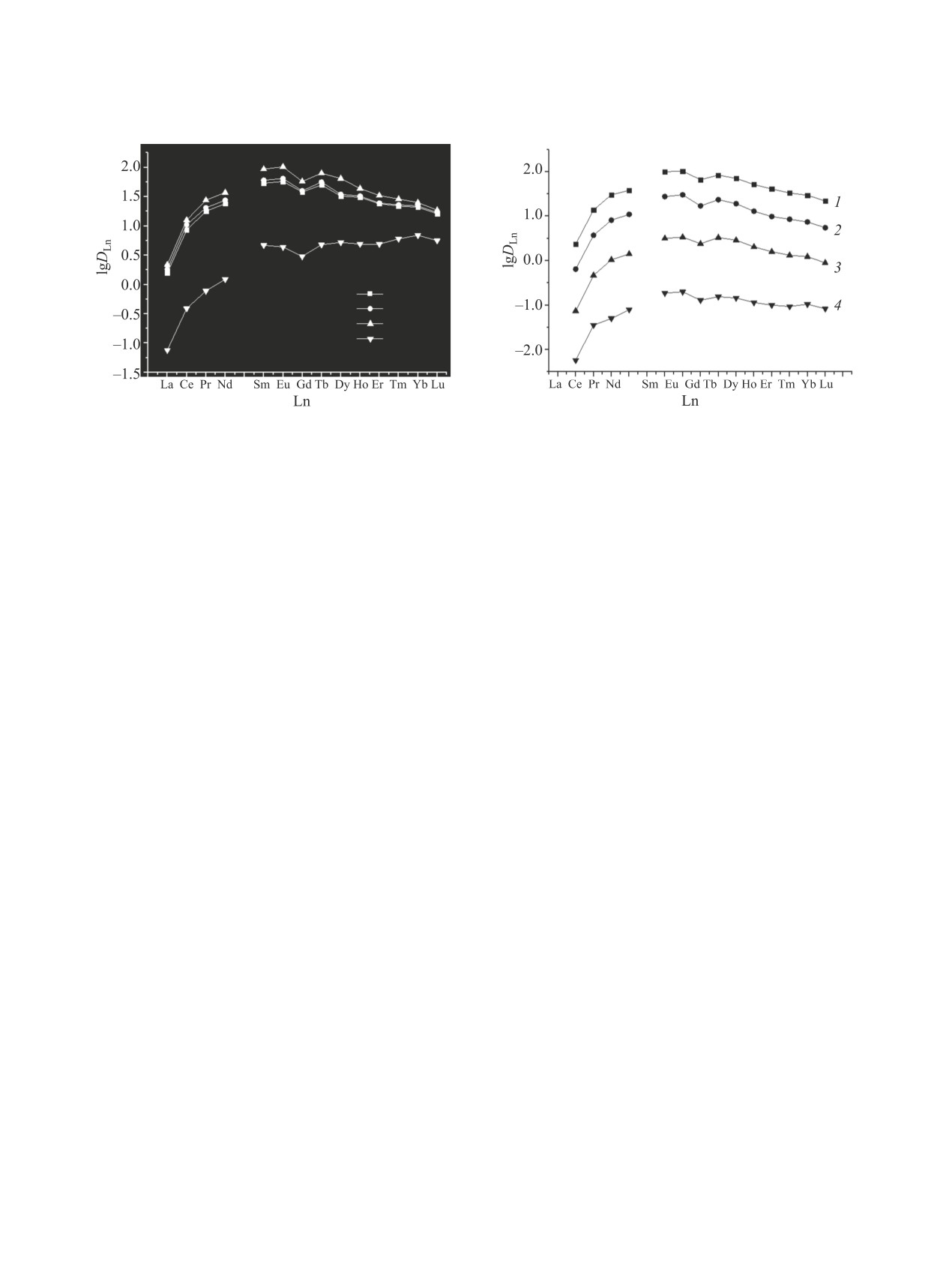
Рис. 1. Зависимость величины lgDLn ионов редкозе-
Рис. 2. Зависимость величины lgDLn ионов редкозе-
мельных элементов(III) при их экстракции 0.03 М.
мельных элементов(III) при их экстракции раствором
растворами пиразолона 4 в толуоле, содержащими
смеси соединений 3 (0.002 моль/л) и 4 (0.02 моль/л) в
0.002 моль/л соединений 1-3 и карбамоилметилфосфин-
CCl4 (1), толуоле (2), дихлорэтане (3) и хлороформе
оксида 5 при рН 2.0.
(4) при рН 2.0.
Тридентатные карбамоилметилфосфиноксиды
тенденция наблюдалась при экстракции смесями
1-3 в смеси с пиразолоном 4 экстрагируют ред-
хелатирующих агентов и монодентатных ней-
коземельные элементы(III) значительно более эф-
тральных экстрагентов типа триалкилфосфи-
фективно, чем бидентатный карбамоилметилфос-
ноксидов Alk3P=O [16, 24]. Значительное сниже-
финоксид 5 (рис. 1), что, по-видимому, связано с
ние эффективности экстракции редкоземельных
участием в комплексообразовании с ионами ред-
элементов(III) при использовании хлороформа
коземельных элементов(III) еще одной электроно-
в качестве растворителя, по-видимому, связано с
донорной группы P=О молекулы.
сольватацией хлороформом фосфорильных и кар-
Различие в эффективности экстракции La(III)
бонильных групп молекулы 3, и поэтому с умень-
и Lu(III) карбамоилметилфосфиноксидами 3 и 5
шением концентрации енольной формы молекулы
DLn(3)/DLn(5) уменьшается от 28.8 до 3.3 соответ-
пиразолона 4 в органической фазе.
ственно по мере уменьшения ионных радиусов
Известно, что редкоземельные элементы(III)
редкоземельных элементов(III). Следует отметить,
экстрагируются растворами пиразолона 4 в инерт-
что длина углеводородной цепочки при атоме азо-
ных органических растворителях в виде пиразо-
та в молекуле соединений 1-3 не оказывает замет-
лонатов (LnP3), сольватированных молекулой 4
ного влияния на эффективность экстракции редко-
[18, 25], в результате реакции (1).
земельных элементов(III) (рис. 1). По-видимому,
Ln 3+(в) + 4 4(o) ↔ LnP34(о) + 3H+(в), KLn,4.
(1)
действие стерических факторов, препятствующих
Здесь символы (в) и (о) относятся к компонентам
комплексообразованию с ионами металлов, ком-
водной и органической фаз соответственно; KLn,4 -
пенсируется увеличением гидрофобности этих
лигандов.
константа экстракции редкоземельных элемен-
тов(III) растворами пиразолона 4.
Существенное влияние на эффективность экс-
тракции редкоземельных элементов(III) смесями
При экстракции редкоземельных элементов(III)
соединений 1-3 и пиразолона 4 оказывает природа
смесью карбамоилметилфосфиноксидов
1-3 и
органического растворителя. Так, при экстракции
пиразолона 4 происходит образованием гидро-
растворами cмеси соединения 3 и пирозолона 4
фобных смешанно-лигандных комплексов редко-
величина DLn возрастает в ряду 1,2-дихлорэтан <
земельных элементов(III) в органической фазе в
толуол < CCl4 по мере снижения полярности ор-
результате вытеснения молекулы пиразолона 4 из
ганических растворителей (рис.
2). Подобная
координационной сферы комплекса LnP3 4.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
420
ТУРАНОВ и др.
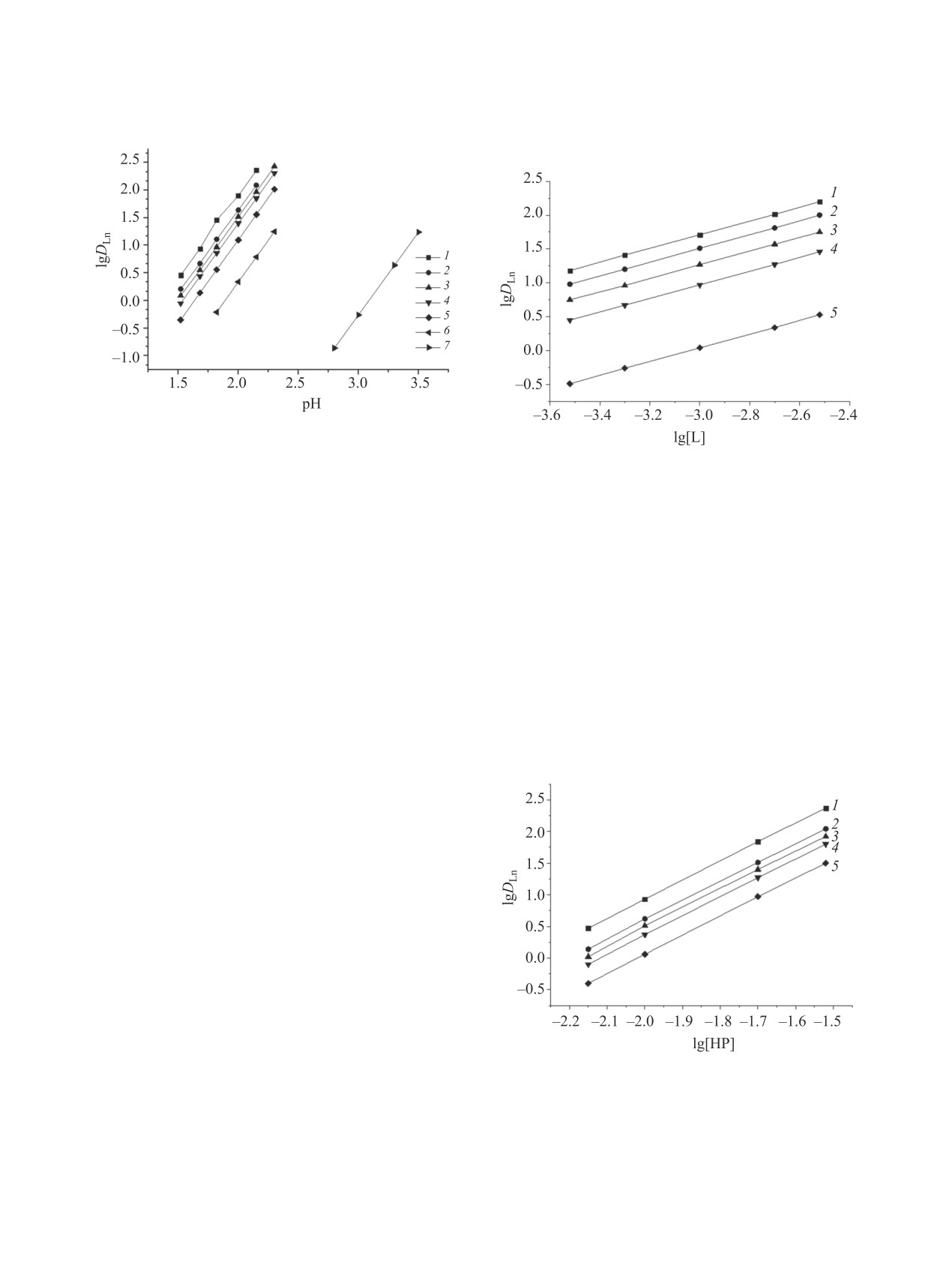
Рис. 3. Зависимость величины коэффициентов рас-
пределения ионов Tb (1, 7), Ho (2), Er (3), Yb (4), Ce
(5) и La (6) при их экстракции раствором 0.03 моль/л
Рис. 4. Зависимость коэффициентов распределения
пиразолона 4 в толуоле (7) и смесью соединений 3
ионов Eu (1), Dy (2), Nd (3), Lu (4) и La (5) от концен-
(0.002 моль/л) и 4 (0.03 моль/л) в толуоле (1-6) от ве-
трации раствора соединения 3 в толуоле, содержащего
личины рН равновесной водной фазы.
0.03 моль/л пиразолона 4, при рН 2.0
Эффективность извлечения редкоземельных
илметилфосфиноксида 6 и пиразолона 4 также
элементов(III) в органическую фазу смесью сое-
отмечено образование комплексов с соотношени-
динения 3 и пиразолона 4 возрастает с увеличени-
ем редкоземельный элемент(III):карбамоилметил-
ем значения рН равновесной водной фазы (рис. 3).
фосфиноксид 6 = 1:1 [18], тогда как при экстракции
При этом тангенс угла наклона зависимости lgDLn
Eu(III) смесью монодентатного триоктилфосфи-
- pH близок к значению 3 для всех редкоземель-
ноксида и пиразолона 4 в хлороформе получено
ных элементов(III), что соответствует переходу
соотношение Eu(III):Oct3P=O = 1:2 [18].
трех ионов H+ в водную фазу в процессе экстрак-
При постоянной концентрации карбамоилме-
ции. Смещение зависимости lgDLn-pH в область
тилфосфиноксида 3 в органической фазе и по-
более высокой кислотности водной фазы при экс-
тракции редкоземельных элементов(III) смесями
карбамоилметилфосфиноксида 3 и пиразолона 4
по сравнению с таковой при экстракции раство-
ром пиразолона 4 указывает на значительный си-
нергетический эффект в системе редкоземельный
элемент(III)-пиразолон 4-лиганд 3.
Для определения стехиометрического соотно-
шения редкоземельный элемент(III)-лиганд 3 в
экстрагируемых комплексах редкоземельных эле-
ментов(III) использовали метод сдвига равнове-
сия. При постоянной концентрации пиразолона 4
в толуоле и постоянном значении рН водной фазы
тангенс угла наклона зависимости lgDLn-lg[L(3)]
близок к значению 1 (рис. 4), что соответствует
Рис. 5. Зависимость коэффициентов распределения
извлечению комплексов с соотношением редко-
ионов Sm (1), Ho (2), Er (3), Yb (4) и Ce (5) от концен-
земельный элемент(III):L = 1:1. При извлечении
трации раствора пиразолона 4 в толуоле, содержащего
смесью октил(фенил)-N,N-диизобутилкарбамо-
0.005 моль/л соединения 3, при рН 2.0.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
ЭКСТР
АКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ(III)
421
Константы равновесия и величины синергетического эффекта в системе редкоземельный элемент(III)-пиразолон 4-
карбамоилметилфосфиноксид 3-толуол
Ln(III)
lg KLn,4 [21]
lg KLn,4,L
lgβ4,L
lgSCa
La
-5.56 ± 0.03
1.61 ± 0.03
7.17 ± 0.06
6.39
Ce
-4.83 ± 0.03
2.37 ± 0.03
7.20 ± 0.06
6.42
Pr
-4.36 ± 0.03
2.71 ± 0.03
7.07 ± 0.06
6.29
Nd
-4.08 ± 0.04
2.84 ± 0.04
6.92 ± 0.08
6.14
Sm
-3.48 ± 0.03
3.24 ± 0.03
6.72 ± 0.06
5.94
Eu
-3.35 ± 0.03
3.28 ± 0.03
6.63 ± 0.06
5.85
Gd
-3.44 ± 0.04
3.03 ± 0.04
6.47 ± 0.08
5.69
Tb
-3.17 ± 0.03
3.17 ± 0.0
6.34 ± 0.03
5.56
Dy
-3.06 ± 0.04
3.08 ± 0.04
6.14 ± 0.04
5.36
Ho
-3.07 ± 0.03
2.91 ± 0.03
5.98 ± 0.06
5.20
Er
-2.94 ± 0.03
2.79 ± 0.03
5.73 ± 0.06
4.95
Tm
-2.67 ± 0.03
2.73 ± 0.03
5.40 ± 0.06
4.63
Yb
-2.43 ± 0.04
2.67 ± 0.04
5.10 ± 0.08
4.32
Lu
-2.46 ± 0.03
2.54 ± 0.03
5.00 ± 0.06
4.22
а [4] = 0.03 моль/л, [3] = 0.005 моль/л, pH 2.0.
стоянной величине рН водной фазы тангенс угла
фазах при экстракции смесями соединений 1-3 и
наклона зависимости lgDLn-lg[4] близок к зна-
пиразолона 4 может быть выражена уравнением
чению 3 (рис. 5), что соответствует извлечению
(5).
комплексов с соотношением редкоземельный эле-
DLn =KLn,4,L[4]3(о)[L](о)[H+]-3(в).
(5)
мент(III):P- = 1:3.
Константы экстракции редкоземельных элемен-
С учетом найденных стехиометрических коэф-
тов(III) смесями карбамоилметилфосфиноксида 3
фициентов межфазное распределение ионов ред-
и пиразолона 4 в толуоле, а также константы обра-
коземельных элементов(III) в процессе их экстрак-
зования смешанно-лигандных комплексов редко-
ции растворами смеси соединений 3 и 4 в толуоле
земельных элементов(III), рассчитанные методом
может быть описано уравнением (2).
наименьших квадратов по уравнениям (5) и (4),
Ln 3+(в) + 3 4(o) + L(o) ↔ LnP3L(о) + 3H+(в), KLn,4,L.
(2)
представлены в таблице. Можно видеть, что значе-
ния KLn,4 и β4,L увеличиваются с ростом атомного
Здесь KLn,4,L - константа экстракции редкоземель-
номера (Z) редкоземельного элемента. Это связано
ных элементов(III) в виде смешанно-лигандных
с увеличением устойчивости комплексов редкозе-
комплексов. Образование таких комплексов в ор-
мельных элементов(III) с жесткими (по Пирсону)
ганической фазе в результате вытеснения молеку-
лигандами по мере увеличения плотности заряда
лы пиразолона 4 из координационной сферы ком-
ионов Ln3+ вследствие уменьшения их ионных ра-
плекса LnP34 может быть описано уравнением (3).
диусов с увеличением Z [26]. Значения KLn,4,L уве-
LnP34(о) + L(o) ↔ LnP3L(о) + 4(o), β4,L.
(3)
личиваются в ряду редкоземельных элементов(III)
Здесь β4,L - константа образования смешанно-ли-
от La(III) до Eu(III), а затем наблюдается немо-
гандных комплексов редкоземельных элемен-
нотонное изменение величин KLn,4,L, связанное с
тов(III). Взаимосвязь KLn,4,L и β4,L выражается
проявлением тетрадного эффекта при экстракции
уравнением (4).
редкоземельных элементов(III) [27, 28]. Такой же
β4,L = KLn,4,L/KLn,4.
(4)
характер зависимости KLn,4,L-Z отмечался при экс-
Зависимость коэффициентов распределения ред-
тракции редкоземельных элементов(III) смесями
коземельных элементов(III) от равновесной кон-
пиразолона 4 с дибутил-(N,N-дибутилкарбамоил-
центрации компонентов в органической и водной
метоксиметил)фосфиноксидом 7 [21].
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
422
ТУРАНОВ и др.
Величина синергетического эффекта SC
(6)
1-Фенил-3-метил-4-бензоил-5-пиразолон мар-
определяется устойчивостью смешанно-лиганд-
ки ХЧ (Вектон) использовали без дополнительной
ных комплексов редкоземельных элементов(III) и
очистки. В качестве органических растворителей
зависит от концентрации карбамоилметилфосфин-
использовали хлороформ, 1,2-дихлорэтан, четы-
оксида 3 и пиразолона 4 в органической фазе (7).
реххлористый углерод и толуол марки ХЧ или
SC = D(DL + D4)-1.
(6)
ЧДА без дополнительной очистки. Растворы экс-
трагентов в органических растворителях готовили
Здесь DL, D4 и D - коэффициенты распределения
по точным навескам.
редкоземельных элементов(III) при экстракции
карбамоилметилфосфиноксидом 3, пиразолоном 4
Исходные водные растворы хлоридов редкозе-
и их смесью соответственно.
мельных элементов готовили растворением соот-
SC = β4,L[4]-1(о)[L](о).
(7)
ветствующих солей в воде с последующим добав-
лением растворов HCl до требуемой концентрации.
При постоянной концентрации соединений 3 и
Постоянную ионную силу полученных растворов
4 в органической фазе величина синергетического
(0.1 М.) поддерживали с помощью NaCl. Концен-
эффекта уменьшается в ряду редкоземельных эле-
трация каждого из редкоземельных элементов(III)
ментов(III) от La(III) к Lu(III) (см. таблицу). Такой
в исходных водных растворах составляла
2
×
же характер зависимости SC-Z отмечался при экс-
10-6 моль/л. Все используемые реактивы соответ-
тракции редкоземельных элементов(III) смесями
ствовали марке ХЧ.
дибутил-(N,N-дибутилкарбамоилметоксиметил)-
фосфиноксида 7 [21] или фосфорилсодержащим
Опыты по экстракции проводили в пробирках
каликс[6]ареном [13] с пиразолоном 4.
с притертыми пробками при температуре 22±1°С
и соотношении объемов органической и водной
Представленные данные показали, что эффек-
фаз 1:1. Контакт фаз осуществляли на роторном
тивность экстракции ионов редкоземельных эле-
аппарате для перемешивания со скоростью враще-
ментов(III) тридентатными карбамоилметилфос-
ния 60 об/мин в течение 1 ч. Предварительно было
финоксидами 1-3 значительно увеличивается в
установлено, что этого времени достаточно для
присутствии
1-фенил-3-метил-4-бензоил-5-пира-
установления постоянных значений DLn.
золона. Обнаруженный синергетический эффект
связан с образованием в органической фазе ги-
Концентрацию редкоземельных элементов(III)
дрофобных смешанно-лигандных комплексов ред-
в исходных и равновесных водных растворах
коземельных элементов(III) состава LnP3L. Вве-
определяли масс-спектральным методом с иони-
дение дополнительной координирующей группы
зацией пробы в индуктивно связанной плазме с
Р=О в амидную часть молекулы нейтрального экс-
использованием масс-спектрометра X-7 (Thermo
тагента приводит к увеличению экстракционной
Electron, США) по ранее описанной методике [30].
способности модифицированных тридентатных
Концентрацию редкоземельных элементов(III) в
карбамоилметилфосфиноксидов 1-3 по сравне-
органической фазе определяли после двукратной
нию с таковой аналогичных по строению биден-
реэкстракции 1 М. раствором HCl. Величины DLn
татных карбамоилметилфосфиноксидов. Анало-
рассчитывали как отношение концентрации редко-
гичное влияние строения фосфорилсодержащего
земельных элементов(III) в равновесных органи-
экстрагента на эффективность синергетической
ческой и водной фазах. Погрешность определения
экстракции было показано в случае использова-
DLn не превышала 5%. Величину pH равновесных
ния бис- [19] и триподандных карбамоилметил-
водных фаз определяли с использованием pH-ме-
фосфиноксидов [19, 20], а также каликсаренов с
тра pH 150 со стеклянным электродом.
Me2P(O)CH2-группами [13].
ФОНДОВАЯ ПОДДЕРЖКА
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Работа выполнена при поддержке Министер-
Синтез дифенил{[N-алкил-N-(2-дифенилфос-
ства науки и высшего образования Российской
финилэтил)]карбамоилметил}фосфиноксидов 1-3
Федерации в рамках государственного задания
[22] и дифенил(N,N-дибутилкарбамоилметил)-
Института физики твердого тела РАН, Института
фосфиноксида 5 [29] описан ранее.
проблем технологии микроэлектроники и особо
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
ЭКСТР
АКЦИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ(III)
423
чистых материалов РАН, Института элементоор-
17.
Rao L., Xia Y., Rapko B.M., Martin P.F. // Solvent
Extr. Ion Exch. 1998. Vol. 16. P. 913. doi
ганических соединений им. А.Н. Несмеянова и
10.1080/07366299808934560
Национального исследовательского центра «Кур-
18.
Santhi P.B., Reddy M.L.P., Ramamohan T.R.,
чатовский институт-ИРЕА».
Damodaran A.D. Mathur J.N., Murali M.S., Iyer R.H. //
Solv. Extr. Ion Exch. 1994. Vol. 12. N 3. P. 633. doi
КОНФЛИКТ ИНТЕРЕСОВ
10.1080/07366299408918229
Авторы заявляют об отсутствии конфликта
19.
Туранов А.Н., Карандашев В.К., Шарова Е.В.,
интересов.
Артюшин О.И., Одинец И.Л. // Радиохимия. 2013.
Т. 55. № 2. С. 156; Turanov A.N., Karandashev V.K.,
СПИСОК ЛИТЕРАТУРЫ
Sharova E.V., Artyushin O.I., Odinets I.L. //
Radiochemistry. 2013. Vol. 55. N 2. P. 203. doi 10.1134/
1.
Михайличенко А.И., Михлин Е.Б., Патрикеев Ю.Б.
S1066362213020100
Редкоземельные металлы. М.: Металлургия, 1987.
20.
Turanov A.N., Matveeva A.G., Kudryantsev I.Yu,
232 с.
Pasechnik M.P, Matveev S.V., Godovikova M.I., Baulina
2.
Ягодин Г.А., Каган С.З., Тарасов В.В. Основы жид-
T.V., Karandashev V.K, Brel V.K. // Polyhedron. 2019.
костной экстракции. М.: Химия, 1981. 400 с.
Vol. 161. P. 276. doi 10.1016/j.poly.2019.01.036
3.
Медведь Т. Я., Чмутова М. К., Нестерова Н. П., Кой-
21.
Turanov A.N., Karandashev V.K., Kharlamov A.V.,
ро О.Э., Кочеткова Н.Е., Мясоедов Б.Ф., Кабачник
Bondarenko N.A. // Solv. Extr. Ion Exch. 2014. Vol. 32.
М.И. // Изв. АН СССР. Сер. хим. 1981. N 9. С. 2121.
N 5. P. 492. doi 10.1080/07366299.2014.908584
4.
Myasoedov B. F., Chmutova M. K., Kochetkova N.
22.
Бондаренко Н.А., Белусь С.К., Артюшин О.И., Пере-
E., Koiro O.E., Pribylova G.A., Nesterova N.P., Med-
гудов А.С. // ЖОХ. 2020. Т. 90. Вып. 12. С 1867. doi
ved T.Y., Kabachnik M.I. // Solvent Extr. Ion Exch. 1986.
10.31857/S004444 60X201200094; Bondarenko N.A.,
Vol. 4. N 1. P. 61.
Belus’ S.K., Artyushin O.I., Peregudov A.S. // Russ. J.
5.
Horwitz E. P., Martin K. A., Diamond H., Kaplan L. //
Gen. Chem. 2020. Vol. 90. N 12. P. 2273. doi 10.1134/
Solvent Extr. Ion Exch. 1986. Vol. 4. N 3. P. 449.
S1070363220120099
6.
Мастрюкова Т.А., Артюшин О.И., Одинец И.Л., Та-
23.
Туранов А.Н., Карандашев В.К., Артюшин О.И.,
нанаев И.Г. // Рос. хим. ж. 2005. Т. 49. № 2. С. 86.
Перегудов А.С., Хвостиков В.А., Бондаренко
7.
Туранов А.Н., Карандашев В.К., Шарова Е.В., Артю-
Н.А. // ЖНХ. 2020. Т. 65. № 6. С. 837. doi 10.31857/
шин О.И., Одинец И.Л. // Цветные металлы. 2012.
S0044457X20060240; Turanov A.N., Karandashev
№ 3. С. 51.
V.K., Artyushin O.I., Peregudov A.S., Khvostikov V.A.,
8.
Turanov A.N., Karandashev V.K., Kharlamov A.V.,
Bondarenko N.A. // Russ. J. Inorg. Chem. 2020. Vol. 65.
Bondarenko N.A., Khvostikov V.A. // Solv. Extr. Ion
Exch.
2019. Vol.
37. N
1. P.
65. doi
N 6. P. 905. doi 10.1134/S0036023620060248
24.
Akiba K., Wada M., Kanno T. // J. Inorg. Nucl. Chem.
10.1080/07366299.2019.1592923
1981. Vol. 43. N 5. P. 1031. doi 10.1016/0022-
9.
Bond A.H., Dietz M.L., Chiarizia R. // Ind. Eng. Chem.
1902(81)80169-8
Res. 2000. Vol. 39. N 10. P. 3442. doi 10.1021/ie000356j
10.
Atanassova M., Kurteva V. // RSC Adv. 2016. Vol. 6. P.
25.
Jordanov V.M., Atanassova M., Dukov I.L. // Sep. Sci.
11303. doi 10.1039/c5ra22306g
Technol. 2002. Vol. 37 N 14. P. 3349. doi 10.1081/SS-
11.
Atanassova M., Kurteva V., Dukov I. // RSC Adv. 2016.
120006166
Vol. 6. P. 81250. doi 10.1039/C6RA18478B
26.
Nash K.L., Jensen M.P. // Sep. Sci. Technol. 2001. Vol.
12.
Tashev E., Atanassova M., Varbanov S., Tosheva T.,
36. N 5-6. P. 1257. doi 10.1081/SS-100103649
Shenkov S., Chauvin A.-S., Dukov I. // Sep. Purif.
27.
Peppard D.F., Mason G.W., Lewey S. // J. Inorg. Nucl.
Technol. 2008. Vol. 64. P. 170. doi 10.1016/j.
Chem. 1969. Vol. 31. N 7. P. 2271. doi 10.1016/0022-
seppur.2008.09.011
1902(69)90044-X
13.
Varbanov S., Tashev E., Vassiliev N., Atanassova M.,
28.
Михайличенко А.И. // Радиохимия. 1975. Т. 17. № 3.
Lachkova V., Tosheva T., Shenkov S., Dukov I.L. //
С. 352; Mikhaylichenko A.I. // Radiochemistry. 1975.
Polyhedron. 2017. Vol. 134. P. 135. doi 10.1016/j.
Vol. 17. N 3. P. 352.
poly.2017.06.013
29.
Туранов А.Н., Карандашев В.К., Харитонов А.В.,
14.
Petrova M.A., Kurteva V.B., Lubenov L.A. // Ind. Eng.
Лежнев А.Н., Сафронова З.В., Яркевич А.Н., Цвет-
Chem. Res. 2011. Vol. 50. P. 12170. doi 10.1021/
ков Е.Н. // ЖОХ. 1999. Т. 69. Вып. 7. С. 1109; Tura-
ie201207n
nov A.N., Karandashev V.K., Kharitonov A.V., Lezh-
15.
Pavithran R., Reddy M.L.P. // Anal. Chim. Acta. 2005.
nev A.N., Safronova Z.V., Yarkevich A.N., Tsvetkov E.N. //
Vol. 536. P. 219. doi 10.1016/j.aca.2004.12.042
Russ. J. Gen. Chem. 1999. Vol. 69. N 7. P. 1068.
16.
Шмидт В.С., Рыбаков К.А., Рубисов В.Н. // Ради-
30.
Туранов А.Н., Карандашев В.К., Баулин В.Е., Цвет-
охимия. 1982. Т. 24. № 1. С. 25; Shmidt V.S., Ryba-
ков Е.А. // ЖНХ. 1995. Т. 40. № 11. С. 1926; Tura-
kov K.A., Rubisov V.N. // Radiochemistry. 1982.
nov A.N., Karandashev V.K., Baulin V.E., Tsvetkov E.N. //
Vol. 24. N 1. P. 25.
Russ. J. Inorg. Chem. 1995. Vol. 40. N 11. P. 1854.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
424
ТУРАНОВ и др.
Extraction of Rare-Earth Elements(III) Ions with Mixtures
of Some Novel Carbamoymethylphosphine Oxides
and 4-Benzoyl-3-methyl-1-phenylpyrazol-5-one
from Hydrochloric Acid Solutions
A. N. Turanova, V. K. Karandashevb, V. A. Khvostikovb,
O. I. Artyushinc, and N. A. Bondarenkod,e,*
a Institute of Solid State Physics, Russian Academy of Sciences, Chernogolovka, 142432 Russia
b Institute of Microelectronics Technology and High Purity Materials, Russian Academy of Sciences, Chernogolovka,
142432 Russia
c A.N. Nesmeyanov Institute of Organoelement Compounds, Russian Academy of Sciences, Moscow,119991 Russia
d Institute of Chemical Reagents and High Purity Chemical Substances of National Research Centre “Kurchatov Institute”,
Moscow, 107076 Russia
e National Research Centre “Kurchatov Institute”, Moscow,123182 Russia
*e-mail: bond039@mail.ru
Received November 25, 2020; revised December 21, 2020; accepted December 30, 2020
The solvent extraction of rare-earth elements(III) ions from hydrochloric acid solutions into an organic phase
with mixtures of 4-benzoyl-3-methyl-1-phenylpyrazol-5-one and novel tridentate carbamoylmethylphosphine
oxides Ph2P(O)CH2CON(R)CH2CH2P(O)Ph2 (R = Me, Bu, Oct) has been studied. The observed significant
synergistic effect is due to the formation of hydrophobic mixed-ligand complexes of rare-earth elements(III)
ions in the organic phase. The stoichiometry of extracted complexes was determined and the equilibrium con-
stants were calculated. The effect of the organic solvent nature and the composition of the aqueous phase on the
extraction efficiency of rare-earth elements(III) ions into the organic phase is considered.
Keywords: tridentate carbamoylmethylphosphine oxides, rare-earth elements(III), synergistic extraction, 4-ben-
zoyl-3-methyl-1-phenylpyrazol-5-one
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021