ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 3, с. 487-492
УДК 546.791.6
СИНТЕЗ, СТРОЕНИЕ И СВОЙСТВА ПОЛИУРАНАТА
ЦЕЗИЯ [Cs2(Н2О)3][(UO2)6O3(OH)8]·2H2O
© 2021 г. О. В. Нипрук*, К. А. Клиньшова, Г. Н. Черноруков,
М. О. Бахметьев, М. Д. Назмутдинов
Нижегородский государственный университет имени Н. И. Лобачевского,
пр. Гагарина 23а, Нижний Новгород, 603950 Россия
*e-mail: nipruk@yandex.ru
Поступило в Редакцию 29 октября 2020 г.
После доработки 10 ноября 2020 г.
Принято к печати 17 ноября 2020 г.
Уранат цезия [Cs2(Н2О)3][(UO2)6O3(OH)8]·2H2O получен при взаимодействии гидратированного оксида
урана(VI) UO3·2.25H2O с водным раствором нитрата цезия в гидротермальных условиях при 100°С в
течение двух недель. Методом химического анализа, ИК спектроскопии, рентгенографии, дифференци-
ально-термического анализа установлен состав и строение полученного соединения, исследованы его
дегидратация и термораспад.
Ключевые слова: гексауранат цезия, рентгенография, ИК спектроскопия, термический анализ
DOI: 10.31857/S0044460X21020136
В природе цезий существует в виде единствен-
[1, 3, 7, 9] - получены методом твердофазного вы-
ного стабильного изотопа с массовым числом 133.
сокотемпературного синтеза в безводном состоянии.
Перечень искусственных радиоактивных изотопов
Большинство технологических схем предпола-
цезия, напротив, весьма широк, их массовые числа
гает разделение урана и продуктов его распада в
находятся в диапазоне от 112 до 151. Среди искус-
водных средах, в которых возможно образование
ственных изотопов радиационно наиболее опасен
соединений урана(VI) и цезия в виде кристалло-
и практически значим изотоп 137Cs с достаточно
гидратов, однако информация о кристаллогидра-
большим периодом полураспада (Т1/2 30.167 лет),
тах уранатов цезия ограничена лишь соединением
с высокой энергией β-частиц (Еβ 1.1, 0.51 МэВ)
Cs3U12O31(OH)13·3H2O [10, 11].
и γ-квантов (Еγ 0.6614 МэВ). Основной источник
В гидротермальных условиях нами по-
получения 137Cs - деление ядер урана (233U, 235U,
лучен неизвестный ранее уранат цезия
238U), поэтому цезий можно считать постоянным
[Cs2(H2O)3][(UO2)6O3(OH)8]·2H2O, изучен его хи-
спутником урана, его доля изменяется от следовых
мический и функциональный состав, установлена
количеств в природном уране до граммовых коли-
роль Н2О в формировании структуры, определены
честв в отработанном ядерном топливе.
рентгенографические и ИК спектроскопические
Существуют различные схемы выделения 137Cs
характеристики. Методом ДТА в сочетании с ме-
из отработанного ядерного топлива. Их эффектив-
тодом высокотемпературной рентгенографии ис-
ность зависит от химической и структурной со-
следованы дегидратация и термораспад ураната
вместимости урана(VI) и цезия и от возможности
цезия, идентифицированы продукты его терморас-
их существования в химически связанном состо-
пада.
янии. Индивидуальные кристаллические соеди-
нения урана(VI) и цезия: CsUO4 [1, 2], Cs2U2O7
По результатам рентгенофлуоресцентного ана-
[2-5], Cs2U4O13 [3, 4], Cs4U5O17 [3, 7, 8], Cs2U7O22
лиза (табл. 1), синтезированное соединение со-
487
488
НИПРУК и др.
Таблица 1. Результаты рентгенофлуоресцентного ана-
вает на слоистую структуру исследуемого соеди-
лиза ураната цезия Cs2U6O19·9H2O (Cs2O·6UO3·9H2O)
нения и на степень окисления урана +6.
Формула оксида
Вычислено, %
Найдено, %
Брутто-формула Cs2U6O19·9H2O (табл. 1) не
Cs2O
13.05
12.88±0.21
дает представления о функциональном составе и
UO3
79.45
79.16±0.83
строении ураната цезия. Для его изучения было
H2O
7.51
7.49±0.08
выполнено ИК-спектроскопическое исследова-
ние. В ИК спектре ураната цезия Cs2U6O19·9H2O
ответствует брутто-формуле Cs2U6O19·9H2O. По
можно выделить несколько условно независимых
соотношению урана и цезия и по содержанию
групп колебаний: колебания уранильного фраг-
молекул Н2О данное соединение отличается от
мента UOδ+, колебания молекул воды различной
известного ураната цезия Cs3U12O31(OH)13·3H2O
степени связанности и колебания гидроксигрупп
[10, 11]. По набору межплоскостных расстоя-
ОН в составе кислородных полиэдров урана UOH.
ний dhkl, по элементному составу соединение
Полоса валентных колебаний νas уранильного
Cs2U6O19·9H2O является формульным и кристал-
фрагмента UOδ+ при 925 см-1 весьма интенсивна
лографическим аналогом исследованных ранее
и, согласно известным корреляциям, соответствует
уранатов MI2U6O19.5·10H2O, где MI = Na, K, Rb
семерной координации уран-кислородных поли-
[12, 13]. В кристаллической фазе (табл. 2) уранат
эдров в структуре ураната цезия. Полоса νs(UOδ+)
цезия Cs2U6O19.5·9H2O в области малых углов 2θ
при 843 см-1 указывает на нелинейную либо не-
содержит интенсивный максимум отражения, что
равноплечную конфигурацию уранильного фраг-
в совокупности с полосами поглощения νas и νs
мента. Правильность отнесения полос νas(UOδ+)
уранильного фрагмента UOδ+ в ИК спектре и с яр-
и νs(UOδ+) подтверждается соотношением νs =
ко-желтой окраской кристаллической фазы указы-
0.912νаs - 1.04 [16].
Таблица 2. Рентгенографические характеристики ураната цезия Cs2U6O19·9H2O
hkl
d
I
hkl
d
I
002
7.505
73
045
2.126
3
101
6.529
4
153
2.087
13
004
3.731
43
323
2.044
32
200
3.597
86
060
2.027
12
130
3.526
30
216
2.009
11
201
3.493
5
244
1.971
29
211
3.359
4
046
1.923
3
104
3.288
4
137
1.820
5
202
3.239
100
401
1.793
18
132
3.188
62
047
1.744
13
220
3.114
3
070
1.739
5
005
2.976
4
350
1.711
5
133
2.875
3
208
1.650
6
213
2.835
3
218
1.635
4
141
2.766
4
336
1.589
5
034
2.739
3
048
1.583
4
204
2.586
34
317
1.577
8
134
2.558
11
360
1.550
3
006
2.482
8
441
1.542
4
026
2.295
4
083
1.454
6
215
2.259
4
076
1.424
3
320
2.234
4
513
1.376
4
242
2.219
5
461
1.342
3
303
2.160
7
284
1.311
6
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
СИНТЕЗ, СТРОЕНИЕ И СВОЙСТВА ПОЛИУР
АНАТА ЦЕЗИЯ
489
Вода в ИК спектре представлена несколькими
видами колебаний, среди которых наиболее ха-
рактерны деформационные колебания δ(Н2О) при
1624 см-1, относящиеся к молекулам воды, сохра-
няющим колебательную индивидуальность. Неко-
торое смещение этой полосы в коротковолновую
область от значения 1595 см-1, характерного для
молекул Н2О в газовой фазе, указывает на участие
молекулярной воды в образовании Н-связей. На
это же указывает форма колебаний νas(HO-H) и
νs(HO-H) в виде широкой интегральной полосы
поглощения в диапазоне 3500-3650 см-1 со слабо-
выраженными максимумами при 3504 и 3611 см-1.
Наряду с колебаниями молекулярной Н2О в спектре
присутствует полоса при 3299 см-1, которая может
быть отнесена к валентным колебаниям ν(UO-H).
К соответствующим деформационным колебани-
ям уран-кислородного фрагмента δ(UOH) можно
отнести полосу при 996 см-1. Такое низкочастот-
ное положение этой полосы обусловлено большой
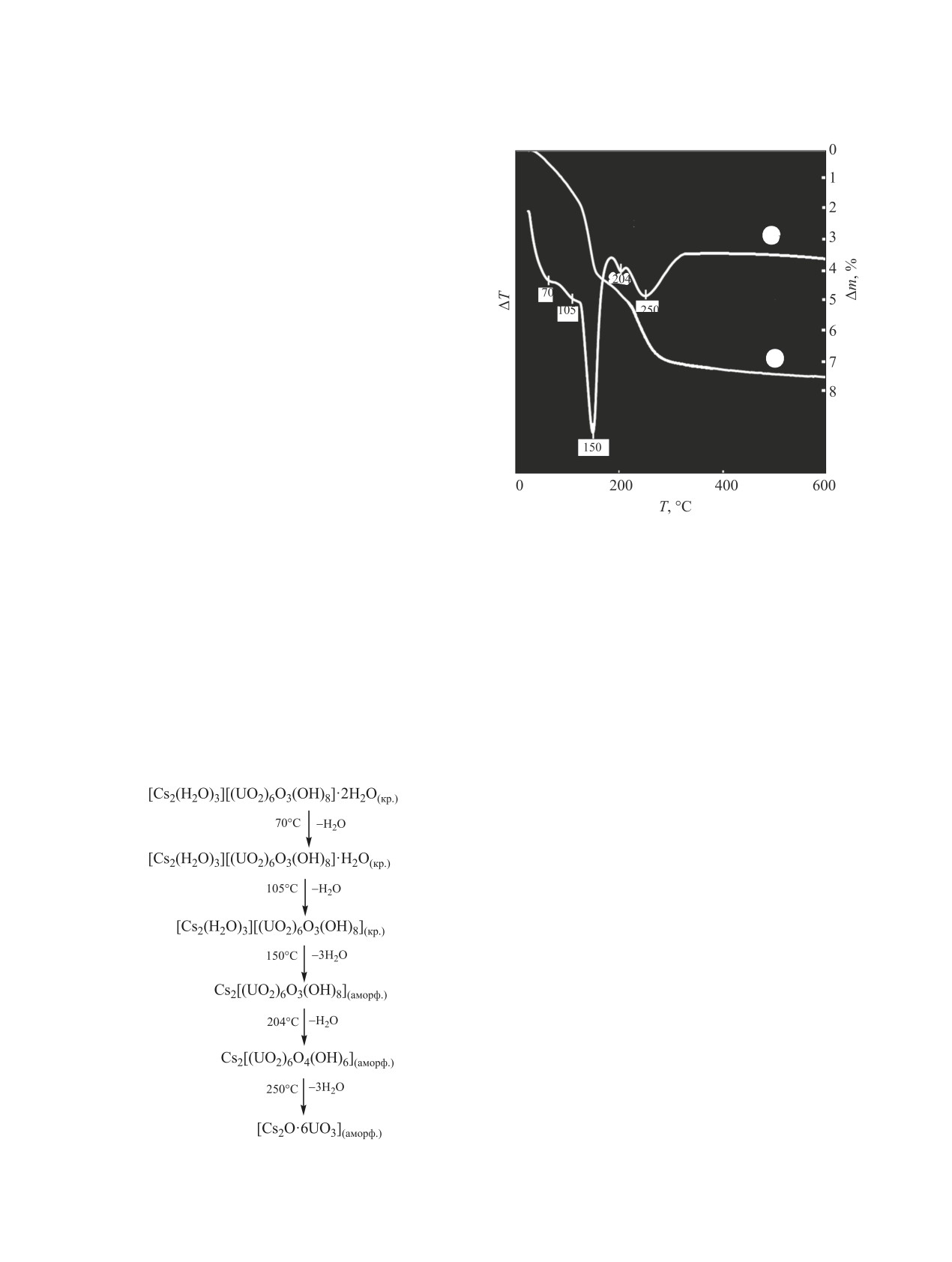
Рис. 1. Термограмма соединения Cs2U6O19·9H2O.
приведенной массой колебательного фрагмента
UOH. Отнесение полос в области 400-680 см-1 к
валентным колебаниям уран-кислородных свя-
Для получения достоверной информации о со-
зей в экваториальной плоскости полиэдра урана
стоянии Н2О и ее роли в формировании структуры
нельзя считать однозначным, поскольку полосы в
ураната цезия, а также для оценки его термической
указанном диапазоне волновых чисел могут быть
устойчивости было проведено термографическое
также обусловлены либрационными колебаниями
исследование в сочетании с методом ИК спектро-
молекул Н2О и колебаниями γ(UOH) [15].
скопии и рентгенографии. Термограмма ураната
цезия Cs2U6O19·9H2O приведена на рис. 1.
Схема 1.
Термическое разложение Cs2U6O19·9H2O про-
текает в несколько стадий (схема 1). Получен-
ные экспериментальные результаты свидетель-
ствуют о том, что молекулы воды в соединении
Cs2U6O19·9H2O не эквивалентны и выполняют
различные функции в формировании его структу-
ры. Первые две из девяти молекул воды удаляются
последовательно при 70 и 105°С.
Это находит отражение в двух небольших эндо-
эффектах на кривой ДТА и подтверждается дан-
ными термогравиметрии. Низкая температура уда-
ления этих молекул воды свидетельствует о том,
что они сохраняют молекулярную индивидуаль-
ность, не занимают самостоятельных кристалло-
графических позиций и удерживаются в структуре
соединения лишь слабыми водородными связями.
Это хорошо согласуется с неизменностью рентге-
нографических характеристик и ИК спектров сое-
динения Cs2U6O19·9H2O при нагревании до 105°С.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
490
НИПРУК и др.
то-формула Cs2U6O19·4H2O должна соответство-
вать соединению Cs2[(UO2)6O3(OH)8], в котором
слои [(UO2)6O3(OH)8]δ- объединены в трехмерную
решетку ионными формами атомов Cs и Н-свя-
зями, образованными гидроксидными группами
противолежащих слоев. Дальнейшее нагревание
фазы Cs2[(UO2)6O3(OH)8] приводит к конденсации
гидроксигрупп (схема 2).
Удаление гидроксигрупп, участвующих в свя-
зывании слоев, приводит к нарушению дальнего
порядка и к полной аморфизации твердой фазы с
образованием сложных оксидов [Cs2O·6UO3]аморф.
(рис. 2, схема 1). Этому процессу соответствуют
последние два эндоэффекта на кривой ДТА при
204 и 250°С. Они сопровождаются убылью массы,
эквивалентной одной и трем молекулам воды соот-
ветственно (схема 1).
Таким образом, синтезированное нами сое-
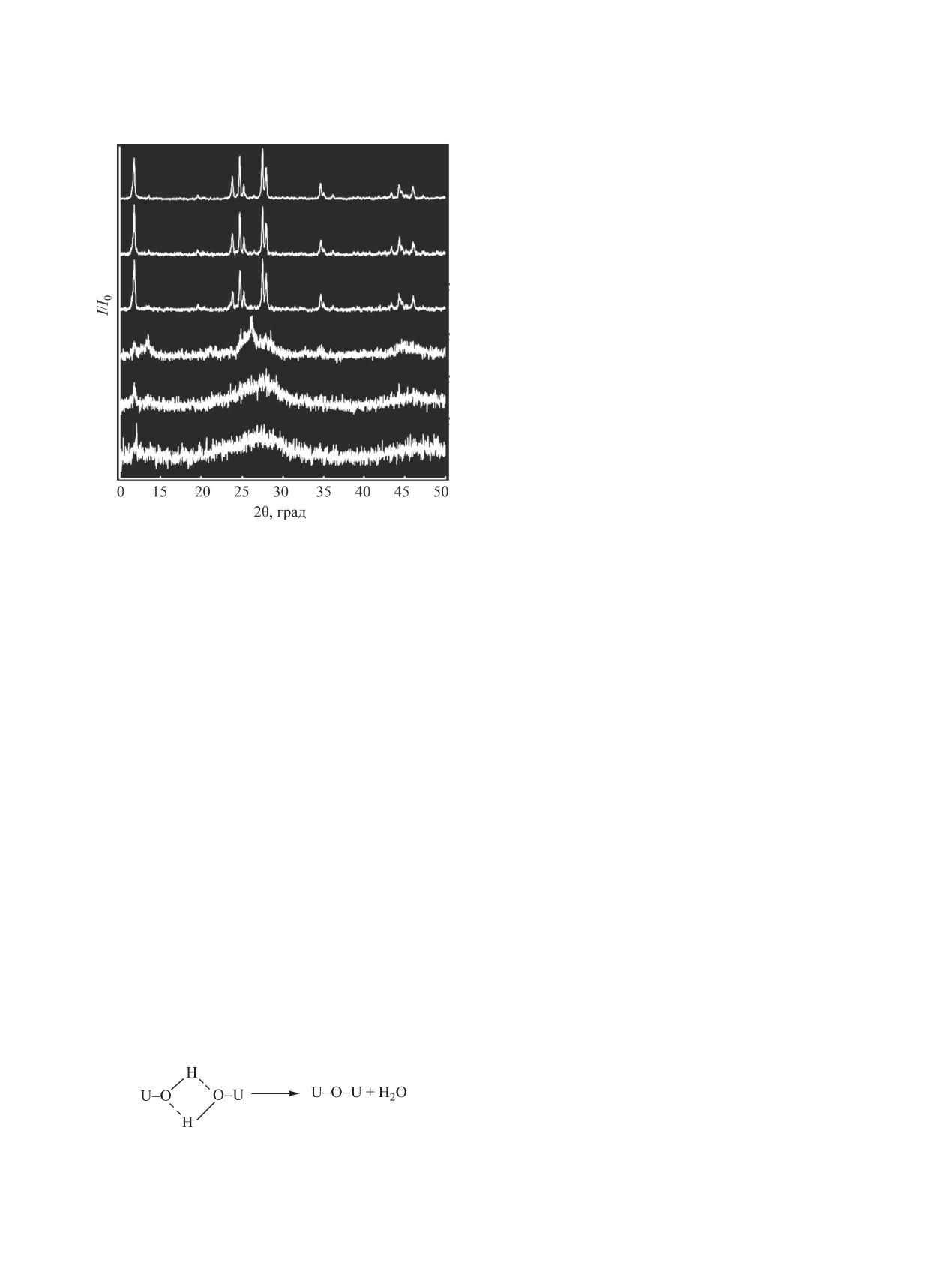
Рис. 2. Рентгенограммы ураната цезия и продуктов его
динение с учетом содержащихся в нем функцио-
дегидратации.
нальных групп представляет собой уранат цезия
Cs2(Н2О)3[(UO2)6O3(OH)8]·2Н2О, его кристалличе-
ская решетка имеет слоистое строение. Катионные
Следующие три молекулы воды удаляются при
формы цезия и молекулы Н2О расположены между
150°С. Их удаление приводит к существенному
слоями [(UO2)6O3(OH)8]δ- и вместе с уран-гидрок-
уширению дифракционных максимумов на рент-
сидными группами осуществляют их связывание.
генограмме и к уменьшению их интенсивности
Вода в уранате цезия Cs2U6O19·9H2O находится в
(рис. 2). Такое изменение рентгенографической
трех различных состояниях. Наиболее легко уда-
картины при нагревании хорошо сформированно-
ляемая Н2О в молекулярной форме сохраняет ко-
го кристаллического соединения Cs2U6O19·9H2O
лебательную индивидуальность и удерживается
указывает на то, что эти три молекулы Н2О входят
в структуре ураната [Cs2(Н2О)3[(UO2)6O3(OH)8]·
в координационное окружение атомов цезия, со-
2Н2О] за счет Н-связей, выполняя функцию ком-
храняя колебательную индивидуальность.
пенсатора заряда слоя. Другая разновидность мо-
В ИК спектре образующейся при 150°С фазы
лекул Н2О также сохраняет колебательную инди-
Cs2U6O19·4H2O исчезают характеристичные
видуальность и удерживается в структуре ураната
для молекулярной Н2О полосы ν(НО-Н) при
[Cs2(Н2О)3[(UO2)6O3(OH)8]·2Н2О] за счет коорди-
3500-3650 см-1 и δ(Н2О) при 1624 см-1, но сохра-
национных связей Cs←OH2, выполняя функцию
няются полосы ν(UО-Н) при 3299 см-1 и δ(UOH)
компенсатора координационной емкости кати-
при 996 см-1. Наблюдаемая трансформация воз-
онных форм цезия. Удаление этих молекул воды
можна, если в соединении Cs2U6O19·4H2O со-
происходит при более высокой температуре и при-
держатся не индивидуальные молекулы Н2О, а
водит к разрушению кристаллической решетки
эквивалентное им количество оксидных (-О-) и
исходного соединения с образованием аморфной
гидроксидных (ОН) групп. В этом случае брут-
фазы Cs2[(UO2)6O3(OH)8]. Последние по темпе-
ратуре удаления 4 молекулы воды входят в состав
Схема 2.
ураната цезия в виде эквивалентного количества
оксидных (-О-) и гидроксидных (ОН) групп, кото-
рые принимают участие в образовании сети водо-
родных связей.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
СИНТЕЗ, СТРОЕНИЕ И СВОЙСТВА ПОЛИУР
АНАТА ЦЕЗИЯ
491
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.
Kim J-G., Jang E., Park Y-S., Ha Y-K. and Song K. //
Asian J. Chem. 2013. Vol. 25. P. 7034. doi 10.14233/
Элементный анализ исследуемого соединения
ajchem.2013.12
проводили на рентгенофлуоресцентном спектро-
3.
Cordfunke E.H.P., Van Egmond A.B. // J. Inorg. Nucl.
метре EDX-900 HS Shimadzu. Массовую долю
Chem. 1975. Vol. 37. P. 1433. doi 10.1016/0022-
воды определяли весовым методом, прокаливая
1902(75)80785-8
исследуемые образцы при 600°С в течение 2 ч.
4.
Morrison G., Read C.M., Smith M.D., zur Loye H.C. //
Кристаллографическую индивидуальность и рент-
CrystEngComm. 2015. Vol. 17. N 9. P. 1968. doi
генографические характеристики образцов опре-
10.1039/c4ce02430c
5.
Van Egmond A.B. // J. Inorg. Nucl. Chem. 1976. Vol. 38.
деляли на дифрактометре XRD-6000 (Shimadzu).
P. 2105. doi 10.1016/0022-1902(76)80477-0
Функциональный состав соединений устанавли-
6.
Ковба Л.М., Ипполитова Е.А., Симанов Ю.П., Спи-
вали по ИК спектрам, полученным на приборе
цын В.И. // ЖФХ. 1961. Т. 35. № 4. С. 719.
FTIR-8400 (Shimadzu). Дегидратацию исследова-
7.
Van Egmond A.B. // J. Inorg. Nucl. Chem. 1976. Vol. 38.
ли методом сканирующей калориметрии на при-
P. 1645. doi 10.1016/0022-1902(76)80652-5
боре Labsys Seteram. Для синтеза использовали
8.
Van den Berghe S., Verwerft M., Laval J.P., Gaudreau B.,
реактивы квалификации ХЧ.
Allen P.G. Van Wyngarden A. // J. Solid State Chem.
Полиуранат
цезия
гидрат
2002. Vol. 66. P. 320. doi 10.1006/jssc.2002.9594
[Cs2(Н2О)3][(UO2)6O3(OH)8]·2H2O. Для синтеза
9.
Van Egmond A.B., Cordfunke E.H.P. // J. Inorg. Nucl.
Chem. 1976. Vol. 38. P. 2245. doi 10.1016/0022-
использовали оксид урана(VI) в форме скупита
1902(76)80203-5
UO3·2.25H2O [16]. Навеску скупита массой 0.5 г
10.
Hill F.C., Burns P.C. // Can. Mineral. 1999. Vol. 37.
и 100 мл 0.5 М. водного раствора нитрата цезия
P. 1283.
при рН 10 (CsOH) помещали в тефлоновую ампу-
11.
Черноруков Н.Г., Нипрук О.В., Кострова Е.Л. //
лу, реакционную смесь нагревали в герметичном
ЖНХ. 2015. Т. 60. № 11. С. 1452. doi 10.7868/
стальном автоклаве при 100°С две недели. Обра-
S0044457X15110021; Chernorukov N.G., Nipruk O.V.,
зовавшийся светло-желтый осадок отфильтровы-
Kostrova E.L. // Russ. J. Inorg. Chem. 2015. Vol. 60.
вали, промывали охлажденной дистиллированной
N 11. P. 1369. doi 10.1134/S0036023615110029
водой и сушили в холодильной камере при 10°С
12.
Нипрук О.В., Черноруков Н.Г., Абражеев Р.В.,
до постоянной массы. Выход >90%. Понижение
Кострова Е.Л. // Неорг. матер. 2017. Т. 53. № 8.
температуры синтеза ниже 100°С, уменьшение рН
С. 829. doi 10.7868/S0002337X17080073; Nipruk O.V.,
Chernorukov N.G., Abrazheev R.V., Kostrova E.L. //
реакционной смеси до 6 и ниже, сокращение про-
Inorg. Mater. 2017. Vol. 53. N 8. P. 816. doi 10.1134/
должительности синтеза приводит к уменьшению
S0020168517080131
выхода продукта реакции. Результаты рентгено-
13.
Нипрук О.В., Черноруков Н.Г., Бахметьев М.О.,
флуоресцентного анализа, соответствующие брут-
Елипашева Е.В., Лелет М.И., Чаплиева К.А. //
то-формуле Cs2U6O19·9H2O, приведены в табл. 1.
ЖОХ. 2019. Т. 89. Вып. 8. С. 1245. doi 10.1134/
ФОНДОВАЯ ПОДДЕРЖКА
S0044460X19080134; Nipruk O.V., Chernorukov N.G.,
Bakhmetiev M.O., Elipasheva E.V., Lelet M.I., Chaplie-
Работа выполнена при финансовой поддержке
va K.A. // Russ. J. Gen. Chem. 2019. Vol. 89. N 8.
Российского научного фонда (проект № 19-73-
P. 1630. doi 10.1134/S1070363219080139
00096).
14.
Bagnall K.W., Wakerley M.W. // J. Inorg. Nucl. Chem.
1975. Vol. 37. P. 329.
КОНФЛИКТ ИНТЕРЕСОВ
15.
Володько М.В., Комяк А.И., Умрейко Д.С. Уранило-
Авторы заявляют об отсутствии конфликта
вые соединения. Минск: БГУ, 1981. Т. 1. 431 с.
интересов.
16.
Нипрук О.В., Князев А.В., Черноруков Г.Н., Пыхо-
ва Ю.П. // Радиохимия. 2011. Т.53. №2. С.128;
СПИСОК ЛИТЕРАТУРЫ
Nipruk O.V., Knyazev A.V., Chernorukov G.N., Pykho-
1. Van Egmond A.B. // J. Inorg. Nucl. Chem. 1976. Vol. 38.
va Y.P. // Radiochemistry. 2011. Vol. 53. N 5. P. 146. doi
P. 1649. doi 10.1016/0022-1902(76)80653-7
10.1134/S1066362211020044
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021
492
НИПРУК и др.
Synthesis, Structure and Properties of Cesium Polyuranate
[Cs2(H2O)3][(UO2)6O3(OH)8]·2H2O
O. V. Nipruk*, K. A. Klinshova, G. N. Chernorukov, M. O. Bakhmetev, and M. D. Nazmutdinov
Lobachevsky State University of Nizhny Novgorod, Nizhny Novgorod, 603950 Russia
*e-mail: nipruk@yandex.ru
Received October 29, 2020; revised November 10, 2020; accepted November 17, 2020
Cesium uranate [Cs2(Н2О)3][(UO2)6O3(OH)8]·2H2O was obtained by reacting hydrated uranium(VI) oxide
UO3·2.25HO with an aqueous solution of cesium nitrate under hydrothermal conditions at 100°С for two weeks.
Composition and structure of the obtained compound was determined by the chemical analysis, IR spectroscopy,
X-ray diffraction, and differential thermal analysis. Its dehydration and thermal decomposition were studied.
Keywords: cesium hexauranate, X-ray diffraction, IR spectroscopy, thermal analysis
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 3 2021