ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 5, с. 659-664
УДК 544.344.3
ДИМЕРИЗАЦИЯ ФТАЛАТ-ИОНА В НЕВОДНЫХ
РАСТВОРИТЕЛЯХ
© 2021 г. В. Г. Носов, К. А. Подрядрова, М. С. Васильева, Н. А. Богачев,
М. Ю. Скрипкин, А. С. Мерещенко*
Санкт-Петербургский государственный университет,
Университетская наб. 7-9, Санкт-Петербург, 199034 Россия
*e-mail: a.mereshchenko@spbu.ru
Поступило в Редакцию 3 февраля 2021 г.
После доработки 3 февраля 2021 г.
Принято к печати 18 февраля 2021 г.
Методом электронной спектроскопии поглощения исследованы растворы фталата тетраэтиламмония в
неводных растворителях: этаноле, диметилсульфоксиде, диметилформамиде и ацетонитриле. Показано,
что в растворах ацетонитрила и диметилформамида происходит димеризация фталат-аниона за счет
π-стекинга, экспериментально определенные константы равновесия составляют 550±50 и 900±50 соот-
ветственно. В растворах этанола и диметилсульфоксида димеризация фталат-аниона не наблюдается.
Ключевые слова: фталат тетраэтиламмония, π-стекинг, константа димеризации, электронная спектро-
скопия
DOI: 10.31857/S0044460X21050012
Бензолдикарбоновые кислоты и их соли нахо-
и цитозина в воде вносят сольватация молекул
дят широкое применение в дизайне металлоорга-
растворенного вещества и структурированность
нических каркасных структур [1-4], где анионы
растворителя. Моделирование димеризации трех
этих кислот выступают в качестве линкеров. В
полиароматических молекул (нафталина, антраце-
связи с этим представляется актуальным изучение
на и тетрацена) в тетрахлорметане, циклогексане и
состояния данных ионов в наиболее распростра-
толуоле методом молекулярной динамики показа-
ненных органических растворителях, использу-
ло [7], что структура растворителя существенным
емых в качестве реакционной среды при синтезе
образом влияет на константу ассоциации аромати-
металлоорганических каркасных структур.
ческих молекул. Так, константа ассоциации в ци-
Бензолдикарбоксилат-анионы являются арома-
клогексане и толуоле существенно выше, чем в те-
тическими соединениями, для которых возможно
трахлорметане. Авторы работы объясняют данный
образование димеров за счет взаимодействия π-
эффект тем, что тетрахлорметан является более
систем, так называемого π-стекинга. На протека-
объемной молекулой, чем циклогексан и толуол,
ние данного процесса существенное влияние ока-
в связи с чем молекулам циклогексана и толуола
зывают свойства растворителя. Так, проведенное
легче интеркалировать между двумя молекулами
В.И. Даниловым с соавторами моделирование ме-
нафталина, антрацена или тетрацена. В работе [8]
тодом Монте-Карло структуры растворов азоти-
исследована зависимость константы димеризации
стых оснований в воде и диметилсульфоксиде [5]
бензойной кислоты в смесях бензол-спирт (спирт =
показало, что в воде эффекты π-стекинга выраже-
октан-1-ол, октан-2-ол) от концентрации послед-
ны слабее. Также из результатов квантово-хими-
него. Высокая сольватирующая способность
ческих расчетов следует [6], что основной вклад
спиртов, большие значения как донорных, так и
в дестабилизацию сэндвичевых димеров гуанина
акцепторных чисел приводит к тому, что при по-
659
660
НОСОВ и др.
данных видно, что в растворах в диметилсульфок-
сиде и этаноле спектры поглощения имеют мак-
симум при 284 нм и не меняют свою форму при
изменении концентрации фталата, в то время как в
случае растворов в диметилформамиде и ацетони-
триле при увеличении концентрации соли форма
спектра поглощения меняется. Это может означать,
что в ацетонитриле и диметилформамиде происхо-
дит либо ассоциация фталат-иона с катионом те-
траэтиламмония, либо полимеризация (наиболее
вероятно, димеризация) фталат-иона. Дополни-
тельно были измерены электронные спектры по-
глощения растворов фталата тетраэтиламмония с
концентрацией 250 мМ. в тонком слое. Отсутствие
новых полос по сравнению с более разбавленными
растворами позволяет исключить возможность по-
лимеризации либо ассоциации в этаноле и ДМСО,
а также предположить, что в ДМФА и ацетонитри-
ле образуется только одна форма ассоциата - ди-
Рис. 1. Нормированные электронные спектры погло-
щения растворов фталата тетраэтиламмония в диме-
мер фталат-иона [C6H4(COO-)2]2 или ионная пара
тилсульфоксиде (а), этаноле (б), ацетонитриле (в) и
с катионом C6H4(COO)2-·NEt+.
диметилформамиде (г) при концентрации соли 0.5 (1),
20 (2) и 250 мМ. (3).
Для определения полноты протекания диссо-
циации фталата тетраэтиламмония в этаноле и
диметилсульфоксиде была построена зависимость
оптической плотности вблизи максимума погло-
вышении их концентрации константа димериза-
щения (280 нм) и на краю полосы (310 нм) от кон-
ции уменьшается, поскольку бензойной кислоте
центрации фталата тетраэтиламмония (рис.
2).
термодинамически более выгодно быть сольвати-
Анализ зависимости оптической плотности от
рованной большим числом молекул спирта, чем
концентрации соли показал, что в диапазоне
образовать димер. Таким образом, по результатам
концентраций 0.1-150 мМ. выполняется закон
анализа литературных данных можно сделать за-
Бугера-Ламберта-Бера (рис. 2), что говорит о не-
ключение о том, что сольватирующая способность
изменности формы существования фталат-иона в
растворителя оказывают существенное влияние на
этаноле и в диметилсульфоксиде в исследованном
π-стекинг: чем большей сольватирующей способ-
интервале составов, т. е. в этих растворах не на-
ностью обладает растворитель, тем менее выгодна
блюдается никаких процессов ассоциации или по-
в нем димеризация. В настоящей работе представ-
лимеризации.
лены результаты систематического эксперимен-
Чтобы выяснить, какой из двух указанных про-
тального исследования димеризации фталат-иона
цессов (ассоциация с катионом тетраэтиламмония
в диметилсульфоксиде, диметилформамиде, аце-
или димеризация фталат-тона) имеет место в аце-
тонитриле и этаноле.
тонитриле и диметилформамиде, были измерены
Для изучения состояния ионов в растворах фта-
электронные спектры поглощения 0.5 мМ. фтала-
лата тетраэтиламмония были измерены электрон-
та тетраэтиламмония с добавкой избытка хлорида
ные спектры поглощения растворов соли в раз-
тетраэтиламмония (250 мМ.), полностью диссо-
ных растворителях (этанол, ацетонитрил, ДМСО,
циирующего в ацетонитриле [9]. Установлено, что
ДМФА) при концентрациях 0.1-40 мМ. в интер-
электронный спектр поглощения раствора, содер-
валах длин волн 265-325 (ДМСО, ДМФА) и 240-
жащего 0.5 мМ. фталата и 250 мМ. хлорида тетраэ-
310 нм (этанол, ацетонитрил). Для примера некото-
тиламмония является суперпозицией спектров по-
рые спектры приведены на рис. 1. Из приведенных
глощения растворов фталата тетраэтиламмония
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
ДИМЕРИЗАЦИЯ ФТАЛАТ-ИОНА В НЕВОДНЫХ РАСТВОРИТЕЛЯХ
661
Рис. 2. Концентрационная зависимость нормированной на толщину кюветы оптической плотности растворов фталата
тетраэтиламмония в диметилсульфоксиде (1) и этаноле (2) при длине волны 280 (а) и 310 нм (б).
(0.5 мМ.) и хлорида тетраэтиламмония (250 мМ.)
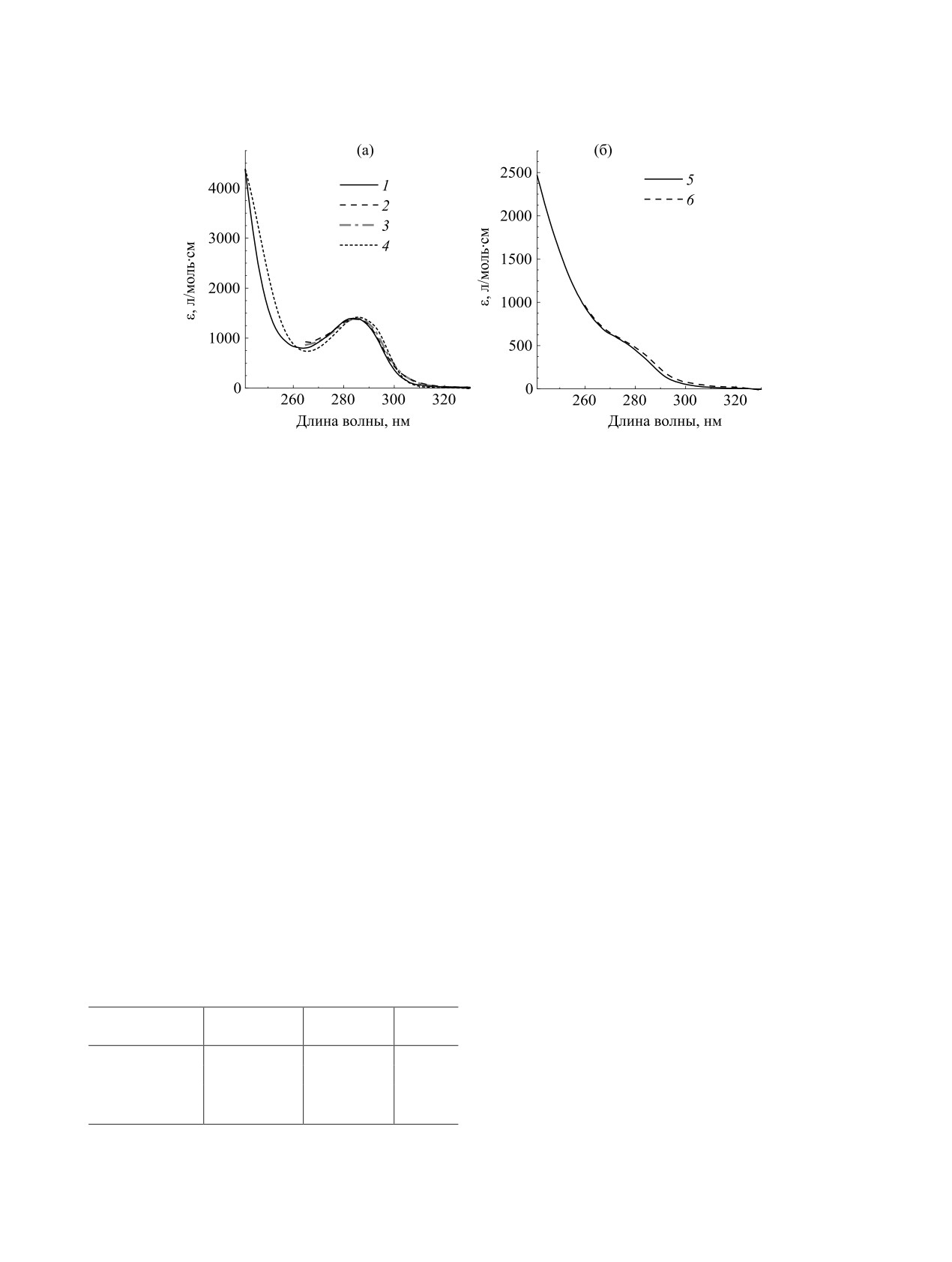
мера фталат-иона присутствуют две основные по-
(рис. 3). Таким образом, при добавлении большого
лосы поглощения: с максимумом при 285 нм (ε285
количества катиона тетраэтиламмония не наблю-
1420 М.-1·см-1) и с максимумом при < 240 нм (ε240
дается смещения равновесия, что свидетельствует
4300 М.-1·см-1) (рис. 4). Димер фталат-иона ха-
об отсутствии ассоциации фталат-иона и катиона
рактеризуется интенсивной полосой поглощения
тетраэтиламмония.
с максимумом при < 240 нм (ε240 2500 М.-1·см-1)
нм с плечом при 280 нм (ε280 480 М.-1·см-1). Вид
Таким образом, наиболее вероятным процессом
спектров поглощения частиц и коэффициенты эк-
является димеризация фталат-иона в растворах
стинкции практически не зависят от природы рас-
ацетонитрила и диметилформамида за счет π-сте-
творителя. Исходя из равновесных концентраций
кинга [7]. С помощью хемометрической обработ-
химических форм были рассчитаны константы ди-
ки данных (программа ReactLab Equilibria) были
меризации фталат-иона в ДМФА и ацетонитриле:
получены индивидуальные электронные спектры
они составили 550±50 и 900±50 в ацетонитриле и
поглощения димера фталат-иона в ДМФА и аце-
диметилформамиде соответственно.
тонитриле, фталат-иона во всех четырех исполь-
зованных растворителях, а также равновесные
Таким образом, полученные в ходе работы экс-
концентрации мономера и димера. В спектре моно-
периментальные данные показывают, что в эта-
Рис. 3. Электронные спектры поглощения растворов 0.5 мМ. фталата тетраэтиламмония в отсутствие (1) и в присутствии
250 мМ. хлорида тетраэтиламмония (2) и 250 мМ. хлорида тетраэтиламмония (3) в ацетонитриле (а) и диметилформамиде
(б). Толщина кюветы - 1 см.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
662
НОСОВ и др.
Рис. 4. Электронные спектры поглощения фталат-аниона (а) в ацетонитриле (1), диметилформамиде (2), диметилсульфок-
сиде (3) и этаноле (4), и димера фталат-аниона (б) в ацетонитриле (5) и диметилформамиде (6), полученные с помощью
хемометрической обработки данных (программа ReactLab Equilibria).
ноле и диметилсульфоксиде фталат тетраэтилам-
условием отсутствия π-стекинга фталат-ионов в
мония полностью диссоциирует с образованием
растворе являются высокие значения обеих ха-
фталат-аниона и катиона тетраэтиламмония, при-
рактеристик - как донорного, так и акцепторного
чем фталат-ион существует в виде мономера в ши-
числа. Последнее обусловлено неоднократно от-
роком концентрационном диапазоне 0.1-250 мМ.
меченной в литературе спецификой сольватации
В диметилформамиде и ацетонитриле фталат те-
ароматических молекул: они взаимодействуют как
траэтиламмония также полностью диссоциирует с
с донорными растворителями за счет сопряженной
образованием фталат-аниона и катиона тетраэти-
системы вакантных π-разрыхляющих МО, так и с
ламмония. При низких концентрациях фталат-ион
акцепторными растворителями, на которые пере-
существует в виде мономера, однако при повыше-
носится электронная плотность с π-связывающих
нии концентрации, начиная с 2 мМ., наблюдается
МО бензольного ядра [11, 12].
образование димера фталат-аниона за счет π-сте-
Таким образом, проведенное исследование со-
кинга. Таким образом, выявлено заметное влияние
стояния фталата тетраэтиламмония в ряде невод-
растворителя на процесс димеризации фталат-и-
ных растворителей показало, что в растворителях,
она. Наблюдаемый эффект не удается объяснить
характеризующихся высокими значениями как
только донорной или только акцепторной спо-
донорного, так и акцепторного числа (диметил-
собностью растворителя: по значению донорно-
сульфоксид, этанол), фталат-ион существует ис-
го числа среди рассматриваемых растворителей
ключительно в мономерной форме. Уменьшение
выделяется только ацетонитрил, значения акцеп-
как донорной (ацетонитрил), так и акцепторной
торного числа достигают минимума у N,N-ди-
(N,N-диметилформамид) силы растворителя спо-
метилформамида (см. таблицу) [10]. Вероятно,
собствует образованию в растворе димерных форм
Свойства растворителей [10] и константы димеризации
посредством π-стекинга, константы равновесия
фталат-иона
димеризации составляют 550±50 и 900±50 соот-
Акцепторное
Донорное
ветственно.
Растворитель
K
димер
число
число
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Этанол
37.1
32.0
-
ДМСО
19.3
29.8
-
В работе использованы следующие реактивы:
ДМФА
16.0
26.6
900±50
фталевая кислота (>99.5%, Sigma-Aldrich), гидрок-
Ацетонитрил
18.9
14.1
550±50
сид тетраэтиламмония (35%-ный водный раствор,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
ДИМЕРИЗАЦИЯ ФТАЛАТ-ИОНА В НЕВОДНЫХ РАСТВОРИТЕЛЯХ
663
Sigma-Aldrich), хлорид тетраэтиламмония (>98%,
СПбГУ «Нанотехнологии», «Оптические и лазер-
Sigma-Aldrich), ацетонитрил (ОСЧ, Криохром),
ные методы исследования вещества» и «Термо-
диметилсульфоксид (ХЧ, Ленреактив), диметил-
гравиметрические и калориметрические методы
формамид (ХЧ, Ленреактив), этанол (ХЧ, Ленре-
исследования»», «Криогенный отдел», «Методы
актив). Хлорид тетраэтиламмония перед исполь-
анализа состава вещества», «Рентгенодифракци-
зованием сушили в вакуумном сушильном шкафу
онные методы исследования», «Вычислительный
при давлении 15 мм рт. ст. и температуре 110°С в
центр», «Магнитно-резонансные методы исследо-
течение 24 ч.
вания».
Фталат тетраэтиламмония. Фталевую кисло-
ФОНДОВАЯ ПОДДЕРЖКА
ту (8 г) растворяли в 40 мл 2.41 М. водного рас-
Работа выполнена при поддержке Российского
твора гидроксида тетраэтиламмония. Полученную
фонда фундаментальных исследований (проект
соль отфильтровывали и сушили в вакуумном
№ 20-33-70025 «Стабильность»).
сушильном шкафу при давлении 15 мм рт. ст. и
температуре 50°С в течение 24 ч. Выход 51%. По-
КОНФЛИКТ ИНТЕРЕСОВ
лученный безводный фталат тетраэтиламмония
Авторы заявляют об отсутствии конфликта
хранили в эксикаторе. Спектр ЯМР 1Н (ДМСО-d6),
интересов.
δ, м. д.: 7.1 д. д (2H, HCAr, J1 5.6, J2 3.2 Гц), 6.9 д. д
(2H, HCAr, J1 5.6, J2 3.2 Гц), 3.1 к (16H, CH3CH2N,
СПИСОК ЛИТЕРАТУРЫ
J 7.2 Гц), 1.1 т (24H, CH3CH2N, J 7.2 Гц). Спектр
1.
Martin N.P., März J., Volkringer C., Henry N., Hennig C.,
ЯМР 13C (ДМСО-d6), δC, м. д.: 172.6 (CO–), 127.2
Ikeda-Ohno A., Loiseau T. // Inorg. Chem. 2017.
(CAr), 124.3 (CAr), 51.8 (CH3CH2N), 7.6 (CH3CH2N).
Vol. 56. N 5. P. 2902. doi 10.1021/acs.inorgchem.6b02962
2.
Du M., Jiang X.J., Zhao X.J. // Inorg. Chem. 2007.
В работе использовали растворы фталата те-
Vol. 46. N 10. P. 3984. doi 10.1021/ic062098+
траэтиламмония в этаноле, диметилсульфоксиде,
3.
Filippova I.G., Gherco O.A., Simonov Y.A., Deseatnic-
ацетонитриле и диметилформамиде со следующи-
Ciloci A.A., Clapco S.F., Tiurina J.P., Baca S.G. //
ми концентрациями: 0.1, 0.2, 0.5, 1, 2, 4, 6, 8, 10, 20,
Polyhedron. 2009. Vol. 29. N 3. P. 1102. doi 10.1016/j.
30, 40, 50, 75, 100, 125, 150 и 250 мМ.; растворы
poly.2009.11.016
4.
Dai A.-Q., Yan Q., Zhong J., Chen S.-C., He M.-Y.,
хлорида тетраэтиламмония в диметилформамиде
Chen Q. // Z. Naturforsch. 2015. Vol. 70b. N 10.
и ацетонитриле с концентрацией 250 мМ., раство-
P. 711. doi 10.1515/znb-2015-0027
ры смеси фталата и хлорида тетраэтиламмония
5.
Данилов В.И., Желтовский Н.В., Слюсарчук О.Н.,
в диметилформамиде и ацетонитриле с концен-
Альдерфер Дж.Л. // Биополимеры и клетка. 1997.
трациями 0.5 и 250 мМ. соответственно, а также
Т. 13. № 1. C. 46. doi 10.7124/bc.000466
6.
Chi H.M. // J. Phys. Chem. (B). 2016. Vol. 120. N 26.
растворы фталата тетраэтиламмония в этаноле и
P. 6010. doi 10.1021/acs.jpcb.6b01934
диметилсульфоксиде с концентрациями 50, 75,
7.
Rury A.S., Ferry C., Hunt J.R., Lee M., Mondal D.,
100, 125 и 150 мМ. Перед проведением спектро-
O’Connell Sean M.O., Mak C.H. // J. Phys. Chem. 2016.
скопических измерений растворы выдерживали
Vol. 120. N 41. P. 23858. doi 10.1021/acs.jpcc.6b08292
при постоянной температуре (25°С) в течение 2 ч.
8.
Hiromichi Y., Kyoko Y., Hiroko W., Genkichi N. //
Talanta. 1995. Vol. 42. N 6. P. 789. doi 10.1016/0039-
Регистрацию спектров поглощения проводили на
9140(95)01480-Y
прецизионном спектрофотометре марки СФ-2000
9.
Видякина А.А., Богачев Н.А., Скрипкин М.Ю., Ме-
в кварцевых кюветах толщиной 1, 0.1 и 0.02 см.
рещенко А.С. // ЖОХ. 2020. Т. 90. № 9. С. 1452;
Представленные в работе оптические плотности
Vidiakina A.A., Bogachev N.A., Skripkin M.Yu.,
нормированы на толщину кюветы, если не ука-
Mereshchenko A.S. // Russ. J. Gen. Chem. 2020. Vol. 90.
зано иное. Обработку результатов осуществляли
N 9. P. 1703. doi 10.1134/S1070363220090170
10.
Yizhak M. Ions in solution and their solvation. Hoboken:
с помощью программного обеспечения ReactLab
John Wiley & Sons, 2015. P. 82.
Еquilibria.
11.
Kuchenbecker D., Jansen G. // ChemPhysChem. 2012.
Vol. 13. P. 2769. doi 10.1002/cphc.201200164
БЛАГОДАРНОСТЬ
12.
Kashyap C., Ullah S.S., Mazumder L.J., Guha A.K. //
Исследования проведены с использованием
Comput. Theor. Chem. 2018. Vol. 130. P. 134. doi
оборудования ресурсных центров Научного парка
10.1016/j.comptc.2018.03.023
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
664
НОСОВ и др.
Dimerization of Phthalate-Ion in Non-Aqueous Solvents
V. G. Nosov, K. A. Podryadrova, M. S. Vasilyeva, N. A. Bogachev,
M. Yu. Skripkin, and A. S. Mereshchenko*
St. Petersburg State University, St. Petersburg, 199034 Russia
*e-mail: a.mereshchenko@spbu.ru
Received February 3, 2021; revised February 3, 2021; accepted February 18, 2021
Solutions of tetraethylammonium phthalate in non-aqueous solvents (ethanol, dimethyl sulfoxide, dimethyl-
formamide, and acetonitrile) were studied by electronic absorption spectroscopy. It was shown that in
solutions of acetonitrile and dimethylformamide, phthalate anion dimerization occurs due to π-stacking with
experimentally obtained dimerization constants of 550±50 and 900±50, respectively. In ethanol and dimethyl
sulfoxide solutions, dimerization of the phthalate anion is not observed.
Keywords: tetraethylammonium phthalate, π-stacking, dimerization constant, solution, electronic spectroscopy
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021