ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 5, с. 778-785
УДК 546.57:546.56:66.094.1
ПОЛУЧЕНИЕ НАНОПЛАСТИН МЕДИ
ВОССТАНОВЛЕНИЕМ Cu(II) В ПРИСУТСТВИИ
АЛКОКСИКАРБОНОВОЙ КИСЛОТЫ
© 2021 г. О. А. Логутенко*, А. И. Титков, А. М. Воробьёв
Институт химии твердого тела и механохимии Сибирского отделения Российской академии наук,
ул. Кутателадзе 18, Новосибирск, 630128 Россия
*e-mail: ologutenko@solid.nsc.ru
Поступило в Редакцию 25 марта 2021 г.
После доработки 6 апреля 2021 г.
Принято к печати 15 апреля 2021 г.
Синтезированы нанопластины меди треугольной и шестиугольной формы восстановлением нитрата ме-
ди(II) гидразингидратом в воде в присутствии 2-[2-(2-метоксиэтокси)этокси]уксусной кислоты. Получен-
ные частицы меди охарактеризованы методами рентгенофазового анализа и электронной микроскопии.
Исследовано влияние температуры, продолжительности синтеза, концентрации стабилизатора, ионов
меди и гидроксида натрия на размер, морфологию и степень полидисперсности образующихся частиц.
Ключевые слова: медь, нанопластины, гидразингидрат, 2-[2-(2-метоксиэтокси)этокси]уксусная кислота,
восстановление
DOI: 10.31857/S0044460X21050164
Материалы на основе нано- и микрочастиц раз-
известные методы синтеза наночастиц позволяют
личных металлов благодаря своим уникальным
получать термодинамически наиболее устойчи-
свойствам широко используются в электронике,
вые частицы меди сферической формы. Однако
катализе и медицине. С развитием цифровых тех-
наиболее востребован синтез анизотропных на-
нологий наночастицы серебра, золота, меди, ни-
ноструктур правильной формы, таких как нано-
келя, алюминия и цинка стали активно применять
проволоки, нанопризмы, нанопластины и т. д., по-
для приготовления чернил и паст для 2D- и 3D-пе-
скольку их оптические, электронные, магнитные
чати электропроводящих элементов печатной
и каталитические свойства зачастую превосходят
электроники, в частности антенн и микроэлектро-
свойства сферических наночастиц. Серебряные и
дов [1-4]. Проводящие чернила и пасты на основе
медные пленки, полученные нанесением на раз-
серебра получили наибольшее распространение
личные подложки чернил и паст на основе частиц
благодаря таким уникальным свойствам серебра,
пластинчатой или чешуйчатой формы, позволяют
как высокая электропроводность и устойчивость
проводить спекание при более низких температу-
к окислению. Однако высокая стоимость серебра
рах при термическом отжиге и имеют более низкое
препятствует его широкому применению, и возни-
сопротивление [6, 7].
кает спрос на более дешевые металлы, например,
Метод химического восстановления ионов ме-
медь, которая почти в 100 раз дешевле серебра, при
таллов или их комплексов наиболее распространен
этом ее электропроводность лишь на 10% ниже.
и эффективен при получении наночастиц с управ-
Для синтеза нано- и микрочастиц меди раз-
ляемой морфологией. Поскольку образование ани-
личной формы разработан ряд физических и хи-
зотропных форм термодинамически невыгодно,
мических методов [5]. В большинстве случаев
для обеспечения анизотропного роста обычно ис-
778
ПОЛУЧЕНИЕ НАНОПЛАСТИН МЕДИ
779
пользуют стабилизаторы, которые могут избира-
бидентатной координации, в результате чего про-
тельно адсорбироваться на различных гранях кри-
исходит эффективная стабилизация полученных
сталлов и таким образом препятствовать их росту
наночастиц [16, 17].
в соответствующих направлениях.
В отличие от синтеза нанопластин серебра и
O
золота синтез нанопластин меди изучен недоста-
H3CO
O
O
OH
точно. Впервые они были получены в инертной
атмосфере при восстановлении ацетата меди(II)
1
гидразином в присутствии поли(1-винилпирроли-
дин-2-она) [8]. Частицы меди плоской формы по-
В результате обменной реакции (1) соли 2 с ни-
лучены восстановлением различных соединений
тратом меди(II) получен раствор 2-[2-(2-метоксиэ-
меди в органических растворителях или в воде в
токси)этокси]ацетата меди(II) 3 в воде.
присутствии стабилизатора [9-12]. Роль стабили-
затора очень важна, поскольку он влияет не толь-
2CH3(OC2H4)2OCH2CO2Na + Cu(NO3)2
ко на морфологию частиц, но и предотвращает
2
их агломерацию и окисление. Нанопластины по-
→ [CH3(OC2H4)2OCH2CO2]2Cu + 2NaNO3.
(1)
лучены при восстановлении хлорида меди аскор-
биновой кислотой в воде в присутствии триме-
3
тил(цетил)аммонийбромида и хлорида в качестве
Исследовано восстановление ионов Cu2+ в воде
стабилизаторов [13], а также при восстановлении
гидразингидратом в присутствии соли 2 в различ-
комплекса Cu(II)-тартрат гипосфитом натрия
ных условиях. Изучена зависимость размера и
(NaH2PO2) в присутствии поли(1-винилпирроли-
морфологии образующихся частиц меди от усло-
дин-2-она) [14]. Получали смесь пластин треу-
вий их синтеза, в частности, от температуры, про-
гольной, усеченной треугольной и шестиугольной
должительности восстановления, концентрации
формы со средней длиной ребра 180-280 нм и тол-
меди, гидразингидрата, щелочи и стабилизатора
щиной около 8 нм. Нанопластины меди можно по-
1. Концентрацию меди варьировали от 0.025 до
лучить при добавлении в систему иода или брома
0.5 моль/л, температуру восстановления - в ин-
[12, 15].
тервале 40-90°C, а длительность восстановления
Разработка простых и дешевых методов по-
при фиксированной температуре - от 10 мин до
лучения устойчивых к окислению нано- и микро-
3 ч. Мольные отношения гидразингидрата и NaOH
пластин меди по-прежнему остается актуальной
к меди варьировали от 3:1 до 20:1 и от 0:1 до 4:1
задачей. Нами предложен простой метод синтеза
соответственно. Данные о составе, размере и мор-
нанопластин меди с размерами сторон 300-500 нм
фологии частиц меди, полученных в этих услови-
и толщиной 20-50 нм с целью их применения для
ях, приведены в таблице.
создания новых композиций электропроводящих
Концентрация NaOH значительно влияет на
чернил и паст для 2D- и 3D-печати. В предлагае-
скорость реакции восстановления ионов Cu2+,
мом методе не требуется использования многоком-
а это, в свою очередь, отражается на составе и
понентных смесей, таких как поли(1-винилпирро-
морфологии образующихся частиц. В отсутствие
лидин-2-он), перекись водорода и цитрат натрия,
NaOH при комнатной температуре ионы меди Сu2+
или предварительно синтезированных зародышей
легко восстанавливаются до Сu+ с образованием
для селективной стабилизации одной из граней ча-
оксида Сu2O, который выпадает из раствора в виде
стиц. Основное внимание уделено исследованию
желто-оранжевого осадка. Дальнейшее восстанов-
влияния различных параметров синтеза на восста-
ление Сu2O до Сu0 в этих условиях затруднено и
новление ионов меди гидразингидратом в водной
протекает лишь при повышенной температуре или
среде в присутствии 2-[2-(2-метоксиэтокси)эток-
в присутствии щелочи. Данные электронной ми-
си]уксусной кислоты 1. Ранее нами найдено, что
кроскопии показывают, что в отсутствие NaOH об-
карбоксильные группы кислоты 1 связывают се-
разуются сферические частицы оксида меди Сu2O
ребро посредством монодентатной и мостиковой
с размерами 100-400 нм. В присутствии щелочи в
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
780
ЛОГУТЕНКО и др.
Влияние условий синтеза на размер и морфологию частиц меди, полученных при восстановлении ионов Cu2+ гидра-
зингидратом в воде в присутствии соли 2 в течение 45 мин
№
Морфология частиц
Влияние NaOH
1
1:0
1:6
1:2
60
Сu2O
100-400
Сферические частицы
2
1:1
1:6
1:2
60
Сu2O
100-300
Сферические частицы
3
1:2
1:6
1:2
60
Cu
Длина 300-500,
Треугольные и шестиугольные пластины
толщина 20-50
4
1:4
1:6
1:2
60
Cu
~ 400
Сферические частицы
5
1:6
1:6
1:2
60
Cu
-
Бесформенные агрегаты из наночастиц
Влияние температуры синтеза
6
1:2
1:3
1:2
40
Сu2O
150-300
Сферические частицы
7
1:2
1:3
1:2
80
Cu
200-400
Бесформенные агрегаты и шестиугольные
пластины
8
1:2
1:3
1:2
90
Cu
от 100 до 200
Преимущественно агрегированные наночастицы
и незначительная доля пластин
Влияние соли 2
9
1:2
1:3
1:0
60
Сu2O
200-400
Близкая к сферической
10
1:2
1:3
1:3
60
Cu
100-300
Бесформенные частицы
11
1:2
1:3
1:4
60
Cu + Сu2O
~ 150
Агрегированные наночастицы
Влияние гидразингидрата
12
1:2
1:3
1:2
40
Сu2O
150-300
Сферические частицы
13
1:2
1:6
1:2
40
Cu
Длина 300-500,
Треугольные и шестиугольные пластины
толщина 20-50
14
1:2
1:9
1:2
40
Cu
300-500
Близкая к сферической
15
1:2
1:20
1:2
40
Cu
-
Бесформенные агрегаты из наночастиц
мольном отношении Сu2+-NaOH 1:1 восстановить
ченных частиц близка к сферической с размером
оксид до металлической меди при 60°С при моль-
около 400 нм, а при Сu2+-NaOH 1:6 образуются
ном отношении медь-гидразингидрат 1:6 также не
бесформенные агрегаты, состоящие из частиц с
удается; образуются наночастицы Сu2O идеальной
размером менее 50 нм.
сферической формы с размерами 100-300 нм и
По-видимому, при высоких концентрациях
более однородные по размеру, чем частицы, полу-
NaOH скорость восстановления ионов Сu2+ уве-
ченные в отсутствие NaOH.
личивается, кинетически контролируемый рост
При мольном отношении Сu2+-NaOH 1:2 через
анизотропных наноструктур меди становится
30 мин происходит полное восстановление ионов
невозможным, и образуются термодинамиче-
меди с образованием усеченных треугольных и
ски устойчивые частицы изотропной формы. По
шестиугольных нанопластин металлической меди
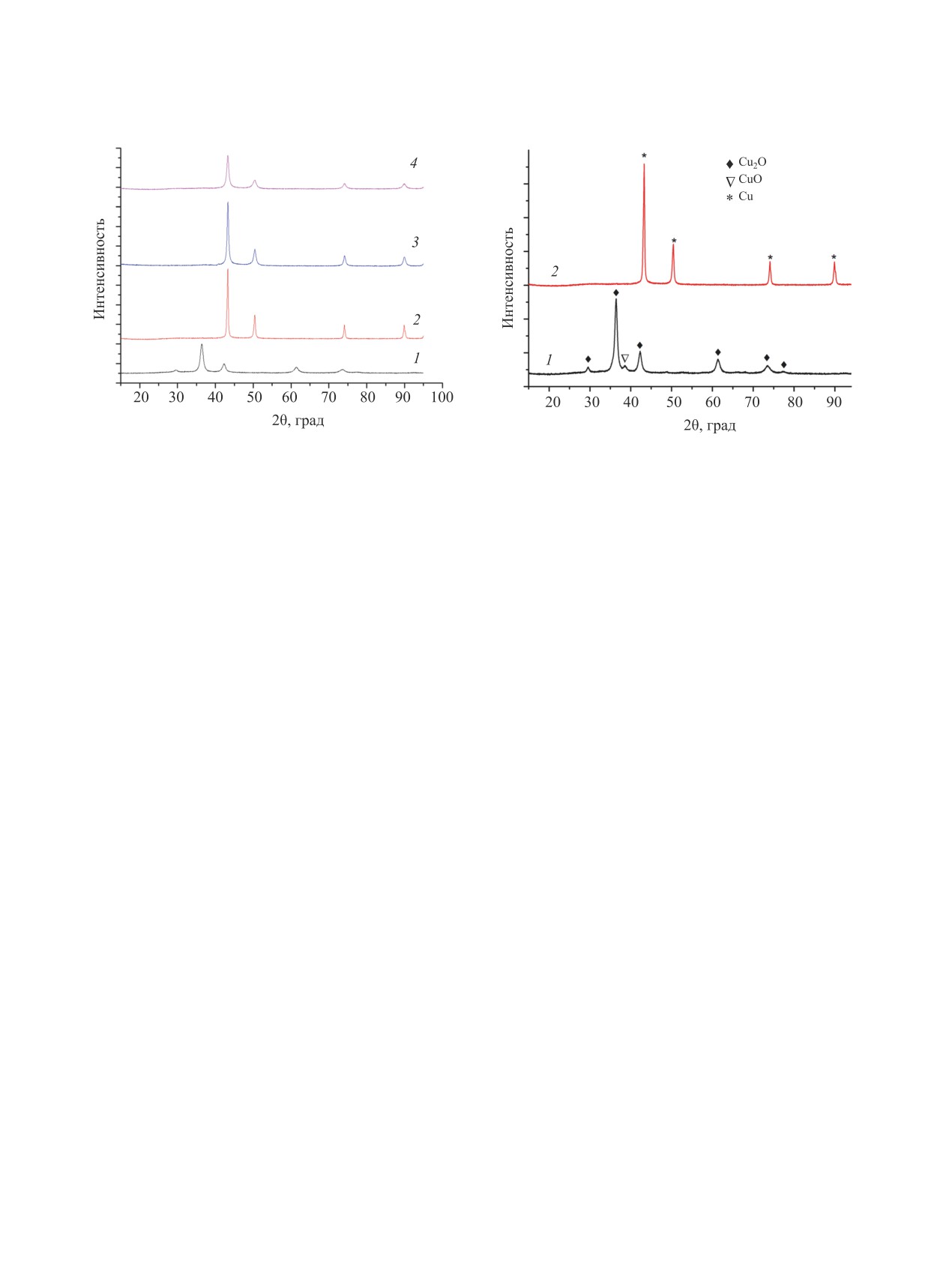
данным РФА (рис. 1), образец, полученный при
с размерами сторон 300-500 нм и толщиной око-
мольном отношении меди к NaOH < 1:2, состоит
ло 50 нм. Дальнейшее увеличение концентрации
из оксида меди Сu2O (2θ 36.27, пространственная
гидроксида натрия приводит к существенному
группа Pn3m, a 0.427 нм, файл PDF 05-0667). При
изменению геометрии полученных частиц. При
отношении Сu2+-NaOH ≥ 1:2 образуется металли-
мольном отношении Сu2+-NaOH 1:4 форма полу-
ческая медь с характерными максимумами при 2θ
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
ПОЛУЧЕНИЕ НАНОПЛАСТИН МЕДИ
781
Рис. 1. Рентгенограммы и микроснимок порошков,
полученных при восстановлении ионов Cu2+ гидразин-
Рис. 2. Рентгенограммы порошков, полученных при
гидратом в присутствии соли 2. Cu2+:гидразингидрат =
восстановлении ионов Cu2+ гидразингидратом в присут-
1:6, Сu2+:соль 2 = 1:2, 60°С. Сu2+:NaOH = 1:0 и 1:1 (1),
ствии соли 2 при 60°С. Cu2+:гидразингидрат:NaOH =
1:2 (2), 1:4 (3) и 1:6 (4).
1:3:2, Сu2+:соль 2 = 1:0 (1) и 1:2 (2).
43.3, 50.4 и 74.2°, соответствующими дифракции
При увеличении концентрации восстановителя
от плоскостей (111), (200) и (220) гранецентриро-
в 2 раза (мольное отношение Сu2+- гидразингидрат
ванной кубической структуры меди (PDF 04-0836).
1:6) треугольные и шестиугольные медные пласти-
Однако наночастицы в форме пластин удается по-
ны с размерами 300-500 нм можно получить при
лучить в этих условиях только при мольном отно-
40°С, а при 80 и 90°С в этих условиях восстановле-
шении Сu2+-NaOH 1:2.
ние ионов меди до металлической меди протекает
Исследовано влияние температуры восстанов-
в отсутствие щелочи. По данным электронной ми-
кроскопии, доля пластин в продукте восстановле-
ления на состав, морфологию и размер частиц,
ния с увеличением температуры заметно уменьша-
полученных при мольном отношении Сu2+-соль
ется, так как повышение температуры приводит к
2-гидразингидрат-NaOH 1:2:3:2. При 40°C и ниже
увеличению скорости восстановления ионов меди,
в системе образуются частицы оксида меди Сu2O
вследствие чего анизотропный рост в этих услови-
сферической формы с размерами 150-300 нм. По-
ях трудно поддается контролю. По данным РФА,
вышение температуры до 60°С приводит к обра-
зованию металлической меди в форме довольно
продукт реакции в этом случае представляет собой
смесь металлической меди и ее оксида Сu2O. По-
однородных пластин с размерами 300-500 нм и
явление фазы оксида меди может быть связано с
толщиной около 50 нм. При увеличении темпера-
уменьшением размера частиц, которые окисляют-
туры до 90°С также образуются нанопластины, од-
ся легче, чем более крупные частицы. Кроме того,
нако их выход уменьшается, а полидисперсность
при высоких температурах устойчивость частиц
возрастает: наряду с пластинами, присутствуют
меди к окислению снижается, чем также можно
несферические агрегаты. На дифрактограммах
всех образцов, полученных при 60°С и выше,
объяснить присутствие оксида меди в образцах.
Таким образом, для синтеза нанопластин меди оп-
присутствуют полосы, характерные для гранецен-
тимален интервал температур 40-60°С.
трированной кубической структуры меди (PDF
04-0836), и отсутствуют рефлексы, характерные
Влияние концентрации стабилизатора на размер
для оксидов Сu2O или СuO, что свидетельствует
и форму образующихся частиц меди исследовали
о полном восстановлении ионов меди до металла.
при 60°С и при мольных отношениях Сu2+-гидра-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
782
ЛОГУТЕНКО и др.
зингидрат-NaOH 1:6:2 и 1:3:2 соответственно. В
стин меди наблюдается только в присутствии соли
отсутствие стабилизатора 2 при мольном отноше-
2. Вероятно, только в этом случае происходит ее
нии Сu2+- гидразингидрат 1:3 образуются частицы
селективная адсорбция на гранях (111) формиру-
сферической формы с размерами 200-400 нм. По
ющихся кристаллов меди, что способствует их ро-
данным РФА (рис. 2, 1), продукт восстановления
сту вдоль грани (100). Можно предположить, что
представляет собой оксид меди Cu2O (максимум
с уменьшением длины углеводородной цепи кар-
дифракции при 2θ 36.27) с примесью CuO. В при-
боновой кислоты ее стабилизирующее влияние на
сутствии стабилизатора при мольном отношении
гранях (111) незначительно или одинаково на обе-
Сu2+-соль 2 1:2, согласно данным РФА и электрон-
их гранях (111) и (100), и в результате происходит
ной микроскопии, в системе образуются треуголь-
изотропный рост частиц. При увеличении длины
ные и шестиугольные нанопластины металличе-
углеводородной цепи стабилизатора, как показа-
ской меди без примеси Cu2O (рис. 2, 2). Однако
ли расчеты [18], комплексообразование сопрово-
при дальнейшем увеличении мольного отноше-
ждается большими потерями конфигурационной
ния Сu2+-соль 2 до 1:3 образуются бесформенные
энтропии (-TΔS), что препятствует образованию
частицы металлической меди с размерами 100-
прочных связей между лигандом и металлом.
300 нм, а при отношении Сu2+-соль 2 1:4 разме-
Для исследования влияния роли восстановите-
ры частиц уменьшаются и полученный порошок
ля на формирование несферических медных нано-
представляет собой сильно агрегированные нано-
частиц при 40°С проведена серия экспериментов,
частицы. По данным РФА, в этих условиях про-
в которых мольное отношение меди к гидразинги-
дукт восстановления состоит в основном из ме-
драту в исходной реакционной смеси изменялось
таллической меди и небольшого количества Сu2O.
от 1:3 до 1:20. Мольные отношения меди к гидрок-
Таким образом, при мольном отношении Сu2+-
сиду натрия и к соли 2 поддерживали на уровне
соль 2 ≥ 1:3 стабилизация частиц усиливается и
1:2. Данные электронной микроскопии показыва-
замедляется их рост, в результате чего размеры
ют, что при мольном отношении меди к гидразин-
образующихся частиц и их устойчивость к окисле-
гидрату 1:3 образуются сильно агрегированные
нию и агрегации существенно уменьшаются. Для
частицы сферической формы с размерами около
обеспечения анизотропного роста частиц восста-
300 нм, которые, согласно данным РФА, представ-
новление следует проводить при мольном отноше-
ляют собой чистый оксид меди(I). Таким образом, в
нии Сu2+-соль 2 1:2.
этих условиях даже при увеличении длительности
На
примере
метоксиуксусной
и
восстановления до 2 ч получить металлическую
алкоксизамещенной
карбоновой
кислоты
медь не удается. При отношении Сu2+:гидразинги-
с более высокой молекулярной массой
драт = 1:6 образуются наночастицы металлической
(CH3O[CH2CH2O]nCH2CH2COOH) установлено
меди в форме треугольных и шестиугольных пла-
влияние длины углеводородной цепи стабили-
стин с размерами сторон 300-500 нм и толщиной
затора на размер и форму образующихся частиц
около 20-50 нм, однако при дальнейшем увеличе-
меди. Восстановление проводили при 60°С, моль-
нии концентрации восстановителя получить на-
ные отношения Сu2+-стабилизатор и Сu2+- гидра-
ночастицы меди анизотропной формы не удается.
зингидрат 1:2 и 1:3 соответственно, т. е. в тех же
При мольном отношении Сu2+:гидразингидрат =
условиях, в которых при использовании соли 2
1:9 образуются частицы с размерами 300-500 нм,
образуются нанопластины меди. В первом случае
форма которых близка к сферической, а при от-
образуются полидисперсные агрегаты неправиль-
ношении Сu2+:гидразингидрат = 1:20 образуются
ной формы с размерами от 100 до 300 нм, а при
бесформенные агрегаты наночастиц. По данным
восстановлении соли меди в присутствии кислоты
РФА, конечный продукт восстановления в этих
с более высокой молекулярной массой образуются
случаях - чистая металлическая медь. Очевидно,
полиэдры с размерами 400-700 нм.
с увеличением концентрации гидразингидрата в
Таким образом, анизотропный рост с образо-
реакционной системе скорость восстановления
ванием треугольных и шестиугольных нанопла-
увеличивается, в результате чего формирования
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
ПОЛУЧЕНИЕ НАНОПЛАСТИН МЕДИ
783
анизотропных наночастиц меди в этих условиях
ства по сравнению с аналогичными пленками,
не происходит. Кроме того, при избытке гидразина
сформированными из сферических частиц [7].
может происходить дополнительная стабилизация
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
всех граней медного кристаллита, так как гидра-
зин не только восстанавливает ионы металлов, но
В работе использовали нитрат меди
и благодаря неподеленным электронным парам на
Cu(NO3)2∙3H2O
(99%, Acros Organics, Китай),
атомах азота ведет себя как бидентатный лиганд,
метоксиуксусную кислоту (98%, Sigma Aldrich,
координирующийся с поверхностью частиц меди
США),
2-[2-(2-метоксиэтокси)этокси]уксусную
[19]. В результате молекулы гидразингидрата мо-
кислоту 1 (≥90%, Sigma Aldrich, США), гидра-
гут адсорбироваться на одной или нескольких гра-
зингидрат (100%) и этиловый спирт (95%, Хим-
нях растущего кристалла и блокировать их рост по
мед, Россия), гидроксид натрия ОСЧ (50%-ный
всем направлениям, что приводит к изотропному
водный раствор). Алкоксикарбоновая кислота
росту и уменьшению размера образующихся ча-
CH3O[CH2CH2O]nCH2CH2COOH (М 350) получе-
стиц. Следовательно, мольное отношение меди и
на окислением соответствующего метоксиполиэ-
гидразингидрата 1:6 оптимально для формирова-
тиленгликоля по опубликованной методике [20].
ния треугольных и шестиугольных структур ме-
Восстановление меди(II). Необходимую
таллической меди.
аликвоту кислоты 1 растворяли в 25 мл воды, до-
Таким образом, при восстановлении ионов
бавляли при перемешивании стехиометрическое
Cu2+ в воде гидразингидратом сначала образуются
количество гидроксида натрия и необходимое ко-
наночастицы оксида меди Cu2O (2) сферической
личество нитрата меди. Мольное отношение ни-
формы. При этом голубой цвет исходного раство-
трата меди к натриевой соли 2 кислоты 1 варьиро-
ра меняется на кирпично-оранжевый. Дальнейшее
вали от 1:2 до 1:4. Полученный раствор нагревали
восстановление Cu2O до металлической меди воз-
в стакане до необходимой температуры, затем к
можно лишь в присутствии щелочи (3) или при
раствору быстро по каплям прибавляли 100%-ный
увеличении температуры синтеза (4), оно сопрово-
гидразингидрат (мольное отношение Cu2+-гидра-
ждается изменением кирпично-оранжевого цвета
зингидрат изменяли от 1:3 до 1:20). Голубой цвет
реакционной смеси на темно-красный.
исходного раствора менялся на оранжевый в ре-
2Cu2+ + N2H4 + H2O → Cu2O↓ + N2↑ + 3H2,
(2)
зультате образовании частиц Cu2O. Через 15 мин
Cu2O + N2H4 + OH- → 2Cu0 + N2↑ + 1/2H2↑ + 2H2O, (3)
перемешивания в реакционную смесь добавляли
2Cu2O + N2H4 → 4Cu + N2↑ + 2H2O.
(4)
раствор NaOH и для завершения образования на-
Этим путем при восстановлении водных рас-
ночастиц реакционную смесь интенсивно пере-
творов нитрата меди гидразингидратом в присут-
мешивали 30 мин. Полученные в результате вос-
ствии соли 2 при мольных отношениях Cu2+-соль
становления темно-красные частицы отделяли от
2, Cu2+-гидразингидрат и Cu2+-NaOH 1:2, 1:3 и
жидкой фазы центрифугированием, промывали
1:2 соответственно при 60°С получены монодис-
осадок несколько раз водой и этанолом, а затем су-
персные треугольные и шестиугольные пластины
шили на воздухе.
меди с размерами 300-500 нм и толщиной около
Рентгенофазовый анализ проводили на диф-
50 нм. Синтезированные в этих условиях порош-
рактометре Bruker D8 Advance (CuKα-излучение,
ки меди стабильны и не окисляются на воздухе в
скорость вращения счетчика 0.1 град/мин). Иден-
течение года. Частицы в форме пластин благодаря
тификацию фаз проводили с использованием
геометрической анизотропии обладают уникаль-
ным спектром плазмонного резонанса [9] и поэто-
базы порошковых дифракционных данных (PDF)
му наиболее перспективны в качестве материала
(картотека ICDD, PDF-2, Release 2011). Исследо-
для сенсоров и диагностики. Пленки, полученные
вание образцов методом растровой электронной
из чернил на основе несферических наночастиц,
микроскопии проводили с использованием скани-
более однородны, имеют меньшее электрическое
рующего электронного микроскопа Hitachi 3400 N
сопротивление и улучшенные механические свой-
(Hitachi Ltd., Япония).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
784
ЛОГУТЕНКО и др.
ФОНДОВАЯ ПОДДЕРЖКА
Chem. Int. Ed. 1988. Vol. 27. P. 1530. doi 10.1002/
anie.198815301
Работа выполнена в рамках государственно-
9.
Pastoriza-Santos I., Sanchez-Iglesias A., Rodrıguez-
го задания Института химии твердого тела и ме-
Gonzalez B., Liz-Marzan L.M. // Small. 2009. Vol. 5.
ханохимии Сибирского отделения РАН (проект
P. 440. doi 10.1002/smll.200801088
№ 0237-2019-0002).
10.
Park Y.S., Chae H.K. // Chem. Mater. 2010. Vol. 22.
P. 6280. doi 10.1021/cm101961g
КОНФЛИКТ ИНТЕРЕСОВ
11.
Xia Y., Xiong Y., Lim B., Skrabalak S.T. // Angew.
Chem. Int. Ed. 2009. Vol. 48. N 1. P. 60. doi 10.1002/
Авторы заявляют об отсутствии конфликта
anie.200802248
интересов.
12.
Li Y., Fan Z., Yang H., Yuan X., Chao Y., Li Y., Wang C.
СПИСОК ЛИТЕРАТУРЫ
// Cryst. Eng. Commun. 2020. Vol. 22. N 45. P. 7786.
doi 10.1039/d0ce01106a
1. Kamyshny А., Steinke J., Magdassi S. // Open Appl.
13.
Xu S., Sun X., Ye H., You T., Song X, Sun S. // Mater.
Phys. J. 2010. Vol. 4. P. 19. doi 10.2174/
Chem. Phys. 2010. Vol. 120. P. 1. doi 10.1016/j.
1874183501104010019
matchemphys.2009.10.049
2. Espera A.H. Jr., Dizon J.R.C., Chen Q., Advincula R.C. //
14.
Sun Y., Xu L., Yin Z., Song X. // J. Mater. Chem. (A).
Prog. Addit. Manuf. 2019. Vol. 4. N 3. P. 245. doi
2013. Vol. 1. P. 12361. doi 10.1039/c3ta12526b
10.1007/s40964-019-00077-7
15.
Lee J.W., Han J., Lee D.S., Bae S., Lee S.H., Lee S.K.,
3. Titkov A.I., Bulina N.V., Ulihin A.S., Shundrina I.K.,
Moon B.J., Choi C.J., Wang G., Kim T.W. // Small. 2018.
Karpova E.V., Gerasimov E.Yu., Yukhin Yu.M., Lya-
Vol. 14. P. 1703312. doi 10.1002/smll.201703312
khov N.Z. // J. Mater. Sci. 2017. Vol. 28. N 2. P. 2029.
16.
Титков А.И., Логутенко О.А., Воробьев А.М., Гера-
doi 10.1007/s10854-016-5762-0
симов Е.Ю., Булина Н.В., Юхин Ю.М., Ляхов Н.З. //
4. Titkov A.I., Shundrina I.K., Gadirov R.M., Odod A.V.,
ЖОХ. 2019. Т. 89. Вып. 1. С. 113; Titkov A.I.,
Kurtsevich A.E.,Yukhin Yu M., Lyakhov N.Z. // Mater.
Logutenko O.A., Vorob’yov A.M., Gerasimov E.Yu.,
Today. 2018. Vol. 5. N 8. Pt 2. P. 16042. doi 10.1016/j.
Bulina N.V., Yukhin Yu.M., Lyakhov N.Z. // Russ. J.
matpr.2018.05.049
Gen. Chem. 2019. Vol. 89. N 1. P. 100. doi 10.1134/
5. Abhinav V.K., Rao V.K.R., Karthik P.S., Singh S.P. //
S1070363219010183
RSC Adv. 2015. N 5. 63985. doi 10.1039/C5RA08205F
17.
Titkov A.I., Logutenko O.A., Gerasimov E.Yu.,
6. Ren H.M., Guo Y., Huang S.Y., Zhang K., Yuen M.M.F.,
Shundrina I.K., Karpova E.V., Lyakhov N.Z. // J. Incl.
Fu X.Z., Yu S., Sun R., Wong C.P. // ACS Appl. Mater.
Phenom. Macrocycl. Chem. 2019. Vol. 94. N 3-4.
Interfaces. 2015. Vol. 7. P. 13685. doi 10.1021/
P. 287. doi 10.1007/s10847-019-00921-x
acsami.5b03571
18.
Tang Z., Zhang Q., Yin Y., Chang C.A. // J. Phys. Chem.
7. Lee Y.I., Kim S., Jung S.B., Myung N.V., Choa Y.H. //
(C). 2014. Vol. 118. P. 21589. doi 10.1021/jp503319s
ACS Appl. Mater. Interfaces. 2013. Vol. 5. N 13.
19.
Medvedeva X., Vidyakina A., Li F., Mereshchenko A.,
P. 5908. doi 10.1021/am401757y
Klinkova A. // Nanomaterials 2019. Vol. 9. P. 1445. doi
8. Curtis A.C., Duff D.G., Edwards P.P., Jefferson D.A.,
10.3390/nano9101445
Johnson B.F. G., Kirkland A.I., Wallace A.S. // Angew.
20.
Lele B.S., Kulkarni M.G. Pat. US 6239252B1.2001.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021
ПОЛУЧЕНИЕ НАНОПЛАСТИН МЕДИ
785
Synthesis of Copper Nanoplates by Reduction of Cu(II)
in the Presence of Alkoxycarboxylic Acid
O. A. Logutenko*, A. I. Titkov, and A. M. Vorobyov
Institute of Solid State Chemistry and Mechanochemistry, Siberian Branch of the Russian Academy of Sciences,
Novosibirsk, 630128 Russia
*e-mail: ologutenko@solid.nsc.ru
Received March 25, 2021; revised April 6, 2021; accepted April 15, 2021
Triangular and hexagonal copper nanoplates were synthesized by reduction of copper(II) nitrate with hydrazine
hydrate in water in the presence of 2-[2-(2-methoxyethoxy)ethoxy]acetic acid. The obtained copper particles
were characterized by X-ray phase analysis and electron microscopy. The effect of temperature, duration of
synthesis, concentration of stabilizer, copper ions and sodium hydroxide on the size, morphology, and polydis-
persity degree of the resulting particles was studied.
Keywords: copper, nanoplates, hydrazine hydrate, 2-[2-(2-methoxyethoxy)ethoxy]acetic acid, reduction
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 5 2021