ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 9, с. 1474-1476
КРАТКИЕ
СООБЩЕНИЯ
УДК 544.344.3
КОМПЛЕКСООБРАЗОВАНИЕ ИОНОВ КОБАЛЬТА(II)
С 4,4′-БИПИРИДИНОМ В НЕВОДНЫХ РАСТВОРИТЕЛЯХ
© 2021 г. М. М. Жеребцова, Н. А. Богачев, М. Ю. Скрипкин, А. С. Мерещенко*
Санкт-Петербургский государственный университет,
Университетская наб. 7-9, Санкт-Петербург, 199034 Россия
*e-mail: a.mereshchenko@spbu.ru
Поступило в Редакцию 4 июня 2021 г.
После доработки 28 июня 2021 г.
Принято к печати 3 июля 2021 г.
Получены электронные спектры комплексов кобальта(II) и 4,4′-бипиридина в неводных растворителях
и определены константы устойчивости комплексов. Величины констант устойчивости комплексов и
донорных чисел растворителей изменяются антибатно.
Ключевые слова: комплексообразование, 4,4′-бипиридин, кобальт, неводные растворители, электронная
спектроскопия
DOI: 10.31857/S0044460X21090201
Ионы кобальта(II) и 4,4′-бипиридин (4,4′-bpy)
мерены электронные спектры поглощения раство-
как бидентатный лиганд используются для созда-
ров Co(ClO4)2 (10 ммоль/л) и 4,4′-бипиридина (0-
ния металлоорганических каркасных структур [1-
200 ммоль/л) в ДМСO, ДМФА, диметилацетамиде
3]. На топологию каркасных структур существен-
и этаноле. Установлено, что во всех растворителях
ным образом влияют условия синтеза, в частности,
образуется только один комплекс - Co(4,4′-bpy)2+.
подбор растворителей, для сольвотермального
Индивидуальные спектры комплекса в разных
синтеза [4]. Наиболее часто в сольвотермальном
растворителях, полученные по результатам хемо-
синтезе применяются полярные донорные орга-
метрической обработки спектров указанных выше
нические растворители, такие как диметилсульф-
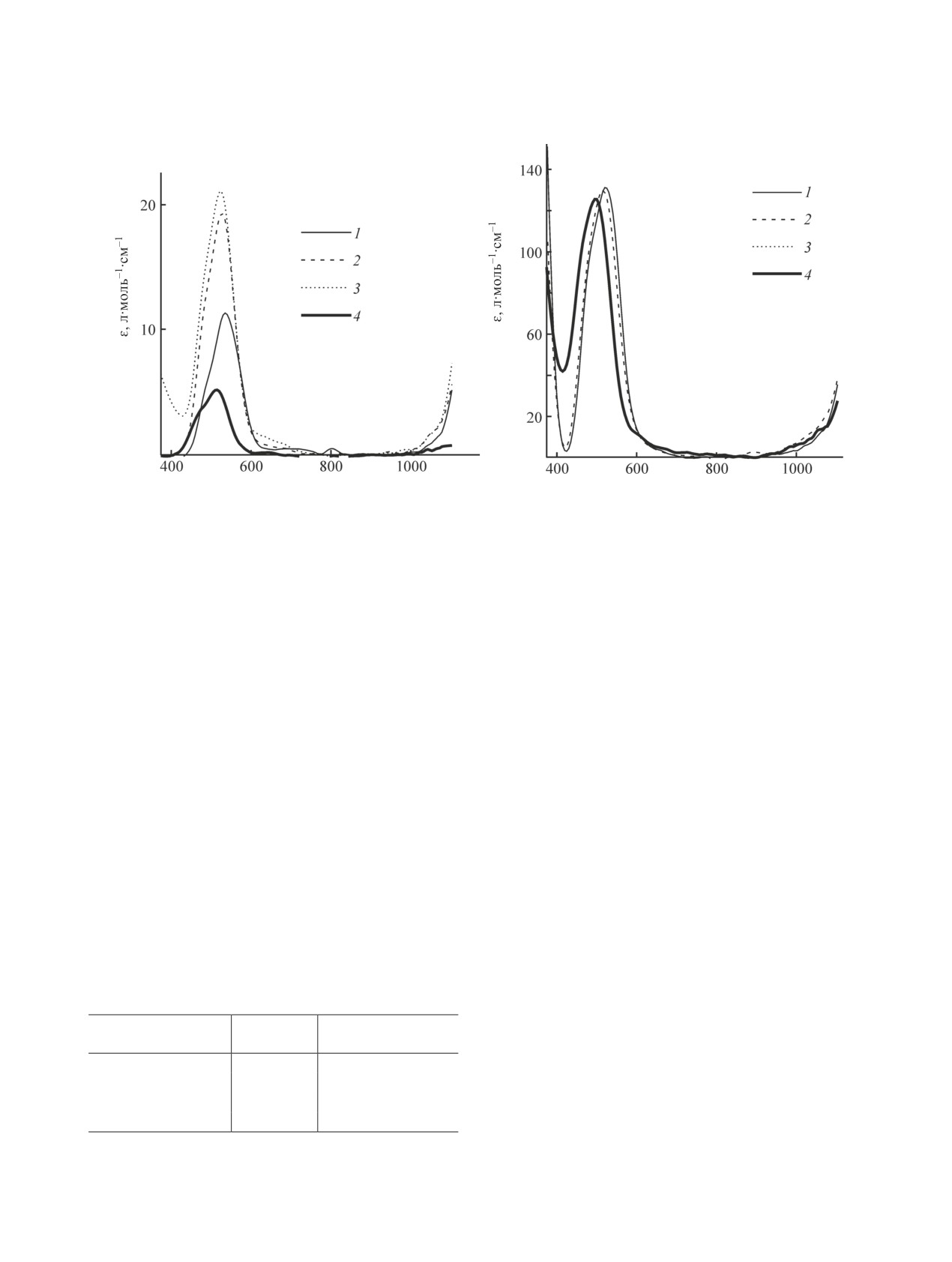
серий растворов, показаны на рис. 1. В исследу-
оксид, диметилформамид, диметилацетамид, эта-
емом спектральном диапазоне наблюдается поло-
нол [5]. Подробные механизм и кинетика кристал-
са поглощения с максимумами поглощения при
лизации каркасных структур не изучены, несмотря
490-525 нм как для сольватокомплексов Co2+, так
на большое число синтезированных соединений и
и для комплексов Co(4,4′-bpy)2+ (d-d-переходы).
широкие области применения [6].
Спектры комплекса Co(4,4′-bpy)2+ характеризуют-
ся более высокими коэффициентами экстинкции,
Нами исследована первая стадия образова-
чем спектры сольватокомплексов, что, по-видимо-
ния вторичных строительных блоков каркасных
му, связано с более низкой симметрией комплек-
структур на основе 4,4′-бипиридина и ионов ко-
сов кобальта(II) с 4,4′-бипиридином, чем сольвато-
бальта(II). Методом УФ спектроскопии исследо-
вано комплексообразование ионов кобальта(II) и
комплексов.
4,4′-бипиридина и определены константы устой-
На основании полученных данных рассчи-
чивости комплексов в неводных растворителях
таны равновесные концентрации комплексов и
(ДМСO, ДМФА, диметилацетамид, этанол). Из-
константы их устойчивости (табл. 1). Выявлена
1474
КОМПЛЕКСООБРАЗОВАНИЕ ИОНОВ КОБАЛЬТА(II)
1475
(а)
(б)
λ, нм
λ, нм
Рис. 1. Электронные спектры поглощения сольватокомплексов Co2+ (а) и комплексов кобальта(II) с 4,4′-бипиридином
(4,4′-bpy): Co(4,4′-bpy)2+ (б) в диметилсульфоксиде (1), диметилацетамиде (2), диметилформамиде (3) и этаноле (4).
антибатность изменения констант устойчивости
та(II) (5 ммоль/л) и различными концентрациями
комплексов кобальта(II) с 4,4′-бипиридином и до-
4,4′-бипиридина (0-200 ммоль/л).
норных чисел растворителей [7]: с увеличением
Измерение спектров проводили в течение 5 мин
основности растворителя константы устойчивости
после приготовления растворов во избежание по-
комплексов уменьшаются. Следовательно, имен-
лимеризации (образования каркасных структур)
но сольватация катиона конкурирует с ацидоком-
при
25°С на прецизионном спектрофотометре
плексообразованием в рассмотренных системах
марки СФ-2000 в кварцевых кюветах толщиной
и определяет возможность формирования каркас-
1 см. Обработку результатов проводили с помощью
ных структур в этих системах.
программного обеспечения ReactLab Еquilibria.
В работе использовали реактивы: 4,4′-бипи-
ИНФОРМАЦИЯ ОБ АВТОРАХ
ридин
(>98%, Sigma-Aldrich), Co(ClO4)2∙6H2O
Жеребцова Марианна Михайловна, ORCID:
(>98%, Sigma-Aldrich), ДМСО (ХЧ, Ленреактив),
ДМФА (ХЧ, Ленреактив), диметилацетамид (ХЧ,
Невареактив), этанол (ХЧ, Ленреактив); растворы
Богачев Никита Александрович, ORCID: http://
с одинаковой концентрацией перхлората кобаль-
orcid.org/0000-0002-9495-0669
Скрипкин Михаил Юрьевич, ORCID: http://
orcid.org/0000-0001-9841-150X
Таблица 1. Полные константы образования комплексов
Мерещенко Андрей Сергеевич, ORCID: http://
кобальта(II) с 4,4′-бипиридином в различных раствори-
orcid.org/0000-0001-9390-1446
телях и донорные числа растворителей
ФОНДОВАЯ ПОДДЕРЖКА
Донорное число,
Растворитель
K1
ккал/моль
Работа выполнена при поддержке Российского
ДМСО
1.52±0.02
29.8
фонда фундаментальных исследований (проект
Диметилацетамид
2.04±0.01
27.8
№ 20-33-70025 «Стабильность») с использованием
ДМФА
3.03±0.05
26.6
оборудования ресурсного центра Научного парка
EtOH
3.28±0.02
19.2
Санкт-Петербургского государственного универ-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021
1476
ЖЕРЕБЦОВА и др.
ситета «Оптические и лазерные методы исследо-
3. Amiri N., Nouir S., Hajji M., Roisnel T., Guerfel T.,
Simonneaux G., Nasri H. // J. Saudi Chem. Soc. 2019.
вания вещества».
Vol. 23. N 7. P. 781. doi 10.1016/j.jscs.2019.03.003
КОНФЛИКТ ИНТЕРЕСОВ
4. Niu Y.-F., Cui L.-T., Han J., Zhao X.-L. // J. Solid
State Chem. 2016. Vol. 241. P. 18. doi 10.1016/j.
Авторы заявляют об отсутствии конфликта
jssc.2016.05.024
интересов.
5. Seetharaj R., Vandana P.V., Arya P., Mathew S. // Arab.
СПИСОК ЛИТЕРАТУРЫ
J. Chem. 2019. Vol. 12. N 3. P. 295. doi 10.1016/j.
arabjc.2016.01.003
1. Zhang Y.-S., Enright G. D., Breeze S. R., Wang S. // New
6. Safaei M., Foroughi M. M., Ebrahimpoor N., Jahani S.,
J. Chem. 1999. Vol. 23. P. 625. doi 10.1039/A900562E
Omidi A., Khatami M. // Trends Analyt. Chem. 2019.
2. Lu J., Yu C., Niu T., Paliwala T., Crisci G., Somosa F.,
Vol. 118. P. 401. doi 10.1016/j.trac.2019.06.007
Jacobson A. J. // Inorg. Chem. 1998. Vol. 37. P. 4637.
7. Marcus Y. Ions in solution and their solvation. Hoboken:
doi 10.1021/ic971614g
John Wiley & Sons, 2015. P. 82.
Complex Formation of Cobalt(II) Ions with 4,4′-Bipyridine
in Non-Aqueous Solvents
M. M. Zherebtsova, N. A. Bogachev, M. Yu. Skripkin, and A. S. Mereshchenko*
St. Petersburg State University, St. Petersburg, 199034 Russia
*e-mail: a.mereshchenko@spbu.ru
Received June 4, 2021; revised June 28, 2021; accepted July 3, 2021
The electronic absorption spectra of cobalt(II) complexes with 4,4′-bipyridine in non-aqueous solvents were
registered, and the stability constants of these complexes were determined. The values of stability constants
decrease by increase of the donor numbers of solvents.
Keywords: complex formation, 4,4′-bipyridine, cobalt, non-aqueous solvents, electronic absorption spectros-
copy
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021