ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2022, том 92, № 8, с. 1310-1324
УДК 539.23
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
И ТЕРМИЧЕСКИЕ ПРЕВРАЩЕНИЯ
АЛЮМИНИЙ-ВАНАДИЕВЫХ ОКСИДНЫХ
ТОНКИХ ПЛЕНОК
© 2022 г. А. И. Абдулагатовa, А. М. Максумоваa, Д. К. Палчаевa,
М. Х. Рабадановa, И. М. Абдулагатовa,*
a Дагестанский государственный университет, ул. Гаджиева 43а, Махачкала, 367000 Россия
*e-mail: ilmutdina@gmail.com
Поступило в редакцию 11 марта 2022 г.
После доработки 11 мая 2022 г.
Принято к печати 19 мая 2022 г.
Алюминий-ванадиевые оксидные (AlxVyOz) нанопленки получены методом атомно-слоевого осаждения
с использованием триметилалюминия, оксохлорида ванадия и воды. Рост пленок исследовали в режиме
in situ методом кварцевого пьезоэлектрического микровзвешивания и ex situ осаждением на Si(100).
При температуре осаждения 115°С наблюдали линейный рост пленок и самоограниченный характер
поверхностных реакций. Были получены два типа пленок Al2.1V0.4O4.1Cl0.1 и Al1.1V0.9O4.4Cl0.2, которые
имели аморфную структуру. Элементный анализ пленок показал присутствие ~2 ат% примесей хлора.
Термической обработкой пленок Al1.1V0.9O4.4Cl0.2 в интервале температур от 500 до 550°С на воздухе бы-
ли получены гетероструктурированные покрытия Al2O3-V2O5. Отжиг при 500°С привел к спонтанному
формированию кристаллического V2O5 путем образования переохлажденных нанокапель оксида ванадия.
При 550°С наблюдали формирование кристаллической нанопленки и монокристаллических нанонитей
V2O5. Термической обработкой при 630°С получены наноразмерные зародыши триклинного AlVO4.
Ключевые слова: атомно-слоевое осаждение, пленки AlxVyOz, монокристаллы V2O5, AlVO4, oртованадат
алюминия
DOI: 10.31857/S0044460X22080182, EDN: IQMDWS
Алюминий-ванадиевые смешанные оксиды
Ранее пленки AlxVyOz были получены из газо-
(AlхVyOz), гетерогенные смеси Al2O3-V2O5 и oрто-
вой фазы магнетронным [9] и импульсным лазер-
ванадат алюминия (AlVO4) применяются или име-
ным напылением [16], а также золь-гель методом
ют перспективы применения в качестве катализато-
в комбинации с центрифугированием [6]. В дан-
ров [1, 2], электродов литий-ионных батарей [3, 4],
ной работе впервые рассмотрен процесс получе-
активных материалов газовых сенсоров [5, 6],
ния тонких пленок AlхVyOz методом термического
ионных сепараторов [7] и высокотемпературной
атомно-слоевого осаждения. Под названием «мо-
сухой смазки [8, 9]. В числе особых свойств AlVO4
лекулярное наслаивание» метод атомно-слоевого
можно отметить аномалию Шотки в теплоемкости
осаждения был впервые разработан в начале 60-x
[10, 11]; привлекательным являются также про-
годов прошлого столетия [17, 18] советскими уче-
двинутые по сравнению с V2O5 фотоэлектронные
ными В.Б. Алесковским и С.И. Кольцовым [19, 20].
свойства [12, 13]. Легирование ионами Al3+ явля-
ется одним из способов управления температуры
Предлагаемый способ роста AlхVyOz можно
структурного фазового перехода в VO2 [14, 15].
представить как комбинацию двух процессов:
1310
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1311
атомно-слоевого осаждения Al2O3 и V2O5. Для
трического микровзвешивания. Химию по-
осаждения Al2O3 методами атомно-слоевого осаж-
верхностного процесса роста пленки Al2O3, со-
дения в качестве прекурсора алюминия ранее при-
стоящего из повторяющихся полуреакций между
менялись: хлорид алюминия, бромид алюминия,
триметилалюминием и H2O, можно представить
хлорид диметилалюминия, триметилалюминий,
следующим образом:
триэтилалюминий, этоксид алюминия, изопропок-
](-OH)x* + Al(CH3)3(г) → ](-O)x - Al(CH3)3-x*
сид алюминия и др. в комбинации с O2, H2O или
+ xCH4(г),
O3 [21]. Среди них наиболее изученным и широко
](-O)x - Al(CH3)3-x* + (3-х)H2O(г) → ](-O)х
используемым в атомно-слоевом осаждении про-
- Al(OH)3-х* + (3-x)CH4(г),
цессом роста Al2O3 является комбинация Al(CH3)3
и H2O. Химия поверхности Al2O3 считается
где ] - поверхность, * - поверхностные реакцион-
«эталонной» [22] и является относительно хорошо
ные группы, x - количество CH3-лигандов, высво-
изученной [23, 24]. Триметилалюминий является
бождаемых после напуска триметилалюминия или
привлекательным прекурсором алюминия ввиду
доля ОН-групп, реагирующих с одной молекулой
его высокой летучести, термической стабильности
триметилалюминия. В предложенных реакциях
и высокой реакционноспособности.
предполагается формирование стехиометрическо-
Оксиды ванадия методом атомно-слоевого
го Al2O3, и CH4 является единственным газофаз-
осаждения ранее получали с использованием: три-
ным продуктом реакции [27].
изопропоксида ванадия [VO(OC3H7)3], ванадила-
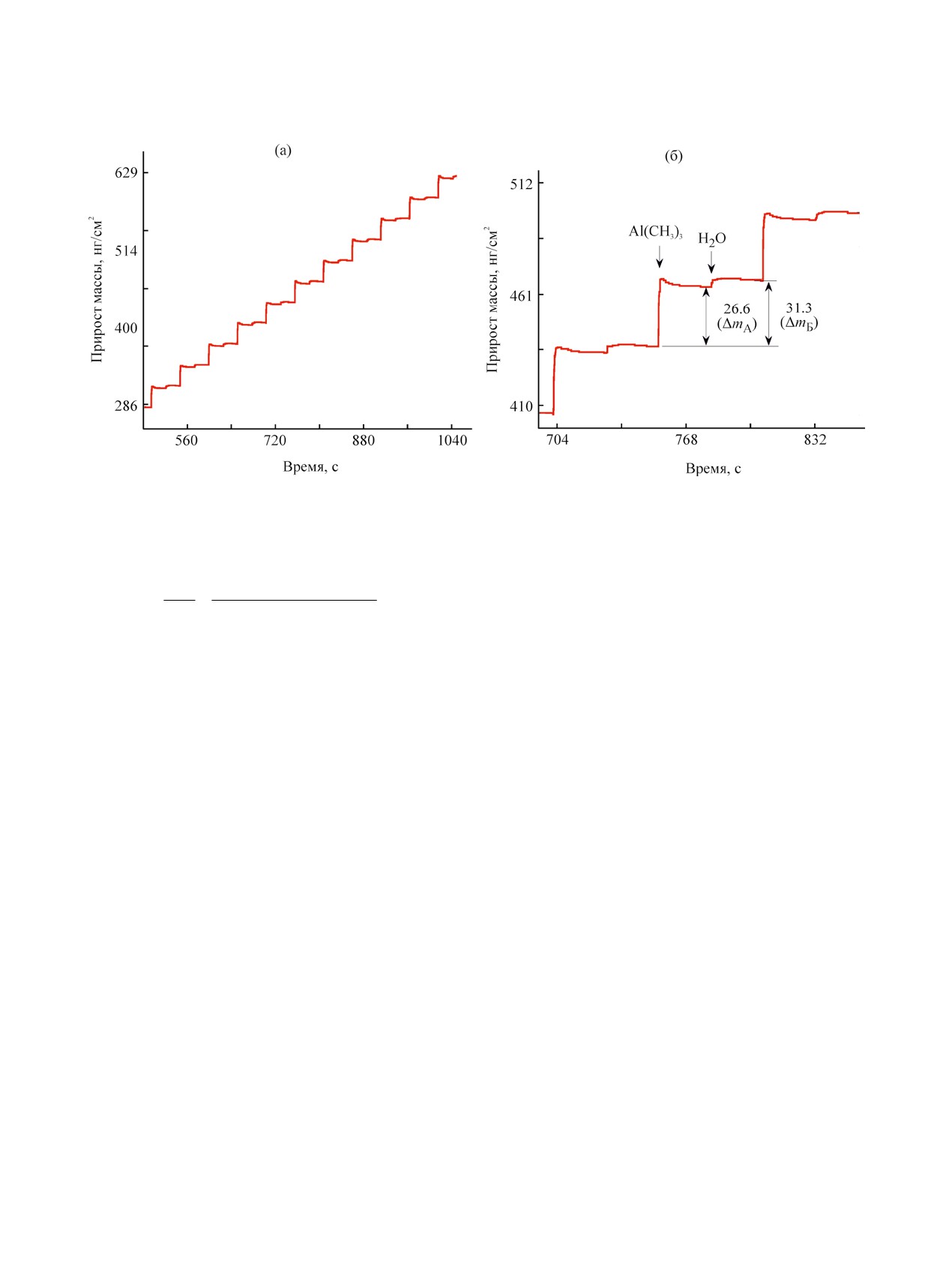
На рис. 1a приведены данные, полученные ме-
цетилацетоната [VO(acac)2], тетракис(этилметил-
тодом кварцевого пьезоэлектрического микровзве-
амино)ванадия(IV) [V(EtMeN)4], трис(диизопро-
шивания (КПМ), по изменению прироста массы
пилацетамидинат)ванадия(III)
[V(iPr-MeAMD)3],
для десяти циклов атомно-слоевого осаждения
а также оксобис(2,2,6,6-тетраметил-3,5-гептади-
Al2O3 при установившемся режиме формирования
онато)ванадия(IV) [VO(tmhd)2] в комбинации с
пленки (после нуклеации).
H2O, H2O2, О2 или O3 [25]. Несмотря на популяр-
ность данных металлоорганических соединений,
Осаждение проводили при 115°С и использова-
ли параметры цикла 1/25/1/25, где время напуска
их использование не редко ведет к формированию
пленок с примесями, что связанно с их низкой тер-
Al(CH3)3 и H2O составляло 1 с, время продувки -
мической стабильностью или реакционноспособ-
25 c. Представленные данные демонстрируют хо-
ностью [25]. В связи с этим, галогениды ванадия
рошо воспроизводимый прирост массы от цикла
обладают рядом преимуществ. Так, VOCl3 облада-
к циклу и линейность роста пленки со временем.
ет достаточным давлением паров при комнатной
Приближенный вид данных КПМ для трех циклов
температуре, термически стабилен и может быть
представлен на рис. 1б. Напуск Al(CH3)3 приводит
относительно легко синтезирован. Кроме этого по-
к приросту массы 26.6 нг/см2, а следующий за ним
верхностные реакции VOCl3 достаточно хорошо
напуск H2O - к увеличению на 4.7 нг/см2. Увели-
изучены [26].
чение массы после напуска H2O соответствует ме-
ханизму реакции, где поверхностные метильные
В данной работе атомно-слоевое осаждение
группы замещаются на гидроксильные. Получен-
AlxVyOz осуществляли с использованием в каче-
стве прекурсоров алюминия триметилалюминия,
ное значение общего прироста массы за цикл 31.3
ванадия - VOCl3, а кислорода - H2O. Комбина-
нг/см2 хорошо согласуется с ранее опубликован-
ция данных прекурсоров для осаждения пленок
ными значениями [22, 28]. Данное значение при-
AlxVyOz используется впервые. Целью данной
роста массы за цикл ниже расчетного для монос-
работы является изучение физико-химических
лоя α-Al2O3, равного 139.2 нг/см2, что говорит о
аспектов роста пленок AlхVyOz, формирования ге-
субмонослойном режиме роста пленки.
тероструктур Al2O3-V2O5 и AlVO4 отжигом на воз-
Используя полученные данные КПМ, из отно-
духе полученных пленок.
шения общего прироста массы, приходящегося на
Исследование атомно-слоевого осаждения
один цикл (ΔmБ), к приросту массы после напуска
Al2O3 и V2O5 методом кварцевого пьезоэлек-
Al(CH3)3 (ΔmА) из уравнения (1) получили x = 1.8.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1312
АБДУЛАГАТОВ и др.
Рис. 1. Данные КПМ по изменению прироста массы, наблюдаемого в процессе роста Al2O3 для 10 (а) и 3-х (б) циклов
атомно-слоевого осаждения при 115°С.
∆m
B
M
(AlO
1.5
)
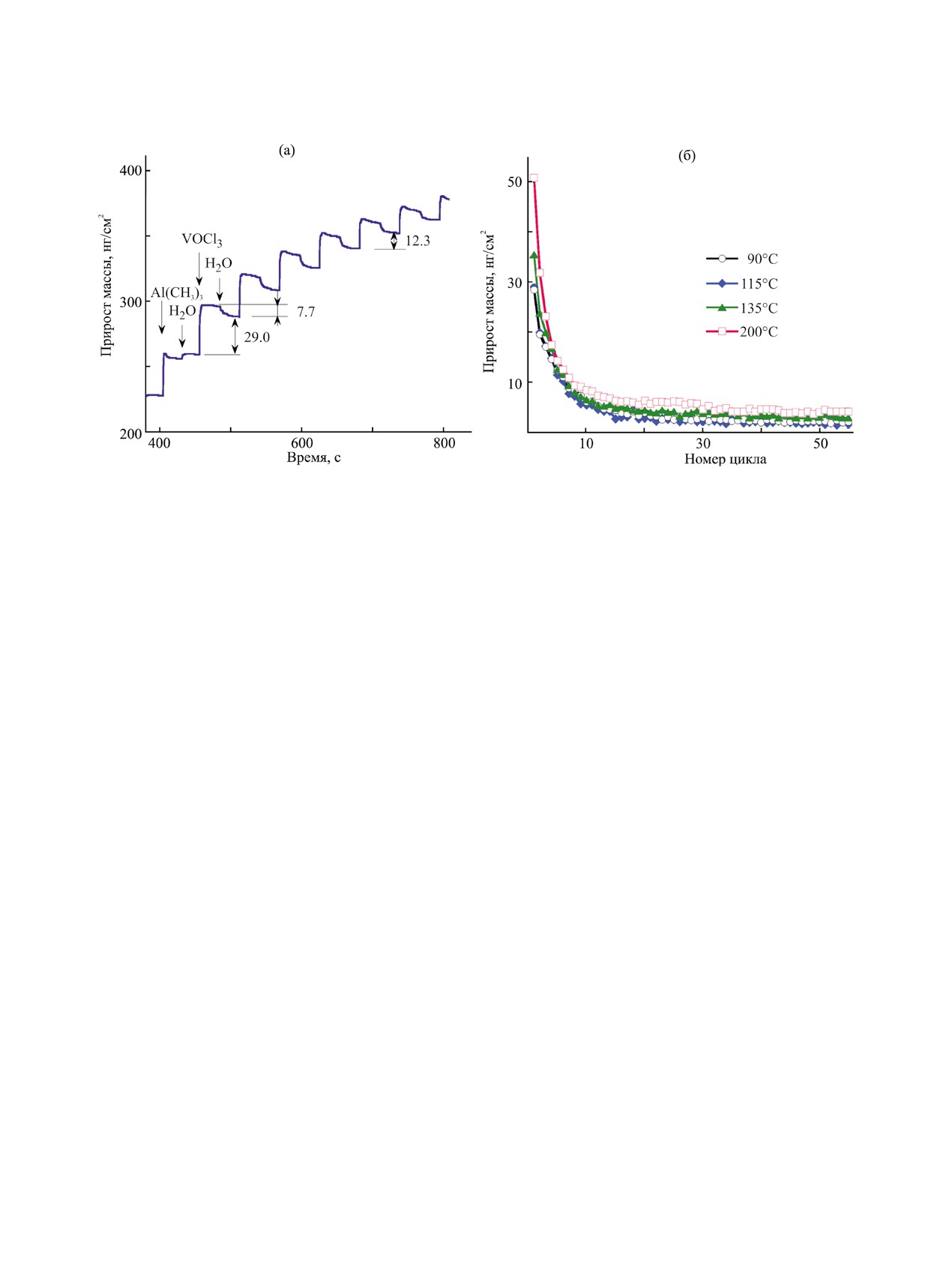
На рис. 2a представлены КПМ данные по изме-
=
,
(1)
∆m
M
[A
l(CH
)
]
− xM
(CH
)
нению массы в процессе атомно-слоевого осажде-
A
3
3
4
ния V2O5 на пленке Al2O3 при 115°С. На рисунке
также показан последний цикл атомно-слоевого
где М - молярная масса.
осаждения Al2O3.
Схожее значение х, равное ~1.7, было ранее
В процессе роста пленки использовали пара-
получено и в других работах для атомно-слоевого
метры цикла 3/30/3/30. Высокая концентрация по-
осаждения Al2O3 при 125°С [27]. Стехиометриче-
верхностных OH-групп и сорбированная вода на
ский Al2O3 образуется при значении x, равном 1.5,
Al2O3 способствуют значительному приросту мас-
что ниже экспериментальных. В связи с этим, фор-
сы во время первого цикла, равному 29.0 нг/см2.
мирование стехиометрического оксида алюминия
Снижение массы после напуска H2O соответствует
объясняли сопутствующими процессами деги-
процессу замещения поверхностных Cl-групп на
дроксилирования и удаления H2O [27].
гидроксильные. В отличие от процесса атомно-
Рост V2O5, состоящий из двух повторяющихся
слоевого осаждения Al2O3 (рис. 1а) с увеличени-
реакций VOCl3 и H2O, может быть представлен
ем количества циклов происходит затухание роста
следующим образом:
пленки; прирост массы на пятом цикле составил
12.3 нг/см2. На рис. 2б представлены данные по
](-OH)х* + VOCl3(г) → ](-O)х - VO(Cl)3-х* + хHCl(г),
изменению прироста массы за цикл от количества
](-O)х - VO(Cl)3-х* + (3-х)H2O(г) → ](–O)х
циклов VOCl3 и H2O при 90, 115, 135 и 200°С на
- VO(OH)3-х* + (3-х)HCl(г).
Al2O3. Вне зависимости от температуры осажде-
Здесь при взаимодействии VOCl3 с гидроксили-
ния, примерно после 15 циклов, прирост массы от
рованной поверхностью должен образоваться мо-
цикла к циклу становится незначительным и ста-
нослой ванадийоксохлоридных групп, а последу-
билизируется в пределах 2.5-7.5 нг/см2 в зависи-
ющий напуск H2O должен привести к замещению
мости от температуры. При этом прирост массы
хлор-лигандов на гидроксильные и, соответствен-
за цикл при 200°С был наибольшим. В процессе
но, регенерации первоначальных функциональ-
роста пленки на поверхности формируется по-
ных групп.
ливанадатный монослой с мостиковыми связя-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1313
Рис. 2. Данные КПМ, полученные в процессе атомно-слоевого осаждения оксида ванадия на пленке Al2O3: (а) прирост
массы со временем; (б) изменение прироста массы от цикла к циклу при температуре от 90 до 200°С.
ми [29, 30], что в итоге приводит к снижению
се осаждения 1Al1VО пленок при 115°С. При этом
количества гидроксильных групп, необходимых
использовали параметры цикла 1/30/3/30/2/30/3/30,
для продолжения роста пленки [31]. Общий при-
где Al(CH3)3 напускали в течение 1 с, VOCl3 - 2 с,
рост массы после 50 циклов составил примерно
H2O - 3 с. Время продувки составляло 30 с. Об-
150.4 нг/см2, что близко к расчетному значению
щий прирост массы в суперцикле составил
для одного монослоя кристаллического V2O5 [29].
75.6 нг/см2, где прирост массы после субцикла
Схожий механизм реакции VOCl3 с гидроксили-
Al(CH3)3/H2O составил 35.6 нг/см2, а VOCl3/H2O -
рованной поверхностью наблюдали в ряде других
40.0 нг/см2. Значения прироста массы после суб-
работ [26, 32]. Данные рис. 2 также указывают на
циклов Al(CH3)3/H2O и VOCl3/H2O были выше
то, что присутствие алюминийоксидных слоев
значений, полученных в процессax атомно-слое-
может обеспечить восстановление реакционных
вого осаждения Al2O3 (31.3 нг/см2, рис. 1б) и атом-
групп, необходимых для роста AlxVyOz.
но-слоевого осаждения V2O5 (2.5 нг/см2, рис. 2б)
Исследование роста пленок AlxVyOz методом
при тех же условиях.
кварцевого пьезоэлектрического микровзве-
Данные по зависимости прироста массы за су-
шивания. Атомно-слоевое осаждение AlxVyOz
перцикл от продолжительности напуска Al(CH3)3,
осуществляли за счет поверхностных реакций
VOCl3 и H2O приведены на рис. 5. Эксперимен-
паров Al(CH3)3, VOCl3 и H2O. Полученные плен-
ты проведены для определения самонасыщаемо-
ки обозначили как 1Al1VО и 1Al8VO, где коэф-
сти поверхностных реакций. Для этого исполь-
фициенты соответствуют количеству субциклов
зовали временной параметр одного суперцикла
Al(CH3)3/H2O и VOCl3/H2O в суперцикле атом-
s/30/1/30/s/30/1/30, где s - варьируемое время на-
но-слоевого осаждения. Для осаждения 1Al1VО
пуска триметилалюминия и VOCl3. Время напуска
использовали восьмиступенчатый суперцикл, со-
триметилалюминия и VOCl3 варьировали одно-
стоящий из поочередного напуска Al(CH3)3, H2O,
временно в интервале времени от 1 до 5 с. Как вид-
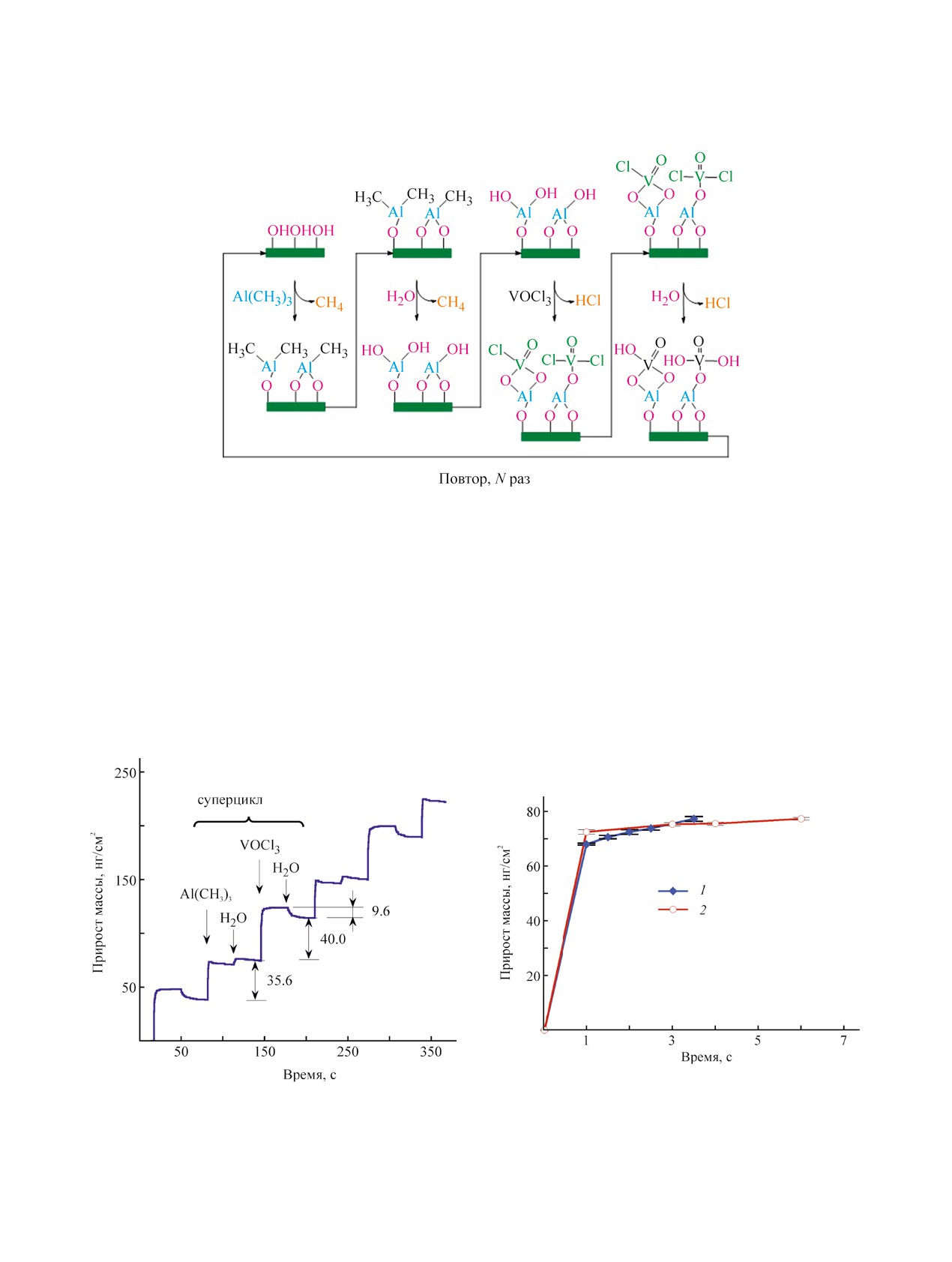
VOCl3, H2O и продувок между ними, что схема-
но из рис. 5, прирост массы за цикл медленно воз-
тично показано на рис. 3.
растает с увеличением времени напуска Al(CH3)3
На рис. 4 показаны КПМ данные по изменению
и VOCl3, что говорит о неидеальном самонасыще-
массы при напуске и продувке реагентов в процес-
нии. На рисунке также представлены результаты
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1314
АБДУЛАГАТОВ и др.
Рис. 3. Очередность подачи реагентов в суперцикле процесса атомно-слоевого осаждения AlxVyOz (1Al1VO).
для H2O. Эти данные получены для времени на-
использованием одного субцикла Al(CH3)3/H2O
пуска и продувки в суперцикле 1/30/s/30/1/30/s/30,
и 8 субциклов VOCl3/H2O в суперцикле (пленки
где s - варьируемое время напуска H2O. Получен-
1Al8VО). На рис. 6 приведены данные КПМ для
ная кривая насыщения для H2O показала самоо-
одного атомно-слоевого осаждения суперцикла
граниченный характер поверхностных процессов.
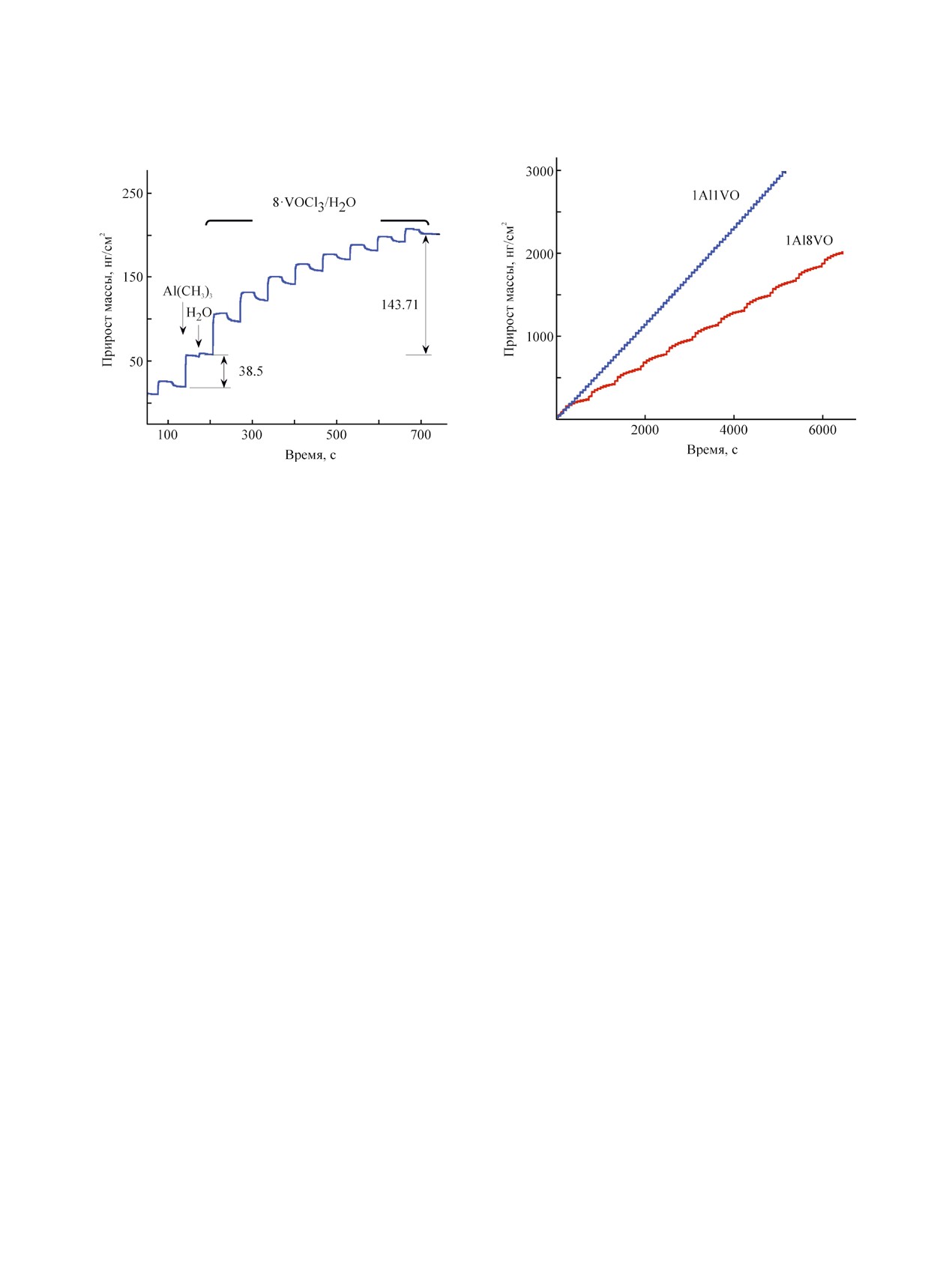
1Al8VО, проводимого с временными параметра-
Для увеличения содержания ванадия в полу-
ми напуска и продувки 2/30/3/30/[(1/30/3/30) × 8]
чаемых пленках осаждение проводили также с
при
115°С. Прирост массы после субцикла
Рис. 5. Данные КПМ по характеру насыщения VOCl3,
Рис. 4. Данные КПМ, полученные в процессе роста
Al(CH3)3 (1) и H2O (2), полученные для атомно-слоево-
AlxVyOz (1Al1VO) при 115°С.
го осаждения AlxVyOz (1Al1VO) при 115°С.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1315
Рис. 7. Зависимость прироста массы по времени в про-
Рис. 6. Сигнал КПМ в процессе одного суперцикла
цессе атомно-слоевого осаждения 1Al1VO и 1Al8VO
атомно-слоевого осаждения AlxVyOz (1Al8VО) при
при 115°С.
115°С.
Al(CH3)3/H2O составил 38.5 нг/см2, а после вось-
лены на рис. 7. Из рисунка видно, что рост пленок
ми VOCl3/H2O субциклов - 143.71 нг/см2. Прирост
имеет линейный характер. Угол наклона линии
массы после Al(CH3)3/H2O для 1Al8VО выше зна-
прироста массы для процесса 1Al1VО выше и,
чений для 1Al1VO и Al2O3, где эти значения рав-
соответственно, скорость роста пленки в данном
ны 35.6 и 31.3 нг/см2 соответственно. Значение
случае выше, чем для 1Al8VО.
количества CH3-лигандов, высвобождаемых после
Характеризация пленок AlхVyOz ex situ. Для
напуска Al(CH3)3 (значение х), рассчитанное для
ex situ анализа пленки осаждали на подложке
пленки 1Al8VО, приняло значение 1.5, что ниже в
Si(100) с естественным слоем оксида кремния при
сравнении с данными для атомно-слоевого осаж-
115°С. Временные параметры суперцикла для пле-
дения 1Al1VO (1.6) и Al2O3 (1.8), т. е. количество
нок 1Al1VО составляли 2/30/3.5/30/2/30/3.5/30, а
CH3-групп на поверхности после напуска Al(CH3)3
для 1Al8VО 1.5/30/3/30/[(4/30/3/30) × 8].
с введением VOCl3/H2O циклов увеличивается.
Эллипсометрия, анализ отражения и дифрак-
Предположительно, данное изменение химии по-
ции рентгеновских лучей. Постоянные роста, полу-
верхности субцикла Al(CH3)3/H2O связано со сни-
ченные с помощью анализа отражения рентгенов-
жением концентрации реакционных ОН-групп и
ских лучей, составили 2.5 и 5.5 Å/суперцикл для
протеканием поверхностных реакций за счет уве-
1Al1VО и 1Al8VО соответственно. Для сравнения:
личения концентрации терминального кислорода
постоянная роста для атомно-слоевого осаждения
ванадия, который может участвовать в формирова-
нии донорно-акцепторных (семиполярных) связей
Al2O3 при 115°С составляет примерно 1.0 Å/цикл.
типа (О)3≡V=O+--Al(CH3)3 за счет перехода пары
Из данных по отражению рентгеновских лучей,
свободных электронов ванадильной группы атому
плотность пленок 1Al1VО и 1Al8VО составила
алюминия. Возможность формирования схожих
3.23 и 3.24 г/см3 соответственно.
комплексов ранее демонстрировалась в реакциях
Для сравнения: плотность аморфной атом-
молекулярного наслаивания [26].
но-слоевого осаждения пленки Al2O3, полученной
КПМ данные по зависимости прироста массы
при той же температуре, равна 3.0 г/см3, а плот-
от времени осаждения в процессе атомно-слоевого
ность кристаллического V2O5 из справочных дан-
осаждения 1Al1VО и 1Al8VО при 115°С представ-
ных равна 3.35 г/см3 [33]. Значения постоянной
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1316
АБДУЛАГАТОВ и др.
роста (ПР) можно также получить расчетным пу-
тем из уравнения (2):
ПР = ΔmБ × ρ-1,
(2)
где ΔmБ - экспериментальное значение прироста
массы за один суперцикл (нг/см2), ρ - плотность
пленки из данных по отражению рентгеновских
лучей (г/см3). Расчетные значения постоянной ро-
ста составили 2.34 и 5.62 Å/суперцикл для 1Al1VО
и 1Al8VО соответственно, что близко к значениям,
полученным методом анализа отражения рентге-
новских лучей. Пленка 1Al1VО толщиной 312.65
Å имела среднеквадратичную шероховатость 5.14
Å, а пленка 1Al8VО толщиной 767.13 Å - 5.03 Å.
Показатели преломления для пленок 1Al1VО
и 1Al8VО при длине волны 633 нм составили
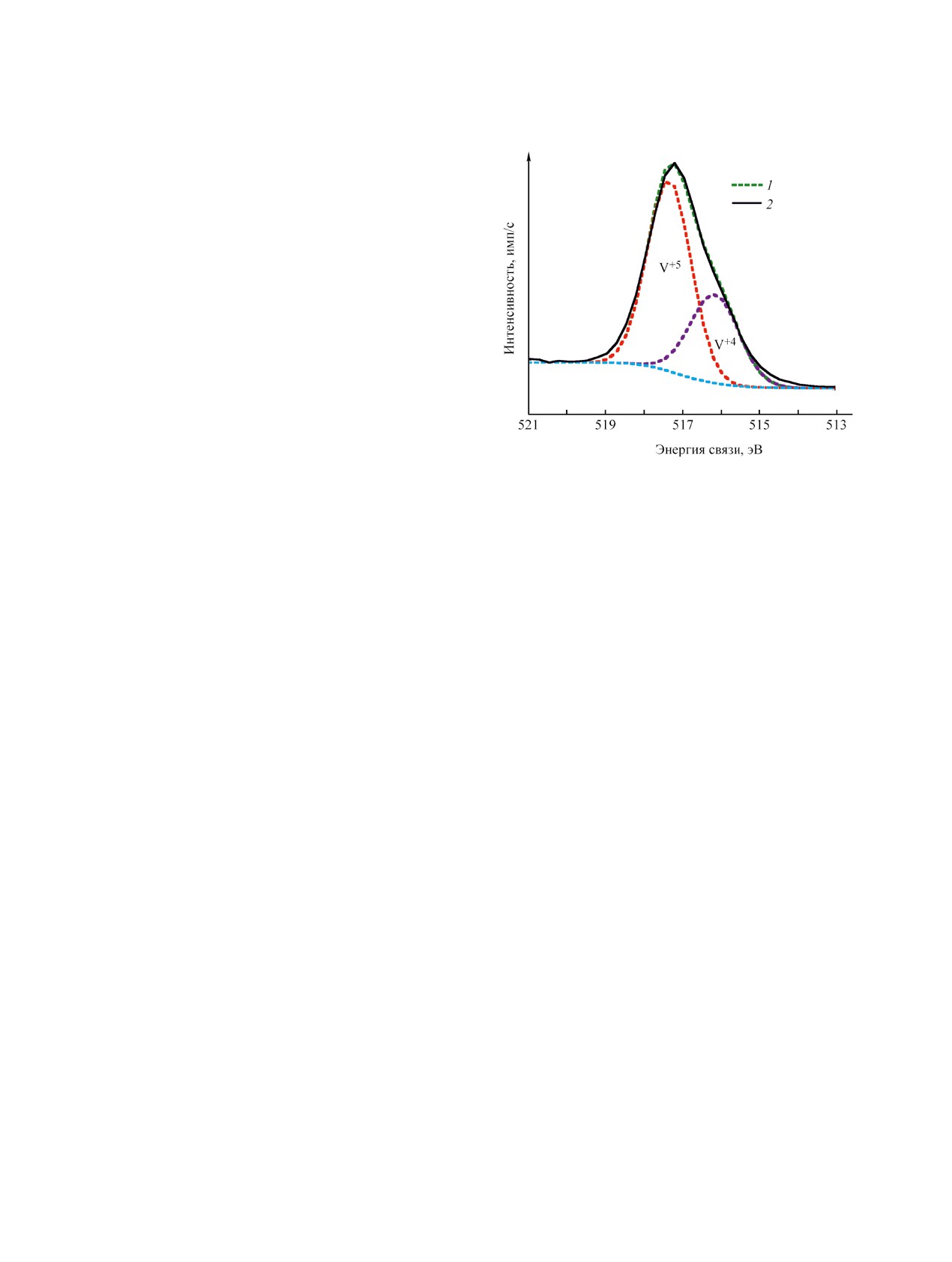
Рис. 8. Спектр РФЭС линии V2p3/2 высокого разреше-
1.76±0.1 и 2.04±0.1 соответственно. Для сравнения:
ния для пленки Al1.1V0.9O4.4Cl0.2. 1 - модель, 2 - данные
показатель преломления атомно-слоевого осажде-
РФЭС.
ния пленок Al2O3 составляет 1.58, а кристалличе-
ского V2O5 ~2.55 [34]. Показатели преломления
смешанных оксидов выше значения для Al2O3 и с
ния, не использовались для определения состава
увеличением содержания ванадия показатель пре-
пленок из-за возможного изменения процентного
ломления увеличивается. При оценке полученных
соотношения Al/V в пленке [37]. Примеси хлора в
данных надо учитывать, что показатель преломле-
образцах могут находиться как в форме не полно-
ния может зависеть от толщины пленки [35, 36].
стью гидратированных связей V-Cl, так и в виде
Дифракционный анализ полученных AlхVyOz
связей Al-Cl. Последние могут образоваться в ре-
пленок показал, что все они имели аморфную
зультате взаимодействия триметилалюминия с не
структуру.
полностью удаленным продуктом реакции (HCl)
Рентгеновская фотоэлектронная спектро-
по схеме:
скопия (РФЭС). Элементный анализ пленок для
Al(CH3)3(г) + 3HCl → AlCl3 + 3CH4(г),
пленки 1Al1VО показал следующий результат:
O (41.15 ат%), C (33.20 ат%), V (3.76 ат%), Al
где ∆G(150°С) = -154 ккал/моль. AlCl3 имеет темпе-
(20.69 ат%), Cl
(1.19 ат%), а для пленки
ратуру плавления 192.6°C [33], что выше темпера-
1Al8VО
- O
(44.33 ат%), C
(33.86 ат%), V
туры осаждения (115°С). Данная реакция может яв-
(9.41 ат%), Al (10.53 ат%), Cl (1.88 ат%). В соот-
ляться причиной неидеальной кривой насыщения
ветствии с данными РФЭС далее в статье пленки
для триметилалюминия и VOCl3, наблюдаемой на
1Al1VО будут обозначаться Al2.1V0.4O4.1Cl0.1, а
рис. 5.
1Al8VО - Al1.1V0.9O4.4Cl0.2. Увеличение количе-
Для детального определения химического со-
ства субциклов VOCl3/H2O от одного (1Al1VО) до
стояния ванадия в пленке Al1.1V0.9O4.4Cl0.2 провели
восьми (1Al8VО) привело к увеличению концен-
РФЭС сканирование высокого разрешения в обла-
трации ванадия примерно в 2.5 раза. Присутствие
сти V2p3/2 (рис. 8). Вычитание фонового состав-
примесей углерода обусловлено загрязнением
ляющего проводили методом Ширли. Разложение
поверхности образцов при контакте с воздухом в
функцией Гаусса фотоэлектронной линии пика
промежутке между осаждением и РФЭС-анали-
V2p3/2 показывает две компоненты, соответству-
зом. После распыления Ar+ концентрация углеро-
ющие состояниям окисления V4+ (517.34 эВ) и V5+
да была ниже чувствительности РФЭС. Данные
(516.16 эВ) соответственно [38]. Присутствие V4+
элементного анализа, полученые после распыле-
компоненты говорит о частичном восстановлении
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1317
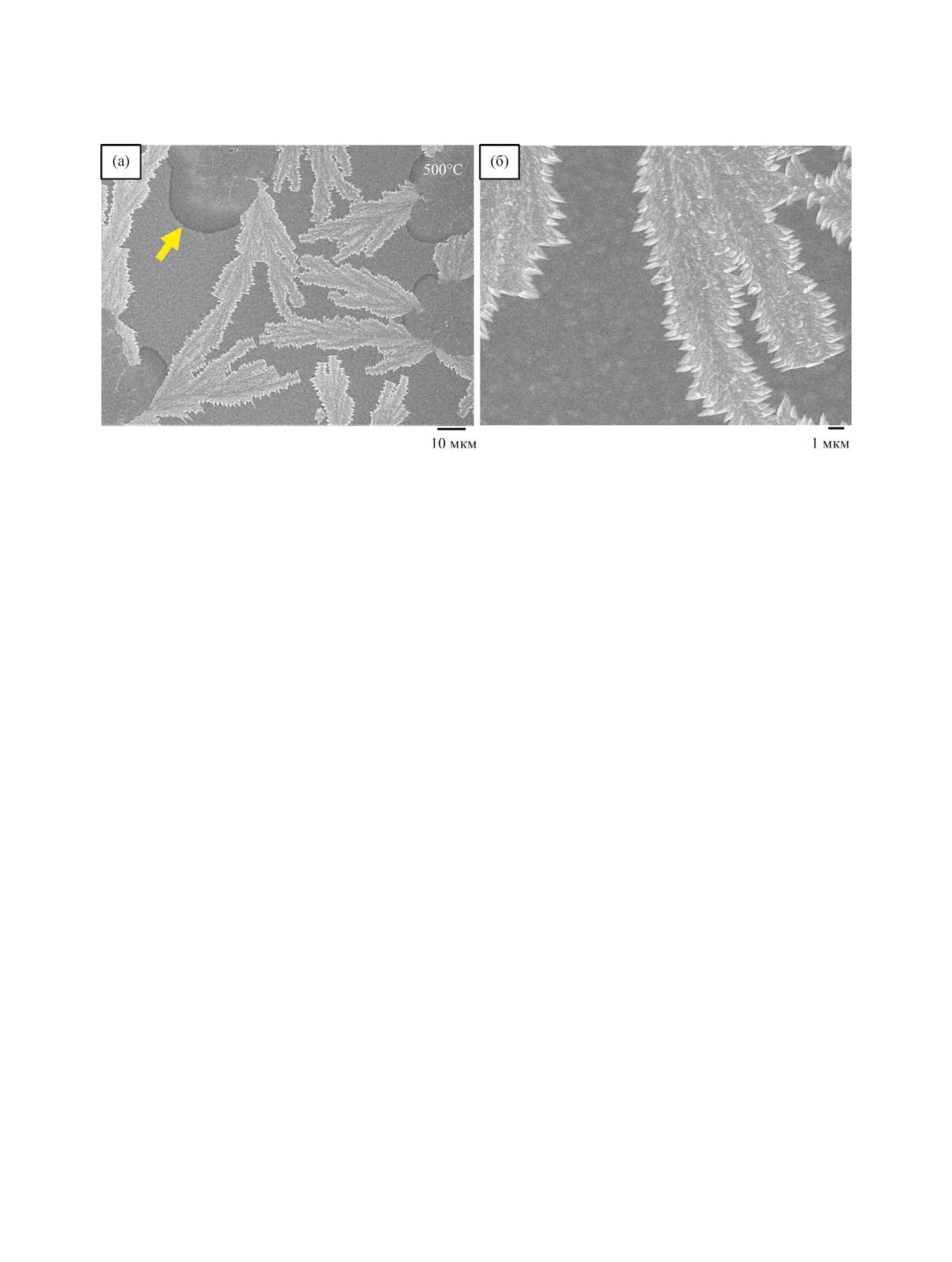
Рис. 9. РЭМ-Изображения поверхности пленки Al1.1V0.9O4.4Cl0.2 после отжига на воздухе в течение 2 ч при 500°С; (а) общий
вид, (б) приближенный вид той же подложки.
ванадия в процессе роста пленки. Из рисунка от-
ственно [46]. Данный процесс схож с процессами
носительная концентрация V+5 выше, чем V+4,
изоморфного замещения. В реакциях оксидов с
однако надо иметь ввиду, что при комнатной тем-
Al(CH3)3 эффект конверсии связывают с высокой
пературе на воздухе может произойти окисление
термодинамической стабильностью Al2O3 в срав-
поверхности пленки [38, 39], что может изменить
нении с конвертируемым оксидом [47]. Оксид
процентное соотношение V+5 и V+4. Восстанов-
алюминия имеет значение энергии Гиббса обра-
ление катионов оксидов металлов в реакциях с
зования (ΔG°f), равное -378.2 ккал/моль [48], что
Al(CH3)3 также наблюдали в ряде других работ
ниже значения -339.3 ккал/моль [48] для V2O5 и
[40-42].
говорит о термодинамически возможной конвер-
Для обоих типов пленок содержание алюминия
сии оксида ванадия. Одним из хорошо известных
превышает содержание ванадия. Используя урав-
примеров конверсии является процесс конверсии
нение, предложенное в работе [43], основанное
слоя ZnO в AlOx при росте атомно-слоевого осаж-
на правиле смесей и КПМ данных по приросту
дения пленок AlxZnyOz, которая выражалась поте-
массы для индивидуальных субциклов в суперци-
рей массы при напуске Al(CH3)3 на ZnO [46, 49].
кле, получили расчетное значение относительной
Как отмечалось ранее, необходимым условием
концентрации ванадия в сравнении с алюминием
конверсии является возможность оксида металла
для 1Al1VО, которое составило 0.55. Это значе-
образовывать летучие комплексные соединения с
ние выше экспериментально полученного из дан-
лигандами напускаемого газофазного прекурсора
ных РФЭС - 0.15. Схожее отклонение от правила
[46]. В данном случае напуск Al(CH3)3 ведет к уве-
смесей наблюдали и в других процессах осаж-
личению прироста массы. Это может говорить об
дения легированных и наноламинатных пленок
отсутствии химического механизма образования
[32, 44, 45]. Среди причин такого поведения си-
летучих комплексов ванадия с метильными груп-
стем называют так называемый эффект «конвер-
пами, которое ведет к частичному уменьшению
сии» [41, 46]. В общем виде конверсию оксидов
количества ванадия.
ранее представляли в виде реакции:
Отжиг AlxVyOz пленок. Полученные на крем-
ниевой подложке пленки подвергались терми-
MOw + NLx(г) → NOy + MLz(г),
ческой обработке в течение 2 часов на возду-
где M - металл исходного оксида, а N и L - ме-
хе при 450, 500, 550 и 630°С. Толщина пленок,
тал и лиганд напускаемого прекурсора, соответ-
использованных для отжига Al2.1V0.4O4.1Cl0.1 и
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1318
АБДУЛАГАТОВ и др.
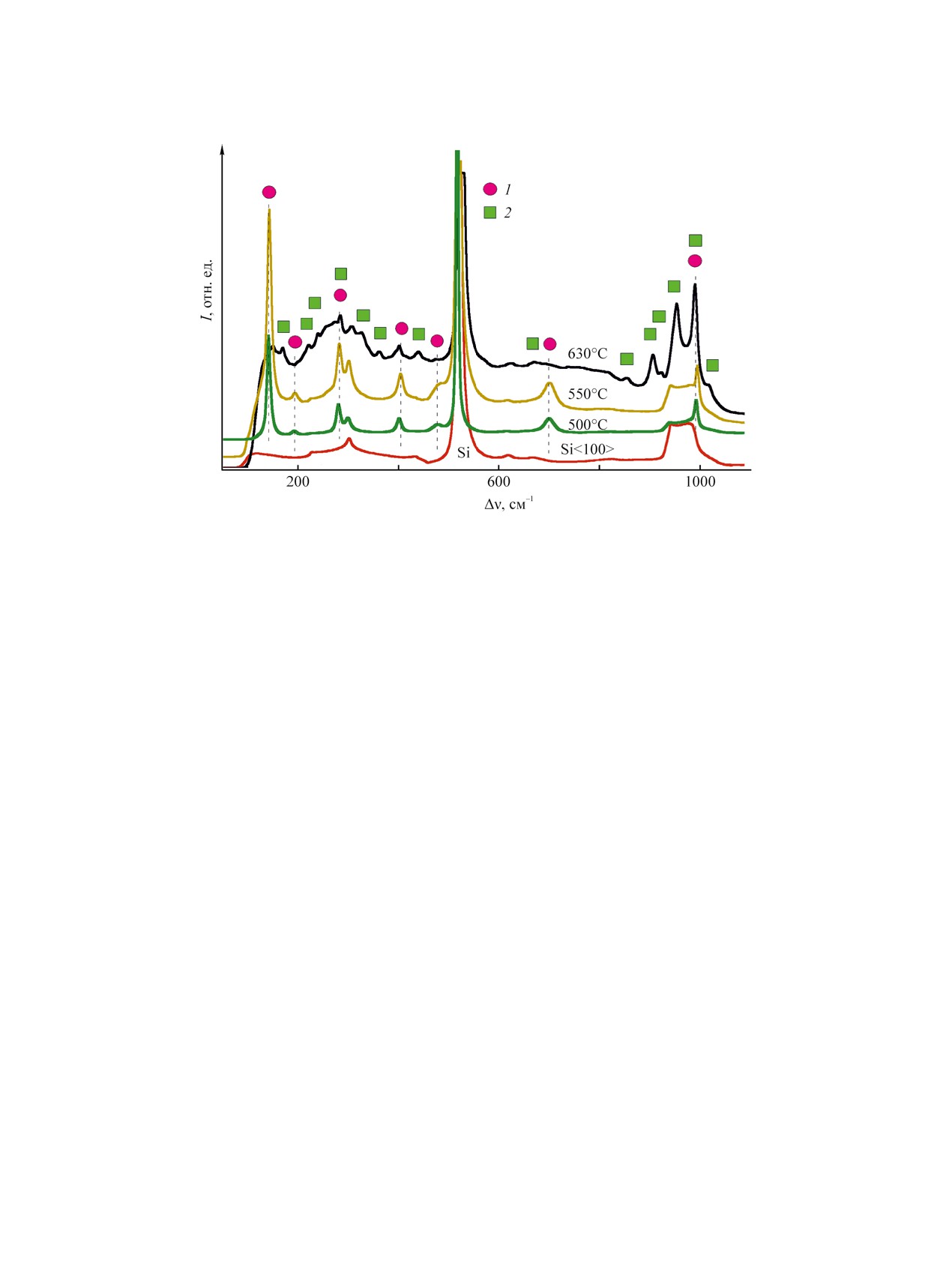
Рис. 10. Рамановские спектры атомно-слоевого осаждения пленок Al1.1V0.9O4.4Cl0.2 после отжига при 500, 550 и 630°C в
течение 2 ч на воздухе в сравнении со спектром подложки Si(100) без покрытия. 1 - орторомбический V2O5, 2 - триклин-
ный AlVO4.
Al1.1V0.9O4.4Cl0.2, составляла 312.65 и 767.13 Å
размера нагреваемых частиц [52].
соответственно. На рис. 9 приведены изображе-
Спонтанная кристаллизация и переохлажде-
ния, полученные с помощью растровой электрон-
ние капель происходит в результате увеличения их
ной микроскопии (РЭМ), поверхности пленки
размера, так как их температура плавления увели-
Al1.1V0.9O4.4Cl0.2 после отжига при 500°С. Здесь
чивается с увеличением размера, при этом размер
можно заметить структуры в виде капель (пока-
капель, предположительно, увеличивается за счет
зано стрелкой), соединенные с выростами, напо-
эффекта Оствальдовского созревания [53]. Комби-
минающими «куриные лапки», которые при рас-
нация направленного Оствальдовского созревания
смотрении в приближенном виде (рис. 9б) имеют
конденсированных из газовой фазы капель V2O5
грануловидную структуру. На рис. 10 представле-
на SiO2 и их последующее переохлаждение в ат-
ны рамановские спектры образцов Al1.1V0.9O4.4Cl0.2
мосфере инертного газа была ранее представле-
после термообработки при различных температу-
на как способ пространственно-контролируемого
рах в сравнении со спектром подложки Si(100) без
синтеза ряда нанонитей VO2 заданной длины [54].
покрытия. Спектральная картина образца после
Кроме этого появление капель оксида ванадия го-
отжига при 500°С указывает на формирование ор-
ворит о том, что покрытие может вести себя как
торомбической фазы монокристаллического V2O5
жидкая смазка, начиная при температурах значи-
[50]. Показанные на рис. 9 структуры представля-
тельно ниже температуры плавления V2O5 [33].
ют собой результат кристаллизации «переохлаж-
денных» капель оксида ванадия. Фазовая сепара-
На рис. 11 показана поверхность образца плен-
ция при данных условиях отжига согласуется с
ки Al1.1V0.9O4.4Cl0.2 после отжига при 550°С. На
данными фазовой диаграммы системы Al2O3-V2O5
поверхности сформировалась прерывистая плен-
[51]. V2O5 имеет относительно низкую температу-
ка, частично покрытая наноразмерными нитями
ру плавления, равную 690°С [33], однако образо-
и выростами в виде гребней. На рис. 11б можно
вание жидкой фазы может происходить задолго до
заметить пористую структуру подложки, образо-
достижения температуры плавления и зависит от
вавшуюся в результате фазовой сепарации. Пики
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1319
Рис. 11. РЭМ-Изображения поверхности пленки Al1.1V0.9O4.4Cl0.2 после отжига на воздухе в течение 2 ч при 550°С;
(а) общий вид, (б) приближенный вид той же подложки.
на рамановском спектре данного образца (рис. 10)
сильные силы сцепления с оксидом алюминия,
схожи с пиками орторомбического V2O5 после на-
чем с TiO2 [58].
грева при 500°С, но имеют более высокую интен-
На рис. 12 показана поверхность подложки по-
сивность. Присутствие орторомбического V2O5
сле отжига при 630°С. Подложка покрыта наноча-
подтверждается также дифракционными картина-
стицами удлиненной формы с длиной примерно от
ми, полученными рентгеновской дифрактометри-
5 до 15 мкм. Рамановские спектры данного образ-
ей (не показано). На рис. 11б наблюдается также
ца показали присутствие одновременно двух кри-
«достройка» нанонити V2O5 (указано стрелкой)
сталлических фаз: триклинного AlVO4 [59] и орто-
вдоль наиболее энергетически выгодной плоско-
ромбического V2O5 [50]. Таким образом, фазовая
сти <001> [55]. Как отмечалось ранее, монокри-
сепарация и следующая после этого твердофазная
сталлический V2O5 со своей слоистой структурой
реакция V2O5 + Al2O3 → 2AlVO4 ведет к образо-
играет роль активного материала в твердых тонко-
ванию зародышей кристаллического AlVO4. Веро-
пленочных смазках, содержащих ванадий [8].
ятно, формирование AlVO4 происходит только на
В нашей предыдущей работе при отжиге атом-
поверхности, где скорость диффузии значительно
но-слоевого осаждения пленок TixVyOz нанонити
выше, чем в толще пленки. Сложность синтеза
монокристаллического V2O5 формировались уже
AlVO4, вероятно, связана с перитектическим ха-
при 450°С за счет темплатного эффекта анатазного
рактером твердофазной реакции [60]. Возможно,
TiO2 [32, 56].
для формирования сплошной пленки требуется
более длительное время отжига [61, 62]. Форми-
По сравнению с TiO2-V2O5 формирование на-
рование AlVO4 согласуется с данным фазовой ди-
нонитей V2O5 в случае Al1.1V0.9O4.4Cl0.2, возмож-
аграммы для данной температуры, а также с экс-
но, связано с отсутствием темплатного эффекта
периментальными работами со спеканием частиц
(кристаллизация Al2O3 требует более высоких
Al2O3 и V2O5 [62].
температур) и низким значением поверхностного
натяжения Al2O3 (~68-70 × 10-6 Дж/см2) по срав-
Отжиг пленок Al1.1V0.9O4.4Cl0.2 при 450°С или
нению с TiO2 (~40 × 10-6 Дж/см2) [57], что может
Al2.1V0.4O4.1Cl0.1 при 500°С не привел к каким-
способствовать медленной диффузии атомов вана-
либо заметным изменениям на поверхности и к
дия, поскольку им необходимо преодолеть более
формированию кристаллической фазы.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1320
АБДУЛАГАТОВ и др.
Рис. 12. РЭМ-Изображения поверхности пленки Al1.1V0.9O4.4Cl0.2 после отжига на воздухе в течение 2 ч при 630°С;
(а) общий вид, (б) приближенный вид той же подложки.
В данной работе атомно-слоевое осаждение
лических нитей V2O5. В результате твердофазной
алюминий-ванадиевых смешанных оксидов про-
реакции Al2O3 и V2O5 при 630°С на поверхности
демонстрировано с использованием Al(CH3)3,
образовались наноструктуры, состоящие из заро-
VOCl3 и H2O. КПМ-Мониторинг атомно-слое-
дышей триклинного AlVO4.
вого осаждения процесса при 115°С показал ли-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
нейность роста пленок с количеством циклов и
самоограничиваемость поверхностных реакций.
Атомно-слоевое осаждение алюминий-ванади-
Несмотря на низкое значение постоянной ро-
евых оксидных пленок проводили на оборудова-
ста пленки V2O5 с использованием VOCl3 и H2O,
нии компании OOO «АСО НаноТех» (Махачкала,
VOCl3 показал высокую эффективность в процес-
Россия). Для осаждения использовали вакуумную
се роста AlxVyOz. По данным РФЭС концентрация
камеру с горячими стенками, которую продували
ванадия была ниже расчетного значения, исходя из
потоком инертного газа. В качестве газа носителя
правила смесей, что связывали с процессами кон-
использовали азот особой степени чистоты (ООО
версии пленки. Термическая обработка на воздухе
«Гермес-газ», 99.999%). Давление N2 в реакторе
Al1.1V0.9O4.4Cl0.2 пленок привела к наноструктури-
поддерживали около отметки ~1.0 Торр. Чисто-
рованию и формированию монокристаллов V2O5
та Al(CH3)3 (CAS 75241, Sigma-Aldrich) и VOCl3
за счет самоорганизации, что является примером
(CAS 7727186, Sigma-Aldrich) составляла ≥97.0 и
диссипативных систем. Отжиг при 500°С привел
99.0 соответственно. VOCl3 загружали в контей-
к фазовой сепарации Al2O3 и V2O5, формированию
нер для дозирования в атмосфере инертного газа.
на поверхности подложки капель оксида ванадия,
Воду использовали хроматографического класса
их переохлаждению и спонтанной кристаллиза-
чистоты (CAS 7732185, каталожный номер W5-1,
ции за счет увеличения их размера. Увеличение
Fisher Chemical). VOCl3 и H2O перед использова-
размера капель происходит по механизму остваль-
нием дегазировали. Все реагенты использовались
довского созревания. Данный эффект может быть
при комнатной температуре.
в дальнейшем использован для контролируемо-
го синтеза наноструктур кристаллического V2O5
Мониторинг процесса роста пленок проводили
или VO2. Отжиг при 550°С привел к усилению
в режиме реального времени с использованием in
фазовой сепарации, на поверхности образовалась
situ кварцевого пьезоэлектрического микровзве-
прерывистая пленка с выростами монокристал-
шивания (КПМ) [22]. Разрешение КПМ по массе
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1321
составляет ~0.3 нг/см2. Погрешности КПМ для ка-
на микрорамановском спектрометре Horiba Jobin
ждой из точек в кривых насыщения прекурсоров
Yvon с Ar+ лазером длиной волны 532 нм с разме-
рассчитывали по стандартным отклонениям ~10
ром пятна пробы ~1.7 мм. Мощность лазера - 50 мВт.
измерений. Для ex situ анализа полученных пленок
Время напуска и продувки прекурсоров во
в качестве подложек использовали полированные
время одного цикла атомно-слоевого осаждения
с одной стороны кремниевые пластины Si(100)
Al2O3 или V2O5 обозначали как t1/t2/t3/t4, где t1 -
размером 1.5 × 1.5 см со слоем естественного ок-
время напуска VOCl3 или Al(CH3)3, t2 и t4 - время
сида кремния толщиной ~20 Å. До использования
продувки, t3 - время напуска H2O. Один супер-
подложки очищали ацетоном, изопропанолом, де-
цикл атомно-слоевого осаждения AlxVyOz обозна-
ионизированной водой и высушивали в потоке N2
чали как t1/t2/t3/t4/t5/t6/t7/t8, где t1 - время напуска
(ОСЧ). До начала осаждения подложки выдержи-
Al(CH3)3; t2, t4, t6, t8 - время продувки; t3, t7 -
вали в реакционной камере в течение ~30 мин.
время напуска H2O, t5 - время напуска VOCl3. Со-
Спектроскопический эллипсометр (J.A. Woollam)
держание ванадия в пленках AlxVyOz варьировали
использовали для определения оптических свойств
изменением количества субциклов (t5/t6/t7/t8) в су-
полученных тонких пленок в диапазоне длин волн
перцикле. Парциальное давление Al(CH3)3 при на-
от 240 до 800 нм. Для моделирования оптиче-
пуске в течение 1 с составляло ~130 мТорр, H2O -
ских свойств использовали программное обеспе-
~50 мТорр. Парциальное давление VOCl3 при на-
чение и файлы, поставленные с эллипсометром
пуске в течение 3 с составляло ~10 мТорр, H2O -
(J.A. Woollam). Данные отражения и дифракции
~50 мТорр.
рентгеновских лучей получены с помощью диф-
ИНФОРМАЦИЯ ОБ АВТОРАХ
рактометра высокого разрешения (Bede D1, Bede
Scientific). Дифрактометр снабжен медным анодом
Абдулагатов Азиз Ильмутдинович, ORCID:
с длиной волны рентгеновского излучения λ 1.54 Å.
Ток нити накала составлял 40 мА при напряже-
нии 40 кВ. С помощью отражения и дифракции
org/0000-0002-3364-5927
рентгеновских лучей была получена инфор-
Рабаданов Муртазали Хулатаевич, ORCID:
мация о толщине, плотности, поверхностной
среднеквадратичной шероховатости и кристал-
лической структуре полученных пленок. Дан-
Абдулагатов Ильмутдин Магомедович, ORCID:
ные рентгеновской фотоэлектронной спектро-
скопии (Physical Electronics PHI Model
5600)
ФИНАНСОВАЯ ПОДДЕРЖКА
получены с использованием монохроматическо-
го AlKα-рентгеновского источника
(1486.6 эВ)
Работа выполнена при финансовой поддержке
с энергией прохода 187.0 эВ и размером шага
Министерства науки и высшего образования РФ
0.8 эВ. С помощью РФЭС определяли атомарный
в рамках государственного задания (FZNZ-2020-
состав и энергию связей в полученных пленках.
0002, А.М. Максумова, Д.К. Палчаев, И.М. Абду-
Отжиг пленок на воздухе проводили путем по-
лагатов).
мещения образцов в печь при заданной темпера-
КОНФЛИКТ ИНТЕРЕСОВ
туре, где выдерживали их в течение двух часов.
Точность поддержания температуры в печи со-
Авторы заявляют об отсутствии конфликта ин-
ставляла ±0.1°C. Одни и те же образцы не подвер-
тересов.
гали отжигу дважды. Изображения высокого раз-
решения поверхности атомно-слоевого осаждения
СПИСОК ЛИТЕРАТУРЫ
пленок до и после термической обработки были
1. Fu X.L., Tang W.M., Ji L., Chen S.F. // Chem. Eng. J.
получены растровым электронным микроскопом
2012. Vol. 180. P. 170. doi 10.1016/j.cej.2011.11.032
(РЭМ, JEOL JSM-7401F) с ускоряющим напря-
2. Scheurell K., Scholz G., Kemnitz E. // J. Solid State
жением в пределах 3.0-5.0 кВ и током пучка 1-
Chem. 2007. Vol. 180. N 2. P. 749. doi 10.1016/J.
10 А. Спектры комбинационного рассеяния сняты
JSSC.2006.12.003
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1322
АБДУЛАГАТОВ и др.
3.
Baddour-Hadjean R., Farcy J., Pereira-Ramos J.P.,
20.
Малыгин А.А. // Тезисы докл. III Международно-
Baffier N. // J. Electrochem. Soc. 1996. Vol. 143. N 7.
го семинара «Атомно-слоевое осаждение: Россия,
P. 2083. doi 10.1002/CHIN.199646019
2021». Санкт-Петербург, 2021. С. 13.
4.
Lim S.H., Kim D.H., Byun J.Y., Kim B.K., Yoon W.Y. //
21.
Ponraj J.S., Attolini G., Bosi M. // Crit. Rev. Solid
Electrochim. Acta. 2013. Vol. 107. P. 681. doi 10.1016/j.
State Mater. Sci. 2013. Vol. 38. N 3. P. 203. doi
electacta.2013.06.045
10.1080/10408436.2012.736886
5.
Palomares-Sánchez S., Chumakov Y., Ponce-
22.
Elam J.W., Groner M.D., George S.M. // Rev. Sci.
Castañeda S., Watts B., Leccabue F., Bocelli G. // J.
Instrum. 2002. Vol. 73. N 8. P. 2981. doi
Mater. Sci. 2007. Vol. 42. P. 8690. doi 10.1007/S10853-
10.1063/1.1490410
007-1800-X
23.
Puurunen R.L. // J. Appl. Phys. 2005. Vol. 97. N 12.
6.
Leyer B., Schmelz H., Gobel H., Meixner H., Scherg T.,
P. 121301. doi 10.1063/1.1940727
24.
George S.M. // Chem. Rev. 2010. Vol. 110. N 1. P. 111.
Knozinger H. // Thin Solid Films. 1997. Vol. 310.
doi 10.1021/cr900056b
N 1-2. P. 228. doi 10.1016/S0040-6090(97)00412-4
25.
Prasadam V.P., Bahlawane N., Mattelaer F., Rampel-
7.
Dhara S., Sarkar S., Basu S., Chattopadhyay P. //
berg G., Detavernier C., Fang L., Jiang Y., Martens K.,
Appl. Radiat. Isot. 2009. Vol. 67. N 10. P. 1764. doi
Parkin I., Papakonstantinou I. // Mater. Today
10.1016/j.apradiso.2009.05.005
Chem. 2019. Vol. 12. P. 396. doi 10.1016/J.
8.
Franz R., Mitterer C. // Surf. Coat. 2013. Vol. 228. P. 1.
MTCHEM.2019.03.004
doi 10.1016/J.SURFCOAT.2013.04.034
26.
Малыгин А.А. // ЖОХ. 2002. Т. 72. № 4. C. 617;
9.
Landälv L., Carlström C., Lu J., Primetzhofer D.,
Malygin A.A. // Russ. J. Gen. Chem. 2002. Vol. 72. N 4.
Jõesaar M., Ahlgren M., Gothelid E., Alling B.,
P. 575. doi 10.1023/A:1016344516638
Hultman L., Eklund P. // Thin Solid Films. 2019.
27.
Wind R.W., Fabreguette F.H., Sechrist Z.A., George S.M. //
Vol. 688. Article ID 137369. doi 10.1016/j.
J. Appl. Phys. 2009. Vol. 105. N 7. Article ID 074309.
tsf.2019.06.019
doi 10.1063/1.3103254
10.
Cheshnitskii S.M., Kozhevnikov V.L., Fotiev A.A. //
28.
Wind R.A., George S.M. // J. Phys. Chem. (A). 2010.
Inorg. Mater. 1985. Vol. 21. N 6. P. 854.
Vol. 114. N 3. P. 1281. doi 10.1021/jp9049268
11.
Cheshnitskii S.M., Kozhevnikov V.L., Fotiev A.A.,
29.
Weckhuysen B.M., Keller D.E. // Catal. Today. 2003.
Surat L.L. // Inorg. Mater. 1985. Vol. 21. N 2. P. 291.
Vol. 78. N 1-4. P. 25. doi 10.1016/S0920-
12.
Pradeep I., Kumar E.R., Suriyanarayanan N.,
5861(02)00323-1
Mohanraj K., Srinivas C., Mehar M.V.K. // New J.
30.
Haber J. // Catal. Today. 2009. Vol. 142. N 3-4. P. 100.
Chem. 2018. Vol. 42. N 6. P. 4278. doi 10.1039/
doi 10.1016/j.cattod.2008.11.007
C7NJ03607H
31.
Malygin A.A. // Compos. Interfaces. 1998. Vol. 5. N 6.
13.
Wang C.C., Lu C.L., Shieu F.S., Shih H.C. // Materials.
P. 561. doi 10.1163/156855498X00072
2021. Vol. 14. N 2. Article ID 359. doi 10.3390/
32.
Абдулагатов А.И., Максумова А.М., Палчаев Д.К.,
ma14020359
Рабаданов М.Х., Абдулагатов И.М. // ЖПХ. 2021.
14.
Macchesney J.B., Guggenheim H.J. // J. Phys. Chem.
Т. 94. № 7. С. 835; Abdulagatov A.I., Maksumova A.M.,
Solids. 1969. Vol. 30. N 2. P. 225. doi 10.1016/0022-
Palchaev D.K., Rabadanov M.Kh., Abdulagatov I.M. //
3697(69)90303-5
Russ. J. Appl. Chem. 2021. Vol. 94. N 7. P. 890. doi
15.
Liu K., Lee S., Yang S., Delaire O., Wu J.Q. //
10.1134/S1070427221070053
Mater. Today. 2018. Vol. 21. N 8. P. 875. doi 10.1016/J.
33.
CRC Handbook of Chemistry and Physics. Cleveland:
MATTOD.2018.03.029
CRC Press, 2007.
16.
Castro-Rodriguez R., Pena J.L., Ares O., Leccabue F.,
34.
Schneider K. // J.Mater Sci: Mater Electron. 2020.
Watts B.E., Melioli E. // Mater. Lett. 2005. Vol. 59.
Vol. 31. P. 10478. doi 10.1007/s10854-020-03596-0
N 24-25. P. 3027. doi 10.1016/S0924-4247(03)00233-4
35.
Jakschik U.S.S., Hecht T., Gutsche M., Seidl H.,
17.
Кольцов С.И. // Тезисы докл. Научно-технической
Bartha J.W. // Thin Solid Films. 2003. Vol. 425. P. 216.
конференции ЛТИ им. Ленсовета. Ленинград, 1963.
doi 10.1016/S0040-6090(02)01262-2
С. 27
36.
Kumar P., Wiedmann M.K., Winter C.H., Avrutsky I. //
18.
Кольцов С.И., Алесковский В.Б. // Тезисы докл. На-
Appl. Opt. 2009. Vol. 48. N 28. P. 5407. doi 10.1364/
учно-технической конференции ЛТИ им. Ленсовета.
AO.48.005407
Ленинград, 1965. С. 67
37.
Chenakin S.P., Silvy R.P., Kruse N. // J. Phys. Chem. (B).
19.
Malygin A.A., Drozd V.E., Malkov A.A., Smirnov V.M. //
2005. Vol. 109. № 30. P. 14611. doi 10.1021/JP051944J
Chem. Vap. Dep. 2015. Vol. 21. N 10-12. P. 216. doi
38.
Hryha E., Rutqvist E., Nyborg L. // Surf. Interface Anal.
10.1002/cvde.201502013
2012. Vol. 44. N 8. P. 1022. doi 10.1002/SIA.3844
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
АТОМНО-СЛОЕВОЕ ОСАЖДЕНИЕ
1323
39.
Tangirala M., Zhang K., Nminibapiel D., Pallem V.R.,
51.
Dąbrowska G., Tabero P., Kurzawa M. // J. Ph.
Dussarrat C., Cao W., Adam T., Johnson C.S., Elsayed-
Equilibria Diffus. 2009. Vol. 30. N 3. P. 220. doi
Ali H., Baumgart H. // ECS J. Solid State Sci. Technol.
10.1007/S11669-009-9503-4
2014. Vol. 3. N 6. P. N89. doi 10.1149/2.006406JSS
52.
Baletto F., Ferrando R. // Rev. Modern Phys. 2005.
40.
Bellenger F., Houssa M., Delabie A., Afanasiev V.,
Vol. 77. N 1. P. 371. doi 10.1103/REVMODPHYS.77.371
Conard T., Caymax M., Meuris M., Meyer K.De.,
53.
Kim M., Lee B., Lee S., Larson C., Baik J.M., Yavuz C.,
Heyns M.M. // J. Electrochem. Soc. 2008. Vol. 155.
Seifert S., Vajda S., Winans R., Moskovits M.,
N 2. P. G33. doi 10.1149/1.2819626
Stucky G., Wodtke A. // Nano Lett. 2009. Vol. 9. N 12.
41.
DuMont J.W., Marquardt A.E., Cano A.M., George S.M. //
P. 4138. doi 10.1021/nl902357q
ACS Appl. Mater. Interfaces. 2017. Vol. 9. N 11.
54.
Lee H., Yang U.J., Kim K.N., Park S., Kil K.H.,
P. 10296. doi 10.1109/EDTM50988.2021.9421056
Kim J.S., Wodtke A., Choi W., Kim M., Baik J.M. //
42.
Abdulagatov A.I., Sharma V., Murdzek J.A.,
Nano Lett. 2019. Vol. 19. N 7. P. 4306. doi 10.1021/acs.
Cavanagh A.S., George S.M. // J. Vac. Sci. Technol.
nanolett.9b00684
(A). 2021. Vol. 39. N 2. Article ID 022602. doi
55.
Glushenkov A.M., Stukachev V.I., Hassan M.F.,
10.1116/6.0000834
Kuvshinov G.G., Liu H.K., Chen Y. // Cryst. Growth Des.
43.
Larsson F., Keller J., Primetzhofer D., Riekehr L.,
2008. Vol. 8. N 10. P. 3661. doi 10.1021/cg800257d
Edoff M., Torndahl T. // J. Vac. Sci. Technol. (A). 2019.
56.
Vejux A., Courtine P. // J. Solid State Chem. 1978.
Vol. 37. N 3. Article ID 030906. doi 10.1116/1.5092877
Vol. 23. N 1-2. P. 93. doi 10.1016/0022-4596(78)90055-5
44.
Mackus A.J.M., Schneider J.R., MacIsaac C., Baker J.G.,
57.
Overbury S.H., Bertrand P.A., Somorjai G.A. //
Bent S.F. // Chem. Mater. 2019. Vol. 31. N 4. P. 1142.
Chem. Rev. 1975. Vol. 75. N 5. P. 547. doi 10.1021/
doi 10.1021/ACS.CHEMMATER.8B02878
CR60297A001
45.
Coll M., Napari M. // Apl. Mater. 2019. Vol. 7. N 11.
58.
Spivey J., Agarwal S., Knözinger H., Taglauer E. //
Article ID 110901. doi 10.1063/1.5113656
Catal. 1993. Vol. 10. P. 1. doi 10.1039/9781847553225-
46.
Myers T.J., Cano A.M., Lancaster D.K., Clancey J.W.,
00001
George S.M. // J. Vac. Sci. Technol. (A). 2021. Vol. 39.
59.
Brázdová V., Ganduglia-Pirovano M., Sauer J. // J.
N 2. Article ID 021001. doi 10.1116/6.0000680
Phys. Chem. (B). 2005. Vol. 109. N 1. P. 394. doi
47.
George S.M. // Acc. Chem. Res. 2020. Vol. 53. N 6.
10.1021/JP046055V
P. 1151. doi 10.1021/acs.accounts.0c00084
60.
Touboul M., Popot A. // J. Therm. Anal. Calorim. 1986.
48.
H. S. C. Chemistry. Version 10. Program for calculating
Vol. 31. N 1. P. 117. doi 10.1007/BF01913892
the thermodynamics of chemical reactions, 2020.
61.
Lewis D.B., Creasey S., Zhou Z., Forsyth J., Ehiasarian A.,
49.
Elam J.W., George S.M. // Chem. Mater. 2003. Vol. 15.
Hovsepian P., Luo Q., Rainforth W.M., Münz W. //
N 4. P. 1020. doi 10.1021/CM020607+
Surf. Coat. Technol. 2004. Vol. 177. P. 252. doi
50.
Su Q., Liu X.Q., Ma H.L., Guo Y.P., Wang Y.Y. // J. Solid
10.1016/J.SURFCOAT.2003.09.041
State Chem. 2008. Vol. 12. N 7-8. P. 919. doi 10.1007/
62.
Черницкий С.М., Фотиев А.А., Сурат Л.Л. // ЖНХ.
s10008-008-0515-5
1983. Т. 28. № 5. С. 1342.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1324
АБДУЛАГАТОВ и др.
Atomic Layer Deposition and Thermal Transformations
of Aluminum-Vanadium Oxide Thin Films
A. I. Abdulagatova, A. M. Maksumovaa, D. K. Palchaeva,
M. Kh. Rabadanova, and I. M. Abdulagatova,*
a Dagestan State University, Makhachkala, 367000 Russia
*e-mail: ilmutdina@gmail.com
Received March 11, 2022; revised May 11, 2022; accepted May 19, 2022
Aluminum-vanadium oxide (AlxVyOz) nanofilms were deposited by atomic layer deposition method using
trimethylaluminum, vanadium oxochloride and water. Film growth was studied using in situ quartz crystal
microbalance and ex situ analysis on Si(100). At a deposition temperature of 115°C, linear film growth and
a self-limiting nature of surface reactions were observed. Two types of amorphous films Al2.1V0.4O4.1Cl0.1
and Al1.1V0.9O4.4Cl0.2 were obtained. Elemental analysis of the films showed the presence of ~2 at% chlorine
impurities. By thermal treatment of Al1.1V0.9O4.4Cl0.2 films in the temperature range from 500 to 550°C in air,
Al2O3-V2O5 heterostructured coatings were obtained. Annealing at 500°C led to spontaneous formation of
crystalline V2O5 through the formation of supercooled vanadium oxide nanodroplets. At 550°C, the formation
of a crystalline nanofilm and single-crystal V2O5 nanowires was observed. Thermal treatment at 630°C yielded
nanosized nuclei of triclinic AlVO4.
Keywords: atomic layer deposition, AlxVyOz films, single crystal V2O5, AlVO4, aluminum orthovanadate
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022