ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2023, том 93, № 5, с. 717-729
547.784.1:[544.127+544.354.081.7]
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
1-ПРОПИЛИМИДАЗОЛ-4,5-ДИКАРБОНОВОЙ КИСЛОТЫ
© 2023 г. М. А. Брусина1,2, С. С. Лысова3, А. А. Оскорбин2, С. М. Рамш2,*
1 Институт экспериментальной медицины, Санкт-Петербург, 197022 Россия
2 Санкт-Петербургский государственный технологический институт (технический университет),
Московский пр. 24-26/49, Санкт-Петербург, 190013 Россия
3 Санкт-Петербургский государственный университет промышленных технологий и дизайна,
Санкт-Петербург, 191186 Россия
*e-mail: sramsh@technolog.edu.ru
Поступило в редакцию 31 марта 2023 г.
После доработки 4 мая 2023 г.
Принято к печати 6 мая 2023 г.
Изучены спектры ЯМР имидазол-4,5-дикарбоновой кислоты и ее 1-алкильных производных С1-С4 в
ДМСО-d6. Показано, что в данном растворителе эти соединения находятся в цвиттер-ионной форме.
Определены константы ионизации 1-пропилимидазол-4,5-дикарбоновой кислоты в воде и выполнено
их отнесение, совместимое с предположением о цвиттер-ионной форме данного соединения и в этом
растворителе. Квантово-химические расчеты подтвердили как это предположение, так и правильность
отнесения констант депротонирования, а также позволили выбрать из нескольких альтернативных струк-
тур предпочтительную цвиттер-ионную и моноанионную форму 1-пропилимидазол-4,5-дикарбоновой
кислоты.
Ключевые слова: 1-пропилимидазол-4,5-дикарбоновая кислота, спектроскопия ЯМР, прототропная тау-
томерия, константы ионизации, квантово-химические расчеты, высокоточные термохимические расчеты
DOI: 10.31857/S0044460X23050074, EDN: DCHIPQ
Глутаматергическая система является основ-
Алкилпроизводные имидазол-4,5-дикарбоно-
ной системой возбуждения в ЦНС, она участвует в
вой кислоты являются амфолитами. Медицинская
процессах обучения и формирования памяти. На-
химия соединения-амфолита не может обойтись
рушения в ее функционировании проявляются в
без знания о том, в какой молекулярной форме,
виде нейродегенеративных расстройств, однако их
нейтральной или цвиттер-ионной, оно находится
можно нивелировать с помощью лекарственных
в водном растворе. Без этого знания, например,
средств [1]. Поэтому поиск молекул, влияющих на
невозможно моделировать взаимодействие моле-
глутаматергическую систему, является актуальной
кулы-лиганда с мишенью в молекулярном докин-
задачей медицинской химии. Этот поиск ведется,
ге, оптимизировать соединение-хит или соедине-
в том числе, в ряду производных имидазол-4,5-ди-
ние-лидер. В рациональном дизайне лекарств не
карбоновой кислоты, которые, как известно, явля-
обойтись и без представления обо всех стадиях
ются лигандами глутаматергических рецепторов.
ионизации соединения-амфолита и определения
В частности, среди 1- и 2-алкилзамещенных ими-
констант ионизации этих стадий. Например, зна-
дазол-4,5-дикарбоновой кислоты найдены веще-
ние констант ионизации позволяет оценить соот-
ства, проявляющие как NMDA-агонистическую,
ношение между заряженными и незаряженными
так и NMDA-антагонистическую активность
молекулярными формами при различных значени-
[2, 3].
ях рН, а учет этого соотношения обязателен при
717
718
БРУСИНА и др.
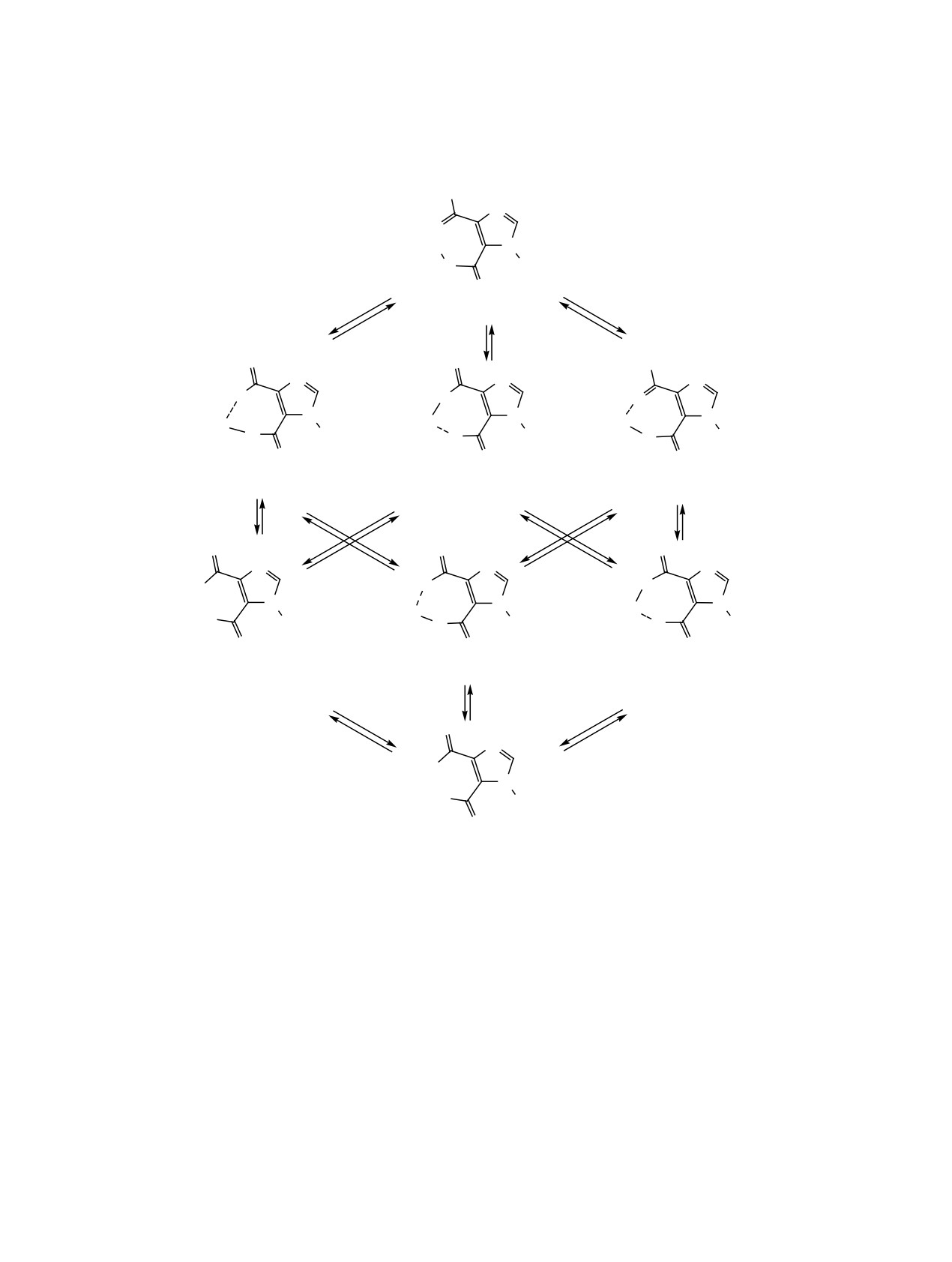
Схема 1.
HO
H
+
N
O
H
N
O
Pr
O
-H+
катион (K)
–H+
+H+
+H+
-H+
+H+
O
O
HO
H
H
+
+
N
N
N
–
O
O
O
N
N
N
H
H
H
–
O
Pr
O
Pr
O
Pr
O
O
O
цвиттер-ионная форма (ZI1)
цвиттер-ионная форма (ZI2)
нейтральная форма (N)
-H+
+H+
+
-H+
+H
+H+
+H+
+H+
+H+
O
-H+
-H+
-H+
-H+
O
H
O
+
N
N
N
–
-O
O
O
N
N
N
H
–
H
–
O
Pr
O
Pr
O
Pr
O
O
O
моноанион 2 (A2)
моноанион 1 (A1)
моноанион 3 (A3)
-H+
+H+
–H+
–H+
O
+
+H+
+H
N
-O
N
–
O
Pr
O
дианион (DA)
выяснении молекулярного механизма биологиче-
проведения оптимизации представляется 1-пропи-
ского действия. Константы ионизации позволя-
лимидазол-4,5-дикарбоновая кислота 1 [2, 4], что
ют рассчитать значение изоэлектрической точки
и предопределило ее выбор в качестве основного
цвиттер-ионного соединения, а этот параметр, на-
объекта данного исследования. Цель работы состо-
ряду с оценкой его ионного состава, необходимо
яла в изучении строения 1-алкилимидазол-4,5-ди-
учитывать при разработке препаративных, с мак-
карбоновых кислот в ДМСО-d6, определении и
симальными выходами, методов выделения цвит-
отнесении констант ионизации 1-пропилимида-
тер-ионного соединения из растворов, способов
зол-4,5-дикарбоновой кислоты 1 в воде, а также
получения его солей и т. п.
в выполнении квантово-химических расчетов мо-
В ряду алкилпроизводных имидазол-4,5-ди-
лекулярных и ионных форм этого соединения для
карбоновой кислоты наиболее подходящей для
оценки корректности интерпретации инструмен-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
719
Таблица 1. Характеристики спектров ЯМР соединений 1-8 в ДМСО-d6
№
δН, м. д.
δC, м. д.
1а
0.87 т (3H, CH2CH2CH3, J 7.6 Гц), 1.79 м (2H,
10.9 (CH2CH2CH3), 23.6 (CH2CH2CH3), 50.5
CH2CH2CH3), 4.49 т (2H, CH2CH2CH3, J 7.6 Гц), 4.65
(CH2CH2CH3), 127.1 (С5), 131.1 (С4), 138.3 (С2), 159.2
уш. с (2H, COOH, NH), 9.19 с (1H, CH)
(СООН), 159.7 (СООН)
2
3.81 с (6H, OCH3), 3.41 уш. с (1H, NH), 7.89 с (1H, CH)
52.4 (СООCH3), 52.5 (СООCH3), 130.2 (С5, С4), 138.6
(С2), 161.6 (СООCH3)
3
4.00 с (3H, CH3), 4.17 уш. с (2H, COOH, NH), 9.10 с
37.1 (CH3), 127.8 (С5), 130.6 (С4), 138.6 (С2), 159.4
(1H, CH)
(СООН), 159.8 (СООН)
4
1.39 т (3H, CH2CH3, J 7.2 Гц), 3.78 уш. с (2H, COOH,
16.2 (CH2CH3), 44.8 (CH2CH3), 127.1 (С5), 130.9 (С4),
NH), 4.49 кв (2H, CH2CH3, J 7.2 Гц), 9.17 с (1H, CH)
137.9 (С2), 159.1 (СООН), 159.6 (СООН)
5
0.89 т (3H, CH2CH2CH2CH3, J 7.4 Гц), 1.26 м (2H,
13.9 (CH2CH2CH2CH3), 19.4 (CH2CH2CH2CH3), 32.4
CH2CH2CH2CH3), 1.75 м (2H, CH2CH2CH2CH3), 3.75
(CH2CH2CH2CH3), 48.9 (CH2CH2CH2CH3), 127.2 (С5),
уш. с (2H, COOH, NH), 4.52 т (2H, CH2CH2CH2CH3, J
131.1 (С4), 138.3 (С2), 159.2 (СООН), 159.7 (СООН)
7.4 Гц), 9.19 с (1H, CH)
6
5.07 уш. с (2H, COOH, NH), 9.10 с (1H, CH).
129.2 (С5, С4), 136.0 (С2), 159.9 (СООН)
7б
0.80 т (3H, CH2CH2CH3, J 7.6 Гц), 1.71 м (2H,
11.1 (CH2CH2CH3), 24.4 (CH2CH2CH3), 48.6
CH2CH2CH3), 4.07 уш. с (2H, COOH, NH), 4.38 т (2H,
(CH2CH2CH3), 127.9 (С5), 137.6 (С4), 140.2 (С2), 161.5
CH2CH2CH3, J 7.6 Гц), 7.93 с (1H, CH)
(СООН), 164.6 (СООН)
8
0.82 т (3H, CH2CH2CH3, J 7.2 Гц), 1.69 м (2H,
11.2 (CH2CH2CH3), 24.5 (CH2CH2CH3), 48.3
CH2CH2CH3), 3.31 т (6H, CH2CH2OH, J 4.8 Гц), 3.74
(CH2CH2CH3), 55.5 (N+HCH2), 55.7 (CH2OH), 128.7
т (6H, CH2CH2OH, J 4.8 Гц), 4.33 т (2H, CH2CH2CH3,
(С5), 138.0 (С4), 140.1 (С2), 162.2 (СООН), 164.0
J 7.2 Гц), 5.17 уш. с (CH2CH2OH, COOH), 7.70 с (1H,
(СООН)
CH), 8.87 уш. с (1H, NH).
а δN, м. д.: 186.5 (N1), 188.5 (N3).
б δN, м. д.: 183.6 (N1), 248.5 (N3).
тальных данных и выявления особенностей его
Данные спектроскопии ЯМР 1Н свидетельству-
тонкого строения в водной среде, недоступных
ют в пользу того, что в ДМСО-d6 это соединение,
экспериментальному изучению.
действительно, находится в цвиттер-ионной фор-
ме. По сравнению с положением сигнала протона
Строение в растворах ДМСО-d6. Схема про-
тотропных превращений и ионизации 1-пропили-
имидазольного цикла С2Н 7.89 м. д. в спектре сое-
мидазол-4,5-дикарбоновой кислоты 1 изображена
динения 2, моделирующего нейтральную форму N
на схеме 1. В представляющем интерес для меди-
1-пропилимидазол-4,5-дикарбоновой кислоты 1, в
цинской химии диапазоне значений pH молекула
спектрах самой кислоты 1, ее гомологов (1-мети-
этого соединения имеет один центр протониро-
лимидазол-4,5-дикарбоновой кислоты 3, 1-этил-
вания - азагруппу (циклический атом азота пири-
имидазол-4,5-дикарбоновой кислоты 4 и 1-бутил-
динового типа), и два центра депротонирования -
имидазол-4,5-дикарбоновой кислоты 5), а также
карбоксильные группы. Качественная оценка
родительской имидазол-4,5-дикарбоновой кисло-
констант ионизации этих центров в воде (первое
ты 6 сигналы аналогичных протонов существен-
депротонирование вицинальных дикарбоновых
но смещены в слабое поле, в область от 9.10 до
кислот: pK1 1.94 у малеиновой, 2.76 у фталевой
9.19 м. д. (табл. 1). Но на вопрос о центре депро-
кислоты; протонирование имидазола: pKBH+ 6.95
тонирования - группа С4C(O)OH или C5C(O)OH -
[5]) приводит к предположению о цвиттер-ионном
анализ спектров ЯМР 1Н ответа не дает. Следует
строении
1-пропилимидазол-4,5-дикарбоновой
отметить, что спектры ЯМР на ядрах 13С и 15N
кислоты 1 с протонированным азотом N3 и депро-
(табл. 1) в плане выявления предпочтительной та-
тонированной карбоксильной группой.
утомерной формы изучаемого соединения - цвит-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
720
БРУСИНА и др.
Таблица
2. Энтальпии образования молекулярных
А3, но не А2. Действительно, сигнал цикличе-
форм 1-пропилимидазол-4,5-дикарбоновой кислоты 1
ского С2Н-протона в спектрах мононатриевой (7)
(обозначения молекулярных форм даны согласно схеме 1)
и триэтаноламмониевой соли
1-пропилимида-
Энтальпия образования,
зол-4,5-дикарбоновой кислоты (8) (табл. 1) реги-
Молекулярная
кДж/моль
стрируется при 7.93 и 7.70 м. д. соответственно.
форма
Эти значения очень близки к химическому сдвигу
G4
G4MP2
циклического С2Н-протона диметилового эфира
-701.4
-692.9
N
имидазол-4,5-дикарбоновой кислоты 2 (7.89 м. д.),
-660.9
-650.4
ZI1
моделирующего нейтральную форму 1-пропили-
–660.8
-650.5
мидазол-4,5-дикарбоновой кислоты N, тогда как у
ZI2
-743.9
-735.0
самой 1-пропилимидазол-4,5-дикарбоновой кис-
N в воде
лоты 1, ее гомологов 3-5 и родительской имида-
-753.9
-743.1
ZI1 в воде
зол-4,5-дикарбоновой кислоты 6, существующих
ZI2 в воде
-753.2
-742.4
в растворе в цвиттер-ионной форме, химические
сдвиги соответствующего протона лежат в диапа-
зоне 9.10-9.19 м. д. (табл. 1).
тер-ион или нейтральная молекула - неинформа-
Имеются и другие убедительные доказатель-
тивны.
ства того, что моноанион не может иметь строение
А2: квантово-химические расчеты свидетельству-
К сожалению, для изучения строения 1-про-
ют в пользу строения А3 (табл. 3), а по данным
пилимидазол-4,5-дикарбоновой кислоты 1 и ее
рентгеноструктурного анализа триэтаноламмони-
гомологов в водной среде спектроскопия ЯМР не
евой соли
1-пропилимидазол-4,5-дикарбоновой
подходит, поскольку растворимость в воде и самих
кислоты 8 [4] в кристаллической фазе строение
кислот, и ключевого модельного соединения - ди-
моноаниона может быть представлено как супер-
метилового эфира имидазол-4,5-дикарбоновой
позиция моноанионов А1 и А3 (нечто среднее
кислоты 2 - слишком низка для данного метода.
Однако результаты квантово-химических расчетов
между ними), с незначительным преобладанием
вклада моноаниона A31.
убедительно свидетельствуют в пользу существо-
вания 1-пропилимидазол-4,5-дикарбоновой кисло-
Кислотно-основные свойства. Кислотно-ос-
ты 1 в водном растворе в цвитттер-ионной форме
новные свойства
1-пропилимидазол-4,5-дикар-
(табл. 2). Изолированная нейтральная молекула N
боновой кислоты 1 были изучены в водных рас-
значительно стабильнее практически одинаковых
творах. Константы диссоциации pKa1 (первое
по стабильности изолированных цвиттер-ионных
депротонирование) и pKa2 (второе депротониро-
форм ZI1 и ZI2, но в воде ситуация обратная:
вание) были определены нами ранее кондуктоме-
цвиттер-ионные формы примерно на 10 кДж/моль
трическим методом, они составляют 3.58 и 7.65
стабильнее нейтральной, причем форма ZI1 с кар-
соответственно [4]. Эти значения практически
боксилатной группой в положении 4 на 0.7 кДж/
совпадают с найденными методом потенциоме-
моль стабильнее формы ZI2 с карбоксилатной
трического титрования значениями 3.60 и 7.67 для
группой в положении 5 гетероцикла.
1-метилимидазол-4,5-дикарбоновой кислоты 3 [6]
Для понимания механизма биологического
1 Положение оставшегося в депротонированном дикарбок-
действия полифункциональных амфолитов важно
сильном фрагменте водорода было достоверно определено из
знать строение не только молекулярных (электро-
разностного синтеза Фурье. Оказалось, что он локализован
нейтральных), но и ионных (заряженных) форм,
между кислородами карбоксилатных остатков таким обра-
в частности - анионов. Данные спектроскопии
зом, что в указанном фрагменте реализуется очень короткая,
ЯМР 1Н свидетельствуют о том, что в растворах
почти симметричная внутримолекулярная водородная связь
солей
1-пропилимидазол-4,5-дикарбоновой кис-
O-∙∙∙H+∙∙∙O- 2.42 Å, т. е. протон почти в равной мере связан с
лоты в ДМСО-d6 азагруппа моноаниона не несет
обоими карбоксилатными остатками: C4C(O)O-∙∙∙H+ 1.17 Å и
протона, т. е. моноанион имеет строение А1 или
C5C(O)O-∙∙∙H+ 1.25 Å.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
721
Таблица 3. Расчетные значения констант депротони-
ению соединений и не укладывающиеся в при-
рования 1-пропилимидазол-4,5-дикарбоновой кислоты
вычные представления. Действительно, для ими-
1 в воде (обозначения молекулярных и ионных форм
дазол-4-карбоновой кислоты, существующей в
даны согласно схеме 1).
цвиттер-ионной форме [10], константы ионизации
pKа
∆G0aq, кДж/моль
имеют следующие значения: константа депрото-
нирования pKa 6.15 [11] или, по другим данным,
Равновесие
6.26 [12] (относится к протонированному азоту);
G4
G4MP2
G4
G4MP2
константа протонирования pKBH+ 2.01 [12] (от-
носится к карбоксилатной группе). Эти значения
N-A3
1.98
2.37
11.3
13.6
близки к найденным нами для 1-пропилимида-
ZI1-A2
14.44
14.60
82.5
83.4
зол-4,5-дикарбоновой кислоты (1) второй кон-
ZI1-A3
3.52
3.58
20.1
20.5
станте депротонирования pKa2 7.65 [4] и констан-
ZI2-A2
14.36
14.53
82.0
82.9
те протонирования pKBH+ 2.20; такое совпадение
ZI2-A3
3.44
3.51
19.6
20.0
подталкивает к ошибочному заключению, что най-
денная нами первая константа депротонирования
1-пропилимидазол-4,5-дикарбоновой кислоты
1
и соотносятся со значениями 4.2 и 8.0 для 2-мети-
(pKa1 3.58 [4]) относится к отщеплению протона от
лимидазол-4,5-дикарбоновой кислоты и 4.0 и 7.8
анионного депротонированного дикарбоксильного
для имидазол-4,5-дикарбоновой кислоты 6 [7].
фрагмента, приводящему к образованию моноа-
ниона А2. То, что одноосновная имидазол-4-кар-
В работе [7] вопросы тонкого строения (прото-
боновая кислота является неподходящей моделью
тропной таутомерии) изученных имидазол-4,5-ди-
карбоновых кислот не обсуждались, и отнесение
для 1-пропилимидазол-4,5-дикарбоновой кислоты
1, обусловлено, в основном, двумя обстоятель-
констант депротонирования сделано не было. В
работах [6, 8, 9] константы pKa1 3.60 и pKa2 7.67
ствами: (1) моноанионы А1 и А3 стабилизированы
1-метилимидазол-4,5-дикарбоновой кислоты
3
сильной внутримолекулярной водородной связью
отнесены следующим образом: первое депрото-
в карбоксил-карбоксилатном фрагменте; (2) моно-
нирование с константой 3.60 соответствует отще-
анион А2 дестабилизирован наличием двух вици-
плению от цвиттер-иона типа ZI1 водородно-свя-
нальных карбоксилатных групп.
занного карбоксильного протона (т. е. отщеплению
Выше мы показали, что в воде и диметилсуль-
протона от анионного депротонированного дикар-
фоксиде
1-пропилимидазол-4,5-дикарбоновая
боксильного фрагмента) с образованием моноани-
кислота 1 присутствует в цвиттер-ионной форме.
она типа А2, а второе с константой 7.67 - отщепле-
Почему же при образовании моноаниона А1 из
нию протона от протонированного циклического
цвиттер-иона ZI1 или моноаниона А3 из цвит-
азота N3 этого моноаниона с образованием диа-
тер-иона ZI2 протон уходит от протонированного
ниона типа DA. Такое отнесение констант депро-
азота пиридинового типа N3H+, а не от карбок-
тонирования
1-метилимидазол-4,5-дикарбоновой
сильной группы? Мы полагаем, что акцепторная
кислоты 3 противоречит установленному нами
карбоксильная группа повышает кислотность
строению моноаниона гомологичной 1-пропили-
N3H+-центра в цвиттер-ионе соединения 1 (пони-
мидазол-4,5-дикарбоновой кислоты 1 как в рас-
жает основность пиридинового азота в моноани-
творе в ДМСО-d6 (табл. 1), так и в кристаллах (см.
оне) по сравнению с кислотностью аналогичного
работу [4]), подтвержденному квантово-химиче-
центра в цвиттер-ионе имидазол-4-карбоновой
скими расчетами (табл. 3), и, по нашему мнению,
кислоты; возможно, в еще большей степени по-
является ошибочным.
вышению кислотности N3H+-центра способствует
Следует подчеркнуть, что константы депро-
особая прочность короткой внутримолекулярной
тонирования имидазол-4,5-дикарбоновых кислот
водородной связи O-H∙∙∙O- в образующемся мо-
имеют аномальные значения, не совпадающие со
ноанионе А1 или А3. С другой стороны, в соот-
значениями констант ионизации близких по стро-
ветствии с хорошо известной закономерностью
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
722
БРУСИНА и др.
в ряду вицинальных дикарбоновых кислот [13],
Предложенное нами отнесение констант депро-
донорная карбоксилатная группа в цвиттер-ионе
тонирования 1-пропилимидазол-4,5-дикарбоновой
ZI1 или ZI2 понижает кислотность карбоксиль-
кислоты 1 согласуется с выявленным методами
ной группы по сравнению с таковой в катионе
спектроскопии ЯМР 1Н (табл. 1) и рентгенострук-
имидазол-4-карбоновой кислоты. Вероятно, даже
турного анализа [4] строением ее триэтаноламмо-
более существенную роль в понижении кислот-
ниевой соли 8. Действительно, при добавлении
ности карбоксильной группы цвиттер-иона 1-про-
в водный раствор 1-пропилимидазол-4,5-дикар-
пилимидазол-4,5-дикарбоновой кислоты 1 играет
боновой кислоты 1 триэтаноламина (pKBH+ 7.76
нестабильность моноаниона А2 с тремя заряжен-
[5, 15]) происходит отщепление протона от коль-
ными центрами, в том числе - с вицинальными
цевой NH+-группы (pKa1 3.58) с образованием со-
карбоксилатными группами, что подтверждается
ответствующего аммониевого катиона и одного
квантово-химическими расчетами (табл. 3). И на-
из возможных моноанионов, А1 или А3. К сожа-
конец, понижению кислотности карбоксильной
лению, из рентгеновских данных [4] не следует,
группы в какой-то мере должна способствовать
какого из них именно: как уже было отмечено (см.
внутримолекулярная водородная связь O-H∙∙∙O- в
сноску 1), в кристалле триэтаноламмониевой соли
цвиттер-ионе.
8 строение моноаниона представляет собой нечто
Итак, определенная нами константа первого
среднее между А1 и A3, с незначительным преоб-
депротонирования
1-пропилимидазол-4,5-дикар-
ладанием вклада моноаниона A3. Однако кванто-
боновой кислоты 1 pKa1 3.58 относится к отще-
во-химические расчеты свидетельствуют в пользу
плению протона от кольцевой N3H+-группы цвит-
формы А3 в водном растворе (табл. 3). Следует
тер-ионной формы (т. е. от протонированного
отметить, что при получении триэтаноламмоние-
пиридинового азота); таким образом, основность
вой соли 8 второе депротонирование должно быть
пиридинового азота N3 в моноанионе 1-пропи-
незначительным, даже если использовать дву-
лимидазол-4,5-дикарбоновой кислоты 1 почти на
кратный избыток триэтаноламина, поскольку его
3 порядка меньше его основности в анионе ими-
основность недостаточна для ионизации карбок-
дазол-4-карбоновой кислоты - 3.58 против 6.26
сильной группы моноаниона (pKa2 7.65).
[12]. Соответственно, константа второго депро-
Оценочное значение pKa депротонирования
нирования pKa2 7.65 относится к отщеплению
цвиттер-ионов ZI1 и ZI2 с образованием моноани-
протона от карбоксильной группы в моноанионе
она А2, полученное расчетными методами, состав-
А1 или А3 (по расчетам - А3, см. табл. 3). Это
ляет порядка 11.5 (табл. 3), что также подтвержда-
больше значений pKa2 для второго депротониро-
ет правильность нашего отнесения констант
вания вицинальных дикарбоновых кислот: суще-
депротонирования
1-пропилимидазол-4,5-дикар-
ственно больше, чем у малеиновой (6.22) и фта-
боновой кислоты 1.
левой кислоты (4.92) [5], и немного больше, чем
Константа протонирования
1-пропилимида-
у циклопент-1-ен-1,2-дикарбоновой кислоты (pK1
зол-4,5-дикарбоновой кислоты 1, определенная
1.64, pK2 7.27) [14], что может быть связано с по-
нами по методу [16, 17], составляет 2.20. Даже с
вышенной стабильностью моноанионов А1 и А3,
учетом всех отмеченных выше факторов пониже-
обусловленной в первую очередь уже упомянутой
ния основности такая величина слишком низка для
аномально сильной внутримолекулярной водород-
основности пиридинового азота N3 этого соедине-
ной связью O-H∙∙∙O- в депротонированном дикар-
ния, поэтому данная константа наверняка отно-
боксильном фрагменте. Действительно, как пока-
сится к протонированию карбоксилатной группы
зано в работе [14], степень внутримолекулярного
в цвиттер-ионе, что, в свою очередь, является еще
водородного связывания O-H∙∙∙O- в моноанионах
одним экспериментальным доказательством цвит-
1,2-дикарбоновых кислот максимальна при длине
тер-ионного строения 1-пропилимидазол-4,5-ди-
водородной связи около 2.45 Å, а определенная из
карбоновой кислоты 1 в водном растворе.
дифракционных данных длина водородной связи
O-H∙∙∙O- в моноанионе 1-пропилимидазол-4,5-ди-
Таким образом, в кислой среде происходит
карбоновой кислоты 1 2.42 Å [4] близка к указан-
присоединение протона к карбоксилатной груп-
ной величине.
пе цвиттер-иона ZI1 или ZI2 (по расчетам - ZI1,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
723
ствии с теорией атомов в молекуле Бейдера (AIM).
Сканирование поверхности потенциальной
энергии различных молекулярных форм 1-пропи-
лимидазол-4,5-дикарбоновой кислоты 1 показало
идентичные результаты, поэтому ниже обсужда-
ются только таковые, полученные для цвиттер-
ионной формы ZI1 с учетом растворителя (вода).
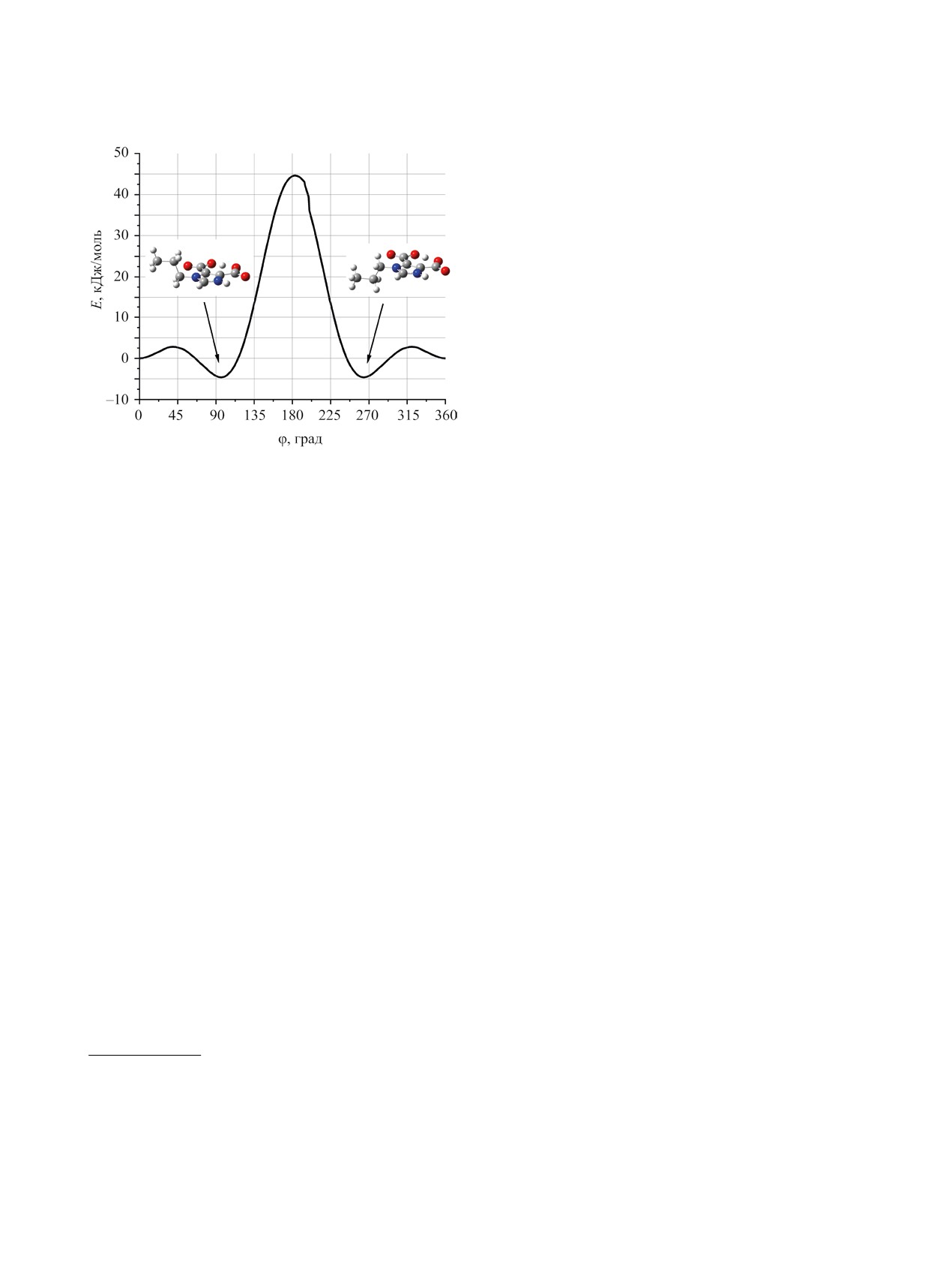
Сечение поверхности потенциальной энергии
представлено на рис. 1.
Минимуму энергии при значениях двугранного
угла между плоскостью гетероциклического фраг-
мента молекулы и плоскостью пропильной группы
0 и 360° соответствует конформация с расположе-
нием всех трех атомов пропильной группы в пло-
скости гетероцикла и ориентацией этой группы в
Рис. 1. Сечение поверхности потенциальной энер-
сторону от карбоксильной группы C5СООН (пла-
гии 1-пропилимидазол-4,5-дикарбоновой кислоты 1,
полученное путем сканирования для цвиттер-ионной
нарная конформация P1); этот минимум принят за
формы ZI1 с учетом растворителя - воды.
нулевое значение. Минимумам энергии при ~97
и ~264° соответствуют конформации, у которых
пропильная группа практически перпендикулярна
см. табл. 2) и образуется катион K (pKBH+ 2.202).
плоскости гетероцикла (две ортогональные кон-
В щелочной среде происходит последовательное
формации O1 и O2, соответственно). Эти конфор-
депротонирование N3H+-центра цвиттер-иона с
мации имеют энергию на ~4.6 кДж/моль меньше,
образованием моноаниона А1 или А3 (pK1 3.583)
чем планарная конформация P1.
(по расчетам - А3, см. табл. 3) и карбоксильной
Максимум при двугранном угле 180° с энерги-
группы моноаниона с образованием дианиона DA
ей 44.6 кДж/моль соответствует планарной кон-
(pK2 7.65).
формации P2 с пропильной группой, развернутой
Квантово-химические расчеты. Для под-
в сторону к карбоксильной группе C5СООН. Такая
тверждения правильности отнесения экспери-
конформация может возникнуть при повороте про-
ментальных констант ионизации 1-пропилимида-
пильной группы из положения над циклом в поло-
зол-4,5-дикарбоновой кислоты 1, а также с целью
жение под циклом через сторону карбоксильной
выяснения преобладающей таутомерной формы
группы при атоме C5 цикла, и резкое увеличение
этого соединения в водной среде были выполнены
энергии происходит из-за нарастающего электро-
следующие теоретические расчеты: оптимизация
статического отталкивания пропильной и карбок-
геометрии молекулярных структур, изображенных
сильной групп. При обычных температурах такой
на схеме 1, со сканированием поверхности потен-
переход маловероятен. Повороту в противополож-
циальной энергии с целью поиска глобального ми-
ную от карбоксильной группы C5СООН сторону
нимума методом теории функционала плотности
соответствует меньший по величине барьер - при-
(DFT) на уровне теории B3LYP/6-311G(d,p); высо-
мерно 2.8 кДж/моль, что сравнимо с кинетической
коточные термохимические расчеты методом ато-
энергией движения молекулы при 298 K.
мизации с использованием результатов расчетов
методами G4 и G4MP2; топологический анализ
Рассчитанное по распределению Больцмана
распределения электронной плотности в соответ-
отношение содержания конформеров в смеси ор-
тогональные конформеры O1 и O2 - планарный
2 Соответствует pKa кислотной ионизации вещества в терми-
конформер P1 составляет 76:24. Далее термохи-
нах руководства [13].
мические данные приводятся для конформеров с
3 Соответствует pKa основной ионизации вещества в терминах
меньшей энергией - ортогональных конформеров
руководства [13].
O1 и O2.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
724
БРУСИНА и др.
Таблица 4. Характеристики критических точек связи в молекулярных формах 1-пропилимидазол-4,5-дикарбоновой
кислоты 1 в водном окруженииа
Молекулярная
Связь
∇
2(ρ), Å-5
ε
ρ, Å-3
H, а. е.
форма
C4С(О)О-Н
-2.770
0.012
0.368
-0.763
Нейтральная N
C5C(O)OH···OC(OH)C4
0.127
0.009
0.065
-0.019
C5С(О)О-Н
-2.314
0.010
0.328
-0.658
N+-H
-2.077
0.025
0.349
-0.563
Цвиттер-ионная
C5C(O)OH···O-(O)C4
0.028
0.016
0.102
-0.061
ZI1
C5С(О)О-Н
-1.464
0.009
0.270
-0.452
N+-H
-2.077
0.025
0.350
-0.563
Цвиттер-ионная
C4C(O)OH···O-(O)C5
-1.316
0.009
0.260
-0.416
ZI2
C4С(О)О-Н
-0.007
0.014
0.111
-0.075
∇
а ρ - электронная плотность, 2(ρ) - лапласиан электронной плотности, ε - эллиптичность, H - локальная потенциальная энергия.
Результаты термохимических расчетов мето-
линии водородной связи в карбоксил-карбоксилат-
дом атомизации с использованием результатов
ном фрагменте. Косвенным аргументом в пользу
расчетов методами G4 и G4MP2 представлены в
такой ионизации является бóльшая сила внутри-
табл. 2. Из них следует, что в воде 1-пропилимида-
молекулярной водородной связи в цвиттер-ионе
зол-4,5-дикарбоновая кислота 1 существует в виде
ZI2, соответствующем аниону А3, по сравнению
цвиттер-иона ZI1, хотя отличие энтальпий образо-
с таковой в цвиттер-ионе ZI1, соответствующем
вания цвиттер-ионных форм находится в пределах
аниону A1 (табл. 4).
погрешности расчетов.
Результаты расчетов констант депротонирова-
Для отнесения констант депротонирования
ния 1-пропилимидазол-4,5-дикарбоновой кислоты
1-пропилимидазол-4,5-дикарбоновой кислоты
1
1 в воде по методу, предложенному в работе [18]
мы попытались рассчитать константы депротони-
для расчета констант депротонирования одноос-
рования нейтральной (N) и цвиттер-ионных (ZI1,
новных карбоновых кислот, приведены в табл. 3.
ZI2) таутомерных форм, соответствующие образо-
В этих расчетах использованы значения энергий
ванию всех возможных таутомерных анионов: A1
Гиббса молекулярных и ионных форм, вычислен-
и A3 из N, A1 и A2 из ZI1, A2 и A3 из ZI2. Однако
ные методами G4 и G4MP2. Полученные для рав-
обнаружить локальный минимум энергии оптими-
новесий ZI2-A3 и ZI1-A3 данные хорошо согласу-
зацией геометрии и сканированием поверхности
ются с экспериментальной величиной показателя
потенциальной энергии методом DFT на уров-
константы первого депротонирования 1-пропили-
не теории B3LYP/6-311G(d,p), соответствующий
мидазол-4,5-дикарбоновой кислоты 1 (3.58). Этот
аниону A1, не удалось: изменение положения кар-
факт, с одной стороны, является убедительным до-
боксильного атома водорода с последующей опти-
казательством цвиттер-ионного строения 1-пропи-
мизацией геометрии, равно как и пошаговое ска-
лимидазол-4,5-дикарбоновой кислоты 1 в воде, а с
нирование по расстоянию между атомом водорода
другой - свидетельствует о корректности расчетов.
и ближайшим атомом кислорода группы O(O)CC5,
Образование аниона А2 энергетически невыгодно
выявляет только единственный локальный мини-
из-за электростатического отталкивания двух кар-
мум, который соответствует аниону A3. Таким
боксилатных остатков и вследствие отсутствия, по
образом, ионизация цвиттер-ионной формы ZI1
сравнению с анионом А3, стабилизирующей водо-
по кислотному типу имеет вид ZI1←А3 + H+, т. е.
родной связи.
депротонирование цвиттер-иона ZI1 приво-
дит к аниону А3 путем синхронного внутри-
Следует отметить, что расчетные данные для
молекулярного
переноса
протона
равновесия N-A3 также вполне согласуются с из-
C5C(O)OH···O-(O)C4→C5C(O)O-···HO(O)C4 по
вестными константами первого депротонирования
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
725
дикарбоновых кислот: малеиновой (pK1 1.94) и
79), спирт этиловый ректификованный из пищево-
фталевой кислоты (pK1 2.76) [5], что подтверждает
го сырья «Экстра» (ООО «Гатчинский спиртовой
корректность расчетного алгоритма.
завод», ГОСТ 5962-2013, 96.3%), стандарт-титр
(фиксанал) соляная кислота 0.1 н. (Уралхиминвест,
Характеристики внутримолекулярных водород-
ТУ 2642-001-33813273-97), стандарт-титр (фикса-
ных связей OH···O в нейтральной и цвиттер-ион-
нал) натрий гидроокись 0.1 н. (Уралхиминвест, ТУ
ных формах 1-пропилимидазол-4,5-дикарбоновой
2642-001-33813273-97).
кислоты 1 в водном окружении, полученные в ре-
зультате топологического анализа распределения
Температуры плавления определены на при-
электронной плотности в соответствии с теорией
боре Franz Kustner Nacht HMK. Спектры ЯМР
атомов в молекуле Бейдера (AIM), представле-
на ядрах 1Н, 13С и 15N записаны на спектрометре
ны в табл. 4. В ней приведены также характери-
Bruker Avance III-400 (400.1, 100.6 и 40.5 МГц со-
стики ковалентных связей O-H и N+-H. Для всех
ответственно). В качестве внутреннего стандарта
приведенных в таблице четырех связей, включая
использованы сигналы остаточных протонов и
водородные, была определена критическая точка
ядер 13С ДМСО-d6; внешнего стандарта - сигна-
связи типа (3; -1); согласно работе [19], это до-
лы ядер 15N жидкого аммиака. Константы депро-
казывает существование устойчивой водородной
тонирования 1-пропилимидазол-4,5-дикарбоновой
связи OH···O между карбоксильными группами в
кислоты 1 были определены нами в работе [4] кон-
нейтральной форме и между карбоксильной и кар-
дуктометрическим методом.
боксилатной группой в цвиттер-ионных формах.
Определение константы протонирования
Можно видеть, что локальная электронная плот-
1-пропилимидазол-4,5-дикарбоновой кислоты
ность водородной связи ρ увеличивается с 0.065
1 спектрофотометрическим методом. Серию
для нейтральной формы до 0.102 и 0.260 для форм
рабочих растворов с различной концентрацией
ZI1 и ZI2 соответственно. Это свидетельствует
1-пропилимидазол-4,5-дикарбоновой кислоты
1
о большей энергии водородной связи в цвиттер-
(0.49-2.87 ммоль/л) в соляной кислоте (1 ммоль/л)
ионных формах, что подтверждается также умень-
готовили весовым методом разбавления. Навеску
шением локальной полной энергии H с -0.019 до
исходного веществам и его растворы взвешивали
-0.061 и -0.416 а. е. соответственно. Согласно ра-
на аналитических весах МВА210-А (Сартогосм,
боте [19], данные значения H относятся к проме-
Россия) с точностью до ±0.1 мг. Плотность рас-
жуточным и сильным водородным связям соответ-
творов исследуемого соединения измеряли плот-
ственно.
номером DMA-5000 M (Anton Paar, Австрия) с
Таким образом, в воде и диметилсульфоксиде
электронной точностью ±5×10-5 г/см3. Спектры
1-пропилимидазол-4,5-дикарбоновая кислота су-
поглощения регистрировали на спектрофотометре
ществует в цвиттер-ионной форме, скорее всего -
Shimadzu UV 2700 (Япония), используя кварцевые
ZI1 с карбоксилатной группой в орто-положении
кюветы толщиной 0.1 см. Контроль температуры
к протонированному азоту. Моноанион образует-
исследуемого раствора и кюветы сравнения осу-
ся в результате отщепления протона от протони-
ществляли с помощью держателя кювет Shimadzu
рованного азота цвиттер-ионной формы и имеет
TCC-100 с термоэлектрическим контролем тем-
строение A3 с карбоксилатной группой в орто-по-
пературы с точностью до ±0.1°С. Все измерения
ложении к N-пропильному фрагменту. В свою оче-
проводили при 25°С. Расчеты молярных коэффи-
редь, катион образуется в результате протонирова-
циентов поглощения электронейтральной и прото-
ния карбоксилатной группы цвиттер-иона.
нированной форм молекулы и термодинамической
константы протонирования проводили по алгорит-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
му, описанному в работе [17]. pKBH+ 2.20±0.02,
что соответствует константе протонирования KBH+
В работе использованы следующие реактивы
6.31×10-3.
и растворители: кислота серная (Вектон, ГОСТ
14262-78, ОСЧ 11-5, 98.3%, d 1.84 г/см3), пероксид
Квантово-химические расчеты проведены
водорода (Вектон, ГОСТ 177-88, Экстра, 33%, d
с использованием программ Gaussian 09 [20] и
1.13 г/см3), натрий углекислый безводный (Реахим,
Gaussian 16 [21]. Топологический анализ проводи-
Михайловский завод химреактивов, ХЧ, ГОСТ 83-
ли с использованием программы MultiWFN [22].
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
726
БРУСИНА и др.
Визуализация молекулярных моделей выполнена в
В расчетах использованы экспериментальные
программе GaussView 5.0 [23].
значения G(H+gas) = -6.28 ккал/моль и ΔGsol(H+) =
Первоначальную оптимизацию геометрии и
-264.61 ккал/моль, как это предлагается в [18], а
исследование поверхности полной энергии с це-
также значения энергий Гиббса молекулярных
лью выявления возможных конформеров, образу-
и ионных форм, рассчитанные методами G4 и
ющихся при вращении пропильной группы, про-
G4MP2.
водили в рамках теории функционала плотности
Показатель константы равновесия рассчитыва-
(DFT) с использованием гибридного функционала
ли по уравнению (1).
B3LYP [24] и базисного набора 6-311G(d,p). Вери-
фикацию точек на поверхности энергии проводили
путем вычисления колебательных частот системы.
(1)
Исследование поверхности потенциальной
энергии проводили путем сканирования по дву-
Топологический анализ распределения элек-
гранному углу между плоскостью гетероцикли-
тронной плотности выполнен в соответствии с
ческого фрагмента молекулы и плоскостью, об-
разованной тремя атомами углерода пропильного
теорией атомов в молекуле Бейдера (AIM) с ис-
фрагмента. Расчеты проводили для нейтральной
пользованием волновой функции, полученной при
и цвиттер-ионной форм молекулы, в изолирован-
оптимизации геометрии на уровне теории B3LYP/
ном состоянии и с учетом растворителя - воды по
aug-cc-pVQZ с учетом влияния растворителя по
модели поляризационного континуума CPCM [25].
модели CPCM. Анализ проводили в программном
Сканирование проводили с шагом 1°.
пакете MultiWFN [22].
Термохимические расчеты были проведены с
1-Алкилимидазол-4,5-дикарбоновые кисло-
использованием высокоточных термохимических
ты (1, 3-5) получены по методу [29]. К раствору
методов G4 [26] и G4MP2 [27] по методу атоми-
10.0 ммоль 1-алкилбензимидазола в 10 мл конц.
зации [28]. Методы G4 и G4MP2 включают в себя
H2SO4 при перемешивании прибавляли по каплям
ряд последовательных расчетов: оптимизация ге-
10 мл (0.11 моль) 33%-ного раствора перокси-
ометрии на уровне B3LYP/6-31G(2df,p), колеба-
да водорода при 95-105°С. Смесь перемешивали
тельный расчет на этом же уровне теории, затем
30 мин при 120-130°С. После охлаждения реакци-
для учета эффекта корреляции расчеты без опти-
онную массу выливали в 30 мл воды, подщелачи-
мизации на уровне CCSD(T)/6-31G*, расчет энер-
вали карбонатом натрия до рН ~2. Осадок отфиль-
гии на MP2 или CCSD(T) для методов G4MP2 и
тровывали и сушили в вакууме.
G4 соответственно, и HF в базисах aug-cc-pVTZ и
aug-cc-pVQZ для учета эффекта расширения бази-
1-Пропилимидазол-4,5-дикарбоновая кисло-
са [26]. Такая последовательность расчетов обе-
та (1). Выход 40%, т. пл. 208-209°С. Найдено, %: С
спечивает высокую точность указанных методов.
48.63; Н 4.78; N 14.38. С8H10N2O4. Вычислено, %:
Растворитель учитывали по модели поляризаци-
С 48.48; Н 5.09; N 14.14.
онного континуума CPCM [25].
Диметиловый эфир имидазол-4,5-дикар-
Расчеты констант депротонирования проводи-
боновой кислоты (2). Выход 2.39 г (65%), т. пл.
ли по схеме, предложенной для расчета показате-
201-203°С (т. пл. 202-203°С [30]).
лей констант кислотности карбоновых кислот [18]
1-Метилимидазол-4,5-дикарбоновая кислота
по термодинамическому циклу:
(3). Выход 53%, т. пл. 262-263°С (т. пл. 261°С [31]).
1-Этилимидазол-4,5-дикарбоновая кислота
(4). Выход 41%, т. пл. 228-229°С (т. пл. 227-229°С
∆Ggas
-
+
[31]).
AHgas
Ag
as
+
H
gas
1-Бутилимидазол-4,5-дикарбоновая кислота
∆Gsol (A-)
∆Gsol (H+)
−∆Gsol
(AH)
(5). Выход 38%, т. пл. 203-204°С. Найдено, %: С
∆G
51.43; Н 5.67; N 12.40. С9H12N2O4. Вычислено, %:
aq
-
+
AHaq
+
H
Aa
q
aq
С 50.94; Н 5.70; N 12.90.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
727
Имидазол-4,5-дикарбоновая кислота (6) по-
СПИСОК ЛИТЕРАТУРЫ
лучена по методу [32]. Выход 1.44 г (92%), т. пл.
1.
Беспалов А.Ю., Звартау Э.Э. Нейропсихофарма-
291-293°С (т. пл. 292-295°С [33]).
кология антагонистов NMDA-рецепторов. СПб:
Мононатриевая соль
1-пропилимида-
Невский Диалект, 2000. 297 с.
2.
Пиотровский Л.Б., Думпис М.А., Блохина Е.А.,
зол-4,5-дикарбоновой кислоты (7). При комнат-
Беспалов А.Ю. Актуальные вопросы профилакти-
ной температуре смешивали 0.20 г (10 ммоль)
ки и терапии интоксикаций. СПб: Астерион, 2005.
соединения 1, 0.05 г (5 ммоль) карбоната натрия
С. 29.
и 15 мл воды. Реакционную массу перемешива-
3.
Институт экспериментальной медицины на рубеже
ли 30 мин, затем отгоняли растворитель в вакуу-
тысячелетий. Достижения в области эксперимен-
ме. Полученный остаток растирали с небольшим
тальной биологии и медицины / Под ред. Б.И. Тка-
ченко. СПб: Наука, 2000. С. 67.
количеством этанола до образования кристаллов
4.
Брусина М.А., Николаев Д.Н., Фундаменский В.С.,
и отфильтровывали образовавшийся осадок. Вы-
Гуржий В.В., Золотарев А.А., Селитреников А.В.,
ход 0.24 г (95%), т. пл. 181-183°С. Найдено, %: С
Зевацкий Ю.Э., Потапкин А.М., Рамш С.М.,
43.63; Н 4.58; N 12.38. C8H9N2NaO4. Вычислено,
Пиотровский Л.Б. // Хим.-фарм. ж. 2018. Т. 52. № 4.
%: С 43.64; Н 4.12; N 12.72.
С. 13; Brusina M.A., Nikolaev D.N., Fundamenskii V.S.,
Gurzhii V.V., Zolotarev A.A., Selitrenikov A.V., Zevats-
Моно(триэтаноламмониевая) соль 1-пропи-
kii Y.É., Potapkin A.M., Ramsh S.M., Piotrovskii L.B. //
лимидазол-4,5-дикарбоновой кислоты (8) по-
Pharm. Chem. J. 2018. Vol. 52. N 4. P. 299. doi 10.1007/
лучена по методу [4]. Выход 1.60 г (92%), т. пл.
s11094-018-1810-9
106-107°С (т. пл. 106-107°С [4]).
5.
National Center for Biotechnology Information.
ИНФОРМАЦИЯ ОБ АВТОРАХ
6.
Harmon K.M., Newman H.K. // J. Mol. Struct. 1995.
Vol. 354. P. 171. doi 10.1016/0022-2860(95)08875-V
Брусина Мария Александровна, ORCID: http://
7.
Эфрос Л.С., Хромов-Борисов Н.В., Давиденков Л.Р.,
orcid.org/0000-0001-8433-120X
Недель М.М. // ЖОХ. 1956. Т. 26. № 2. С. 455.
8.
Harmon K.M., LaFave N.J. // J. Mol. Struct. 1997.
Лысова Светлана Сергеевна, ORCID: http://
Vol. 404. P. 297. doi 10.1016/S0022-2860(96)09431-8
orcid.org/0000-0003-0147-9829
9.
Harmon K.M., Gill S.H., Rasmussen P.G., Hard-
Оскорбин Александр Александрович, ORCID:
grove G.L.Jr. // J. Mol. Struct. 1999. Vol. 478. P. 145.
doi 10.1016/S0022-2860(98)00669-3.
10.
Cao Q., Duan B.-R., Zhu B., Cao Zh. // Acta Crystallogr.
Рамш Станислав Михайлович, ORCID: http://
(E). 2012. Vol. 68. Pt. 1. P. o134. doi 10.1107/
orcid.org/0000-0003-4613-068X
S1600536811052998
11.
Schneider F. // Hoppe-Seyler’s Z. Physiol. Chem. 1963.
ФИНАНСОВАЯ ПОДДЕРЖКА
Vol. 334. P. 26. doi 10.1515/bchm2.1963.334.1.26
12.
Litchfield G.J., Shaw G. // J. Chem. Soc. (C). 1971.
Работа выполнена в рамках государственного
P. 817. doi 10.1039/J39710000817
задания Министерства образования и науки Рос-
13.
Альберт А., Сержент Е. Константы ионизации кис-
сии (2022-2025 г. г., «Поиск молекулярных ми-
лот и оснований. М.-Л.: Химия, 1964. C. 128, 107;
Albert A., Serjeant E.P. Determination of ionization
шеней для фармакологического воздействия при
constants: a laboratory manual. London; New York:
аддиктивных и нейроэндокринных нарушениях и
Chapman and Hall, 1984. 218 p.
создание новых фармакологически активных ве-
14.
McCoy L.L. // J. Am. Chem. Soc. 1967. Vol. 89. N 7.
ществ, действующих на рецепторы ЦНС», шифр
P. 1673. doi 10.1021/ja00983a024
FGWG-2022-0004).
15.
Dean J.A. Lange’s Handbook of Chemistry. New York:
McGraw-Hill Professional, 1998. 1424 p.
КОНФЛИКТ ИНТЕРЕСОВ
16.
Зевацкий Ю.Э. // Изв. СПбГТИ(ТУ). 2018. Т. 45.
Вып. 71. С. 3.
Авторы заявляют об отсутствии конфликта
17.
Лысова С.С., Скрипникова Т.А., Зевацкий Ю.Э. //
интересов.
ЖФХ. 2017. Т. 91. № 12. С. 2072; Lysova S.S.,
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
728
БРУСИНА и др.
Skripnikova T.A., Zevatskii Y.E. // Russ. J. Phys.
Staroverov V.N., Keith T.A., Kobayashi R., Normand J.,
Chem. 2017. Vol. 91. N 12. P. 2366. doi 10.7868/
Raghavachari K., Rendell A.P., Burant J.C.,
S0044453717110152
Iyengar S.S., Tomasi J., Cossi M., Millam J.M.,
18. Liptak M.D., Shields G.C. // J. Am. Chem. Soc. 2001.
Klene M., Adamo C., Cammi R., Ochterski J.W.,
Vol. 123. N 30. P. 7314. doi 10.1021/ja010534f
Martin R.L., Morokuma K., Farkas O., Foresman J.B.,
19. Parthasarathi R., Subramanian V., Sathyamurthy N. //
Fox D.J., Gaussian 16 Rev. C.01, Gaussian Inc.,
J. Phys. Chem. (A). 2006. Vol. 110. N 10. P. 3349. doi
Wallingford CT, 2016.
10.1021/jp060571z
22.
Lu T., Chen F. // J. Comput. Chem. 2012. Vol. 33. N 5.
20. Frisch M.J., Trucks G.W., Schlegel H.B., Scuseria G.E.,
P. 580. doi 10.1002/jcc.22885
Robb M.A., Cheeseman J.R., Scalmani G., Barone V.,
23.
Dennington R., Keith T., Millam J., GaussView, Ver. 5.
Mennucci B., Petersson G.A., Nakatsuji H., Caricato M.,
Semichem Inc., Shawnee Mission, KS, 2009.
Li X., Hratchian H.P., Izmaylov A.F., Bloino J., Zheng G.,
24.
Lee C., Yang W., Parr R.G. // Phys. Rev. (B). 1988.
Sonnenberg J.L., Hada M., Ehara M., Toyota K.,
Vol. 37. N 2 . P. 785. doi 10.1103/PhysRevB.37.785
Fukuda R., Hasegawa J., Ishida M., Nakajima T.,
25.
Takano Y., Houk K. // J. Chem. Theory Comput. 2005.
Honda Y., Kitao O., Nakai H., Vreven T., Montgo-
Vol. 1. N 1. P. 70. doi 10.1021/ct049977a
mery Jr.J.A., Peralta J.E., Ogliaro F., Bearpark M.,
26.
Curtiss L.A., Redfern P.C., Raghavachari K. // J.
Heyd J.J., Brothers E., Kudin K.N., Staroverov V.N.,
Keith T., Kobayashi R., Normand J., Raghavachari K.,
Chem. Phys. 2007. Vol. 126. N 8. P. 84108. doi
Rendell A., Burant J.C., Iyengar S.S., Tomasi J.,
10.1063/1.2436888
Cossi M., Rega N., Millam J.M., Klene M., Knox J.E.,
27.
Curtiss L.A., Redfern P.C., Raghavachari K. // J.
Cross J.B., Bakken V., Adamo C., Jaramillo J.,
Chem. Phys. 2007. Vol. 127. N 12. P. 124105. doi
Gomperts R., Stratmann R.E., Yazyev O., Austin
10.1063/1.2770701
A.J., Cammi R., Pomelli C., Ochterski J.W., Martin
28.
Nicolaides A., Rauk A., Glukhovtsev M.N., Radom L. //
R.L., Morokuma K., Zakrzewski V.G., Voth G.A.,
J. Phys. Chem. 1996. Vol. 100. N 44. P. 17460. doi
Salvador P., Dannenberg J.J., Dapprich S.,
10.1021/jp9613753
Daniels A.D., Farkas O., Foresman J.B., Ortiz J.V.,
29.
Пиотровский Л.Б., Брусина М.А., Николаев Д.Н.,
Cioslowski J., Fox D.J., Gaussian 09, Gaussian Inc.,
Рамш С.М. Пат. РФ 2665712 (2018).
Wallingford CT, 2013.
30.
Виноградова Н.Б., Хромов-Борисов Н.В. // ЖОХ.
21. Frisch M.J., Trucks G.W., Schlegel H.B., Scuseria G.E.,
1961. Т. 31. № 5. С. 1471.
Robb M.A., Cheeseman J.R., Scalmani G., Barone V.,
31.
Александрова И.Я., Хрусталева В.С., Хромов-Бори-
Petersson G.A., Nakatsuji H., Li X., Caricato M.,
сов Н.В. // ЖОрХ. 1983. Т. 19. № 2. С. 416.
Marenich A.V., Bloino J., Janesko B.G., Gomperts R.,
32.
Брусина М.А., Губина Ю.А., Николаев Д.Н.,
Mennucci B., Hratchian H.P., Ortiz J.V., Izmaylov A.F.,
Рамш С.М., Пиотровский Л.Б. // ЖОХ. 2018.
Sonnenberg J.L., Williams D., Ding F., Lipparini F.,
Т. 88. № 5. С. 729; Brusina M.A., Gubina Yu.A.,
Egidi F., Goings J., Peng B., Petrone A., Henderson T.,
Nikolaev D.N., Ramsh S.M., Piotrovskii L.B. // Russ.
Ranasinghe D., Zakrzewski V.G., Gao J., Rega N.,
Zheng G., Liang W., Hada M., Ehara M., Toyota K.,
J. Gen. Chem. 2018. Vol. 88. N 5. P. 874. doi 10.1134/
Fukuda R., Hasegawa J., Ishida M., Nakajima T.,
S1070363218050055
Honda Y., Kitao O., Nakai H., Vreven T., Throssell K.,
33.
Schubert H., Hoffmann S., Lehmann G., Barthold I.,
Montgomery Jr. J.A., Peralta J.E., Ogliaro F.,
Meichsner H., Polster H.-E. // Z. Chem. 1975. Vol. 15.
Bearpark M.J., Heyd J.J., Brothers E.N., Kudin K.N.,
N 12. P. 481. doi 10.1002/zfch.19750151209
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СТРОЕНИЕ И КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА
729
Structure and Acid-Base Properties
of 1-Propylimidazole-4,5-dicarboxylic Acid
M. A. Brusinaa,b,*, S. S. Lysovac, A. A. Oskorbinb, and S. M. Ramshb
a Institute of Experimental Medicine, St. Petersburg, 197022 Russia
b St. Petersburg State Institute of Technology (Technical University), St. Petersburg, 190013 Russia
c St. Petersburg State University of Industrial Technologies and Design, St. Petersburg, 191186 Russia
*e-mail: sramsh@technolog.edu.ru
Received March 31, 2023; revised May 4, 2023; accepted May 6, 2023
NMR spectra of 1-propylimidazole-4,5-dicarboxylic acid in DMSO-d6 were studied. It was revealed that it
presents in a zwitterion form in solution. The ionization constants in water were determined and their attribution
to the certain sites was performed, at that for the deprotonation constants, the correctness of the attribution was
confirmed by calculations. Based on the results of calculations, the preferred zwitterion and monoanion forms
of 1-propylimidazole-4,5-dicarboxylic acid were selected from several alternative structures.
Keywords: 1-propylimidazole-4,5-dicarboxylic acid, NMR spectroscopy, prototropic tautomerism, ionization
constants, DFT calculations, high-precision thermochemical calculations
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023