ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ, 2019, том 55, № 3, с. 395-401
УДК 547.816 + 547.642 + 546.47 + 547.514
ВЗАИМОДЕЙСТВИЕ МЕТИЛ
1-БРОМЦИКЛОПЕНТАНКАРБОКСИЛАТА С ЦИНКОМ И
1-АРИЛ-3-(2-ГИДРОКСИФЕНИЛ)ПРОП-2-ЕН-1-ОНАМИ
© 2019 г. Е. А. Никифорова*, Д. В. Байбародских, Н. Ф. Кириллов,
М. В. Дмитриев, С. Н. Шуров
ФГБОУ ВО «Пермский государственный национальный исследовательский университет»,
614990, Россия, г. Пермь, ул. Букирева 15
*e-mail: vikro@ya.ru
Поступила в редакцию 7 ноября 2018 г.
После доработки 28 ноября 2018 г.
Принята к публикации 15 декабря 2018 г.
Взаимодействием реактива Реформатского, полученного из метил 1-бромциклопентанкарбоксилата и
цинка с 1-арил-3-(2-гидроксифенил)проп-2-енонами, получены 4-(2-арил-2-оксоэтил)-6-R-спиро[хроман-
3,1'-циклопентан]-2-оны. На основе квантово-химических расчетов методом DFT/TZVP предложена
механизм реакции.
Ключевые слова: Реакция Реформатского,
1-бромциклоалканкарбоксилаты,
1-бромциклопентан-
карбоксилат, спирогетероциклы, хроман-2-оны, гидроксихалконы, спирохроманоны.
DOI: 10.1134/S051474921903011X
Ранее было показано, что в результате
полученного из метил
1-бромциклопентанкар-
взаимодействия карбоциклических реактивов
боксилата и цинка, с
1-арил-3-(2-гидрокси-5-R-
Реформатского с халконами образуются 4,6-ди-
фенил)проп-2-енонами
2a-l. Согласно литера-
арил-3,4-дигидро-2H-спиро[пиран-3,1'-циклоал-
турным данным продуктами реакции могли бы
кан]-2-оны, проявляющие анальгетическую актив-
быть 6-арил-4-(2-гидрокси-5-R-фенил)-3,4-дигидро-
ность [1-3]. В качестве ключевых интермедиатов в
2H-спиро[пиран-3,1'-циклопентан]-2-оны 4. Нами
этих реакциях постулируются 1,3-диарил-4,4-три
было установлено, что в результате взаимодейст-
(или тетра-)метилен-5-метоксикарбонил-пент-1-ен-
вия реактива 1 с халконами 2a-l с выходами 48-
1-оксицинк бромиды (А), которые циклизуются за
78% образуются 4-(2-арил-2-оксоэтил)-6-R-спиро-
счет атаки атома кислорода остатка OZnBr на атом
[хроман-3,1'-циклопентан]-2-оны 3a-l (cхема 1).
углерода метоксикарбонильной группы.
Состав и строение синтезированных соединений
2
Ar
3a-l подтверждено данными элементного анализа,
ИК и ЯМР 1Н спектроскопии. В ИК спектрах соеди-
Ar1
(CH2)n
нений 3a-l присутствуют полосы в области 1768-
O
1750 см-1, обусловленные валентными колебаниями
OMe
Zn O
лактонных карбонилов С2=О и полосы в области
Br
1691-1664 см-1, принадлежащие кетонным карбонилам
A
фрагментов ArC=O. Отсутствие полосы валентных
колебаний гидроксильных групп в ИК спектрах поз-
Введение в халконы дополнительной гидрокси-
воляет исключить структуру типа 4. В спектрах ЯМР
льной группы, способной превратиться в группу
1Н наиболее характерными являются двойные дублеты
OZnBr, расширяет синтетические возможности
(или триплеты) протонов хромановых циклов С4-Н в
реакции первых с реактивами Реформатского.
области 3.48-3.54 м.д. и двойные дублеты неэквива-
Целью настоящей работы является исследо-
лентных метиленовых протонов С4Н-СН2-СО с близ-
вание взаимодействия реактива Реформатского 1,
кими химическими сдвигами в области 3.09-3.16 м.д.
395
396
НИКИФОРОВА и др.
Схема 1.
Ar
R
O
R
Ar
O O
Br
OMe
OH
O
Zn
3a_l
2a_l
COOMe
OZnBr
R
-Zn(OMe)Br
1
HO
Ar
O
O
4
2-4: R = H, Ar = Ph (a), 4-BrC6H4 (b), 4-ClC6H4 (c), 4-MeOC6H4 (d); R = Br, Ar = Ph (e), 4-MeC6H4 (f), 2,4-Me2C6H4 (g),
2,5-Me2C6H4 (h), 4-BrC6H4 (i), 4-ClC6H4 (j), 4-MeOC6H4 (k); 4-EtOC6H4 (l).
С целью более точного установления структуры
роваться с атомом кислорода О=С сложноэфирной
синтезированных соединений был проведен
группы (интермедиаты I-3 и I-3А). Отщепление
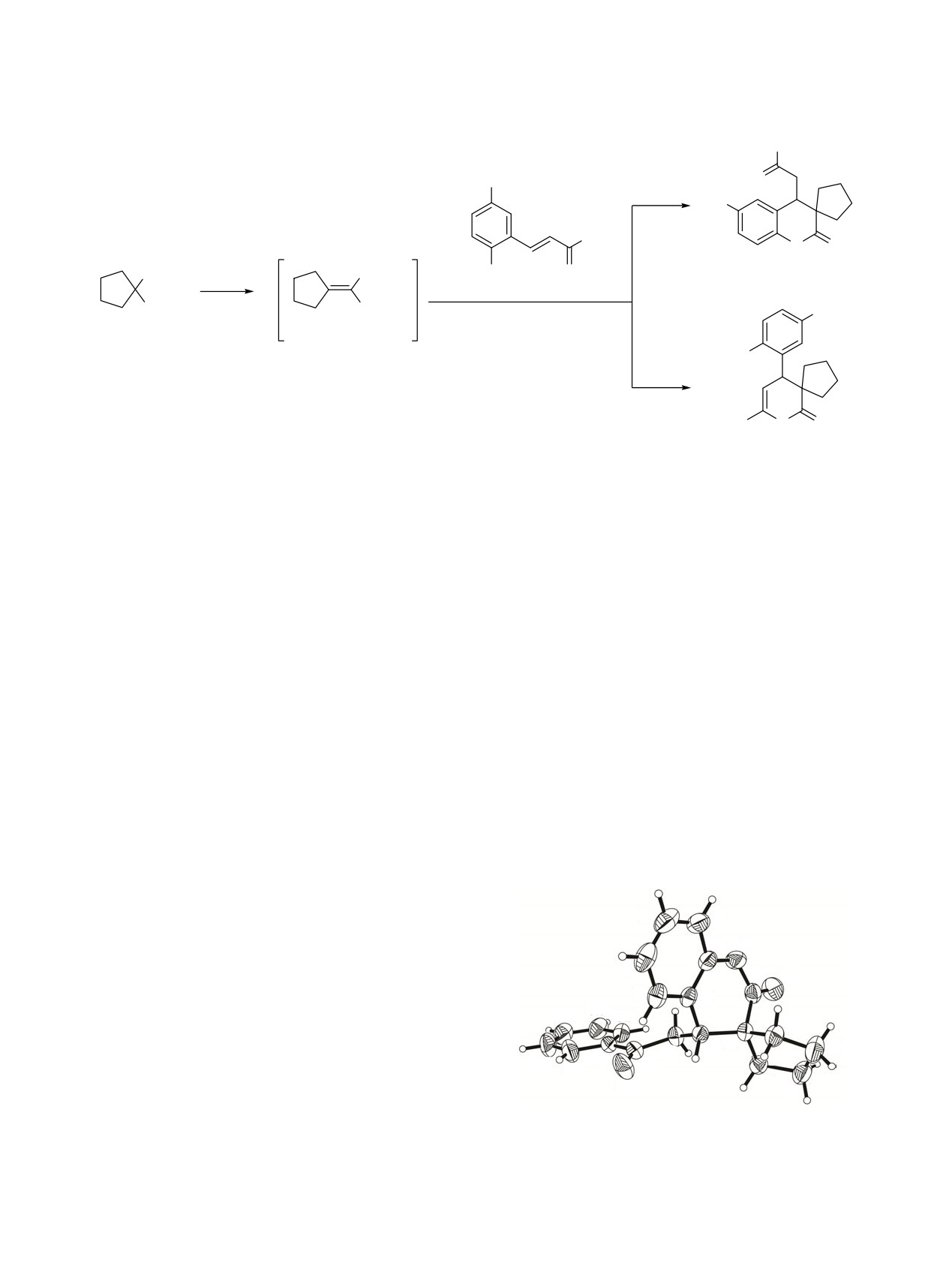
рентгеноструктурный анализ соединения 3a. По
молекулы бромцинкметилата от этих интермедиатов
данным РСА (см. рисунок) соединение 3a кристал-
приводит к интермедиатов I-4 и I-4А, содержащих,
лизуется в центросимметричной пространственной
соответственно, фрагменты хромана и пирана.
группе моноклинной сингонии. Пирановый цикл
Гидролиз интермедиата I-4 через енол I-5
находится в конформации искаженная софа,
приводит к
4-(2-оксо-2-фенилспиро[хроман-3,1'-
фрагмент C1C2C3C4C5C6C7O1 плоский в пределах
циклопентан]-2-ону
3a. Гидролиз интермедиата
0.02 Å, атомы С9 и С8 выходят из плоскости на 0.30
I-4А мог бы дать 4-(2-гидроксифенил)-6-фенил-3,4-
и 0.82 Å соответственно. Неплоский фенацильный
дигидро-2H-спиро[пиран-3,1'-циклопентан]-2-он 4,
заместитель расположен в псевдоаксиальной
образование которого не зафиксировано.
позиции, диэдральный угол между плоскостями
Для подтверждения принципиальной возмож-
фенильного цикла и фрагмента C14C15C16O3 равен
ности реализации предложенной схемы мы провели
10.8°. Циклопентановый фрагмент принимает
квантово-химические расчеты энергетических
конформацию искаженный конверт с выходом
характеристик вероятных интермедиатов методом
атома С10 из плоскости остальных четырех атомов
теории функционала плотности (функционал
на 0.53 Å. Межмолекулярные водородные связи и
B3LYP) с базисным набором TZVP c оптимизацией
иные значимые укороченные контакты в кристалле
отсутствуют.
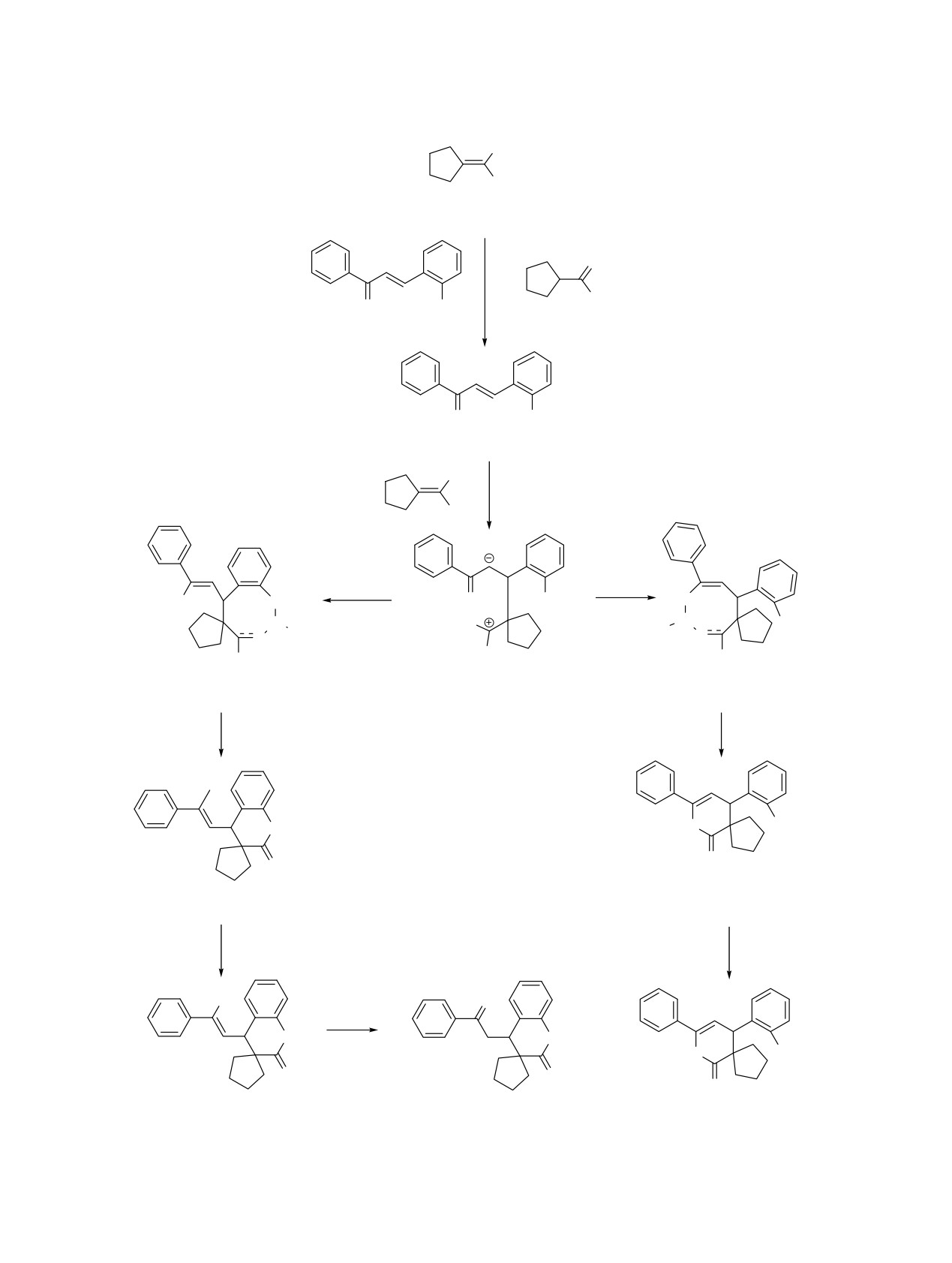
Возможная схема образования соединений 3a-l,
С3
С4
рассмотренная на примере спирохроманона
3a,
С5 O1
приведена ниже (схема 2). Она включает взаимо-
действие реактива Реформатского 1 с халконом 2a,
С2
С9
O2
как с соединением, содержащим «активный водород»,
С1
С6
что приводит к интермедиату I-1. Далее к этому
С19
С18
С17
С10
интермедиату присоединяется еще одна молекула
С7
С11
реактива 1, что может дать цвиттер-ионный интер-
С8
С20
С16
С15 С14
медиат I-2. Его стабилизация связана с миграцией
С21
С13
С12
группы ZnBr к атому кислорода карбонильной
O3
группы. Продукт миграции содержит два фрагмента
Общий вид молекулы соединения 3a по данным РСА в
OZnBr, атомы цинка в которых могут координи-
тепловых эллипсоидах 50% вероятности.
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 3 2019
ВЗАИМОДЕЙСТВИЕ МЕТИЛ 1-БРОМЦИКЛОПЕНТАНКАРБОКСИЛАТА С ЦИНКОМ
397
Схема 2.
OMe
OZnBr
1
Etot. = _4777.3884 хартри
O
_
OMe
O
OH
2a
Etot. = _729.5588 хартри
Etot. = _424.6171 хартри
O
OZnBr
I-1
Etot. = _5082.6664 хартри
OMe
OZnBr
путь А
путь Б
O
OZnBr
O
BrZnO
O
Zn
BrZnO
Zn
OZnBr
Br
Br
O
O
MeO
OMe
OMe
I-3
I-2
I-3А
Etot. = _9860.4478 хартри
Etot. = _
9860.4128 хартри
_Zn(OMe)Br
_Zn(OMe)Br
BrZnO
O
OZnBr
O
O
O
I-4
I-4А
Etot. = _5391.5069 хартри
Etot. = _5391.4993 хартри
H2O
-Zn(OH)Br
H2O
_Zn(OH)Br
OH
O
O
O
O
OH
O
O
O
I-5
3a
4
Etot. = _1038.3874 хартри
Etot. = _1038.4076 хартри
Etot. = _1038.3834 хартри
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 3 2019
398
НИКИФОРОВА и др.
всех геометрических параметров. Полные энергии
синтезированных соединений сняты в вазелиновом
возможных интермедиатов Etot. в единицах хартри
масле на Фурье-спектрометре SpectrumTwo фирмы
приведены под формулами. Стартовая геометрия
PerkinElmer. Спектры ЯМР
1H растворов этих
халкона 2a заимствована из данных рентгеност-
соединений в CDCl3 сняты на спектрометре
руктурных исследований [4]. Образование О-ZnBr
MercuryPlus-300 (300 МГц), внутренний стандарт -
производного халкона 2a (интермедиат I-1) и выде-
ТМС. Элементный анализ выполнен на
ление метил циклопентанкарбоксилата, по-видимому,
анализаторе vario MICRO cube. Квантово-
термодинамически выгодно. Далее к атому С3
химические расчеты выполнены с помощью пакета
интермедиата I-1 присоединяется электроноизбы-
программ Firefly [5].
точный атом углерода реактива Реформатского 1,
Для рентгеноструктурного анализа использован
что должно привести к интермедиату I-2. Однако
обломок бесцветного кристалла размером
«зафиксировать» его в расчете не удалось, и
0.65×0.55×0.50 мм. Кристалл моноклинный, прост-
поэтому его образование лишь предполагается.
ранственная группа P21/n, a 9.5533(17), b 16.774(3),
При сближении частиц I-1 и 1 в ходе компью-
c 10.6445(17) Å, β 91.335(16)°, V 1705.3(5) Å3,
терного эксперимента происходила миграция
C21H20O3, Z 4. Набор экспериментальных отражений
группы ZnBr к атому кислорода кетонной группы и
получен на монокристальном автоматическом
возникновение метоксикарбонильного фрагмента.
дифрактометре XcaliburR с ССD-детектором по
Атом кислорода СН3О-С=О образовавшегося
стандартной методике (MoKα-излучение, 295(2) K,
сложноэфирного фрагмента теоретически может
ω-сканирование, шаг сканирования 1°). Поглощение
далее координироваться с атомом цинка любой из
учтено эмпирически с использованием алгоритма
OZnBr групп. Согласно расчетам интермедиат I-3
SCALE3 ABSPACK [6]. Всего измерено 8675 отра-
на 0.035 хартри (91.9 кДж/моль) стабильнее альтер-
жений, из них независимых 4010, 3000 отражений
нативного интермедиата I-3А, и его образование
с I>2σ(I). Структура определена прямым методом
следует считать более предпочтительным.
по программе SHELXS-97 и уточнена полномат-
Отщепление метоксицинкбромида от этого
ричным МНК по F2 в анизотропном приближении
интермедиата дает цинк-енолят (I-4), гидролиз
для всех неводородных атомов с использованием
которого в условиях эксперимента приводит к
программы SHELXL-97
[7]. Атомы водорода
енолу (I-5). Превращение енола I-5 в продукт
включены в уточнение в модели «наездника» в
реакции 3a сопровождается выигрышем энергии,
изотропном приближении с зависимыми тепловыми
равным 0.020 хартри (53.0 кДж/моль). Согласно
параметрами. Окончательные параметры уточнения:
расчетам энергия хромонона 3a на 0.024 хартри
R1 0.0534, wR2 0.1329 [для отражений с I>2σ(I)], R1
(63.0 кДж/моль) ниже региоизомерногопирана 4.
0.0732, wR2 0.1455 (для всех отражений), S 1.058.
Более низкая энергия ключевого интермедиата I-3
Результаты рентгеноструктурного исследования
предопределяет течение реакции по пути А
зарегистрированы в Кембриджском центре
несмотря на то, что интермедиат I-4А несколько
кристаллографических данных под номером CCDC
стабильнее интермедиата I-4.
1894482. Эти материалы находятся в свободном
Как следует из расчетов наиболее вероятной
доступе и могут быть запрошены по адресу
схемой образования хромона
3a, является
приведенная ниже:
Общая методика. К смеси 3 г цинка, 0,5 г
1a → I-1 → I-2→ I-3 → I-4 →I-5 → 3a
метилового эфира 1-бромциклопентанкарбоновой
кислоты, каталитического количества HgCl2 и 5 мл
По-видимому, хромоны
3b-l образуются по
толуола после начала реакции прикапывали смесь
аналогичной схеме.
10 ммоль 1-арил-3-(2-гидроксифенил)проп-2-ен-1-
Соединения
3f-i, k, l проявляют анальгети-
она, 22 ммоль (4.55 г) метилового эфира 1-бром-
ческую активность на уровне эталонного препарата
циклопентанкарбоновой кислоты, 3 мл ГМФТА и
анальгина.
20 мл толуола. Затем реакционную смесь кипятили
4 ч, охлаждали, сливали с избытка цинка,
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
гидролизовали 5%-ной уксусной кислотой, орга-
нический слой отделяли, из водного слоя продукты
Температуры плавления измерены на приборе
реакции дважды экстрагировали этилацетатом.
MP-70 фирмы MettlerToledo. ИК спектры
После высушивания экстракта безводным
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 3 2019
ВЗАИМОДЕЙСТВИЕ МЕТИЛ 1-БРОМЦИКЛОПЕНТАНКАРБОКСИЛАТА С ЦИНКОМ
399
сульфатом натрия растворители отгоняли и
т.пл. 145-146°С. ИК спектр, ν, см-1: 1755, 1683
синтезированные соединения перекристаллизо-
(C=O).Спектр ЯМР 1H, δ, м.д.: 1.46-1.96 м (7H),
вывали из этилацетата.
2.49 м [1Н, (CH2)4], 3.15 д.д (1H, CH2, J 9.0 Гц,
17.1 Гц), 3.16 д.д (1H, CH2, J 4.5 Гц, 17.1 Гц), 3.51
4-(2-Оксо-2-фенилэтил)спиро[хроман-3,1'-
д.д (1H, H4, J 4.5 Гц, 9.0 Гц), 6.87 д (1Н, H8, J
циклопентан]-2-он (3a). Выход 1.95 г (61%), т.пл.
8.4 Гц), 7.30 д.д (1Н, H7, J 8.4 Гц, 2.1 Гц), 7.49 д
114-115°С. ИК спектр, ν, см-1:
1750,
1681
(1Н, H5, J 2.1 Гц), 7.41 т, 7.53 т, 7.83 д (5H, Ph, J
(C=O).Спектр ЯМР 1H, δ, м.д.: 1.48-1.97 м (7H),
7.5 Гц). Найдено, %: C 63.28; H 4.73; Br 19.87.
2.51 м [1Н, (CH2)4], 3.16 д (2Н, СH2, J 6.9 Гц), 3.54 т
C21H19 BrO3. Вычислено, %: C 63.17; H 4.80, Br
(1H, H4, J 6.9 Гц), 6.98 т (1H, Н7, J 7.8 Гц), 7.00 д
20.01.
(1H, Н8, J 7.8 Гц), 7.18 т (1H, Н6, J 7.8 Гц), 7.32 д
(1H, Н5, J 8.1 Гц), 7.37 т, 7.50 т, 7.80 д (5Н, Ph, J
6-Бром-4-[2-(4-метилфенил)-2-оксоэтил]-
7.5 Гц). Найдено, %: C 78.87; H 6.21. C21H20O3.
спиро[хроман-3,1'-циклопентан]-2-он (3f). Выход
Вычислено, %: C 78.73; H 6.29.
1.98 г (48%), т.пл. 110-111°С. ИК спектр, ν, см-1:
1764, 1673 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.49-1.97
4-[2-(4-Бромфенил)-2-оксоэтил]спиро[хро-
м (7H), 2.49 м [1Н, (CH2)4], 2.37 с (3H, Me), 3.11 д.д
ман-3,1'-циклопентан]-2-он
(3b). Выход 2.87 г
(1Н, СH2, J 8.4 Гц, 17.7 Гц), 3.14 д.д (1Н, СH2, J
(72%), т.пл. 132-133°С. ИК спектр, ν, см-1: 1756,
4.8 Гц, 17.7 Гц), 3.51 д.д (1H, H4, J 4.8 Гц, 8.4 Гц),
1691 (C=O). Спектр ЯМР 1H, δ, м.д.: 1.47-1.97 м
6.88 д (1Н, H8, J 8.7 Гц), 7.30 д.д (1Н, H7, J 8.7 Гц,
(7H), 2.49 м [1Н, (CH2)4], 3.10 д.д (1Н, СH2, J
2.4 Гц), 7.49 д (1Н, H5, J 2.4 Гц), 7.21 д, 7.73 д (4H,
6.0 Гц, 15.0 Гц), 3.12 д.д (1Н, СH2, J 7.5 Гц,
4-MeC6H4, J 8.4 Гц). Найдено, %: C 64.11; H 4.98;
15.0 Гц), 3.49 д.д (1H, H4, J 6.0 Гц, 7.5 Гц), 6.98 т
Br 19,64. C22H21BrO3. Вычислено, %: C 63.93; H
(1H, Н7, J 7.5 Гц), 6.99 д (1H, Н8, J 7.5 Гц), 7.19 т
5.12, Br 19.33.
(1H, Н6, J 7.5 Гц), 7.27 д (1H, Н5, J 7.5 Гц), 7.51 д,
6-Бром-4-[2-(2,4-диметилфенил)-2-оксоэтил]-
7.64 д (4Н, 4-BrC6H4, J 8.4 Гц). Найдено, %: C
спиро[хроман-3,1'-циклопентан]-2-он
(3g).
62.96; H 4.91; Br 19.84. C21H19BrO3. Вычислено, %:
Выход 2.39 г (56%), т.пл. 97-98°С. ИК спектр, ν, см-1:
C 63.17; H 4.80; Br 20.01.
1768, 1668 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.48-1.96
4-[2-Оксо-2-(4-хлорфенил)этил]спиро-
м (7H), 2.48 м [1Н, (CH2)4], 2.30 с (3Н, Ме), 2.42 с
[хроман-3,1'-циклопентан]-2-он
(3c). Выход
(3Н, Ме), 3.01 д.д (1Н, СH2, J 9.6 Гц, 17.1 Гц), 3.10
2.09 г (59%), т.пл. 110-111°С. ИК спектр, ν, см-1:
д.д (1Н, СH2, J 4.2 Гц, 17.1 Гц), 3.48 д.д (1H, H4, J
1760, 1689 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.48-1.98
4.2 Гц, 9.6 Гц), 6.98 д, 7.01 с, 7.34 д (3H, 2,4-
м (7H), 2.50 м [1Н, (CH2)4], 3.11 д (2Н, СH2, J 6.6 Гц),
Ме2C6H3, J 7.8 Гц), 6.87 д (1Н, H8, J 8.4 Гц), 7.31 д.д
3.50 т (1H, H4, J 6.6 Гц), 6.98 т (1H, Н7, J 7.8 Гц),
(1Н, H7, J 8.4 Гц, 2.1 Гц), 7.43 д (1Н, H5, J 2.1 Гц).
6.99 д (1H, Н8, J 7.8 Гц), 7.19 т (1H, Н6, J 7.8 Гц),
Найдено, %: C 64.45; H 5.55; Br 18.57. C23H23BrO3.
7.25 д (1H, Н5, J 7.8 Гц), 7.35 д, 7.71 д (4Н, 4-ClC6H4,
Вычислено, %: C 64.64; H 5.42, Br 18.70.
J 8.4 Гц). Найдено, %: C 70.91; H 5.47; Cl 10.12.
6-Бром-4-[2-(2,5-диметилфенил)-2-оксоэтил]-
C21H19ClO3. Вычислено, %: C 71.09; H 5.40; Cl 9.99.
спиро[хроман-3,1'-циклопентан]-2-он
(3h).
4-[2-(4-Метоксифенил)-2-оксоэтил]спиро-
Выход 2.18 г (51%), т.пл. 135-136°С. ИК спектр, ν,
[хроман-3,1'-циклопентан]-2-он
(3d). Выход
см-1: 1764, 1672 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.49-
1.89 г (54%), т.пл. 88-89°С. ИК спектр, ν, см-1:
1.97 м (7H), 2.49 м [1Н, (CH2)4], 2.29 c (3H, Me),
1758, 1674 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.45-1.97
2.37 с (3H, Me), 3.05 д.д (1Н, СH2, J 9.0 Гц,
м (7H), 2.50 м [1Н, (CH2)4], 3.10 д.д (1Н, СH2, J
17.1 Гц), 3.09 д.д (1Н, СH2, J 4.2 Гц, 17.1 Гц), 3.49
5.4 Гц, 17.1 Гц), 3.11 д.д (1Н, СH2, J 7.8 Гц,
д.д (1H, H4, J 4.2 Гц, 9.0 Гц), 6.88 д (1Н, H8, J
17.1 Гц), 3.53 д.д (1H, H4, J 5.4 Гц, 7.8 Гц), 3.82 с
8.4 Гц), 7.32 д.д (1Н, H7, J 8.4 Гц, 2.4 Гц), 7.46 д
(3Н, ОСН3), 6.84 д, 7.78 д (4H, 4-МеOC6H4, J
(1Н, H5, J 2.4 Гц), 7.07 д, 7.14 д, 7.18 с (3H, 2,5-
9.0 Гц), 6.98 т (1H, Н7, J 7.5 Гц), 6.99 д (1H, Н8, J
Me2C6H3, J 7.8 Гц). Найдено, %: C 64.42; H 5.32; Br
7.5 Гц), 7.18 т (1H, Н6, J 7.5 Гц), 7.29 д (1H, Н5, J
18.89. C23H23BrO3. Вычислено, %: C 64.64; H 5.42,
7.5 Гц). Найдено, %: C 75.29; H 6.47. C22H22O4.
Br 18.70.
Вычислено, %: C 75.41; H 6.33.
6-Бром-4-[2-(4-бромфенил)-2-оксоэтил]спиро-
6-Бром-4-(2-оксо-2-фенилэтил)спиро[хроман-
[хроман-3,1'-циклопентан]-2-он (3i). Выход 2.53 г
3,1'-циклопентан]-2-он (3e). Выход 2.64 г (66%),
(53%), т.пл. 147-149°С. ИК спектр, ν, см-1: 1764,
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 3 2019
400
НИКИФОРОВА и др.
1678 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.45-1.96 м
д.д (1Н, СH2, J 5.1 Гц, 17.4 Гц), 3.51 д.д (1H, H4, J
(7H), 2.49 м [1Н, (CH2)4], 3.10 д.д (1H, CH2, J
5.1 Гц, 7.8 Гц), 4.06 к (2Н, ОСН2СН3, J 7.2 Гц), 6.85
8.7 Гц, 17.7 Гц), 3.12 д.д (1H, CH2, J 4.5 Гц,
д, 7.80 д (4H, 4-EtOC6H4, J 8.7 Гц), 6.87 д (1Н, H8, J
17.7 Гц), 3.49 д.д (1H, H4, J 4.5 Гц, 8.7 Гц), 6.88 д
8.7 Гц), 7.30 д.д (1Н, H7, J 8.7 Гц, 2.1 Гц), 7.48 д
(1Н, H8, J 8.4 Гц), 7.31 д.д (1Н, H7, J 8.4 Гц, 2.4 Гц),
(1Н, H5, J 2.1 Гц), Найдено, %: C 62.27; H 5.41; Br
7.48 д (1Н, H5, J 2.4 Гц), 7.55 д, 7.69 д (4Н, 4-BrC6H4,
17.82. C23H23BrO4. Вычислено, %: C 62.31; H 5.23,
J 8.4 Гц). Найдено, %: C 52.93; H 3.70; Br 33.16.
Br 18.02.
C21H18 Br2O3. Вычислено, %: C 52.75; H 3.79, Br
33.42.
ФОНДОВАЯ ПОДДЕРЖКА
6-Бром-4-[2-оксо-2-(4-хлорфенил)этил]спиро-
Работа выполнена при финансовой поддержке
[хроман-3,1'-циклопентан]-2-он (3j). Выход 2.13 г
Российского Фонда Фундаментальных Исследова-
(49 %), т.пл. 123-124°С. ИК спектр, ν, см-1: 1765,
ний (грант № 18-33-00509).
1678 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.46-1.96 м
(7H), 2.49 м [1Н, (CH2)4], 3.09 д.д (1Н, СH2, J
КОНФЛИКТ ИНТЕРЕСОВ
8.7 Гц, 17.1 Гц), 3.14 д.д (1Н, СH2, J 4.8 Гц,
17.1 Гц), 3.49 д.д (1H, H4, J 8.7 Гц, 4.8 Гц), 6.88 д
Авторы заявляют об отсутствии конфликта
(1H, Н8, J 8.7 Гц), 7.31 д.д (1Н, H7, J 8.7 Гц, 2.4 Гц),
интересов.
7.47 д (1Н, H5, J 2.4 Гц), 7.38 д, 7.77 д (4Н, 4-
ClC6H4, J 8.7 Гц). Найдено, %: C 57.92; H 4.25.
C21H18BrClO3. Вычислено, %: C 58.15; H 4.18.
СПИСОК ЛИТЕРАТУРЫ
6-Бром-4-[2-(4-метоксифенил)-2-оксоэтил]-
1. Кириллов Н.Ф., Гаврилов А.Г. ЖОХ. 2008, 78, 1189.
спиро[хроман-3,1'-циклопентан]-2-он
(3k).
[Kirillov N.F., Gavrilov A.G. Russ. J. Gen. Chem. 2008,
Выход 2.62 г (61%), т.пл. 137-138°С. ИК спектр, ν,
78, 1422.] doi 10.1134/S1070363208070244
см-1: 1760, 1664 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.46-
2. Кириллов Н.Ф., Гаврилов А.Г. ЖОрХ. 2008, 44, 975.
1.95 м (7H), 2.48 м [1Н, (CH2)4], 3.09 д.д (1Н, СH2, J
[Kirillov N.F., Gavrilov A.G. Russ. J. Org. Chem. 2008,
8.1 Гц, 17.1 Гц), 3.11 д.д (1Н, СH2, J 4.8 Гц,
44, 963.] doi 10.1134/S1070428008070051
17.1 Гц), 3.51 д.д (1H, H4, J 4.8 Гц, 8.1 Гц), 3.83 с
3. Кириллов Н.Ф., Махмудов Р.Р., Гаврилов А.Г.,
(3Н, ОМе), 6.87 д, 7.81 д (4H, 4-МеOC6H4, J 8.7 Гц),
Марданова Л.Г., Вахрин М.И. Хим.-Фарм. Ж. 2013,
6.87 д (1Н, H8, J 8.7 Гц), 7.30 д.д (1Н, H7, J 8.7 Гц,
47,
41.
[Kirillov N.F., Makhmudov R.R., Gavri-
lov A.G., Mardanova L.G., Vakhrin M.I. Pharm. Chem.
2.4 Гц), 7.48 д (1Н, H5, J 2.4 Гц), Найдено, %: C
J. 2013, 47, 40.] doi 10.1007/s11094-013-0892-7
61.70; H 5.07; Br 18.44. C22H21BrO4. Вычислено, %:
4. Yeap G.Y., Feng M.-C., Ng A.-C., Tiekink E.R.T.
C 61.55; H 4.93, Br 18.61.
Zeitsch. Kristall.
1996,
211,
949. doi
10.1524/
6-Бром-4-[2-оксо-2-(4-этоксифенил)этил]-
zkri.1996.211.12.949
спиро[хроман-3,1'-циклопентан]-2-он (3l). Выход
3.46 г (78%), т.пл. 159-160°С. ИК спектр, ν, см-1:
6. CrysAlisPro, Agilent Technologies, Version 1.171.37.33
1763, 1669 (C=O).Спектр ЯМР 1H, δ, м.д.: 1.41 т
(release 27-03-2014 CrysAlis171.NET).
(3Н, Ме, J 7.2 Гц), 1.46-1.95 м (7H), 2.48 м [1Н,
7. Sheldrick G.M. Acta Cryst.
2008, A64,
112. doi
(CH2)4], 3.09 д.д (1Н, СH2, J 7.8 Гц, 17.4 Гц), 3.11
10.1107/S0108767307043930
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 3 2019
ВЗАИМОДЕЙСТВИЕ МЕТИЛ 1-БРОМЦИКЛОПЕНТАНКАРБОКСИЛАТА С ЦИНКОМ
401
Interaction of Methyl 1-Bromocyclopentanecarboxylate
with Zinc and 1-Aryl-3-(2-hydroxyphenyl)prop-2-en-1-ones
E. A. Nikiforova*, D. V. Baibarodskikh, N. F. Kirillov, M. V. Dmitriev, and S. N. Shurov
Perm State University, 614990 Russia, Perm, ul. Bukireva 15
*e-mail: vikro@ya.ru
Received November 7, 2018
Revised November 28, 2018
Accepted December 15, 2018
By the interaction of Reformatsky reagent, derived from methyl 1-bromocyclobutanecarboxylate and zinc, with
1-aryl-3-(2-hydroxyphenyl)-1-phenylprop-2-en-1-ones,
4-(2-aryl-2-oxoethyl)spiro[chromane-3,1'-cyclopentan]-
2-onesis obtained. The reaction mechanism based on carried out quantum-chemical calculationsby the DFT/
TZVP methods proposed.
Keywords: Reformatsky reaction, 1-bromocycloalkanecarboxylates, 1-bromocyclopentanecarboxylate, spiro-
heterocycles, chromane-2-ones, hydroxychalcones, spirochromanones
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 3 2019