ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ, 2019, том 55, № 8, с. 1172-1175
УДК 547.493 + 547.426
МЕТИЛИРОВАНИЕ АНИЛИНА И ЕГО ПРОИЗВОДНЫХ
ДИМЕТИЛКАРБОНАТОМ ПОД ДЕЙСТВИЕМ
ГРАНУЛИРОВАННОГО ЦЕОЛИТА FeHY-mmm
© 2019 г. Р. И. Хуснутдинов*, Н. А. Щаднева, Ю. Ю. Маякова, А. Н. Абдрахманов,
А. Н. Хазипова, Б. И. Кутепов
ФГБУН «Институт нефтехимии и катализа РАН»,
450075, Россия, Республика Башкортостан, г.Уфа, пр. Октября 141
*e-mail: inklab4@gmail.com
Поступила в редакцию 24 января 2019 г.
После доработки 29 марта 2019 г.
Принята к публикации 12 апреля 2019 г.
Осуществлено селективное метилирование анилина и его производных диметилкарбонатом под
действием микро-, макро- и мезопористого цеолита FeHY-mmm без связующих с получением N-
монометиланилинов.
Ключевые слова: N-метиланилины, диметилкарбонат, метилирование, цеолиты, замещенные анилины.
DOI: 10.1134/S0514749219080044
N-Метиланилины - важный класс азотсодер-
известного реагента «зеленой химии». Для успеш-
жащих соединений. Они используются для
ного протекания реакции необходимы основание -
получения лекарственных препаратов, красителей
К2СО3 и межфазный катализатор - полиэтилен-
и взрывчатых веществ. N-Метиланилин - экологи-
гликоль PEG-6000. Несмотря на использование
чески малоопасная антидетонационная добавка к
избытка основания, конверсия анилинов не превы-
бензинам. Промышленно важным методом полу-
шает 50% [3]. Кроме К2СО3, метилирование анилина
чения N-метиланилинов является метилирование
с использованием ДМК катализируют гидротал-
анилинов алкилгалогенидами и метанолом
[1].
циды магния и алюминия при 240-275°С в течение
Общим недостатком указанного метода является
2 ч [4]. В качестве катализаторов N-метилирования
низкая селективность. Так, например, в реакциях
анилина с помощью ДМК применяют цеолиты NaY
анилинов с метанолом наряду с N-алкилированием
и KY, взятые в двукратном избытке по отношению
проходит и N,N-диалкилирование, а также наблю-
к ароматическому амину [5]. Реакция в их присутс-
дается алкилирование в кольцо с образованием
твии проходит в относительно мягких условиях
толуидинов (выход 1-54%). Эти реакции проходят
(100°С, 2-3 ч) и приводит к N-метиланилину с
в присутствии медь-, ванадий-, железо-, кобальт-
выходом 97%. Аналогичная реакция ДМК с заме-
алюмофосфатов (M-AlPO4, М = Cu, V, Fe, Co) при
щенными анилинами общей формулы X-PhNH2
повышенной температуре (200-300°С) [2].
(где X = п-CH3, o-CH3, п-OCH3, п-NO2 и п-COOH) в
присутствии NaY и KY проходит очень медленно,
Образование смеси N-моно- и N,N-диметилани-
а выходы N-метиланилинов не превышают 6% [5].
линов создает большие трудности при их выде-
лении в индивидуальном виде, так они имеют
Осуществлено N-метилирование анилина и его
близкие температуры кипения. Особенно сложно
производных диметилкарбонатом в присутствии
разделить N-метиланилин и N,N-диметиланилин,
10 масс. % микро-, мезо- и макропористых цеолитов
которые имеют т.кип. 196 и 194°С соответственно.
KNaX, NaY и НY [6]. В условиях 150°С в течение
Согласно [3], N-монометилирование анилинов
1 ч в зависимости от кислотности цеолита образует-
можно осуществить с использованием в качестве
ся смесь N-метил- или N,N-диметиланилинов (соот-
метилирующего агента диметилкарбоната (ДМК) -
ношение 88:5 - 2:90) с общим выходом 60-90%.
1172
МЕТИЛИРОВАНИЕ АНИЛИНА И ЕГО ПРОИЗВОДНЫХ ДИМЕТИЛКАРБОНАТОМ
1173
Схема 1.
NH2
NHMe
FeHY-mmm (5 масс. %)
+ MeOCO2Me
C, 3 ч, 99%
120o
_MeOH, _CO2
1 : 4
1
1a
Схема 2.
NH2
Me
NHMe
Me
2
NH2
2a, 78%
NHMe
Me
FeHY-mmm (5 масс. %)
3
MeOCO2Me
120оС, 3 ч,
4 экв.
Me
_MeOH, _CO
2
NH2
3a, 92%
NHMe
Me
4
Me
4a, 99%
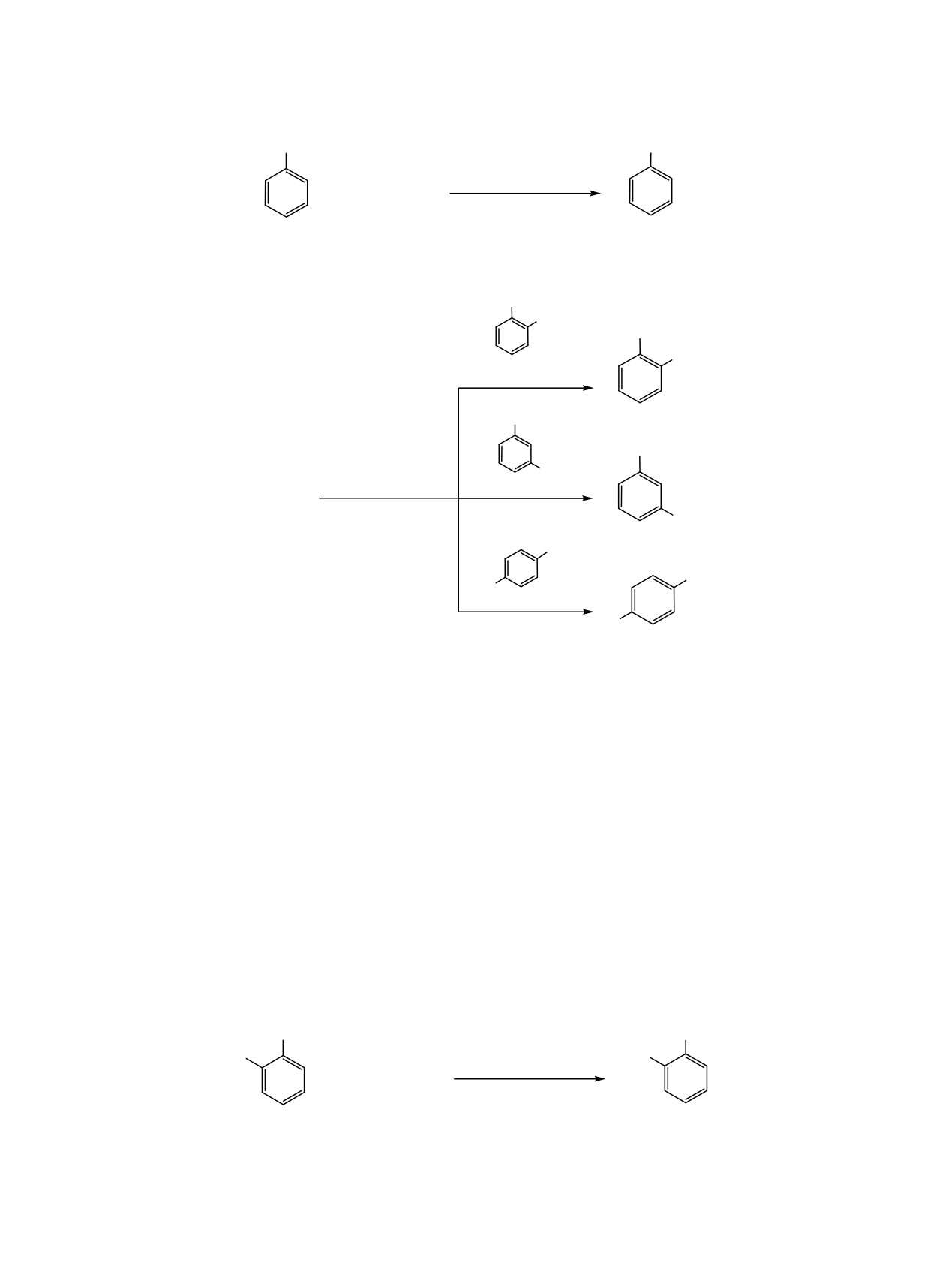
В настоящей работе установлено, что эффек-
Расположение метильного заместителя в толуи-
тивным катализатором N-монометилирования ани-
динах оказывает заметное влияние на их конвер-
лина и его производных с помощью ДМК является
сию, максимальный выход N-метилпроизводного
цеолитный катализатор FeHY-mmm, приготовлен-
наблюдается для п-толуидина (схема 2).
ный пропиткой микро-, макро- и мезопористого
При увеличении продолжительности реакции (5 ч)
цеолита НY-mmm, не содержащего связующих
или концентрации катализатора (10 масс. %) кон-
веществ, раствором Fe(NO3)3·9H2O c последующей
версия о- и м-толуидинов возрастает, но одновре-
термообработкой в 2 режимах: при 150°С (4 ч) и при
менно снижается селективность процесса из-за
450°С (3 ч). Таким способом были получены образцы
образования N,N-диметилтолуидинов, выход которых
катализатора с содержанием Fe2O3 3-5 масс. %.
может достигать 50%. Увеличение температуры
Так, реакция анилина (1) с ДМК (1:4) при 120°С
также приводит к снижению селективности
в течение 3 ч в присутствии катализатора FeHY-
реакции.
mmm (5 масс.%) приводит к образованию N-
метиланилина
(1а) с количественным выходом
Очень активно реагирует с ДМК в присутствии
(схема 1).
FeHY-mmm о-хлоранилин (5), который количест-
Схема 3.
NH2
NHMe
Cl
Cl
FeHY-mmm (5 масс. %)
+ MeOCO2Me
120oC, 3 ч, 99%
_MeOH, _CO2
1 : 4
5
5a
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 8 2019
1174
ХУСНУТДИНОВ и др.
Схема 4.
NH2
NHMe
FeHY-mmm (5 масс. %)
+ MeOCO2Me
120oC, 3 ч, 99%
CO2
_MeOH, _
X
X
1 : 4
6_8
5a_7a
X = Cl (6, 6a), Br (7, 7a), NO2 (8, 8a).
венно превращается в N-метил-о-хлоранилин (5а)
щей стали объемом 17 мл или стеклянную ампулу
(схема 3).
объемом 20 мл (результаты параллельных опытов
практически не отличаются) помещали 5 масс. %
Также гладко проходит N-монометилирование
катализатора FeHY без связующего (FeHY-БС),
п-хлор-, n-бром- и n-нитроанилинов (6-8) (схема 4).
100 ммоль анилина или его производного и 400 ммоль
Таким образом, разработан метод селективного
ДМК, автоклав герметично закрывали (ампулу запаи-
синтеза моно-N-метиланилинов с помощью реа-
вали) и нагревали при 120°С 3 ч. После окончания
гента «зеленой химии» ДМК с использованием
реакции автоклав охлаждали до комнатной темпе-
цеолитного микро-, мезо- и макропористого
ратуры, вскрывали, реакционную массу фильтро-
катализатора FeНY-mmm без связующих.
вали через слой Al2O3. ДМК отгоняли, остаток
перегоняли при атмосферном давлении или в
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
вакууме, или перекристаллизовывали из этанола.
Строение синтезированных соединений дока-
Анилин, о-, м- и п-толуидины, о-хлоранилин, п-
зано спектральными методами и сравнением их с
хлор, п-бром-, п-нитроанилины и диметилкарбонат
известными образцами [6].
использованы коммерческие доступные реагенты
фирмы «Sigma-Aldrich».
БЛАГОДАРНОСТИ
Спектры ЯМР
1Н и 13С регистрировали на
приборе Bruker Avance-400 (400.13 и 100.62 МГц
Структурные исследования соединений прове-
соответственно) в СDCl3. Масс-спектры снимали на
дены в Центре коллективного пользования
приборе Shimadzu GCMS-QP2010Plus, капилляр-
«Агидель» при Институте нефтехимии и катализа
ная колонка SPB-5, 30 м×0.25 мм, газ-носитель -
УФИЦ РАН г. Уфа.
гелий, температура от 40 до 300°С (8 град/мин),
температура испарения 280°С, энергия ионизации
КОНФЛИКТ ИНТЕРЕСОВ
70 эВ. Элементный состав образцов определяли на
элементном анализаторе Каrlo Erba 1106.
Авторы заявляют об отсутствии конфликта
интересов.
Ход реакций и чистоту полученных соединений
контролировали методом газо-жидкостной
CПИСОК ЛИТЕРАТУРЫ
хроматографии на приборе Shimadzu GC-9A, GC-
2014, колонка 2 м×3 мм, неподвижная фаза -
1. March J., Advanced Organic Chemistry, 4 Edn., New
силикон SE-30 (5%) на носителе Chromaton N-AW-
York: Wiley, 1999, 441.
HMDS, температурный режим от 50 до 270°С
2. Nagaraja N., Kuriakosa G. New J. Chem. 2003, 27, 765.
(8 град/мин), газ-носитель - гелий (47 мл/мин).
doi 10.1039/B208085K
3. Trotta F., Tundo P., Moraglio G. J. Org. Chem. 1987,
Образцы цеолита FeHY без связующего (FeHY-
52, 1300-1304. doi 10.1021/jo00383a024
БС), промотированные оксидом железа, были
4. Juárez R., Padilla A., Corma A., Garcia H. Ind. Eng.
приготовлены на основе цеолита HY-mmm по
Chem. Res. 2008, 47, 8043. doi 10.1021/ie800126t
методике [7].
5. Sreekumar K., Mathew T., Mirajkar S. P., Sugunan S.,
Метилирование анилинов с помощью ДМК
Rao B.S. Appl. Catal. A. 2000, 201, L1. doi 10.1016/
(общая методика). В микроавтоклав из нержавею-
S0926-860X(00)00418-X
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 8 2019
МЕТИЛИРОВАНИЕ АНИЛИНА И ЕГО ПРОИЗВОДНЫХ ДИМЕТИЛКАРБОНАТОМ
1175
6. Хуснутдинов Р.И., Щаднева Н.А., Маякова Ю.Ю.,
7. Кутепов Б.И., Травкина О.С., Павлова И.Н.,
Ардиева С.И., Хазипова А.Н., Кутепов Б.И. ЖОрХ.
Хазипова А.Н., Григорьева Н.Г., Павлов М.Л. ЖПХ.
2016, 52, 1574. [Khusnutdinov R.I., Shchadneva N.A.,
2015, 88, 70. [Kutepov B.I., Travkina O.S., Pavlova I.N.,
Mayakova Yu.Yu, Ardieva S.I., Khazipova A.N.,
Khazipova A.N., Grigor’eva N.G., Pavlov M.L. Russ.
Kutepov B.I. Russ. J. Org. Chem. 2016, 52, 1565.] doi
J. Appl. Chem.
2015,
88,
65.] doi
10.1134/
10.1134/S1070428016110038
S1070427215010103
Methylation of Aniline and Its Derivatives with Dimethyl
Carbonate under the Action of the Zeolite FeHY-mmm
R. I. Khusnutdinov*, N. A. Shchadneva, Yu. Yu. Mayakova, A. N. Abdrakhmanov,
A. N. Khazipova, and B. I. Kutepov
Institute of Petrochemistry and Catalysis, Russian Academy of Sciences,
450075, Russia, Republic of Bashkortostan, Ufa, pr. Oktyabrya 141
*e-mail: inklab4@gmail.com
Received January 24, 2019; revised March 29, 2019; accepted April 12, 2019
Carried out selective methylation of aniline and its derivatives with dimethyl carbonate under the action of
micro-, macro- and mesoporous zeolite FeHY-mmm without binder with obtaining N-monomethylaniline.
Keywords: N-methylaniline, dimethyl carbonate, methylation, zeolites, substituted anilines
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 55 № 8 2019