ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ, 2020, том 56, № 5, с. 726-734
УДК 547.413.5:547.298.4
СИНТЕЗ N,N'-ДИЗАМЕЩЕННЫХ
ДИТИООКСАМИДОВ МОДИФИЦИРОВАННОЙ
РЕАКЦИЕЙ ВИЛЬГЕРОДТА-КИНДЛЕРА
© 2020 г. Т. Н. Пономарёваa, Е. В. Елисеенковb, А. А. Петровb, *, В. П. Боярскийb
a ФГБОУ ВО «Санкт-Петербургский государственный технологический институт (технический университет)»,
190013, Россия, г. Санкт-Петербург, Московский пр. 26
b ФГБОУ ВО «Санкт-Петербургский государственный университет»,
199034, Россия, г. Санкт-Петербург, Университетская наб. 7/9
*e-mail: aap1947@yandex.ru
Поступила в редакцию 20 января 2020 г.
После доработки 06 февраля 2020 г.
Принята к публикации 09 февраля 2020 г.
Оптимизированы условия реакции тетрахлорэтилена с серой и аминами (модифицированная реакция
Вилъгеродта-Киндлера). Реакция тетрахлорэтилена с серой и оснóвными первичными и вторичными
аминами алифатического ряда в диметилформамиде в мягких условиях приводит к N,N'-дизамещенным
дитиооксамидам с выходами 30-70% при 100% конверсии тетрахлорэтилена.
Ключевые слова: тетрахлорэтилен, N,N'-дизамещенные дитиооксамиды, реакция Вилъгеродта-Кин-
длера.
DOI: 10.31857/S0514749220050092
Дитиооксамид и его N- и N,N'-дизамещенные
самидом [11, 12], реакция Вильгеродта-Киндлера
широко используются в различных областях хи-
с глиоксалем, серой и аминами [13], а также мо-
мии [1], в частности, в качестве бинуклеофильных
дифицированная реакция Вильгеродта-Киндлера
лигандов для получения комплексов с металлами
(длительное кипячении смеси полихлорэтиленов
и аналитических реагентов для обнаружения и
(или полихлорэтанов) с серой и амином в органи-
количественного определения металлов [2-4], в
ческих растворителях (углеводородах, спиртах)
качестве билдинг-блоков в синтезе гетероциклов
[14, 15]. Метод тионирования амидов пентасуль-
[5, 6]. Среди производных дитиооксамидов най-
фидом фосфора является двустадийным - требует
дены вещества с антибактериальной активностью
предварительного синтеза соответствующих окса-
[7], галогенидные комплексы сурьмы(III) с N,N'-
ламидов и приводит к невысоким выходам конеч-
дициклогексилдитиооксамидом обладают цито-
ных продуктов. Реакция переамидирования дити-
статической активностью [8]. Наличие двух «мяг-
ооксамида не является универсальным методом,
ких» атомов серы наряду с «жесткими» атомами
поскольку пригодна только для первичных алифа-
азота в тиоамидной части делает эти молекулы
тических аминов, кроме того, в качестве побочных
мощными лигандами в координационной химии
продуктов реакции образуются амидины и проис-
[9].
ходит выделение сероводорода. Недостатком мо-
Основными методами синтеза дитиооксамидов
дифицированной реакции Вильгеродта-Киндлера
являются: тионирование амидов пентасульфидом
является проведение ее при высокой температуре
фосфора или реагентом Лавессона [10, 11], реак-
(> 100°C) в течение длительного времени (более
ция первичных алифатических аминов с дитиоок-
20 ч) с использованием избытка серы и амина.
726
СИНТЕЗ N,N'-ДИЗАМЕЩЕННЫХ ДИТИООКСАМИДОВ
727
В то же время в литературе описаны иссле-
стью. Найденные условия проведения реакции яв-
дования по оптимизации классической реакции
ляются более мягкими по сравнению с литератур-
Вильгеродта-Киндлера с ароматическими альде-
ными (100-110°С, 30 ч в толуоле) [15].
гидами и кетонами [16, 17]. В ряде работ [18-21]
С целью выделения продукта реакции в анало-
отмечали существенное ускорение реакции при
гичных условиях была проведена препаративная
использовании диметилформамида (ДМФА). Хотя
реакция с 10 ммоль тетрахлорэтилена. Масса по-
полный детальный механизм этой реакции до сих
лученного сырого соединения 1 составила 1670 мг
пор остаётся неизвестным, отдельные его стадии
(89%), после перекристаллизации из пропан-2-
представляются весьма обоснованными. На пер-
ола выход составил 1433 мг (77%), т.пл. 150-151°С
вой стадии элементарная сера (S8) взаимодейству-
(лит. 151-152°С [15]). Полученное соединение да-
ет с амином (R2NH) по нескольким параллельным
лее анализировали методами масс-спектрометрии
реакциям, в том числе, по реакции с образованием
высокого разрешения (ESI-MS), а также спектро-
аминотиола - потенциального S-нуклеофила [22]:
скопии ядерно-магнитного резонанса на ядрах 1H
R2NH + S8 = R2N(S7)SH.
и 13C.
Целью настоящей работы является оптими-
В области отрицательных ионов самый боль-
шой пик имеет m/z 283.1310, а в области поло-
зация условий проведения реакции тетрахлорэ-
жительных ионов - 307.1272, что подтверждает
тилена, серы и аминов различного строения в
брутто-формулу анализируемого продукта реак-
ДМФА (модифицированная реакция Вильгеродта-
ции (см. экспериментальную часть). В спектре
Киндлера) (схема 1).
ЯМР 13C наблюдается 5 сигналов, соответству-
Оптимизацию условий проведения процесса
ющих 5 неэквивалентным атомам углерода в мо-
первоначально проводили на примере реакции
лекуле анализируемого вещества. Слабопольный
тетрахлорэтилена с серой и циклогексиламином
сигнал с химическим сдвигом 182.97 м.д. соответ-
в ДМФА (для сопоставления полученных нами
ствует атому углерода в группе C=S. Сигнал при
данных с литературными) Реакцию проводили
55.77 м.д. - атому углерода в циклогексановом
при нагревании перемешиванием отмеренных ко-
кольце, связанном с электроотрицательным ато-
личеств реагентов в пробирке с завинчивающейся
мом азота. Три сигнала в сильном поле соответ-
крышкой, внутреннего стандарта для ГЖХ (н-но-
ствуют трём неэквивалентным атомам углерода
нан или хлорбензол) и растворителя (ДМФА).
циклогексанового кольца. В спектре ЯМР 1H сла-
Соотношение тетрахлорэтилена, серы и амина со-
бопольный синглет при 10.37 м.д. (интенсивность
ставляло 1:3:8 {избыток серы (1.5) и амина (1.3)
2H) соответствует протонам, связанным с атомами
обычно используют в реакциях Вильгеродта-
азота в тиоамидных группах, мультиплет в обла-
Киндлера ввиду образования побочных продуктов
сти 4.26 м.д. (2Н) относится к протонам фрагмента
[14, 15, 23, 24]}. При этом 4 моля амина необходи-
C-H, связанным с атомом азота. В сильном поле
мы для связывания 4 молей HCl.
имеется 5 групп мультиплетов (20 H), соответству-
ющих протонам двух циклогексановых колец.
При проведении реакции в течение 1.5 ч при
60°С конверсия тетрахлорэтилена составила 36%
Таким образом, в присутствии ДМФА рассма-
(опыт 1), а за 5.5 ч при 100°С - 99% (опыт 2), т.е.
триваемая реакция протекает с образованием же-
тетрахлорэтилен реагирует практически полно-
лаемого замещенного дитиооксамида 1 и ускоря-
Схема 1.
Cl
Cl
R1R2N
S
+ S + R1R2NH
+ (R1R2NH2)Cl
Cl
Cl
S
NR1R2
1-6
R1 = H, R2 = C6H11 (1), CH3OCH2CH2 (2), Ph (6); R1 + R2 = (CH2)5 (3), CH2CH2OCH2CH2 (4); R1 = R2 = н-Bu (5).
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
728
ПОНОМАРЁВА и др.
Таблица 1. Конверсия тетрахлорэтилена в реакции с серой и аминами в ДМФА при варьировании температуры и
времени реакции.
№ опыта
Амин
рКа
Время реакции, ч
Температура, °С
Конверсия С2Сl4, %
3
Циклогексиламин
10.63
5.5
100
99
4
Циклогексиламин
10.63
1.5
60
37
5
2-Метоксиэтиламин
9.89
5.5
100
100
6
2-Метоксиэтиламин
9.89
2.0
100
99
7
2-Метоксиэтиламин
9.89
71
28
90
8
Дибутиламин
11.31
5.5
100
95
9
Пиперидин
11.24
1.5
75
88
10
Пиперидин
11.24
1.5
60
59
11
Пиперидин
11.24
71
28
67
12
Морфолин
8.49
2.2
100
81
13
Морфолин
8.49
1.5
75
50
14
Морфолин
8.49
1.5
60
22
15
Анилин
4.60
5.5
100
0
ется примерно в 5 раз по сравнению с описанной в
При сопоставлении реакционной способно-
литературе реакцией в толуоле [15].
сти аминов в реакциях тетрахлорэтилена с серой
и аминами с их основностью оказалось, что на
Далее мы изучали реакции с первичными али-
качественном уровне выполняется простое соот-
фатическими аминами - 2-метоксиэтиламином,
ношение между конверсией тетрахлорэтилена и
вторичными алифатическими аминами - пипери-
основностью амина: чем выше основность амина,
дином, морфолином, дибутиламином и аромати-
тем больше конверсия субстрата при идентичных
ческим амином - анилином. Полученные данные
условиях проведения процесса. Так, например,
представлены в табл. 1.
8.46)
в большинстве опытов с морфолином (pKa
Оказалось, что пиперидин оказался более ак-
конверсия тетрахлорэтилена ниже, чем с пипери-
тивным реагентом в рассматриваемых реакциях
дином (pKa 11.22) (табл. 1).
по сравнению с циклогексиламином. Высокая кон-
версия тетрахлорэтилена в реакции с пиперидином
Строение соединений 2-4 установлено на осно-
достигается в более мягких условиях, чем в реак-
вании данных ЯМР 1Н и 13С и метода масс-спектро-
ции с циклогексиламином - уменьшается и время
метрии высокого разрешения (ESI-MS). Строение
проведения реакции, и температура. Для циклогек-
соединения 5 доказано методом масс-спектроме-
силамина конверсия тетрахлорэтилена 99% дос-
трии высокого разрешения (ESI-MS). В спектрах
тигалась за 5.5 ч при 100°С (опыт 3), а для пипе-
ЯМР 1Н и 13С соединения 4 все сигналы прото-
ридина конверсия 88% за 1.5 ч при 75°С (опыт 9).
нов и атомов углерода удвоены по интеграль-
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
СИНТЕЗ N,N'-ДИЗАМЕЩЕННЫХ ДИТИООКСАМИДОВ
729
ной интенсивности. В спектре ЯМР 13C наблю-
других неперекрывающихся сигналов (спиновая
даются сигналы атома углерода группы C=S при
система типа АBX).
192.35 м.д. и три сигнала атомов углерода морфо-
В случае слабоосновного амина - анилина (pKa
линового кольца, принадлежащие соответственно
4.60) за 5.5 ч при 100°С конверсия составила менее
атомам углерода СН2OСН2 при 66.15 м.д. и атомам
0.05%. Литературные данные для классической
углерода СН2NСН2 при 52.02 и 47.68 м.д. (явля-
реакции Вильгеродта-Киндлера с карбонильными
ющиеся магнитно-неэквивалентными по причине
соединениями, например, с бензальдегидом, также
частичной двоесвязанности связи С-N). Атомы
свидетельствуют об инертности анилина в типич-
углерода СН2NСН2 морфолинового кольца в цис-
ных условиях процесса [19].
и транс-положениях по отношению к группе С=S
При рассматриваемом способе реакции те-
вследствие анизотропии имеют значительную раз-
трахлорэтилена с серой и амином в присут-
ницу химических сдвигов.
ствии ДМФА смесь, как правило, гетерогенна.
В спектре ЯМР 1H соединения 4 наблюдаются
Растворимость серы в ДМФА при 25°С не превы-
5 групп сигналов протонов морфолинового коль-
шает 0.191 масс % [25]. По мере протекания ре-
ца при 4.47 д.т. (2Н), 4.04 д.д.д. (2Н), 3.87 м (8Н),
акции количество серы уменьшается, и из реакци-
3.67 д.д.д (2Н) и 3.57 д.д.д (2Н) м.д. Отнесение
онной смеси постепенно выпадает замещенный
сигналов в спектре сделано на основании спек-
дитиооксамид. Особенно низкой растворимостью
тра HSQC, в котором наблюдаются кросс-пики
обладает высокоплавкий
1,2-диморфолиноэ-
C2 66.15/3.87 (4H2, 2H6), C2 66.15/3.67 (2H6), C5
тан-1,2-дитион (4).
52.02/3.87 (2H5), C5 52.02/3.57 (2H5), C6 47.68/4.47
Мы попытались провести реакцию в гомо-
(2H3), C6 47.68/4.04 (2H3). Кросс-пики в спектре
генных условиях, используя для растворения
COSY дают возможность однозначного отнесения
серы смеси органический растворитель/ДМФА.
всех вицинальных протонов к аксиальным и эк-
С учетом очень низкой растворимостью серы в
ваториальным: 3.57 м (2Н, H5ax), 3.67 м (2Н, H6ax),
большинстве органических растворителей для
3.87 м [8Н (2H2ax, 2H2eq, 2H5eq, 2H6eq)], 4.04 м (2Н,
проведения опытов были выбраны циклогексан,
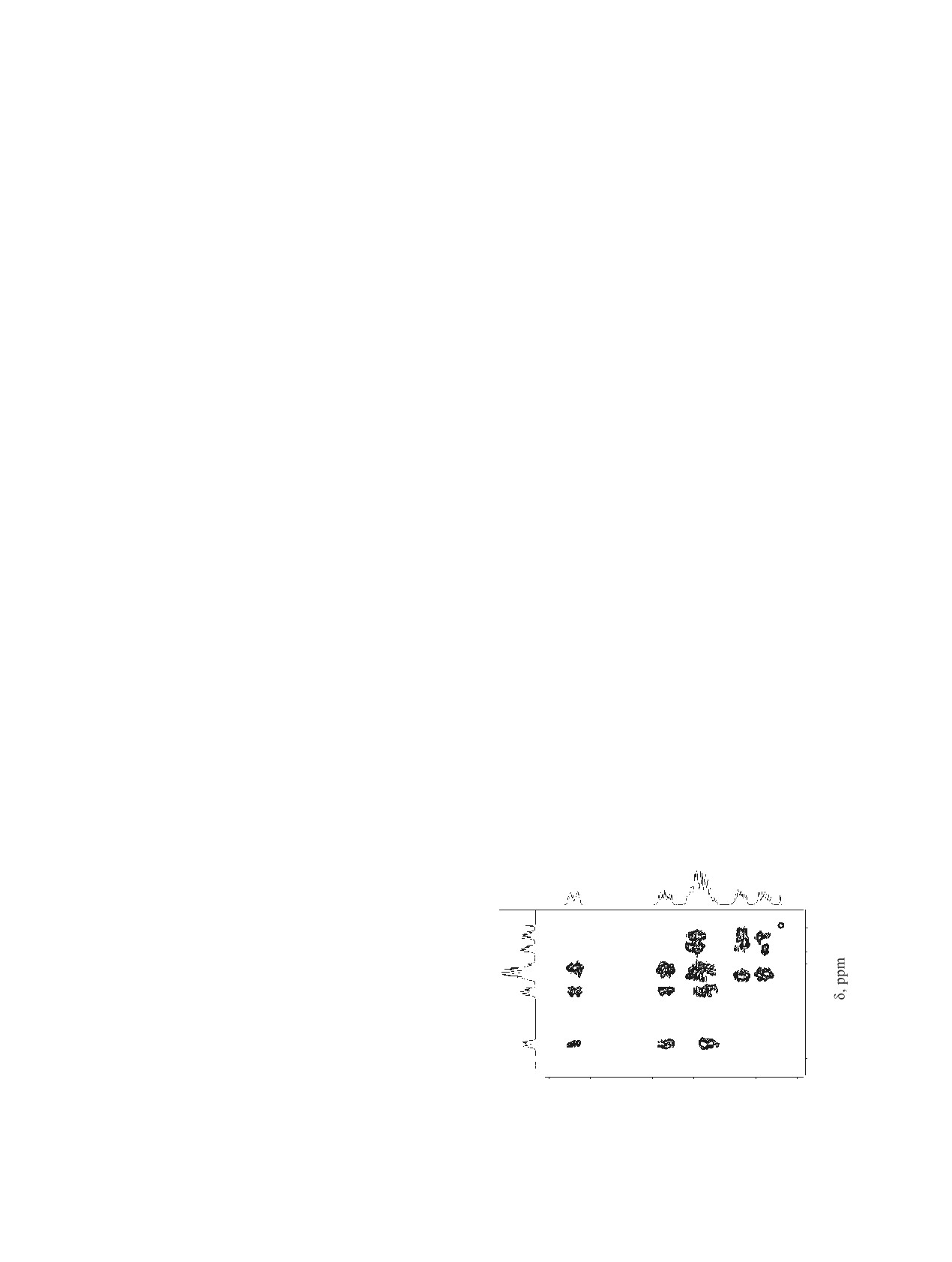
H3ax), 4.47 д.т (2Н, H3eq) (см. рисунок). Если обра-
диоксан и бензол. Были приготовлены насыщен-
тить внимание на наборы констант всех непере-
ные растворы серы в указанных растворителях.
крывающихся сигналов, а также на их сумму, то
Рассчитанное количество исходной реакционной
можно заключить, что их мультиплетная структу-
смеси тетрахлорэтилена (с внутренним стандар-
ра одинаковая (д.д.д.), но набор величин констант
том), амина и ДМФА добавляли к насыщенному
для самого слабопольного из них чуть меньше (в
сумме примерно на 3-4 Гц) по сравнению со все-
2eq,
ми остальными тремя. Следовательно, он является
6eq,
13eq
15eq
преимущественно экваториальный, а остальные
2ax,
5eq,
13ax
преимущественно аксиальные. Термин «преиму-
16eq
6ax, 5ax,
3eq,
3ax,
щественно» используется здесь для указания на
12eq
12ax
15ax 16ax
время жизни этого протона в экваториальном или
аксиальном состоянии. Такая терминология услов-
3.5
на, поскольку в морфолиновых кольцах происхо-
дит быстрый в шкале времени ЯМР конформаци-
онный обмен типа кресло-кресло, и все вициналь-
4.0
ные константы усреднены. Величины констант
четырёх неперекрывающихся сигналов не могут
быть установлены простым измерением расстоя-
4.5
ний между компонентами этих сигналов, посколь-
ку перекрывающиеся сигналы восьми протонов в
4.50
4.00
3.50
δ, ppm
области 3.8 м.д. образуют сильно связанные си-
стемы, которые искажают мультиплетность всех
Фрагмент спектра COSY соединения 4.
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
730
ПОНОМАРЁВА и др.
Таблица 2. Конверсия тетрахлорэтилена в реакциях с аминами и растворенной серой.
№ опыта
Сорастворитель
Амин
Температура, °С
Время, ч
Конверсия С2Сl4, %
16
Циклогексан
Пиперидин
75
22.5
47
17
Циклогексан
Морфолин
75
22.5
30
18
Диоксан
Пиперидин
60
25
23
19
Диоксан
Циклогексиламин
60
25
22
20
Бензол
Пиперидин
75
23
58
21
Бензол
Циклогексиламин
75
23
29
22
Бензол
Морфолин
75
23
23
23
Бензол
Морфолин
75
71
39
24
Бензол
2-Метоксиэтиламин
75
71
34
25
Бензол
Дибутиламин
75
71
52
(1-2 масс %) раствору серы в органическом раство-
некоторые выводы. Практически все изученные
рителе. По стандартной методике проводили реак-
амины при соответствующем выборе температуры
ции и определяли конверсию тетрахлорэтилена.
и времени проведения реакции (достаточно 4-7 ч
Полученные результаты представлены в табл. 2.
при 100°С) способны образовывать замещённые
дитиооксамиды со средними и с высокими выхо-
При сопоставлении полученных данных с ре-
дами.
зультатами опытов в гетерогенной среде (в ДМФА
без добавления другого органического раство-
Препаративные реакции проводили в двух ва-
рителя) следует учитывать, что при разбавлении
риантах: а и б. В варианте а реакции проводили
ДМФА инертным органическим растворителем
при мольном соотношении тетрахлорэтилен-
скорость реакции существенно снижается. Для
сера-амин 1:3:8. Количество амина по сравнению
достижения больших конверсий тетрахлорэтилена
с требуемым по стехиометрии может быть сокра-
приходилось в несколько раз увеличивать время
щено до 2.5-3.0 моль на моль тетрахлорэтилена,
реакции.
если проводить реакцию в ДМФА в присутствии
основания (K2CO3) (вариант б). При проведении
Хорошо известно, что для классической реак-
реакции тетрахлорэтилена с серой и циклогек-
ции Вильгеродта-Киндлера характерно наличие
силамином в ДМФА в присутствии поташа (со-
большого числа побочных продуктов. Целый ряд
отношение реагентов 1:3.0:3.0:2.2) при 100°С в
из них образуется без участия карбонильного сое-
течение 6 ч масса сырого продукта 1 составила
динения, как результат реакции серы с амином, на-
95%, после перекристаллизации из метанола вы-
пример, R2N(Sn)NR2 (n = 1-6) [22]. Нами при ана-
ход составил 72%. Количество ДМФА составляло
лизе реакционных смесей методом ГХМС в ряде
0.5-1.5 мл на 1 ммоль тетрахлорэтилена. В каче-
случаев были обнаружены следовые количества
стве инертных сорастворителей при проведении
некоторых других продуктов побочных реакций,
реакции могут быть использованы метилцелло-
например, 4,4-дитиодиморфолин, циклогексили-
зольв (т.кип. 124°С) и 1-пропанол (т.кип. 97°С) в
зотиоцианат.
количестве 0.5-1.5 мл на 1 ммоль тетрахлорэти-
Результаты, полученные при изучении зави-
лена. Использование инертных сорастворителей
симости конверсии тетрахлорэтилена в условиях
способствует более мягкому течению процесса
реакции Вильгеродта-Киндлера от природы силь-
и облегчает перемешивание реакционной смеси,
ноосновного амина, позволяют сформулировать
особенно в присутствии поташа.
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
СИНТЕЗ N,N'-ДИЗАМЕЩЕННЫХ ДИТИООКСАМИДОВ
731
Таким образом, оптимизированы условия про-
сан-дихлорметан (2:1 по объёму)] и в течение
ведения реакции тетрахлорэтилена с серой и пер-
0.5-1.0 ч сушили прокаленным сульфатом натрия
вичными и вторичными алифатическими аминами
(50-100 мг). 1 мкл полученного разбавленного
в ДМФА с образованием замещённых дитиоами-
раствора анализировали методом ГХМС.
дов щавелевой кислоты. На качественном уровне
Методика очистки тетрахлорэтилена. В дели-
выполняется зависимость между реакционной
тельной воронке смешивали 100 мл С2Сl4 и 10 мл
способностью амина в реакции с тетрахлорэти-
HCl, встряхивали, отделяли C2Cl4. Промывали его
леном и серой и его основностью, т.е. величиной
водой от соляной кислоты (в делительной воронке)
pKa.
и один раз 5%-ным раствором NaHCO3, добавляли
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
15 г Na2SO4 и 1 г Na2CO3 в качестве осушителей.
Оставили на сутки. Перегоняли тетрахлорэтилен
Спектры ЯМР
1H, 13С регистрировали на
в вакууме при 160 мм рт.ст., собирая фракцию,
спектрометре Bruker Avance II+ [рабочая часто-
кипящую при 72-73°С. По данным ГХМС препа-
та 400.13 (1Н), 100.61 (13C) МГц], при комнатной
рат содержит следовые (меньше 0.2%) количества
температуре. Химические сдвиги измеряли отно-
1,1,2-трихлорэтана и 1,1,2,2-тетрахлорэтана.
сительно остаточных сигналов протона и атома
углерода растворителя: δH 7.27 м.д. (CHCl3), δС
1,2-Ди(циклогексиламино)этан-1,2-дитион
77.0 м.д. (CDCl3). Масс-спектры регистрировали
(1). а. Смесь 1742 мг (10.51 ммоль) тетрахлор-
на приборе Bruker micrOTOF с ионизацией элек-
этилена, 1011мг (31.53 ммоль) тонкоизмельчён-
трораспылением (ESI), сканирование m/z в диа-
ной серы, 5213 мг (52.56 ммоль) циклогексила-
пазоне 50-3000. Напряжение ионного источника
мина, 5.5 мл ДМФА (соотношение масс ДМФА и
на входе ±4500 В и на выходе из капилляра ±70-
C2Cl4 3:1) и 4 мл метилцеллозольва перемешивали
150 В. Образцы для анализа растворяли в MeОН.
при 100°С в течение 16 ч. По завершению реак-
Хромато-масс-спектрометрический анализ был
ции реакционную смесь выливали в стакан с 30-
проведён на приборе Shimadzu GCMS QP-2010
40 мл дистиллированной воды, хорошо переме-
SE, с ионизацией электронным ударом (70 эВ),
шивали и нейтрализовали добавлением 2-3% HCl.
сканирование m/z в диапазоне 50-500, темпе-
Получившийся продукт реакции отфильтровы-
ратура детектора 220°С, колонка 1 - Rtx-5MS
вали, промывали на фильтре дистиллированной
(30 м×0.32 мм×0.25 мкм), колонка 2 - Optima - 1
водой и оставляли до полного высыхания. Масса
(25 м×0.32 мм×0.35 мкм), поток газа-носителя
сырого соединения 1 составила 1670 мг (89.4%),
(аргон) 0.8 мл/мин. В работе использовали ком-
т.пл. 143-144°С, после перекристаллизпции из
мерческие неорганические соединения и амины
пропан-2-ола 1433 мг (76.7%), т.пл. 150-151°С
марки «хч» и «чда» фирм Вектон, Acros и Merck.
(лит. 151-152°С [15], 149.0-149.5°С [11]). Спектр
Тетрахлорэтилен фирмы Вектон предварительно
ЯМР 1Н (CDCl3), δ, м.д.: 1.35 м (2Н, СН2), 1.47 м
очищали (см. экспериментальную часть).
(8Н, 4СН2), 1.68 м (2Н, СН2), 1.79 м (4H, 2СН2),
2.07 м (4H, 2СН2), 4.26 м (2H, 2СН), 10.37 c (2H,
Методика проведения качественного и коли-
2NH). Спектр ЯМР 13С (CDCl3), δ, м.д.: 24.31
чественного анализа методом ГХМС. Все ана-
(СН2), 25.42 (СН2), 30.60 (СН2), 55.77 (СНN),
лизы методом ГХМС проводили на капиллярных
182.97 (С=S). Масс-спектр (ESI): m/z
283.1310
колонках (1 или 2) в режиме программирования
[M - H]-. C14H23N2S2. Вычислено: 283.1308 [M -
температуры при полном разделении анализиру-
H]-; m/z 307.1272 [M + Na]+. C14H24N2NaS2. Вы-
емых компонентов за 15-20 мин. Пробу реакци-
числено 307.1274 [M + Na]+.
онной смеси разбавляли дистиллированной водой
в 20-50 раз, тщательно нейтрализовали 1%-ной
Синтез
1,2-ди(циклогексиламино)этан-
соляной кислотой, экстрагирововали диэтило-
1,2-дитиона (1) в присутствии поташа. б. Смесь
вым эфиром. Органический экстракт встряхива-
1090 мг (6.57 ммоль) тетрахлорэтилена, 632 мг
ли с 5-кратным объёмом дистиллированной воды.
(19.71 ммоль) тонкоизмельчённой серы, 1930 мг
Пробу органического слоя объёмом 0.05-0.1 мл
(19.55 ммоль) циклогексиламина,
2010 мг
разбавляли 1.0-1.7 мл н-гексана [или смеси н-гек-
(14.54 ммоль) поташа, 3.5 мл диметилформами-
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
732
ПОНОМАРЁВА и др.
да и 6.5 мл метилцеллозольва перемешивали при
4.33 м (2H, СН2N). Спектр ЯМР 13С (CDCl3), δ,
100°С в течение 7 ч. Последующую обработку
м.д.: 23.99 (СН2), 25.13 (СН2), 26.07 (СН2), 48.46
реакционной смеси проводили по вышеописан-
(СН2N), 52.72 (СН2N), 191.90 (С=S). Масс-спектр
ной методике. Выход 1765 мг (94.4%). После пе-
(ESI-MS): m/z 279.0966 [M + Na]+. C12H20N2NaS2.
рекристаллизации из метанола получали 1343 мг
Вычислено 279.0969 [M + Na]+.
(71.8%) соединения 1, т.пл. 150-151°С.
Синтез
1,2-дипиперидиноэтан-1,2-дитиона
1,2-Ди(2-метоксиэтиламино)этан-1,2-дитион
(3) в присутствии поташа. б. Смесь 1050 мг тетра-
(2). а. Смесь 936 мг тетрахлорэтилена (5.64 ммоль),
хлорэтилена (6.33 ммоль), 690 мг (21.52 ммоль)
542 мг (16.92 ммоль) серы, 3389 мг (45.12 ммоль)
тонкоизмельчённой серы, 1600 мг (18.79 ммоль)
2-метоксиэтиламина и 5.6 мл ДМФА перемешива-
пиперидина, 2030 мг (14.69 ммоль) К2СО3, 3.5 мл
ли при 95°С 8 ч. Последующую обработку реак-
ДМФА и 7 мл метилцеллозольва перемешивали
ционной смеси проводили по обычной методике.
при 100°С в течение 8 ч. Последующую обработку
Выход сырого продукта 816 мг, после перекри-
реакционной смеси проводили по вышеописанной
сталлизации из этанола получено 683 мг (51.0%),
методике. Выход сырого продукта реакции 833 мг
т.пл. 101-102°С (лит. 99-99.5°С [26]). Спектр ЯМР
(51.3%), т.пл. 90-92°С. После перекристаллизации
1Н (CDCl3), δ, м.д.: 3.42 с (6Н, ОСН3), 3.67 м (4Н,
из смеси хлороформ-гексан (1:2 по объему), а за-
2ОСН2), 3.86 м (4Н, NСН2), 10.48 c (2H, NH).
тем из метанола получено 408 мг (25.1%) соедине-
Спектр ЯМР 13С (CDCl3), δ, м.д.: 47.16 (OСН3),
ния 3, т.пл. 169-170°С (лит. 126°С [27].
59.02 (OСН2), 184.98 (С=S). Масс-спектр (ESI):
1,2-Диморфолиноэтан-1,2-дитион
(4).
а.
m/z 259.0545 [M + Na]+. C8H16N2NaS2. Вычислено
Смесь 860 мг тетрахлорэтилена (5.19 ммоль),
259.0551.
499 мг (15.57 ммоль) тонкоизмельчённой серы,
Синтез
1,2-ди(2-метоксиэтиламино)этан-
3617 мг (41.52ммоль) морфолина, 6 мл ДМФА
1,2-дитиона (2) в присутствии поташа. б. Смесь
перемешивали при 100°С в течение 7 ч. Пос-
1210 мг тетрахлорэтилена (7.30 ммоль), 702 мг
ледующую обработку реакционной смеси про-
(21.9 ммоль) серы, 1420 мг (18.91 ммоль) 2-ме-
водили по вышеописанной методике. Получено
токсиэтиламина, 1690 мг (12.23 ммоль) поташа
852 мг (63.0%) сырого продукта реакции, т.пл.
и 5.6 мл ДМФА. перемешивали при 95°С 8 ч.
248-249°С, после перекристаллизации из этанола
Последующую обработку реакционной смеси про-
выход 704 мг (52.1%), т.пл. 284-285°С (лит. 255°С
водили по обычной методике. Масса сырого про-
[14]). Спектр ЯМР 1Н (CDCl3), δ, м.д.: 3.57 м (2Н,
дукта составила 1124 мг (65.0%), т.пл. 98-99°С.
H5ax), 3.67 м (2Н, H6ax), 3.87 м (8Н, 2H2ax, 2H2eq, 2H5eq,
После перекристаллизации из этанола получили
2H6eq), 4.04 м (2Н, H3ax), 4.47 д.т (2Н, H3eq). Спектр
929 мг (53.9%) соединения 2 с т. пл. 100-101°С.
ЯМР 13С (CDCl3), δ, м.д.: 47.68 и 52.02 (СNС),
66.15 (СН2, СOС), 192.35 (С=S). Масс-спектр
1,2-Дипиперидиноэтан-1,2-дитион (3). Син-
(ESI): m/z 283.0549 [M + Na]+. C19H16N2NaS2. Вы-
тезирован по методике а нагреванием при 95°С в
числено 283.0545.
течение 9 ч 1046 мг (6.31 ммоль) тетрахлорэтиле-
на, 607 мг (18.93 ммоль) тонкоизмельчённой серы,
Методика проведения реакции тетрахлор-
4298 мг (50.48 ммоль) пиперидина, 8.5 мл диметил-
этилена c серой и дибутиламином. Смесь 65 мг
формамида и 10 мл 1-пропанола. Последующую
(0.51 ммоль) тетрахлорэтилена, 49 мг (1.53 ммоль)
обработку реакционной смеси проводили по вы-
тонкоизмельчённой серы, 527 мг (4.08 ммоль)
шеописанной методике. Выход сырого продукта
дибутиламина и 1 мл ДМФА перемешивали при
реакции 940 мг (58%), т.пл. 90-92°С. После пере-
100°С в течение 5.5 ч. Последующую обработку
кристаллизации из смеси хлороформ-гексан (1:2
реакционной смеси проводили по вышеописан-
по объему), а затем из метанола получено 440 мг
ной методике. Структура 1,2-ди(дибутиламино)-
(27.2%) соединения 3, т.пл. 169-170°С (лит. 126°С
этан-1,2-дитиона (5) доказана методом масс-спек-
[27]). Спектр ЯМР 1Н (CDCl3), δ, м.д.: 1.54 м (2Н,
трометрии высокого разрешения (ESI-MS):
СН2), 1.72 м (8Н, 4СН2), 1.95 м (2Н, СН2), 3.50
367.2205
[M + Na]+.C18H36N2NaS2. Вычислено
м (2H, СН2), 3.70 м (2H, СН2), 4.02 м (2H, СН2),
367.2213. Соединение 5 описано в патенте [28].
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
СИНТЕЗ N,N'-ДИЗАМЕЩЕННЫХ ДИТИООКСАМИДОВ
733
БЛАГОДАРНОСТИ
11.
Hurd R.N., De La Mater G., McElheny G.C.,
Turner R.J., Wallingford V.H. J. Org. Chem. 1961, 26,
Работа выполнена с использованием обору-
3980-3987. doi 10.1021/jo01068a080
дования ресурсных центров СПбГУ «Магнитно-
12.
Woodburn H.M., Sroog C.E. J. Org. Chem. 1952, 17,
резонансные методы исследования»,
«Методы
371-378. doi 10.1021/jo01137a007
анализа состава вещества» и «Образовательный
13.
Dutron-Woitrin F., Merényi R., Viehe H.G. Synthesis.
ресурсный центр по направлению химия».
1985, 77-79. doi 10.1055/s-1985-31114
ФОНДОВАЯ ПОДДЕРЖКА
14.
Milligan B., Swan J.M. J. Chem. Soc. 1961, 1194-
Работа выполнена при финансовой поддержке
1200. doi 10.1039/JR9610001194
РНФ (грант № 19-13-00008).
15.
Becke F., Hagen H. Франц. заявка FR
1560926
(1967). C.A. 1970, 72, 54878x.
КОНФЛИКТ ИНТЕРЕСОВ
16.
Li J.J. Name Reactions. A Collection of Detailed
Авторы заявляют об отсутствии конфликта ин-
Mechanisms and Synthetic Applications. Berlin,
тересов
Heidelberg: Springer-Verlag, 2009. p. 576.
СПИСОК ЛИТЕРАТУРЫ
17.
Priebbenow D.L., Bolm C. Chem. Soc. Rev. 2013, 42,
1.
Vahrenkamp H. Angew. Chem. Int. Ed. 1975, 14, 322-
7870-7880. doi 10.1039/c3cs60154d
329. doi 10.1002/anie.197503221
18.
Wang Z. Comprehensive Organic. Name Reactions and
2.
Abbasi S., Bahiraei A. Food Chem. 2012, 133, 1075-
Reagents. Hoboken: John Wiley & Sons. 2010, 318.
1080. doi 10.1016/j.foodchem.2012.02.003
doi 10.1002/9780470638859.conrr672
3.
Giannetto A., Puntoriero F., Notti A., Parisi M.F.,
19.
Nguyen T.B., Tran M.Q., Ermolenko L., Al-Mourabit A.
Ielo I., Nastasi F., Bruno G., Campagna S., Lanza S.
Org. Lett. 2013, 16, 310-313. doi 10.1021/ol403345e
Eur. J. Inorg. Chem. 2015, 5730-5742. doi 10.1002/
20.
Kanyonyo M.R., Ucar Н., Isa M., Carato P., Lesieur D.,
ejic.201501050
Renard P., Poupaert J.H. Bull. Soc. Chim. Belg. 1996,
4.
Giannetto A., Puntoriero F., Barattucci A., Lanza S.,
105, 17-22. doi 10.1002/bscb.19961050105
Campagna S. Inorg. Chem. 2009, 48, 10397-10404.
21.
Kasséhin U.C., Gbaguidi F.A., Kapanda C.N.,
doi 10.1021/ic900875b
McCurdy C.R., Poupaert J.H. Org. Chem. Int. 2014, ID
5.
Низовцева Т.В., Комарова Т.Н., Нахминович А.С.,
486540. doi 10.1155/2014/486540
Елохина В.Н. ЖОХ, 2008, 78, 342-343. [Nizovtse-
22.
Воронков М.Г., Дерягина Э.Н., Нахманович А.С,
va T.V., Komarova T.N., Nakhmanovich A.S., Elokhi-
Усов В.А. Реакции серы с органическими соедине-
na V.N. Russ. J. Gen. Chem. 2008, 78, 327-328.]
doi 10.1134/S107036320802028X
ниями. Новосибирск: Наука, 1979. 368.
6.
Розенцвейг Г.Н., Федотова А.И., Серых В.Ю.,
23.
Tayade Y.A., Jangale A.D., Dalal D.S. ChemistrySelect.
Чернышев К.А., Розенвейг И.Б. ЖОрХ.
2012,
2018, 3, 8895-8900. doi 10.1002/slct.201801553
48,
483-486.
[Rozentsveig G.N., Fedotova A.I.,
24.
Kale A.D., Tayade Y.A., Mahale S.D., Patil R.D.,
Serykh V.Yu., Chernyshev K.A., Rozentsveig I.B.
Dala D.S. Tetrahedron. 2019, 75, 130575. doi 10.1016/
Russ. J. Org. Chem. 2012, 48, 481-484.] doi 10.1134/
j.tet.2019.130575
S1070428012040021
25.
Gilbert B. Gmelins Handbuch der Anorganischen
7.
Ozturk I.I., Urgut O.S., Banti C.N., Kourkoumelis N.,
Chemie. Schwefel. Teil A. Weinheim: John Wiley &
Owczarzak A.M., Kubicki M., Charalabopoulos K.,
Sons. 1953. 121.
Hadjikakou S.K. Polyhedron. 2014, 70, 172-179. doi
10.1016/j.poly.2013.12.025
26.
Kibbel H.U., Kucken M., Peters E., Weber H.
J. Prakt. Chem. 1981, 323, 41-48. doi 10.1002/
8.
Abdulghani A.J., Abbas N.M. Bioinorg. Chem. Appl.
prac.19813230107
2011, ID 706262. doi 10.1155/2011/706262
9.
Desseyn H.O. Pure Appl. Chem. 1989, 61, 867-872.
27.
Hoppe H., Hartke K. Arch. Pharm. 1975, 308, 526-
doi 10.1351/pac198961050867
541. doi 10.1002/ardp.19753080708
10.
Ozturk T., Ertas E., Mert O. Chem. Rev. 2010, 110,
28.
Rollick K.L., Gillick J.G., Kuczkowski J.A. Европ.
3419-3478. doi 10.1021/cr900243d
заявка EP 278890. 1988. C.A. 1989, 110, 77271.
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020
734
ПОНОМАРЁВА и др.
Synthesis of N,N'-Disubstituted Dithiooxamides Derivatives
of the Modified Willgerodt-Kindler Reaction
T. N. Ponomarevaa, E. V. Eliseenkovb, A. A. Petrovb, *, and V. P. Boyarskiib
a St. Petersburg State Institute of Technology (Technical University),
190013, Russia, St. Petersburg, Moskovskii pr. 26
b St. Petersburg State University, 199034, Russia, St. Petersburg, Universitetskaya nab. 7-9
*e-mail: aap1947@yandex.ru
Received January 20, 2020; revised February 6, 2020; accepted February 9, 2020
The conditions of the reaction of trichloroethylene with sulfur and amines were optimized (modified reaction
of Willgerodt-Kindler). The reaction of tetrachloroethylene with sulfur and some basic primary and secondary
amines of the aliphatic series in dimethylformamide under mild conditions leads to N,N'-disubstituted
dithiooxamides with 30-70% yields at 100% conversion of tetrachloroethylene.
Keywords: tetrachloroethylene, N,N'-disubstituted dithiooxamide, the reaction of Willgerodt-Kindler
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 56 № 5 2020